

Pará (Bula do profissional de saúde)
SUPERA FARMA LABORATÓRIOS S.A
IDENTIFICAÇÃO DO MEDICAMENTO
Pará
nitazoxanida
Suspensão oral 20 mg/mL
Medicamento similar equivalente ao medicamento de referência.
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Pó para suspensão oral
Embalagem contendo frasco com 45 mL ou 100 mL após reconstituição + seringa1 dosadora.
USO ORAL
USO PEDIÁTRICO ACIMA DE 1 ANO
COMPOSIÇÃO:
Cada 1 mL de suspensão reconstituída de Pará contém:
| nitazoxanida | 20 mg |
| veículo q.s.p. | 1 mL |
Veículo: benzoato de sódio, sacarose, goma xantana, celulose microcristalina, ácido cítrico, citrato de sódio di- hidratado, corante vermelho e aroma de morango.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE2
INDICAÇÕES
Pará é indicado no tratamento das seguintes infecções3:
- gastroenterites virais provocadas por rotavírus e norovírus;
- helmintíases provocadas por nematódeos, cestódeos e trematódeos, como: Enterobius vermicularis, Ascaris lumbricoides, Strongyloides stercolaris, Ancylostoma duodenale, Necator americanus, Trichuris trichiura, Taenia sp. e Hymenolepis nana;
- amebíase, para tratamento da diarreia4 por amebíase intestinal aguda ou disenteria amebiana causada pelo complexo Entamoeba histolytica/díspar;
- giardíase, para tratamento da diarreia4 causada por Giardia lamblia ou Giardia intestinalis;
- criptosporidíase, para tratamento da diarreia4 causada por Cryptosporidium parvum;
- blastocistose, balantidíase e isosporíase, causadas, respectivamente, por Blastocistis hominis, Balantidium coli e Isospora belli.
RESULTADOS DE EFICÁCIA
Diarreia4 causada por Giardia lamblia em adultos e adolescentes com idade igual ou superior a 12 anos
Em um estudo duplo-cego5 controlado, conduzido em adultos e adolescentes com diarreia4 causada por Giardia lamblia, um esquema de três dias de tratamento com nitazoxanida comprimido 500 mg, duas vezes ao dia, foi comparado com um comprimido de placebo6 por três dias. Um outro estudo duplo-cego5 controlado, conduzido em adultos e adolescentes com diarreia4 causada por Giardia lamblia, comparou comprimidos de nitazoxanida 500 mg, duas vezes ao dia, por três dias com um comprimido de placebo6. As taxas de resposta clínica, quatro a sete dias após o tratamento, foram superiores a 83% em ambos os estudos.(1)
Diarreia4 causada pela Giardia lamblia em pacientes pediátricos com 1 a 11 anos de idade
Em um estudo randomizado7 controlado, conduzido no Peru com cento e dez pacientes pediátricos com diarreia4 causada por Giardia lamblia, um curso de três dias de tratamento com nitazoxanida suspensão oral (100 mg, duas vezes ao dia em crianças de 24 a 47 meses; 200 mg, duas vezes ao dia em crianças de 4 a 11 anos) foi comparado com um curso de cinco dias de tratamento com metronidazol (125 mg, duas vezes ao dia em crianças de 2 a 5 anos; 250 mg, duas vezes ao dia em crianças de 6 a 11 anos). A resposta clínica, avaliada três a sete dias após o início do tratamento, foi de 85% no grupo nitazoxanida versus 80% no grupo metronidazol.(2)
Diarreia4 causada por Cryptosporidium parvum em adultos e adolescentes com idade igual ou superior a 12 anos
Em um estudo duplo-cego5 controlado, conduzido no Egito em adultos e adolescentes com diarreia4 causada por Cryptosporidium parvum, um curso de tratamento de três dias com nitazoxanida comprimido 500 mg, duas vezes ao dia, foi comparado a um comprimido de placebo6 por três dias. Um segundo grupo de pacientes recebeu, em regime aberto, uma suspensão oral de nitazoxanida 500 mg/25 mL, duas vezes ao dia, por três dias. As taxas de resposta clínica foram 96% e 87%, respectivamente, para nitazoxanida comprimido e suspensão oral, versus 41% para o grupo que recebeu o placebo6. (3)
Diarreia4 causada por Cryptosporidium parvum em pacientes pediátricos com 1 a 11 anos de idade
Em dois estudos duplo-cegos controlados, em pacientes pediátricos com diarreia4 causada por Cryptosporidium parvum, um curso de três dias de tratamento com nitazoxanida suspensão oral (100 mg, duas vezes ao dia em crianças de 12 a 47 meses; 200 mg, duas vezes ao dia em crianças de 4 a 11 anos) foi comparado com um placebo6. As taxas de resposta clínica, três a sete dias pós-tratamento, foram 88% no grupo tratado com a suspensão oral de nitazoxanida e 38% no grupo placebo6.(4)
Em um estudo realizado em Zâmbia com crianças desnutridas e internadas, com idade entre 12 a 35 meses, a taxa de resposta clínica à nitazoxanida foi de 56% versus 23% para o grupo de pacientes tratados com placebo6.(5)
Diarreia4 causada por rotavíus
Um estudo clínico duplo-cego randomizado8 e controlado por placebo6, em pacientes pediátricos com idade de 5 meses a 7 anos (idade mediana = 11 meses), internados com grave diarreia4, tendo o rotavírus como único agente etiológico9 da gastroenterite10, avaliou a nitazoxanida suspensão oral 7,5 mg/kg e o placebo6, duas vezes ao dia, por três dias. Todos os pacientes permaneceram hospitalizados por sete dias após o início do tratamento. O desfecho primário foi o tempo desde a primeira dose até a resolução da doença, sendo usada a análise por intenção de tratar modificada. A análise de sobrevivência11 mostrou que o tempo mediano para a resolução da doença foi de trinta e uma horas (IQR: 22-73) para o grupo tratado com a nitazoxanida, comparado com setenta e cinco horas (IQR: 51-124) para o grupo placebo6 (p = 0,0137), mostrando que o curso com nitazoxanida reduziu significativamente a duração da doença pelo rotavírus em pacientes pediátricos hospitalizados. Não foram relatados eventos adversos.(6)
Diarreia4 causada por vírus12 em adolescentes e adultos
Cinquenta pacientes ambulatoriais com idade igual ou superior a 12 anos (média 33,5 anos), apresentando diarreia4 e exame de fezes positivo (ELISA) para norovírus, rotavírus e adenovírus, foram inscritos em um ensaio clínico duplo- cego controlado por placebo6 para avaliar a nitazoxanida no tratamento de gastroenterites virais. Os pacientes foram randomicamente designados para o tratamento com nitazoxanida comprimidos 500 mg ou placebo6, duas vezes ao dia, por três dias. O desfecho primário foi o tempo, a partir da primeira dose, até a resolução dos sintomas13. A análise foi por intenção de tratar para quarenta e cinco pacientes, excluindo-se cinco pacientes com outros enteropatógenos no período basal. Os resultados mostraram que o tempo mediano de resolução dos sintomas13, a partir da primeira dose, foi 1,5 dias (IQR: 0,5-2,5) para os pacientes tratados com nitazoxanida e 2,5 dias (IQR: 1,5-4,5) para o grupo placebo6. Significantes reduções no tempo de resolução dos sintomas13 foram observadas em todos os pacientes analisados (p < 0,0001) e nos subgrupos de pacientes com rotavírus (p = 0,0052) e norovírus (p = 0,0295). Não se observaram eventos adversos.(7)
Infecções3 parasitárias mistas
Um estudo para avaliar a eficácia e a segurança da nitazoxanida como agente único para tratamento de um amplo espectro de infecções3 parasitárias mistas por protozoários14 e helmintos15, foi conduzido no México. Três amostras fecais de 1.824 adultos e crianças foram rastreadas para presença de oocistos, cistos, trofozoítas, ovos ou larvas de protozoários14 ou helmintos15 intestinais. Duzentos e quarenta e seis adultos e crianças infectadas com pelo menos um protozoário16 e dois helmintos15 receberam 7,5 mg/kg de nitazoxanida (500 mg para adultos e 200 mg para crianças com menos de 12 anos de idade) a cada doze horas, por três dias consecutivos. Amostras de fezes foram examinadas nos dias 6, 7, 8, 13, 14 e 15 (± 1) após o início do tratamento, usando a técnica de formalina-éter de concentração e de Kato-Katz de contagem de ovos. O tratamento com nitazoxanida foi eficaz em 71-100% na eliminação da evidência de infecção17 por Entamoeba histolytica/E. díspar, Giardia duodenalis, Bastocystis hominis, Isospora belli, Enterobius vermicularis, Ascaris lumbricoides, Trichuris trichiura e Hymenolepis nana. Os valores químicos clínicos e hematológicos obtidos antes e após o tratamento não foram afetados pela nitazoxanida. O medicamento foi bem tolerado e apenas quinze pacientes (6,1%) relataram leve dor abdominal que cedeu em menos de vinte e quatro horas.(8)
Referências bibliográficas
- Rossignol JF, Ayoub A, Ayers MS. Treatment of Diarrhea Caused by Giardia intestinalis and Entamoeba histolytica or E. dispar: A Randomized, Double-Blind, Placebo6-Controlled Study of Nitazoxanide. Journal of Infectious Diseases. 2001; 184:381-4.
- Ortiz JJ, Ayoub A, Gargala G, Chegne N L & Favennec L. Randomized clinical study of nitazoxanide compared to metronidazole in the treatment of symptomatic giardiasis in children from Northern Peru. Aliment Pharmacol Ther 2001; 15: 1409±1415. Aliment Pharmacol Ther 2001; 15: 1409-15.
- Rossignol JF, Kabil SM, El-Gohary Y and Younis AM. Effect of Nitazoxanide in Diarrhea and Enteritis Caused by Cryptosporidium Species. Clinical Gastroenterology and Hepatology 2006;4:320-4.
- Rossignol JF, Ayoub A and Ayers MS. Treatment of Diarrhea Caused by Cryptosporidium parvum: A Prospective Randomized, Double-Blind, Placebo6-Controlled study of Nitazoxanide. The Journal of Infectous Diseases 2001;184:103-6.
- Amadi B, Mwiva M, Musuku J, Watuka A, Sianongo S, Ayoub A and Kelly P. Effect of nitazoxanide on mobility and mortality in Zambian children with cryptosporidiosis: a randomized controlled trial. Lancet 2002 Nov2;360(9343): 1375-80.
- Rossignol JF, Abu-Zekry M and Santoro MG. Effect of nitazoxanide for treatment of severe rotavirus diarrhea: randomized double-blind placebo6-controlled trial. Lancet 2006 June 13; 368(9530):124-9.
- Rossignol JF and El-Gohary M. Nitazoxanide in treatment of viral gastroenteritis: a randomized double-blind placebo6-controlled clinical trial. Aliment Pharmacol Ther 2006; 24: 1423-30.
- Cabello RR et al. Nitazoxanide for the treatment of intestinal protozoan and helmintic infections in Mexico. Transactions of the Royal Society of Tropical Medicine and Hygiene, 1997; 91: 701-703.
CARACTERÍSTICAS FARMACOLÓGICAS
A nitazoxanida é um antiparasitário sintético, de amplo espectro, derivado da nitrotiazolil-salicilamida, para administração oral. É um pó cristalino18 amarelo brilhante, pouco solúvel em etanol e praticamente insolúvel em água. Quimicamente é a 2-acetiloxi-N-(5-nitro-2-tiazolil) benzamida. A fórmula molecular é C12H9N3O5S e seu peso molecular, 307,3.
FARMACODINÂMICA
Acredita-se que a atividade antiprotozoário da nitazoxanida seja devida a sua interferência na reação de transferências de elétrons dependente da enzima19 piruvato20-ferredoxina oxidorredutase (PFOR) no parasita21, a qual é essencial para o seu metabolismo22 energético anaeróbico. No entanto, é possível que este não seja o único meio através do qual a nitazoxanida exerça a sua atividade antiprotozoário.
O mesmo parece ocorrer em relação aos vermes, embora outros mecanismos, ainda não totalmente esclarecidos, possam estar envolvidos.
A ação sobre vírus12 se dá através da inibição da síntese da estrutura viral, bloqueando a habilidade do vírus12 em se replicar.
O tempo médio de início de ação do medicamento está estimado entre duas a quatro horas após a sua administração.
FARMACOCINÉTICA
Absorção
Após administração oral da nitazoxanida, em comprimidos ou suspensão oral, as concentrações plasmáticas máximas dos seus metabólitos23 ativos tizoxanida e tizoxanida glicuronídeo são observadas dentro de uma a quatro horas. Sendo assim, a nitazoxanida não é detectada no plasma24. A biodisponibilidade relativa da suspensão oral, comparada a do comprimido, é de 70%.
Efeito do alimento
Quando a nitazoxanida em comprimidos é administrada com alimento, a AUC25 da tizoxanida e da tizoxanida glicuronídeo no plasma24 aumenta quase duas vezes e a Cmáx, quase 50%.
Quando a nitazoxanida em suspensão oral é administrada com alimento, a AUC25 da tizoxanida e tizoxanida glicuronídeo aumenta cerca de 45-50% e a Cmáx, ? 10%.
Distribuição
No plasma24, mais de 99% da tizoxanida estão ligados às proteínas26.
Metabolismo22
Após administração oral em humanos, a nitazoxanida é rapidamente hidrolisada a um metabólito27 ativo, a tizoxanida (desacetil-nitazoxanida), que, então, sofre conjugação, primariamente glicuronização. In vitro, estudos de metabolismo22 demonstraram que a tizoxanida não tem efeito inibitório significativo sobre as enzimas do sistema citocromo P450.
Eliminação
A tizoxanida é excretada na urina28, bile29 e fezes e a tizoxanida glicuronídeo é excretada na urina28 e na bile29. Aproximadamente dois terços da dose oral de nitazoxanida são excretados nas fezes e um terço, na urina28.
A farmacocinética da nitazoxanida após a sua administração na forma de comprimidos em pacientes pediátricos com menos de 12 anos de idade não foi estudada. Também não se estudou a farmacocinética da nitazoxanida após a sua administração na forma de suspensão oral em crianças com menos de 1 ano de idade.
CONTRAINDICAÇÕES
Pará não deve ser administrado nas seguintes situações:
- doenças hepáticas30 ou doença renal31;
- hipersensibilidade a qualquer um dos componentes da fórmula.
Este medicamento (pó para suspensão oral) é contraindicado para menores de 1 ano.
ADVERTÊNCIAS E PRECAUÇÕES
Instruir o paciente quanto às medidas de higiene recomendadas para combater as parasitoses:
- Lavar bem as frutas e verduras;
- Lavar bem os utensílios domésticos;
- Manter os alimentos e depósitos de água cobertos;
- Manter as mãos32 sempre limpas e as unhas33 cortadas, evitar levá-las à boca34 e lavá-las antes das refeições e após ir ao banheiro;
- Utilizar água tratada, filtrada ou fervida e não beber água em recipientes impróprios;
- Manter local adequado para depósito de fezes humanas ou de animais (fossas e latrinas), evacuar em local apropriado (vaso sanitário) e manter as instalações sanitárias limpas;
- Não utilizar fezes humanas como adubo;
- Não comer carne suína e/ou bovina crua ou mal cozida;
- Não adquirir carne de procedência duvidosa;
- Não andar descalço em locais possivelmente infectados.
Lactação35
Não se sabe se a nitazoxanida é excretada no leite humano. Portanto, Pará somente deve ser utilizado durante a lactação35 se os benefícios justificarem o risco potencial para o lactente36.
Gravidez37
Estudos de reprodução38 foram realizados com doses de até 3.200 mg/kg/dia em ratos (aproximadamente 26 vezes a dose clínica para adultos, ajustada à área de superfície corporal) e 100 mg/kg/dia em coelhos (aproximadamente 2 vezes a dose clínica para adultos, ajustada à área de superfície corporal) e não evidenciaram dano ao feto39 devido à nitazoxanida. No entanto, como não há estudos controlados avaliando o uso em mulheres grávidas, Pará somente deve ser utilizado durante a gravidez37 se os benefícios justificarem o risco potencial para o feto39.
Categoria B de risco na gravidez37: Os estudos em animais não demonstraram risco fetal, mas também não há estudos controlados em mulheres grávidas; ou então, os estudos em animais revelaram riscos, mas que não foram confirmados em estudos controlados em mulheres grávidas.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista. Atenção: Este medicamento contém açúcar40, portanto, deve ser usado com cautela em portadores de Diabetes41.
INTERAÇÕES MEDICAMENTOSAS
Interação medicamento-medicamento
A nitazoxanida não tem efeitos significativos na inibição do citocromo P450 e, portanto, não são esperadas interações medicamentosas. No entanto, a nitazoxanida possui alta taxa de ligação às proteínas26 plasmáticas, e por isso, deve-se ter cautela no caso de coadministração com outros fármacos com elevada taxa de ligação proteica, como os anticoagulantes42 cumarínicos (por ex., varfarina) e o anticonvulsivante fenitoína.
Interação medicamento-alimento
A ingestão da nitazoxanida com alimento aumenta a área sob a curva (AUC25) de concentração plasmática em relação ao tempo e também a Cmáx.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar em temperatura ambiente (15–30°C).
O prazo de validade é de 24 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Após preparo, manter a suspensão oral guardada na embalagem original firmemente fechada por até sete dias.
Características físicas e organolépticas do produto
Pará apresenta-se como pó homogêneo de cor bege, com odor de morango, isento de partículas estranhas. Após a reconstituição, apresenta-se como suspensão de cor rosa, com odor de morango, isenta de partículas estranhas.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Modo de usar
Pará deve ser administrado com alimentos, o que garante uma elevada absorção do medicamento. Prepare a suspensão imediatamente antes de usá-la pela primeira vez, conforme instrução abaixo:
|
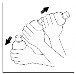
1. Agite vigorosamente o frasco ainda fechado, para soltar o pó do fundo. |
 |
|
2. Adicione água fervida ou filtrada, até a marcação indicada no rótulo. |
 |
|
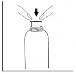
3. Coloque o adaptador para seringa1 no frasco. |
 |
|
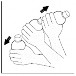
4. Tampe o frasco e agite vigorosamente para obtenção de uma suspensão homogênea. Se necessário, adicione novamente água filtrada até a marcação indicada no rótulo e agite para homogeneizar. |
 |
|
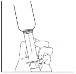
5. O volume da suspensão deve ser medido com a seringa1. Ajuste a seringa1 no orifício da tampa interna do frasco, vire-o de cabeça43 para baixo e puxe o êmbolo44 até o volume prescrito por seu médico. |
 |
|
6. A suspensão pode ser administrada diretamente da seringa1 à boca34 ou, se desejado, pode ser transferida para a colher antes da administração. |
 |
Qualquer quantidade não utilizada da suspensão oral, após o período máximo de armazenamento de sete dias, deve ser descartada.
Atenção: Seringa1 dosadora para uso exclusivo de Pará suspensão. Após o uso, lave-a em água corrente e guarde-a para a próxima dosagem.
Antes de cada administração, a suspensão deve ser bem agitada.
Posologia
|
Indicação |
Dosagem |
Duração |
|
Gastroenterites virais causadas por rotavírus e norovírus |
0,375 mL (7,5 mg) por Kg, 2 vezes por dia (a cada 12 horas) |
3 dias consecutivos |
|
Helmintíases, amebíase, giardíase, isosporíase, balantidíase, blastocistose |
0,375 mL (7,5 mg) por Kg, 2 vezes por dia (a cada 12 horas) |
3 dias consecutivos |
|
Criptosporidíase em pacientes sem imunodepressão |
0,375 mL (7,5 mg) por Kg, 2 vezes por dia (a cada 12 horas) |
3 dias consecutivos |
|
Criptosporidíase em pacientes imunodeprimidos, se a contagem de CD4 for superior a 50 células45/mm³ |
0,375 mL (7,5 mg) por Kg, 2 vezes por dia (a cada 12 horas) |
14 dias consecutivos |
|
Criptosporidíase em pacientes imunodeprimidos, se a contagem de CD4 for inferior a 50 células45/mm³ |
0,375 mL (7,5 mg) por Kg, 2 vezes por dia (a cada 12 horas) |
Deve-se manter a medicação por, no mínimo, oito semanas ou até a resolução dos sintomas13 e negativação dos oocistos |
REAÇÕES ADVERSAS
Reações comuns (> 1/100 e < 1/10): dor abdominal do tipo cólica, diarreia4, náusea46, vômito47 e dor de cabeça43.
Reações incomuns (> 1/1.000 e < 1/100): reação alérgica48, aumento dos níveis sanguíneos de transaminase glutâmica pirúvica, anemia49, aumento do apetite, aumento da creatinina50 no sangue51, hiperidrose52, tontura53, coloração amarelo claro no olho54, febre55, flatulência, hipertensão56, prurido57, rinite58, aumento das glândulas salivares59, taquicardia60, coloração amarelada ou amarelo-esverdeada da urina28 ou esperma61.
Pará pode produzir alteração da cor dos fluidos fisiológicos (por ex., urina28 e esperma61) para amarelo esverdeado, sem qualquer significado clínico. Isto se deve à coloração de alguns dos componentes da fórmula.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
No caso de uso de uma grande dose, os sintomas13 e sinais62 podem se limitar a dores abdominais, náusea46, vômito47 e diarreia4. Lavagem gástrica63 pode ser eficaz, se realizada logo após a ingestão do medicamento. Os pacientes devem ser cuidadosamente observados e receber suporte sintomático64.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS: 1.0372.0258
Farm. Resp.: Dra. Silmara Souza Carvalho Pinheiro. CRF-SP n° 37.843
Registrado por:
Supera Farma Laboratórios S.A.
Avenida das Nações Unidas, 22532, bloco 1, Vila Almeida – São Paulo – SP
CNPJ: 43.312.503/0001-05
Indústria Brasileira
Comercializado por:
Supera RX Medicamentos Ltda.
Pouso Alegre – MG.
SAC 0800 708 1818






