

Fluimucil (Bula do profissional de saúde)
ZAMBON LABORATÓRIOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Fluimucil®
acetilcisteína1
Injetável 100 mg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Embalagem com 5 ampolas de 3 mL
USO INJETÁVEL INTRAVENOSO E USO INALATÓRIO
USO ADULTO E PEDIÁTRICO ACIMA DE 2 ANOS (EXCETO USO INTRAVENOSO)
COMPOSIÇÃO:
Cada mL de Fluimucil® injetável contém:
| acetilcisteína1 | 100 mg |
| veículo q.s.p. | 1 mL |
Veículo: edetato dissódico, hidróxido de sódio, água para injeção2.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE3
INDICAÇÕES
Este é um medicamento indicado quando se tem dificuldade para expectorar e há muita secreção densa e viscosa, tais como: bronquite aguda4, bronquite crônica5 simples e suas exacerbações, enfisema6, pneumonia7, atelectasias8 pulmonares, fibrose cística9 (mucoviscidose10) - doença hereditária que produz muco espesso. Também é indicado como antídoto11 na intoxicação acidental ou voluntária por paracetamol.
RESULTADOS DE EFICÁCIA
Comparação da administração intravenosa e oral
A acetilcisteína1 por via intravenosa tem um pico máximo de concentração em plasma12 até 20 vezes maior que uma dose semelhante por via oral (Borgstrom L e cols. 1986). A maior disponibilidade de acetilcisteína1 por via intravenosa acontece tanto na forma total como reduzida e poderia ser atribuída à ausência do metabolismo13 hepático de primeira passagem que acontece após a administração oral (Olsson B e cols. 1988).
Intoxicação por paracetamol
A acetilcisteína1 é recomendada como antídoto11 para a superdose de paracetamol com possível risco de toxicidade14 hepática15 (Wolf SJ e cols. 2007). Estudo comparou 100 casos de intoxicação por paracetamol tratados com acetilcisteína1 intravenosa e 57 casos que receberam unicamente tratamento de suporte (Prescott LF e cols. 1979). Demonstrou-se uma redução importante da toxicidade14 hepática15 grave (58% suporte a 2% no grupo acetilcisteína1) quando o tratamento foi administrado nas primeiras 10 horas após a ingestão de paracetamol.
Em um estudo de coorte16 que avaliou 4084 pacientes intoxicados por paracetamol, foram comparados os pacientes que receberam regime de acetilcisteína1 por via oral (regime de 72 horas) e por via intravenosa (regime de 20 h). Os pacientes que receberam tratamento endovenoso nas primeiras 12 horas após a ingestão de paracetamol tiveram menor toxicidade14 hepática15 (RR 0,54, CI95% 0,38 a 0,75 às 4 horas; RR 0.84, CI95% 0,71 a 1,00 às 12 horas e 12 minutos). Entre 12 e 18 horas após a ingestão de paracetamol, o tratamento endovenoso com acetilcisteína1 diminuiu a toxicidade14 hepática15 de forma semelhante ao tratamento oral. Ainda é destacada a vantagem de poder utilizar o tratamento endovenoso em pacientes que apresentam vômitos17 (Yarema MC e cols. 2009). Em estudo com pacientes pediátricos, a acetilcisteína1 intravenosa por 52 horas mostrou eficácia semelhante ao regime com acetilcisteína1 oral por 72 horas (Perry HE e Shannon MW. 1998).
A acetilcisteína1 na Síndrome18 do Desconforto Respiratório do Adulto
Estudo controlado em pacientes com Síndrome18 do Desconforto Respiratório do Adulto avaliou 32 pacientes que receberam acetilcisteína1 por via intravenosa e 29 que receberam placebo19 por infusão contínua nas 72 horas posteriores à sua admissão em terapia intensiva20. Os pacientes que receberam acetilcisteína1 tiveram melhora rápida nos índices de oxigenação, com diminuição significativa no suporte ventilatório mecânico no segundo e terceiro dia de tratamento (Suter PM e cols. 1994).
Uso da acetilcisteína1 nas atelectasias8 pulmonares
Pacientes com atelectasias8 pulmonares foram tratados com lavagem broncoscópica com solução salina fisiológica21 e acetilcisteína1 na proporção de 7:3. Resultados radiológicos positivos foram vistos no seguimento de 48 dos 51 pacientes tratados. Houve completa regressão da atelectasia22 em 37 casos e regressão parcial em 11 casos. Entretanto, houve recorrência23 da atelectasia22 em 8 casos nas 48 horas seguintes (Perruchoud A e cols. 1980).
Instilação de acetilcisteína1 para a sinusite24 crônica
Uma solução da associação de 300 mg de acetilcisteína1 e 750 mg de tianfenicol foi usada para realizar instilação local após lavagem e drenagem25 dos seios paranasais26 em 498 pacientes com sinusite24 maxilar crônica. Os pacientes foram tratados até se obter uma lavagem limpa ou uma sinumanometria normal. Em 36,25% dos casos, houve regressão completa do quadro de sinusite24 crônica, sem necessidade de intervenções adicionais, inclusive cirúrgicas (Bertrand B e Eloy P. 1993).
CARACTERÍSTICAS FARMACOLÓGICAS
Farmacodinâmica
O princípio ativo do Fluimucil® é a acetilcisteína1, que exerce intensa ação mucolítico-fluidificante das secreções mucosas27 e mucopurulentas, despolimerizando os complexos mucoproteícos e os ácidos nucléicos que dão viscosidade28 ao escarro e às outras secreções, além de melhorar a depuração mucociliar29. Estas atividades tornam Fluimucil® particularmente adequado para o tratamento das afecções30 agudas e crônicas do aparelho respiratório31 caracterizadas por secreções mucosas27 e mucopurulentas densas e viscosas.
Além disso, a acetilcisteína1 exerce ação antioxidante direta, sendo dotada de um grupo tiol livre (-SH) nucleofílico em condições de interagir diretamente com os grupos eletrofílicos dos radicais oxidantes. De particular interesse é a recente demonstração de que a acetilcisteína1 protege a alfa-1-antitripsina, enzima32 inibidora da elastase, de ser inativada pelo ácido hipocloroso (HClO), potente agente oxidante que é produzido pela enzima32 mieloperoxidase dos fagócitos33 ativados. A estrutura da sua molécula lhe permite, além disso, atravessar facilmente as membranas celulares. No interior da célula34, a acetilcisteína1 é desacetilada, ficando assim disponível a L-cisteína, aminoácido indispensável para a síntese da glutationa (GSH). O GSH é um tripeptídio extremamente reativo que se encontra difundido por igual nos diversos tecidos dos organismos animais e é essencial para a manutenção da capacidade funcional e da integridade da morfologia celular, pois é o mecanismo mais importante de defesa intracelular contra os radicais oxidantes (tanto exógenos como endógenos) e contra numerosas substâncias citotóxicas, incluindo o paracetamol.
O paracetamol exerce sua ação citotóxica pelo empobrecimento progressivo de GSH. A acetilcisteína1 desempenha seu principal papel mantendo níveis adequados de GSH, contribuindo, assim para a proteção celular. Portanto a acetilcisteína1 é um antídoto11 específico para intoxicação por paracetamol.
A acetilcisteína1 reduz a toxicidade14 hepática15 do NAPQI (N-acetil-p-benzoquinonaimina), o metabólito35 intermediário altamente reativo após a ingestão de uma alta dose de paracetamol, pelos seguintes mecanismos:
A acetilcisteína1 atua como um precursor para a síntese de glutationa e, portanto, mantém a glutationa celular em um nível suficiente para inativar o NAPQI. Acredita-se que este seja o principal mecanismo pelo qual a acetilcisteína1 atua nos estágios iniciais da toxicidade14 do paracetamol, com benefício observado principalmente em pacientes tratados dentro de 8-10 horas após a superdosagem.
Quando o tratamento com acetilcisteína1 é iniciado mais de 8 a 10 horas após a sobredosagem de paracetamol, a sua eficácia na prevenção da hepatotoxicidade36 (com base nos indicadores séricos) diminui progressivamente com o prolongamento do intervalo de tratamento com overdose (o tempo entre a sobredosagem de paracetamol e o início do tratamento).
A acetilcisteína1 demonstrou ser ainda eficaz quando a perfusão é iniciada até 12 horas após a ingestão de paracetamol, quando a maior parte do analgésico37 terá sido metabolizada no seu metabólito35 reativo. Nesse estágio, acredita-se que a acetilcisteína1 atue reduzindo os grupos tiol oxidados nas enzimas-chave.
Há evidências de que ainda pode ser benéfico quando administrado até 24 horas após a superdosagem. Nesta fase tardia da hepatotoxicidade36 do paracetamol, os efeitos benéficos da acetilcisteína1 podem ser devidos à sua capacidade de melhorar a hemodinâmica38 sistêmica e o transporte de oxigênio, embora o mecanismo pelo qual isso possa ocorrer ainda não tenha sido determinado.
Farmacocinética
– Absorção
Administração Oral
Em humanos, a acetilcisteína1 é completamente absorvida após administração oral. Devido ao metabolismo13 na parede intestinal e o efeito de primeira passagem, a biodisponibilidade da acetilcisteína1 ingerida oralmente é muito baixa (cerca de 10%). Não foram referidas diferenças entre as várias formas farmacêuticas. Em pacientes com diferentes doenças respiratórias ou cardíacas, a concentração máxima no plasma12 é obtida entre uma e três horas após a administração e, os níveis permaneceram elevados por um período de 24 horas.
Administração Intravenosa como Antídoto11
Após a infusão intravenosa, utilizando a modelagem de 20 horas, os níveis plasmáticos de acetilcisteína1 atingiram 300-900 mg / L poucos minutos após o início da infusão, diminuindo para 11 - 90mg / L no final da infusão.
– Distribuição
A acetilcisteína1 é distribuída na forma não metabolizada (20%) e metabolizada - ativa (80%) e, pode ser encontrada principalmente no fígado39, rins40, pulmões41 e secreções brônquicas.
O volume de distribuição da acetilcisteína1 varia de 0,33 a 0,47 L/kg. A ligação às proteínas42 é de cerca de 50% após 4 horas da administração da dose e cai para 20% em 12 horas.
Não há informações sobre se a acetilcisteína1 atravessa a barreira hematoencefálica ou se é excretada no leite materno. A acetilcisteína1 atravessa a placenta.
Metabolismo13
A acetilcisteína1 passa por um metabolismo13 rápido e extensivo na parede intestinal e fígado39 após a administração oral.
O composto resultante, cisteína, é considerado o metabólito35 ativo. Após essa fase de transformação, a acetilcisteína1 e a cisteína compartilham a mesma via metabólica.
O clearance renal43 pode representar cerca de 30% do clearance total do organismo. Após a administração oral a meia vida terminal de acetilcisteína1 total é de 6,25 h.
– Excreção
Após uma dose intravenosa única de acetilcisteína1, a concentração plasmática de acetilcisteína1 total mostra um declínio poli-exponencial com uma semivida terminal (T1 / 2) de 5,6 horas. A depuração renal43 foi definida em 0,11 litros / h / kg e pode representar cerca de 30% da depuração corporal total.
Linearidade / Não Linearidade
A farmacocinética da acetilcisteína1 é proporcional à dose administrada no intervalo de dose entre 200-3200 mg / m2 para AUC44 e Cmax.
Populações especiais
Pacientes Pediátricos: A meia-vida terminal média da acetilcisteína1 é maior nos neonatos45 (11 horas) do que nos adultos (5,6 horas)8,25. Nenhuma informação está disponível em outras faixas etárias.
Insuficiência Hepática46: Em indivíduos com insuficiência hepática46 grave, associada a cirrose47 alcoólica (pontuação de 7-14 na escala de Child-Pugh) ou cirrose47 biliar primária ou secundária (5-7 na escala de Child-Pugh), a semi-vida de eliminação (T1 / 2) aumentou 80% a eliminação diminuiu em 30%, em comparação ao grupo controle 8. Insuficiência renal48 Não há dados farmacocinéticos disponíveis em pacientes com insuficiência renal48.
Dados Pré Clinicos
Os dados não clínicos não revelam riscos especiais para o ser humano, com base em estudos convencionais de farmacologia49 de segurança, toxicidade14 de dose repetida, genotoxicidade e toxicidade14 para a reprodução50 e desenvolvimento. O tratamento com altas doses em ratas prenhes e coelhos não revelou evidência de comprometimento da fertilidade feminina ou dano ao feto51 devido à acetilcisteína1. O tratamento de ratos machos durante 15 semanas com acetilcisteína1 a uma dose oral considerada suficiente em excesso, em comparação com a dose humana recomendada, não afetou a fertilidade ou o desempenho reprodutivo geral dos animais.
CONTRAINDICAÇÕES
Agente Mucolitico
Este medicamento é contraindicado para pacientes52 com histórico de hipersensibilidade conhecida a acetilcisteína1 e/ou demais componentes de sua formulação.
Criancas abaixo de 2 anos de idade.
Antídoto11
Não há contra-indicações para o tratamento da superdosagem de paracetamol com acetilcisteína1.
Categoria B: Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião dentista. Este medicamento é contraindicado para uso por crianças menores de 2 anos exceto para uso intravenoso.
ADVERTÊNCIAS E PRECAUÇÕES
A presença de odor sulfúreo (enxofre) não indica alteração no medicamento, pois é característico do princípio ativo contido no mesmo. É recomendada precaução quando utilizado por pacientes com úlcera péptica53 ou histórico de úlcera54, especialmente no caso de administração concomitante a outros medicamentos com conhecido efeito irritativo à mucosa55 gástrica.
A administração da acetilcisteína1, principalmente no início do tratamento, pode fluidificar a secreção brônquica e aumentar seu volume. Se efetivamente o paciente não conseguir expectorar, pode ser realizada a drenagem25 postural e/ou outras medidas de drenagem25 de secreção.
Pacientes que sofrem de asma56 brônquica devem ser monitorados durante o tratamento. A acetilcisteína1 deve ser interrompida imediatamente se o paciente apresentar broncoespasmo57 e um tratamento apropriado deve ser iniciado.
Acetilcisteína1 deve ser administrada por via endovenosa por supervisão médica. Os efeitos indesejáveis de perfusão de acetilcisteína1 aparecem mais comumente se o medicamento é administrado muito rápido ou em quantidade excessiva. Portanto as indicações de posologia devem ser rigorosamente seguidas. Fluimucil® usado durante a inalação pode ser administrado concomitantemente com vasoconstritores e broncodilatadores58 comumente utilizados.
Recomenda-se que, no caso de administração concomitante para inalação com outros medicamentos, a solução seja preparada na hora e seja utilizada uma vez só para garantir que não haverá comprometimento da estabilidade química da mistura.
Deve-se ter cautela na administração de doses como antídoto11 em intoxicações por paracetamol em pacientes com peso corporal abaixo dos 40 kg por causa de possível risco de sobrecarga de líquido com consequente hiponatremia59, convulsão60 e óbito61. Portanto, recomenda-se seguir estritamente as orientações referentes à dosagem do produto.
A administração da acetilcisteína1 em doses como antídoto11 em intoxicações por paracetamol pode prolongar o tempo de protrombina62 (queda do índice de protrombina62, elevação de INR ou RNI: relação normatizada internacional).
Fluimucil® contém 43 mg (1.9mmol) de sódio por ampola. Essa informação deve ser considerada em pacientes submetidos à dieta controlada de sódio. Em casos muito raros, reações anafilactóides foram fatais. Após a administração parenteral, as reações de hipersensibilidade anafilactóide à acetilcisteína1 geralmente ocorrem entre 15 e 60 minutos após o início da infusão e, em muitos casos, os sintomas63 são aliviados com a interrupção da infusão. Um medicamento anti-histamínico pode ser necessário, e ocasionalmente podem ser necessários corticosteróides.
A maioria das reações anafilactóides pode ser controlada suspendendo-se temporariamente a infusão de acetilcisteína1, administrando-se os cuidados de suporte apropriados e reiniciando-se a uma menor taxa de infusão. Uma vez que uma reação anafilactóide está sob controle, a infusão pode ser reiniciada normalmente a uma taxa de infusão de 50 mg / kg durante 4 horas, seguida pela infusão final de 16 horas (100 mg/kg durante 16 horas).
Gravidez64 e Lactação65
Há escassez de dados clínicos sobre mulheres expostas à acetilcisteína1 durante a gravidez64. Estudos com animais não sugerem nenhum efeito nocivo, direto ou indireto, sobre a gravidez64, desenvolvimento embriônico-fetal, nascimento ou desenvolvimento pós-natal.
Não há informações disponíveis sobre a excreção pelo leite materno, por isso não se recomenda utilizar este medicamento durante esta fase. O produto só deve ser usado durante a gravidez64 e lactação65 depois de cuidadosa avaliação de risco-benefício.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião dentista.
Fertilidade
Não há informação disponível sobre o efeito da acetilcisteína1 na fertilidade humana.
Estudos em animais não indicam efeitos nocivos com relação à fertilidade para humanos nas doses recomendadas.
Populações especiais
Uso em idosos: Devem-se seguir as orientações gerais descritas para o medicamento, salvo em situações especiais.
Uso pediátrico: Devem-se seguir as orientações gerais descritas para o medicamento.
Este medicamento é contraindicado para uso por crianças menores de 2 anos exceto uso intravenoso.
Pacientes portadores de asma56 brônquica: Devem ser rigorosamente controlados durante o tratamento; se ocorrer broncoespasmo57, o tratamento deverá ser suspenso imediatamente.
Na administração por via aerossólica, como pode ocorrer em qualquer aplicação aerossólica e independente do fármaco66 utilizado, em pacientes predispostos e/ou asmáticos é aconselhável associar um broncodilatador67, de modo a prevenir eventuais reações broncoespásticas.
Efeitos na habilidade de dirigir e operar máquinas
Fluimucil® não interfere na habilidade de dirigir e operar máquinas enquanto estiver fazendo uso do medicamento.
INTERAÇÕES MEDICAMENTOSAS
Os estudos de interação foram realizados apenas em adultos.
Acetilcisteína1 não deve ser administrada concomitantemente com fármacos antitussígenos, pois a redução do reflexo da tosse pode levar ao acúmulo de secreções brônquicas.
A administração concomitante de nitroglicerina e acetilcisteína1 tem mostrado hipotensão68 significante e aumento da dilatação da artéria69 temporal. Se houver necessidade de tratamento concomitante com nitroglicerina e acetilcisteína1, os pacientes devem ser monitorados, pois pode ocorrer hipotensão68, inclusive grave, devendo-se ter atenção para a possibilidade de cefaleias70.
Avise seu médico ou farmacêutico se você usar medicamentos a base de nitrato, em conjunto com o uso de Fluimucil®.
Relatos de inativação de antibióticos com acetilcisteína1 foram encontrados apenas em estudos “in vitro” onde as substâncias foram misturadas diretamente. Portanto, dissolução (mistura) de formulações de acetilcisteína1 com outros medicamentos não é recomendada.
Interações com exames laboratoriais
A acetilcisteína1 pode interferir no método de ensaio colorimétrico de mensuração do salicilato e interferir também, no teste de cetona na urina71.
Interações com alimentos
Por ser de uso injetável ou inalatório, não são conhecidas interferências entre o medicamento e alimentos.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar em temperatura ambiente (15–30°C).
Número de lote e datas de fabricação e validade: vide embalagem. Fluimucil® é válido por 24 meses.
Não use medicamento com prazo de validade vencido. Guarde-o em sua embalagem original.
Após aberto, para usos injetável e inalatório, o conteúdo da ampola deste medicamento deve ser utilizado imediatamente
Características físicas e organolépticas do produto
Fluimucil® é uma solução incolor e límpida de odor sulfúreo (enxofre), que é característico da acetilcisteína1.
Fluimucil® excepcionalmente, tanto conservado na ampola aberta ou no nebulizador, pode adquirir uma coloração rosada, o que não significa que o medicamento perdeu sua atividade.
Como a acetilcisteína1 pode reagir quimicamente com certos materiais como borracha, ferro, cobre, é conveniente utilizar dispositivos nebulizadores feitos de vidro e plástico, lavando-os com água após o uso.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
MODO DE USAR
– Uso intravenoso
A administração de Fluimucil® por via intravenosa deve ser realizada por profissional da saúde3 especializado, com os materiais necessários e suporte médico.
– Uso inalatório
A administração para inalação deve proceder da seguinte forma:
- Romper a ampola no local indicado, protegendo os dedos para não cortá-los conforme Instruções para abertura da ampola;
- Depositar a dose de Fluimucil® no copo do inalador, podendo utilizar uma seringa72 para retirar o medicamento da ampola e transportar para o copo. Se for o caso, adicionar outros medicamentos conforme a prescrição médica e adicionar solução fisiológica21 para completar o volume;
- Realizar a inalação pelo tempo determinado.
Instruções para a abertura da ampola:
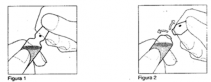
- Segure a ampola como indicado na figura 1;
- Pressione para baixo com os polegares posicionados local indicado pelo ponto, conforme figura 2.
POSOLOGIA
A duração do tratamento deve ser determinada com base na evolução clínica, mas a grande tolerabilidade geral e local do medicamento permite tratamentos prolongados.
Uso intravenoso não como antídoto11
Fluimucil® deve ser administrado através da infusão lenta em solução salina ou solução glicosada 5%.
- Adultos: 1 ampola, 1 ou 2 vezes por dia;
- Crianças acima de 2 anos: meia ampola, 1 ou 2 vezes por dia.
Uso intravenoso como antídoto11
Na intoxicação acidental ou voluntária por paracetamol, a terapia com acetilcisteína1 deve ser iniciada o quanto antes. O tratamento deve ser iniciado dentro de 0 a 8 horas da ingestão do paracetamol. Para uma administração de acetilcisteína1 durante 15 horas após a superdosagem de paracetamol, o tratamento é praticamente ineficaz, mas há evidência na literatura de um tratamento bem sucedido 16 - 24 horas após a ingestão de paracetamol.
A injeção2 é administrada por infusão intravenosa.
A infusão deve ser realizada lentamente para reduzir o risco de efeitos indesejáveis.
Para o tratamento como antídoto11 são recomendados os seguintes esquemas de tratamento:
Pacientes com peso corporal ≥ 40 kg
- Dose de ataque: 150 mg/kg em 200 mL de solução por 60 min;
- Segunda dose: 50 mg/kg em 500 mL por 4 horas;
- Terceira dose: 100 mg/kg em 1000 mL por16 horas.
Pacientes com peso corporal ≥ 20 a 40 kg
- Dose de ataque: 150 mg/kg em 100 mL de solução por 60 min;
- Segunda dose: 50 mg/kg em 250 mL por 4 horas;
- Terceira dose: 100 mg/kg em 500 mL por 16 horas.
Pacientes com peso corporal abaixo de 20 kg
A solução deve ser compatível (5% dextrose73 em água, 0,45% cloreto de sódio ou água para injeção2).
- Dose de ataque: 150 mg/kg em 3 mL/kg de solução por 60 min;
- Segunda dose: 50 mg/kg em 7 mL/kg por 4 horas;
- Terceira dose: 100 mg/kg em 14 mL/kg por 16 horas.
Uso inalatório
- Nebulização74 (adultos e crianças acima de 2 anos): Utiliza-se 1 ampola em cada sessão, diluída em igual quantidade de soro75 fisiológico76, efetuando- se 1 a 2 sessões por dia, durante 5 a 10 dias, de acordo com a necessidade.
Devido à elevada tolerabilidade do medicamento, a frequência das sessões, as doses e a duração do tratamento podem ser modificadas a critério médico, em limites bastante amplos, sem necessidade de diferenciar as doses para adultos das usadas na pediatria; - Instilações endotraqueal ou endobrônquicas (adultos e crianças acima de 2 anos): Administra-se através da cânula de traqueostomia77 do tubo endotraqueal ou do broncoscópio78, 1 ampola por vez, 1ou 2 vezes por dia, de acordo com a necessidade.
REAÇÕES ADVERSAS
As seguintes reações adversas foram relatadas pós-comercialização. Sua frequência não é conhecida (não pode ser estimada através dos dados disponíveis).
Uso inalatório: hipersensibilidade, broncoespasmo57, rinorreia79, estomatite80, vômito81, náusea82, urticária83, rash84 (erupção85 cutânea86) e prurido87.
Uso intravenoso: choque anafilático88, reação anafilática89, reação anafilactóide, hipersensibilidade, taquicardia90, broncoespasmo57, dispneia91, vômito81, náusea82, angioedema92, urticária83, rubor, erupção85 cutânea86, prurido87, edema93 facial, hipotensão68 e tempo prolongado de protrombina62.
Em casos raríssimos houve relato de reações severas da pele94, como síndrome18 de Stevens-Johnson e síndrome18 de Lyell, com relação temporal com a administração da acetilcisteína1. Na maioria dos casos havia envolvimento provável de, pelo menos uma droga co-suspeita na provocação da síndrome18 muco-cutânea86 relatada.
Por isso, é preciso consultar o médico assim que ocorrer alguma nova alteração na pele94 ou em membranas mucosas27, onde nesse caso a acetilcisteína1 deve ser interrompida imediatamente.
Alguns estudos relatam uma diminuição da taxa de agregação plaquetária na presença de acetilcisteína1. A significância clínica dessa reação ainda não foi definida.
Notificação de Evento Adverso
Para a avaliação contínua da segurança do medicamento é fundamental o conhecimento de seus eventos adversos. Notifique qualquer evento adverso ao SAC Zambon (0800 017 70 11 ou www.zambon.com.br)
Em casos de eventos adversos notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Uso intravenoso
Os sintomas63 da superdosagem são semelhantes, mas são mais graves do que os observados em caso de ocorrência de reações adversas.
O tratamento da superdosagem baseia-se na descontinuação imediata da administração da infusão e tratamento sintomático95 e ressuscitação. Não há antídoto11 específico. A acetilcisteína1 é dialisável.
Uso inalatório
Não há relato de casos de superdosagem por via inalatória.
Teoricamente, quando a acetilcisteína1 é administrada em altas doses, pode ocorrer um alto grau de liquefação96 de secreções mucopurulentas, especialmente em pacientes com reflexo tussígeno ou expectoração97 inadequados.
População pediátrica
Os mesmos sintomas63 e tratamento aplicam-se à população pediátrica.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
Informe-se também com o SAC Zambon (0800 017 70 11 ou www.zambon.com.br) em casos de dúvidas.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Registro MS -1.0084.0075
Farmacêutica Responsável: Juliana Paes de O. Rodrigues - CRF-SP 56.769
Fabricado por: ZAMBON S.p.A
Via della Chimica, 9, Vicenza – Itália
Importado por:
ZAMBON Laboratórios Farmacêuticos Ltda.
Est. Municipal, SN – Quadra Lote, Lote 001C – Anexo98 Parte 9
Fazenda Santo Antônio – Aparecida de Goiânia – GO - CEP: 74.971-451
Registrado por:
ZAMBON Laboratórios Farmacêuticos Ltda.
Av. Presidente Juscelino Kubitschek, 2041 – Bloco E – 5º Andar
Vila Nova Conceição – São Paulo – SP
CEP: 04543-011
CNPJ nº. 61.100.004/0001-36
Indústria Brasileira
SAC 0800 0177011
Referências bibliográficas
- Bertrand B, Eloy P. Temporary nasosinusal drainage and lavage in chronic maxillary sinusitis. Statistical study on 847 maxillary sinuses. Ann Otol Rhinol Laryngol. 1993 Nov;102 (11):858-62.
- Borgstrom L, et al: Pharmacokinetics of N-acetylcysteine in man. Eur J Clin Pharmacol 1986; 31: 217-222.
- Olsson B, et al: Pharmacokinetics and bioavailability of reduced and oxidized N-acetylcysteine. Eur J Clin Pharmacol 1988; 34: 77-82.
- Perruchoud A, et al. Atelectasis of the lung: bronchoscopic lavage with acetylcysteine. Experience in 51 patients. Eur J Respir Dis Suppl. 1980;111:163- 8.
- Perry HE, Shannon MW. Efficacy of oral versus intravenous N-acetylcysteine in acetaminophen overdose: results of an open-label, clinical trial. J Pediatr. 1998 Jan;132(1):149-52.
- Prescott LF, et al. Intravenous N-acetylcystine: the treatment of choice for paracetamol poisoning. Br Med J. 1979 Nov 3;2(6198):1097-100.
- Suter PM, et al. N-acetylcysteine enhances recovery from acute lung injury in man. A randomized, double-blind, placebo19-controlled clinical study. Chest. 1994 Jan;105(1):190-4.
- Wolf SJ, et al. Clinical policy: critical issues in the management of patients presenting to the emergency department with acetaminophen overdose. American College of Emergency Physicians. Ann Emerg Med. 2007 Sep;50 (3):292-313.
- Yarema MC, et al. Comparison of the 20-hour intravenous and 72-hour oral acetylcysteine protocols for the treatment of acute acetaminophen poisoning. Ann Emerg Med. 2009 Oct;54(4):606-14.
- CHM Paracetamol overdose. New guidance on use of intravenous acetylcysteine. 03 September 2012 http://webarchive.nationalarchives.gov.uk/20141205195633/http://www.mhra.gov.uk/Safetyinformation/Safetywarningsalertsandrecalls/Safetywarn ingsandmessagesformedicines/C ON178225 Last access on 13/01/2018.
- DRUGDEX® Evaluations, MICROMEDEX- Drug Summary, Acetylcysteine, 2018.
- MHRA. Paracetamol overdose: Acetylcysteine Core Summary of Product characteristics. September 2012 http://webarchive.nationalarchives.gov.uk/20141206113129/http://www.mhra.gov.uk/home/groups/plp/documents/drugsafetymessage/con178657. pdf Last access on 13/01/2018.
- Martindale. The Complete Drug Reference. Volume A, Drugs monographs, 39th Edition, 2008, 1685-1687.
- Teratogenicity study of N-acetyl-L-cysteine administered by oral route to rats. Internal report. Zambon SpA Milano (Italy). Teratogenicity study of N-acetyl-L-cysteine administered by oral route in rabbits. Internal report. Zambon SpA Milano (Italy).
- Wiest DB, Jenkins D. Antenatal Pharmacokinetics and placental transfer of N- acetylcysteine in chorioamnionitis for fetal neuroprotection. The Journal of Paediatrics 2014, 165 (4): 672-677 e2 https://doi.org/10.1016/j.jpeds.2014.06.044 http://www.sciencedirect.com/science/article/pii/S0022347614005666 Last access on 18/01/2018.
- Fertility study in the female rat with N-Acetyl-L-Cysteine administered by oral route. Internal report. Zambon S.p.A. Milan (Italy).
- 28-week toxicity study in male and female rats and fertility study in the male rat with N- Acetyl-L-Cysteine administered by oral route. Internal report. Zambon S.p.A Milano (Italy).
- Borgstrom L, Kagedal B, Paulsen O. Pharmacokinetics of N-acetylcysteine in man. Eur J Clin Pharmacol 1986; 31:217-222. https://link.springer.com/article/10.1007/BF00606662 Last access on 04/09/2018.
- Olsson B, Johansson M, Gabrielsson J, Bolme P. Pharmacokinetics and bioavailability of reduced and oxidized N-acetylcysteine. Eur J Clin Pharmacol 1988; 34:77-82. https://link.springer.com/article/10.1007%2FBF01061422 Last access on 04/09/2018.
- Rodenstein D, De Coster A, Gazzaniga A. Pharmacokinetics of oral acetylcysteine: absorption, binding and metabolism in patients with respiratory disorders. Clinical Pharmacokinetics, 1978; 3: 247-254. https://link.springer.com/article/10.2165/00003088- 197803030-00005 Last access on 04/09/2018.
- Horowitz RS, Dart RC, Jarvie DR, Bearer CF, Gupta U. Placental transfer of N- acetylcysteine following human maternal acetaminophen toxicity. Journal of Toxicology - Clinical Toxicology, Volume 35, Issue number 5, 1997: 447-451 https://cwru.pure.elsevier.com/en/publications/placental- transfer-of-n-acetylcysteine-following- human-maternal-a-2 Last access on 10 September 2018.
- Sadowska AM, Verbraecken J, Darquennes K, De Backer WA. Role of N-acetylcysteine in the management of COPD. International Journal of COPD 2006; 1 (4): 1-10 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2707813/ Last access on 04/09/2018.
- Acute toxicity study of N-acetylcysteine in rats and mice. Internal report. Zambon SpA Research Laboratories Milano (Italy).
- Twelve week toxicity study in the rat on N-acetyl-L-cysteine administered by oral route. Internal report. Zambon SpA Milano (Italy). Fifty-two week toxicity study of N-acetyl-L-cysteine by oral route to dogs. Internal report. Zambon SpA Milano (Italy).






