Metroniflex
BAXTER HOSPITALAR LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Metroniflex
metronidazol
Injetável 5 mg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO
Solução Injetável
Bolsa plástica de 100 mL. Viaflex. SISTEMA FECHADO
USO INTRAVENOSO
USO ADULTO E PEDIÁTRICO
COMPOSIÇÃO
Cada bolsa plástica de 100 mL de solução a 0,5% contém:
| metronidazol | 500 mg |
| excipientes q.s.p | 100 mL |
Excipientes: fosfato de sódio dibásico dodeca-hidratado, ácido cítrico anidro, cloreto de sódio, água para injetáveis.
Cada 1 mL de solução contém 5 mg de metronidazol.
INFORMAÇÕES AO PACIENTE
PARA QUE ESSE MEDICAMENTO É INDICADO?
Este medicamento está indicado na profilaxia e tratamento das infecções1 causadas por bactérias anaeróbias (que crescem na presença de baixas concentrações de oxigênio ou até mesmo na sua ausência) como Bacteroides fragilis e outros bacteróides, Fusobacterium sp; Clostridium sp; Eubacterium sp; e cocos anaeróbios. Está indicado, também, na prevenção e tratamento das infecções1 pós-cirúrgicas, nas quais os anaeróbios tenham sido identificados ou suspeitados.
Metronidazol solução injetável deve ser administrado nos casos em que a via oral está contraindicada ou impossibilitada.
COMO ESTE MEDICAMENTO FUNCIONA?
Metronidazol é um anti-infeccioso que apresenta atividade antimicrobiana, que abrange exclusivamente microrganismos anaeróbios, e atividade antiparasitária. A absorção máxima ocorre ao final da infusão.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Metronidazol não deve ser usado se você já teve alergia2 ao metronidazol ou outro derivado imidazólico e/ou aos demais componentes do produto.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Advertências e precauções
O tratamento com duração prolongada com Metronidazol deve ser cuidadosamente avaliado. O uso deste medicamento para tratamento de duração prolongada deve ser avaliado com cuidado
Caso o tratamento com metronidazol, por razões especiais, necessite de uma duração maior do que a geralmente recomendada, procure seu médico para realizar testes hematológicos (sangue3) regularmente, principalmente contagem de leucócitos4, seu médico irá monitorá-lo quanto ao aparecimento de reações adversas, como neuropatia5 (doença que afeta um ou vários nervos) central ou periférica, por exemplo: parestesia6 (sensações cutâneas7 subjetivas como frio, calor, formigamento, pressão), ataxia8 (falta de coordenação dos movimentos), vertigem9 (tontura10) e crises convulsivas.
Metronidazol pode provocar escurecimento da urina11 (devido aos metabólitos12 de metronidazol). Você não deve ingerir bebidas alcoólicas ou medicamentos que contenham álcool em sua formulação durante e no mínimo 1 dia após o tratamento com metronidazol, devido à possibilidade de efeito antabuse13, com aparecimento de rubor (vermelhidão), vômito14 e taquicardia15 (aceleração do ritmo cardíaco).
Foram reportados casos de hepatotoxicidade16 (toxicidade17 no fígado18)/insuficiência hepática19 aguda (redução da função do fígado18), incluindo casos fatais, com início muito rápido após o começo do tratamento, em pacientes com Síndrome20 de Cockayne [(doença hereditária rara, caracterizada por várias anomalias, entres as quais: transtornos de fotossensibilidade (excesso de sensibilidade à luz solar), atraso grave do desenvolvimento físico, retardo mental grave, microcefalia21, envelhecimento prematuro, perda auditiva e, dependendo da gravidade, morte precoce)] usando medicamentos contendo metronidazol para uso sistêmico22. Portanto, nesta população, o metronidazol deve ser utilizado após uma cuidadosa avaliação de risco-benefício, e apenas se não houver tratamento alternativo disponível.
Os testes da função do fígado18 devem ser realizados imediatamente antes do início do tratamento, durante e após o término do tratamento até que a função do fígado18 esteja dentro dos limites normais ou até que os valores basais sejam atingidos. Se os testes da função do fígado18 se tornarem acentuadamente elevados durante o tratamento, o medicamento deve ser descontinuado.
Os pacientes com Síndrome20 de Cockayne devem ser aconselhados a informar imediatamente ao seu médico quaisquer sintomas23 de potencial dano ao fígado18 e parar de utilizar metronidazol.
Foram notificados casos de reações cutâneas7 bolhosas severas, como síndrome20 de Stevens Johnson (SSJ), necrólise epidérmica tóxica24 (NET) ou pustulose exantemática generalizada aguda (PEGA) com metronidazol (vide Reações adversas). Se estiverem presentes sintomas23 ou sinais25 de SSJ, NET ou PEGA, o tratamento com Metroniflex (metronidazol) deve ser imediatamente interrompido.
Gravidez26 e amamentação27
O uso de metronidazol durante a gravidez26 deve ser cuidadosamente avaliado visto que atravessa a barreira placentária e seus efeitos sobre a organogênese (formação das células28 que estão formando o feto29) fetal humana ainda são desconhecidos.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Visto que o metronidazol é excretado no leite materno, a exposição desnecessária ao medicamento deve ser evitada.
Populações especiais
Não há advertências e recomendações especiais sobre o uso adequado desse medicamento em pacientes idosos.
Metronidazol deve ser administrado com cautela em pacientes com encefalopatia30 hepática31 (disfunção do sistema nervoso central32 em associação com falência hepática31), pois o mesmo é metabolizado pelo fígado18. Siga a orientação do seu médico.
Metronidazol deve ser utilizado com cautela em pacientes com doença severa, ativa ou crônica, do sistema nervoso central32 e periférico, devido ao risco de agravamento do quadro neurológico. Siga a orientação do seu médico.
Alterações na capacidade de dirigir veículos e operar máquinas
Você não deve dirigir veículos ou operar máquinas caso estes sintomas23 ocorram: confusão, tontura10, alucinações33, convulsões ou alterações visuais (vide “8. Quais os males que este medicamento pode me causar?”).
INTERAÇÕES MEDICAMENTOSAS
Álcool: bebidas alcoólicas e medicamentos contendo álcool não devem ser ingeridos durante o tratamento com metronidazol e, no mínimo, 1 dia após o mesmo, devido à possibilidade de reação do tipo dissulfiram (efeito antabuse13), com aparecimento de rubor, vômito14 e taquicardia15.
Dissulfiram: foram relatadas reações psicóticas em pacientes utilizando concomitantemente metronidazol e dissulfiram.
Terapia com anticoagulante34 oral (tipo varfarina): potencialização do efeito anticoagulante34 e aumento do risco hemorrágico35 causado pela diminuição da metabolização desta medicação pelo fígado18. Em caso de administração concomitante, o médico deve monitorar o tempo de protrombina36 com maior frequência e realizar ajuste posológico da terapia anticoagulante34 durante o tratamento com metronidazol.
Lítio: os níveis no plasma37 de lítio podem ser aumentados pelo metronidazol. O médico deve monitorar as concentrações plasmáticas de lítio, creatinina38 e eletrólitos39 enquanto durar o tratamento com metronidazol.
Ciclosporina: risco de aumento dos níveis no plasma37 de ciclosporina. Os níveis plasmáticos de ciclosporina e creatinina38 devem ser rigorosamente monitorados pelo médico.
Fenitoína ou fenobarbital: aumento da eliminação de metronidazol, resultando em níveis no plasma37 reduzidos.
Fluoruracila: o uso concomitante com metronidazol aumenta a sua toxicidade17.
Bussulfano: os níveis no plasma37 de bussulfano podem ser aumentados pelo metronidazol, o que pode levar a uma severa toxicidade17 do bussulfano.
Informe ao seu médico se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde40.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Metronidazol deve ser mantido em temperatura ambiente (entre 15 e 30ºC). Proteger da luz e umidade.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Depois de aberto, este medicamento deve ser utilizado imediatamente. Não é recomendado o reaproveitamento do seu conteúdo ou seu armazenamento em geladeiras para ser novamente reutilizado em pacientes.
Características do medicamento
Líquido límpido apresentando uma ligeira coloração amarela e isento de partículas.
Antes de usar observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
Por ser um medicamento que deverá ser manipulado e administrado exclusivamente por profissionais especializados, as orientações para manipulação e administração do medicamento e descarte estão contidas no texto de bula destinado aos profissionais de saúde40. Em caso de dúvidas, consulte o seu médico.
Não há estudos dos efeitos de Metronidazol injetável administrado por vias não recomendadas. Portanto, por segurança e para eficácia deste medicamento, a administração deve ser somente pela via intravenosa.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento de seu médico.
Modo de usar
Usar somente se a solução estiver límpida, sem partículas visíveis e se a embalagem não estiver danificada. Administrar imediatamente após a inserção do equipo de administração.
Não remover a bolsa da sobrebolsa até que esteja pronta para uso. A sobrebolsa mantém a esterilidade41 do produto.
Não usar embalagens primarias em conexões em serie. Tal procedimento pode causar embolia42 gasosa devido ao ar residual
aspirado da primeira embalagem antes que a administração de fluído da segunda embalagem seja completada. A solução deve ser administrada com equipo estéril usando técnica asséptica. O equipo deve ser preparado primado com a solução a fim de impedir que o ar entre no sistema.
Adição de outros medicamentos ou uso de uma técnica de administração incorreta pode causar o aparecimento de reações febris, devido à possível introdução de pirogênios. No caso de reação adversa, a infusão deve ser interrompida imediatamente.
Descartar após o uso único.
Descarte qualquer porção não utilizada.
Não reconectar bolsas parcialmente utilizadas.
Para abrir:
- Segurar o invólucro protetor (sobrebolsa) com ambas as mãos43, rasgando-o no sentido do picote, de cima para baixo, e retirar a bolsa contendo solução. Pequenas gotículas entre a bolsa e a sobrebolsa podem estar presentes e é característica do produto e processo produtivo. Alguma opacidade do plástico da bolsa pode ser observada devido ao processo de esterilização. Isto é normal e não afeta a qualidade ou segurança da solução. A opacidade irá diminuir gradualmente.
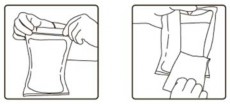
- Verificar se existem vazamentos mínimos comprimindo a embalagem primária com firmeza.
- Se for observado vazamento de solução descartar a bolsa, pois a sua esterilidade41 pode estar comprometida.
- No preparo e administração das soluções parenterais, devem ser seguidas as recomendações da Comissão de Controle de Infecção44 em Serviços de Saúde40 quanto a: desinfecção45 do ambiente e de superfícies, higienização das mãos43, uso de EPIs e desinfecção45 de ampolas, frascos, pontos de adição dos medicamentos e conexões das linhas de infusão.
Preparação para administração
Utilizar material estéril.
- Suspender a embalagem pela alça de sustentação.
- Remover o protetor de plástico do tubo de saída da solução no fundo da embalagem.
Utilizar técnica asséptica para preparar a infusão.
Conectar o equipo de infusão da solução. Consultar as instruções de uso do equipo.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Seu médico terá as instruções de quando administrar este medicamento para você. Entretanto, se você acha que uma dose não foi administrada, converse com seu médico.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento).
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento).
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento).
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento).
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento).
Distúrbios gastrintestinais: dor epigástrica (dor de estômago46), náusea47, vômito14, diarreia48, mucosite49 oral (inflamação50 dos tecidos moles da boca51), alterações no paladar52 incluindo gosto metálico, anorexia53(redução ou perda do apetite) , casos reversíveis de pancreatite54 (inflamação50 no pâncreas55), descoloração da língua56/ sensação de língua56 áspera (devido ao crescimento de fungos, por exemplo).
Distúrbios do sistema imunológico57: angioedema58 (presença de edema59 de pele60, mucosas61 ou vísceras, acompanhadas de urticárias), choque anafilático62 (reação alérgica63 grave).
Distúrbios do sistema nervoso64: neuropatia5 (doença que afeta um ou vários nervos) sensorial periférica, dores de cabeça65, convulsões, tontura10, relatos de encefalopatia30 (por exemplo, confusão) e síndrome20 cerebelar subaguda66 [por exemplo, ataxia8, disartria67 (dificuldade de articular as palavras), alteração da marcha (dificuldade de andar), nistagmo68 (movimento involuntário, rápido e repetitivo do globo ocular69) e tremor], que podem ser resolvidos com a descontinuação do tratamento com o medicamento, meningite asséptica70 (inflamação50 nas membranas e tecidos que envolvem o cérebro71 sem causa infecciosa).
Distúrbios psiquiátricos: alterações psicóticas incluindo confusão e alucinações33, humor depressivo.
Distúrbios visuais: alterações visuais transitórias como diplopia72 (visão73 dupla) e miopia74 (visão73 curta), visão73 borrada, diminuição da acuidade (qualidade) visual e alteração da visualização das cores, neuropatia5 óptica (doença que afeta um ou vários nervos, neste caso o nervo óptico)/neurite75 (inflamação50 do nervo óptico).
Distúrbios no sangue3 e no sistema linfático76: foram relatados casos de agranulocitose77 (diminuição acentuada na contagem de células brancas do sangue78), neutropenia79 (diminuição do número de neutrófilos80 no sangue3) e trombocitopenia81 (diminuição no número de plaquetas82 sanguíneas).
Distúrbios hepatobiliares83:
- foram relatados casos de aumento das enzimas do fígado18 (AST, ALT, fosfatase alcalina84), hepatite85 colestática ou mista (tipos de inflamações86 do fígado18) e lesão87 das células28 do fígado18, algumas vezes se manifestando com icterícia88 (cor amarelada da pele60 e olhos89).
- foram relatados casos de falência da função do fígado18 necessitando de transplante em pacientes tratados com metronidazol em associação com outras drogas antibióticas.
Distúrbios na pele e tecido subcutâneo90: rash91 (erupções cutâneas7), prurido92 (coceira), rubor, urticária93 (erupção94 na pele60, geralmente de origem alérgica, que causa coceira), erupções pustulosas (pequenas bolhas com conteúdo amarelado "pus"), síndrome de Stevens-Johnson95 (forma grave de reação alérgica63 caracterizada por bolhas em mucosas61 e em grandes áreas do corpo), necrólise epidérmica tóxica24 (quadro grave, caracterizado por erupção94 generalizada, com bolhas rasas extensas e áreas de necrose96 epidérmica, à semelhança de grande queimadura, resultante principalmente de uma reação tóxica a vários medicamentos).
Distúrbios gerais: febre97.
Informe ao seu médico ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento.
Informe também a empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Apesar de a correta via de administração desta apresentação de Metronidazol ser intravenosa e, não se dispor de informações sobre casos de superdosagem por esta via, cabe informar que foram relatadas ingestões orais únicas de doses de até 12 g de metronidazol em tentativas de suicídio e superdoses acidentais. Em caso de suspeita de superdose maciça, deve-se instituir tratamento sintomático98 e de suporte. Os sintomas23 ficaram limitados a vômito14, ataxia8 (falta de coordenação dos movimentos) e desorientação leve. Não existe antídoto99 específico para superdoses com metronidazol. Em caso de suspeita de superdose maciça, será instituído tratamento sintomático98 e de suporte pelo médico.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
USO RESTRITO A HOSPITAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Reg. MS n° 1.0683.0115
Farm. Resp.: Luiz Gustavo Tancsik CRF/SP: 67.982
Registrado por:
Baxter Hospitalar Ltda.
Av. Dr. Chucri Zaidan, 1.240
Torre B, 12º andar, conj 1201 e 1204 – São Paulo – SP – Brasil.
CNPJ nº 49.351.786/0001-80
Fabricado e Embalado por:
Baxter Hospitalar Ltda.
Av. Eng. Eusebio Stevaux, 2555 - Sao Paulo - SP - Brasil
CNPJ. 49.351.786/0002-61
Indústria Brasileira
SAC 08000 12 5522