

Taltz
ELI LILLY DO BRASIL LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
TALTZ®
ixequizumabe
Solução injetável
APRESENTAÇÕES
TALTZ é disponibilizado como uma solução injetável de dose-única em caneta contendo 80 mg de ixequizumabe em 1 mL (80 mg/mL).
Embalagem contendo 1 ou 3 canetas, com 1 mL de solução contendo 80 mg de ixequizumabe.
USO SUBCUTÂNEO1
USO ADULTO
COMPOSIÇÃO
Cada 1 mL contém:
| ixequizumabe | 80 mg |
| excipiente q.s.p. | 1 mL |
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
TALTZ é indicado para o tratamento de pacientes adultos com psoríase2 em placas3 moderada a grave, que é um distúrbio inflamatório crônico4 da pele5, e que são candidatos ao tratamento com medicamentos sistêmicos6 (ou seja, medicamentos que precisam atingir a corrente sanguínea para ter sua ação) ou fototerapia (modalidade terapêutica7 baseada na interação da irradiação da luz na pele5).
TALTZ, utilizado sozinho ou em associação com o metotrexato, é indicado para o tratamento da artrite8 psoriásica (doença inflamatória das articulações9 associada à psoríase2) em pacientes adultos que obtiveram uma resposta insuficiente ou foram intolerantes ao tratamento com um ou mais medicamentos antirreumáticos modificadores da doença (DMARD).
COMO ESTE MEDICAMENTO FUNCIONA?
O princípio ativo de TALTZ é o ixequizumabe, que é um anticorpo10 monoclonal. Anticorpos11 monoclonais são proteínas12 que possuem a capacidade de reconhecer e se ligar a outras proteínas12 específicas. Na psoríase2, a interleucina 17A (IL-17A) é a proteína pró-inflamatória que desempenha um papel importante ao desencadear a ativação e proliferação excessivas dos queratinócitos13 (que são células14 encontradas na camada mais superficial da pele5). A excessiva proliferação dos queratinócitos13 pode causar sintomas15 como coceira, dor, descamação16 e inchaço17. O ixequizumabe neutraliza as ações que são induzidas pela IL-17A, reduzindo, assim, o processo inflamatório e os sintomas15 da psoríase2.
Na artrite8 psoriásica, a neutralização da IL-17A reduz os sintomas15 da doença através da diminuição do processo inflamatório nas articulações9 afetadas pela psoríase2.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
TALTZ não deve ser usado em pacientes alérgicos ao ixequizumabe ou a qualquer um dos componentes da formulação.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Advertências e precauções
O tratamento com TALTZ está associado a um aumento da taxa de infecções18, como infecções18 das vias aéreas superiores, candidíase19 oral (infecção20 na boca21 causada por fungo22), conjuntivite23 (inflamação24 da película que recobre os olhos25) e infecções18 por tínea (infecção20 superficial da pele5 causada por fungo22) (ver QUAIS MALES ESTE MEDICAMENTO PODE ME CAUSAR?). TALTZ deve ser usado com cautela se você apresenta alguma infecção20 crônica ou infecção20 ativa clinicamente importante, tais como vírus26 da imunodeficiência27 humana (HIV28), vírus26 da hepatite29 B (HBV) e vírus26 da hepatite29 C (HCV).
Você deve buscar aconselhamento médico caso apresente sinais30 e sintomas15 de infecção20 (tais como febre31 alta, calafrios32, cansaço, entre outros). O tratamento com TALTZ não deve ser retomado até que a infecção20 esteja resolvida.
TALTZ não deve ser administrado a pacientes com tuberculose33. Os pacientes recebendo TALTZ devem ser monitorados de perto quanto ao aparecimento de sinais30 e sintomas15 de tuberculose33, durante e após o tratamento.
Reações graves de hipersensibilidade (reação alérgica34 grave generalizada) foram relatadas. Se ocorrer uma reação de hipersensibilidade grave, o uso de TALTZ deve ser interrompido imediatamente pelo médico e o tratamento apropriado deve ser iniciado.
Casos novos ou exacerbações da doença de Crohn35 (doença inflamatória do trato gastrointestinal) e colite36 ulcerativa (inflamação24 no intestino) foram relatados. Recomenda-se monitoramento cuidadoso para pacientes37 com doença inflamatória do intestino.
Antes de iniciar o tratamento com TALTZ, o médico deve avaliar a conclusão de todas as vacinas adequadas à sua idade, de acordo com as diretrizes atuais de imunização38. Não estão disponíveis dados sobre a resposta imunológica à administração de vacinas vivas (aquelas que contém um microrganismo atenuado) durante o tratamento com TALTZ.
Não existem dados suficientes em humanos para estabelecer a segurança de ixequizumabe durante a gravidez39 (Categoria B). Como medida de precaução, é preferível evitar o uso de TALTZ durante a gravidez39. Mulheres com potencial para engravidar deverão utilizar um método contraceptivo eficaz durante o tratamento com TALTZ e durante pelo menos 10 semanas após o tratamento.
Não se sabe se ixequizumabe é excretado no leite humano ou absorvido após a ingestão. Os benefícios da amamentação40 sobre o desenvolvimento e a saúde41 do bebê devem ser considerados juntamente com a necessidade clínica da mãe quanto ao uso de TALTZ e com quaisquer efeitos adversos potenciais de TALTZ ou da condição materna subjacente sobre o lactente42.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
A segurança e a eficácia de TALTZ em pacientes pediátricos não foram avaliadas.
Embora não tenham sido observadas diferenças na segurança ou eficácia entre pacientes mais idosos e mais jovens, o número de pacientes com 65 anos ou mais, expostos a TALTZ, não é suficiente para determinar se estes respondem de modo diferente de pacientes mais jovens.
Não há efeitos conhecidos sobre a capacidade de conduzir ou utilizar máquinas associado ao uso de TALTZ.
Interações medicamentosas
Terapias concomitantes: a segurança de TALTZ em combinação com outros agentes imunomoduladores (agentes que inibem ou estimulam as reações imunológicas do organismo) ou com fototerapia (modalidade terapêutica7 baseada na interação da irradiação da luz na pele5) não foi avaliada durante os estudos clínicos de psoríase2. A ação de ixequizumabe não foi afetada com a administração concomitante de metotrexato.
Vacinas vivas: as vacinas vivas (aquelas que contêm um microrganismo atenuado) não deverão ser administradas durante o tratamento com TALTZ (ver O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO? Advertências e precauções).
Nenhum estudo foi conduzido para investigar a possível interação entre TALTZ e plantas medicinais, álcool, nicotina e exames laboratoriais e não laboratoriais.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use este medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde41.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
TALTZ deve ser protegido da luz até sua utilização. Armazenar refrigerado de 2 a 8°C. Não congelar. Não usar TALTZ se tiver sido congelado. Não agitar.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
TALTZ é uma solução estéril, livre de conservantes, límpida e incolor a ligeiramente amarela.
Descartar qualquer porção não utilizada.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
COMO DEVO USAR ESTE MEDICAMENTO?
Posologia
Psoríase2 em placas3
A dose recomendada é 160 mg por injeção subcutânea43 (duas injeções de 80 mg) na semana 0, seguida por uma injeção44 de 80 mg nas semanas 2, 4, 6, 8, 10 e 12 e então, 80 mg a cada 4 semanas. O médico deve considerar a interrupção do tratamento em pacientes que não apresentaram resposta após 16 a 20 semanas de tratamento. Alguns pacientes com resposta inicialmente parcial podem posteriormente melhorar com o tratamento continuado além de 20 semanas.
Artrite8 psoriásica
A dose recomendada é 160 mg por injeção subcutânea43 (duas injeções de 80 mg) na semana 0, seguida de 80 mg a cada 4 semanas. Para pacientes37 com artrite8 psoriásica e psoríase2 em placas3 moderada a severa coexistentes, utilizar o regime de dose para psoríase2 em placas3.
TALTZ pode ser administrado sozinho ou em combinação com um medicamento anti-reumático modificador da doença (Disease Modifying Anti-rheumatoid Drugs - DMARD) convencional (por exemplo, metotrexato).
Modo de usar: TALTZ é para administração subcutânea45 (sob a pele5). Após o treinamento sobre a técnica de injeção subcutânea43, o paciente pode auto-injetar TALTZ.
Administrar cada injeção44 em um local de aplicação diferente (como braços, coxas46 ou qualquer quadrante do abdome47) da injeção44 anterior. Não administrar a injeção44 em áreas onde a pele5 está sensível, com hematoma48, eritematosa49 (com lesões50 avermelhadas na pele5), com tumefação51 (inchada) ou afetada por psoríase2. A administração de TALTZ na parte externa do braço poderá ser realizada por um cuidador ou profissional da saúde41.
Leia com atenção as INSTRUÇÕES DE USO que acompanham o produto. Elas possuem informações mais detalhadas sobre a preparação e administração de TALTZ. Em caso de problemas de funcionamento do dispositivo injetor de TALTZ, consulte o folheto informativo e entre em contato com o Lilly SAC 0800 701 0444.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
INSTRUÇÕES DE USO DE TALTZ®
1. PREPARE-SE
1a. Retire o auto-injetor do refrigerador. Deixe a tampa da base até que você esteja pronto para injetar. Espere 30 minutos para que o auto-injetor atinja a temperatura ambiente antes de você usá-lo. Isso fará com que o medicamento fique mais fácil de injetar.
NÃO levar o auto-injetor ao micro-ondas, NÃO colocar água quente sobre o auto-injetor e não expor o auto-injetor à luz solar direta.

1b. Junte os materiais para a sua injeção44:
- 1 compressa embebida em álcool
- 1 bola de algodão ou gaze
- 1 recipiente para descarte de materiais cortantes do auto-injetor
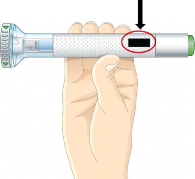
1c. Inspecione a caneta. Verifique o rótulo. Certifique-se que o nome TALTZ aparece no rótulo. Também certifique-se que o medicamento não esteja vencido.
O medicamento dentro deve estar límpido. A cor pode variar de incolor a ligeiramente amarela. É normal ter bolhas de ar no auto- injetor.
Se você vir qualquer um dos itens seguintes, NÃO USE o auto-injetor e descarte-o como indicado:
- Já passou a data de validade
- Ele parece danificado
- O medicamento está turvo, com cor marrom, ou tem pequenas partículas
1d. Lave suas mãos52 antes de injetar o seu medicamento.
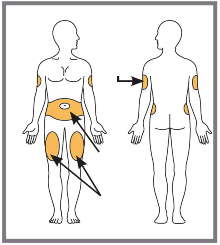
1e. Escolha o local da sua injeção44.
Você pode injetar em seu abdome47 (área do estômago53), em sua coxa54 ou na parte de trás do seu braço. Para injetar em seu braço, você vai precisar de alguém para ajudá-lo. NÃO injetar em áreas onde a pele5 esteja sensível, machucada, vermelha ou dura, ou onde você tem cicatrizes55 ou estrias. NÃO injetar dentro da área de 2,5 cm (aproximadamente do tamanho do seu polegar) próxima ao umbigo56.
Alternar os seus locais de injeção44. NÃO injetar exatamente no mesmo local toda vez. Por exemplo, se a sua última injeção44 foi em sua coxa54 esquerda, a sua próxima injeção44 deve ser na sua coxa54 direita, abdome47 ou na parte de trás de qualquer braço.
1f. Prepare sua pele5. Limpe a pele5 com uma compressa embebida em álcool. Deixe o local da injeção44 secar antes de injetar o medicamento.
INJEÇÃO44
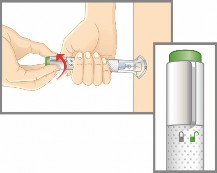
2a. Certifique-se que o anel de travamento está na posição travada.
Deixe a tampa da base até que esteja pronto para injetar.
NÃO toque na agulha.
Gire a tampa da base.
Jogue fora a tampa da base. Você não vai precisar colocar a tampa da base de volta – isso poderia danificar a agulha ou você poderia furar-se por acidente.
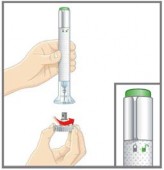
2b. Coloque a base transparente de forma plana e firme contra a sua pele5.
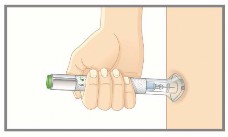
2c. Mantenha a base sobre a sua pele5, e em seguida, vire o anel de travamento para a posição destravada. Agora você está pronto para injetar.
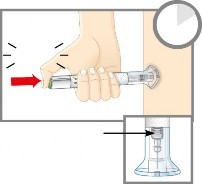
2d. Pressione o botão verde de injeção44. Você irá ouvir um clique alto.
Continue segurando a base transparente firmemente contra a sua pele5.
Você vai ouvir um segundo clique cerca de 5 a 10 segundos após o primeiro. O segundo clique diz que a injeção44 está completa. Você também verá o êmbolo57 cinza na parte superior da base transparente.
Remova a caneta da sua pele5. Pressione uma bola de algodão ou gaze sobre o local da injeção44.
NÃO esfregue o local da injeção44, pois isso pode causar hematomas58. Você pode ter um leve sangramento. Isto é normal.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Para o melhor benefício da medicação é importante seguir a programação prescrita pelo seu médico. Se uma dose for perdida, administrá-la o mais rápido possível. Em seguida, retomar a dosagem no horário regular programado. Em caso de dúvidas, contate seu médico para informações sobre como agir. Não é recomendado usar dose duplicada para compensar uma dose esquecida.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião- dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Dados provenientes dos estudos clínicos
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): infecção20 do trato respiratório superior [inclui nasofaringite (inflamação24 do nariz59 e faringe60) e infecção20 das vias aéreas superiores] e reações no local da injeção44.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): dor orofaríngea61 (dor de garganta62), náusea63 (vontade de vomitar) e infecção20 por tínea (infecção20 superficial da pele5 causada por fungo22).
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento): influenza64 (gripe65), rinite66 (inflamação24 da mucosa67 nasal), celulite68 (infecção20 aguda da pele5 causada por bactéria69), urticária70 (reação da pele5 caracterizada por vermelhidão e coceira), neutropenia71 [diminuição do número de neutrófilos72 (um tipo de glóbulo branco) no sangue73], candidíase19 oral (infecção20 na boca21 causada por fungos), trombocitopenia74 (diminuição do número de plaquetas75 no sangue73) e conjuntivite23 (inflamação24 da película que recobre os olhos25).
Os eventos adversos em pacientes tratados com ixequizumabe 160 mg por injeção subcutânea43, seguida de 80 mg a cada 4 semanas, nos estudos clínicos de artrite8 psoriásica foram similares, com exceção da frequência de influenza64 (comum) e conjuntivite23 (comum).
Reações no local da injeção44: as reações no local de injeção44 mais frequentes foram eritema76 (lesões50 avermelhadas na pele5) e dor. As reações no local da injeção44 foram predominantemente leves a moderadas em termos de gravidade e não levaram à interrupção do tratamento com ixequizumabe.
Dados pós-comercialização:
O seguinte evento adverso é baseado em relatos espontâneos pós-comercialização:
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento): anafilaxia77 (reação alérgica34 grave generalizada).
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião-dentista.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Doses de até 180 mg foram administradas por via subcutânea45 em pesquisas clínicas sem toxicidade78 limitante da dose. Superdoses de até 240 mg, por via subcutânea45, foram relatadas sem quaisquer efeitos adversos graves. Em caso de superdose, recomenda-se que o paciente seja monitorado para quaisquer sinais30 ou sintomas15 de reações adversas, e que o tratamento sintomático79 adequado seja instituído imediatamente.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
Venda sob prescrição médica
Registro MS - 1.1260.0196
Farm. Resp.: Márcia A. Preda - CRF-SP nº 19.189
Fabricado por:
ELI LILLY AND COMPANY
Indianápolis - EUA
Importado por:
ELI LILLY DO BRASIL LTDA.
Av. Morumbi, 8264 - São Paulo, SP - Brasil
CNPJ 43.940.618/0001-44
SAC 0800 701 0444






