

Lynoz
CRISTÁLIA PRODUTOS QUÍMICOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Lynoz
linezolida
Solução para infusão 2 mg/mL
Medicamento similar equivalente ao medicamento de referência.
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução para infusão
Embalagens contendo 1 ou 10 bolsas de solução para infusão
USO INTRAVENOSO
USO ADULTO E PEDIÁTRICO
SISTEMA FECHADO
COMPOSIÇÃO:
Cada mL de Lynoz contém:
| linezolida | 2 mg |
| veículo q.s.p. | 1 mL |
Veículo: citrato de sódio di-hidratado, ácido cítrico, glicose1, ácido clorídrico2* e água para injetáveis.
* para ajuste de pH
| Conteúdo eletrolítico | |
| Sódio (Na+) | 16,73 mEq/L |
| Citrato (C6 H5O7 3-) | 30,00 mEq/L |
| Osmolaridade3: | 286 mOsm/L |
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Lynoz (linezolida) é indicado para o tratamento de infecções4, quando se sabe ou se presume que a infecção5 seja causada por bactérias suscetíveis (sensíveis) a linezolida. Nessas infecções4 estão incluídas pneumonias (hospitalares ou adquiridas na comunidade), infecções4 de pele6 e de tecidos moles (incluindo pé diabético, não associado à osteomielite7 – infecção5 do osso) e infecções4 enterocócicas (causadas por um tipo de bactéria8).
COMO ESTE MEDICAMENTO FUNCIONA?
Lynoz pertence a uma nova classe de antibióticos. A linezolida atua inibindo e interrompendo o processo de multiplicação de alguns tipos de bactérias.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Lynoz é contraindicado a pacientes que apresentam hipersensibilidade (alergia9) a linezolida ou a qualquer componente da fórmula. A linezolida também é contraindicada a pacientes que estejam usando qualquer medicamento que seja um inibidor da enzima10 monoaminoxidase (proteína que aumenta a velocidade de uma determinada reação química) (ex.: fenelzina, isocarboxazida) ou até duas semanas de uso de qualquer um destes medicamentos. A linezolida é contraindicada a pacientes que apresentam: hipertensão11 (pressão alta) não controlada, feocromocitoma12 (tumor13, normalmente benigno, que causa aumento da pressão), tireotoxicose (conjunto de sintomas14 como nervosismo, perda de peso, suor excessivo, entre outros, que ocorrem pelo excesso de hormônios da tireoide15), síndrome16 carcinoide (conjunto de sintomas14 causados por um tipo especifico de câncer17) e/ou pacientes utilizando algum dos seguintes tipos de medicamentos: agentes simpatomiméticos de ação direta ou indireta (ex.: pseudoefedrina, fenilpropanolamina), agentes vasoconstritores (ex.: epinefrina, norepinefrina), agentes dopaminérgicos (ex.: dopamina18, dobutamina), inibidores de recaptação de serotonina, antidepressivos tricíclicos, agonistas do receptor de serotonina 5-HT1 (triptanos), meperidina ou buspirona.
Atenção: Este medicamento contém AÇÚCAR19, portanto, deve ser usado com cautela em diabéticos.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Leia também a resposta da questão “8. Quais os males que este medicamento pode me causar?”.
Gerais: Não foram estabelecidas a segurança e a eficácia de linezolida quando administrada por períodos superiores a 28 dias. A linezolida não tem atividade clínica contra patógenos Gram-negativos e não é indicado para o tratamento de infecções4 Gram-negativas. É exigida terapia Gram-negativa específica caso se confirme ou se suspeite de um patógeno Gram-negativo concomitante.
Relatou-se a ocorrência de colite20 pseudomembranosa, de grau leve a risco de morte, com o uso de quase todos os agentes antibacterianos, incluindo a linezolida.
Mielossupressão (supressão da formação de células21 que formam o sangue22 pela medula óssea23): Mielossupressão reversível (anemia24, trombocitopenia25, leucopenia26 e pancitopenia27) foi relatada em alguns pacientes recebendo linezolida, que pode ser dependente da duração da terapia com linezolida. Deve-se considerar o monitoramento com hemograma completo de pacientes que tenham risco aumentado de sangramento, com história de mielossupressão preexistente, que receberem, concomitantemente, medicações que possam diminuir os níveis de hemoglobina28, a contagem ou a função das plaquetas29 ou que receberem linezolida por mais de 2 semanas.
Neuropatia periférica30 e óptica: Caso surjam sintomas14 de insuficiência31 visual, como alterações na acuidade visual32 (visão33 embaçada, perda de foco), visão33 de cores, visão33 embaçada ou defeito no campo visual34, é recomendada uma avaliação oftálmica imediata. A função visual deve ser monitorada em todos os pacientes recebendo linezolida por períodos prolongados (3 meses ou mais) e em todos os pacientes que relatarem novos sintomas14 visuais.
Síndrome serotoninérgica35: Relatos espontâneos muito raros de Síndrome serotoninérgica35 (pressão alta, rigidez muscular, tremores, aumento da temperatura, aumento dos batimentos cardíacos) incluindo casos fatais foram relatados com a coadministração de linezolida e agentes serotoninérgicos (vide item 3. Quando não devo usar este medicamento?).
Infecções4 da corrente sanguínea relacionadas ao cateter, incluindo pacientes com infecções4 relacionadas ao acesso vascular36: A linezolida não é aprovada e não deve ser usada para o tratamento de pacientes com infecções4 da corrente sanguínea relacionadas ao cateter ou infecções4 relacionadas ao acesso vascular36.
Diarreia37 associada a Clostridium difficile: Foi relatada diarreia37 associada a Clostridium difficile com a maioria dos agentes antibacterianos, incluindo a linezolida, que pode variar de diarreia37 leve a colite20 fatal. Se há suspeita ou confirmação de diarreia37 associada a C. difficile, pode ser necessário interromper o uso de antibiótico em curso não dirigido contra C. difficile. A administração de eletrólitos38 e fluido adequado, suplementação39 de proteína, tratamento antibiótico do C. difficile e avaliação cirúrgica devem ser instituídos como clinicamente indicado.
Acidose40 láctica41
Acidose40 láctica41 foi relatada com o uso de linezolida. Pacientes que apresentaram náusea42 ou vômito43 recorrente, acidose40 não explicada ou baixo nível de bicarbonato durante o tratamento com linezolida devem receber atenção médica imediata.
Convulsões
Houve raros relatos de convulsões em pacientes tratados com linezolida. Na maioria dos casos, já havia um histórico ou fatores de risco de convulsões.
Hipoglicemia44 (diminuição do açúcar19 no sangue22)
Foram relatados casos pós-comercialização de hipoglicemia44 sintomática45 em pacientes com diabetes46 mellitus recebendo insulina47 ou agentes hipoglicemiantes orais48 quando tratados com linezolida, um inibidor da MAO49 não seletivo, reversível. Alguns inibidores da MAO49 foram associados com episódios hipoglicêmicos em pacientes diabéticos que receberam insulina47 ou agentes hipogliêmicos. Embora uma relação causal entre a linezolida e a hipoglicemia44 não tenha sido estabelecida, os pacientes diabéticos devem ser alertados do potencial de reações hipoglicêmicos quando tratados com linezolida. Se ocorrer hipoglicemia44, pode ser necessária uma diminuição da dose de insulina47 ou do agente hipoglicêmico oral, ou a descontinuação do agente hipoglicemiante50 oral, insulina47 ou a linezolida.
Desenvolvimento de resistência bacteriana
Na ausência de infecção5 bacteriana comprovada, fortemente suspeita ou de indicação profilática, é improvável que a prescrição da linezolida possa oferecer benefício aos pacientes; no entanto, pode aumentar o risco de desenvolvimento de resistência bacteriana.
Gravidez51 e Lactação52
Não há estudos adequados e bem controlados em gestantes. Portanto, a linezolida deve ser usada durante a gravidez51 somente se o benefício potencial justificar o risco potencial para o feto53.
Não se sabe se a linezolida é excretada no leite humano. Portanto, deve-se ter cautela quando a linezolida é administrada a mulheres lactantes54.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-- dentista.
Efeitos na habilidade de dirigir e usar máquinas
O efeito da linezolida sobre a habilidade de dirigir ou operar máquinas não foi sistematicamente avaliada.
Interações medicamentosas
Alguns pacientes recebendo linezolida podem apresentar aumento leve e reversível da pressão sanguínea induzida pelas medicações pseudoefedrina ou fenilpropanolamina. As doses iniciais de fármacos adrenérgicos55, como a dopamina18 ou agonistas da dopamina18, devem ser reduzidas e ajustadas pelo seu médico para se alcançar a resposta desejada.
Antibióticos
Não foram observadas interações nos estudos de farmacocinética com o aztreonam ou a gentamicina. O mecanismo da interação entre rifampicina e linezolida e seu significado clínico são desconhecidos. Sempre avise ao seu médico todas as medicações que você toma quando ele for prescrever uma medicação nova. O médico precisa avaliar se as medicações reagem entre si alterando a sua ação, ou da outra; isso se chama interação medicamentosa.
Informações importantes sobre um dos componentes do medicamento
Atenção: Este medicamento contém AÇÚCAR19, portanto, deve ser usado com cautela em portadores Diabetes46.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde56.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Lynoz, solução para infusão, deve ser conservado em temperatura ambiente (15–30°C), protegido da luz e pode ser utilizado por 24 meses a partir da data de fabricação.
Por ser uma medicação de uso hospitalar, de clinicas ou instituições estas condições devem ser asseguradas pelos mesmos.
A bolsa deve estar protegida da luz dentro do envelope e caixa até o momento do uso. Nessas condições a solução é estável de acordo com o prazo de validade descrito na embalagem externa, antes da abertura da bolsa.
Usar imediatamente após a abertura. Se não for usada imediatamente, nas condições de armazenamento recomendadas, não se garantem a eficácia e principalmente a segurança de uso. O medicamento é de uso único e qualquer solução não utilizada deve ser devidamente descartada.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Solução límpida, incolor a amarelada, essencialmente livre de partículas visíveis.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Lynoz pode ser utilizado tanto como tratamento inicial quanto para a substituição ou continuidade de outros tratamentos em infecções4 bacterianas. Os pacientes que iniciam o tratamento com a formulação parenteral podem passar a receber a formulação oral, quando clinicamente indicado.
Duração e dosagens recomendadas
|
Infecções4 * |
Dosagens e Vias de Administração |
Duração recomendada de tratamento |
|
|
Pacientes pediátricos† (do nascimento até 11 anos de idade) |
Adultos e Adolescentes (com 12 anos de idade ou acima) |
||
|
Infecções4 complicadas de pele6 e tecidos moles |
10 mg/kg IV a cada 8 horas |
600 mg IV a cada 12 horas |
10–4 dias consecutivos |
|
Pneumonia57 adquirida na comunidade, incluindo bacteremia58 concomitante |
|||
|
Pneumonia57 hospitalar |
|||
|
Infecções4 enterocócicas resistentes a vancomicina, incluindo bacteremia58 concomitante |
10 mg/kg IV a cada 8 horas |
600 mg IV a cada 12 horas |
14–28 dias consecutivos |
|
Infecções4 não complicadas de pele6 e tecidos moles |
< 5 anos: 10 mg/kg IV† a cada 8 horas 5–11 anos: 10 mg/kg IV a cada 12 horas |
600 mg IV a cada 12 horas |
10–14 dias consecutivos |
|
* de acordo com os patógenos designados. † neonatos59 < 7 dias: a maioria dos neonatos59 pré-termo < 7 dias de idade (idade gestacional < 34 semanas) apresentam valores menores de depuração sistêmica de linezolida e valores maiores de AUC60 que muitos neonatos59 a termo e lactentes61 com idades superiores. O tratamento para estes neonatos59 deve ser iniciado com uma dose de 10 mg/kg a cada 12 horas. Deve-se considerar o uso de uma dose de 10 mg/kg a cada 8 horas em neonatos59 com uma resposta clínica inadequada. Todos os pacientes neonatos59 devem receber 10 mg/kg a cada 8 horas a partir dos 7 dias de vida. |
|||
Dosagens especiais
Pacientes Idosos: não é necessário ajuste de dose.
Pacientes com Insuficiência Renal62 Leve a Moderada: não é necessário ajuste posológico.
Pacientes com Insuficiência Renal62 Grave: não é necessário ajuste de dose. Porém, linezolida deve ser administrada com cautela nestes pacientes e somente quando os benefícios esperados superarem os riscos teóricos. A linezolida deve ser utilizada com especial cuidado em pacientes com insuficiência renal62 grave, submetidos à diálise63 e somente quando os benefícios previstos superarem o risco teórico. Não há dados sobre a experiência de linezolida administrada a pacientes submetidos a diálise peritoneal64 ambulatorial continua ou tratamentos alternativos para falência renal65 (outros que a hemodiálise66).
Pacientes com Insuficiência Hepática67: não é necessário ajuste de dose. No entanto, recomenda-se que a linezolida seja administrada em tais pacientes somente quando o benefício previsto supere o risco teórico.
Instruções para uso e manuseio: Para abrir a embalagem:
- Rasgue o envoltório externo no picote e remova a bolsa com a solução.
- Verificar se existem vazamentos mínimos comprimindo a embalagem primária com firmeza. Se for observado vazamento de solução, descartar a embalagem, pois a sua esterilidade68 pode estar comprometida.
- Não use se a solução estiver turva ou se houver algum precipitado.
- Use equipo estéril.
ADVERTÊNCIA: Não use as bolsas flexíveis em conexões em série. Esse tipo de uso pode resultar em embolia69 gasosa devido ao fato de que ar residual pode ser aspirado da embalagem primária antes que o líquido da embalagem secundária tenha terminado.
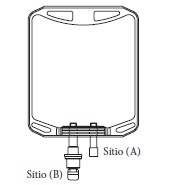
- Essa linha possui dois sítios diferentes e independentes: um sítio (A) que pode ser utilizado tanto para aditivação de medicamento como para aspiração da solução e um sítio (B) para conexão do equipo;
- Há um lacre de segurança que protege o sítio conexão do equipo (B) e outro lacre de que protege o sítio de aditivação (A) que precisam ser removidos somente no momento do uso. Eles são independentes, portanto, o lacre do sítio de aditivação não precisa ser retirado caso não seja administrada medicação;
- Colocar a bolsa sobre a bancada;
- Fazer a assepsia70 da embalagem primária utilizando álcool 70%; 5 - Romper o lacre de segurança;
- Mesmo após a remoção do lacre, há um disco de elastômero protetor que sela o contato da solução com o ambiente externo;
- Introduzir o equipo (consultar as instruções de uso do equipo com o fabricante) no elastômero até conectá-lo totalmente ou até o seu segundo degrau. A conexão resultante deve ser firme e segura;
- Durante a introdução do equipo, a pinça rolete e a entrada de ar com filtro, se houver, devem estar fechadas;
- Ajustar o nível da solução na câmara gotejadora e realizar o preenchimento do equipo de modo a retirar todo o ar do sistema antes de conectar ao paciente;
- Administrar a solução por gotejamento conforme prescrição médica.
Toda solução não utilizada deve ser desprezada. Administre a solução para infusão intravenosa em um período de 30 a 120 minutos. Não utilize as bolsas de infusão intravenosa em conexões seriadas. Não introduza aditivos na solução. Se a infusão de linezolida for realizada concomitantemente à administração de outro fármaco71, cada fármaco71 deve ser administrado separadamente, de acordo com as doses recomendadas e a via de administração para cada produto. Do mesmo modo, se for necessário usar o mesmo cateter intravenoso para a infusão sequencial de várias drogas, o cateter deve ser lavado antes e depois da administração de linezolida, com pequeno volume de uma solução de infusão compatível. A solução para infusão é compatível com as seguintes soluções: dextrose72 a 5%, cloreto de sódio a 0,9%, Ringer-lactato73 para injeção74 (Solução de Hartmann para injeção74).
A solução para infusão é fisicamente incompatível com os seguintes compostos quando em sistema Y: anfotericina B, cloridrato de clorpromazina, diazepam, isetionato de pentamidina, lactobionato de eritromicina, fenitoína sódica e sulfametoxazol/trimetoprima e quimicamente incompatível com a ceftriaxona sódica.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento de seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Como Lynoz é um medicamento de uso em serviços relacionados à assistência à saúde56, o plano de tratamento é definido pelo médico que acompanha o caso. Se você não receber uma dose deste medicamento, o médico pode redefinir a programação do tratamento. O esquecimento da dose pode comprometer a eficácia do tratamento.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): monilíase, trombocitopenia25 (diminuição das células21 de coagulação75 do sangue22: plaquetas29), anemia24 (diminuição do número de hemoglobina28), cefaleia76, vômito43, diarreia37, náusea42, dor abdominal (na barriga) incluindo cólicas77 abdominais, rash78 (vermelhidão da pele6), testes de função do fígado79 anormais.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento): pancitopenia27 (diminuição de todas as células21 do sangue22), leucopenia26 (redução de células21 de defesa no sangue22), convulsões, neuropatia periférica30 (disfunção dos neurônios80 que pode levar a perda sensorial, atrofia81 e fraqueza muscular, e decréscimos nos reflexos profundos), alteração do paladar82, neuropatia83 (doença que afeta um ou vários nervos) óptica (dos olhos84), cólicas77 abdominais, distensão abdominal, descoloração da língua85, distúrbios da pele6 bolhosa, reações adversas cutâneas86 (da pele6) graves, angioedema87 (inchaço88 das partes mais profundas da pele6 ou da mucosa89, geralmente de origem alérgica), testes hematológicos (do sangue22) anormais.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento): anemia sideroblástica90, anafilaxia91 (reação alérgica92 grave), acidose40 lática93 (acúmulo de ácido láctico no corpo), descoloração superficial dos dentes, vasculite94 (inflamação95 da parede dos vasos sanguíneos96) de hipersensibilidade.
Frequência desconhecida: necrólise epidérmica tóxica97, síndrome de Stevens-Johnson98 (reação alérgica92 grave com bolhas na pele6 e mucosas99).
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Lynoz deve ser sempre utilizado perante a supervisão de um médico e dentro de hospitais, clínicas ou instituições de saúde56. A posologia, frequência da utilização e possíveis doses diferentes das preconizadas nesta bula serão avaliadas pelos médicos responsáveis. Não foram relatados casos de superdose. Entretanto, as seguintes informações podem ser úteis: recomenda-se tratamento de suporte, juntamente com a manutenção da filtração glomerular (função do rim100). Aproximadamente 30% de uma dose de linezolida é removida pela hemodiálise66.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
SÓ PODE SER VENDIDO COM RETENÇÃO DA RECEITA
USO RESTRITO A HOSPITAIS
Reg. MS Nº 1.0298.0471
Farm. Resp.: Dr. José Carlos Módolo - CRF-SP Nº 10.446
Registrado por:
CRISTÁLIA – Produtos Químicos Farmacêuticos Ltda.
Rodovia Itapira-Lindóia, km 14 - Itapira - SP
CNPJ nº 44.734.671/0001-51
Indústria Brasileira
Fabricado por:
CRISTÁLIA – Produtos Químicos Farmacêuticos Ltda.
Avenida das Quaresmeiras, 451 - Distrito Industrial - Pouso Alegre - MG
CNPJ nº 44.734.671/0025-29
Indústria Brasileira
SAC 0800 701 19 18






