

Aristab (Suspensão oral) (Bula do profissional de saúde)
Aché Laboratórios Farmacêuticos S.A
IDENTIFICAÇÃO DO MEDICAMENTO
Aristab
aripiprazol
Suspensão oral 1 mg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Suspensão oral
Frasco contendo 100 mL e 150 mL + copo dosador
USO ORAL
USO ADULTO
COMPOSIÇÃO:
Cada 1 mL de Aristab Suspensão oral contém:
| aripiprazol | 1 mg |
| veículo q.s.p. | 1 mL |
Veículo: metilparabeno, propilparabeno, edetato dissódico di-hidratado, glicerol, sucralose, celulose microcristalina, carmelose sódica, goma xantana, polissorbato 60, hidróxido de sódio, ácido cítrico e água purificada.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE1
INDICAÇÕES
Esquizofrenia21
Aristab é indicado para o tratamento de esquizofrenia2. A eficácia de aripiprazol foi estabelecida em quatro estudos com duração entre 4 e 6 semanas. A eficácia na manutenção foi demonstrada em um estudo [vide 2. RESULTADOS DE EFICÁCIA].
1CID F20 – Esquizofrenia2
Transtorno Bipolar2
Monoterapia: Aristab é indicado para o tratamento agudo3 e de manutenção de episódios de mania e mistos associados ao transtorno bipolar do tipo I em adultos. A eficácia foi estabelecida em quatro estudos de monoterapia de 3 semanas. A eficácia na manutenção foi demonstrada em um estudo de monoterapia [vide 2. RESULTADOS DE EFICÁCIA].
Terapia Adjuntiva: Aristab é indicado como terapia adjuntiva ao lítio ou valproato para o tratamento agudo3 de episódios de mania ou mistos associados ao transtorno bipolar do tipo I, com ou sem traços psicóticos. A eficácia foi estabelecida em um estudo de terapia adjuntiva de 6 semanas [vide 2. RESULTADOS DE EFICÁCIA].
2CID F31 (exceto F31.3, F31.4, F31.5) – Transtorno afetivo bipolar
RESULTADOS DE EFICÁCIA
Esquizofrenia2
A eficácia de aripiprazol no tratamento de esquizofrenia2 foi avaliada em cinco estudos de curta duração (4 e 6 semanas), controlados por placebo4, em pacientes hospitalizados com recidiva5 aguda, os quais predominantemente atendiam os critérios do DSM-III/IV para esquizofrenia2.
Quatro dos cinco estudos foram capazes de distinguir aripiprazol do placebo4, exceto por um estudo (o menor). Três desses estudos também incluíam um grupo de controle ativo consistindo em risperidona (um estudo) ou haloperidol (dois estudos). No entanto, eles não foram desenhados para permitir uma comparação entre aripiprazol e os comparadores ativos.
Nos quatro estudos positivos para aripiprazol, quatro medidas primárias foram utilizadas para avaliar os sinais6 e sintomas7 psiquiátricos. A Escala da Síndrome8 Positiva e Negativa (PANSS) é um inventário com múltiplos itens de psicopatologia geral utilizados para avaliar os efeitos do tratamento sobre a esquizofrenia2. A subescala positiva da PANSS é um subconjunto de itens na PANSS que classifica sete sintomas7 positivos de esquizofrenia2 (delírios, desorganização conceitual, comportamento alucinatório, excitação, grandiosidade, desconfiança/perseguição e hostilidade).
A subescala negativa da PANSS é um subconjunto de itens na PANSS que classifica sete sintomas7 negativos de esquizofrenia2 (embotamento9 afetivo, apatia10, relacionamento insatisfatório, afastamento social passivo, dificuldade de pensamento abstrato, falta de espontaneidade/fluência no discurso, pensamento estereotipado). A avaliação da Impressão Clínica Global (CGI) reflete a impressão de um observador qualificado e totalmente familiar com manifestações de esquizofrenia2 acerca do estado clínico geral do paciente.
Em um estudo de quatro semanas (n= 414) para comparação de duas doses fixas de aripiprazol (15 mg/dia ou 30 mg/dia) ao placebo4, as doses de aripiprazol foram superiores ao placebo4 na classificação total da PANSS, subescala positiva da PANSS e classificação de gravidade da CGI. Além disso, a dose de 15 mg foi superior ao placebo4 na subescala negativa da PANSS.
Em um estudo de quatro semanas (n= 404) para comparação de duas doses fixas de aripiprazol (20 mg/dia ou 30 mg/dia) ao placebo4, as doses de aripiprazol foram superiores ao placebo4 na classificação total da PANSS, subescala positiva da PANSS, subescala negativa da PANSS e classificação de gravidade da CGI.
Em um estudo de seis semanas (n= 420) para comparação de três doses fixas de aripiprazol (10 mg/dia, 15 mg/dia ou 20 mg/dia) ao placebo4, as doses de aripiprazol foram superiores ao placebo4 na classificação total da PANSS, subescala positiva da PANSS e subescala negativa da PANSS.
Em um estudo de seis semanas (n= 367) para comparação de três doses fixas de aripiprazol (2 mg/dia, 5 mg/dia ou 10 mg/dia) ao placebo4, a dose de 10 mg de aripiprazol foi superior ao placebo4 na classificação total da PANSS, a medição primária do resultado do estudo. As doses de 2 mg e 5 mg não demonstraram superioridade ao placebo4 na medição primária do resultado.
Em um quinto estudo, um estudo de quatro semanas (n= 103) para comparação de aripiprazol na faixa entre 5 mg/dia e 30 mg/dia ao placebo4, o aripiprazol foi diferente do placebo4 de forma significativa apenas em uma análise de pacientes responsivos com base na classificação de gravidade da CGI, um resultado primário para aquele estudo.
Desta maneira, a eficácia das doses diárias de 10 mg, 15 mg, 20 mg e 30 mg foi estabelecida em dois estudos para cada dose. Entre essas doses, não houve evidência de que os grupos de doses mais altas ofereceram qualquer vantagem sobre o grupo de dose mais baixa desses estudos.
Um exame dos subgrupos de população não revelou nenhuma evidência clara de resposta diferenciada com relação à idade, sexo ou raça.
Um estudo de longo prazo incluiu 310 pacientes hospitalizados ou ambulatoriais que atendiam os critérios do DSM-IV para esquizofrenia2 e que eram estáveis com relação ao histórico e aos sintomas7 com o uso de outros medicamentos antipsicóticos pelo período de 3 meses ou mais. Esses pacientes tiveram seus medicamentos antipsicóticos descontinuados e foram randomizados para 15 mg/dia de aripiprazol ou placebo4 por até 26 semanas de observação para recidiva5. A recidiva5 durante a fase duplo-cega foi definida como uma pontuação de melhora da CGI ? 5 (piora mínima), pontuações ? 5 (moderadamente grave) nos itens de hostilidade ou atitude não cooperativa da PANSS, ou aumento ? 20% na pontuação total da PANSS. Os pacientes que receberam 15 mg/dia de aripiprazol apresentaram um tempo significativamente maior até a recidiva5 nas 26 semanas subsequentes, em comparação àqueles que receberam placebo4.
Transtorno Bipolar Monoterapia
A eficácia de aripiprazol no tratamento agudo3 de episódios maníacos foi estabelecida em quatro estudos de três semanas controlados por placebo4 em pacientes hospitalizados que atendiam os critérios do DSM-IV para transtorno bipolar do tipo I com episódios de mania ou mistos. Esses estudos incluíram pacientes com ou sem traços psicóticos, e dois dos estudos incluíram também pacientes cicladores rápidos ou não.
O instrumento primário utilizado na avaliação de sintomas7 maníacos foi a escala de classificação de sintomas7 maníacos Y-MRS (Young Mania Rating Scale), uma escala com 11 itens para classificação clínica utilizada tradicionalmente na avaliação do grau de sintomatologia maníaca (irritabilidade, comportamento agressivo/disruptivo, sono, euforia, fala, atividade aumentada, interesse sexual, transtorno da fala/pensamento, conteúdo de pensamento, aparência e discernimento) em uma variação entre 0 (sem traços maníacos) e 60 (pontuação máxima). Um instrumento secundário fundamental foi a classificação da Impressão Clínica Global – Bipolar (CGI-BP).
Em quatro estudos positivos de três semanas, controlados por placebo4 (n= 268; n= 248; n= 480; n= 485), os quais avaliaram aripiprazol na faixa entre 15 mg e 30 mg uma vez ao dia (com uma dose inicial de 15 mg/dia em dois estudos e 30 mg/dia nos outros dois estudos), aripiprazol foi superior ao placebo4 na redução da pontuação total da Y-MRS e da pontuação da Escala de Gravidade da Doença pela CGI-BP (mania). Em dois estudos com uma dose inicial de 15 mg/dia, 48% e 44% dos pacientes recebiam 15 mg/dia no endpoint. Em dois estudos com uma dose inicial de 30 mg/dia, 86% e 85% dos pacientes recebiam 30 mg/dia no endpoint.
Foi conduzido um estudo em pacientes que atendiam os critérios do DSM-IV para transtorno bipolar do tipo I com um episódio maníaco ou misto recente, que haviam sido estabilizados no aripiprazol aberto e que mantiveram uma resposta clínica por, no mínimo, seis semanas. A primeira fase desse estudo foi um período de estabilização aberta no qual pacientes hospitalizados e ambulatoriais foram estabilizados clinicamente e então mantidos em aripiprazol aberto (15 mg/dia ou 30 mg/dia, com uma dose inicial de 30 mg/dia) por, no mínimo, seis semanas consecutivas. 161 pacientes ambulatoriais foram randomizados a seguir de maneira duplo-cega para a mesma dose de aripiprazol recebida enquanto estavam no final do período de estabilização e manutenção, ou para placebo4. Eles foram então monitorados quanto a recidivas11 maníacas ou depressivas. Durante a fase de randomização, o aripiprazol foi superior ao placebo4 no tempo até o número de recidivas11 afetivas combinadas (maníacas e depressivas), desfechos primários para esse estudo. A maioria dessas recidivas11 foi decorrente mais de sintomas7 maníacos do que de depressivos. Não há dados suficientes para saber se aripiprazol é eficaz em retardar o tempo até a ocorrência de depressão em pacientes com transtorno bipolar do tipo I.
Um exame dos subgrupos de população não revelou nenhuma evidência clara de resposta diferencial com relação à idade e sexo; no entanto, houve quantidade insuficiente de pacientes de cada um dos grupos étnicos para avaliar de forma adequada as diferenças intergrupais.
Terapia Adjuntiva
A eficácia de aripiprazol adjuntiva com lítio ou valproato concomitantes no tratamento de episódios maníacos ou mistos foi estabelecida em um estudo de seis semanas, controlado por placebo4 (n= 384), com uma fase de duas semanas de monoterapia com introdução de estabilizador de humor em pacientes adultos que atendem os critérios do DSM-IV para transtorno bipolar do tipo I. Esse estudo incluiu pacientes com episódios maníacos ou mistos, e com ou sem traços psicóticos.
Os pacientes foram introduzidos no lítio (0,6 mEq/L a 1,0 mEq/L) ou valproato (50 μg/mL a 125 μg/mL) abertos a níveis séricos terapêuticos e permaneceram em doses estáveis por duas semanas. No final de duas semanas, os pacientes que demonstravam resposta inadequada (melhora na pontuação total da Y-MRS ≥ 16 e ≤ 25%) a lítio ou valproato foram randomizados para receber aripiprazol (15 mg/dia ou elevação para 30 mg/dia logo no dia 7) ou placebo4 como terapia adjuntiva ao lítio ou valproato abertos.
Na fase controlada por placebo4 de seis semanas, o aripiprazol adjuntivo iniciado a 15 mg/dia com lítio ou valproato concomitante (em uma faixa terapêutica12 de 0,6 mEq/L a 1,0 mEq/L ou 50 μg/mL a 125 μg/mL, respectivamente) foi superior ao lítio ou valproato com placebo4 adjuntivo na redução da pontuação total da Y-MRS e na pontuação da Gravidade da Enfermidade pela CGI-BP (mania). Setenta e um por cento (71%) dos pacientes que receberam valproato concomitantemente e 62% pacientes que receberam lítio da mesma forma estavam na dose de 15 mg/dia no endpoint de seis semanas.
CARACTERÍSTICAS FARMACOLÓGICAS
Descrição
O aripiprazol é o 7-[4-4-(2,3-diclorofenil)-1-piperazinil]-butoxi]-3,4-dihidrocarbostiril. A fórmula empírica é C23H27Cl2N3O2 e seu peso molecular é 448,38. Sua estrutura química é:
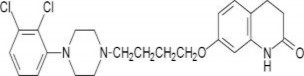
Mecanismo de Ação
O mecanismo de ação do aripiprazol, como ocorre com outras drogas eficazes no tratamento de esquizofrenia2 e transtorno bipolar, é desconhecido. No entanto, foi proposto que a eficácia do aripiprazol é mediada por uma combinação da atividade agonista13 parcial nos receptores D2 e 5-HT1A e da atividade antagonista14 nos receptores 5-HT2A. Interações com outros receptores fora D2, 5-HT1A e 5-HT2A podem explicar alguns dos outros efeitos clínicos de aripiprazol (por ex., hipotensão15 ortostática observada com o aripiprazol pode ser explicada por sua atividade antagonista14 nos receptores adrenérgicos16 alfa-1).
Farmacodinâmica
O aripiprazol apresenta grande afinidade com os receptores D2 e D3 de dopamina17, e 5-HT1A e 5-HT2A de serotonina (valores Ki de 0,34 nM, 0,8 nM, 1,7 nM e 3,4 nM, respectivamente), afinidade moderada com os receptores D4 de dopamina17, 5-HT2C e 5-HT7 de serotonina, alfa-1 adrenérgico18 e H1 de histamina19 (valores Ki de 44 nM, 15 nM, 39 nM, 57 nM e 61 nM, respectivamente) e afinidade moderada com os sítios de recaptação da serotonina (Ki = 98 nM). O aripiprazol não apresenta afinidade relevante com os receptores muscarínicos colinérgicos (CI50 > 1000 nM). Aripiprazol age como agonista13 parcial dos receptores D2 de dopamina17 e 5-HT1A de serotonina e como antagonista14 do receptor 5-HT2A de serotonina.
Farmacocinética
A atividade de aripirazol é principalmente devida à droga inalterada, aripiprazol, e em menor medida ao seu metabólito20 principal, dehidro-aripiprazol, que demonstrou afinidade com os receptores D2 similar à da droga inalterada, representando 40% da exposição da droga inalterada no plasma21. As meias-vidas médias de eliminação são de aproximadamente 75 horas e 94 horas para o aripiprazol e dehidro-aripiprazol, respectivamente. As concentrações no estado de equilíbrio são atingidas em até 14 dias da dosagem das duas porções ativas. O acúmulo de aripiprazol é previsível a partir da farmacocinética de dose única. No estado de equilíbrio, a farmacocinética do aripiprazol é proporcional à dose. A eliminação de aripiprazol é feita predominantemente por meio do metabolismo22 hepático envolvendo duas isoenzimas P450, CYP2D6 e CYP3A4.
Absorção
O aripiprazol é bem absorvido após a administração por via oral, com concentrações de pico no plasma21 ocorrendo entre 3 e 5 horas; a biodisponibilidade oral absoluta de aripiprazol é de 87%. Aripiprazol pode ser administrado com ou sem alimentos. A administração de aripiprazol com uma refeição padrão com alto teor de gordura23 não afetou de modo significativo o Cmáx ou AUC24 (Área Sob a Curva) de aripiprazol ou seu metabólito20 ativo dehidro-aripiprazol, mas retardou o Tmáx em 3 horas para o aripiprazol e 12 horas para o dehidro-aripiprazol.
Suspensão oral: Um estudo para avaliação da biodisponibilidade relativa do fármaco25 aripiprazol – aripiprazol 1 mg/mL sob a forma de suspensão oral versus o aripiprazol 10 mg sob a forma de comprimidos simples, em indivíduos sadios de ambos os sexos e em jejum – mostrou que a razão entre a média geométrica dos valores de Cmáx do aripiprazol suspensão em relação ao aripiprazol comprimidos foi de 95,17% e da AUC0–96 foi de 91,27%, ou seja, que não há diferença significativa em relação à velocidade e extensão de absorção do aripiprazol nas formas farmacêuticas avaliadas, as quais foram consideradas bioequivalentes.
Distribuição
O volume da distribuição no estado de equilíbrio de aripiprazol após a administração intravenosa é alto (404 L ou 4,9 L/kg), indicando distribuição extravascular26 extensiva. Em concentrações terapêuticas, a ligação do aripiprazol e seu metabólito20 principal a proteínas27 séricas, principalmente albumina28, é superior a 99%. Em voluntários humanos adultos que receberam entre 0,5 mg/dia e 30 mg/dia de aripiprazol por 14 dias, houve uma ocupação do receptor D2 dependente da dose, indicando penetração cerebral do aripiprazol em humanos.
Metabolismo22 e Eliminação
O aripiprazol é metabolizado principalmente por três vias de biotransformação: desidrogenação, hidroxilação e N-dealquilação. Com base em estudos in vitro, as enzimas CYP3A4 e CYP2D6 são responsáveis pela desidrogenação e hidroxilação de aripiprazol, e a N-dealquilação é catalisada pela CYP3A4. O aripiprazol é a porção ativa predominante da droga na circulação29 sistêmica. No estado de equilíbrio, o dehidro-aripiprazol, o qual é o metabólito20 ativo, representa cerca de 40% da AUC24 de aripiprazol no plasma21.
Aproximadamente 8% dos caucasianos não apresentam capacidade para metabolizar os substratos de CYP2D6 e são classificados como metabolizadores “pobres” (MP), enquanto que os demais são metabolizadores extensivos (ME). Para metabolizadores pobres dos
substratos de CYP2D6 é necessário ajuste da dose de aripiprazol [vide 8. POSOLOGIA E MODO DE USAR]. Os MPs apresentam um aumento de aproximadamente 80% na exposição do aripiprazol e redução de cerca de 30% na exposição ao metabólito20 ativo em comparação aos MEs, resultando em uma exposição aproximadamente 60% superior às porções ativas totais de uma dose determinada de aripiprazol em comparação aos MEs. A coadministração de aripiprazol com inibidores conhecidos de CYP2D6 nos MEs, como quinidina ou fluoxetina, praticamente dobra a exposição plasmática do aripiprazol, e é necessário um ajuste da dose [vide 6. INTERAÇÕES MEDICAMENTOSAS]. As meias-vidas médias de eliminação são de aproximadamente 75 horas e 146 horas para aripiprazol nos MEs e MPs, respectivamente. O aripiprazol não inibe ou induz a via da CYP2D6.
Após uma dose oral única de aripiprazol marcado com [14C], aproximadamente 25% e 55% da radioatividade administrada foi recuperada na urina30 e nas fezes, respectivamente. Menos de 1% de aripiprazol inalterado foi excretado na urina30 e aproximadamente 18% da dose oral foi recuperada inalterada nas fezes.
Farmacocinética em populações especiais
Insuficiência Renal31: Em pacientes com insuficiência renal31 grave (clearance da creatinina32 <30 mL/min), a Cmáx de aripiprazol (administrado em uma dose única de 15 mg) e de dehidro-aripiprazol aumentou em 36% e 53%, respectivamente, mas a AUC24 foi 15% menor para o aripiprazol e 7% maior para o dehidro-aripiprazol. A excreção renal33 de aripiprazol e dehidro-aripiprazol inalterados é inferior a 1% da dose. Não é necessário ajuste da dose em indivíduos com insuficiência renal31.
Insuficiência Hepática34: Em um estudo de dose única (15 mg de aripiprazol) em indivíduos com graus variáveis de cirrose35 hepática36 (Classes Child-Pugh A, B e C), a AUC24 de aripiprazol, em comparação a indivíduos saudáveis, aumentou em 31% na insuficiência hepática34 leve, 8% na insuficiência hepática34 moderada e diminuiu 20% na insuficiência hepática34 grave. Não foi necessário ajuste da dose em nenhuma dessas diferenças.
Sexo: A Cmáx e a AUC24 de aripiprazol e seu metabólito20 ativo, dehidro-aripiprazol, são de 30% a 40% maiores em mulheres do que em homens e, equivalentemente, o clearance oral aparente de aripiprazol é menor nas mulheres. No entanto, essas diferenças são explicadas basicamente pelas diferenças no peso corporal (25%) entre homens e mulheres. Não há recomendação de ajuste de dose com base no sexo.
Raça: Apesar de não ter sido conduzido um estudo farmacocinético específico para investigar os efeitos da raça sobre a disposição de aripiprazol, a avaliação farmacocinética da população não revelou evidência de diferenças relacionadas à raça clinicamente significativas na farmacocinética de aripiprazol. Não há recomendação de ajuste de dose com base na raça.
Tabagismo: Com base em estudos com enzimas hepáticas37 humanas in vitro, o aripiprazol não é um substrato para CYP1A2 e também não sofre glicuronidação direta. Por isso, o tabagismo não deve apresentar efeito sobre a farmacocinética de aripiprazol. De forma consistente com esses resultados in vitro, a avaliação farmacocinética da população não revelou diferenças significativas na farmacocinética entre fumantes e não fumantes. Não há recomendação de ajuste de dose com base no tabagismo.
CONTRAINDICAÇÕES
O Aristab é contraindicado para pacientes38 que são hipersensíveis ao aripiprazol ou qualquer um dos seus excipientes. As reações variaram de prurido39/urticária40 a anafilaxia41 [vide 9. REAÇÕES ADVERSAS].
ADVERTÊNCIAS E PRECAUÇÕES
Uso em pacientes idosos com psicose42 associada à demência43
Aumento da mortalidade44 em pacientes idosos com psicose42 associada à demência43: Os pacientes idosos com psicose42 associada à demência43 tratados com drogas antipsicóticas correm maior risco de morte. Análises de dezessete estudos controlados por placebo4 (duração modal de dez semanas) basicamente em pacientes que recebiam drogas antipsicóticas atípicas revelou risco de morte em pacientes tratados com drogas de 1,6 a 1,7 vezes maior que em pacientes tratados com placebo4. Apesar das causas das mortes serem variadas, a maioria dos óbitos pareceu ter natureza cardiovascular (como insuficiência cardíaca45, morte súbita) ou infecciosa (como pneumonia46). Aristab não é aprovado para tratamento de pacientes com psicose42 associada à demência43.
Eventos adversos cardiovasculares, incluindo AVC (Acidente Vascular Cerebral47): Em estudos clínicos controlados por placebo4 (estudo de duas doses variáveis e uma fixa) de psicose42 associada à demência43, houve uma incidência48 elevada de eventos adversos cardiovasculares (como AVC, ataque isquêmico49 transitório), incluindo fatalidades, em pacientes tratados com aripiprazol (idade média: 84 anos; faixa: 78–88 anos). No estudo de dose fixa, houve uma relação de resposta à dose estatisticamente significativa para os eventos adversos cerebrovasculares em pacientes tratados com aripiprazol. O aripiprazol não é aprovado para o tratamento de pacientes com psicose42 associada à demência43.
Experiência de segurança em pacientes idosos com psicose42 associada à Doença de Alzheimer50: Em três estudos de dez semanas e controlados por placebo4 de aripiprazol em pacientes idosos com psicose42 associada à Doença de Alzheimer50 (n= 938; idade média: 82,4 anos; faixa: 56–99 anos), os eventos adversos emergentes do tratamento que foram relatados com uma incidência48 ≥ 3% e incidência48 com o aripiprazol no mínimo duas vezes maior que com placebo4 foram letargia51 [placebo4 2%, aripiprazol 5%], sonolência (incluindo sedação52) [placebo4 3%, aripiprazol 8%] e incontinência53 (principalmente incontinência urinária54) [placebo4 1%, aripiprazol 5%], salivação excessiva [placebo4 0%, aripiprazol 4%] e tontura55 [placebo4 1%, aripiprazol 4%].
Síndrome8 Neuroléptica Maligna (SNM)
Um complexo de sintomas7 potencialmente fatal ocasionalmente chamado de Síndrome8 Neuroléptica Maligna (SNM) pode ocorrer com a administração de drogas antipsicóticas, incluindo aripiprazol. Casos raros de SNM ocorreram durante o tratamento com aripiprazol na base de dados clínica mundial. As manifestações clínicas da SNM são hipertermia, rigidez muscular, estado mental alterado e evidência de instabilidade autonômica (pulso ou pressão arterial56 irregular, taquicardia57, diaforese58 e arritmia59 cardíaca).
Sinais6 adicionais podem incluir creatinofosfoquinase elevada, mioglobinúria (rabdomiólise60) e insuficiência renal31 aguda.
A avaliação diagnóstica dos pacientes com essa síndrome8 é complicada. Ao se chegar a um diagnóstico61, é importante excluir casos em que a apresentação clínica inclua enfermidades médicas sérias (como pneumonia46 e infecção62 sistêmica) e sinais6 e sintomas7 extrapiramidais (SEP) não tratados ou tratados de forma inadequada. Outras considerações importantes no diagnóstico61 diferencial incluem toxicidade63 anticolinérgica central, intermação, febre64 medicamentosa e patologia65 do sistema nervoso central66.
O tratamento da SNM deve incluir: 1) descontinuação imediata de drogas antipsicóticas e outras drogas não essenciais à terapia concomitante; 2) tratamento sintomático67 intensivo e monitoramento médico; e 3) tratamento de quaisquer problemas médicos sérios concomitantes para os quais haja tratamentos específicos. Não há consenso quanto a regimes de tratamento farmacológico específicos para SNM não complicada. Se um paciente precisar tratamento com droga antipsicótica após se recuperar da SNM, deve-se considerar com cautela a reintrodução de terapia. O paciente deve ser monitorado cuidadosamente, já que recidivas11 de SNM têm sido relatadas.
DiscinesiaTardia
A síndrome8 de movimentos discinéticos potencialmente involuntários e irreversíveis pode ser desenvolvida por pacientes tratados com drogas antipsicóticas. Apesar de aparentemente haver maior prevalência68 dessa síndrome8 entre idosos, especialmente mulheres idosas, é impossível confiar em estimativas de prevalência68 para prever, na introdução do tratamento antipsicótico, quais pacientes tem maior chance de desenvolver a síndrome8. É desconhecido se produtos medicamentosos antipsicóticos diferem quanto ao potencial de causar discinesia tardia69.
Acredita-se que o risco de desenvolver discinesia tardia69 e a possibilidade de que ela se torne irreversível aumenta conforme a duração do tratamento e a dose total acumulada de drogas antipsicóticas administradas ao paciente aumentem. No entanto, embora menos comumente, a síndrome8 pode se desenvolver após períodos de tratamento relativamente curtos a doses baixas.
Não há tratamentos conhecidos para casos estabelecidos de discinesia tardia69, apesar de que a síndrome8 pode diminuir parcial ou completamente se o tratamento antipsicótico for interrompido. Por si só, o tratamento antipsicótico pode, no entanto, suprimir total ou parcialmente os sinais6 e sintomas7 da síndrome8 e, assim, mascarar o processo subjacente. O efeito que a supressão sintomática70 possui no processo de longo prazo da síndrome8 é desconhecido.
Dadas essas considerações, o aripiprazol deve ser prescrito de forma que seja mais provável minimizar a ocorrência de discinesia tardia69. O tratamento antipsicótico crônico71 deve ser geralmente reservado a pacientes que sofrem de uma enfermidade crônica (1) que se sabe que seja responsiva a drogas antipsicóticas e (2) para os quais tratamentos alternativos, igualmente eficazes, mas possivelmente menos danosos, não estejam disponíveis ou não sejam adequados. Em pacientes que necessitem de tratamento crônico71, a menor dose e a menor duração do tratamento que produza uma resposta clínica satisfatória devem ser buscadas. A necessidade de tratamento contínuo deve ser reavaliada periodicamente.
Se aparecerem sinais6 e sintomas7 de discinesia tardia69 em um paciente que esteja recebendo aripiprazol, a descontinuação da droga deve ser considerada. No entanto, alguns pacientes talvez precisem do tratamento com este medicamento, independentemente da presença da síndrome8.
Hiperglicemia72 e Diabetes73 mellitus
Foi relatada hiperglicemia72, em alguns casos extrema e associada à cetoacidose ou coma74 hiperosmolar75 ou morte, em pacientes tratados com antipsicóticos atípicos. Houve poucos relatos de hiperglicemia72 em pacientes tratados com aripiprazol [vide 9. REAÇÕES ADVERSAS]. Apesar de menos pacientes terem sido tratados com aripiprazol, não é conhecido se essa experiência mais limitada é a única razão para a falta de relatos desse tipo. A avaliação da relação entre o uso de antipsicóticos atípicos e anormalidades da glicose76 é complicada pela possibilidade de um risco elevado subjacente de diabetes73 mellitus em pacientes com esquizofrenia2 e uma incidência48 elevada de diabetes73 mellitus na população em geral. Dados esses aspectos conflitantes, a relação entre o uso de antipsicóticos atípicos e eventos adversos relacionados à hiperglicemia72 não é totalmente compreendida. No entanto, estudos epidemiológicos que não incluíam aripiprazol sugerem um risco elevado de eventos adversos emergentes do tratamento e relacionados à hiperglicemia72 em pacientes tratados com antipsicóticos atípicos incluídos nesses estudos.
Em virtude de aripiprazol não ser comercializado no momento em que esses estudos foram realizados, não se sabe se aripiprazol está associado a esse risco elevado. Estimativas precisas de risco para eventos adversos relacionados à hiperglicemia72 em pacientes tratados com antipsicóticos atípicos não estão disponíveis.
Pacientes com diagnóstico61 estabelecido de diabetes73 mellitus que começaram a receber antipsicóticos atípicos devem ser monitorados regularmente quanto à piora do controle glicêmico. Pacientes com fatores de risco para diabetes73 mellitus (como obesidade77, histórico familiar de diabetes73) que estejam dando início ao tratamento com antipsicóticos atípicos devem se submeter a testes de glicose76 sérica em jejum no início do tratamento e periodicamente durante o tratamento. Todos os pacientes tratados com antipsicóticos atípicos devem ser monitorados quanto a sintomas7 de hiperglicemia72, incluindo polidipsia78, poliúria79, polifagia80 e fraqueza. Pacientes que desenvolverem sintomas7 de hiperglicemia72 durante o tratamento com antipsicóticos atípicos devem se submeter a testes de glicose76 sérica em jejum. Em alguns casos, a hiperglicemia72 foi resolvida quando o antipsicótico atípico foi descontinuado. No entanto, alguns pacientes precisaram continuar o tratamento antidiabético, apesar da descontinuação da droga suspeita.
Comportamentos compulsivos
Relatos de casos pós-comercialização sugerem que pacientes podem apresentar impulsos intensos e incapacidade de controlar esses impulsos durante o tratamento com aripiprazol. Outros impulsos compulsivos, relatados com menos frequência, incluem: impulsos sexuais, compras, compulsão alimentar e outros comportamentos impulsivos ou compulsivos. Como os pacientes podem não reconhecer esses comportamentos como anormais, é importante que o médico responsável pela prescrição questione aos pacientes ou aos cuidadores destes pacientes especificamente sobre o desenvolvimento de desejos anormais, como impulsos intensos por jogos, compulsões sexuais, por compras, alimentares ou outros impulsos enquanto os pacientes estiverem em tratamento com o aripiprazol. Deve-se notar que os sintomas7 impulsivos também podem estar associados à doença do paciente. Recomenda-se precaução inclusive do uso deste medicamento por pacientes com alto risco de comportamentos incontroláveis, o que inclui pacientes com histórico pessoal ou familiar de transtorno obsessivo-compulsivo, transtorno de controle de impulsos, transtorno bipolar, personalidade impulsiva, alcoolismo, abuso de drogas ou comportamento de vícios. Em alguns casos, embora não em todos, observou-se que os impulsos cessaram quando a dose de aripiprazol foi reduzida ou quando o medicamento foi descontinuado. Comportamentos compulsivos podem resultar em danos para o paciente e outros, se não forem reconhecidos. O médico deve considerar a redução da dose ou a descontinuação do medicamento se o paciente desenvolver tais impulsos.
Hipotensão15 Ortostática
O aripiprazol pode causar hipotensão15 ortostática possivelmente em virtude de seu antagonismo ao receptor α1-adrenérgico18. A incidência48 de eventos relacionados à hipotensão15 ortostática em estudos de curta duração e controlados por placebo4 em pacientes adultos recebendo aripiprazol oral (n= 2467) incluiu (incidência48 com aripiprazol, incidência48 com placebo4): hipotensão15 ortostática (1%, 0,3%), tontura55 postural (0,5%, 0,3%) e síncope81 (0,5%, 0,4%).
A incidência48 de uma alteração ortostática significativa na pressão arterial56 (definida como uma redução na pressão arterial sistólica82 ? 20 mmHg acompanhada de uma elevação na frequência cardíaca ≥ 25 em comparação entre a posição em pé e a posição supina) para o aripiprazol não foi significativamente diferente do placebo4 (incidência48 com aripiprazol, incidência48 com placebo4) em pacientes adultos tratados com aripiprazol oral (4%, 2%).
O aripiprazol deve ser usado com cautela em pacientes com doença cardiovascular conhecida (histórico de infarto do miocárdio83 ou doença cardíaca isquêmica, insuficiência cardíaca45 ou anormalidades da condução), doença cerebrovascular84 ou condições que poderiam predispor os pacientes à hipotensão15 (desidratação85, hipovolemia86 e tratamento com medicamentos anti-hipertensivos).
Distúrbios vasculares87
Casos de tromboembolismo88 venoso (TEV) foram notificados com medicamentos antipsicóticos. Uma vez que pacientes tratados com antipsicóticos apresentam frequentemente fatores de risco adquiridos para o TEV, todos os possíveis os fatores de riscos para TEV devem ser identificados antes e durante o tratamento com aripiprazol.
Quedas
Os antipsicóticos, incluindo o aripiprazol, podem causar sonolência, hipotensão15 postural, instabilidade motora e sensorial, que podem levar a quedas e, consequentemente, fraturas ou outras lesões89. Para pacientes38 com doenças, condições ou que estejam utilizando medicamentos que possam exacerbar esses efeitos, deve-se avaliar o risco de quedas ao iniciar o tratamento antipsicótico, assim como avaliar recorrentemente este risco em pacientes em tratamento com terapia antipsicótica de longo prazo.
Leucopenia90, Neutropenia91 e Agranulocitose92
Efeito da classe: em estudos clínicos e/ou experiência pós-comercialização, têm sido relatados eventos de leucopenia90/neutropenia91 relacionados temporariamente a agentes antipsicóticos, incluindo aripiprazol.
Também foi relatada agranulocitose92.
Fatores de risco possíveis para leucopenia90/neutropenia91 incluem contagem de leucócitos93 (WBC) pré-existente baixa e histórico de leucopenia90/neutropenia91 induzidas pela droga. Pacientes com histórico de WBC baixa clinicamente significativa ou leucopenia90/neutropenia91 induzidas pela droga devem ter seu hemograma completo (CBC) monitorado frequentemente durante os primeiros meses de terapia e a descontinuação de aripiprazol deve ser considerada ao primeiro sinal94 de queda clinicamente significativa na WBC na ausência de outros fatores causais. Pacientes com neutropenia91 clinicamente significativa devem ser monitorados cuidadosamente quanto à febre64 ou outros sinais6 ou sintomas7 de infecção62 e tratados imediatamente, se tais sintomas7 ou sinais6 ocorrerem. Pacientes com neutropenia91 grave (contagem absoluta de neutrófilos95 <1000/mm3) devem descontinuar estemedicamento e ter sua WBC monitorada até a recuperação.
Convulsões
Em estudos de curto prazo e controlados por placebo4, convulsões ocorreram em 0,1% (3/2467) dos pacientes adultos tratados com aripiprazol oral. Como ocorre com outras drogas antipsicóticas, o aripiprazol deve ser utilizado com cautela em pacientes com histórico de convulsões ou com condições que reduzam o limiar convulsivo, como no caso de demência43 de Alzheimer96. Condições que reduzam o limiar convulsivo podem ser mais predominantes em uma população com idade a partir de 65 anos.
Potencial para comprometimento cognitivo97 ou motor
Aristab, como outros antipsicóticos, pode comprometer potencialmente as habilidades de julgamento, pensamento ou motoras. Por exemplo, em estudos de curto prazo e controlados por placebo4, a sonolência (incluindo sedação52) foi relatada em pacientes adultos (n= 2467) tratados com aripiprazol oral (incidência48 com aripiprazol: 11%, incidência48 com placebo4: 6%). A sonolência (incluindo sedação52) levou à descontinuação em 0,3% (8/2467) dos pacientes adultos que recebiam aripiprazol em estudos de curto prazo e controlados por placebo4.
Efeitos na habilidade de dirigir e usar máquinas
Apesar da incidência48 de aumento relativamente modesta desses eventos em comparação ao placebo4, os pacientes devem ser alertados sobre o risco de operar máquinas perigosas, incluindo automóveis, até que eles tenham certeza razoável de que a terapia com aripiprazol não os afeta de modo adverso.
Durante o tratamento, o paciente não deve dirigir veículos ou operar máquinas, pois sua habilidade e atenção podem estar prejudicadas.
Regulação da temperatura corporal
A perda da habilidade do corpo em reduzir a temperatura corporal central tem sido atribuída a agentes antipsicóticos. Recomenda-se atenção adequada na prescrição de aripiprazol para pacientes38 que passarão por situações que possam contribuir para uma elevação na temperatura corporal central (como exercício extenuante, exposição a calor extremo, administração concomitante de medicamento com atividade anticolinérgica, ou sujeição à desidratação85) [vide 9. REAÇÕES ADVERSAS].
Suicídio
A possibilidade de tentativa de suicídio é inerente a enfermidades psicóticas e transtorno bipolar. Uma supervisão cuidadosa de pacientes de alto risco deve ser realizada durante a terapia. Deve-se prescrever aripiprazol na menor quantidade consistente com o controle eficaz do paciente de modo a reduzir o risco de superdosagem [vide 9. REAÇÕES ADVERSAS].
Disfagia98
A falta de motilidade do esôfago99 e aspiração tem sido associadas ao uso de drogas antipsicóticas, incluindo este medicamento. A pneumonia46 por aspiração é uma causa comum de morbidade100 e mortalidade44 em pacientes idosos, especialmente entre aqueles com demência43 de Alzheimer96 avançada. O aripiprazol e outras drogas psicóticas devem ser utilizados com cuidado em pacientes com risco de pneumonia46 por aspiração [vide 5. ADVERTÊNCIAS E PRECAUÇÕES: Uso em pacientes idosos com psicose42 associada à demência43 e 9. REAÇÕES ADVERSAS].
Uso em pacientes com enfermidade concomitantes
A experiência clínica com aripiprazol em pacientes com certas enfermidades sistêmicas concomitantes é limitada. Aripiprazol não foi avaliado ou utilizado em uma extensão considerável em pacientes com histórico recente de infarto do miocárdio83 ou doença cardíaca instável. Pacientes com esses diagnósticos foram excluídos dos estudos clínicos pré-comercialização [vide 5. ADVERTÊNCIAS E PRECAUÇÕES].
Abuso e Dependência
Aripiprazol não foi estudado sistematicamente em humanos com relação ao seu potencial de abuso, tolerância ou dependência física. Em estudos de dependência física em macacos, sintomas7 de abstinência foram observados mediante a interrupção abrupta da administração. Enquanto estudos clínicos não revelaram qualquer tendência para comportamento de busca pela droga, essas observações não foram sistemáticas e não é possível prever com base nessa experiência limitada até que ponto uma droga que age no sistema nervoso central66 será mal utilizada, usada com fins recreativos e/ou excessivamente utilizada, uma vez que seja comercializada. Consequentemente, os pacientes devem ser avaliados cuidadosamente quanto a um histórico de abuso de drogas. Tais pacientes devem ser rigorosamente observados com relação a sinais6 de mau uso ou abuso (como desenvolvimento de tolerância, aumento na dose, comportamento de busca pela droga).
Carcinogênese, Mutagênese, Comprometimento da Fertilidade
Carcinogênese: Estudos de carcinogênese foram conduzidos em camundongos ICR e ratos Sprague-Dawley (SD) e F344. O aripiprazol foi administrado por dois anos na dieta a doses de 1 mg/kg/dia, 3 mg/kg/dia, 10 mg/kg/dia e 30 mg/kg/dia a camundongos ICR, e 1 mg/kg/dia, 3 mg/kg/dia e 10 mg/kg/dia a ratos F344 (0,2 vezes a 5 vezes e 0,3 vezes a 3 vezes a dose humana máxima recomendada [DHMR] em mg/m2, respectivamente).
Ademais, os ratos SD receberam doses orais por dois anos a 10 mg/kg/dia, 20 mg/kg/dia, 40 mg/kg/dia e 60 mg/kg/dia (3 vezes a 19 vezes a DHMR em mg/m2). O aripiprazol não induziu tumores em camundongos ou ratos machos. Em camundongos fêmeas, as incidências de adenomas na glândula101 pituitária e adenocarcinomas e adenoacantomas das glândulas102 mamárias foram altas a doses de 3 mg/kg/dia a 30 mg/kg/dia na dieta (0,1 vez a 0,9 vez a exposição humana à DHMR em mg/m2). Em ratos fêmeas, a incidência48 de fibroadenomas nas glândulas102 mamárias foi elevada a uma dose de 10/mg/kg/dia na dieta (0,1 vez a exposição humana à DHMR com base na AUC24 e 3 vezes a DHMR em mg/m2); e as incidências de carcinomas adrenocorticais e adenomas/carcinomas adrenocorticais combinados foram elevadas a uma dose oral de 60 mg/kg/dia (14 vezes a exposição humana à DHMR com base na AUC24 e 19 vezes a DHMR em mg/m2).
Alterações proliferativas na glândula101 mamária e pituitária de roedores têm sido observadas após a administração crônica de outros agentes antipsicóticos e são consideradas mediadas pela prolactina103. A prolactina103 sérica não foi medida nos estudos de carcinogenicidade de aripiprazol. No entanto, elevações nos níveis séricos de prolactina103 foram observados em camundongos fêmeas em um estudo de treze semanas nas doses associadas aos tumores pituitário e da glândula101 mamária. A prolactina103 sérica não foi elevada em ratos fêmeas em estudos de dieta de quatro e treze semanas na dose associada a tumores na glândula101 mamária. A relevância para o risco em humanos dos achados de tumores endócrinos mediados pela prolactina103 em roedores é desconhecida.
Mutagênese: O potencial mutagênico de aripiprazol foi testado no ensaio in vitro de mutação104 reversa bacteriana, ensaio in vitro de reparo de DNA bacteriano, ensaio in vitro de mutação genética105 sequencial de células106 de linfoma107 de camundongos, ensaio in vitro de aberração cromossômica em células106 de pulmão108 de hamster chinês (CHL, em inglês), ensaios in vivo de micronúcleos de camundongos e em estudo de síntese não programado de DNA em ratos. O aripiprazol e o metabólito20 (2,3-DCPP) foram clastogênicos em ensaios in vitro de aberração cromossômica em células106 CHL com e sem ativação metabólica. O metabólito20 2,3-
DCPP produziu elevações no número de aberrações no ensaio in vitro nas células106 CHL na ausência de ativação metabólica. Uma resposta positiva foi obtida no ensaio in vivo de micronúcleos de camundongos; no entanto, a resposta foi devida a um mecanismo não considerado relevante em humanos.
Comprometimento da Fertilidade: Ratos fêmeas foram tratados com doses orais de 2 mg/kg/dia, 6 mg/kg/dia e 20 mg/kg/dia (0,6 vez, 2 vezes e 6 vezes a dose humana recomendada máxima [DHMR] em mg/m2) de aripiprazol duas semanas antes do acasalamento até o dia 7 de gestação. Irregularidades no ciclo estrogênico e aumento do corpo lúteo foram observados em todas as doses, mas não foi observado comprometimento da fertilidade. Aumento nas perdas de pré-implantação foi observado nas doses de 6 mg/kg e 20 mg/kg, e diminuição do peso fetal foi observada na dose de 20 mg/kg.
Ratos machos foram tratados com doses orais de 20 mg/kg/dia, 40 mg/kg/dia e 60 mg/kg/dia (6 vezes, 13 vezes e 19 vezes a DHMR em mg/m2) de aripiprazol nove semanas antes do acasalamento e durante o acasalamento. Distúrbios na espermatogênese foram observados na dose de 60 mg/kg, e atrofia109 na próstata110 foi observada nas doses 40 mg/kg e 60 mg/kg, mas não foi observado comprometimento da fertilidade.
Gravidez111 e Lactação112
Categoria C. Em estudos com animais, o aripiprazol demonstrou toxicidade63 do desenvolvimento, incluindo possíveis efeitos teratogênicos113 em ratos e coelhos.
Ratas prenhes foram tratadas com doses orais de 3 mg/kg/dia, 10 mg/kg/dia e 30 mg/kg/dia (1 vez, 3 vezes e 10 vezes a dose humana recomendada máxima [DHMR] em mg/m2) de aripiprazol durante o período de organogênese. A gestação foi levemente prolongada a 30 mg/kg. O tratamento causou um leve atraso no desenvolvimento fetal, conforme evidenciado pelo peso fetal reduzido (30 mg/kg), testículos114 retidos (30 mg/kg) e atraso na ossificação esquelética (10 mg/kg e 30 mg/kg). Não houve efeitos adversos na sobrevivência115 embriofetal ou do filhote. A prole nascida apresentou peso corporal reduzido (10 mg/kg e 30 mg/kg) e incidências elevadas de nódulos hepatodiafragmáticos e hérnia116 diafragmática a 30 mg/kg (os outros grupos de dose não foram examinados com relação a esses achados). Também foi observada baixa incidência48 de hérnia116 diafragmática em fetos expostos a 30 mg/kg.
No período pós-natal, foi observada abertura vaginal tardia a 10 mg/kg e 30 mg/kg e desempenho reprodutivo comprometido (redução da taxa de fertilidade, de corpo lúteo, de implantes e de fetos vivos, e aumento na perda pós-implantação, provavelmente mediada por efeitos na prole feminina) foi observado a 30 mg/kg. Foi observada certa toxicidade63 materna a 30 mg/kg. No entanto, não houve evidências que sugiram que esses efeitos no desenvolvimento foram secundários à toxicidade63 materna.
Coelhas prenhes foram tratadas com doses orais de 10 mg/kg/dia, 30 mg/kg/dia e 100 mg/kg/dia (2 vezes, 3 vezes e 11 vezes a exposição humana da DHMR com base na AUC24 e 6 vezes, 19 vezes e 65 vezes a DHMR em mg/m2) de aripiprazol durante o período de organogênese. Foram observados redução no consumo alimentar materno e elevação nos abortos a 100 mg/kg. O tratamento causou elevação na mortalidade44 fetal (100 mg/kg), peso fetal reduzido (30 mg/kg e 100 mg/kg), incidência48 elevada de uma anormalidade esquelética (sternebrae fundida a 30 mg/kg e 100 mg/kg) e variações esqueléticas de menor relevância (100 mg/kg).
Em um estudo no qual ratos foram tratados com doses orais de 3 mg/kg/dia, 10 mg/kg/dia e 30 mg/kg/dia (1 vez, 3 vezes e 10 vezes a DHMR em mg/m2) de aripiprazol no pré-natal e no pós-natal (do dia 17 de gestação até o dia 21 pós-parto), toxicidade63 materna leve e gestação levemente prolongada foram observadas a 30 mg/kg. Uma elevação no número de natimortos e reduções no peso dos filhotes (persistindo durante a idade adulta) e na sobrevivência115 foram observadas nessa dose.
Não há estudos adequados e bem controlados em mulheres grávidas. É desconhecido se aripiprazol pode causar danos ao feto117 quando administrado a uma mulher grávida ou se pode afetar a capacidade reprodutiva. Recém-nascidos que foram expostos à fármacos antipsicóticos durante o terceiro trimestre de gravidez111 apresentam o risco para sintomas7 extrapiramidais e/ou de abstinência após o parto. Há relatos de agitação, hipertonia118, hipotonia119, tremor, sonolência, dificuldade respiratória e distúrbio alimentar nestes recém-nascidos. Essas complicações variaram em gravidade; enquanto que em alguns casos os sintomas7 foram autolimitados, em outros foi requerido suporte da unidade de terapia intensiva120 (UTI) e de hospitalização prolongada. Existem relatos muito raros desses eventos com a exposição ao aripiprazol. As pacientes devem avisar ao médico se engravidarem ou se pretendem engravidar durante o tratamento com aripiprazol. Aristab (suspensãooral) deve ser utilizado durante a gravidez111 apenas se os benefícios potenciais compensarem o possível risco ao feto117.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Trabalho de parto: O efeito de aripiprazol no trabalho de parto em humanos é desconhecido.
Uso por lactantes121: Aripiprazol é excretado no leite materno humano. As pacientes devem ser avisadas para não amamentarem caso esteja em tratamento com aripiprazol.
Uso em populações específicas
Uso pediátrico: Não há indicação aprovada para o uso deste medicamento em pacientes pediátricos.
Uso geriátrico: Em estudos formais de farmacocinética de dose única (com aripiprazol administrado em dose única de 15 mg), o clearance do aripiprazol foi 20% menor em indivíduos idosos (≥ 65 anos) em comparação a indivíduos adultos mais jovens (18 a 64 anos). No entanto, não houve efeito detectável atribuível à idade na análise de farmacocinética da população de pacientes esquizofrênicos. Além disso, a farmacocinética de aripiprazol após múltiplas doses em pacientes idosos aparentou ser semelhante à observada em indivíduos saudáveis e jovens. Não há recomendação de ajuste de dose para pacientes38 idosos [vide 5. ADVERTÊNCIAS E PRECAUÇÕES].
Dos 13.543 pacientes tratados com aripiprazol oral em estudos clínicos, 1.073 (8%) tinham no mínimo 65 anos de idade e 799 (6%) tinham no mínimo 75 anos de idade. A maior parte (81%) dos 1.073 pacientes foi diagnosticada com Demência43 do tipo de Alzheimer96.
Estudos de aripiprazol controlados por placebo4 em esquizofrenia2 e mania bipolar não incluíram uma quantidade suficiente de indivíduos com no mínimo 65 anos de idade para determinar se eles respondem de forma diferente dos indivíduos mais jovens.
Estudos em pacientes idosos com psicose42 associada à Doença de Alzheimer50 sugeriram que possa haver um perfil de tolerância diferente nessa população em comparação a pacientes mais jovens com esquizofrenia2 [vide 5. ADVERTÊNCIAS E PRECAUÇÕES: Uso em pacientes idosos com psicose42 associada à demência43]. A segurança e a eficácia de aripiprazol no tratamento de pacientes com psicose42 associada à Doença de Alzheimer50 não foram estabelecidas. Se for decidido tratar tais pacientes com aripiprazol, deve-se ter cautela.
INTERAÇÕES MEDICAMENTOSAS
Em virtude dos efeitos principais de aripiprazol sobre o sistema nervoso central66, deve-se ter cautela quando aripiprazol for administrado em combinação com álcool ou outras drogas com ação central.
Devido ao seu antagonismo do receptor alfa adrenérgico18, aripiprazol possui o potencial de intensificar os efeitos de certos agentes anti-hipertensivos.
Potencial de outras drogas afetarem Aristab
Aripiprazol não é um substrato das enzimas CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19 ou CYP2E1. Aripiprazol também não sofre glicuronidação direta. Isto sugere que uma interação de aripiprazol com inibidores ou indutores dessas enzimas, ou outros fatores, como tabagismo, seja improvável.
CYP3A4 e CYP2D6 são responsáveis pelo metabolismo22 de aripiprazol. Os agentes indutores de CYP3A4 (como carbamazepina) podem causar uma elevação no clearance de aripiprazol e redução nos níveis séricos. Inibidores de CYP3A4 (como cetoconazol) ou CYP2D6 (como quinidina, fluoxetina ou paroxetina) podem inibir a eliminação de aripiprazol e causar elevação nos níveis séricos.
Cetoconazol e outros inibidores de CYP3A4: A coadministração de cetoconazol (200 mg/dia por quatorze dias) com uma dose única de 15 mg de aripiprazol elevou a AUC24 de aripiprazol e de seu metabólito20 ativo em 63% e 77%, respectivamente. O efeito de uma dose mais alta de cetoconazol (400 mg/dia) não foi estudado. Quando cetoconazol é administrado concomitantemente com aripiprazol, a dose de aripiprazol deve ser reduzida para a metade de sua dose normal. Espera-se que outros inibidores fortes de CYP3A4 (itraconazol) tenham efeitos similares e necessitem de reduções semelhantes na dose; inibidores moderados (eritromicina, suco de toranja [grapefruit, em inglês]) não foram estudados. Quando um inibidor de CYP3A4 for retirado da terapia combinada122, a dose de aripiprazol deve ser elevada.
Quinidina e outros inibidores de CYP2D6: A coadministração de uma dose única de 10 mg de aripiprazol com quinidina (166 mg/dia por treze dias), um potente inibidor de CYP2D6, elevou a AUC24 de aripiprazol em 112%, mas reduziu a AUC24 de seu metabólito20 ativo, dehidro-aripiprazol, em 35%. A dose de aripiprazol deve ser reduzida para a metade de sua dose normal quando quinidina for administrada concomitantemente com aripiprazol. Espera-se que outros inibidores significativos de CYP2D6, como fluoxetina ou paroxetina, tenham efeitos similares e levem a reduções semelhantes da dose. Quando um inibidor de CYP2D6 for retirado da terapia combinada122, a dose de aripiprazol deve ser elevada.
Inibidores de CYP3A4 e CYP2D6: O uso concomitante de aripiprazol com inibidores de CYP3A4 (por exemplo, cetoconazol e itraconazol) e inibidores de CYP2D6 (por exemplo, quinidina, fluoxetina e paroxetina) aumenta a exposição de aripiprazol em comparação com o uso de aripiprazol isolado. Quando o uso de aripiprazol for realizado concomitantemente com inibidores de CYP2D6 e CYP3A4, a dose aripiprazol deve ser reduzida a um quarto da dose usual [vide 8. POSOLOGIA E MODO DE USAR].
Carbamazepina e outros indutores de CYP3A4: A coadministração de carbamazepina (200 mg, duas vezes ao dia), um indutor potente de CYP3A4, com aripiprazol (30 mg/dia) resultou em uma redução aproximada de 70% nos valores da Cmáx e AUC24 de aripiprazol e seu metabólito20 ativo, dehidro-aripiprazol. Quando carbamazepina é adicionada à terapia com aripiprazol, a dose deste deve ser dobrada. Aumentos adicionais na dose devem ser baseados na avaliação clínica. Quando carbamazepina for retirada da terapia combinada122, a dose de aripiprazol deve ser reduzida.
Potencial de aripiprazol afetar outras drogas
Há baixa probabilidade de aripiprazol causar interações farmacocinéticas clinicamente importantes com drogas metabolizadas pelas enzimas do citocromo P450. Em estudos in vivo, doses entre 10 mg/dia e 30 mg/dia de aripiprazol não apresentaram efeito significativo no metabolismo22 por substratos de CYP2D6 (dextrometorfano), CYP2C9 (varfarina), CYP2C19 (omeprazol, varfarina) e CYP3A4 (dextrometorfano). Além disso, aripiprazol e dehidro-aripiprazol não apresentaram potencial para alterar o metabolismo22 mediado por CYP1A2 in vitro.
Não foram observados efeitos de aripiprazol sobre a farmacocinética de lítio ou valproato.
Álcool: Não houve diferença significativa entre aripiprazol administrado concomitantemente com etanol e placebo4 coadministrado com etanol sobre o desempenho das habilidades motoras totais ou sobre as respostas a estímulos em indivíduos saudáveis. Como ocorre com a maior parte dos medicamentos psicoativos, os pacientes devem ser alertados para evitar ingerir álcool durante o tratamento com aripiprazol.
Drogas sem interações clinicamente importantes com Aristab
Famotidina: A coadministração de aripiprazol (em uma dose única de 15 mg) com uma dose única de 40 mg do antagonista14 de H2, famotidina, um bloqueador potente do ácido gástrico123, reduziu a solubilidade de aripiprazol e, consequentemente, sua taxa de absorção, reduzindo em 37% e 21% a Cmáx de aripiprazol e dehidro-aripiprazol, respectivamente, e em 13% e 15% a extensão de absorção (AUC24), respectivamente.
Não é necessário ajuste na dosagem de aripiprazol quando administrado concomitantemente a famotidina.
Valproato: Quando valproato (500 mg/dia – 1500 mg/dia) e aripiprazol (30 mg/dia) foram administrados concomitantemente, a Cmáx e a AUC24 de aripiprazol no estado de equilíbrio foram reduzidas em 25%. Não é necessário ajuste na dosagem de aripiprazol quando administrado concomitantemente ao valproato. Quando aripiprazol (30 mg/dia) e valproato (1000 mg/dia) foram administrados concomitantemente, no estado de equilíbrio não houve alterações clinicamente significativas na Cmáx ou AUC24 de valproato. Não é necessário ajuste na dosagem de valproato quando administrado concomitantemente ao aripiprazol.
Lítio: Uma interação farmacocinética entre aripiprazol e lítio é improvável em virtude deste último não se ligar a proteínas27 plasmáticas, não ser metabolizado e ser quase que totalmente excretado inalterado na urina30. A coadministração de doses terapêuticas de lítio (1200 mg/dia – 1800 mg/dia) por vinte e um dias com aripiprazol (30 mg/dia) não resultou em alterações clinicamente significativas na farmacocinética de aripiprazol ou de seu metabólito20 ativo, dehidro-aripiprazol (Cmáx e AUC24 tiveram elevação inferior a 20%).
Não é necessário ajuste na dosagem de aripiprazol quando administrado concomitantemente a lítio. A coadministração de aripiprazol (30 mg/dia) com lítio (900 mg/dia) não resultou em alterações clinicamente significativas na farmacocinética do lítio. Não é necessário ajuste na dosagem de lítio quando administrado concomitantemente ao aripiprazol.
Lamotrigina: A coadministração entre 10 mg/dia e 30 mg/dia de doses orais de aripiprazol por quatorze dias a pacientes com transtorno bipolar do tipo I não apresentou efeitos sobre a farmacocinética no estado de equilíbrio entre 100 mg/dia e 400 mg/dia de lamotrigina, um substrato da UDP-glucuronosiltransferase 1A4. Não é necessário ajuste na dosagem de lamotrigina quando aripiprazol for incluído na terapia com lamotrigina.
Dextrometorfano: Aripiprazol a doses entre 10 mg/dia e 30 mg/dia por quatorze dias não apresentou efeito sobre a O-dealquilação de dextrometorfano ao seu metabólito20 principal, dextrorfano, uma via dependente da atividade de CYP2D6. Aripiprazol também não apresentou efeito sobre a N-demetilação de dextrometorfano ao seu metabólito20 3-metoximorfinano, uma via dependente da atividade de CYP3A4. Não é necessário ajuste na dosagem de dextrometorfano quando administrado concomitantemente a aripiprazol.
Varfarina: A dose de 10 mg/dia de aripiprazol por quatorze dias não apresentou efeito sobre a farmacocinética de R-varfarina e S-varfarina ou sobre o ponto final da farmacodinâmica da Razão Normalizada Internacional, indicando ausência de efeito clinicamente relevante de aripiprazol sobre o metabolismo22 de CYP2C9 e CYP2C19 ou sobre a ligação de varfarina à proteínas27 plasmáticas de alta afinidade. Não é necessário ajuste na dosagem de varfarina quando administrada concomitantemente a aripiprazol.
Omeprazol: A dose de 10 mg/dia de aripiprazol por quinze dias não apresentou efeito sobre a farmacocinética de uma dose única de 20 mg de omeprazol, um substrato de CYP2C19, em indivíduos saudáveis. Não é necessário ajuste na dosagem de omeprazol quando administrado concomitantemente a aripiprazol.
Anormalidades em testes laboratoriais
Uma comparação entre grupos em estudos de três a seis semanas e controlados por placebo4 em adultos não revelou diferenças medicamente importantes entre os grupos de aripiprazol e placebo4 nas proporções de pacientes apresentando alterações potencial e clinicamente significativas nos parâmetros de rotina de bioquímica sérica, hematologia ou análise de urina30. De maneira semelhante, não foram observadas diferenças entre aripiprazol e placebo4 na incidência48 de descontinuações em razão de alterações na bioquímica sérica, hematologia ou análise de urina30 em pacientes adultos.
Em um estudo de longo prazo (26 semanas) controlado por placebo4, não foram observadas diferenças medicamente importantes entre os pacientes recebendo aripiprazol e aqueles recebendo placebo4 na alteração média a partir da linha basal nos valores de prolactina103, glicose76 em jejum, triglicérides124, HDL125, LDL126 ou colesterol127 total.
Alterações no ECG
Comparações entre grupos para a análise conjunta de estudos controlados por placebo4 em pacientes com esquizofrenia2 e mania bipolar não revelaram diferenças significativas entre aripiprazol oral e placebo4 na proporção de pacientes apresentando alterações potencialmente importantes nos parâmetros do ECG.
Aripiprazol foi associado a uma elevação mediana na frequência cardíaca de duas batidas por minuto, em comparação à ausência de elevação entre pacientes recebendo placebo4.
Interação com nicotina
A avaliação farmacocinética da população não revelou diferenças farmacocinéticas significativas entre fumantes e não fumantes (vide 3. CARACTERÍSTICAS FARMACOLÓGICAS: Farmacocinética em Populações Especiais – Tabagismo).
Interação com alimentos
Este medicamento pode ser administrado com ou sem alimentos (vide 3. CARACTERÍSTICAS FARMACOLÓGICAS: Farmacocinética – Absorção).
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar este medicamento em temperatura ambiente (15–30°C). Proteger da luz. Prazo de validade: até 24 meses após a data de fabricação.
Número do lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original. Após aberto, válido por 60 dias.
Características físicas e organolépticas do produto
Aristab se apresenta na forma de suspensão branca homogênea.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Aristab deve ser utilizado exclusivamente por via oral. Recomenda-se que, para a administração da suspensão oral, seja utilizado o copo dosador que acompanha o frasco na embalagem. Agite antes de usar.
Esquizofrenia2
A dose de início e a dose alvo recomendadas para Aristab é de 10 mg/dia ou 15 mg/dia uma vez ao dia, independente das refeições. Aristab tem sido avaliado sistematicamente e demonstrou ser eficaz em uma variação de dose entre 10 mg/dia e 30 mg/dia; no entanto, doses superiores a 10 mg/dia ou 15 mg/dia não foram mais eficazes. Em geral, aumentos na dosagem não devem ser feitos antes de duas semanas, o tempo necessário para se atingir o estado de equilíbrio [vide 2. RESULTADOS DE EFICÁCIA].
Tratamento de Manutenção: A manutenção da eficácia na esquizofrenia2 foi demonstrada em um estudo envolvendo pacientes com esquizofrenia2 que permaneceram com sintomas7 estáveis ao receber outros medicamentos antipsicóticos por períodos de, no mínimo, três meses. Esses pacientes tiveram seus medicamentos descontinuados, foram randomizados para 15 mg/dia de aripiprazol ou placebo4 e foram monitorados quanto à recidiva5 [vide 2. RESULTADOS DE EFICÁCIA]. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de continuar com o tratamento de manutenção.
Troca de outros antipsicóticos: Não há dados coletados de forma sistemática para avaliar especificamente pacientes com esquizofrenia2 que tenham trocado outros antipsicóticos por Aristab, ou dados relativos à administração concomitante com outros antipsicóticos. Ao passo que a descontinuação imediata do tratamento antipsicótico anterior possa ser aceitável para alguns pacientes com esquizofrenia2, a descontinuação mais gradual pode ser mais adequada para os demais pacientes. Em todos os casos, o período de sobreposição da administração dos antipsicóticos deve ser minimizado.
Transtorno Bipolar
A dose de início e a dose alvo recomendada é de 15 mg uma vez ao dia como monoterapia ou como terapia adjuntiva com lítio ou valproato. Aristab deve ser administrado independentemente das refeições. A dose pode ser elevada para 30 mg/dia com base na resposta clínica. A segurança das doses superiores a 30 mg/dia não foi avaliada em estudos clínicos [vide 2. RESULTADOS DE EFICÁCIA].
Tratamento de Manutenção: A manutenção da eficácia no transtorno bipolar do tipo I foi demonstrada em um estudo envolvendo pacientes que permaneceram com sintomas7 estáveis ao receberem aripiprazol (15 mg/dia ou 30 mg/dia, como monoterapia) por, no mínimo, seis semanas consecutivas. Esses pacientes tiveram seus medicamentos descontinuados, foram randomizados para aripiprazol ou placebo4 na mesma dose em que foram estabilizados e foram monitorados quanto à recidiva5 [vide 2. RESULTADOS DE EFICÁCIA]. Os pacientes devem ser reavaliados periodicamente para determinar a necessidade de continuar com o tratamento de manutenção.
Ajuste da Dosagem
Ajustes da dosagem em adultos não são habitualmente indicados de acordo com a idade, sexo, raça ou estado da insuficiência renal31 ou hepática36 [vide 5. ADVERTÊNCIAS E PRECAUÇÕES].
Ajuste da dosagem para pacientes38 recebendo aripiprazol concomitantemente a inibidores fortes de CYP3A4: Quando for indicada a administração concomitante de aripiprazol com inibidores fortes de CYP3A4, como cetoconazol ou claritromicina, a dose de aripiprazol deve ser reduzida para a metade da dose habitual.
Quando um inibidor de CYP3A4 for retirado da terapia combinada122, a dose de aripiprazol deve ser então elevada [vide 6. INTERAÇÕES MEDICAMENTOSAS].
Ajuste da dosagem para pacientes38 recebendo aripiprazol concomitantemente a inibidores de CYP2D6 em potencial: Quando ocorrer a administração concomitante de aripiprazol com inibidores de CYP2D6 em potencial, como quinidina, fluoxetina ou paroxetina, a dose de aripiprazol deve ser reduzida, no mínimo, até a metade de sua dose normal. Quando um inibidor de CYP2D6 for retirado da terapia combinada122, a dose de aripiprazol deve ser então elevada [vide 6. INTERAÇÕES MEDICAMENTOSAS].
Ajuste da dosagem para pacientes38 recebendo indutores de CYP3A4 em potencial: Quando um indutor de CYP3A4 em potencial, como carbamazepina, é incluído na terapia com aripiprazol, a dose de aripiprazol deve ser dobrada. Aumentos adicionais na dose devem ser baseados na avaliação clínica. Quando um indutor de CYP3A4 for retirado da terapia combinada122, a dose de aripiprazol deve ser reduzida para 10 mg ou 15 mg [vide 6. INTERAÇÕES MEDICAMENTOSAS].
Ajuste de dosagem para pacientes38 recebendo aripiprazol concomitantemente com inibidores de CYP3A e CYP2D6: A dose de aripiprazol deve ser reduzida a um quarto da dose usual em pacientes que possam receber aripiprazol concomitantemente com medicamentos inibidores das CYP3A4 e CYP2D6 [vide 6. INTERAÇÕES MEDICAMENTOSAS]. Ajustes adicionais podem ser necessários com base na avaliação clínica.
Ajuste de dosagem para pacientes38 metabolizadores pobres de substratos de CYP2D6: A dose habitual de aripiprazol deve ser reduzida pela metade em pacientes metabolizadores pobres de substratos de CYP2D6 [vide 3. CARACTERÍSTICAS FARMACOLÓGICAS]. Ajustes adicionais podem ser necessários com base na avaliação clínica.
Não há estudos sobre os efeitos da suspensão oral de aripiprazol administrada por vias não recomendadas. Dessa forma, para a segurança e eficácia da apresentação farmacêutica, a administração deve ser feita apenas por via oral.
REAÇÕES ADVERSAS
As reações adversas mais comuns em pacientes adultos em estudos clínicos (≥ 10%) foram náusea128, vômito129, constipação130, cefaleia131, vertigem132, acatisia133, ansiedade, insônia e inquietação.
Aripiprazol foi avaliado quanto à segurança em 13.543 pacientes adultos que participaram de estudos clínicos de doses múltiplas em esquizofrenia2, transtorno bipolar, Transtorno Depressivo Maior, Demência43 do tipo de Alzheimer96, mal de Parkinson e alcoolismo, os quais tiveram uma exposição de aproximadamente 7619 pacientes/ano a aripiprazol. Um total de 3390 pacientes foi tratado com aripiprazol por, no mínimo, 180 dias e 1933 pacientes tratados com aripiprazol oral tiveram, no mínimo, um ano de exposição.
As condições e a duração do tratamento com aripiprazol (monoterapia e terapia adjuntiva com antidepressivos ou estabilizadores de humor) incluiu (em categorias de sobreposição) estudos duplo-cegos, abertos, comparativos e não comparativos, estudos com pacientes hospitalizados ou ambulatoriais, estudos com dose fixa ou variável e exposição com prazos mais longos e mais curtos.
Os eventos adversos durante a exposição foram obtidos por meio da coleta voluntária de eventos adversos, bem como resultados de exames físicos, sinais vitais134, pesos, análises laboratoriais e ECG. Experiências adversas foram registradas pelos investigadores clínicos com a terminologia de sua própria escolha. Nas tabelas e tabulações a seguir, a terminologia do dicionário MedDRA foi utilizada para classificar eventos adversos relatados em uma quantidade menor de categorias padronizadas de eventos, de modo a fornecer uma estimativa significativa da proporção de indivíduos que apresentaram eventos adversos.
As frequências declaradas das reações adversas representam a proporção de indivíduos que apresentaram no mínimo uma vez o evento adverso emergente do tratamento do tipo listado. Um evento foi considerado emergente do tratamento se ocorreu pela primeira vez ou piorou enquanto o paciente recebia a terapia após a avaliação da linha basal. Não se procurou utilizar as avaliações de causalidade segundo o investigador, ou seja, todos os eventos que atendiam aos critérios, independentemente da causalidade segundo o investigador, foram incluídos.
As reações adversas são relatadas ao longo desta seção. São eventos adversos que foram considerados razoavelmente associados ao uso de aripiprazol (reações medicamentosas adversas), com base na avaliação abrangente das informações disponíveis sobre o evento adverso. Uma associação causal com aripiprazol geralmente não pode ser estabelecida com segurança em casos individuais.
Os valores nas tabelas e tabulações não podem ser utilizados para prever a incidência48 de efeitos colaterais135 no decorrer da prática médica normal, em que características do paciente e outros fatores diferem daqueles que prevaleceram em estudos clínicos. De forma semelhante, as frequências mencionadas não podem ser comparadas aos valores obtidos a partir de outras investigações clínicas envolvendo outros tratamentos, utilizações e investigadores. No entanto, os valores mencionados de fato fornecem ao médico responsável pela prescrição algum fundamento para a estimativa da contribuição relativa de fatores medicamentosos e não medicamentosos à incidência48 de reações adversas na população estudada.
Experiência de estudos clínicos
Esquizofrenia2
Os achados abaixo são baseados em uma combinação de cinco estudos controlados por placebo4 (quatro de 4 semanas e um de 6 semanas), nos quais aripiprazol foi administrado em doses que variaram entre 2 mg/dia e 30 mg/dia.
Reações adversas associadas à descontinuação do tratamento: No geral, houve pouca diferença na incidência48 de descontinuação devida a reações adversas em pacientes tratados com aripiprazol (7%) e aqueles tratados com placebo4 (9%). Os tipos de reações adversas que levaram à descontinuação foram semelhantes para os pacientes tratados com aripiprazol e os tratados com placebo4.
Reações adversas comumente observadas: A única reação adversa mais frequentemente observada associada ao uso de aripiprazol em pacientes com esquizofrenia2 (incidência48 de, no mínimo, 5% e incidência48 do aripiprazol pelo menos o dobro da incidência48 do placebo4) foi acatisia133 (aripiprazol 8%; placebo4 4%).
Mania Bipolar
Monoterapia: Os achados abaixo foram baseados em uma combinação de estudos de três semanas, controlados por placebo4, de mania bipolar, nos quais aripiprazol foi administrado a doses de 15 mg/dia ou 30 mg/dia.
Reações adversas associadas à descontinuação do tratamento: No geral, houve pouca diferença na incidência48 de descontinuação devida a reações adversas em pacientes com mania bipolar tratados com aripiprazol (11%) e tratados com placebo4 (10%). Os tipos de reações adversas que levaram à descontinuação foram semelhantes entre os pacientes tratados com aripiprazol e os tratados com placebo4.
Reações adversas comumente observadas: As reações adversas mais frequentemente observadas associadas ao uso de aripiprazol em pacientes com mania bipolar (incidência48 de, no mínimo, 5% e incidência48 do aripiprazol pelo menos o dobro da incidência48 do placebo4) são apresentadas na Tabela 1.
Tabela 1. Reações adversas comumente observadas em estudos de curto prazo e controlados por placebo4 em pacientes com mania bipolar tratados com monoterapia oral de aripiprazol.
|
Porcentagem de pacientes que relataram reação |
||
|
Termo Preferencial |
Aripripazol |
Placebo4 |
|
Acatisia133 |
13 |
4 |
|
Sedação52 |
8 |
3 |
|
Inquietação |
6 |
3 |
|
Tremores |
6 |
3 |
|
Distúrbio Extrapiramidal |
5 |
2 |
Reações Adversas Menos Comuns: A Tabela 2 enumera a incidência48 combinada, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (até seis semanas em esquizofrenia2 e até três semanas em mania bipolar), incluindo apenas aquelas reações que ocorreram em pelo menos 2% dos pacientes tratados com aripiprazol (doses ≥ 2 mg/dia) e cuja incidência48 em pacientes tratados com aripiprazol foi superior à incidência48 em pacientes tratados com placebo4 no conjunto de dados combinado.
Tabela 2. Reações adversas em estudos de curto prazo e controlados por placebo4 em pacientes tratados com aripiprazol
|
Porcentagem de pacientes que relataram reaçãoa |
||
|
Classe de sistemas de órgãos |
Aripiprazol |
Placebo4 |
|
Distúrbios oculares |
||
|
Visão136 embaçada |
3 |
1 |
|
Distúrbios gastrintestinais |
||
|
Náusea128 |
15 |
11 |
|
Constipação130 |
11 |
7 |
|
Vômito129 |
11 |
6 |
|
Dispepsia137 |
9 |
7 |
|
Boca138 seca |
5 |
4 |
|
Dor de dente139 |
4 |
3 |
|
Desconforto abdominal |
3 |
2 |
|
Desconforto escomacal |
3 |
2 |
|
Distúrbios gerais |
||
|
Fadiga140 |
6 |
4 |
|
Dor |
3 |
2 |
|
Distúrbio Muscoloesquelético e do Tecido conjuntivo141 |
||
|
Rigidez musculoesquelética |
4 |
3 |
|
Dor na extremidade |
4 |
2 |
|
Mialgia142 |
2 |
1 |
|
Espasmos143 musculares |
2 |
1 |
|
Distúrbios do sistema nervoso144 |
||
|
Cefaleia131 |
27 |
23 |
|
Vertigem132 |
10 |
7 |
|
Acatisia133 |
10 |
4 |
|
Sedação52 |
7 |
4 |
|
Distúrbio extrapiramidal |
5 |
3 |
|
Tremores |
5 |
3 |
|
Sonolência |
5 |
3 |
|
Transtornos psiquiátricos |
||
|
Agitação |
19 |
17 |
|
Insônia |
18 |
13 |
|
Ansiedade |
17 |
13 |
|
Inquietação |
5 |
3 |
|
Distúrbios respiratórios, torácicos e mediastinais |
||
|
Dor faringolaríngea |
3 |
2 |
|
Tosse |
3 |
2 |
|
a Reações adversas relatadas por, no mínimo, 2% dos pacientes tratados com aripiprazol, exceto por reações adversas com incidência48 menor ou igual ao placebo4. |
||
Um exame dos subgrupos de população não revelou nenhuma evidência clara de incidência48 diferencial de reação adversa com relação à idade, sexo ou raça.
Terapia adjuntiva com mania bipolar
Os achados abaixo são baseados em um estudo controlado por placebo4 em pacientes adultos com transtorno bipolar nos quais o aripiprazol foi administrado a doses de 15 mg/dia ou 30 mg/dia como terapia adjuntiva ao lítio ou valproato.
Reações adversas associadas à descontinuação do tratamento: Em um estudo com pacientes que já toleravam lítio ou valproato como monoterapia, as taxas de descontinuação devida a reações adversas foram de 12% para pacientes38 tratados com aripiprazol em terapia adjuntiva, em comparação a 6% dos pacientes tratados com placebo4 em terapia adjuntiva.
As reações medicamentosas adversas mais comuns associadas à descontinuação em pacientes tratados com aripiprazol em terapia adjuntiva, em comparação a pacientes tratados com placebo4 em terapia adjuntiva, foram acatisia133 (5% e 1%, respectivamente) e tremores (2% e 1%, respectivamente).
Reações adversas comumente observadas: As reações adversas mais frequentemente observadas associadas ao aripiprazol em terapia adjuntiva e lítio ou valproato em pacientes com mania bipolar (incidência48 de, no mínimo, 5% e incidência48 de pelo menos o dobro no placebo4 em terapia adjuntiva) foram: acatisia133, insônia e distúrbio extrapiramidal.
Reações adversas menos comuns em pacientes sob terapia adjuntiva em mania bipolar: A Tabela 3 enumera a incidência48, arredondada para o percentual mais próximo, de reações adversas que ocorreram durante a terapia aguda (até seis semanas), incluindo apenas aquelas reações que ocorreram em, no mínimo, 2% dos pacientes tratados com aripiprazol em terapia adjuntiva (doses de 15 mg/dia ou 30 mg/dia) e lítio ou valproato, e cuja incidência48 em pacientes tratados com essa combinação foi superior à incidência48 nos pacientes tratados com placebo4 mais lítio ou valproato.
Tabela 3. Eventos adversos em estudo de curto prazo e controlado por placebo4 sobre a terapia adjuntiva em pacientes com transtorno bipolar
|
|
Porcentagem de pacientes que relataram a relaçãoa |
|
|
Classe de Sistemas de Órgãos |
Aripiprazol + Li ou Val* |
Placebo4 + Li ou Val* |
|
Distúrbios Gastrointestinais |
||
|
Náusea128 |
8 |
5 |
|
Vômito129 |
4 |
0 |
|
Hipersecreção Salivar |
4 |
2 |
|
Boca138 seca |
2 |
1 |
|
Infecções145 e Infestações |
||
|
Nasofaringite |
3 |
2 |
|
Investigações |
||
|
Aumento de peso |
2 |
1 |
|
Distúrbios do Sistema Nervoso144 |
||
|
Acatisia133 |
19 |
5 |
|
Tremores |
9 |
6 |
|
Distúrbio Extrapiramidal |
5 |
1 |
|
Vertigem132 |
4 |
1 |
|
Sedação52 |
4 |
2 |
|
Transtornos Psiquiátricos |
||
|
Insônia |
8 |
4 |
|
Ansiedade |
4 |
1 |
|
Inquietação |
2 |
1 |
|
a Reações adversas relatadas por, no mínimo, 2% dos pacientes tratados com aripiprazol, exceto por reações adversas com incidência48 menor ou igual ao placebo4. |
||
Reações adversas relacionadas à dose
Esquizofrenia2: As relações de resposta à dose para a incidência48 de eventos adversos emergentes do tratamento foram avaliadas a partir de quatro estudos em pacientes adultos com esquizofrenia2 comparando doses fixas variadas (2 mg/dia, 5 mg/dia, 10 mg/dia, 15 mg/dia, 20 mg/dia e 30 mg/dia) de aripiprazol ao placebo4. Essa análise, estratificada por estudo, indicou que a única reação adversa possivelmente relacionada à dose, e mais notável apenas com 30 mg, foi sonolência [incluindo sedação52]; (incidências para o placebo4: 7,1%; 10 mg, 8,5%; 15 mg, 8,7%;20 mg, 7,5%; 30 mg, 12,6%).
Sintomas7 Extrapiramidais
Esquizofrenia2: Em estudos de curto prazo e controlados por placebo4 em esquizofrenia2 em adultos, a incidência48 de eventos relacionados à síndrome8 extrapiramidal relatados, exceto por eventos relacionados à acatisia133, para pacientes38 tratados com aripiprazol, foi de 13% versus 12% para placebo4. A incidência48 de eventos relacionados à acatisia133 para pacientes38 tratados com aripiprazol foi de 8% versus 4% para placebo4.
Dados coletados objetivamente a partir desses estudos foram reunidos na Escala de Classificação de Simpson Angus (para síndrome8 extrapiramidal), Escala de Acatisia133 de Barnes (para acatisia133) e nas Avaliações das Escalas de Movimento Involuntário (para discinesia). Em estudos de esquizofrenia2 em adultos, os dados coletados objetivamente não apresentaram uma diferença entre aripiprazol e placebo4, exceto pela Escala de Acatisia133 de Barnes (aripiprazol, 0,08; placebo4, -0,05).
De maneira semelhante, em um estudo de longo prazo (26 semanas), controlado por placebo4, de esquizofrenia2 em adultos, os dados coletados objetivamente na Escala de Classificação de Simpson Angus (para síndrome8 extrapiramidal), Escala de Acatisia133 de Barnes (para agitação motora) e nas Avaliações das Escalas de Movimento Involuntário (para discinesia) não apresentaram diferença entre aripiprazol e placebo4.
Mania Bipolar: Em estudos de curto prazo e controlados por placebo4 em mania bipolar em adultos, a incidência48 de eventos relacionados à síndrome8 extrapiramidal relatados, exceto por eventos relacionados à acatisia133, para pacientes38 tratados com aripiprazol em monoterapia, foi de 16% versus 8% para placebo4. A incidência48 de eventos relacionados à acatisia133 para pacientes38 tratados com aripiprazol em monoterapia foi de 13% versus 4% para placebo4. Em um estudo de seis semanas, controlado por placebo4, em mania bipolar para terapia adjuntiva com lítio ou valproato, a incidência48 de eventos relacionados à síndrome8 extrapiramidal relatados, exceto por eventos relacionados à acatisia133, para pacientes38 tratados com aripiprazol em terapia adjuntiva, foi de 15% versus 8% para placebo4 em terapia adjuntiva. A incidência48 de eventos relacionados à acatisia133 para pacientes38 tratados com aripiprazol em terapia adjuntiva foi de 19% versus 5% para placebo4 em terapia adjuntiva.
Nos estudos de monoterapia de aripiprazol em adultos com mania bipolar, a Escala de Classificação de Simpson Angus e a Escala de Acatisia133 de Barnes demonstraram uma diferença significativa entre aripiprazol e placebo4 (aripiprazol, 0,50; placebo4, -0,01 e aripiprazol, 0,21; placebo4, -0,05). As alterações nas Avaliações das Escalas de Movimento Involuntário foram semelhantes para os grupos de aripiprazol e placebo4. Em estudos de mania bipolar com aripiprazol como terapia adjuntiva com lítio ou valproato, a Escala de Classificação de Simpson Angus e a Escala de Acatisia133 de Barnes demonstraram uma diferença significativa entre aripiprazol e placebo4 em terapia adjuntiva (aripiprazol, 0,73; placebo4, 0,07 e aripiprazol, 0,30; placebo4, 0,11). As alterações nas Avaliações das Escalas de Movimento Involuntário foram semelhantes para os grupos de aripiprazol e placebo4 em terapia adjuntiva.
Distonia146: Sintomas7 de distonia146, contrações anormais prolongadas de conjuntos de músculos147, podem ocorrer em indivíduos susceptíveis durante os primeiros dias de tratamento. Os sintomas7 da distonia146 incluem: espasmos143 nos músculos do pescoço148, algumas vezes progredindo para compressão da garganta149, dificuldade em engolir, dificuldade em respirar e/ou protrusão da língua150. Embora estes sintomas7 possam ocorrer em doses baixas, eles ocorrem mais frequentemente e com maior gravidade sob concentrações maiores e doses mais altas de drogas antipsicóticas de primeira geração. Um risco elevado de distonia146 aguda é observado em grupos de homens e indivíduos mais jovens.
Ganho de Peso: Em estudos de quatro a seis semanas em adultos com esquizofrenia2, houve uma leve diferença no ganho de peso médio entre pacientes recebendo aripiprazol e placebo4 (+0,7 kg versus -0,05 kg, respectivamente) e também foi observada diferença na proporção de pacientes que atendiam ao critério de ganho de peso ?7% do peso corporal [aripiprazol (8%) comparado a placebo4 (3%)]. Em estudos de três semanas de monoterapia de aripiprazol em adultos com mania, o ganho de peso médio para pacientes38 recebendo aripiprazol e placebo4 foi de 0,1 kg versus 0,0 kg, respectivamente. A proporção de pacientes que atenderam ao critério de ganho de peso ?7% do peso corporal foi de 2% com aripiprazol em comparação a 3% com placebo4. No estudo de seis semanas em Mania com aripiprazol como terapia adjuntiva com lítio ou valproato, o ganho de peso médio para os pacientes recebendo aripiprazol e placebo4 foi de 0,6 kg versus 0,2 kg, respectivamente. A proporção de pacientes que atenderam ao critério de ganho de peso ? 7% do peso corporal foi de 3% com aripiprazol em comparação a 4% com placebo4 em terapia adjuntiva.
A Tabela 4 fornece os resultados na alteração de peso de um estudo de longo prazo (26 semanas), controlado por placebo4, de aripiprazol em adultos com esquizofrenia2, a alteração média a partir da linha basal e as proporções de pacientes que atenderam ao critério de ganho de peso de ≥ 7% o peso corporal relativo à linha basal, categorizado pelo índice de massa corporal151 (IMC152) na linha basal. Apesar de não haver aumento no peso médio, o grupo de aripiprazol tendeu a apresentar mais pacientes com um ganho de peso ≥ 7%.
Tabela 4. Resultados na alteraçõ de peso categorizados pelo índice de massa corporal151 na linha basal: estudo controlado por placebo4 em esquizofrenia2, amostra de segurança
|
|
IMC152 < 23 |
IMC152 23–27 |
IMC152 > 27 |
|||
|
Placebo4 |
Aripiprazol |
Placebo4 |
Aripiprazol |
Placebo4 |
Aripiprazol |
|
|
Alteração média a partir da linha basal (kg) |
-0,5 |
-0,5 |
-0,6 |
-1,3 |
-1,5 |
-2,1 |
|
% com aumento ≥ 7% o peso corporal |
3,7% |
6,8% |
4,2% |
5,1% |
4,1% |
5,7% |
A Tabela 5 fornece os resultados na alteração de peso de um estudo de longo prazo (52 semanas) de aripiprazol em adultos com esquizofrenia2, a alteração média a partir da linha basal e as proporções de pacientes que atenderam ao critério de ganho de peso ≥ 7% o peso corporal relativo à linha basal, categorizado pelo índice de massa corporal151 (IMC152) na linha basal:
Tabela 5. Resultados na alteração de peso categorizados pelo índice de massa corporal151 na linha basal: estudo controlado ativamente em esquizofrenia2, amostra de segurança
|
IMC152 < 23 |
IMC152 23–27 |
IMC152 > 27 |
|
|
(n=314) |
(n=265) |
(n=260) |
|
|
Alteração média a partir da linha basal (kg) |
2,6 |
1,4 |
-1,2 |
|
% com aumento ≥ 7% o peso corporal |
30% |
19% |
8% |
Achados adicionais observados em estudos clínicos
Reações adversas em estudo de longo prazo, duplo-cegos e controlados por placebo4: As reações adversas relatadas em um estudo duplo-cego153 de 26 semanas, comparando aripiprazol e placebo4 em pacientes com esquizofrenia2, foram em geral consistentes com aquelas relatadas em estudos de curto prazo e controlados por placebo4, exceto por uma incidência48 maior de tremores [8% (12/153) para aripiprazol versus 2% (3/153) para placebo4]. Neste estudo, a maioria dos casos de tremores teve intensidade leve (8/12 leve e 4/12 moderada), ocorreu no início da terapia (9/12 ≤ 49 dias) e apresentou duração limitada (7/12 ≤ 10 dias). Em casos raros, os tremores levaram à descontinuação (<1%) de aripiprazol. Ademais, em um estudo de longo prazo (52 semanas), controlado por medicamento ativo, a incidência48 de tremores foi de 5% (40/859) para aripiprazol. Um perfil semelhante foi observado em um estudo de longo prazo com transtorno bipolar.
Outras reações adversas observadas durante a avaliação pré-comercialização de aripiprazol: Abaixo pode ser encontrada uma relação dos termos do MedDRA que refletem as reações adversas como definidas em REAÇÕES ADVERSAS, relatadas por pacientes tratados com aripiprazol oral em doses múltiplas ? 2 mg/dia durante qualquer fase de um estudo no banco de dados de 13.543 pacientes adultos.
Todos os eventos avaliados como possíveis reações adversas foram incluídos, exceto pelos eventos mais frequentes. Além disso, reações adversas médica ou clinicamente significativas, em especial aquelas provavelmente mais úteis para o médico responsável pela prescrição, ou que apresentam plausibilidade farmacológica, também foram incluídas. Eventos já listados em outras partes de REAÇÕES ADVERSAS, ou aqueles mencionados em ADVERTÊNCIAS E PRECAUÇÕES ou SUPERDOSE foram excluídos.
Apesar de as reações relatadas terem ocorrido durante o tratamento com aripiprazol, elas não foram necessariamente causadas pelo medicamento.
Os eventos são, ainda, categorizados pela classe de sistemas de órgãos e listados em frequência decrescente de acordo com as definições abaixo:
- Comum (frequente): ocorreram em ≥ 1/100 e < 1/10 dos pacientes (apenas aqueles ainda não listados nos resultados tabelados de estudos controlados por placebo4 aparecem nessa relação);
- Incomum (infrequente): ocorreram em ≥ 1/1000 e < 1/100 dos pacientes;
- Raro: ocorreram em ≥ 1/10000 e < 1/1000 dos pacientes.
Distúrbios do sistema linfático154 e sanguíneo:
- Incomuns – leucopenia90, neutropenia91, trombocitopenia155.
Distúrbios cardíacos:
- Incomuns – bradicardia156, palpitações157, insuficiência158 cardiopulmonar, infarto do miocárdio83, parada cardiorrespiratória, bloqueio atrioventricular, extrassístoles, taquicardia57 sinusal, fibrilação atrial, angina159 pectoris, isquemia160 miocárdica;
- Raros – flutter atrial, taquicardia57 supraventricular, taquicardia57 ventricular.
Distúrbios oculares:
- Incomuns – fotofobia161, diplopia162, edema163 na pálpebra, fotopsia.
Distúrbios gastrintestinais:
- Incomuns – diarreia164, doença do refluxo gastroesofágico165, edema163 de língua150, esofagite166;
- Raro – pancreatite167.
Distúrbios gerais e condições no local de administração:
- Comuns – astenia168, edema163 periférico, dor no peito169, pirexia170, irritabilidade;
- Incomuns – edema163 facial, angioedema171, sede;
- Raro – hipotermia172.
Distúrbios hepatobiliares173:
- Raros– hepatite174, icterícia175.
Distúrbios do sistema imunológico176:
- Incomum – hipersensibilidade.
Lesões89, intoxicação e complicações do procedimento:
- Comum – queda; Incomum – automutilação;
- Raro – insolação.
Investigações:
- Comuns – redução do peso, creatinofosfoquinase elevada;
- Incomuns – enzima177 hepática36 elevada, glicose76 sérica elevada, prolactina103 sérica elevada, ureia178 sérica elevada, prolongamento do QT no eletrocardiograma179, creatinina32 sérica elevada, bilirrubina180 sérica elevada;
- Raros – lactato181 desidrogenase sérico elevada, hemoglobina glicosilada182 elevada, gama glutamil transferase elevada.
Distúrbios metabólicos e nutricionais:
- Comum – apetite reduzido;
- Incomuns – hiperlipidemia183, anorexia184, diabetes73 mellitus (incluindo insulina185 sérica elevada, tolerância a carboidratos reduzida, diabetes73 mellitus não dependente de insulina185, tolerância à glicose76 prejudicada, glicosúria186), hiperglicemia72, hipocalemia187, hiponatremia188, hipoglicemia189, polidipsia78;
- Raro – cetoacidose diabética190.
Distúrbio musculoesquelético e do tecido conjuntivo141:
- Incomuns – rigidez muscular, fraqueza muscular, compressão muscular, mobilidade reduzida;
- Raro – rabdomiólise60.
Distúrbios do sistema nervoso144:
- Comuns – coordenação anormal, discinesia; Incomuns – distúrbio na fala, parkinsonismo, comprometimento da memória, rigidez de roda dentada, acidente vascular cerebral47, hipocinesia, discinesia tardia69, hipotonia119, mioclonia191, hipertonia118, acinesia, bradicinesia192;
- Raros – convulsão193 de grande mal, coreoatetose.
Transtornos psiquiátricos:
- Comum – ideação suicida;
- Incomuns – agressividade, perda da libido194, tentativa de suicídio, hostilidade, libido194 elevada, raiva195, anorgasmia196, delírios, automutilação intencional, suicídio concluído, tique197, ideação homicida;
- Raros – catatonia, sonambulismo.
Distúrbios renais e urinários:
- Incomuns – retenção urinária198, poliúria79, noctúria.
Distúrbios do sistema reprodutor e das mamas199:
- Incomuns – menstruação200 irregular, disfunção erétil, amenorreia201, dor nas mamas199;
- Raros – ginecomastia202, priapismo203.
Distúrbios respiratórios, torácicos e mediastinais:
- Comuns – congestão nasal, dispneia204, pneumonia46 por aspiração.
Distúrbios cutâneos e subcutâneos:
- Comuns – rash205 (incluindo rash205 eritematoso206, esfoliativo, generalizado, macular, maculopapular207, papular; dermatite208 acneiforme, alérgica, de contato, esfoliativa, seborreica, neurodermatite e erupção209 medicamentosa), hiperidrose210;
- Incomuns – prurido39, reação fotossensível, alopecia211, urticária40.
Distúrbios vasculares87:
- Comum – hipertensão212;
- Incomum – hipotensão15.
Experiência pós-comercialização
As reações adversas abaixo foram identificadas durante o uso após a aprovação de aripiprazol. Em razão de essas reações serem relatadas voluntariamente por uma população de tamanho indeterminado, nem sempre é possível estabelecer uma relação causal com a exposição à droga: ocorrências raras de reação alérgica213 (reação anafilática214, angioedema171, laringoespasmo, prurido39/urticária40 ou espasmo215 orofaríngeo216), gripe217, crise oculogírica (movimentos involuntários dos olhos218), dor testicular, depressão, dor esofágica, apetite aumentado, tendinite219, arrepios, perturbação afetiva, mal estar, doença de Parkinson220, leucocitose221 (aumento da contagem de leucócitos93 no sangue222), disgeusia223 (alteração do paladar224), eructação225 (arrotos), irritação na garganta149, comportamento anormal, tromboembolismo88 venoso, oscilação da glicose76 sérica e comportamentos compulsivos relacionados à jogos, alimentação, compras e sexo. Estes comportamentos compulsivos são raros, ocorrem em especial no início ou aumento de dose do medicamento e cessaram com a redução da dose ou interrupção do tratamento.
Os profissionais de saúde1 devem monitorar e alertar os pacientes e cuidadores sobre a possibilidade de ocorrência de comportamento compulsivo. Deve ser considerada a redução de dose ou a interrupção do tratamento com aripiprazol, caso o paciente apresente este comportamento.
Atenção: este produto é um medicamento que possui nova forma farmacêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos
Em casos de eventos adversos, notifique ao Sistema de Notificação de Eventos Adversos a Medicamentos – VIGIMED, ou para a Vigilância Sanitária Estadual ou Municipal.
SUPERDOSE
A terminologia do MedDRA tem sido utilizada para classificar as reações adversas.
Experiência em humanos
Um total de 76 casos de superdosagem deliberada ou acidental com aripiprazol oral foi reportado mundialmente. Eles incluem superdosagens com aripiprazol isolado e combinado a outras substâncias. Não foi relatada fatalidade nesses casos. Dos 44 casos com resultados conhecidos,
33 casos tiveram recuperação sem sequelas226 e em um caso houve recuperação com sequelas226 (midríase227 e sensação de anormalidade). O maior caso conhecido de ingestão aguda com resultado conhecido envolveu 1080 mg de aripiprazol (36 vezes a dose diária recomendada máxima) por um paciente que teve recuperação completa. Nos 76 casos, estão incluídos 10 casos de superdosagem deliberada ou acidental de crianças (com, no máximo, 12 anos de idade) envolvendo ingestões de aripiprazol de até 195 mg, sem fatalidades.
As reações adversas comuns (relatadas em, no mínimo, 5% de todos os casos de superdosagem) relatadas na superdosagem de aripiprazol oral (isolado ou combinado a outras substâncias) incluem vômito129, sonolência e tremores. Outros sinais6 e sintomas7 clinicamente importantes observados em um ou mais pacientes com superdosagem de aripiprazol (isolado ou combinado a outras substâncias) incluem acidose228, agressividade, aspartato aminotransferase elevado, fibrilação atrial, bradicardia156, coma74, estado de confusão, convulsão193, creatinofosfoquinase sérica elevada, nível de consciência deprimido, hipertensão212, hipocalemia187, hipotensão15, letargia51, perda de consciência, prolongamento do complexo QRS, prolongamento do QT, pneumonia46 por aspiração, parada respiratória, condição epiléptica e taquicardia57.
Conduta em caso de superdose
Não há informações específicas sobre o tratamento da superdosagem com aripiprazol. Deve ser realizado um eletrocardiograma179 em caso de superdosagem. Se houver prolongamento do intervalo QT, deve-se fazer o monitoramento cardíaco. De outra forma, a conduta em caso de superdosagem deve se concentrar em terapia de apoio, mantendo as vias aéreas adequadas, oxigenadas e ventiladas, além de tratar os sintomas7. Deve-se manter uma supervisão e um monitoramento médico rigoroso até a recuperação do paciente.
Carvão vegetal: Em caso de superdosagem deste medicamento, a administração precoce de carvão vegetal pode ser útil para evitar parcialmente a absorção de aripiprazol. A administração de 50 g de carvão vegetal ativado, uma hora após uma dose oral única de 15 mg de aripiprazol, reduziu a AUC24 e a Cmáx médias de aripiprazol em 50%.
Hemodiálise229: Apesar de não haver informações sobre o efeito da hemodiálise229 no tratamento de uma superdosagem de aripiprazol, é improvável que a hemodiálise229 seja útil na resolução da superdosagem, já que aripiprazol tem grande afinidade com as proteínas27 séricas.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
REFERÊNCIAS
- Bramer S, et al. An open label study of aripiprazole (OPC-14597) in healthy adults with poor and extensive metabolizer genotypes for cytochrome P450 2D6, and the effect of coadministered quinidine on aripiprazole pharmacokinetics (Study No. 31-98-207). Otsuka Maryland Research Institute, 1º de junho de 2001. Número de controle de documentos BMS 920011708. Tabela 11.3.2A, p62.
- Bramer S, et al. A Double-Blind, Placebo4-controlled Study of the Effects of Oral Administered Ketoconazole on OPC-14597 Pharmacokinetics in Healthy Adult Male and Female Subjects (Study No. 31-98-206). Otsuka Maryland Research Institute, 5 de junho de 2001. Número de controle de documentos BMS 920011707. Tabelas 11.3.1A-11.3.1B, p62–63.
- Kornhauser D et al. Safety, tolerability and pharmacokinetics of aripiprazole and carbamazepine in patients with schizophrenia and schizoaffective disorder: Interim report on pharmacokinetics and preliminary safety data. (Study No. CN138-022). Bristol-Myers Squibb Company. 9 de agosto de 2002. Número de controle de documentos BMS 930002163. Tabela 11.2.1, p 62.
- Kornhauser D et al. Safety, tolerability and pharmacokinetics of aripiprazole and carbamazepine in patients with schizophrenia and schizoaffective disorder: Interim report on pharmacokinetics and preliminary safety data. (Study No. CN138-022). Bristol-Myers Squibb Company. 9 de agosto de 2002. Número de controle de documentos BMS 930002163. Tabela 11.2.1, p 62 e Tabela 11.2.2 p 64.
- Guidelines for Preparing Core Clinical-Safety Information on Drugs, Second Edition. Report of CIOMS Working Groups III and V, Geneva 1999. 104 Caraco, Y, Sheller J, and Wood, A., Pharmacogenetic Determinants of Codeine Induction by Rifampin: The Impact on Codeine’s Respiratory, Psychomotor and Miotic Effects. Journal of Pharmacology and Experimental Therapeutics. Volume 281 p 330-336, 1997.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
SÓ PODE SER VENDIDO COM RETENÇÃO DA RECEITA
MS - 1.0573.0724
Farmacêutica Responsável: Gabriela Mallmann CRF-SP nº 30.138
Registrado por:
Aché Laboratórios Farmacêuticos S.A.
Av. Brigadeiro Faria Lima, 201 – 20º andar
São Paulo – SP
CNPJ 60.659.463/0029-92
Indústria Brasileira
Fabricado por:
Aché Laboratórios Farmacêuticos S.A.
Guarulhos - SP
SAC 0800 701 6900






