Stelara
JANSSEN-CILAG FARMACÊUTICA LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
STELARA®
ustequinumabe
Solução injetáve
APRESENTAÇÕES
Solução injetável de Stelara® 45 mg/0,5 mL em embalagem com 1 frasco-ampola ou 1 seringa1 preenchida.
Solução injetável de Stelara® 90 mg/1,0 mL em embalagem com 1 seringa1 preenchida.
As seringas preenchidas possuem um dispositivo de proteção da agulha.
USO SUBCUTÂNEO2
USO ADULTO
COMPOSIÇÃO
Cada frasco-ampola Stelara® 45 mg/0,5 mL contém:
| ustequinumabe | 45 mg |
| excipiente q.s.p. | 0,5 mL |
Cada frasco-ampola Stelara® 90 mg/1 mL contém:
| ustequinumabe | 90 mg |
| excipiente q.s.p. | 1 mL |
Excipientes: água para injetáveis, L-histidina, cloridrato de L-histidina monoidratado, polissorbato 80 e sacarose.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Stelara® é indicado no tratamento da psoríase3 em placa4, moderada a grave, em adultos que não responderam, ou que têm uma contraindicação, ou que são intolerantes a outras terapêuticas sistêmicas, incluindo ciclosporina, metotrexato e radiação ultravioleta A associada à administração de psoraleno (PUVA).
Stelara®, isolado ou em combinação com metotrexato, é indicado para o tratamento da artrite5 psoriásica ativa em pacientes adultos, quando a resposta ao tratamento com drogas antirreumáticas modificadoras da doença (DMARD) foi inadequada.
Stelara® é indicado para o tratamento de pacientes adultos com Doença de Crohn6 ativa de moderada a grave, que tiveram uma resposta inadequada, perda de resposta ou que foram intolerantes à terapia convencional7 ou ao anti-TNF-alfa ou que tem contraindicações médicas para tais terapias.
COMO ESTE MEDICAMENTO FUNCIONA?
Stelara® é um anticorpo8 monoclonal IgG1kappa completamente humano que se liga com especificidade à subunidade compartilhada proteica p40 das citocinas9 humanas: interleucina (IL)-12 e IL-23. Stelara® inibe a bioatividade da IL-12 e da IL-23 humanas impedindo que a p40 se ligue ao receptor proteico IL-12Rbeta1 expresso na superfície das células10 do sistema imunológico11. Stelara® não se liga a IL-12 nem a IL-23 já ligadas aos receptores de superfície celular IL-12Rbeta1. Assim, não é provável que Stelara® contribua para a citotoxicidade mediada por complemento ou anticorpo8 das células10 expressando receptores de IL-12 e/ou IL-23.
A IL-12 e IL-23 são citocinas9 heterodiméricas secretadas pelas células10 apresentadoras de antígeno12 ativadas, como macrófagos13 e células dendríticas14. A IL-12 estimula as células10 “natural killer” (NK) e conduz a diferenciação das células10 T CD4+ para o fenótipo15 de células10 auxiliares T1 (Th1) e estimula a produção de gamainterferona (IFN?). A IL-23 induz a via da célula16 auxiliar T17 (Th17) e promove a secreção de IL-17A, IL-21 e IL-22. Os níveis de IL-12 e IL-23 são elevados na pele17 e no sangue18 de pacientes com psoríase3, e a IL12/23p40 sérica faz a distinção entre pacientes com artrite5 psoriásica e indivíduos sadios, implicando a IL-12 e IL-23 na fisiopatologia19 de doenças inflamatórias psoriásicas. Polimorfismos genéticos nos genes da IL-23A, IL-23R e IL-12B conferem susceptibilidade20 a estas doenças. Adicionalmente a IL-12 e a IL-23 são altamente expressas na pele17 psoriásica lesionada e a indução de INF? mediada pela IL-12 está correlacionada com a atividade da doença psoriásica. Células10 T responsivas para IL-23 foram encontradas na êntese em um modelo de artrite5 inflamatória de camundongo, onde a IL-23 dirige a inflamação21 da êntese.
Além disso, há evidência pré-clínica implicando a IL-23 e vias descendentes na erosão óssea e destruição óssea através do aumento do ligante do receptor ativador do fator nuclear-kappa B (RANKL), a qual ativa os osteoclastos22.
Em pacientes com doença de Crohn6, IL-12 e IL-23 estão elevadas nos intestinos23 e gânglios linfáticos24. Isto é acompanhado por aumentos séricos dos níveis de IFN? e IL-17A, sugerindo que a IL-12 e IL- 23 promovem a ativação do Th1 e Th17 na doença de Crohn6. Tanto a IL-12 quanto a IL-23 também podem estimular a produção de TNF-alfa por células10 T, resultando na inflamação21 intestinal crônica e lesão25 das células10 epiteliais. Associações significativas foram encontradas entre a doença de Crohn6 e polimorfismos genéticos nos genes IL23R e IL12B, sugerindo um potencial papel causal para a IL- 12/23 de sinalização na doença. Isto é suportado pelos dados pré-clínicos que demonstram que a sinalização IL-12/23 é necessária para a lesão25 intestinal nos modelos de rato para doença inflamatória intestinal.
Ao se ligar a subunidade p40 compartilhada da IL-12 e IL-23, Stelara® pode exercer seus efeitos clínicos tanto na psoríase3, na artrite5 psoriásica e na doença de crohn6 através da interrupção das vias das citocinas9 relacionadas à Th1 e Th17, que são centrais na fisiopatologia19 destas doenças.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
O uso de Stelara® não é indicado para pessoas com hipersensibilidade grave ao ustequinumabe ou a qualquer um dos excipientes do produto.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Infecções26
Stelara® é um imunossupressor27 seletivo e pode ter o potencial de aumentar o risco de infecções26 e reativar infecções26 latentes.
Em estudos clínicos, infecções26 bacterianas, fúngicas28 e virais graves têm sido observadas em pacientes que receberam Stelara®.
Stelara® não deve ser administrado a pacientes com infecção29 ativa clinicamente importante. Deve-se ter cautela ao considerar o uso de Stelara® em pacientes com infecção29 crônica ou história de infecção29 recorrente.
Antes de iniciar o tratamento com Stelara®, os pacientes devem ser avaliados para infecção29 por tuberculose30. Stelara® não deve ser administrado a pacientes com tuberculose30 ativa. O tratamento de infecção29 de tuberculose30 latente deve ser iniciado antes da administração de Stelara®. A terapia antituberculose também deve ser considerada antes do início de Stelara® em pacientes com história pregressa de tuberculose30 latente ou ativa nos quais um curso adequado de tratamento não puder ser confirmado. Os pacientes que recebem Stelara® devem ser monitorados rigorosamente para sinais31 e sintomas32 de tuberculose30 ativa durante e após o tratamento.
Os pacientes devem ser orientados a procurar ajuda médica se ocorrerem sinais31 ou sintomas32 sugestivos de infecção29. Se um paciente desenvolver uma infecção29 grave, deve ser monitorado rigorosamente e Stelara® não deve ser administrado até a resolução da infecção29 (vide “Quais os males que este medicamento pode causar?”).
Malignidades
Stelara® é um imunossupressor27 seletivo. Agentes imunossupressores têm o potencial de aumentar o risco de malignidade. Alguns pacientes que receberam Stelara® em estudos clínicos desenvolveram malignidades cutâneas33 e não cutâneas33 (vide “Quais os males que este medicamento pode causar?”). Stelara® não foi estudado em pacientes com história de malignidade. Deve-se ter cautela quando se considerar o uso de Stelara® em pacientes com história de malignidade ou continuar o tratamento em pacientes que desenvolverem uma malignidade.
Todos os pacientes, em particular aqueles com idade superior a 60 anos, com histórico de tratamento prolongado com imunossupressores ou aqueles com um histórico de tratamento PUVA, devem ser monitorados para o aparecimento de câncer34 de pele17 que não-melanoma35.
Reações de hipersensibilidade
Na experiência de pós-comercialização, foram reportadas reações alérgicas graves, incluindo anafilaxia36 e angioedema37. Se ocorrer reação anafilática38 ou outra reação alérgica39 grave, deve ser instituída terapia adequada e a administração de Stelara® deve ser descontinuada.
Imunizações
Recomenda-se que as vacinas bacterianas ou virais de microrganismos vivos não sejam administradas concomitantemente com Stelara®.
Não existem dados disponíveis sobre a transmissão secundária de infecção29 por vacinas com microrganismos vivos em pacientes recebendo Stelara®. Aconselha-se precaução ao administrar algumas vacinas de microrganismos vivos para contatos domiciliares dos pacientes que recebem Stelara® devido ao risco potencial a partir do contato familiar e transmissão para o paciente.
Os pacientes que recebem Stelara® podem receber vacinas inativadas ou de microrganismos não-vivos.
O tratamento em longo prazo com Stelara® não suprime a resposta imune humoral40 para as vacinas contra tétano41 ou pneumocócica polissacarídica.
Imunossupressão42
Nos estudos em psoríase3, a segurança e a eficácia de Stelara® em combinação aos agentes imunossupressores ou fototerapia não foram avaliadas. Em estudos em artrite5 psoriásica, o uso concomitante de metotrexato não pareceu influenciar a segurança ou a eficácia de Stelara®. Nos
estudos em doença de Crohn6, a segurança ou eficácia de Stelara® não pareceram ser influenciadas com o uso concomitante de imunomoduladores [6-mercaptopurina (6-MP), azatioprina (AZA), metotrexato (MTX)] ou corticosteroides. Deve-se ter cautela ao se considerar o uso concomitante de agentes imunossupressores e Stelara® ou quando há transição a partir de outros agentes. Imunoterapia
Stelara® não foi avaliado em pacientes que foram submetidos à imunoterapia para alergia43. Stelara® pode afetar a imunoterapia para alergia43. Recomenda-se precaução em pacientes recebendo ou que tenham recebido imunoterapia para doenças alérgicas, especialmente para anafilaxia36.
Geral
A tampa da agulha da seringa1 preenchida contém borracha natural seca (um derivado do látex), a qual pode causar reações alérgicas em indivíduos sensíveis ao látex.
Pacientes pediátricos
Não foram conduzidos estudos específicos de Stelara® em pacientes pediátricos.
Pacientes idosos
Entre os 5884 pacientes expostos ao Stelara® havia 310 com idade igual ou superior a 65 anos (183 pacientes com psoríase3 e 69 pacientes com artrite5 psoriásica e 58 pacientes com doença de Crohn6). Não foram observadas diferenças importantes relacionadas à idade na depuração ou no volume de distribuição em estudos clínicos. Embora não tenham sido observadas diferenças na segurança ou eficácia entre pacientes mais jovens e idosos, o número de pacientes com 65 anos ou mais não é suficiente para determinar se eles respondem diferentemente dos pacientes mais jovens.
Insuficiência hepática44
Não foram conduzidos estudos específicos em pacientes com insuficiência hepática44.
Insuficiência renal45
Não foram conduzidos estudos específicos em pacientes com insuficiência renal45.
Fertilidade
O efeito de Stelara® na fertilidade humana não foi avaliado. Em um estudo de toxicidade46 sobre a fertilidade feminina conduzido em camundongos, nenhum efeito adverso sobre os parâmetros de fertilidade feminina foi identificado.
Efeitos sobre a capacidade de dirigir veículos e operar máquinas
Nenhum estudo quanto a efeitos sobre a capacidade de dirigir veículos e operar máquinas foi realizado.
Gravidez47
Não há evidências em estudos com animais de teratogenicidade, malformações48 congênitas49 ou atrasos no desenvolvimento com níveis de dose de até aproximadamente 45 vezes maiores do que a dose equivalente mais alta que se pretende administrar a pacientes com psoríase3. Entretanto, os estudos de reprodução50 e desenvolvimento animal não são sempre preditivos da resposta em humanos.
Como medida de precaução é preferível evitar a utilização de Stelara® durante a gravidez47. As mulheres em risco de engravidar deverão utilizar um método contraceptivo durante o tratamento e até 15 semanas após o tratamento.
Não é conhecido se Stelara® pode causar danos fetais quando administrado a mulheres grávidas ou se pode afetar a capacidade de reprodução50. Stelara® deve ser administrado a mulheres grávidas somente se o benefício for claramente superior ao risco.
Amamentação51
Stelara® foi excretado no leite de macacas lactantes52 que receberam Stelara®. Não se sabe se Stelara® é absorvido sistemicamente após a ingestão. Como muitos medicamentos e imunoglobulinas53 são excretados no leite humano e devido ao potencial de reações adversas de Stelara® em bebês54 em fase de amamentação51, deve-se decidir entre descontinuar a amamentação51 ou o medicamento.
Interações medicamentosas
Não foram conduzidos estudos de interações medicamentosas em humanos com Stelara®.
Os efeitos da IL-12 ou IL-23 na regulação das enzimas do CYP450 foram avaliados em um estudo in vitro utilizando hepatócitos humanos, o qual demonstrou que a IL-12 e/ou a IL-23 em níveis de 10 ng/mL não alteraram as atividades das enzimas do CYP450 humano (CYP1A2, 2B6, 2C9, 2C19, 2D6, ou 3A4). Estes resultados não sugerem haver necessidade de ajustes de dose em pacientes que estejam recebendo substratos de CYP450 concomitantemente.
Vacinas de microrganismos vivos não devem ser administradas concomitantemente a Stelara®. Atenção diabéticos: contém açúcar55.
Medicamentos imunossupressores podem ativar focos primários de tuberculose30. Os médicos que acompanham pacientes sob imunossupressão42 devem estar alertas quanto à possibilidade de surgimento de doença ativa, tomando, assim, todos os cuidados para o diagnóstico56 precoce e tratamento.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde57.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
As embalagens de Stelara® devem ser mantidas sob refrigeração (entre 2°C e 8°C), protegido da luz e não deve ser congelado. Não agitar.
Número de lote e datas de fabricação e validade: vide embalagem. Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
O produto deve ser mantido na embalagem secundária para proteger da luz.
Aspecto físico
Stelara® é fornecido como solução estéril em frasco-ampola de vidro ou em seringa1 preenchida, ambos para uso único. Stelara® não contém conservantes. O frasco-ampola é fechado com um batoque revestido. A solução é límpida a levemente opalescente, incolor a amarelo claro com pH de aproximadamente 6,0.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
COMO DEVO USAR ESTE MEDICAMENTO?
Dosagem
Psoríase3 em placa4 - Adultos
Para o tratamento da psoríase3 em placa4 Stelara® é administrado por injeção subcutânea58.A dose recomendada de Stelara® é 45 mg administrada nas Semanas 0 e 4 e, depois, a cada 12 semanas. A interrupção do tratamento deve ser considerada em pacientes que não apresentem qualquer resposta ao tratamento até as 28 semanas. Alternativamente, a dose de 90 mg pode ser usada em pacientes com peso corpóreo maior que 100 kg, nos mesmos intervalos de tempo.
Ajuste de dose
Para pacientes59 que respondem inadequadamente a 45 mg a cada 12 semanas, pode-se considerar a possibilidade de tratamento com 90 mg a cada 12 semanas. Para pacientes59 que responderam inadequadamente à posologia de 90 mg a cada 12 semanas, uma dose de 90 mg a cada 8 semanas pode ser considerada.
Retratamento
O retratamento com um esquema posológico nas Semanas 0 e 4 após interrupção da terapia mostrou ser seguro e eficaz.
Artrite5 psoriásica - Adultos
A dose recomendada de Stelara® é 45 mg, administrada nas Semanas 0 e 4 e, depois, a cada 12 semanas. Alternativamente, a dose de 90 mg pode ser usada em pacientes com peso corpóreo maior que 100 kg.
Doença de Crohn6
No regime de tratamento, a primeira dose de Stelara® é administrada por via intraveno. Para a posologia do regime de dosagem intravenosa, vide bula de Stelara® 130 mg solução injetável.
A primeira administração subcutânea60 de 90 mg de Stelara® deve ocorrer na Semana 8 após a dose intravenosa. Depois disso, recomenda-se a administração a cada 12 semanas.
Os pacientes que não apresentarem resposta adequada nas 8 semanas após a primeira dose subcutânea60, podem receber uma segunda dose subcutânea60.
Os pacientes que perderem a resposta na dosagem a cada 12 semanas podem se beneficiar de um aumento na frequência de dosagem a cada 8 semanas.
Os pacientes podem ser administrados posteriormente a cada 8 semanas ou a cada 12 semanas de acordo com o julgamento clínico.
Deve-se considerar a interrupção do tratamento em pacientes que não apresentarem evidência de benefício terapêutico na Semana 16 ou 16 semanas após a mudança para a dose de 8 semanas.
Instruções para uso, manipulação e descarte
Stelara® deve ser utilizado sob supervisão e orientação médica. Stelara® pode ser autoaplicado por você, se o seu médico considerar apropriado, após treinamento adequado na técnica de administração subcutânea60 e descarte. Durante o tratamento recomenda-se o acompanhamento médico, conforme necessário.
Os pacientes devem ser instruídos a injetar a quantidade prescrita de Stelara® de acordo com as instruções fornecidas no folheto informativo do paciente. A tampa da agulha na seringa1 preenchida contém borracha natural seca (um derivado de látex), que pode causar reações alérgicas em indivíduos sensíveis ao látex.
A) Instruções para o uso da seringa1 preenchida
Para reduzir o risco de perfurações acidentais com a agulha, cada seringa1 preenchida é equipada com um dispositivo de proteção da agulha que é ativado automaticamente para cobrir a agulha após a liberação completa do conteúdo da seringa1.
Não agite a seringa1 preenchida de Stelara® em nenhum momento. A agitação vigorosa e prolongada pode danificar o produto. Não use o produto, caso tenha sido agitado vigorosamente.
1. Preparação para o uso da seringa1 preenchida
Êmbolo61 – Corpo – Janela de visualização – Tampa da agulha
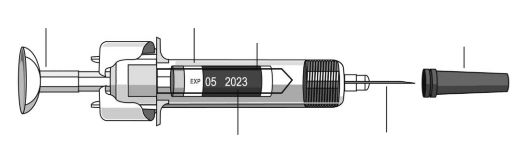
Retirar a seringa1 de Stelara® da geladeira
Verifique na embalagem se a dose está correta de acordo com a sua prescrição médica.
Verificação da data de validade de Stelara®
Abra a embalagem e retire a seringa1 preenchida. Verifique o prazo de validade na seringa1 preenchida e no cartucho. Não use o medicamento se o prazo de validade estiver vencido.
Preparação de materiais necessários para a aplicação
Prepare o material que será necessário para a aplicação. Incluindo compressa com álcool, bola de algodão ou gaze e recipiente para o descarte de seringas.
Verificação da solução do interior da seringa1
Mantenha a seringa1 preenchida com a agulha coberta apontando para cima. Certifique-se de que a seringa1 não está danificada. Também se certifique de que a solução ou o líquido em seu interior é límpido a ligeiramente opalescente e incolor a levemente amarelado. NÃO USE se o produto estiver congelado, com coloração diferente da original, turvo ou se contiver partículas grandes.
NÃO REMOVA a tampa da agulha da seringa1 preenchida.
NÃO PUXE o êmbolo61 da seringa1 para trás em nenhum momento.
2. Escolha e Preparação do Local de Aplicação
Escolha do local de aplicação*
Os locais recomendados para a aplicação da injeção62 são a parte superior da coxa63 e na barriga, mas cerca de 5 cm abaixo do umbigo64. Se possível, evite as áreas envolvidas com psoríase3. Se for aplicado por outra pessoa, a parte superior do braço também pode ser utilizada.
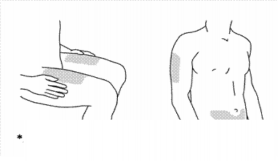
As áreas em cinza são os locais recomendados para a aplicação.
Preparação do local da injeção62
Lave bem as mãos65 com sabão e água morna. Passe uma compressa com álcool no local da injeção62.
NÃO TOQUE nesta área novamente antes de aplicar a injeção62.
3. Aplicação do medicamento
Remoção da tampa da agulha
Quando você estiver pronto (a) para injetar, segure o corpo da seringa1 preenchida com uma mão66 e com a outra retire a tampa da agulha. Jogue a tampa no lixo. Pode haver uma pequena bolha67 de ar na seringa1, mas não é necessário removê-la. Pode haver, também, uma gota68 de líquido na ponta da agulha, mas isto é normal. Não toque na agulha. Não deixe que a agulha toque em nada.
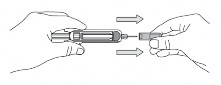
Nota: a tampa da agulha NÃO deve ser removida até você estar pronto para aplicar a dose. Não use a seringa1 se ela cair sem a tampa da agulha. Se você deixar a seringa1 cair sem a tampa da agulha, contate seu médico.
Aplicação da injeção62
Gentilmente, segure uma prega de pele17 entre o dedão e o indicador. Não aperte.
Introduza a agulha da seringa1 na prega de pele17. Mantendo a prega de pele17 entre os dedos, empurre o êmbolo61 com o polegar até o final, lentamente e de forma uniforme, para injetar o produto.
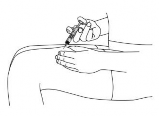
Quando o êmbolo61 atingir o final do corpo da seringa1 e todo o medicamento tiver sido injetado, solte a prega de pele17 e remova gentilmente a agulha. Após o término da injeção62, o dispositivo de proteção da agulha irá automaticamente se estender sobre a agulha e travar à medida que você soltar o êmbolo61.
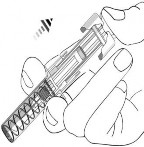
4. Após a aplicação da injeção62
Descarte da seringa1 vazia
Descarte imediatamente a seringa1 vazia em um recipiente apropriado. Para a sua segurança e a segurança de outras pessoas, agulhas e seringas NUNCA devem ser reutilizadas.
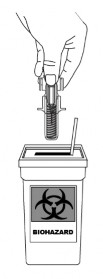
Use uma bola de algodão ou gaze
Pode haver uma pequena quantidade de sangue18 ou de líquido no local da injeção62, o que é normal. Você pode pressionar uma bola de algodão ou uma gaze sobre o local da injeção62 e manter pressionado por 10 segundos. Não esfregue o local da injeção62. Se necessário, pode-se colocar um curativo adesivo pequeno sobre o local da injeção62.
B) Instruções para o uso do frasco-ampola
Você deve injetar a quantidade total de Stelara® do frasco-ampola, de acordo com as orientações a seguir:
Não agite o frasco-ampola de Stelara® em nenhum momento. A agitação vigorosa e prolongada pode danificar o produto. Não use o produto, caso tenha sido agitado vigorosamente. Stelara® não deve ser misturado com outros líquidos para injeção62.
1. Verificação do frasco-ampola e preparação dos materiais necessários para aplicação
Retirar o frasco-ampola da geladeira
Verifique na embalagem se a dose está correta de acordo com a prescrição médica. Se a dose é de 90 mg, você poderá administrar 1 frasco-ampola de 90 mg ou 2 de 45 mg. Se você for aplicar 2 frascos- ampola de 45 mg para a dose de 90 mg, será necessário aplicar 2 injeções, sendo 1 injeção62 após a outra.
Verificação da data de validade de Stelara®
Abra a embalagem e remova o frasco-ampola. Verifique o prazo de validade no frasco-ampola e no cartucho. Não use o medicamento se o prazo de validade estiver vencido.
Verificação da solução do interior do frasco
Verifique se o frasco-ampola não está danificado e se a solução ou o líquido em seu interior é límpido a ligeiramente opalescente e incolor a levemente amarelado. NÃO USE se o produto estiver congelado, com coloração diferente da original, turvo ou se contiver partículas grandes.
Preparação de materiais necessários para a aplicação
Prepare o material que será necessário para a aplicação incluindo compressa com álcool, bola de algodão ou gaze e recipiente para o descarte de seringas.
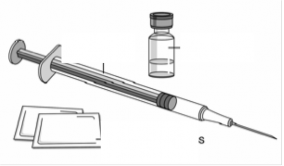
2. Escolha e preparação do local de aplicação
Escolha do local de aplicação*
Os locais recomendados para a aplicação da injeção62 são a parte superior da coxa63 e na barriga, mas cerca de 5 cm abaixo do umbigo64. Se possível, evite as áreas envolvidas com psoríase3. Se for aplicado por outra pessoa, a parte superior do braço também pode ser utilizada.
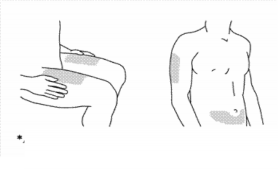
As áreas em cinza são os locais recomendados para a aplicação
Preparação do local de aplicação
Lave bem as mãos65 com sabão e água morna. Passe uma compressa com álcool no local da injeção62.
NÃO TOQUE nesta área novamente antes de aplicar a injeção62.
3. Preparação da dose
Remova a tampa da parte superior do frasco-ampola, mas não remova a tampa de borracha. Limpe a tampa de borracha com uma compressa com álcool.
Remova a tampa da agulha da seringa1. Não toque na agulha. Não deixe a agulha tocar em nada.
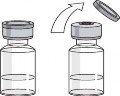
Coloque o frasco-ampola sobre uma superfície plana e introduza a agulha da seringa1 na tampa de borracha. Vire o frasco-ampola e a seringa1 de cabeça69 para baixo, puxe o êmbolo61 da seringa1 para enchê-la com a quantidade de líquido prescrita (0,5 mL ou 1,0 mL). É importante que a agulha esteja sempre dentro do líquido para evitar a formação de bolhas no interior da seringa1.
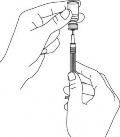
Remova a agulha do frasco-ampola. Mantenha a seringa1 e a agulha apontadas para cima para checar se há bolhas de ar no seu interior. Se houver bolhas de ar, bata gentilmente na lateral da seringa1 até que as bolhas de ar se desloquem para a parte superior da seringa1 e pressione o êmbolo61 até que todo o ar (mas não o líquido) seja removido. Não deite a seringa1 e não deixe a agulha tocar em nada.
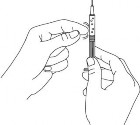
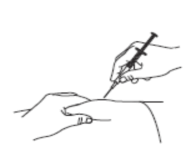
4. Aplicação do medicamento
Gentilmente, segure uma prega de pele17 entre o polegar e o indicador. Não aperte.
Introduza a agulha da seringa1 na prega de pele17. Mantendo a prega de pele17 entre os dedos, empurre o êmbolo61 com o polegar até o final, lentamente e de forma uniforme, para injetar o produto. Em seguida, retire a agulha e solte a pele17.
Descarte da seringa1 vazia e do frasco-ampola
Descarte imediatamente a seringa1 vazia em um recipiente apropriado. Os frascos-ampola podem ser descartados em lixeiras normais Para a sua segurança e a de outras pessoas, frascos-ampola, agulhas e seringas NUNCA devem ser reutilizados.
Use uma bola de algodão ou gaze
Pode haver uma pequena quantidade de sangue18 ou líquido no local da injeção62, o que é normal. Você pode pressionar uma bola de algodão ou gaze sobre o local da injeção62 e manter pressionado por 10 segundos. Não esfregue o local da injeção62. Se necessário, pode-se colocar um curativo adesivo pequeno sobre o local da injeção62.
Para a dose de 90 mg utilizando dois frascos de 45 mg será necessário aplicar uma segunda injeção62 logo após a primeira injeção62. Use uma nova agulha e seringa1. Escolha um local diferente para a aplicação da segunda injeção62.
Após a administração de Stelara®, a seringa1 deve ser descartada de acordo com as práticas médicas para seringas usadas.
Incompatibilidades: como não há estudos de compatibilidade, este medicamento não deve ser misturado a outros medicamentos.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento de seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Se você se esquecer de uma dose, contate seu médico. Não se recomenda o uso de dose duplicada para compensar uma dose esquecida.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
As reações adversas são apresentadas nesta seção. Reações adversas são eventos adversos que foram considerados razoavelmente associados ao uso de ustequinumabe, com base na avaliação abrangente das informações de eventos adversos disponíveis. Em casos individuais, uma relação causal com ustequinumabe não pode ser estabelecida com confiança. Portanto, pelo fato de que os estudos clínicos são conduzidos em condições amplamente variadas, as taxas de reações adversas observadas nos estudos clínicos de um medicamento não podem ser comparadas com as taxas nos estudos clínicos de outros medicamentos e podem não refletir as taxas observadas na prática clínica.
Experiência dos Estudos Clínicos em Pacientes com Psoríase3 e/ou Artrite5 Psoriásica e Dença de Crohn
Os dados de segurança descritos a seguir refletem a exposição ao Stelara®, em 12 estudos de fase 2 e 3 controlados em 5884 pacientes (4135 pacientes com psoríase3 e/ou artrite5 psoriásica e 1749 pacientes com doença de Crohn6), com duração de exposição ao Stelara® apresentada na tabela a seguir.
|
Tabela 4: Exposição de longo prazo ao Stelara® em estudos clínicos fase 2 e fase 3 |
|
|
Exposição |
Número de pacientes |
|
6 meses |
4105a |
|
1 ano |
2846a |
|
≥ 4 anos |
1482b |
|
≥ 5 anos |
838b |
|
a Número total de pacientes em estudos de psoríase3, artrite5 psoriásica e doença de Crohn6. |
|
As reações adversas mais comuns (> 5%) em períodos controlados dos estudos clínicos de Stelara® em psoríase3, artrite5 psoriásica e doença de Crohn6 com Stelara® foram nasofaringite e cefaleia70. A maioria foi considerada leve e não necessitou descontinuação do medicamento. O perfil de segurança global de Stelara® foi semelhante em pacientes com psoríase3 e doença de Crohn6. Nos pacientes com doença de Crohn6, não foram identificadas novas preocupações de segurança em pacientes com até 2 anos de tratamento.
A seguir é apresentado um resumo das reações adversas dos estudos clínicos de psoríase3,artrite5 psoriásica e de doença de Crohn6. A frequência destas reações adversas foi baseada naquelas que ocorreram durante os períodos iniciais controlados dos estudos clínicos. As reações adversas são classificadas por frequência, conforme apresentado a seguir:
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento):
- Infecções26 e infestações: infecção29 do trato respiratório superior, nasofaringite. Distúrbios do sistema nervoso71: tontura72, cefaleia70.
- Distúrbios respiratórios, torácicos e do mediastino73: dor na orofaringe74. Distúrbios gastrintestinais: diarreia75, náusea76, vômito77.
- Distúrbios do tecido78 cutâneo79 e subcutâneo2: prurido80.
- Distúrbios musculoesqueléticos e do tecido conjuntivo81: lombalgia82 (dor na região lombar83),, mialgia84 (dor muscular),, artralgia85 (dor nas articulações86)..
- Distúrbios gerais e condições no local da administração: fadiga87, eritema88 no local da aplicação (vermelhidão na pele17), dor no local da aplicação.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento):
- Infecções26 e infestações: celulite89, infecções26 dentárias, herpes zoster90, infecção29 viral do trato respiratório superior, infecção29 micótica vulvovaginal.
- Distúrbios psiquiátricos: depressão.
- Distúrbios respiratórios, torácicos e do mediastino73: congestão nasal.
- Distúrbios do tecido78 cutâneo79 e subcutâneo2: acne91.
- Distúrbios gerais e condições no local da administração: reações no local da aplicação (incluindo hemorragia92, hematoma93, infiltração, inchaço94 e prurido80), astenia95 (fraqueza).
Infecções26
Em estudos controlados por placebo96 em pacientes com psoríase3 , artrite5 psoriásica e doença de Crohn6, as taxas de infecção29 ou infecção29 grave foram semelhantes entre os pacientes tratados com Stelara® e os tratados com placebo96. No período controlado por placebo96 dos estudos clínicos de pacientes com psoríase3, pacientes com artrite5 psoriásica e pacientes com doença de Crohn6, a taxa de infecção29 foi de 1,38 por paciente/ano de acompanhamento dos pacientes tratados com Stelara® e 1,35 por paciente/ano de acompanhamento dos pacientes tratados com placebo96. Infecções26 graves ocorreram em 0,03 por paciente/ano de acompanhamento nos pacientes tratados com Stelara® (27 infecções26 graves em 829 pacientes/ano de acompanhamento) e 0,03 por paciente/ano de acompanhamento em pacientes tratados com placebo96 (11 infecções26 graves em 385 pacientes/ano de acompanhamento). Nos períodos controlados e não controlados dos estudos clínicos de psoríase3, artrite5 psoriásica e doença de Crohn6, representando 10953pacientes/ano de exposição em 5884pacientes, a mediana de acompanhamento foi de 0,99 anos; 3,2 anos para os estudos de psoríase3,1,0 ano para os estudos de artrite5 psoriásica e 0,6 anos para os estudos de doença de Crohn6. A taxa de infecção29 foi de 0,91 por paciente/ano de acompanhamento nos pacientes tratados com Stelara®. A taxa de infecções26 graves foi de 0,02 por paciente/ano de acompanhamento em pacientes tratados com o Stelara® (178 infecções26 graves em 10953 pacientes/ano de acompanhamento) e incluiu abcesso anal, diverticulite97, celulite89, pneumonia98, gastroenterite99 e infecção29 viral.
Em estudos clínicos, os pacientes com tuberculose30 latente que foram tratados concomitantemente com a isoniazida não desenvolveram tuberculose30.
Malignidade
No período dos estudos clínicos de psoríase3, artrite5 psoriásica e de doença de Crohn6 controlados por placebo96, a incidência100 de malignidades, exceto câncer34 de pele17 não-melanoma35, foi de 0,12 por 100 pacientes/ano de acompanhamento para os pacientes tratados com Stelara® (1 paciente em 829 pacientes/ano de acompanhamento) em comparação a 0,26 por 100 pacientes/ano de acompanhamento para os pacientes tratados com placebo96 (1 paciente em 385 pacientes/ano de acompanhamento).
A incidência100 de câncer34 de pele17 não-melanoma35 foi de 0,48 por 100 pacientes/ano de acompanhamento para os pacientes tratados com Stelara® (4 pacientes em 829 pacientes/ano de acompanhamento) em comparação a 0,52 por 100 pacientes/ano de acompanhamento para os pacientes tratados com o placebo96 (2 pacientes em 385 pacientes/ano de acompanhamento).
Nos períodos controlados e não controlados dos estudos clínicos de psoríase3, artrite5 psoriásica e de doença de Crohn6 representando 10935 pacientes/ano de exposição em 5884 pacientes, a mediana de acompanhamento foi de 1,0 anos; 3,2 anos para os estudos de psoríase3, 1,0 ano para os estudos de artrite5 psoriásica e 0,6 ano para doença de Crohn6. Malignidades, excluindo cânceres de pele17 não- melanoma35, foram relatadas em 58 pacientes de 10935pacientes/ano de acompanhamento (incidência100 de 0,53 por 100 pacientes/ano de acompanhamento para pacientes59 tratados com Stelara®). Esta incidência100 de malignidades reportada em pacientes tratados com Stelara® foi comparável à incidência100 esperada na população geral [taxa de incidência100 padronizada = 0,87 (intervalo de confiança de 95%: 0,66 - 1,14), ajustado para idade, sexo e raça]. As malignidades mais frequentemente observadas, além de câncer34 de pele17 não-melanoma35, foram de próstata101, melanoma35, colorretal e de mama102. A incidência100 de câncer34 de pele17 não-melanoma35 foi de 0,49por 100 pacientes/ano de acompanhamento para pacientes59 tratados com Stelara® (53 pacientes de 10919 pacientes/ano de acompanhamento). A proporção de pacientes com câncer34 de pele17 de células10 basais versus escamosas (4:1) é comparável à proporção esperada na população geral (vide “Advertências e Precauções”).
Reações de hipersensibilidade e de infusão
Administração subcutânea60
Durante os períodos controlados dos estudos clínicos de psoríase3 e artrite5 psoriásica de Stelara®, erupção103 cutânea104 e urticária105 foram observadas cada uma em < 1% dos pacientes.
Administração intravenosa
Nos estudos de indução da doença de Crohn6, não foram relatados eventos de anafilaxia36 ou outras reações graves à infusão. Nestes estudos, 2,4% de 466 pacientes tratados com placebo96 e 2,6% de 470 pacientes tratados com a dose recomendada de Stelara® relataram eventos adversos que ocorreram durante ou uma hora após a infusão.
Imunogenicidade
Nos estudos clínicos de psoríase3 e artrite5 psoriásica, até 8% dos pacientes tratados com Stelara® desenvolveram anticorpos106 contra o ustequinumabe. Nos estudos clínicos da doença de Crohn6, menos de 3% dos pacientes tratados com Stelara® desenvolveram anticorpos106 contra o ustequinumabe. Nenhuma correlação reações no local da aplicação foi observada. Os pacientes positivos para anticorpos106 contra o ustequinumabe tenderam a ter eficácia menor, entretanto, a positividade para anticorpos106 não impediu a resposta clínica.
Experiência pós-comercialização
As reações adversas descritas a seguir estão agrupadas por frequência.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento):
- Distúrbios do tecido78 cutâneo79 e subcutâneo2: psoríase3 pustular.
- Distúrbios do sistema imune107: reações de hipersensibilidade (incluindo erupção103 cutânea104, urticária105). Infecções26 e infestações: infecção29 do trato respiratório inferior.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento):
- Distúrbios do sistema imune107: reações alérgicas graves (incluindo anafilaxia36 e angioedema37).
- Distúrbios respiratórios, torácicos e do mediastino73: alveolite alérgica, pneumonia98 eosinofílica.
- Distúrbios do tecido78 cutâneo79 e subcutâneo2: psoríase3 eritrodérmica.
OBS: A frequência de reação adversa pós-comercialização é derivada da porção controlada por placebo96 de 11 estudos clínicos se as mesmas fossem observadas nesses estudos. Em contrapartida, estimou-se que seriam mais baixas do que certa frequência considerando a exposição nos 11 estudos clínicos nos quais a reação adversa não foi observada.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
Atenção: este produto é um medicamento que possui nova indicação terapêutica108 no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidas. Nesse caso, informe seu médico.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Doses únicas de até 6 mg/kg por via intravenosa foram administradas em estudos clínicos sem toxicidade46 dose-limitante. No caso de superdosagem, recomenda-se que o paciente seja monitorado para quaisquer sinais31 ou sintomas32 de efeitos ou reações adversas e que tratamento sintomático109 adequado seja instituído imediatamente.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.1236.3394
Farm. Resp.: Marcos R. Pereira - CRF-SP no 12.304
Registrado por:
JANSSEN-CILAG FARMACÊUTICA LTDA.
Avenida Presidente Juscelino Kubitschek, 2041, São Paulo – SP
CNPJ 51.780.468/0001-87
Fabricado por:
Cilag AG
Schaffhausen - Suíça
Importado por:
Janssen-Cilag Farmacêutica Ltda.
Rodovia Presidente Dutra, km 154
São José dos Campos – SP
CNPJ 51.780.468/0002-68
SAC 0800 701 1851