

Strensiq
ALEXION FARMACEUTICA BRASIL IMPORTACAO E DISTRIBUICAO DE PRODUTOS E SERVICOS DE ADMINISTRACAO
IDENTIFICAÇÃO DO MEDICAMENTO
Strensiq
alfa-asfotase
Injetável 18 mg, 28 mg, 40 mg ou 80 mg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Embalagens com doze frascos-ampola de solução injetável de uso único
VIA SUBCUTÂNEA
USO ADULTO E PEDIÁTRICO
COMPOSIÇÃO:
Strensiq 40 mg/ml solução injetável
Cada 1 ml de Strensiq contém:
| Alfa-asfotase* | 40 mg |
Excipientes: cloreto de sódio, fosfato de sódio dibásico hepta-hidratado, fosfato de sódio monobásico mono-hidratado, água para injetáveis.
- Cada frasco para injetáveis de 0,45 ml contém 18 mg de alfa-asfotase.
- Cada frasco para injetáveis de 0,7 ml contém 28 mg de alfa-asfotase.
- Cada frasco para injetáveis de 1,0 ml contém 40 mg de alfa-asfotase.
Strensiq 40 mg/ml solução injetável
Cada 1 ml de Strensiq contém:
| Alfa-asfotase | 100 mg |
Excipientes: cloreto de sódio, fosfato de sódio dibásico hepta-hidratado, fosfato de sódio monobásico mono-hidratado, água para injetáveis.
- Cada frasco para injetáveis de 0,8 ml contém 80 mg de alfa-asfotase.
Este medicamento contém menos de 1 mmol de sódio (23 mg) por frasco para injetáveis.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Strensiq é indicado para o tratamento de pacientes com hipofosfatasia (HPP) de início perinatal/infantil e juvenil.
COMO ESTE MEDICAMENTO FUNCIONA?
Pacientes com hipofosfatasia têm níveis baixos de uma enzima chamada fosfatase alcalina que é importante para várias funções do organismo, incluindo o endurecimento adequado dos ossos e dos dentes. Os pacientes têm problemas com o crescimento e resistência dos ossos, que podem causar a fratura dos ossos, dor nos ossos e dificuldade em andar, assim como dificuldades com a respiração e risco de crises convulsivas.
A substância ativa em Strensiq pode substituir a enzima que falta (fosfatase alcalina) na hipofosfatasia. É utilizada para o tratamento de substituição da enzima de longa duração para controlar os sintomas.
Strensiq demonstrou benefícios na mineralização do esqueleto e crescimento dos pacientes.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Não utilize este medicamento em caso já tenha tido reações alérgicas aos componentes da fórmula.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Que precauções devo adotar?
Antes de usar Strensiq, informe o seu médico sobre todas as suas condições médicas:
- se for alérgico à alfa-asfotase ou a qualquer um dos ingredientes em Strensiq.
- se estiver grávida ou planejando engravidar. Não se sabe se Strensiq pode prejudicar seu bebê.
- se estiver amamentando ou se planeja amamentar. Não se sabe se Strensiq passa para o leite materno. Converse com seu médico sobre a melhor forma de alimentar o seu bebê se estiver utilizando Strensiq.
Informe o seu médico sobre todos os medicamentos que toma, incluindo prescritos e sem prescrição, vitaminas e fitoterápicos.
Strensiq pode causar reações alérgicas em algumas pessoas. Os sintomas destas reações incluem vômitos, tontura, dificuldade em respirar, sensação de asfixia, batimentos rápidos do coração, descida rápida da tensão arterial, urticária ou erupção na pele. Se tiver qualquer um destes sintomas, informe imediatamente o seu médico. Pode ser necessário que lhe sejam administrados outros medicamentos para evitar uma reação alérgica (anti-histamínicos ou corticosteroides). Outras reações de hipersensibilidade relatadas em pacientes tratados com Strensiq foram: vômito, náusea, febre, dor de cabeça, rubor facial, irritabilidade, calafrios, eritema cutâneo, erupção cutânea, prurido e hipoestesia oral.
O desenvolvimento de proteínas sanguíneas contra Strensiq, também chamado de anticorpos antidrogas, pode ocorrer durante o tratamento. Fale com o seu médico se tiver uma eficácia reduzida com Strensiq.
Em estudos foram notificados alguns efeitos secundários relacionados com os olhos, tanto em doentes que utilizavam Strensiq como em doentes que não o utilizavam, provavelmente associados à hipofosfatasia. Fale com o seu médico no caso de perturbações da visão. Pacientes com HPP estão em risco aumentado de desenvolver calcificações ectópicas. Eventos de calcificação ectópica, incluindo calcificação oftalmológica (conjuntival e da córnea) e nefrocalcinose, foram relatados na experiência do ensaio clínico com Strensiq. Não havia informação suficiente para determinar se os eventos relatados foram ou não compatíveis com a doença ou devido ao Strensiq. Não foram relatadas alterações visuais ou alterações na função renal resultantes da ocorrência de calcificações ectópicas. Exames oftalmológicos e ultrassonografias renais são recomendados no período basal e periodicamente durante o tratamento com Strensiq para monitorar sinais e sintomas de calcificações ectópicas oftalmológicas e renais, e para alterações na visão ou função renal.
Foi notificada a fusão precoce dos ossos da cabeça em crianças com menos de 5 anos de idade em ensaios clínicos de crianças com hipofosfatasia, com e sem a utilização de Strensiq. Informe o seu médico se detetar qualquer alteração na forma da cabeça do seu bebê.
Se está a ser tratado com Strensiq, pode ter uma reação no local da injeção (dor, nódulo, erupção na pele, alteração da cor da pele) durante a injeção do medicamento ou nas horas que se seguem à injeção. Se tiver qualquer reação severa no local de injeção, informe imediatamente o seu médico.
Lipohipertrofia (aumento ou espessamento do tecido) e atrofia localizada (depressão na pele) foram relatados em locais de injeção depois de vários meses em pacientes tratados com Strensiq em estudos clínico. Siga corretamente as instruções de administração e alterne os locais de injeção.
Foi notificado, em estudos, um aumento da concentração do hormônio da paratiroide ou paratormônio e níveis baixos de cálcio. Como consequência, o seu médico poderá pedir-lhe para tomar suplementos de cálcio e de vitamina D oral, se necessário.
Pode ocorrer um ganho de peso durante o seu tratamento com Strensiq. O seu médico dar- lhe-á conselhos dietéticos, se necessário.
Gravidez e Lactação
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Gravidez: não existem dados suficientes sobre a utilização de alfa-asfotase em mulheres grávidas para determinar se a exposição à alfa-asfotase durante a gravidez representa algum risco para a mãe ou o feto. Após administração subcutânea repetida em ratas gravidas na dose terapeutica de ( 0,5 mg / kg), os níveis de asfotase alfa foram quantificáveis em fetos em todas as doses testadas, sugerindo o transporte de asfotase alfa pela placenta. Estudos em animais são insuficiente em relação à toxicidade reprodutiva. A asfotase alfa não é recomendado durante a gravidez e em mulheres com potencial para engravidar que não usem método de contracepção.
Se está grávida ou amamentando, se pensa estar grávida ou planeja engravidar, consulte o seu médico antes de utilizar este medicamento.
Lactação: existem dados insuficientes sobre a excreção de alfa-asfotase no leite humano, os efeitos no lactente amamentado, ou os efeitos sobre a produção de leite. Os benefícios do desenvolvimento e de saúde do aleitamento materno devem ser considerados juntamente com a necessidade clínica da mãe para Strensiq e quaisquer potenciais efeitos adversos no lactente amamentado devido à alfa-asfotase ou à condição materna subjacente.
Fertilidade: estudos pré-clínicos de fertilidade foram realizados e não mostraram evidências de efeito sobre a fertilidade e o desenvolvimento embrião-fetal.
Populações especiais
Uso Pediátrico: a segurança e a eficácia de Strensiq foram estabelecidas em pacientes pediátricos. O uso de Strensiq é baseado em 4 estudos clínicos prospectivos, abertos realizados em 112 pacientes adultos e pediátricos com HPP de início perinatal/infantil ou início juvenil. A maioria dos pacientes eram pacientes pediátricos de 1 dia a 16 anos de idade (99/112 [88%]).
Uso em Pacientes Idosos: nenhum paciente com HPP de início perinatal/infantil ou de início juvenil com 65 anos foram incluídos em estudos clínicos de Strensiq. Portanto, não há informações disponíveis para determinar se pacientes com idades entre 65 anos ou mais respondem diferentemente de pacientes mais jovens.
Insuficiência renal e hepática: a segurança e eficácia de Strensiq em pacientes com insuficiência renal ou hepática não foram avaliadas e nenhum regime posológico específico pode ser recomendado para esses pacientes.
Interação com outros medicamentos
Informe o seu médico sobre os medicamentos que esteja usando ou que utilizou recentemente.
A fosfatase alcalina é utilizada como o reagente de detecção em muitos ensaios laboratoriais de rotina.
Para evitar resultados errôneos de teste para pacientes tratados com Strensiq, seu médico irá informar à equipe do laboratório que você está sendo tratado com Strensiq e discutirá o a melhor forma para realizar o teste.
Efeitos na habilidade de dirigir e operar máquinas
Strensiq não tem ou tem influência desprezível sobre a capacidade de conduzir e utilizar máquinas.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Mantenha Strensiq em sua embalagem original, sob refrigeração (2°C – 8°C) e protegido da luz. Não congelar. Não agitar.
Uma vez retirado da refrigeração, Strensiq deve ser administrado dentro de 3 horas. A estabilidade física e química em uso foi demonstrada até 3 horas em temperatura ambiente (até 30°C).
Strensiq está acondicionado em frascos de utilização única, portanto, deve-se descartar qualquer quantidade residual de produto não utilizado.
Não utilize este medicamento após o prazo de validade impresso no rótulo e na embalagem exterior.
Número de lote, data de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Strensiq é fornecido como uma solução aquosa estéril, não pirogênica, sem conservantes, transparente, ligeiramente opalescente ou opalescente, incolor a ligeiramente amarela; algumas pequenas partículas translúcidas ou brancas podem estar presentes.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
- Veja as "Instruções de Uso" para obter instruções detalhadas sobre a maneira correta de usar Strensiq.
- Esteja atento à concentração descrita no rótulo de Strensiq e na dosagem prescrita pelo seu médico. Use Strensiq exatamente como o seu médico lhe indicou.
- Seu médico irá orientá-lo sobre a quantidade de Strensiq que você deve usar e sobre quando utilizar.
- O seu médico pode alterar a dose, se necessário.
- Alterne o local de administração a cada injeção. Não use o mesmo local para cada injeção.
6.1 Dosagem para HPP de Início Perinatal/Infantil
O regime de dose recomendado de Strensiq para o tratamento de HPP de início perinatal/infantil é de 6 mg/kg por semana administrados por via subcutânea das seguintes maneiras:
- 2 mg/kg, três vezes por semana,
ou - 1 mg/kg, seis vezes por semana. Reações no local da injeção podem limitar a tolerabilidade do regime de seis vezes por semana.
A dose de Strensiq pode ser aumentada para que se atinja a resposta clínica esperada, conforme critério médico (a eficácia pode ser avaliada pela melhora no status respiratório, crescimento ou achados radiográficos) até 9 mg/kg por semana administrados por via subcutânea como 3 mg/kg, três vezes por semana.
6.2 Dosagem para HPP de Início Juvenil
O regime de dose recomendado de Strensiq para o tratamento de HPP de início juvenil é de 6 mg/kg por semana, administrados por via subcutânea das seguintes maneiras:
- 2 mg/kg, três vezes por semana,
ou - 1 mg/kg, seis vezes por semana. Reações no local da injeção podem limitar a tolerabilidade do regime de seis vezes por semana.
6.3 Tabelas de Preparação e Dosagem Baseada no Peso
Cuidado: Não utilizar o frasco de 80 mg/0,8 mL de Strensiq em pacientes pediátricos com peso inferior a 40 kg, porque a exposição sistêmica da alfa-asfotase alcançada com o frasco de 80 mg/0,8 mL (concentração maior) é menor que a obtida com os frascos de outras concentrações (concentração menor). Uma exposição menor pode não ser adequada para este subgrupo de pacientes.
1. Determinar o volume semanal total necessário para a dose prescrita com base no peso do paciente e a dosagem recomendada. Seguir estes passos para determinar a dose do paciente.
Dose total semanal (mg) = peso do paciente (kg) x dose prescrita (mg/kg/semana)
Volume de injeção total (mL) por semana = Dose total (mg) dividida pela concentração (40 mg/mL ou 100 mg/mL).
Arredondar o volume total da injeção para o centésimo mais próximo de um mL
Número total de frascos por semana = Volume total de injeção dividido pelo volume do frasco (mL)
2. Determinar número de dias de injeções por semana (três ou seis por semana).
3. Determinar a dose por injeção diária. Os pesos dos pacientes devem ser arredondados para o quilograma mais próximo para determinar a dose. Usar as seguintes tabelas de orientação para os pacientes que administram 2 mg/kg, três vezes por semana (Tabela 1), 1 mg/kg, seis vezes por semana (Tabela 2) e para os aumentos da dose para 3 mg/kg três vezes por semana, recomendado apenas para pacientes com HPP de início perinatal/infantil (Tabela 3).
4. Ao se preparar um volume de injeção superior a 1 mL, dividir o volume igualmente entre duas seringas, e administrar duas injeções. Ao administrar as duas injeções, utilizar dois locais de injeção separados.
Tabela 1: Dosagem Baseada no Peso para Administração de 2 mg/kg Três Vezes por Semana
|
Peso Corporal (kg)* |
Dose para Injetar |
Volume para Injetar |
Configuração do Frasco |
|
3 |
6 mg |
0,15 mL |
18 mg/0,45 mL |
|
4 |
8 mg |
0,20 mL |
18 mg/0,45 mL |
|
5 |
10 mg |
0,25 mL |
18 mg/0,45 mL |
|
6 |
12 mg |
0,30 mL |
18 mg/0,45 mL |
|
7 |
14 mg |
0,35 mL |
18 mg/0,45 mL |
|
8 |
16 mg |
0,40 mL |
18 mg/0,45 mL |
|
9 |
18 mg |
0,45 mL |
18 mg/0,45 mL |
|
10 |
20 mg |
0,50 mL |
28 mg/0,7 mL |
|
15 |
30 mg |
0,75 mL |
40 mg/1.0 mL |
|
20 |
40 mg |
1.00 mL |
40 mg/1.0 mL |
|
25 |
50 mg |
1,25 mL |
Dois frascos de 28 mg/0,7 mL |
|
30 |
60 mg |
1,50 mL |
Dois frascos de 40 mg/1.0 mL |
|
35 |
70 mg |
1,75 mL |
Dois frascos de 40 mg/1.0 mL |
|
40 |
80 mg |
0,80 mL |
80 mg/0,8 mL |
|
50 |
100 mg |
1.00 mL |
Dois frascos de 80 mg/0,8 mL |
|
60 |
120 mg |
1,20 mL** |
Dois frascos de 80 mg/0,8 mL |
|
70 |
140 mg |
1,40 mL** |
Dois frascos de 80 mg/0,8 mL |
|
80 |
160 mg |
1,60 mL** |
Dois frascos de 80 mg/0,8 mL |
*Não utilizar o frasco de 80 mg/0,8 mL de Strensiq em pacientes pediátricos com peso inferior a 40 kg.
** Ao se preparar um volume de injeção superior a 1 mL, dividir o volume igualmente entre duas seringas e administrar duas injeções. Ao administrar as duas injeções, utilizar dois locais de injeção separados.
Tabela 2: Dosagem Baseada no Peso para Administração de 1 mg/kg Seis Vezes por Semana
|
Peso Corporal (kg)* |
Dose para Injetar |
Volume para Injetar |
Configuração do Frasco |
|
3 |
3 mg |
0,08 mL |
18 mg/0,45 mL |
|
4 |
4 mg |
0,10 mL |
18 mg/0,45 mL |
|
5 |
5 mg |
0,13 mL |
18 mg/0,45 mL |
|
6 |
6 mg |
0,15 mL |
18 mg/0,45 mL |
|
7 |
7 mg |
0,18 mL |
18 mg/0,45 mL |
|
8 |
8 mg |
0,2 mL |
18 mg/0,45 mL |
|
9 |
9 mg |
0,23 mL |
18 mg/0,45 mL |
|
10 |
10 mg |
0,25 mL |
18 mg/0,45 mL |
|
15 |
15 mg |
0,38 mL |
18 mg/0,45 mL |
|
20 |
20 mg |
0,50 mL |
28 mg/0,7 mL |
|
25 |
25 mg |
0,63 mL |
28 mg/0,7 mL |
|
30 |
30 mg |
0,75 mL |
40 mg/1 mL |
|
35 |
35 mg |
0,88 mL |
40 mg/1 mL |
|
40 |
40 mg |
1.00 mL |
40 mg/1 mL |
|
50 |
50 mg |
0,50 mL |
80 mg/0,8 mL |
|
60 |
60 mg |
0,60 mL |
80 mg/0,8 mL |
|
70 |
70 mg |
0,70 mL |
80 mg/0,8 mL |
|
80 |
80 mg |
0,80 mL |
80 mg/0,8 mL |
|
90 |
90 mg |
0,90 mL |
Dois frascos de 80 mg/0,8 mL |
|
100 |
100 mg |
1.00 mL |
Dois frascos de 80 mg/0,8 mL |
Não utilizar o frasco de 80 mg/0,8 mL de Strensiq em pacientes pediátricos com peso inferior a 40 kg.
Tabela 3: Dosagem Baseada no Peso para Administração de 3 mg/kg Três Vezes por Semana - Apenas para HPP de Início Perinatal/Infantil*
|
Peso Corporal (kg)** |
Dose para Injetar |
Volume para Injetar |
Configuração do Frasco |
|
3 |
9 mg |
0,23 mL |
18 mg/0,45 mL |
|
4 |
12 mg |
0,30 mL |
18 mg/0,45 mL |
|
5 |
15 mg |
0,38 mL |
18 mg/0,45 mL |
|
6 |
18 mg |
0,45 mL |
18 mg/0,45 mL |
|
7 |
21 mg |
0,53 mL |
28 mg/0,7 mL |
|
8 |
24 mg |
0,6 mL |
28 mg/0,7 mL |
|
9 |
27 mg |
0,68 mL |
28 mg/0,7 mL |
|
10 |
30 mg |
0,75 mL |
40 mg/mL |
|
15 |
45 mg |
1,13 mL*** |
Dois frascos de 28 mg/0,7 mL |
|
20 |
60 mg |
1,5 mL*** |
Dois frascos de 40 mg/mL |
|
25 |
75 mg |
1,88 mL*** |
Dois frascos de 40 mg/mL |
Um regime de 3 mg/kg três vezes por semana é recomendado apenas para pacientes com HPP de início perinatal/juvenil.
** Não utilizar o frasco de 80 mg/0,8 mL de Strensiq em pacientes pediátricos com peso inferior a 40 kg.
*** Ao se preparar um volume de injeção superior a 1 mL, dividir o volume igualmente entre duas seringas e administrar duas injeções. Ao administrar as duas injeções, utilizar dois locais de injeção separados.
5. Examinar a solução no(s) frasco(s) para detecção de partículas e descoloração. Strensiq é fornecido como uma solução aquosa límpida, ligeiramente opalescente ou opalescente, incolor a ligeiramente amarela; algumas pequenas partículas translúcidas ou brancas podem estar presentes. Descartar quaisquer frascos não compatíveis com esta aparência.
6. Montar os suprimentos de injeção. Administrar Strensiq usando seringas de 1 mL estéreis descartáveis e agulhas de injeção de ½ polegada, calibres entre 25 a 29 são recomendados. Recomenda-se o uso de duas agulhas de calibre diferente, uma agulha de diâmetro maior (por exemplo, calibre 25) para retirada do medicamento e uma agulha de diâmetro menor (por exemplo, calibre 29) para a injeção. Para doses superiores a 1 ml, o volume de injeção deve ser dividido igualmente entre duas seringas de 1 mL. Sempre usar uma nova seringa e agulha para cada injeção.
7. Remover a tampa do frasco, preparar de forma asséptica o frasco e inserir a seringa no frasco para retirar a dose prescrita para administração.
8. Remover as bolhas de ar na seringa e verificar a dose correta.
6.4 Administração
Strensiq é apenas para injeção subcutânea. O volume máximo de medicamento do estudo por injeção não deve exceder 1 mL. Se for necessário mais de 1 mL, várias injeções podem ser administradas no mesmo dia, em locais diferentes.
- Administrar Strensiq dentro de 3 horas após a remoção do(s) frasco(s) da refrigeração. Retire o(s) frasco(s) de Strensiq da geladeira 15 a 30 minutos antes da injeção para permitir que o líquido atinja a temperatura ambiente. Não aqueça o frasco de Strensiq de nenhuma outra maneira (por exemplo, não aqueça no microondas ou na água quente).
- Alternar a injeção entre os seguintes locais para reduzir o risco de lipodistrofia: área abdominal, coxa, deltoide ou nádegas.
- NÃO administrar injeções em áreas que estejam avermelhadas, inflamadas ou inchadas.
- Injetar Strensiq por via subcutânea no local determinado e descartar a seringa e a agulha.
- Os frascos de Strensiq são apenas para utilização única. Descartar qualquer produto não utilizado. Qualquer medicamento não utilizado ou resíduos devem ser descartados de acordo com os requisitos locais.
6.5 Cuidados na administração
Preparação
- Quando se prepara um volume de injeção superior a 1 mL, dividir o volume igualmente entre duas seringas e administrar duas injeções. Ao administrar as duas injeções, utilizar dois locais de injeção separados.
- Examinar a solução no(s) frasco(s) para detecção de partículas e descoloração.
- Montar os suprimentos de injeção. Administrar Strensiq usando seringas descartáveis estéreis e agulhas de injeção. As seringas devem ser de um volume pequeno o suficiente de forma que a dose prescrita possa ser retirada do frasco com uma exatidão razoável. Sempre usar uma nova seringa e agulha para cada injeção.
- Remover a tampa do frasco, de forma asséptica preparar o frasco e inserir a seringa no frasco para retirar a dose prescrita para administração.
- Remover as bolhas de ar na seringa e verificar a dose correta.
Administração
- Administrar Strensiq dentro de 3 horas após a remoção do(s) frasco(s) da refrigeração. Retire o(s) frasco(s) de Strensiq da geladeira 15 a 30 minutos antes da injeção para permitir que o líquido atinja a temperatura ambiente. Não aqueça o frasco de Strensiq de nenhuma outra maneira (por exemplo, não aqueça no microondas ou na água quente).
- Alternar o local de injeção para reduzir o risco de lipohipertrofia e atrofia no local de injeção.
- NÃO administrar injeções em áreas que estejam avermelhadas, inflamadas ou inchadas.
- Injetar Strensiq por via subcutânea no local determinado e descartar a seringa e a agulha corretamente.
- Os frascos de Strensiq são apenas para utilização única. Descartar qualquer produto não utilizado. Qualquer medicamento não utilizado ou resíduos devem ser descartados de acordo com os requisitos locais.
Reações de Hipersensibilidade
- As reações relacionadas com a administração da injeção podem ocorrer durante e após o tratamento com Strensiq. O seu médico lhe informará sobre os sinais e sintomas de reações de hipersensibilidade. Se você identificar qualquer um desses sinais e sintomas deve procurar cuidados médicos imediatos.
Lipodistrofia
- Lipohipertrofia (aumento ou espessamento do tecido) e atrofia localizada (depressão na pele) foram relatados em locais de injeção depois de vários meses. Seguir a técnica de injeção adequada e alternar os locais de injeção.
Instruções de Uso
Strensiq – Solução Injeção por via subcutânea
Leia estas instruções de uso antes de utilizar Strensiq. Pode haver novas informações. Estas informações não substituem falar com o seu médico sobre sua condição médica ou o seu tratamento. Não compartilhe suas seringas ou agulhas com qualquer outra pessoa. Você pode lhes passar uma infecção ou pegar uma infecção delas.
Utilize este medicamento exatamente como descrito nestas instruções e conforme orientação de seu médico, farmacêutico ou enfermeiro. A dose correta é calculada pelo seu médico. Somente após receber a orientação de seu médico e ser treinado por um profissional de saúde especializado, você poderá auto aplicar Strensiq em sua casa.
Preparando a sua dose de Strensiq:
- Prepare uma superfície plana e limpa, como uma mesa ou balcão
- Reunir todos os suprimentos que você precisa para administrar sua injeção de Strensiq
- Lave as mãos com água e sabão
Etapa 1: Verifique o líquido no frasco Strensiq.
O líquido de Strensiq deve parecer claro ou ligeiramente amarelo e pode ter algumas pequenas partículas brancas.
Não use se o líquido estiver sem cor ou contiver quaisquer protuberâncias ou partículas grandes. Jogue fora e pegue um novo frasco.
Etapa 2: Com o polegar, vire a tampa de plástico para fora do frasco de Strensiq.

Etapa 3: Remova a agulha da embalagem. Pegue a seringa e coloque a agulha na ponta da seringa. Empurre para baixo e rode a agulha na seringa até estar apertada.
Etapa 4: Segure a seringa com a agulha apontando para cima e puxe o êmbolo até que a parte superior do êmbolo atinja a linha para a sua dose prescrita.
Etapa 5: Retire a tampa da agulha em linha reta.
Não toque na agulha ou deixe que a agulha toque em qualquer superfície.

Etapa 6: Mantenha o frasco Strensiq firmemente sobre uma superfície plana, em seguida, empurre a agulha através da rolha de borracha do frasco de Strensiq.

Etapa 7: Mantendo a agulha no frasco de Strensiq, levante o frasco e vire de cabeça para baixo com a agulha apontando para o teto. Lentamente empurre o êmbolo todo o caminho para dentro.

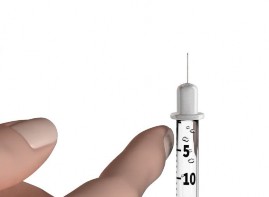
Etapa 8: Com a ponta da agulha ainda no líquido, puxe de volta o êmbolo até que a parte superior do êmbolo atinja a linha um pouco além da linha para a dose prescrita. Não puxe a agulha para fora do frasco de Strensiq. Lentamente empurre o êmbolo até que a parte superior do êmbolo atinja a linha para a dose prescrita.
Verifique a seringa para se certificar de que você tem a dose certa.
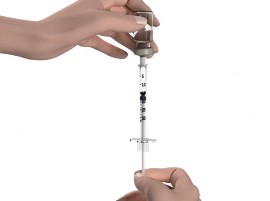
Etapa 9: Vire o frasco de Strensiq vertical para cima e puxe a seringa para fora da rolha de borracha do frasco.
Não toque na agulha ou permita que a agulha toque em qualquer superfície.
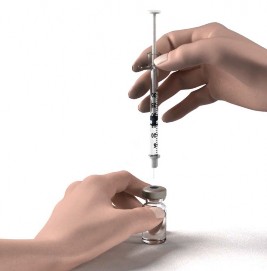
Etapa 10: Segure a seringa com a agulha apontando para cima e toque no corpo da seringa com o dedo para remover quaisquer bolhas de ar.
Administrando a sua injeção de Strensiq:
- Injete seu Strensiq exatamente como o seu médico lhe mostrou.
- Você deve usar o Strensiq dentro de 3 horas depois de retirá-lo do refrigerador.
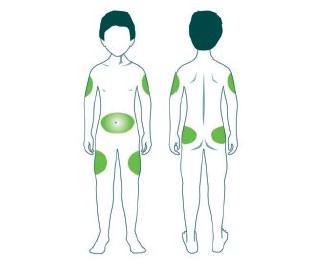
Etapa 11: Escolha o local da injeção.
Strensiq é injetado sob a pele (por via subcutânea) de sua área da barriga (abdómen), braços ou coxas.
- Mude (alterne) o local de administração a cada injeção. Não use o mesmo local para cada injeção.
- Não injete Strensiq em pele vermelha, quente ou inchada.
- Limpe a pele com um algodão embebido em álcool. Deixe o local secar antes de injetar a sua dose.
Etapa 12: Aperte a pele. Segure a seringa em um ângulo de 90° (para cima e para baixo) e insira a agulha sob a pele. Para os pacientes com pouca gordura, segure a seringa em um ângulo de 45o e insira a agulha sob a pele.
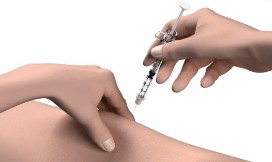
Etapa 13: Empurre o êmbolo todo o caminho para administrar a sua dose.
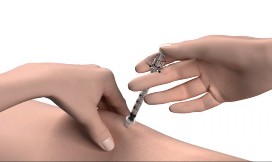
Etapa 14: Retire a agulha da sua pele.
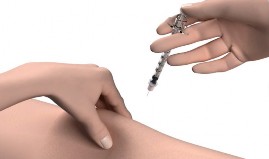
- Se você ver sangue depois de tirar a agulha da sua pele, pressione o local de injeção com um pedaço de gaze ou algodão embebido em álcool.
- Não retampe a agulha. Retampar a agulha pode levar a um ferimento por agulha.
Se você precisar de uma segunda injeção para a sua dose prescrita, pegue outro frasco de Strensiq e repita as etapas de 1 a 14.
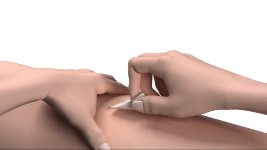
Qualquer medicamento não utilizado ou resíduos devem ser eliminados de acordo com as exigências locais.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Não injete uma dose a mais para compensar dose que esqueceu de injetar e consulte o seu médico.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Strensiq pode causar efeitos colaterais severos, incluindo:
- Reações alérgicas severas (hipersensibilidade). Reações alérgicas severas ocorreram em algumas pessoas que usaram Strensiq. Pare de usar Strensiq e vá ao pronto-socorro do hospital mais próximo imediatamente se você apresentar qualquer um dos sinais e sintomas de uma reação alérgica severa, incluindo:
- dificuldade para respirar
- inchaço dos olhos, lábios ou língua
- urticária
- sensação de desmaio
- náusea ou vômito
- tontura
- coceira nos lábios, língua ou garganta
- sensação de asfixia
- Espessamento da pele ou depressões no local da injeção (lipodistrofia). Lipodistrofia no local de injeção aconteceu depois de vários meses usando Strensiq.
- Acúmulo de cálcio em seus olhos e rins. Seu médico deve verificar seus olhos e rins enquanto você estiver utilizando Strensiq.
Os dados descritos abaixo refletem a exposição a Strensiq em 112 pacientes com HPP de início perinatal/infantil (n = 89), juvenil (n = 22) e adulto (n = 1) (idade de 1 dia a 66,5 anos) tratados com Strensiq, a maioria por mais de 2 anos (de 1 dia a 391,9 semanas [7,5 anos]): a maioria dos pacientes (69) recebeu pelo menos 120 semanas (2,3 anos) de tratamento, dos quais 44 pacientes receberam 240 semanas (4,6 anos) ou mais de tratamento.
As reações no local da injeção ocorreram em 74% dos pacientes que receberam Strensiq. A maioria das reações no local de injeção foi resolvida em uma semana. Um paciente foi retirado do estudo devido à hipersensibilidade no local da injeção.
A Tabela 9 apresenta as reações adversas observadas nos ensaios clínicos. As reações adversas relatadas com uma frequência muito comum (≥1 / 10), comum (≥1 / 100 a <1/10) ou incomum (≥1 / 1.000 a <1/100) com alfa-asfotase são listadas por classe de sistema de órgãos e termo preferido. Devido à pequena população de pacientes (n = 112), a categorização da frequência pode não refletir a ocorrência de uma reação adversa em uma população maior de pacientes. Dentro de cada grupo de frequências, reações adversas são apresentadas em ordem decrescente de gravidade.
Tabela 9: Reações Adversas Relatadas em Pacientes com HPP (de 1 dia a 66,5 anos de idade, com duração de tratamento de 1 dia a 391 semanas [7,5 anos]) nos Estudos Clínicos de Strensiq
|
Classe de Sistema de Orgãos MedDRA |
Frequência |
Reação adversa |
|
Distúrbios gerais e alterações no local de administração |
Muito comum |
Reações no local da injeçãoa Reações associadas a injeçãob |
|
Distúrbios do sistema imunológico |
Comum |
Hipersensibilidadec |
|
Distúrbios cutâneos e do tecido subcutâneo |
Comum |
Descoloração da pele |
|
Incomum |
Hiperpigmentação da pele |
|
|
Distúrbios renais e urinários |
Comum |
Nefrolitíase |
|
Metabolismo e nutrição |
Comum |
Hipocalcemia |
aOs termos preferenciais considerados como reações no local da injeção são apresentados na seção abaixo bOs termos preferenciais considerados como reações associadas a injeção são apresentados na seção abaixo cForam observados sinais e sintomas consistentes com a anafilaxia [vide Advertências e Precauções (5.2)]
Reações no local da injeção
Reações no local da injeção (incluindo atrofia no local da injeção, abscesso, eritema, descoloração, dor, prurido, mácula, inchaço, contusão, hematomas, lipodistrofia (lipoatrofia ou lipo-hipertrofia), endurecimento, reação, nódulo, erupção cutânea, pápula, hematoma, inflamação, urticária, calcificação, calor , hemorragia, celulite, cicatriz, massa, extravasamento, esfoliação e vesículas) são as reações adversas mais comuns.
Reações associadas à injeção
Reações associadas à injeção (incluindo hipersensibilidade, irritabilidade, pirexia, erupção cutânea, prurido, calafrios, eritema, náusea, vômito, rubor, hipoestesia oral, dor de cabeça, taquicardia e tosse) são reações adversas muito comuns, observadas em aproximadamente 22/112 (19,6%) dos pacientes nos estudos clínicos. Alguns relatos de casos de reação anafilactóide / hipersensibilidade também foram recebidos e foram associados a sinais e sintomas de dificuldade em respirar, sensação de asfixia, edema periorbital e tontura.
Imunogenicidade
Não foram observadas tendências em eventos adversos (EAs) com base no status do anticorpo em ensaios clínicos concluídos. Além disso, os pacientes confirmados como positivos para anticorpos não mostraram sinais de taquifilaxia após administração subcutânea de Strensiq. Dados de casos pós-comercialização sugerem que o desenvolvimento de anticorpos pode afetar a eficácia clínica.
Estes não são todos os possíveis efeitos colaterais da Strensiq. Para mais informações, pergunte ao seu médico ou farmacêutico.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião-dentista.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Em caso de utilização de quantidade maior que a recomendada, procure orientação de seu médico.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Registro MS: 1.9811.0002
Farm. Resp.: Luciana Maciel Zuicker Maziero, CRF-SP nº 24212
Fabricado por:
Ajinomoto Althea, Inc., San Diego, Estados Unidos da América. Alexion Pharma International Operations Limited, Athlone, Irlanda
Embalado por (embalagem secundária):
Almac Pharma Services Ltd, Craigavon, Reino Unido.
Alexion Pharma International Operations Limited, Dublin, Irlanda
Registrado por:
Alexion Serviços e Farmacêutica do Brasil Ltda.
Av Dr Chucri Zaidan 1240 Conj 1501 e 1503 andar 15 - Torre A Edif Morumbi Golden Tower - Vl São Francisco (Zona Sul), São Paulo/SP
CEP: 04.711-130
CNPJ 10.284.284/0001-49
SAC 0800 7725007






