Isentress (Bula do profissional de saúde)
MERCK SHARP & DOHME FARMACEUTICA LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Isentress®
raltegravir
Comprimidos 400 mg e 100 mg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Comprimidos revestidos de 400 mg e comprimidos mastigáveis de 100 mg
Frascos com 60 comprimidos.
USO ORAL
USO ADULTO E PEDIÁTRICO ACIMA DE 2 ANOS DE IDADE
COMPOSIÇÃO:
Cada comprimido revestido de Isentress® contém:
| raltegravir potássico (como sal, equivalente a 400 mg de raltegravir, sem fenol) | 434,4 mg |
| excipiente q.s.p. | 1 comprimido |
Excipientes: celulose microcristalina, lactose1 monoidratada, fosfato de cálcio dibásico, hipromelose, poloxâmer (contém 0,01% de hidroxitolueno butilado como antioxidante), estearilfumarato de sódio, estearato de magnésio, álcool polivinílico, dióxido de titânio, macrogol, talco, óxido de ferro vermelho e óxido de ferro preto.
Cada comprimido mastigável de Isentress® contém:
| raltegravir potássico (como sal, equivalente a 100 mg de raltegravir, sem fenol) | 108,6 mg |
| excipiente q.s.p. | 1 comprimido mastigável |
Excipientes: hiprolose, sucralose, sacarina2 sódica, citrato de sódio, manitol, óxido de ferro vermelho, óxido de ferro amarelo, glicirrizinato de amônio, sorbitol3, frutose4, aroma natural de banana e aroma natural e artificial (laranja e agente de mascaramento que contém aspartame5), crospovidona, estearato de magnésio, estearilfumarato de sódio, etilcelulose 20 cP, hidróxido de amônio, cadeia média de triglicerídeos, ácido oleico, hipromelose 2910/6 cP e macrogol/PEG 400.
INFORMAÇÕES TÉCNICAS AO PROFISSIONAL DE SAÚDE6
INDICAÇÕES
Isentress® é indicado em combinação com outros agentes antirretrovirais para o tratamento da infecção7 por HIV8-1.
RESULTADOS DE EFICÁCIA
Adultos
Descrição dos Estudos Clínicos: as evidências de eficácia durável de Isentress® baseiam-se nas análises dos dados de 96 semanas de 2 estudos randômicos, duplo-cegos e controlados por placebo9: BENCHMRK 1 e BENCHMRK 2 (Protocolos 018 e 019), compostos por pacientes adultos infectados por HIV8-1 já tratados com agentes antirretrovirais e na análise dos dados de 240 semanas de um estudo randômico, duplo-cego, controlado com fármaco10 ativo, o STARTMRK (P021).
Pacientes Já Tratados: BENCHMRK 1 e BENCHMRK 2 são estudos fase III para avaliar a segurança e a atividade antirretroviral de Isentress® 400 mg 2x/dia em combinação com uma Terapia Otimizada de Base (OBT), versus a OBT isoladamente, em pacientes infectados pelo HIV8, com 16 anos de idade ou mais, com resistência documentada a pelo menos 1 fármaco10 de cada uma das 3 classes (ITRNs, ITRNNs, IPs) de tratamento antirretroviral. A distribuição randômica foi estratificada por grau de resistência ao IP (1 IP vs. > 1 IP) e uso de enfuvirtida na OBT. Antes da distribuição randômica, a OBT foi selecionada pelo pesquisador com base no teste de resistência genotípica/fenotípica11 e no histórico anterior de ART.
A Tabela 1 mostra as características demográficas entre os pacientes do braço Isentress® 400 mg 2x/dia e os pacientes do braço que recebeu placebo9.
Tabela 1: Características no Período Basal
|
BENCHMRK 1 e 2 agrupados |
Isentress® 400 mg 2x/dia + OBT (N = 462) |
Placebo9 + OBT (N = 237) |
|
Sexo n (%) |
||
|
Masculino |
405 (87,7) |
210 (88,6) |
|
Feminino |
57 (12,3) |
27 (11,4) |
|
Raça n (%) |
||
|
Brancos |
301 (65,2) |
173 (73,0) |
|
Negros |
65 (14,1) |
26 (11,0) |
|
Asiáticos |
16 (3,5) |
6 (2,5) |
|
Hispânicos |
53 (11,5) |
19 (8,0) |
|
Outros |
27 (5,8) |
13 (5,5) |
|
Idade (anos) |
||
|
Mediana (mín., máx.) |
45,0 (16 a 74) |
45,0 (17 a 70) |
|
Contagem de Células12 CD4 |
||
|
Mediana (mín, máx), células12/mm3 |
119 (1 a 792) |
123 (0 a 759) |
|
≤ 50 células12/mm3, n (%) |
146 (31,6) |
78 (32,9) |
|
50 < e ≤ 200 células12/mm3, n (%) |
173 (37,4) |
85 (35,9) |
|
RNA de HIV8 Plasmático |
||
|
Mediana (mín., máx.), log10 cópias/mL |
4,8 (2,3 a 5,9) |
4,7 (2,3 a 5,9) |
|
> 100.000 cópias/mL, n (%) |
165 (35,7) |
78 (32,9) |
|
Histórico de AIDS n (%) |
||
|
Sim |
427 (92,4) |
215 (90,7) |
|
Uso Anterior de ART, Mediana (1o trimestre, 3o trimestre) |
||
|
Anos de uso de ART |
10,1 (7,3 a 12,1) |
10,2 (7,9 a 12,4) |
|
Número de ARTs |
12,0 (9 a 15) |
12,0 (9 a 14) |
|
Coinfecção por Hepatite† n (%) |
||
|
Sem Hepatite13 B ou C |
385 (83,3) |
200 (84,4) |
|
Hepatite13 B apenas |
36 (7,8) |
7 (3,0) |
|
Hepatite13 C apenas |
37 (8,0) |
28 (11,8) |
|
Coinfecção por Hepatite13 B e C |
4 (0,9) |
2 (0,8) |
|
Estrato n (%) |
||
|
Enfuvirtida na OBT |
175 (37,9) |
89 (37,6) |
|
Resistente a ≥ 2 IPs |
447 (96,8) |
226 (95,4) |
|
†Positivo para antígeno14 de superfície da hepatite13 B ou positivo para anticorpo15 da hepatite13 C. |
||
A Tabela 2 compara as características dos pacientes sob terapia otimizada de base no período basal que receberam Isentress® 400 mg 2x/dia versus as características dos pacientes do braço de controle.
Tabela 2. Características da Terapia Otimizada de Base no Período Basal
|
BENCHMRK 1 e 2 agrupados |
Isentress® 400 mg 2x/dia |
Placebo9 |
|
Número de ARTs na OBT |
||
|
Mediana (mín., máx.) |
4,0 (1 a 7) |
4,0 (2 a 7) |
|
Número de IPs Ativos na OBT pelo Teste de Resistência Fenotípica† |
||
|
0 |
165 (35,7) |
96 (40,5) |
|
1 ou mais |
278 (60,2) |
137 (57,8) |
|
Escore de Sensibilidade Fenotípica11 (ESF)‡ |
||
|
0 |
67 (14,5) |
43 (18,1) |
|
1 |
144 (31,2) |
71 (30,0) |
|
2 |
142 (30,7) |
66 (27,8) |
|
3 ou mais |
85 (18,4) |
48 (20,3) |
|
Escore de Sensibilidade Genotípica (ESG)‡ |
||
|
0 |
116 (25,1) |
65 (27,4) |
|
1 |
177 (38,3) |
95 (40,1) |
|
2 |
111 (24,0) |
49 (20,7) |
|
3 ou mais |
51 (11,0) |
23 (9,7) |
|
†O uso de darunavir na OBT em pacientes que não haviam recebido darunavir foi contabilizado como um IP ativo. ‡O Escore de Sensibilidade Fenotípica11 (ESF) e o Escore de Sensibilidade Genotípica (ESG) foram definidos como o total de ARTs orais na OBT aos quais um isolado viral do paciente apresentou sensibilidade fenotípica11 e sensibilidade genotípica, respectivamente, com base nos testes de resistência fenotípica11 e genotípica. O uso de enfuvirtida na OBT de pacientes que não haviam recebido enfuvirtida foi contabilizado como um fármaco10 ativo na OBT no ESG e no ESF. Da mesma maneira, o uso de darunavir na OBT em pacientes que não haviam recebido darunavir foi contabilizado como um fármaco10 ativo na OBT. |
||
Os resultados da 48a e da 96ª semanas para os 699 pacientes distribuídos de forma randômica e que receberam a dose recomendada de Isentress® 400 mg 2x/dia dos estudos BENCHMRK 1 e 2 agrupados são mostrados na Tabela 3.
Tabela 3. Resultados por Grupo de Tratamento até a 48ªe 96ª Semanas
|
Estudos Randômicos Protocolos 018 e 019 |
Resultado na 48ª Semana |
Resultado na 96ª Semana |
||
|
Isentress® |
Placebo9 |
Isentress® |
Placebo9 |
|
|
Pacientes com RNA de HIV8 menor que 400 cópias/mL* |
332 (72,3) |
88 (37,1) |
283 (61,5) |
67 (28,3) |
|
Pacientes com RNA de HIV8 menor que 50 cópias/mL* |
285 (62,1) |
78 (32,9) |
262 (57,0) |
62 (26,2) |
|
Pacientes com redução de RNA de HIV8 maior que 1 log10 ou RNA de HIV8 menor que 400 cópias/mL* |
348 (75,8) |
94 (39,7) |
294 (63,9) |
69 (29,1) |
|
Alteração média de RNA de HIV8 em relação ao período basal (log10 cópias/mL)* |
-1,71 |
-0,78 |
-1,51 |
-0,60 |
|
Alteração média de contagem de células12 CD4 em relação ao período basal (células12/mm3)* |
109,4 |
44,6 |
123,4 |
48,9 |
|
Falha virológica (confirmada)† |
105 (22,7) |
134 (56,5) |
150 (32,5) |
148 (62,4) |
|
Não respondeu |
12 (2,6) |
72 (30,4) |
12 (2,6) |
72 (30,4) |
|
Rebote |
93 (20,1) |
62 (26,2) |
138 (29,9) |
76 (32,1) |
|
Óbito‡ |
10 (2,2) |
6 (2,5) |
13 (2,8) |
6 (2,5) |
|
Condição Definidora de AIDS – Julgada (CDA)‡ |
17 (3,7) |
11 (4,6) |
18 (3,9) |
11 (4,6) |
|
Descontinuação devido a eventos adversos clínicos‡ |
10 (2,2) |
7 (3,0) |
16 (3,5) |
10 (4,2) |
|
Descontinuação devido a eventos adversos laboratoriais‡ |
1 (0,2) |
0 (0,0) |
1 (0,2) |
0 (0,0) |
|
Descontinuação devido a outros motivos‡§ |
11 (2,4) |
4 (1,7) |
38 (8,2) |
19 (8,0) |
|
*Abordagem para manuseio dos valores faltantes: para desfechos binários (proporções), a ausência de resposta equivale à falha. Para alteração em relação ao período basal em log10 RNA de HIV8 e alteração em relação ao período basal em contagem de células12 CD4, a abordagem de Falha Observada (FO) assume que o valor do período basal foi transportado para pacientes16 que descontinuaram a terapia designada por falta de eficácia. †Falha virológica: definida como pacientes que não responderam ao tratamento e não atingiram redução > 1,0 log10 de RNA de HIV8 ou < 400 cópias de RNA de HIV8/mL na 16a semana, ou rebote viral, definido como: (a) RNA de HIV8 > 400 cópias/mL (em 2 medidas consecutivas com pelo menos 1 semana de intervalo) após a resposta inicial com RNA de HIV8 < 400 cópias/mL ou (b) aumento > 1,0 log10 de RNA de HIV8 acima do nível do ponto mais baixo (em 2 medidas consecutivas com pelo menos 1 semana de intervalo). ‡O resultado na 48a semana incluiu dados de pelo menos 48 semanas. O resultado na 96a semana incluiu dados até a 96ª semana. §Inclui perda de acompanhamento, retirada do consentimento do paciente, falta de adesão, violação do protocolo e outros motivos. Nota: Isentress® e placebo9 foram administrados com terapia otimizada de base. N = número de pacientes em cada grupo de tratamento. |
||||
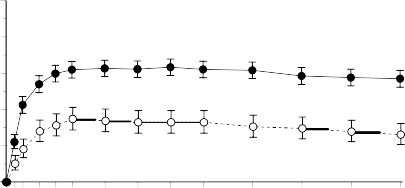
O percentual (IC 95%) de pacientes que atingiram RNA de HIV8 < 50 cópias/mL em função do tempo é apresentado na Figura 1.
Figura 1. Proporção de Pacientes com RNA de HIV8 < 50 Cópias/mL (IC 95%) Em Função do Tempo (Não Completo = Falha)
As respostas virológicas na 96ª semana por escore de sensibilidade genotípica e fenotípica11 no período basal são mostradas na Tabela 4.
Tabela 4. Resposta Virológica na 96a Semana por Escore de Sensibilidade Genotípica/Fenotípica11 no Período Basal†
|
BENCHMRK 1 e 2 agrupados (abordagem de falhas virológicas levadas adiante) |
Isentress® 400 mg 2x/dia |
Placebo9 |
||||
|
n |
Porcentagem com RNA de HIV8 < 400 cópias/mL na 96a semana |
Porcentagem com RNA de HIV8 < 50 cópias/mL na 96a semana |
n |
|
Porcentagem com RNA de HIV8 < 50 cópias/mL na 96a semana |
|
|
Escore de Sensibilidade Fenotípica‡ |
||||||
|
0 |
63 |
51 |
48 |
43 |
5 |
5 |
|
1 |
131 |
69 |
65 |
68 |
26 |
24 |
|
2 |
134 |
74 |
69 |
60 |
37 |
35 |
|
3 ou mais |
74 |
62 |
54 |
40 |
53 |
48 |
|
Escore de Sensibilidade Genotípica‡ |
||||||
|
0 |
111 |
46 |
41 |
64 |
5 |
5 |
|
1 |
160 |
76 |
72 |
89 |
31 |
28 |
|
2 |
102 |
75 |
70 |
41 |
61 |
61 |
|
3 ou mais |
45 |
62 |
53 |
21 |
48 |
38 |
|
†Abordagem de falha observada ‡ O ESF e o ESG foram definidos como o total de ARTs orais na OBT aos quais um isolado viral do paciente apresentou sensibilidade fenotípica11 e sensibilidade genotípica, respectivamente, com base nos testes de resistência fenotípica11 e genotípica. O uso de enfuvirtida na OBT de pacientes que não haviam recebido enfuvirtida foi contabilizado como fármaco10 ativo na OBT no ESG e no ESF. Da mesma maneira, o uso de darunavir na OBT em pacientes que não haviam recebido darunavir foi contabilizado como fármaco10 ativo na OBT. |
||||||
Troca de Pacientes Suprimidos de Lopinavir/Ritonavir para Raltegravir
Os estudos SWITCHMRK 1 e 2 avaliaram pacientes infectados por HIV8 recebendo tratamento supressor17 (RNA de HIV8 na triagem < 50 cópias/mL; regime estável > 3 meses) com lopinavir 200 mg/ritonavir 50 mg, 2 comprimidos 2x/dia mais pelo menos 2 inibidores nucleosídeos de transcriptase reversa e os distribuíram de forma randômica na proporção de 1:1 para continuar com lopinavir/ritonavir 2 comprimidos 2x/dia (n = 174 e n = 178, respectivamente) ou substituir lopinavir/ritonavir por raltegravir 400 mg 2x/dia (n = 174 e n = 176, respectivamente). Os pacientes com histórico anterior de falha virológica não foram excluídos e o número de tratamentos antirretrovirais anteriores não era limitado.
Esses estudos foram encerrados após a análise primária de eficácia na 24ª semana porque não conseguiram demonstrar a não inferioridade do raltegravir versus lopinavir/ritonavir. Em ambos os estudos na 24a semana, a supressão do RNA de HIV8 para menos de 50 cópias/mL foi mantida em 84,4% do grupo raltegravir versus 90,6% do grupo lopinavir/ritonavir (não completo = falha). Em pacientes que nunca apresentaram falha virológica antes da entrada no estudo, taxas de resposta virológica similares foram observadas nos grupos do raltegravir e do lopinavir/ritonavir.
Pacientes Não Tratados Previamente
O STARTMRK é um estudo Fase III para avaliar a segurança e a atividade antirretroviral de Isentress® 400 mg 2x/dia + entricitabina/fumarato de tenofovir desoproxila versus efavirenz + entricitabina/fumarato de tenofovir desoproxila em pacientes infectados por HIV8 nunca expostos a tratamento com RNA de HIV8 > 5.000 cópias/mL. A distribuição randômica foi estratificada por nível de triagem de RNA de HIV8 (≤ 50.000 cópias/mL; e > 50.000 cópias/mL) e por status de hepatite13.
A Tabela 5 mostra as características demográficas entre pacientes do grupo que recebeu Isentress® 400 mg 2x/dia e pacientes do grupo que recebeu efavirenz.
Tabela 5. Características Basais dos Pacientes
|
|
Isentress® |
Efavirenz 600 mg |
Total |
|
Sexo n (%) |
|||
|
Masculino |
227 (80,8) |
231 (81,9) |
458 (81,3) |
|
Feminino |
54 (19,2) |
51 (18,1) |
105 (18,7) |
|
Raça n (%) |
|||
|
Brancos |
116 (41,3) |
123 (43,6) |
239 (42,5) |
|
Negros |
33 (11,7) |
23 (8,2) |
56 (9,9) |
|
Asiáticos |
36 (12,8) |
32 (11,3) |
68 (12,1) |
|
Hispânicos |
60 (21,4) |
67 (23,8) |
127 (22,6) |
|
Nativos Americanos |
1 (0,4) |
1 (0,4) |
2 (0,4) |
|
Multirraciais |
35 (12,5) |
36 (12,8) |
71 (12,6) |
|
Região n (%) |
|||
|
América Latina |
99 (35,2) |
97 (34,4) |
196 (34,8) |
|
Sudeste Asiático |
34 (12,1) |
29 (10,3) |
63 (11,2) |
|
América do Norte |
82 (29,2) |
90 (31,9) |
172 (30,6) |
|
UE/Austrália |
66 (23,5) |
66 (23,4) |
132 (23,4) |
|
Idade (anos) |
|||
|
18–64 n (%) |
279 (99,3) |
278 (98,6) |
557 (98,9) |
|
≥ 65 n (%) |
2 (0,7) |
4 (1,4) |
6 (1,1) |
|
Média (DP) |
37,6 (9,0) |
36,9 (10,0) |
37,2 (9,5) |
|
Mediana (mín, máx) |
37,0 (19 a 67) |
36,0 (19 a 71) |
37,0 (19 a 71) |
|
Contagem de Células12 CD4 (células12/microL) |
|||
|
N† |
281 |
281 |
562 |
|
Média (DP) |
218,9 (124,2) |
217,4 (133,6) |
218,1 (128,8) |
|
Mediana (mín, máx) |
212,0 (1 a 620) |
204,0 (4 a 807) |
207,5 (1 a 807) |
|
RNA de HIV8 Plasmático (log10 cópias/mL) |
|||
|
N† |
281 |
282 |
563 |
|
Média (DP) |
5,0 (0,6) |
5,0 (0,6) |
5,0 (0,6) |
|
Mediana (mín., máx.) |
5,1 (2,6 a 5,9) |
5,0 (3,6 a 5,9) |
5,0 (2,6 a 5,9) |
|
RNA de HIV8 Plasmático (cópias/mL) |
|||
|
N† |
281 |
282 |
563 |
|
Média geométrica |
103.205 |
106.215 |
104.702 |
|
Mediana (mín., máx.) |
114.000 (400 a 750.000) |
104.000 (4.410 a 750.000) |
110.000 (400 a 750.000) |
|
Histórico de AIDS n (%) |
|||
|
Sim |
52 (18,5) |
59 (20,9) |
111 (19,7) |
|
Estrato n (%) |
|||
|
RNA de HIV8 na triagem ≤ 50.000 |
75 (26,7) |
80 (28,4) |
155 (27,5) |
| Positivo para Hepatite13 B ou C‡ | 18 (6,4) | 16 (5,7) | 34 (6,0) |
|
Subtipo Viral n (%) |
|||
|
Clade B |
219 (77,9) |
230 (81,6) |
449 (79,8) |
|
Não Clade B§ |
59 (21,0) |
47 (16,7) |
106 (18,8) |
|
Faltante |
3 (1,1) |
5 (1,8) |
8 (1,4) |
|
RNA de HIV8 Plasmático Basal† n (%) |
|||
|
≤ 50.000 cópias/mL |
79 (28,1) |
84 (29,8) |
163 (29,0) |
|
> 50.000 cópias/mL |
202 (71,9) |
198 (70,2) |
400 (71,0) |
|
≤ 100.000 cópias/mL |
127 (45,2) |
139 (49,3) |
266 (47,2) |
|
> 100.000 cópias/mL |
154 (54,8) |
143 (50,7) |
297 (52,8) |
|
Contagem Basal de Células12 CD4 n (%) |
|||
|
≤ 50 células12/mm3 |
27 (9,6) |
31 (11,0) |
58 (10,3) |
|
> 50 células12/mm3 e ≤ 200 células12/mm3 |
104 (37,0) |
105 (37,2) |
209 (37,1) |
|
> 200 células12/mm3 |
150 (53,4) |
145 (51,4) |
295 (52,4) |
|
Faltante |
0 (0,0) |
1 (0,4) |
1 (0,2) |
|
†Pacientes com resultados faltantes excluídos. ‡Evidência de antígeno14 de superfície de hepatite13 B ou evidência de RNA de HCV por teste quantitativo de reação de cadeia de polimerase (PCR18) para vírus19 de hepatite13 C. §Subtipos Não Clade B (nº de pacientes): Clade A (4), A/C (1), A/G (2), A1(1), AE (29), AG (12), BF (6), C (37), D (2), F (2), F1 (5), G (2), Complexo (3) Notas: |
|||
Na análise da semana 240, o regime de Isentress® foi superior ao regime de efavirenz com base na eficácia virológica e imunológica. Os resultados da 48a e 240a semanas do STARTMRK são mostrados na Tabela 6.
Tabela 6. Resultados por Grupo de Tratamento até a 48ª e 240ª Semanas*
|
Estudo Randômico Protocolo 021 |
Resultado na 48ª Semana |
Resultado na 240ª Semana |
||||
|
Isentress® 400 mg |
Efavirenz 600 mg |
Diferença (Isentress® |
Isentress® 400 mg |
Efavirenz 600 mg |
Diferença (Isentress® |
|
|
Pacientes com RNA de HIV8 menor que 50 cópias/mL*† |
241 (86,1) |
230 (81,9) |
4,2% (-1,9, 10,3) |
198 (71,0) |
171 (61,3) |
9,5% (1,7, 17,3) 7,3 |
|
Pacientes com RNA de HIV8 menor que 400 cópias/mL*† |
252 (90,0) |
241 (85,8) |
4,1% (-1,3, 9,7) |
206 (73,8) |
181 (64,9) |
8,8% (1,2, 16,4) |
|
Alteração média em relação ao período basal da contagem de células12 CD4 (células12/mm3)† |
189,1 |
163,3 |
25,8 |
373,7 |
311,6 |
62,1 (21,9, 102,2) |
|
Falha virológica (confirmada) ‡ (< 50) |
27 (9,6) |
39 (13,8) |
(4,4, 47,2) |
55 (19,6) |
59 (20,9) |
|
|
Não respondeu |
10 (3,6) |
24 (8,5) |
10 (3,6) |
24 (8,5) |
||
|
Rebote |
17 (6,0) |
15 (5,3) |
45 (16,0) |
35 (12,4) |
||
|
Óbito20 |
2 (0,7) |
0 (0,0) |
5 (1,8) |
5 (1,8) |
||
|
Descontinuação por eventos adversos clínicos |
8 (2,8) |
17 (6,0) |
14 (5,0) |
25 (8,9) |
||
|
Descontinuação por eventos adversos laboratoriais |
0 (0,0) |
1 (0,4) |
0 (0,0) |
3 (1,1) |
||
|
Descontinuação por outros motivos§ |
12 (4,3) |
15 (5,3) |
51 (18,1) |
60 (21,3) |
||
|
*Concluiu-se que Isentress® não é inferior ao efavirenz se o limite inferior do IC de 95% para a diferença na resposta porcentual for superior a 12 pontos percentuais. Pode-se ainda concluir que Isentress® é superior ao efavirenz se o limite inferior exceder zero. †Abordagem para manipulação de valores faltantes: para desfechos binários (proporções), pacientes que não completaram o tratamento = falha. Para alteração em relação ao período basal na contagem de células12 CD4, a abordagem de Falha Observada (FO) assume que o valor basal foi transportado para pacientes16 que descontinuaram o tratamento designado devido à falta de eficácia. ‡Falha virológica = definida como pacientes que não responderam para aqueles com (1) RNA de HIV8 > 50 cópias/mL no momento da descontinuação para pacientes16 que descontinuaram prematuramente o tratamento do estudo ou (2) RNA de HIV8 > 50 cópias/mL na 24ª semana; ou rebote virológico para aqueles com RNA de HIV8 > 50 cópias/mL (em 2 medidas consecutivas com pelo menos 1 semana de intervalo) após resposta inicial com RNA de HIV8 < 50 cópias/mL. §Inclui perda de acompanhamento, paciente retirou o consentimento, falta de adesão, violação do protocolo e outros motivos. Nota: Isentress® e efavirenz foram administrados com TRUVADATM. n (%) = número (porcentagem) de pacientes em cada categoria. |
||||||
A Figura 2 apresenta a proporção de pacientes com RNA de HIV8 plasmático < 50 cópias/mL em função do tempo por grupo de tratamento. Os pacientes tratados com Isentress® atingiram supressão viral (RNA de HIV8 < 50 cópias/mL) mais cedo que os que receberam EFV. Durante 240 semanas de tratamento, 71% do grupo que recebeu Isentress® 400 mg 2x/dia e 61% no grupo comparador atingiram RNA de HIV8 < 50 cópias/mL (abordagem NC = F).
Figura 2. Proporção de Pacientes com RNA de HIV8 < 50 Cópias/mL (IC 95%) Em Função do Tempo (NC = F)
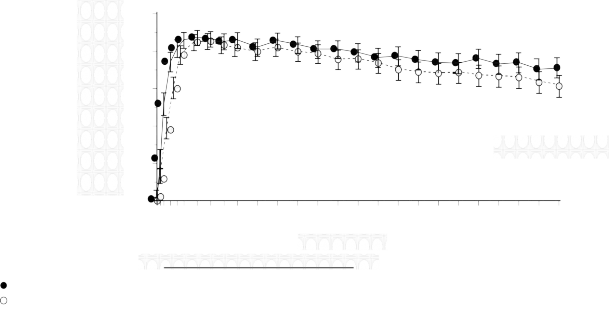
No estudo STARTMRK da terapia de combinação antirretroviral em pacientes nunca expostos a tratamento, Isentress® com entricitabina/fumarato de tenofovir desoproxila demonstrou eficácia virológica e imunológica consistente em relação ao efavirenz com entricitabina/fumarato de tenofovir desoproxila por meio de dados demográficos e fatores prognósticos basais, incluindo: nível basal de RNA de HIV8 plasmático > 100.000 cópias/mL, células12 CD4 basais ≤ 50 células12/mm3, grupos demográficos (incluindo idade, sexo, região e raça), com status de coinfecção por hepatites21 (hepatite13 B e/ou C) e subtipos virais (comparando clade não B com um grupo clade B).
Observou-se eficácia consistente de Isentress® em todos os subtipos de HIV8, com 89,6% (155/173) e 87,0% (40/46) dos pacientes com subtipos B e não B, respectivamente, atingindo RNA de HIV8 < 50 cópias/mL na 240ª semana (abordagem FO).
Durante 240 semanas de terapia, Isentress® demonstrou efeitos mínimos sobre os níveis lipídicos séricos com pequenos aumentos de colesterol22 total, HDL23, LDL24, triglicérides25 e colesterol22 não HDL23. O grupo tratado com efavirenz apresentou alteração média significativamente maior em relação ao período basal dos níveis de colesterol22 total, HDL23, LDL24, triglicérides25 e colesterol22 não HDL23.
Pacientes Pediátricos 2 a 18 anos de idade
O estudo IMPAACT P1066 é um estudo aberto e multicêntrico Fase I/II para avaliar o perfil farmacocinético, a segurança, a tolerabilidade e a eficácia de raltegravir em crianças infectadas pelo HIV8. Esse estudo admitiu 126 crianças e adolescentes de 2 a 18 anos de idade já tratados. Os pacientes foram estratificados por idade, admitindo adolescentes primeiramente e, então, crianças mais jovens, sucessivamente. Os pacientes receberam a formulação de comprimidos de 400 mg (6 a 18 anos de idade) ou a formulação de comprimidos mastigáveis (2 a 11 anos de idade). O raltegravir foi administrado a um regime de base otimizado.
O estágio de definição da dose inicial incluiu avaliação farmacocinética intensiva. A seleção da dose foi baseada na obtenção de exposição plasmática similar de raltegravir e concentração de vale, conforme observado em adultos, e segurança aceitável de curto prazo. Após a seleção da dose, outros pacientes foram admitidos para avaliação da segurança, tolerabilidade e eficácia prolongada. Dos 126 pacientes, 96 receberam a dose recomendada de Isentress® (veja 8. POSOLOGIA E MODO DE USAR).
Esses 96 pacientes tinham idade mediana de 13 (faixa de 2 a 18) anos, 51% eram do sexo feminino, 34% caucasianos e 59% negros. No período basal, o nível médio plasmático de RNA de HIV8-1 era de 4,3 log10 cópias/mL, a contagem mediana de células12 CD4, de 481 células12/mm3 (intervalo: 0–2.361) e a % mediana de CD4 era de 23,3% (intervalo: 0–44). No geral, 8% apresentaram níveis plasmáticos basais de RNA de HIV8-1 > 100.000 cópias/mL e 59% apresentaram classificação clínica de CDC HIV8 categoria B ou C. A maioria dos pacientes havia utilizado anteriormente pelo menos um ITRNN (78%) ou um IP (83%).
Noventa e três (97%) pacientes com 2 a 18 anos de idade completaram 24 semanas de tratamento (3 descontinuaram por falta de adesão). Na 24a semana, 72% atingiram redução ≥ 1 log10 RNA de HIV8 em relação ao período basal ou < 400 cópias/mL; 54% atingiram RNA de HIV8 < 50 cópias/mL. O aumento médio da contagem de CD4 (porcentagem) do período basal até a 24ª semana foi de 119 células12/mm3 (3,8%).
Setenta e dois (95%) pacientes com 6 a 18 anos de idade completaram 48 semanas de tratamento (4 descontinuaram por falta de adesão). Na 48a semana, 77% atingiram redução ≥ 1 log10 RNA de HIV8 em relação ao período basal ou < 400 cópias/mL; 56% atingiram RNA de HIV8 < 50 cópias/mL. O aumento médio da contagem de CD4 (porcentagem) do período basal até a 48a semana foi de 155 células12/mm3 (4,7%).
CARACTERÍSTICAS FARMACOLÓGICAS
Isentress® é um inibidor da integrase, enzima26 responsável pela transferência do filamento de DNA viral do HIV8, ativo contra o vírus19 da imunodeficiência27 humana (HIV8-1).
Mecanismo de Ação
O raltegravir inibe a atividade catalítica da integrase do HIV8, uma enzima26 decodificada pelo HIV8 e necessária para a replicação viral. A inibição da integrase evita a inserção ou integração covalente do genoma do HIV8 no genoma da célula28 hospedeira durante a fase inicial da infecção7. Os genomas do HIV8 que não conseguem se integrar, não conseguem dirigir a produção de novas partículas infecciosas virais e, dessa forma, a inibição da integração impede a propagação da infecção7 viral. O raltegravir não inibiu de forma significativa as fosforiltransferases humanas, incluindo as polimerases α, β, e γ do DNA.
Absorção
O raltegravir é rapidamente absorvido em jejum com Tmáx de aproximadamente 3 horas após a dose. A AUC29 e a Cmáx do raltegravir aumentam de forma proporcional com a dose no intervalo de dose de 100 mg a 1.600 mg. A C12h do raltegravir aumenta proporcionalmente com a dose no intervalo de dose de 100 a 800 mg e aumenta um pouco menos que proporcionalmente com a dose no intervalo de dose de 100 mg a 1.600 mg. Com a administração 2x/dia, o estado de equilíbrio farmacocinético é atingido rapidamente, aproximadamente nos primeiros 2 dias de administração. Existe pouco ou nenhum acúmulo de AUC29 e de Cmáx e evidências de discreto acúmulo de C12h. A biodisponibilidade absoluta do raltegravir ainda não foi estabelecida. Em pacientes que recebem monoterapia com 400 mg 2x/dia, a exposição ao raltegravir foi caracterizada por uma AUC290–12h média geométrica de 14,3 μM•h e C12h de 142 nM.
Efeito da Presença de Alimentos sobre a Absorção Oral
Isentress® pode ser administrado com ou sem alimentos. O raltegravir foi administrado independentemente da presença de alimentos nos principais estudos de segurança e eficácia em pacientes infectados pelo HIV8. O efeito do consumo de refeições com baixo, moderado e alto teor de gorduras sobre a farmacocinética de estado de equilíbrio do raltegravir foi determinado em voluntários saudáveis. A administração de doses múltiplas de raltegravir após uma refeição de teor moderado de gorduras não afetou a AUC29 do raltegravir em um grau clinicamente significativo, com um aumento de 13% em relação ao estado de jejum. A C12h do raltegravir foi 66% maior e a Cmáx foi 5% maior após uma refeição com teor moderado de gorduras em comparação com o estado de jejum. A administração de raltegravir após uma refeição com alto teor de gorduras aumentou a AUC29 e a Cmáx em aproximadamente 2 vezes e aumentou a C12h em 4,1 vezes. A administração do raltegravir após uma refeição com baixo teor de gorduras diminuiu a AUC29 e a Cmáx. em 46% e a 52%, respectivamente; a C12h ficou basicamente inalterada. A presença de alimentos parece aumentar a variabilidade farmacocinética em relação ao estado de jejum.
Distribuição
O raltegravir apresenta taxa de ligação a proteínas30 plasmáticas de aproximadamente 83% no intervalo de concentração de 2 a 10 µM. O raltegravir atravessa prontamente a placenta de ratas, porém, não penetrou o cérebro31 em grau perceptível. Em dois estudos com indivíduos infectados com HIV8-1 que receberam raltegravir 400 mg 2x/dia, o raltegravir foi rapidamente detectado no fluido cerebrospinal. No primeiro estudo (n = 18), a mediana da concentração do fluido cerebrospinal foi de 5,8% (faixa de 1 a 53,5%) da concentração correspondente no plasma32. No segundo estudo (n = 16), a mediana da concentração do fluido cerebrospinal foi de 3% (faixa de 1 a 61%) da concentração correspondente no plasma32. As proporções dessas medianas são aproximadamente 3 a 6 vezes inferiores às da fração livre de raltegravir no plasma32.
Metabolismo33 e Eliminação
A meia-vida terminal aparente do raltegravir é de aproximadamente 9 horas, com uma meia-vida de fase α mais curta (~1 hora) respondendo pela maior parte da AUC29. Após a administração de uma dose oral de raltegravir radiomarcado, aproximadamente 51% e 32% da dose foram excretados nas fezes e urina34, respectivamente. Nas fezes, apenas o raltegravir estava presente, e a maioria provavelmente era derivada da hidrólise do glicuronídeo de raltegravir na bile35, conforme observado nas espécies pré-clínicas. Dois componentes, raltegravir e glicuronídeo de raltegravir, foram detectados na urina34 e responderam por cerca de 9% e 23% da dose, respectivamente. A principal entidade circulante era o raltegravir, representando aproximadamente 70% da radioatividade total; a radioatividade restante no plasma32 foi atribuída ao glicuronídeo de raltegravir. Estudos que utilizaram inibidores químicos seletivos da isoforma e as UDP-glicuronosiltransferases (UGT) expressas pelo cDNA mostram que a UGT1A1 é a principal enzima26 responsável pela formação do glicuronídeo de raltegravir. Assim, os dados indicam que o principal mecanismo de depuração do raltegravir em humanos é a glicuronidação mediada por UGT1A1.
Características em Pacientes
Sexo: um estudo sobre a farmacocinética do raltegravir foi realizado em homens e mulheres jovens, adultos e saudáveis. Além disso, em uma análise composta dos dados farmacocinéticos de 103 indivíduos saudáveis e 28 pacientes com HIV8 que receberam monoterapia com raltegravir administrada em jejum foi avaliada se haveria alguma diferença de resposta recorrente do sexo. Essa hipótese também foi avaliada em uma análise da farmacocinética populacional (PK) dos dados de concentração de 80 indivíduos saudáveis e pacientes com HIV8 que recebem apenas raltegravir ou raltegravir em combinação com outros fármacos, na presença ou não de alimentos. Não houve nenhuma diferença farmacocinética clinicamente importante decorrente do sexo. Não é necessário ajuste de dose.
Idade: o efeito da idade (18 anos ou mais) sobre a farmacocinética do raltegravir foi avaliado na análise composta e na análise de farmacocinética populacional. Não houve efeito clinicamente significativo decorrente da idade sobre a farmacocinética do raltegravir. Não é necessário ajuste de dose.
Pacientes Pediátricos: com base em um estudo de comparação de formulação em voluntários adultos saudáveis, o comprimido mastigável possui maior biodisponibilidade oral em comparação com o comprimido de 400 mg. Nesse estudo, a administração do comprimido mastigável com uma refeição com alto teor de gorduras levou à redução média de 6% da AUC29, à redução de 62% da Cmáx, e ao aumento de 188% da C12h em comparação com a administração em jejum. A administração do comprimido mastigável com uma refeição de alto teor de gorduras não afeta a farmacocinética do raltegravir em um grau clinicamente significativo e o comprimido mastigável pode ser administrado independentemente da presença de alimentos.
As doses recomendadas a crianças e adolescentes infectados com HIV8 de 2 a 18 anos de idade (veja 8. POSOLOGIA E MODO DE USAR) resultou em perfil farmacocinético de raltegravir similar ao observado em adultos recebendo 400 mg 2x/dia. A Tabela 7 mostra os parâmetros farmacocinéticos do comprimido de 400 mg e do comprimido mastigável por peso corporal.
Tabela 7. Parâmetros Farmacocinéticos de Raltegravir do IMPAACT P1066 Após Administração das Doses em POSOLOGIA E ADMINISTRAÇÃO
|
Peso Corporal |
Formulação |
Dose |
N* |
Média Geométrica |
Média Geométrica |
|
≥ 25 kg |
Comprimido revestido |
400 mg 2x/dia |
18 |
14,1 (121%) |
233 (157%) |
|
≥ 25 kg |
Comprimido mastigável |
Administração baseada no peso, veja Tabela 9 |
9 |
22,1 (36%) |
113 (80%) |
|
11 a menos de 25 kg |
Comprimido mastigável |
Administração baseada no peso, veja Tabela 9 |
13 |
18,6 (68%) |
82 (123%) |
|
* Número de pacientes com resultados farmacocinéticos (PK) intensivos na dose final recomendada. † Coeficiente de variação geométrica. |
|||||
A farmacocinética dos comprimidos mastigáveis de raltegravir em crianças com menos de 2 anos de idade não foi estabelecida.
Raça: o efeito da raça sobre a farmacocinética do raltegravir foi avaliado na análise composta. Não houve efeito clinicamente significativo da raça sobre a farmacocinética do raltegravir. Não é necessário ajuste de dose.
Índice de Massa Corporal36 (IMC37): a análise composta avaliou o efeito do IMC37 na farmacocinética do raltegravir. Não houve efeito clinicamente significativo do IMC37 na farmacocinética do raltegravir em adultos. Além disso, nenhum efeito clinicamente significativo do peso corporal na farmacocinética do raltegravir foi identificado na análise da farmacocinética populacional. Não é necessário ajuste de dose.
Insuficiência Hepática38: o raltegravir é eliminado principalmente por glicuronidação no fígado39. Um estudo da farmacocinética do raltegravir foi realizado em pacientes adultos com insuficiência hepática38 moderada. Além disso, a insuficiência hepática38 foi avaliada na análise farmacocinética composta. Não houve diferença farmacocinética clinicamente importante entre os pacientes com insuficiência hepática38 moderada e os indivíduos saudáveis. Não é necessário ajuste de dose para pacientes16 com insuficiência hepática38 leve a moderada. O efeito da insuficiência hepática38 grave sobre a farmacocinética do raltegravir não foi estudado.
Insuficiência Renal40: a depuração renal41 do fármaco10 inalterado é uma via de eliminação de menor importância. Um estudo da farmacocinética do raltegravir foi realizado em pacientes adultos com insuficiência renal40 grave. Além disso, a insuficiência renal40 foi avaliada na análise farmacocinética composta. Não houve diferenças farmacocinéticas clinicamente compostas entre os pacientes com insuficiência renal40 grave e os indivíduos saudáveis. Não é necessário ajuste de dose. Como o grau em que Isentress® pode ser dialisável é desconhecido, deve-se evitar a administração do medicamento antes de uma sessão de diálise42.
Polimorfismo da UGT1A1: não há evidências de que os polimorfismos comuns da UGT1A1 alterem a farmacocinética do raltegravir em uma extensão clinicamente significativa. Em uma comparação de 30 indivíduos adultos com genótipo43 *28/*28 (associado à atividade reduzida da UGT1A1) com 27 indivíduos adultos com genótipo43 tipo selvagem, a razão média geométrica (IC 90%) da AUC29 foi de 1,41 (0,96; 2,09).
Farmacodinâmica
Microbiologia: o raltegravir em concentrações de 31 ± 20 nM resultou em inibição de 95% (CI95) da disseminação viral (em relação a uma cultura não tratada infectada por vírus19) em culturas de células12 linfoides44 T humanas infectadas com a linhagem de célula28 adaptada HIV8-1, variante H9IIIB. Além disso, o raltegravir em concentrações de 6 a 50 nM resultou em inibição de 95% da disseminação viral em culturas de células12 mononucleares de sangue45 periférico humano ativadas por mitógeno infectadas por isolados clínicos primários diversos de HIV8-1, incluindo isolados de 5 subtipos não B, e isolados resistentes a inibidores da transcriptase reversa e a inibidores da protease46. Em um ensaio de infecção7 de ciclo único, o raltegravir inibiu a infecção7 de 23 isolados de HIV8 representando 5 subtipos não B e 5 formas recombinantes circulantes com valores CI50, variando de 5 a 12 nM. O raltegravir também inibiu a replicação de um isolado de HIV8-2 quando avaliado em células12 CEMx174 (CI95 = 6 nM). Foi observada atividade antirretroviral aditiva à sinérgica quando células12 linfoides44 T humanas infectadas com H9IIIB variante do HIV8-1 foram incubadas com o raltegravir em combinação com inibidores nucleosídeos análogos da transcriptase reversa (zidovudina, zalcitabina, estavudina, abacavir, fumarato de tenofovir desoproxila, didanosina ou lamivudina); inibidores não nucleosídeos da transcriptase reversa (efavirenz, nevirapina ou delavirdina); inibidores da protease46 (indinavir, saquinavir, ritonavir, amprenavir, lopinavir, nelfinavir ou atazanavir); ou com o inibidor de entrada do HIV8 em células12 (enfuvirtida).
Resistência ao Medicamento: as mutações observadas na HIV8-1 integrase que contribuíram para a resistência ao raltegravir (desenvolvida tanto in vitro como em pacientes tratados com o raltegravir) geralmente incluíram substituição tanto em Y143 (alterado para C, H, ou R) ou Q148 (alterado para H, K, ou R) como em N155 (alterado para H) acrescida de uma ou mais mutações adicionais (p.ex., L74I/M, E92Q, E138A/K, G140A/S ou V151I). A substituição aminoácida no Y143C/H/R é outra via de resistência ao raltegravir.
Os vírus19 recombinantes com uma única mutação47 primária (Q148H, K ou R, ou N155H) apresentaram capacidade de replicação e sensibilidade reduzidas ao raltegravir in vitro. As mutações secundárias diminuem ainda mais a sensibilidade ao raltegravir e algumas vezes agiram como mutações compensatórias para capacidade de replicação viral.
As mutações que conferem resistência ao raltegravir geralmente também conferem resistência ao elvitegravir, inibidor da transferência de cadeia da integrase. As mutações no aminoácido 143 conferem uma maior resistência ao raltegravir que ao elvitegravir, e a mutação47 E92Q confere uma maior resistência ao elvitegravir do que ao raltegravir. Vírus19 com mutação47 no aminoácido 148, juntamente com uma ou mais outras mutações de resistência ao raltegravir, também podem ter resistência clinicamente significativa ao dolutegravir.
Eletrofisiologia Cardíaca: em um estudo randômico, controlado com placebo9 e cruzado, 31 indivíduos saudáveis receberam uma dose única oral supraterapêutica de 1.600 mg de raltegravir e placebo9. Não houve efeito sobre o intervalo QTc. Os picos das concentrações plasmáticas de raltegravir foram aproximadamente 4 vezes mais altos dos que os picos das concentrações após uma dose de 400 mg.
CONTRAINDICAÇÕES
Isentress® é contraindicado para pacientes16 com hipersensibilidade conhecida a qualquer componente deste medicamento.
ADVERTÊNCIAS E PRECAUÇÕES
Gravidez48 e Lactação49
Os estudos de toxicidade50 ao desenvolvimento foram realizados em coelhos (em doses de até 1.000 mg/kg/dia) e ratos (em doses de até 600 mg/kg/dia). As doses mais altas nestes estudos produziram exposições sistêmicas nessas espécies aproximadamente 3 a 4 vezes acima da exposição à dose recomendada para humanos. Não foram observadas alterações externas, viscerais ou esqueléticas relacionadas ao tratamento em coelhos. Foram observados aumentos relacionados ao tratamento em relação aos controles na incidência51 de costelas52 supranumerárias em ratos na dose de 600 mg/kg/dia (exposições 4,4 vezes acima da exposição à dose humana recomendada). Tanto em coelhos como em ratos, não foram observados efeitos relacionados ao tratamento na sobrevida53 embriofetal ou no peso dos fetos.
Em ratos, a dose administrada a fêmeas prenhes foi de 600 mg/kg/dia, e as concentrações plasmáticas médias do fármaco10 no plasma32 de fetos foram aproximadamente 1,5 a 2,5 vezes maiores que no plasma32 materno 1 hora e 24 horas pós-dose, respectivamente. Em coelhos, uma dose de 1.000 mg/kg/dia foi administrada a fêmeas prenhes, e as concentrações médias do fármaco10 no plasma32 fetal foram aproximadamente 2% da concentração materna média tanto 1 como 24 horas após a dose. Estudos toxicocinéticos demonstraram transferência placentária do fármaco10 em ambas as espécies.
Registro de uso de Antirretrovirais na Gravidez48
Com a finalidade de monitorar os resultados materno-fetais de pacientes grávidas expostas ao Isentress®, foi criado um Registro Internacional de uso de Antirretrovirais na Gravidez48 e pode ser acessado por meio eletrônico em www.apregistry.com.
Dados do Registro de uso de Antirretrovirais na Gravidez48 (RAG): baseados em relatórios restropectivos do RAG de um total de 644 relatos prospectivos de gravidez48, dos quais 312 foram exposições no primeiro trimestre, não houve diferença entre o risco geral de nascimentos com defeitos para raltegravir comparado com a taxa de fundo de 2,7% nos Estados Unidos da população de referência do Programa de Defeitos Congênitos54 de Atlanta (Metropolitan Atlanta Congenital Defects Program – MACDP).
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Lactação49: não se sabe se o raltegravir é secretado no leite humano; no entanto, o raltegravir é secretado no leite de ratas lactantes55. Em ratas que receberam doses de 600 mg/kg/dia, as concentrações médias do fármaco10 no leite foram aproximadamente 3 vezes maiores do que no plasma32 materno. A amamentação56 não é recomendada durante o tratamento com Isentress®. Além disso, recomenda-se que mães infectadas pelo HIV8 não amamentem seus bebês57 para evitar o risco de transmissão pós-natal do HIV8.
Reações Cutâneas58 e de Hipersensibilidade Graves
Foram relatadas reações cutâneas58 graves, potencialmente fatais e fatais em pacientes usando Isentress® concomitantemente com outros medicamentos associados a essas reações. Essas reações incluem casos de síndrome de Stevens-Johnson59 e necrólise epidérmica tóxica60.
Reações de hipersensibilidade também foram relatadas e foram caracterizadas por erupção61 cutânea62, achados constitucionais e, algumas vezes, disfunção orgânica, incluindo insuficiência hepática38. Interromper o tratamento com Isentress® e outros agentes suspeitos imediatamente se sinais63 ou sintomas64 de reações cutâneas58 ou de hipersensibilidade graves se desenvolverem (incluindo, porém não se limitando a, erupção61 cutânea62 grave ou erupção61 cutânea62 acompanhada de febre65, mal-estar geral, fadiga66, dores musculares ou articulares, bolhas, lesões67 orais, conjuntivite68, edema69 facial, hepatite13, eosinofilia70, angioedema71). O status clínico, incluindo as aminotransferases hepáticas72, deve ser monitorado e deve-se iniciar o tratamento apropriado. Postergar a interrupção do tratamento com Isentress® ou outros agentes suspeitos após o início da erupção61 cutânea62 grave pode resultar em uma reação potencialmente fatal.
Interações Medicamentosas
Deve-se ter cuidado ao se coadministrar Isentress® com fortes indutores da uridina difosfato glicuronosiltransferase (UGT) 1A1 (p.ex., rifampicina) em razão da redução de concentração plasmática do raltegravir (veja 6. INTERAÇÕES MEDICAMENTOSAS).
Síndrome73 de Reconstituição Imunológica: durante a fase inicial do tratamento, os pacientes que respondem ao tratamento antirretroviral podem desenvolver resposta inflamatória a infecções74 oportunistas indolentes ou residuais (como Mycobacterium avium complexo, citomegalovírus75, pneumonia76 por Pneumocystis jiroveci e tuberculose77 ou reativação do vírus19 da varicela78-zóster), que podem precisar de avaliação e tratamento adicionais.
Distúrbios autoimunes79 (como doença de Graves) também têm sido reportados no contexto da reconstituição imunológica; porém, o tempo relatado para o início da reação é variável e tais eventos podem ocorrer muitos meses após o início do tratamento.
Uso Pediátrico: a segurança, a tolerabilidade, o perfil farmacocinético e a eficácia de Isentress® foram avaliados em criança e adolescentes infectados pelo HIV8-1 com 2 a 18 anos de idade em um estudo clínico aberto e multicêntrico, o IMPAACT P1066 utilizando os comprimidos de 400 mg e os comprimidos mastigáveis (veja 3. CARACTERÍSTICAS FARMACOLÓGICAS, Características em Pacientes e 2. RESULTADOS DE EFICÁCIA). O perfil de segurança foi comparável ao observado em adultos (veja 9. REAÇÕES ADVERSAS). Veja 8. POSOLOGIA E MODO DE USAR para recomendações posológicas para crianças com 2 anos de idade ou mais.
Uso em Idosos: estudos clínicos com Isentress® não incluíram número suficiente de pacientes com 65 anos ou mais para determinar se eles respondem de forma diferente de pacientes mais jovens. Outras experiências clínicas relatadas não identificaram diferença de resposta entre pacientes idosos e jovens. Em geral, a seleção da dose para um paciente idoso deve ser feita com cautela, refletindo a frequência mais alta de insuficiência hepática38, renal41 ou cardíaca e de doenças concomitantes ou outros tratamentos medicamentosos.
Atenção: o uso incorreto causa resistência do vírus19 da AIDS e falha no tratamento.
Informações importantes sobre um dos componentes do medicamento
Atenção fenilcetonúricos80: contém FENILALANINA81.
Isentress® comprimidos mastigáveis contém fenilalanina81, um componente do aspartame5. Cada comprimido de 100 mg de Isentress® contém cerca de 0,10 mg de fenilalanina81. A fenilalanina81 pode ser perigosa para pacientes16 portadores de fenilcetonúria82.
INTERAÇÕES MEDICAMENTOSAS
O raltegravir não é um substrato das enzimas do citocromo P450 (CYP) e não inibe (CI50 > 100 µM) a CYP1A2, a CYP2B6, a CYP2C8, a CYP2C9, a CYP2C19, a CYP2D6 ou a CYP3A in vitro. Além disso, o raltegravir não induziu a CYP3A4 in vitro. Um estudo de interação medicamentosa com midazolam confirmou a baixa propensão do raltegravir para alterar a farmacocinética dos agentes metabolizados pela CYP3A4 in vivo pela demonstração da ausência de efeito significativo do raltegravir sobre a farmacocinética do midazolam, um substrato sensível à CYP3A4.
Da mesma maneira, o raltegravir não é um inibidor (CI50 > 50 µM) das UDP-glicuronosiltransferases (UGTs) avaliadas (UGT1A1, UGT2B7) e não inibe o transporte mediado pela glicoproteína-P. Com base nesses dados, não se espera que Isentress® afete a farmacocinética dos medicamentos substratos dessas enzimas ou da glicoproteína-P (p.ex., inibidores da protease46, ITRNNs, metadona, analgésicos83 opioides, vastatinas, antifúngicos azois, inibidores da bomba de prótons, e agente[s] para o tratamento da disfunção erétil).
Com base nos estudos in vivo e in vitro, o raltegravir é eliminado principalmente pelo metabolismo33 via glicuronidação mediada pela UGT1A1.
A coadministração de Isentress® com medicamentos que são potentes indutores da UGT1A1, como a rifampicina (indutor de várias enzimas metabolizantes de fármacos), reduz as concentrações plasmáticas de Isentress®. Deve-se ter cuidado ao se coadministrar Isentress® com rifampicina ou outros fortes indutores da UGT1A1 (veja 5. ADVERTÊNCIAS E PRECAUÇÕES). O impacto de outros potentes indutores de enzimas metabolizadoras de fármacos, como fenitoína e fenobarbital, sobre a UGT1A1 é desconhecido. Outros indutores menos potentes (p.ex., efavirenz, nevirapina, rifabutina, glicocorticoides, erva-de-são-joão, pioglitazona) podem ser utilizados com a dose recomendada de Isentress®.
A coadministração de Isentress® com medicamentos conhecidos por serem potentes indutores da UGT1A1 (p.ex., atazanavir) aumenta os níveis plasmáticos de Isentress®. No entanto, o aumento é discreto e o tratamento combinado com esses inibidores foi bem-tolerado nos estudos clínicos, de forma que nenhum ajuste de dose é necessário.
A coadministração de Isentress® com antiácidos84 contendo cátions metálicos bivalentes podem reduzir a absorção de raltegravir por quelação, resultando em queda dos níveis de raltegravir no plasma32. A administração de um antiácido85 contendo alumínio e magnésio 6 horas antes da administração de Isentress® reduziu significativamente os níveis de raltegravir no plasma32. Portanto, não é recomendada a coadministração de Isentress® com antiácidos84 contendo alumínio e/ou magnésio. A coadministração de Isentress® com um antiácido85 de carbonato de cálcio reduziu os níveis de raltegravir no plasma32; porém, essa interação não é considerada clinicamente significativa. Assim sendo, quando Isentress® é coadministrado com antiácidos84 contendo carbonato de cálcio, não há recomendação de ajuste da dose.
A coadministração de Isentress® com medicamentos conhecidos por aumentarem o pH gástrico (p.ex., omeprazol) pode aumentar os níveis plasmáticos de Isentress® com base no aumento da solubilidade de Isentress® em pH mais alto. Em indivíduos que receberam Isentress® em combinação com inibidores da bomba de prótons ou bloqueadores de H2 nos Protocolos 018 e 019, foram observados perfis de segurança comparáveis neste subgrupo em relação a indivíduos não recebendo inibidores da bomba de prótons ou bloqueadores da H2. Com base nesses dados, os inibidores da bomba de prótons ou bloqueadores da H2 podem ser coadministrados com Isentress® sem ajuste de dose.
Efeito do Raltegravir sobre a Farmacocinética de Outros Agentes: nos estudos de interação medicamentosa, o raltegravir não apresentou efeitos clinicamente significativos sobre a farmacocinética de contraceptivos hormonais, metadona, fumarato de tenofovir desoproxila, midazolam, lamivudina, etravirina, darunavir/ritonavir e boceprevir. Em um estudo de interação medicamentosa de doses múltiplas, os valores de AUC29 de etinilestradiol e de norelgestromina foram de 98% e 114%, respectivamente, quando coadministrados com raltegravir em comparação com quando administrados sem raltegravir. Em um estudo de interação medicamentosa de doses múltiplas, a AUC29 e as concentrações de vale do fumarato de tenofovir desoproxila coadministrado com o raltegravir foram de 90% e 87% dos valores obtidos com a monoterapia com o fumarato de tenofovir desoproxila. Em outro estudo de interação medicamentosa, a AUC29 do midazolam coadministrado foi 92% do valor obtido com o midazolam isoladamente. Em um estudo fase II, a farmacocinética da lamivudina foi semelhante em pacientes que receberam combinações com raltegravir versus com efavirenz.
Efeito de Outros Agentes sobre a Farmacocinética do Raltegravir: nos estudos de interação medicamentosa, atazanavir, efavirenz, ritonavir, fumarato de tenofovir desoproxila e tipranavir/ritonavir não apresentaram efeito clinicamente significativo sobre a farmacocinética do raltegravir. A rifampicina, forte indutora das enzimas metabolizadoras de medicamentos, causou redução dos níveis de vale do raltegravir. Antiácido85 com alumínio e magnésio reduziu significativamente os níveis de raltegravir no plasma32. Não é recomendada a coadministração de Isentress® com antiácidos84 contendo alumínio e/ou magnésio. Todos os estudos de interação foram realizados em adultos. As interações medicamentosas encontram-se descritas adicionalmente na Tabela 8.
Tabela 8. Efeito de Outros Agentes sobre a Farmacocinética do Raltegravir
|
Fármaco10 Coadministrado |
Dose/Esquema do Fármaco10 Coadministrado |
Dose/Esquema do Raltegravir |
Razão (IC 90%) dos Parâmetros Farmacocinéticos do Raltegravir Com/Sem Fármaco10 Coadministrado; |
|||
|
n |
Cmáx |
AUC29 |
Cmín |
|||
|
antiácido85 com hidróxido de alumínio e magnésio |
20 mL dose única com raltegravir |
400 mg 2x/dia |
25 |
0,56 |
0,51 |
0,37 |
|
20 mL dose única 2 horas antes de raltegravir |
23 |
0,49 |
0,49 |
0,44 |
||
|
20 mL dose única 2 horas depois de raltegravir |
23 |
0,78 |
0,70 |
0,43 |
||
|
20 mL dose única 6 horas antes de raltegravir |
16 |
0,90 |
0,87 |
0,50 |
||
|
20 mL dose única 6 horas depois de raltegravir |
|
16 |
0,90 |
0,89 |
0,51 |
|
|
atazanavir |
400 mg/dia |
100 mg dose única |
10 |
1,53 |
1,72 |
1,95 |
|
atazanavir/ritonavir |
300 mg/100 mg/dia |
400 mg 2x/dia |
10 |
1,24 |
1,41 |
1,77 |
|
boceprevir |
800 mg 3x/dia |
400 mg dose única |
22 |
1,11 |
1,04 |
0,75 |
|
antiácido85 de carbonato |
3.000 mg dose |
400 mg 2x/dia |
24 |
0,48 |
0,45 |
0,68 |
|
darunavir/ritonavir |
600 mg/100 |
400 mg 2x/dia |
6 |
0,67 |
0,71 |
1,38 |
|
efavirenz |
600 mg/dia |
400 mg dose única |
9 |
0,64 |
0,64 |
0,79 |
|
etravirina |
200 mg 2x/dia |
400 mg 2x/dia |
19 |
0,89 |
0,90 |
0,66 |
|
omeprazol |
20 mg/dia |
400 mg dose única |
14 (10 para AUC29) |
4,15 |
3,12 |
1,46 |
|
rifampicina |
600 mg/dia |
400 mg dose única |
9 |
0,62 |
0,60 |
0,39 |
|
rifampicina |
600 mg/dia |
800 mg 2x/dia |
14 |
1,62* |
1,27* |
0,47* |
|
ritonavir |
100 mg 2x/dia |
400 mg dose única |
10 |
0,76 |
0,84 |
0,99 |
|
fumarato de tenofovir desoproxila |
300 mg/dia |
400 mg 2x/dia |
9 |
1,64 |
1,49 |
1,03 |
|
tipranavir/ritonavir |
500 mg/200 mg 2x/dia |
400 mg 2x/dia |
15 (14 para Cmín) |
0,82 |
0,76 |
0,45 |
|
*Comparado com 400 mg 2x/dia administrados isoladamente. |
||||||
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar o frasco fechado em temperatura ambiente (15–30°C).
Comprimidos Mastigáveis: Conserve na embalagem original com o frasco fechado. Mantenha o dessecante no frasco para proteger da umidade.
Prazo de validade: 24 meses após a data de fabricação impressa na embalagem. Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
- Isentress® 400 mg comprimidos revestidos é um comprimido rosa, oval, biconvexo, com a gravação “227” em um lado e plano de outro.
- Isentress® 100 mg comprimidos mastigáveis é um comprimido laranja claro, oval, sulcado, com a gravação "477" e o logo da empresa.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Isentress® está disponível como uma formulação de comprimidos de 400 mg e uma formulação de comprimidos mastigáveis nas concentrações de 100 mg (sulcado).
Como as formulações não são bioequivalentes, não substitua os comprimidos mastigáveis pelo comprimido de 400 mg.
A dose máxima do comprimido mastigável é de 300 mg 2x/dia.
Isentress® pode ser administrado com ou sem alimentos.
Isentress® deve ser administrado em um regime de combinação com outros agentes antirretrovirais. Para o tratamento de pacientes com infecção7 por HIV8-1, a posologia de Isentress® é a seguinte:
Posologia
Adultos: um comprimido de 400 mg duas vezes ao dia, por via oral.
Crianças e Adolescentes:
- 12 anos de idade ou mais (com pelo menos 25 kg): um comprimido de 400 mg duas vezes ao dia, por via oral.
- 6 a 11 anos de idade (2 opções posológicas):
- um comprimido de 400 mg duas vezes ao dia, por via oral (se tiver pelo menos 25 kg de peso); OU
- comprimidos mastigáveis: peso baseado na dose máxima de 300 mg, duas vezes ao dia, conforme especificado na Tabela 9.
- 2 a 5 anos anos de idade:
- comprimidos mastigáveis: peso baseado na dose máxima de 300 mg, duas vezes ao dia, conforme especificado na Tabela 9.
Tabela 9. Dose Recomendada* para Comprimidos Mastigáveis de Isentress® em Pacientes Pediátricos 2 a 11 Anos de Idade
|
Peso Corporal |
Dose |
Número de Comprimidos Mastigáveis por dose |
|
14 a < 20 |
100 mg 2x/dia |
1 x 100 mg 2x/dia |
|
20 a < 28 |
150 mg 2x/dia |
1,5 x 100 mg† 2x/dia |
|
28 a < 40 |
200 mg 2x/dia |
2 x 100 mg 2x/dia |
|
Pelo menos 40 |
300 mg 2x/dia |
3 x 100 mg 2x/dia |
|
*A recomendação de administração baseada no peso para o comprimido mastigável é baseada em aproximadamente 6 mg/kg/dose 2x/dia. |
||
|
† O comprimido mastigável de 100 mg pode ser dividido em metades iguais. |
||
Comprimido de 400 mg: este medicamento não deve ser partido, aberto ou mastigado.
REAÇÕES ADVERSAS
Adultos
Reações Adversas Em Pacientes Já Tratados
A avaliação da segurança de Isentress® baseou-se nos relatos de eventos adversos em pacientes já tratados desde os estudos clínicos randômicos P018 e P019 nos quais foi utilizada a dose recomendada de Isentress®, 400 mg 2x/dia, em combinação com a Terapia Otimizada de Base (OBT) em 462 pacientes, em comparação com 237 pacientes que receberam placebo9 em combinação com OBT. Durante o tratamento duplo-cego, o acompanhamento total foi de 1.051 pacientes-anos do grupo recebendo Isentress® 400 mg 2x/dia e 322 pacientes-anos do grupo recebendo placebo9.
Entre os pacientes do grupo de tratamento com Isentress® 400 mg 2x/dia + OBT (acompanhamento médio de 118,7 semanas) e do grupo para comparação, no qual foi administrado placebo9 + OBT (acompanhamento médio de 71,0 semanas), na análise agrupada para os estudos P018 e P019, os eventos adversos clínicos mais comumente relatados (> 10% em qualquer um dos grupos) de todas as intensidades e independentemente da causalidade foram: diarreia86 em 26,6% e 24,9%; náuseas87 em 13,6% e 16,0%; cefaleia88 em 12,1% e 13,5%; nasofaringite em 14,3% e 8,9%; fadiga66 em 12,1% e 5,9%; infecção7 do trato respiratório superior em 15,8% e 10,1%; bronquite em 12,1% e 6,8%; pirexia89 em 9,7% e 13,9%; e vômitos90 em 8,9% e 11,0% dos pacientes, respectivamente. Nessa análise agrupada, a taxa de descontinuação do tratamento em razão de eventos adversos (clínicos e laboratoriais) foi de 4,5% entre os pacientes que receberam Isentress® + OBT e de 5,5% entre os pacientes que receberam placebo9 + OBT.
Eventos Adversos Relacionados ao Medicamento
Os eventos adversos clínicos listados abaixo foram considerados moderados a graves pelos pesquisadores. A causa de tais eventos pode ser atribuída a Isentress® ou placebo9 apenas ou em combinação com OBT.
Os eventos adversos de intensidade moderada a grave relacionados ao medicamento que ocorreram em ≥ 2% dos pacientes adultos que já receberam tratamento em qualquer um dos grupos de tratamento são apresentados na Tabela 10.
Tabela 10. Porcentagem de Pacientes com Eventos Adversos de Intensidade Moderada a Grave e Relacionados ao Medicamento que ocorreram em ≥ 2% dos Pacientes Adultos Já Tratados em Qualquer Grupo de Tratamento
|
Classe de Órgão Sistêmico91 |
Estudos Randômicos P018 e P019 |
|
|
|
Isentress® 400 mg 2x/dia |
Placebo9 |
|
|
Acompanhamento Médio |
Acompanhamento Médio |
|
Distúrbios Gastrintestinais |
||
|
Diarreia86 |
1,5 |
2,1 |
|
Distúrbios do Sistema Nervoso92 |
||
|
Cefaleia88 |
2,2% |
0,4% |
|
* Inclui eventos adversos possível, provável ou muito provavelmente relacionados ao medicamento. **N = número total de pacientes por grupo de tratamento. |
||
Os eventos adversos clínicos moderados a graves relacionados ao medicamento, que ocorreram em menos de 2% dos pacientes já tratados (n = 462) e que haviam recebido Isentress® + OBT são listados abaixo, por classe de órgão sistêmico91.
[Comuns (≥ 1/100, < 1/10), Incomuns (≥ 1/1.000, < 1/100)]
Distúrbios Cardíacos: Incomum: extrassístoles ventriculares.
Distúrbios de Ouvido e Labirinto93: Incomum: vertigem94.
Distúrbios Oculares: Incomuns: comprometimento visual.
Distúrbios Gastrintestinais: Comum: diarreia86, náuseas87. Incomuns: dor abdominal, distensão abdominal, dor abdominal alta, vômitos90, constipação95, desconforto abdominal, dispepsia96, flatulência, gastrite97, doença de refluxo gastroesofágico98, boca99 seca, eructação100.
Distúrbios Gerais e Condições no Local da Administração: Comuns: astenia101, fadiga66. Incomuns: pirexia89, calafrios102, edema69 de face103, edema69 periférico.
Distúrbios Hepatobiliares104: Incomum: hepatite13.
Distúrbios do Sistema Imunológico105: Incomum: hipersensibilidade ao medicamento.
Infecções74 e Infestações: Incomuns: herpes simples, herpes genital, gastrenterite.
Investigação: Incomuns: aumento de peso, redução de peso.
Distúrbios Metabólicos e Nutricionais: Incomuns: diabetes106 mellitus, dislipidemia, aumento do apetite, redução do apetite.
Distúrbios Musculoesqueléticos e do Tecido Conjuntivo107: Incomuns: artralgia108, mialgia109, lombalgia110, dor musculoesquelética, osteoporose111, poliartrite.
Distúrbios do Sistema Nervoso92: Incomuns: tontura112, neuropatia periférica113, parestesia114, sonolência, cefaleia88 tensional, tremor.
Distúrbios Psiquiátricos: Incomuns: depressão, insônia, ansiedade.
Distúrbios Renais e Urinários: Incomuns: nefrite115, nefrolitíase, noctúria, insuficiência renal40, nefrite115 tubulointersticial.
Distúrbios do Sistema Reprodutivo e da Mama116: Incomuns: ginecomastia117.
Distúrbios Respiratórios, Torácicos e do Mediastino118: Incomuns: epistaxe119
Distúrbios da Pele120 e do Tecido Subcutâneo121: Incomuns: lipodistrofia122 adquirida, erupção61 cutânea62, hiper-hidrose, dermatite123 acneiforme, eritema124, lipo-hipertrofia125, sudorese126 noturna, erupção61 cutânea62 macular, erupção61 cutânea62 maculopapular127, erupção61 cutânea62 prurítica, xerodermia, prurigo, lipoatrofia128, prurido129.
Eventos Graves
Relacionados ao Medicamento: nos estudos clínicos foram relatados os seguintes eventos adversos clínicos graves relacionados ao medicamento: gastrite97, hepatite13, insuficiência renal40, herpes genital, superdosagem acidental.
Eventos adversos em pacientes nunca tratados anteriormente
A avaliação a seguir da segurança de Isentress® em pacientes nunca expostos a tratamento é baseada no estudo randômico, duplo-cego, controlado com agente ativo de pacientes nunca tratados anteriormente, Protocolo 021 (STARTMRK) com Isentress® 400 mg 2x/dia em combinação com uma dose fixa de entricitabina 200 mg (+) fumarato de tenofovir desoproxila 245 mg, (N = 281) versus efavirenz (EFV) 600 mg à noite antes de dormir em combinação com entricitabina (+) fumarato de tenofovir desoproxila (N = 282). Durante o tratamento duplo-cego, o acompanhamento total para pacientes16 com Isentress® 400 mg 2x/dia + entricitabina (+) fumarato de tenofovir desoproxila foi de 1.104 pacientes-anos e 1.036 pacientes-anos para pacientes16 com efavirenz 600 mg à noite antes de dormir + entricitabina (+) fumarato de tenofovir desoproxila.
Os números (%) de pacientes com eventos adversos clínicos e com eventos adversos relacionados ao medicamento no grupo recebendo Isentress® foram menos frequentes que no grupo recebendo efavirenz com base nos valores de P nominais (0,325 e < 0,001, respectivamente). Neste estudo, as taxas de descontinuação da terapia devido a eventos adversos (clínicos e laboratoriais) foram de 5,0% em pacientes recebendo Isentress® + entricitabina (+) fumarato de tenofovir desoproxila e 10,0% em pacientes recebendo efavirenz + entricitabina (+) fumarato de tenofovir desoproxila.
Para pacientes16 do grupo recebendo Isentress® 400 mg 2x/dia + entricitabina (+) fumarato de tenofovir desoproxila e do grupo recebendo o agente comparador, efavirenz 600 mg à noite antes de dormir + entricitabina (+) fumarato de tenofovir desoproxila , os eventos adversos clínicos mais comumente relatados (> 10% em qualquer grupo), de todas as intensidades e independentemente da relação causal são mostrados na Tabela 11.
Tabela 11. Porcentagem de Indivíduos com os Eventos Adversos Mais Comumente Relatados (> 10%) de Todas as Intensidades e Independentemente da Relação Causal Ocorrendo em Pacientes Adultos Nunca Expostos a Tratamento em Qualquer Grupo de Tratamento
|
Classe de Sistema Orgânico, Eventos Adversos |
Estudo Randômico P021 |
|
|
Isentress® 400 mg |
Efavirenz 600 mg |
|
|
Distúrbios Gastrintestinais |
||
|
Diarreia86 |
25,6 |
27,0 |
|
Náusea130 |
16,7 |
14,5 |
|
Vômitos90 |
8,2 |
10,6 |
|
Distúrbios Gerais e Condições no Local de Administração |
||
|
Fadiga66 |
9,3 |
13,5 |
|
Pirexia89 |
15,7 |
13,8 |
|
Infecções74 e Infestações |
||
|
Influenza131 |
11,7 |
13,5 |
|
Nasofaringite |
26,7 |
22,3 |
|
Infecção7 do trato respiratório superior |
21,4 |
20,2 |
|
Distúrbios Musculoesqueléticos e do Tecido Conjuntivo107 |
||
|
Artralgia108 |
8,5 |
11,7 |
|
Lombalgia110 |
12,1 |
9,9 |
|
Distúrbios do Sistema Nervoso92 |
||
|
Tontura112 |
16,4 |
38,3 |
|
Cefaleia88 |
26,0 |
28,4 |
|
Distúrbios Psiquiátricos |
||
|
Sonhos anormais |
8,2 |
13,1 |
|
Ansiedade |
8,9 |
11,0 |
|
Depressão |
10,3 |
11,7 |
|
Insônia |
15,7 |
14,9 |
|
Distúrbios Respiratórios, Torácicos e do Mediastino118 |
||
|
Tosse |
16,7 |
12,1 |
|
Distúrbios da Pele120 e do Tecido Subcutâneo121 |
||
|
Erupção61 cutânea62 |
7,8 |
13,8 |
|
*As intensidades são definidas a seguir: leve (consciência do sinal132 ou sintoma133, mas facilmente tolerada); moderada (desconforto suficiente para causar interferência nas atividades usuais); grave (incapacitante com incapacidade de trabalhar ou realizar as atividades usuais). †n = número total de indivíduos por grupo de tratamento. |
||
Eventos do Sistema Nervoso Central134 (SNC135)
Em pacientes nunca expostos a tratamento (P021) os eventos adversos do sistema nervoso central134 (SNC135), conforme medido pela proporção de pacientes com 1 ou mais sintomas64 do SNC135 (descritos abaixo), foram relatados significativamente com menos frequência no grupo de Isentress® + entricitabina (+) fumarato de tenofovir desoproxila em comparação com o grupo efavirenz + entricitabina (+) fumarato de tenofovir desoproxila , valores de P < 0,001 , < 0,001 e < 0,001 para eventos cumulativos até as Semanas 8, 48 e 96, respectivamente. No grupo Isentress®, a porcentagem de pacientes com 1 ou mais sintomas64 do SNC135 foi de 20,3% em comparação com 52,1% no grupo de efavirenz na Semana 8, e 26,3% em comparação com 58,5% na Semana 48, e 28,8% em comparação com 60,6% na Semana 96. Os eventos adversos do SNC135 para esta análise foram tontura112, insônia, dificuldade de concentração, sonolência, depressão, pesadelos, estado confusional, ideias suicidas, distúrbio do sistema nervoso92, distúrbio psicótico, sonhos anormais, tentativa de suicídio, psicose136 aguda, delírio137, nível de consciência deprimido, alucinação138, alucinação138 auditiva, consumação de suicídio e depressão maior.
Eventos Adversos Relacionados ao Medicamento
As reações adversas clínicas listadas abaixo foram consideradas pelos investigadores como sendo de intensidade moderada a grave e a relação causal com Isentress®/efavirenz apenas ou em combinação com entricitabina (+) fumarato de tenofovir desoproxila.
As reações adversas clínicas relacionadas ao medicamento de intensidade moderada a grave ocorrendo em ≥ 2% dos pacientes adultos nunca tratados anteriormente com qualquer grupo de tratamento são apresentadas na Tabela 12.
Tabela 12. Porcentagem de Pacientes com Eventos Adversos Relacionados ao Medicamento de Intensidade Moderada a Grave Ocorrendo em ≥ 2% dos Pacientes Adultos Nunca Tratados Anteriormente em Qualquer Grupo de Tratamento
|
Classe de Sistema Orgânico, Termo Preferido |
Estudo Randômico P021 |
|
|
|
Isentress® 400 mg 2x/dia + Entricitabina (+) fumarato de tenofovir desoproxila |
Efavirenz 600 mg |
|
Distúrbios Gastrintestinais |
||
|
Diarreia86 |
1,1 |
2,8 |
|
Náusea130 |
2,8 |
3,5 |
|
Distúrbios Gerais e Condições no Local da Administração |
||
|
Fadiga66 |
1,8 |
2,8 |
|
Distúrbios do Sistema Nervoso92 |
||
|
Tontura112 |
1,8 |
6,4 |
|
Cefaleia88 |
3,9 |
5,0 |
|
Distúrbios Psiquiátricos |
||
|
Insônia |
3,6 |
3,9 |
|
Distúrbios da Pele120 e do Tecido Subcutâneo121 |
||
|
Erupção61 Cutânea62 |
0,0 |
2,8 |
|
Erupção61 Cutânea62 Maculopapular127 |
0,0 |
2,5 |
|
* Inclui eventos adversos pelo menos possível, provável, ou muito provavelmente relacionados ao medicamento |
||
Os eventos adversos clínicos relacionados ao medicamento, que ocorreram em menos de 2% dos pacientes nunca tratados anteriormente (n = 281) que receberam Isentress® + entricitabina (+) fumarato de tenofovir desoproxila e de intensidade moderada a grave estão listados abaixo por Classe de Sistema Orgânico.
[Comuns (≥ 1/100, < 1/10), Incomuns (≥ 1/1.000, < 1/100)]
Distúrbios de Sangue45 e Sistema Linfático139: Incomuns: dor no linfonodo140, neutropenia141, anemia142, linfadenopatia.
Distúrbios de Ouvido e Labirinto93: Incomuns: tinido, vertigem94.
Distúrbios Gastrintestinais: Comuns: diarreia86, dor abdominal.
Incomuns: vômitos90, dor abdominal superior, dispepsia96, duodenite erosiva, doença de refluxo gastroesofágico98, distensão abdominal.
Distúrbios Gerais e Condições no Local da Administração: Comuns: fadiga66, astenia101. Incomuns: massa submandibular.
Distúrbios Hepatobiliares104: Incomum: hepatite13 alcoólica.
Distúrbios do Sistema Imune143: Incomum: síndrome73 de reconstituição imune.
Infecções74 e Infestações: Incomuns: herpes-zóster, gastroenterite144, foliculite, abscesso145 de linfonodo140.
Distúrbios Metabólicos e Nutricionais: Incomuns: redução do apetite, hipercolesterolemia146, alteração na distribuição de gordura147 corpórea.
Distúrbios Músculoesqueléticos e do Tecido Conjuntivo107: Incomuns: artrite148, dor no pescoço149.
Distúrbios do Sistema Nervoso92: Comum: tontura112. Incomuns: hipersonia, sonolência, comprometimento da memória.
Distúrbios Psiquiátricos: Comuns: anormalidade no padrão de sonhos, pesadelos, depressão. Incomuns: ansiedade, distúrbio mental, estado confusional, depressão maior, tentativa de suicídio.
Distúrbios Renais e Urinários: Comum: nefrolitíase.
Distúrbios do Sistema Reprodutivo e da Mama116: Incomum: disfunção erétil.
Distúrbios da Pele120 e do Tecido Subcutâneo121: Incomuns: acne150, alopecia151, lesão152 cutânea62, lipoatrofia128.
Eventos Graves
Os seguintes eventos adversos graves relacionados ao medicamento foram relatados no estudo clínico P021 em pacientes nunca tratados anteriormente que receberam Isentress® + entricitabina (+) fumarato de tenofovir desoproxila: anemia142, síndrome73 de reconstituição imunológica, distúrbio mental, tentativa de suicídio e depressão.
Eventos adversos selecionados adultos
Foram observados casos de câncer153 em pacientes já tratados anteriormente que iniciaram tratamento com Isentress® ou placebo9, ambos com OBT, e em pacientes nunca expostos ao tratamento que iniciaram tratamento com Isentress® ou efavirenz, ambos com entricitabina (+) fumarato de tenofovir desoproxila; vários eram recidivantes154. Os tipos e taxas de câncer153 específicos foram os esperados em uma população altamente imunodeficiente (muitos apresentavam contagens de CD4+ abaixo de 50 células12/mm3 e a maioria apresentava diagnóstico155 anterior de AIDS). O risco de desenvolvimento de câncer153 nesses estudos foi similar no grupo que recebeu Isentress® e no grupo que recebeu o agente comparador.
Foram observadas anormalidades laboratoriais de creatina quinase Graus 2–4 em indivíduos tratados com Isentress® (veja Tabela 5). Miopatia156 e rabdomiólise157 foram relatadas. Utilizar com cautela em pacientes com risco aumentado de miopatia156 ou rabdomiólise157, como pacientes recebendo medicamentos concomitantes conhecidos por causar essas condições.
Erupção61 cutânea62 ocorreu mais comumente em pacientes já tratados anteriormente recebendo regimes contendo Isentress® + darunavir em comparação com pacientes recebendo Isentress® sem darunavir ou darunavir sem Isentress®. No entanto, a erupção61 cutânea62 que foi relacionada ao medicamento ocorreu em taxas similares em todos os três grupos. Essas erupções cutâneas58 foram de gravidade leve a moderada e não limitaram a terapia; não houve nenhuma descontinuação devido a esses eventos. A erupção61 cutânea62 ocorreu menos comumente em pacientes nunca tratados anteriormente recebendo Isentress® em comparação com efavirenz, cada qual em combinação com entricitabina (+) fumarato de tenofovir desoproxila.
Pacientes com Condições Coexistentes
Pacientes Coinfectados pelo Vírus19 da Hepatite13 B e/ou Hepatite13 C
Nos estudos Fase III, os pacientes já tratados anteriormente (N = 114/699 ou 16%) e os pacientes nunca tratados anteriormente (N = 34/563 ou 6%) com coinfecção crônica (porém não aguda) ativa por hepatite13 B e/ou hepatite13 C poderiam ser admitidos desde que os testes de função hepática158 no período basal não tivessem excedido 5 vezes o limite superior do normal. Em geral, o perfil de segurança de Isentress® em pacientes com coinfecção por hepatite13 B e/ou hepatite13 C foi similar ao de pacientes sem coinfecção por hepatite13 B e/ou
hepatite13 C, embora as taxas de anormalidades de AST e ALT tenham sido um pouco maiores no subgrupo com coinfecção por hepatite13 B e/ou hepatite13 C para ambos os grupos de tratamento.
Eventos adversos pediátricos
2 a 18 Anos de Idade
Isentress® foi estudado em 126 crianças e adolescentes de 2 a 18 anos de idade infectados com HIV8-1 já tratados com antirretrovirais em combinação com outros antiretrovirais no IMPAACT P1066 (veja 5. ADVERTÊNCIAS E PRECAUÇÕES, Uso Pediátrico, 3. CARACTERÍSTICAS FARMACOLÓGICAS e 2. RESULTADOS DE EFICÁCIA). Dos 126 pacientes, 96 receberam a dose recomendada de Isentress®.
Nessas 96 crianças e adolescentes, a frequência, tipo e gravidade das reações adversas relacionadas ao medicamento até a 24ª semana foram comparáveis aos observados em adultos.
Um paciente apresentou reações adversas clínicas relacionadas ao medicamento de hiperatividade psicomotora159 Grau 3, comportamento anormal e insônia; um paciente apresentou uma erupção61 adversa grave Grau 2 relacionada ao medicamento.
Um paciente apresentou anormalidades laboratoriais relacionadas ao medicamento, AST Grau 4 e ALT Grau 3, as quais foram consideradas graves.
Experiência Pós-comercialização
Os seguintes eventos adversos adicionais foram relatados na experiência pós-comercialização independentemente da relação causal:
- Distúrbios de Sangue45 e Sistema Linfático139: trombocitopenia160.
- Distúrbios Hepatobiliares104: insuficiência hepática38 (com e sem hipersensibilidade associada) em pacientes com doença hepática158 subjacente e/ou medicações concomitantes.
- Distúrbios Musculoesqueléticos e do Tecido Conjuntivo107: rabdomiólise157.
- Distúrbios do Sistema Nervoso92: ataxia161 cerebelar.
- Distúrbios Psiquiátricos: depressão (particularmente em pacientes com histórico preexistente de doença psiquiátrica), incluindo ideias e comportamentos suicidas.
- Distúrbios da Pele120 e do Tecido Subcutâneo121: síndrome de Stevens-Johnson59, erupção61 cutânea62 com eosinofilia70 e sintomas64 sistêmicos162 (DRESS)
Achados de Exames Laboratoriais
Anormalidades Laboratoriais: nos estudos P018 e P019, as porcentagens de pacientes adultos já tratados anteriormente que receberam Isentress® 400 mg 2x/dia ou placebo9 (ambos com OBT) com anormalidades laboratoriais selecionadas, de Grau 2 a 4, que representam agravamento de Grau em relação ao período basal são apresentadas na Tabela 13.
Tabela 13. Anormalidades Laboratoriais Selecionadas, de Grau 2 a 4, em Pacientes Já Tratados
|
Parâmetro Laboratorial (Unidade) |
Limite |
Estudos Randômicos P005, P018 e P019 |
|
|
Isentress® 400 mg 2x/dia |
Placebo9 |
||
|
Bioquímica sanguínea |
|||
|
Exame de glicemia163 sérica de jejum (não aleatório) |
|||
|
Grau 2 |
126 – 250 |
11,3% |
7,5% |
|
Grau 3 |
251 – 500 |
2,9% |
1,3% |
|
Grau 4 |
> 500 |
0,0% |
0,0% |
|
Bilirrubina164 sérica total |
|||
|
Grau 2 |
1,6–2,5 x ULN |
5,6% |
3,0% |
|
Grau 3 |
2,6–5,0 x ULN |
3,0% |
2,5% |
|
Grau 4 |
>5,0 x ULN |
0,9% |
0,0% |
|
Aspartato aminotransferase sérica |
|||
|
Grau 2 |
2,6–5,0 x ULN |
9,5% |
8,5% |
|
Grau 3 |
5,1–10,0 x ULN |
4,3% |
3,0% |
|
Grau 4 |
>10,0 x ULN |
0,7% |
1,3% |
|
Alanina aminotransferase sérica |
|
|
|
|
Grau 2 |
2,6–5,0 x ULN |
10,8% |
9,7% |
|
Grau 3 |
5,1–10,0 x ULN |
4,8% |
2,5% |
|
Grau 4 |
>10,0 x ULN |
1,3% |
1,7% |
|
Fosfatase alcalina165 sérica |
|||
|
Grau 2 |
2,6–5,0 x ULN |
2,2% |
0,4% |
|
Grau 3 |
5,1–10,0 x ULN |
0,4% |
1,3% |
|
Grau 4 |
> 10,0 x ULN |
0,7% |
0,4% |
|
Creatina quinase sérica |
|||
|
Grau 2 |
6,0–9,9 x LSN |
2,6% |
2,1% |
|
Grau 3 |
10,0–19,9 x LSN |
4,1% |
2,5% |
|
Grau 4 |
≥ 20,0 x LSN |
3,0% |
1,3% |
LSN = limite superior ao intervalo normal
As porcentagens de pacientes adultos sem tratamento anterior recebendo tanto Isentress® 400 mg 2x/dia ou efavirenz (ambos com entricitabina (+) fumarato de tenofovir desoproxila), no estudo P021 com anormalidades laboratoriais selecionadas de Graus 2 a 4 que representam um pior grau do parâmetro inicial estão apresentados na Tabela 14.
Tabela 14. Anormalidades Laboratoriais Selecionadas de Graus 2 a 4 Relatadas em Pacientes Não Tratados Anteriormente
|
Parâmetro Laboratorial |
Limite |
Estudo Randômico P021 |
|
| Isentress® 400 mg 2x/dia + Entricitabina (+) fumarato de tenofovir esoproxila (N = 281) |
Efavirenz 600 mg |
||
|
Bioquímica sanguínea |
|||
|
Teste em jejum (não randômico) glicose166 sérica (mg/dL167) |
|||
|
Grau 2 |
126–250 |
6,6% |
6,0% |
|
Grau 3 |
251–500 |
1,8% |
0,8% |
|
Grau 4 |
> 500 |
0,0% |
0,0% |
|
Bilirrubina164 sérica total |
|||
|
Grau 2 |
1,6–2,5 x ULN |
4,6% |
0,4% |
|
Grau 3 |
2,6–5,0 x ULN |
0,7% |
0,0% |
|
Grau 4 |
> 5,0 x ULN |
0,4% |
0,0% |
|
Aspartato aminotransferase sérica |
|||
|
Grau 2 |
2,6–5,0 x ULN |
7,5% |
10,4% |
|
Grau 3 |
5,1–10,0 x ULN |
4,6% |
2,9% |
|
Grau 4 |
> 10,0 x ULN |
1,1% |
0,4% |
|
Alanina aminotransferase sérica |
|||
|
Grau 2 |
2,6–5,0 x ULN |
11,0% |
11,8% |
|
Grau 3 |
5,1–10,0 x ULN |
1,8% |
2,2% |
|
Grau 4 |
> 10,0 x ULN |
1,8% |
0,7% |
|
Fosfatase alcalina165 sérica |
|||
|
Grau 2 |
2,6–5,0 x ULN |
1,1% |
3,2% |
|
Grau 3 |
5,1–10,0 x ULN |
0,0% |
0,7% |
|
Grau 4 |
> 10,0 x ULN |
0,4% |
0,4% |
|
ULN = limite superior de faixa normal |
|||
Lipídios, alteração em relação ao período basal.
Para P021, alterações em relação ao período basal em testes de lipídios em jejum são mostradas na Tabela 15.
Tabela 15. Valores de Lipídios em P021, Alteração em Relação ao Período Basal em Lipídios Séricos na Semana 240
|
Parâmetro Laboratorial Termo Preferencial (Unidade) |
Isentress® |
Efavirenz |
||
|
|
Alteração em Relação ao Período Basal na Semana 240 |
|
Alteração em Relação ao Período Basal na Semana 240 |
|
|
Média Basal |
Variação Média (IC 95%)† |
Média Basal |
Variação Média (IC 95%)† |
|
|
Colesterol22 Total (mg/dL167)‡ |
158,8 |
16,0 (11,5, 20,6) |
157,1 |
44,0 (37,7, 50,4) |
|
Colesterol22 HDL23 (mg/dL167)‡ |
37,9 |
5,7 (4,3, 6,9) |
38,4 |
12,6 (10,9, 14,4) |
|
Colesterol22 LDL24 (mg/dL167)‡ |
96,2 |
9,92 (6,1, 13,8) |
92,5 |
25,4 (20,1, 30,7) |
|
Triglicérides25 (mg/dL167)‡ |
128,3 |
1,5 (-9,9, 13,0) |
140,6 |
37,3 (14,3, 60,2) |
|
Total: taxa HDL23-C |
4,4 |
-0,2 (-0,4, -0,1) |
4,4 |
0,1 (-0,3, 0,2) |
|
Não HDL23-C (mg/dL167) |
121,0 |
10,3 (6,13, 14,6) |
118,7 |
31,4 (25,1, 37,7) |
|
†Os ICs 95% intragrupos foram baseados na distribuição t. ‡Testes laboratoriais em jejum (não randômico) na 240ª semana Notas: Isentress® e efavirenz foram administrados com entricitabina (+) fumarato de tenofovir desoproxila N = número total de indivíduos por grupo de tratamento com pelo menos um resultado disponível de teste. A análise está baseada em todos os dados disponíveis. Valor de P ≤ 0,001 para comparação de Isentress® vs. efavirenz, exceto total: taxa HDL23-C (valor de P = 0,061) e triglicérides25 (valor de P = 0,004). O conceito Last Obs. Carry Forward (LOCF) é aplicado para dados faltantes quando estas faltas devem-se a lipídios aumentados (ex., uso de terapia de resgate). |
||||
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Nenhuma informação específica está disponível sobre o tratamento de superdosagem com Isentress®. Foram estudadas doses únicas de até 1.600 mg e doses múltiplas de 800 mg 2x/dia na fase I, sem evidências de toxicidade50. Doses ocasionais de 1.800 mg por dia foram administradas nos estudos fase II/III, sem evidência de toxicidade50. Com base nos dados disponíveis, o raltegravir parece ser bem-tolerado em doses de até 800 mg 2x/dia e quando administrado com medicamentos que aumentam a exposição em 50–70% (como o fumarato de tenofovir desoproxila e o atazanavir). O raltegravir apresentou ampla margem terapêutica168; portanto o potencial para toxicidade50 decorrente da superdose é limitado.
No caso de uma superdose, devem ser adotadas medidas-padrão de suporte, por exemplo, remoção do material não absorvido do trato gastrintestinal, monitoramento clínico (incluindo a obtenção de eletrocardiograma169) e instituição de tratamento de apoio, se necessário. A extensão em que Isentress® pode ser dialisável é desconhecida.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS 1.0029.0173
Farm. Resp.: Fernando C. Lemos – CRF-SP nº 16.243.
Registrado e importado por:
Merck Sharp & Dohme Farmacêutica Ltda.
Rua 13 de Maio, 815 - Sousas, Campinas/SP
CNPJ: 45.987.013/0001-34 - Brasil
Isentress® 100 mg:
Fabricado por: Patheon Pharmaceuticals Inc., Cincinnati, Ohio, EUA
Embalado por: Merck Sharp & Dohme B.V., Haarlem, Holanda
Isentress® 400 mg:
Fabricado por: MSD International GmbH T/A MSD Ireland (Ballydine), Clonmel, Irlanda
Embalado por: Merck Sharp & Dohme B.V., Haarlem, Holanda
SAC 0800 0122232