

Drusolol (Bula do profissional de saúde)
UNIÃO QUÍMICA FARMACÊUTICA NACIONAL S/A
IDENTIFICAÇÃO DO MEDICAMENTO
Drusolol®
cloridrato de dorzolamida + maleato de timolol
Solução oftálmica estéril 2,0% + 0,5%
Medicamento similar equivalente ao medicamento de referência.
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução oftálmica estéril
Embalagem contendo frasco de 5 mL
USO OFTÁLMICO
USO ADULTO
COMPOSIÇÃO:
Cada mL de Drusolol® (24 gotas) contém:
| cloridrato de dorzolamida (equivalente a 20 mg de dorzolamida) | 22,26 mg (0,83 mg/gota1) |
| maleato de timolol (equivalente a 5 mg de timolol) | 6,83 mg (0,21 mg/gota1) |
| veículo q.s.p. | 1 mL |
Veículo: hietelose, cloreto de benzalcônio, manitol, citrato de sódio di-hidratado, hidróxido de sódio, ácido clorídrico2 e água para injetáveis.
Cada mL corresponde a 24 gotas. Cada gota1 contém 0,83 mg de dorzolamida e 0,21 mg de timolol.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE3
INDICAÇÕES
Drusolol é indicado para o tratamento da pressão intraocular4 (PIO) elevada de pacientes com hipertensão5 ocular, glaucoma6 de ângulo aberto, glaucoma6 pseudoesfoliativo ou outros glaucomas secundários de ângulo aberto, quando o tratamento combinado for adequado.
RESULTADOS DE EFICÁCIA
Foram conduzidos estudos clínicos de até 15 meses de duração para comparar o efeito redutor da PIO desta associação medicamentosa 2x/dia (administrada pela manhã e à noite) com o efeito de timolol a 0,5% e da dorzolamida a 2,0% administrados individual e concomitantemente a pacientes com glaucoma6 ou hipertensão5 ocular para os casos em que o tratamento combinado fosse indicado. Esses casos incluem tanto pacientes não tratados como pacientes controlados de forma inadequada com a monoterapia com timolol. O efeito redutor da PIO desta associação medicamentosa 2x/dia foi maior do que o da monoterapia de dorzolamida a 2% 3x/dia ou de timolol a 0,5% 2x/dia. O efeito redutor da PIO desta associação medicamentosa 2x/dia foi equivalente ao do tratamento combinado com dorzolamida 2x/dia e timolol 2x/dia.
Comparação com o tratamento combinado (pacientes tratados inicialmente com timolol)
Em um estudo clínico de grupos paralelos, randomizado7, duplo-cego e com duração de 3 meses, os pacientes que receberam esta associação medicamentosa 2x/dia (n=151) foram comparados aos pacientes que receberam timolol a 0,5% 2x/dia mais dorzolamida a 2,0% 2x/dia concomitantemente (n=148). Na concentração de vale matutina (hora 0) e na concentração de pico matutina (hora 2), os pacientes que receberam esta associação medicamentosa apresentaram redução da PIO equivalente à observada em pacientes que receberam os componentes individuais concomitantemente. Foram observadas as seguintes reduções de PIO em relação ao período basal, obtidas após 2 semanas de monoterapia com timolol a 0,5% 2x/dia:
Tabela 1. Redução média adicional da PIO em relação ao período basal com timolol (mmHg) * (redução média % da PIO)
|
|
Dia 90 |
Dia 90 |
|
Associação (cloridrato de dorzolamida + maleato de timolol) 2x/dia |
4,2 [16,3%] |
5,4 [21,6%] |
|
timolol a 0,5 % 2x/dia + dorzolamida a 2,0 % 2x/dia |
4,2 [16,3%] |
5,4 [21,8%] |
* Os pacientes deveriam apresentar PIO no período basal ? 22 mmHg para serem admitidos.
Comparação com a monoterapia (pacientes submetidos a washout do tratamento)
Um estudo clínico de grupos paralelos, randomizado7, duplo-cego e com duração de 3 meses comparou esta associação medicamentosa 2x/dia (n=114) com a monoterapia com timolol a 0,5% 2x/dia (n=112) e a monoterapia com dorzolamida a 2,0% 3x/dia (n=109) em pacientes para os quais o tratamento combinado fosse indicado. Após um período de washout de 3 semanas de todas as medicações hipotensoras oculares anteriores, os pacientes que receberam esta associação medicamentosa apresentaram redução da PIO tanto na concentração de vale matutina (hora 0) como na concentração de pico matutina (hora 2), que foi maior do que a observada em pacientes que receberam cada um dos componentes isoladamente.
Tabela 2: Redução média da PIO em relação ao período basal (mmHg) * (redução média % da PIO)
|
|
Dia 90 |
Dia 90 |
|
Associação (cloridrato de dorzolamida + maleato de timolol) 2x/dia |
7,7 [27,4%] |
9,0 [32,7%] |
|
dorzolamida a 2,0 % 3x/dia |
4,6 [15,5%] |
5,4 [19,8%] |
|
timolol a 0,5 % 2x/dia |
6,4 [22,2%] |
6,3 [22,6%] |
* Os pacientes deveriam apresentar PIO no período basal ? 24 mmHg para serem admitidos.
Comparação com a monoterapia (pacientes que iniciaram o tratamento com timolol)
Em um estudo clínico de grupos paralelos, randomizado7, duplo-cego, com duração de 3 meses e conduzido em pacientes com PIO elevada controlada de forma inadequada após 3 semanas de monoterapia com timolol a 0,5% 2x/dia, os pacientes que receberam esta associação medicamentosa 2x/dia (n=104) apresentaram redução da PIO tanto na concentração de vale matutina (hora 0) como na concentração de pico matutina (hora 2), que foi maior do que a observada em pacientes que receberam tanto com monoterapia com timolol a 0,5% 2x/dia (n=98) como monoterapia com dorzolamida a 2,0% 3x/dia (n=51).
Tabela 3: Redução média adicional da PIO em relação ao período basal com timolol (mmHg) * (redução média % da PIO)
|
|
Dia 90 |
Dia 90 |
|
Associação (cloridrato de dorzolamida + maleato de timolol) 2x/dia |
2,8 [10,6%] |
4,4 [17,3%] |
|
dorzolamida a 2,0 % 3x/dia |
1,4 [4,9%] |
2,0 [7,4%] |
|
timolol a 0,5 % 2x/dia |
1,7 [6,7%] |
1,6 [6,6%] |
* Os pacientes deveriam apresentar PIO no período basal ? 22 mmHg para serem admitidos.
Estudos de longo prazo
Foram conduzidas extensões abertas de dois estudos, por até 12 meses. Durante esse período, demonstrou-se o efeito redutor da PIO desta associação medicamentosa 2x/dia durante todo o dia e esse efeito foi mantido durante a administração a longo prazo.
Referências bibliográficas:
- Boyle JE, Ghosh K, Gieser DK, Adamsons IA, the Dorzolamide-Timolol Study Group. A randomized trial comparing the dorzolamide timolol combination given twice daily to monotherapy with timolol and dorzolamide. Ophthalmology 1998;105(10):1945-51.
- Clineschmidt CM, Williams RD, Snyder E, Adamsons IA, the Dorzolamide-Timolol Combination Study Group. A randomized trial in patients inadequately controlled with timolol alone comparing the dorzolamide-timolol combination to monotherapy with timolol or dorzolamide. Ophthalmology 1998;105(10):1952-9.
- Hutzelmann J, Owens S, Shedden A, Adamsons I, Vargas E, the International Clinical Equivalence Study Group. Comparison of the safety and efficacy of the fixed combination of dorzolamide/timolol and the concomitant administration of dorzolamide and timolol: a clinical equivalence study. Br J Ophthalmol 1998; 82:1249-53.
- Strohmaier K, Snyder E, DuBiner H, Adamsons I, the Dorzolamide- Timolol Study Group. The efficacy and safety of the dorzolamide timolol combination versus the concomitant administration of its components. Ophthalmology 1998;105(10):1936-44.
CARACTERÍSTICAS FARMACOLÓGICAS
Drusolol solução oftálmica estéril é a primeira combinação de um inibidor da anidrase carbônica e um agente bloqueador de receptores beta-adrenérgicos8, ambos de uso tópico9 ocular.
Mecanismo de ação
Drusolol é constituído de dois componentes: cloridrato de dorzolamida e maleato de timolol. Cada um desses dois componentes diminui a pressão intraocular4 elevada, por meio da redução da secreção de humor aquoso10, mas com diferentes mecanismos de ação.
O cloridrato de dorzolamida é um potente inibidor da anidrase carbônica tipo II humana. A inibição da anidrase carbônica nos processos ciliares do olho11 reduz a secreção do humor aquoso10, presumivelmente por diminuir a formação de íons12 bicarbonato com redução subsequente do transporte de sódio e de fluido. O maleato de timolol é um bloqueador não-seletivo dos receptores betadrenérgicos sem atividade simpatomimética intrínseca, depressora miocárdica direta ou anestésica local (estabilizante da membrana) significativa. O efeito combinado desses dois agentes resulta em redução adicional da pressão intraocular4, quando comparada à administração de cada componente isoladamente.
Após a administração tópica, Drusolol reduz a pressão intraocular4 elevada, associada ou não ao glaucoma6. A pressão intraocular4 elevada é um importante fator de risco13 na patogênese14 do dano ao nervo óptico e da perda do campo visual15 no glaucoma6. Quanto mais elevada a pressão intraocular4, maior a probabilidade de perda do campo visual15 e dano ao nervo óptico glaucomatoso. Drusolol reduz a pressão intraocular4 sem os efeitos adversos comuns aos mióticos, tais como cegueira noturna, espasmo16 de acomodação e constrição17 pupilar.
Farmacocinética e farmacodinâmica
- cloridrato de dorzolamida
Ao contrário dos inibidores da anidrase carbônica para uso oral, a administração tópica de cloridrato de dorzolamida permite que a medicação atue diretamente no olho11 em doses substancialmente menores e, portanto, com menos exposição sistêmica. Em estudos clínicos, esse fato resultou na redução da pressão intraocular4 sem os distúrbios ácido-base ou as alterações eletrolíticas características dos inibidores da anidrase carbônica por via oral.
Quando aplicada por via tópica, a dorzolamida atinge a circulação18 sistêmica. Para avaliar o potencial de inibição sistêmica da anidrase carbônica após a administração tópica, foram avaliadas as concentrações da medicação e de seus metabólitos19 nas hemácias20 e no plasma21 e a inibição da anidrase carbônica nas hemácias20. A dorzolamida se acumula nas hemácias20 durante a administração crônica como resultado da ligação seletiva à anidrase carbônica tipo II, embora sejam mantidas concentrações extremamente baixas de medicação livre no plasma21. O composto original forma um único metabólito22 N-desetil, que inibe a anidrase carbônica tipo II com potência inferior à do composto original, mas também inibe uma isoenzima menos ativa (anidrase carbônica tipo I). O metabólito22 também se acumula nas hemácias20, nas quais se liga principalmente à anidrase carbônica tipo I. A dorzolamida se liga moderadamente às proteínas23 plasmáticas (aproximadamente 33%); é excretada principalmente na urina24, de forma inalterada; e seu metabólito22 também é excretado pela urina24. Ao final da administração, a dorzolamida é eliminada das hemácias20 de forma não linear, o que resulta em rápido declínio inicial da concentração da medicação, seguido por uma fase de eliminação mais lenta, com meia-vida de aproximadamente 4 meses.
Quando a dorzolamida foi administrada por via oral para simular a exposição sistêmica máxima após administração tópica ocular prolongada, o estado de equilíbrio foi alcançado em 13 semanas. No estado de equilíbrio, praticamente não havia medicação livre ou metabólito22 no plasma21; a inibição da anidrase carbônica nas hemácias20 foi menor do que a supostamente necessária para produzir efeito farmacológico na função renal25 ou respiração. Resultados farmacocinéticos similares foram observados após administração tópica crônica de cloridrato de dorzolamida. Entretanto, alguns pacientes idosos com disfunção renal25 (depuração de creatinina26 estimado em 30-60 mL/min) apresentaram concentrações mais altas de metabólitos19 nas hemácias20, mas a diferença significativa na inibição da anidrase carbônica ou os efeitos adversos sistêmicos27 clinicamente significativos não foram diretamente atribuídos a esse achado.
- maleato de timolol
Em um estudo da concentração plasmática da medicação envolvendo 6 indivíduos, a exposição sistêmica ao timolol foi determinada após administração tópica de solução oftálmica de maleato de timolol a 0,5% duas vezes ao dia. O pico médio da concentração plasmática foi de 0,46 ng/mL após a administração pela manhã e de 0,35 ng/mL após a administração vespertina.
CONTRAINDICAÇÕES
Drusolol é contraindicado para pacientes28 com:
- doença reativa das vias aéreas, asma29 brônquica ou histórico de asma29 brônquica ou doença pulmonar obstrutiva crônica grave;
- bradicardia30 sinusal, bloqueio sinoatrial, bloqueio atrioventricular de segundo ou terceiro graus, insuficiência cardíaca31 manifesta, choque32 cardiogênico;
- hipersensibilidade a qualquer componente do produto.
Essas contraindicações têm como base os componentes e não são específicas da associação.
ADVERTÊNCIAS E PRECAUÇÕES
A exemplo de outros agentes oftálmicos tópicos, esse medicamento pode ser absorvido por via sistêmica. O timolol é um betabloqueador; portanto, os mesmos tipos de reações adversas observadas com a administração sistêmica dos betabloqueadores podem ocorrer com a administração tópica.
Reações cardiorrespiratórias
Por causa da presença do maleato de timolol, a insuficiência cardíaca31 deve ser adequadamente controlada antes de se iniciar o tratamento com Drusolol. Pacientes com histórico de doença cardiovascular, incluindo insuficiência cardíaca31, devem ser monitorados para sinais33 de deterioração dessas doenças e a frequência cardíaca deve ser verificada.
Devido ao efeito negativo no tempo de condução, os betabloqueadores devem ser prescritos com cautela para pacientes28 com bloqueio cardíaco34 de primeiro grau.
Reações respiratórias e cardíacas, incluindo morte por broncoespasmo35 em pacientes com asma29 e raramente morte em associação com insuficiência cardíaca31, foram relatadas após a administração da solução oftálmica de maleato de timolol.
Em pacientes com doença pulmonar obstrutiva crônica (DPOC) leve/moderada, Drusolol deve ser usado com cautela, e apenas se o benefício potencial superar o risco potencial.
Distúrbios vasculares36
Pacientes com distúrbios/doenças circulatórias periféricas graves (ex. formas graves da doença de Raynaud37 ou síndrome38 de Raynaud) devem ser tratados com cautela.
Mascaramento de sintomas39 de hipoglicemia40 em pacientes com diabetes mellitus41: agentes bloqueadores beta-adrenérgicos8 devem ser administrados com cautela em pacientes sujeitos a hipoglicemia40 espontânea ou pacientes diabéticos (especialmente àqueles com diabetes42 instável) que recebem insulina43 ou agentes hipoglicemiantes orais44. Os agentes bloqueadores beta-adrenérgicos8 podem mascarar os sinais33 e sintomas39 de hipoglicemia40 aguda.
Mascaramento da tireotoxicose
Agentes bloqueadores beta-adrenérgicos8 podem mascarar determinados sinais33 clínicos do hipertireoidismo45 (ex. taquicardia46). Pacientes com suspeita de desenvolvimento de tireotoxicose devem ser monitorados com cuidado para evitar a retirada abrupta do agente beta- adrenérgico47, o que pode precipitar uma crise de tireoide48.
Anestesia49 cirúrgica
A necessidade ou conveniência da retirada de agentes bloqueadores beta-adrenérgicos8 antes de grandes cirurgias é controversa. Se necessário durante a cirurgia, os efeitos dos agentes bloqueadores beta-adrenérgicos8 podem ser revertidos por doses suficientes de agonistas adrenérgicos8 (ver item “10. Superdose”).
Disfunção renal25 e hepática50
Drusolol não foi estudado em pacientes com disfunção renal25 grave (depuração de creatinina26 < 30 mL/min). Uma vez que o cloridrato de dorzolamida e seus metabólitos19 são excretados predominantemente pelos rins51, Drusolol não é recomendado para esses pacientes.
Drusolol não foi estudado em pacientes com disfunção hepática50, portanto, deve ser usado com cautela nesses pacientes.
Imunologia e hipersensibilidade
A exemplo de outros agentes oftálmicos tópicos, esse medicamento pode ser absorvido por via sistêmica. A dorzolamida é uma sulfonamida; portanto, os mesmos tipos de reações adversas observadas durante a administração sistêmica de sulfonamidas podem ocorrer com a administração tópica, como síndrome de Stevens-Johnson52 e necrólise epidérmica tóxica53. Caso ocorram sinais33 de reações graves ou hipersensibilidade, o uso da preparação deve ser suspenso.
Em estudos clínicos, foram relatados efeitos adversos oculares locais com a administração crônica de solução oftálmica de cloridrato de dorzolamida principalmente conjuntivite54 e reações palpebrais. Algumas dessas reações tiveram aparência e curso clínico de reações do tipo alérgicas e desapareceram com a suspensão do tratamento medicamentoso. Reações semelhantes foram relatadas com esta associação medicamentosa. Se tais reações forem observadas, deve-se considerar a suspensão do tratamento com Drusolol. Enquanto estiverem recebendo betabloqueadores, pacientes com histórico de atopia ou reações anafiláticas55 graves a uma variedade de alérgenos56 podem ser mais reativos à estimulação repetida acidental, diagnóstica ou terapêutica57 com tais alérgenos56. Esses pacientes podem não apresentar resposta às doses usuais de epinefrina usadas para tratar reações anafiláticas55.
Tratamento combinado
Existe a possibilidade de efeito aditivo sobre os efeitos sistêmicos27 conhecidos da inibição da anidrase carbônica em pacientes que recebem inibidores orais e tópicos da anidrase carbônica concomitantemente. A administração concomitante de Drusolol e de inibidores da anidrase carbônica por via oral não foi estudada e não é recomendada.
Pacientes que já estão recebendo bloqueadores beta-adrenérgicos8 sistêmicos27 e começam a utilizar Drusolol devem ser observados quanto ao possível efeito aditivo sobre a pressão intraocular4 ou sobre os efeitos sistêmicos27 conhecidos do bloqueio beta-adrenérgico47. O uso de dois bloqueadores beta-adrenérgicos8 tópicos não é recomendado.
Outros
O controle de pacientes com glaucoma6 agudo58 de ângulo fechado requer outras intervenções terapêuticas além de agentes oculares hipotensores. Drusolol não foi estudado em pacientes com glaucoma6 agudo58 de ângulo fechado.
Foi relatado descolamento da coroide59 com a administração de tratamento supressor60 de humor aquoso10 (por exemplo, timolol, acetazolamida, dorzolamida) após procedimentos de filtração.
Pacientes com baixa contagem de células61 endoteliais são mais propensos ao desenvolvimento de edema62 de córnea63. Deve-se tomar precauções quando Drusolol for prescrito para esse grupo de pacientes.
Uso de lentes de contato
Drusolol contém o conservante cloreto de benzalcônio, que pode se depositar nas lentes de contato gelatinosas; portanto, Drusolol não deve ser administrado quando essas lentes estiverem sendo utilizadas. As lentes devem ser retiradas antes da aplicação das gotas e só devem ser recolocadas 15 minutos depois.
Gravidez64 e Lactação65
Categoria C – Não existem estudos adequados e bem controlados em grávidas. Drusolol deve ser usado durante a gravidez64 somente se os benefícios potenciais justificarem os possíveis riscos para o feto66.
Não se sabe se o cloridrato de dorzolamida é excretado no leite materno. O maleato de timolol é excretado no leite materno. Uma vez que reações adversas graves podem ocorrer em lactentes67, deve-se decidir entre descontinuar o aleitamento ou a medicação, levando-se em consideração sua importância para a mãe.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista. Uso pediátrico
A segurança e a eficácia da solução oftálmica de cloridrato de dorzolamida 2% foi estabelecida em estudo clínico com crianças menores de 6 anos de idade. Neste estudo, pacientes menores de 6 anos e maiores de 2 anos de idade cuja PIO não foi controlada com monoterapia receberam esta associação medicamentosa. Nesses pacientes a associação medicamentosa foi geralmente bem tolerada.
Populações especiais
Uso em idosos: Do número total de pacientes dos estudos clínicos com esta associação medicamentosa, 49% tinham 65 anos ou mais e 13% tinham 75 anos ou mais.
No geral, nenhuma diferença na eficácia ou no perfil de segurança foi observada entre esses pacientes e pacientes mais novos, mas o aumento da sensibilidade individual em alguns idosos não pode ser desconsiderado.
Efeitos na habilidade de dirigir e operar máquinas
Existem efeitos adversos associados ao uso desta associação medicamentosa que podem afetar a capacidade em alguns pacientes de dirigir e/ou operar máquinas (ver item “9. Reações adversas”).
Este medicamento pode causar doping.
INTERAÇÕES MEDICAMENTOSAS
Não foram realizados estudos de interações medicamentosas específicos com Drusolol.
Em estudos clínicos, esta associação medicamentosa foi usada concomitantemente com as seguintes medicações sistêmicas, sem evidência de interações adversas: inibidores da ECA, bloqueadores dos canais de cálcio, diuréticos68, anti-inflamatórios não esteroidais, incluindo ácido acetilsalicílico e hormônios (por exemplo, estrogênio, insulina43, tiroxina).
Entretanto, é possível que ocorram efeitos aditivos, hipotensão69 e/ou bradicardia30 acentuada quando a solução oftálmica de maleato de timolol for administrada concomitantemente com bloqueadores dos canais de cálcio, medicações depletoras de catecolamina, antiarrítmicos, parassimpatomiméticos ou bloqueadores beta-adrenérgicos8 por via oral.
Há relato de potencialização de bloqueio beta-adrenérgico47 sistêmico70 (por exemplo, diminuição da frequência cardíaca, depressão) durante tratamento concomitante com inibidores da CYP2D6 (por exemplo: quinidina, inibidores da recaptação de serotonina) e timolol.
O componente dorzolamida de Drusolol é um inibidor da anidrase carbônica e, embora administrado por via tópica, é absorvido por via sistêmica. Em estudos clínicos, a solução oftálmica de cloridrato de dorzolamida não foi associada a distúrbios ácido-base. Entretanto, esses distúrbios foram relatados com inibidores orais da anidrase carbônica e, algumas vezes, resultaram em interações medicamentosas (por exemplo, toxicidade71 associada ao tratamento com altas doses de salicilato). Portanto, a possibilidade de tais interações medicamentosas deve ser considerada em pacientes que estejam recebendo Drusolol.
Os agentes bloqueadores beta-adrenérgicos8 orais podem exacerbar a hipertensão5 de rebote que pode ocorrer após a suspensão de clonidina.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Manter o produto em sua embalagem original e conservar em temperatura ambiente (15–30°C); proteger da luz. O prazo de validade é de 24 meses após a data de fabricação (vide cartucho).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Líquido incolor a levemente amarelado.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
A dose é de uma gota1 de Drusolol no(s) olho11(s) afetado(s) duas vezes ao dia.
Quando Drusolol for substituir outro(s) agente(s) oftálmico(s) antiglaucomatoso(s), descontinue o(s) outro(s) agente(s) após a administração apropriada em um dia, e comece a administrar Drusolol no dia seguinte.
Se outro agente oftálmico tópico9 estiver sendo usado, Drusolol e o outro agente devem ser administrados com um intervalo de, pelo menos, 10 minutos.
Quando se utiliza a oclusão nasolacrimal ou se fecha as pálpebras72, durante 2 minutos, a absorção sistêmica é reduzida. Isso pode resultar em aumento da atividade local.
Instruções de uso
- Antes de utilizar a medicação pela primeira vez, o paciente deve certificar-se de que o lacre de segurança na tampa do frasco está intacto. A existência de um espaço entre o frasco e a tampa é normal quando o frasco ainda não foi aberto.
- Para abrir o frasco, deve-se girar a tampa na direção indicada pelas setas, quebrando o lacre de segurança. NÃO AGITAR ANTES DE USAR.
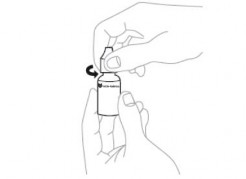
- Para aplicar o medicamento, o paciente deve inclinar a cabeça73 para trás e puxar levemente a pálpebra inferior para formar uma bolsa entre a pálpebra e o olho11.
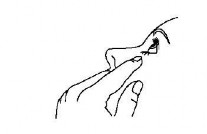
- O paciente deve inverter o frasco, apertando-o levemente com o dedo polegar ou indicador sobre o frasco, como demonstrado na figura a seguir, até que uma única gota1 seja dispensada no olho11, conforme orientação médica.
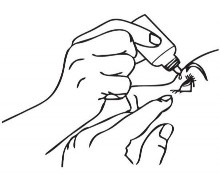
NÃO TOQUE A PONTA DO FRASCO NOS OLHOS74 OU NAS PÁLPEBRAS72.
Se manuseados inadequadamente, os medicamentos oftálmicos podem ser contaminados por bactérias comuns, conhecidas por causar infecções75 oculares. O uso de medicamentos oftálmicos contaminados pode causar lesões76 oculares graves e perda da visão77. Em caso de suspeita de contaminação do medicamento ou se o paciente desenvolver uma infecção78 ocular, o paciente deve ser orientado a contatar o médico imediatamente. - Após o uso de Drusolol, o paciente deve pressionar com o dedo o canto do olho11 próximo ao nariz79 (conforme demonstrado na figura abaixo) por 2 minutos. Isso ajuda a manter Drusolol no olho11.
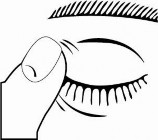
- Repetir os passos 3 e 4 para aplicar o medicamento no outro olho11, se recomendado.
- O paciente deve recolocar a tampa, rosqueando-a até que esteja firmemente fechado.
- A ponta gotejadora foi desenhada para liberar uma única gota1; portanto, o furo da ponta gotejadora NÃO deve ser alargado.
- Após a utilização de todas as doses, irá sobrar um pouco de Drusolol no frasco. Oriente o paciente a não se preocupar, pois foi acrescentada uma quantidade extra de Drusolol no frasco para utilizar a quantidade integral de Drusolol prescrita. Oriente-o também a não tentar remover o excesso de medicamento do frasco.
REAÇÕES ADVERSAS
Nos estudos clínicos para esta associação medicamentosa as reações adversas observadas são consistentes com aquelas relatadas previamente com cloridrato de dorzolamida e/ou maleato de timolol. Durante os estudos clínicos, 1.035 pacientes foram tratados com esta associação medicamentosa. Aproximadamente 2,4% de todos os pacientes descontinuaram a terapia com esta associação medicamentosa devido a reações adversas oculares locais e, aproximadamente 1,2% de todos os pacientes descontinuaram devido a reações adversas locais sugestivas de alergia80 ou hipersensibilidade (como inflamação81 palpebral e conjuntivite54). Como outros medicamentos oftálmicos aplicados topicamente, timolol é absorvido na circulação18 sistêmica. Isso pode causar reações adversas semelhantes aos agentes betabloqueadores sistêmicos27. A incidência82 de reações adversas sistêmicas após a administração oftálmica tópica é menor que administração sistêmica.
As seguintes reações adversas foram relatadas com esta associação medicamentosa ou um de seus componentes durante os estudos clínicos ou durante a experiência pós-comercialização:
As reações podem ser classificadas em:
|
Categoria |
Frequência |
|
Muito comum |
≥ 10% |
|
Comum |
≥ 1% e < 10% |
|
Incomum |
≥ 0,1% e < 1% |
|
Raro |
≥ 0,01% e < 0,1% |
|
Muito raro |
< 0,01% |
|
Desconhecida |
Não pode ser estimada pelos dados disponíveis |
Distúrbios do sistema imunológico83
Associação medicamentosa:
- Rara: sinais33 e sintomas39 de reações alérgicas sistêmicas incluindo angioedema84, urticária85, prurido86, erupção87 cutânea88, anafilaxia89.
maleato de timolol colírio90, solução:
- Rara: sinais33 e sintomas39 de reações alérgicas incluindo angioedema84, urticária85, prurido86, erupção87 cutânea88 localizada e generalizada, anafilaxia89.
- Desconhecido: prurido86.
Distúrbios do metabolismo91 e nutrição92
maleato de timolol colírio90, solução:
- Desconhecido: hipoglicemia40.
Distúrbios psiquiátricos
maleato de timolol colírio90, solução:
- Incomum: depressão*.
- Rara: insônia*, pesadelos*, perda de memória.
Distúrbios do sistema nervoso93
cloridrato de dorzolamida colírio90, solução:
- Comum: cefaleia94*.
- Rara: tontura95*, parestesia96*.
maleato de timolol colírio90, solução:
- Comum: cefaleia94*.
- Incomum: tontura95*, síncope97*.
- Rara: parestesia96*, aumento dos sinais33 e sintomas39 de miastenia98 grave, redução da libido99*, acidente vascular cerebral100*, isquemia101 cerebral.
Distúrbios oculares
Associação medicamentosa:
- Muito comum: queimação e ardência.
- Comum: injeção102 conjuntival, visão77 turva, erosão corneana, coceira ocular, lacrimação.
cloridrato de dorzolamida colírio90, solução:
- Comum: inflamação81 palpebral*, irritação palpebral*. Incomum: iridociclite*.
- Rara: irritação, incluindo vermelhidão* e dor*, crosta palpebral*, miopia103 transitória (solucionada com a descontinuação da terapia), edema62 corneano*, hipotonia104 ocular*, descolamento coroidal (após cirurgia de filtração) *.
maleato de timolol colírio90, solução:
- Comum: sinais33 e sintomas39 de irritação ocular, incluindo blefarite105*, ceratite*, redução da sensibilidade corneana e olhos74 secos*.
- Incomum: distúrbios visuais, incluindo alterações de refração (em alguns casos, devido à descontinuação da terapia miótica)*.
- Rara: ptose106, diplopia107, descolamento coroidal (após cirurgia de filtração) *.
- Desconhecido: coceira, lacrimejamento, vermelhidão, visão77 turva, erosão da córnea63.
Distúrbios do ouvido e labirinto108
maleato de timolol colírio90, solução:
- Rara: zumbido*.
Distúrbios cardíacos
maleato de timolol colírio90, solução:
- Incomum: bradicardia30*.
- Rara: dor torácica*, palpitação109*, edema62*, arritmia110*, insuficiência cardíaca congestiva111*, bloqueio cardíaco34*, parada cardíaca*.
- Desconhecido: bloqueio atrioventricular, insuficiência cardíaca31.
Distúrbios vasculares36
maleato de timolol colírio90, solução:
- Rara: hipotensão69*, claudicação112, fenômeno de Raynaud113, mão114 e pés frios.
Distúrbios respiratórios, torácicos e do mediastino115
Associação medicamentosa:
- Comum: sinusite116.
- Rara: falta de ar, insuficiência respiratória117, rinite118, raramente broncoespasmo35.
cloridrato de dorzolamida colírio90, solução:
- Rara: epistaxe119*.
maleato de timolol colírio90, solução:
- Incomum: dispneia120*.
- Rara: broncoespasmo35 (predominantemente em pacientes com doença broncoespástica preexistente) *, insuficiência respiratória117, tosse*.
Distúrbios gastrintestinais
Associação medicamentosa:
- Muito comum: disgeusia121.
cloridrato de dorzolamida colírio90, solução:
- Comum: náusea122*.
- Rara: irritação da garganta123, boca124 seca*.
maleato de timolol colírio90, solução:
- Incomum: náusea122*, dispepsia125*.
- Rara: diarreia126, boca124 seca*.
- Desconhecido: disgeusia121, dor abdominal, vômito127.
Distúrbios da pele128 e do tecido subcutâneo129
Associação medicamentosa:
- Rara: dermatite130 de contato, síndrome de Stevens-Johnson52, necrólise epidérmica tóxica53.
cloridrato de dorzolamida colírio90, solução:
- Rara: erupção87 cutânea88*.
maleato de timolol colírio90, solução:
- Rara: alopecia131*, erupção87 cutânea88 psoriasiforme ou exacerbação da psoríase132*.
- Desconhecido: erupção87 cutânea88.
Distúrbios musculoesqueléticos e do tecido conjuntivo133
maleato de timolol colírio90, solução:
- Rara: lúpus134 eritematoso135 sistêmico70.
- Desconhecido: mialgia136.
Distúrbios renais e urinários
Associação medicamentosa:
- Incomum: urolitíase.
Distúrbios do sistema reprodutivo e da mama137
maleato de timolol colírio90, solução:
- Rara: doença de Peyronie*, diminuição da libido99.
- Desconhecido: disfunção sexual.
Distúrbios gerais e condições no local de administração
cloridrato de dorzolamida colírio90, solução:
- Comum: astenia138/fadiga139*.
maleato de timolol colírio90, solução:
- Incomum: astenia138/fadiga139*.
*Essas reações adversas também foram observadas com esta associação medicamentosa durante a experiência pós-comercialização.
** Reações adversas adicionais foram observadas com betabloqueadores oftálmicos e podem potencialmente ocorrer com esta associação medicamentosa.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Não há dados disponíveis a respeito da superdose em humanos por ingestão acidental ou proposital de Drusolol.
Há relatos de superdose acidental com solução oftálmica de maleato de timolol, a qual resultou em efeitos sistêmicos27 semelhantes aos observados com bloqueadores beta-adrenérgicos8 sistêmicos27, tais como tontura95, cefaleia94, falta de ar, bradicardia30, broncoespasmo35 e parada cardíaca. Os sinais33 e sintomas39 mais comuns que podem ocorrer com a superdose de dorzolamida são desequilíbrio eletrolítico, desenvolvimento de estado acidótico e, possivelmente, efeitos no sistema nervoso central140.
O tratamento deve ser sintomático141 e de suporte. Os níveis séricos de eletrólitos142 (particularmente potássio) e o pH sanguíneo devem ser monitorados. Estudos têm mostrado que o timolol não é dialisado prontamente.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Registro MS – 1.0497.1281
Farm. Resp.: Florentino de Jesus Krencas CRF-SP n° 49136
UNIÃO QUÍMICA FARMACÊUTICA NACIONAL S/A
Rua Cel. Luiz Tenório de Brito, 90 Embu-Guaçu – SP – CEP 06900-000
CNPJ 60.665.981/0001-18
Indústria Brasileira
Fabricado na unidade fabril:
Avenida Prefeito Olavo Gomes de Oliveira, 4.550
Bairro Aeroporto
Pouso Alegre – MG – CEP: 37560-100
CNPJ: 60.665.981/0005-41
Indústria Brasileira
SAC 0800 011 1559






