Gino-Mizonol (Bula do profissional de saúde)
GEOLAB INDÚSTRIA FARMACÊUTICA S/A
IDENTIFICAÇÃO DO MEDICAMENTO
Gino-Mizonol
nitrato de miconazol
Creme 20 mg/g
Medicamento similar equivalente ao medicamento de referência.
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Creme vaginal
Embalagem contendo 1 bisnaga de 80 g + 14 aplicadores
USO GINECOLÓGICO
USO ADULTO
COMPOSIÇÃO:
Cada grama1 de Gino-Mizonol contém:
| nitrato de miconazol | 20 mg |
| excipiente q.s.p. | 1 g |
Excipientes: miristato de isopropila, álcool cetoestearílico, álcool cetoestearílico etoxilado, petrolado líquido, butil- hidroxianisol, ácido benzoico, monoestearato de glicerila, propilenoglicol e água purificada.
INFORMAÇÕES TÉCNICAS AOS PROFISSINAIS DE SAÚDE2
INDICAÇÕES
Gino-Mizonol é destinado ao tratamento de infecções3 vulvovaginais e perianais produzidas por Candida.
RESULTADOS DE EFICÁCIA
A eficácia do miconazol no tratamento de vulvovaginites causadas por fungos foi avaliada em um estudo duplo-cego4 controlado com placebo5, envolvendo 230 pacientes com cultura positiva para alguma espécie de Candida (principalmente, Candida albicans). O controle terapêutico, da mesma forma que o diagnóstico6 e identificação do patógeno, foi feito através de exames ginecológicos e laboratoriais. As pacientes foram tratadas com: miconazol creme 1%, miconazol creme 2%, comparativo por via oral ou creme contendo apenas o veículo. Ao final do tratamento, o grupo miconazol creme 2% apresentou taxa de cura (95%) significantemente melhor que os grupos miconazol 1% creme, comparativo por via oral (p < 0,0001) e controle (p < 0,0001).1
Em um estudo randomizado7 envolvendo 139 pacientes com diagnóstico6 de candidíase8 da vulva9 e da vagina10, das quais 46 eram gestantes, foi realizado o tratamento com creme de nitrato de miconazol 2% (1 aplicador uma vez ao dia, ao deitar, durante 14 dias) ou com um comparativo por via oral. Entre as 56 pacientes tratadas com miconazol na forma de creme, 51 (91,1%) obtiveram cura em comparação com 46 (76,7%) daquelas tratadas por via oral.2
Foi realizado um estudo clínico envolvendo 48 pacientes com teste laboratorial positivo para Candida e com presença de leucorreia11 e prurido12. Dessas pacientes 35 eram portadoras de vaginite13 aguda e 13 de vaginite13 crônica ou recidivante14, com idade média de 33 anos. A posologia preconizada15 de 1 aplicador tratamento e, ao final deste, os exames laboratoriais foram negativos em 91,7% dos casos.3
Referências:
- PROOST, J. et al. Miconazole in the Treatment of Mycotic Vulvovaginitis. Am J Obstet Gynecol, v.112, n.5, p.688-92, mar. 1972.
- DAVES, J.E., et al. Comparative Evaluation of Monistat and Mycostatin in the Treatment of Vulvovaginal Candidiasis. Obstetrics and Gynecology. v.44, n.3, p. 403-406, fev.1974.
- GODTS, P., VERMYLER, P., VAN CUTSEM. J. Clinical Evaluation of Miconazole Nitrate in the Treatment of Vaginal Candidiasis. Arzneim. Forsch., v.21, p.65-257, 1971.
CARACTERÍSTICAS FARMACOLÓGICAS
Propriedades Farmacodinâmicas:
O nitrato de miconazol, substância ativa de Gino-Mizonol, é um agente antifúngico com amplo espectro de ação, atingindo igualmente os dermatófitos16 e leveduras patogênicos para o homem. Apresenta uma ação fungistática de alta potência, capaz de inibir o crescimento de colônias de diferentes espécies de Candida.
Seu mecanismo de ação está baseado na inibição da biossíntese de ergosterol do fungo17 e alteração da composição de outros componentes lipídicos da membrana do fungo17, o que resulta na necrose18 destas células19.
As pesquisas realizadas demonstraram que após a adição do nitrato de miconazol às culturas de fungos em meio líquido de Sabouraud, incubadas a 25°C durante 14 dias, não houve crescimento de Candida albicans ou outra espécie desse gênero. Mesmo nas formas mais rebeldes à terapia, que são as que acometem as gestantes e as diabéticas, os resultados são excelentes.
Seu efeito antipruriginoso é potente, proporcionando alívio imediato após as primeiras aplicações.
Propriedades Farmacocinéticas:
Absorção: o miconazol persiste na vagina10 por até 72 horas após uma única aplicação. A absorção sistêmica do miconazol após administração intravaginal é limitada, com biodisponibilidade de 1 a 2% após a administração intravaginal de uma dose de 1200 mg. As concentrações plasmáticas de miconazol são mensuráveis após 2 horas de administração de alguns pacientes, com níveis máximos observáveis após 12 a 24 horas depois da administração.
A concentração plasmática diminui lentamente a seguir, sendo ainda mensurável na maioria dos pacientes, 96 horas após a aplicação. Uma segunda dose administrada 48 horas após, resultou em um perfil plasmático semelhante ao da primeira aplicação.
Distribuição: o miconazol absorvido fica ligado às proteínas20 plasmáticas em 88,2% e aos eritrócitos21 em 10,6%.
Metabolismo22 e excreção: a pequena quantidade de miconazol que é absorvida é eliminada predominantemente nas fezes, igualmente como droga inalterada ou seus metabólitos23, em um período de até quatro dias após a administração. Quantidades menores da droga inalterada e seus metabólitos23 também aparecem na urina24. A meia-vida média de eliminação aparente é de 57 horas.
CONTRAINDICAÇÕES
Hipersensibilidade ao nitrato de miconazol ou aos excipientes da formulação.
Durante as primeiras semanas da gravidez25 e durante a amamentação26, o uso de qualquer medicação deve ser feito sob orientação médica.
Categoria de risco na gravidez25: Categoria C.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
ADVERTÊNCIAS E PRECAUÇÕES
O tratamento deve ser interrompido se ocorrer reação alérgica27 ou de hipersensibilidade local ao medicamento.
Quando o parceiro sexual também estiver infectado, deve-se indicar terapia apropriada. O contato de nitrato de miconazol com diafragmas e preservativos a base de látex, usados para contracepção28, deve ser evitado, uma vez que a borracha pode ser danificada.
É sabido que a administração sistêmica de miconazol inibe a CYP3A4/2C9. Devido à disponibilidade sistêmica limitada após aplicação vaginal, é improvável que ocorram interações clinicamente relevantes. Entretanto, em pacientes recebendo anticoagulantes29 orais, como varfarina, deve-se ter cautela e o efeito anticoagulante30 deve ser monitorado.
Medidas habituais de higiene devem ser tomadas, como por exemplo, não compartilhar a toalha de banho. O parceiro sexual também deve ser tratado.
Gravidez25 e Lactação31
É contraindicado o uso durante as primeiras semanas da gravidez25 e durante a amamentação26.
Categoria de risco na gravidez25: Categoria C.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
INTERAÇÕES MEDICAMENTOSAS
É sabido que a administração sistêmica de miconazol inibe a CYP3A4/2C9. Devido à disponibilidade sistêmica limitada após aplicação vaginal, é muito raro ocorrer interações clinicamente relevantes. Em pacientes recebendo anticoagulantes29 orais, como varfarina, deve-se ter cautela e o efeito anticoagulante30 deve ser monitorado. As ações e os efeitos colaterais32 de alguns outros medicamentos como hipoglicemiantes orais33 e fenitoína, quando administrados concomitantemente ao miconazol, podem ser aumentados, devendo-se ter cautela.
O contato de nitrato de miconazol com diafragmas e preservativos (camisinha) a base de látex, usados para contracepção28, deve ser evitado, uma vez que a borracha pode ser danificada.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Gino-Mizonol deve ser mantido em temperatura ambiente (15–30°C), protegido da luz e umidade.
Prazo de validade: 24 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Gino-Mizonol apresenta-se na forma de creme homogêneo, branco e isento de grumos.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Não interrompa as aplicações durante o período menstrual. Veja as instruções de uso do aplicador a seguir:
- Retire a tampa da bisnaga e perfure o lacre da bisnaga, introduzindo o pino perfurante da tampa.
- Adapte o aplicador ao bico da bisnaga.
- Aperte a base da bisnaga com os dedos, de maneira a forçar a entrada do creme no aplicador, preenchendo todo o espaço vazio, com cuidado para que o creme não extravase o êmbolo34.
- Retire o aplicador e feche novamente a bisnaga.
- Introduza delicadamente o aplicador na vagina10, o mais profundamente possível, e empurre o êmbolo34 para dentro, até esvaziar o aplicador.
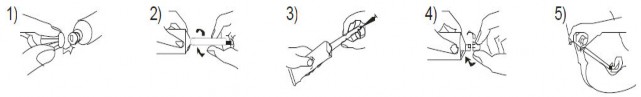
- A aplicação faz-se com maior facilidade estando a paciente deitada de costas35, com as pernas dobradas.
- Quando utilizado seguindo as instruções, o aplicador cheio contém a dose adequada (5 g de creme), considerando ainda o resíduo que permaneceu no aplicador.
Utilizar um aplicador completamente preenchido com aproximadamente 5 g, inserido o mais profundamente possível na vagina10, uma vez ao dia, ao deitar, durante 14 dias consecutivos.
Não deve ser utilizado mais de 5 g (1 aplicador preenchido) por dia.
REAÇÕES ADVERSAS.
Dados de estudo clínico: Eventos adversos, independentemente da causa, relatados em dois estudos clínicos fase III estão demonstrados abaixo. Um total de 537 mulheres com candidíase8 microbiologicamente confirmada e sintomas36 (prurido12 vulvovaginal, ardência/irritação); ou sinais37 de eritema38 vulvar, edema39, escoriações40; eritema38 vaginal ou edema39 foram tratados com miconazol intravaginal. As pacientes foram randomicamente agrupadas para o tratamento com uma cápsula de 1200 mg em dose única ou 7 dias de aplicação de creme vaginal a 2% de miconazol. Não houve controle com placebo5. A segurança foi autoavaliada diariamente com um cartão de eventos. Na tabela estão incluídos os eventos relatados por 5% das pacientes em cada grupo de tratamento.
|
Orgão ou sistema |
Miconazol creme 2% 7 dias |
Miconazol cápsula 1200 mg |
|
Evento adverso |
(N = 265), % |
(N = 272), % |
|
Todos os eventos adversos |
64 |
70 |
|
Distúrbios do sistema nervoso41 |
||
|
cefaleia42 |
18,9 |
17,6 |
|
Distúrbios urinários e renais |
||
|
Infecção43 do trato urinário44 não especificada |
--- |
5,1 |
|
Distúrbios da mama45 e sistema reprodutivo |
||
|
Prurido12 genital feminino |
26,8 |
19,1 |
|
Sensação de ardência genital |
23,8 |
26,1 |
|
Irritação vaginal |
15,5 |
20,2 |
|
Corrimento vaginal |
4,5 |
10,3 |
Pós-comercialização
As reações adversas obtidas através de relatos espontâneos durante o período de pós- comercialização mundial com nitrato de miconazol encontram-se abaixo, segundo o critério a seguir. As reações adversas estão ordenadas por frequência, usando a seguinte convenção:
|
Frequência das Reações Adversas |
|
|
> 1/10 (> 10%) |
muito comum |
|
> 1/100 e < 1/10 (> 1% e < 10%) |
comum (frequente) |
|
> 1/1000 e < 1/100 (> 0,1% e < 1%) |
incomum (infrequente) |
|
> 1/10.000 e < 1/1000 (> 0,0 1% e < 0,1%) |
rara |
|
< 1/10.000 (< 0,01%) |
muito rara |
As frequências observadas abaixo refletem as taxas de reações adversas relatadas espontaneamente e não representam a estimativa mais precisa da incidência46 que poderia ser obtida em estudos clínicos ou epidemiológicos.
Relatos de eventos adversos pós-comercialização:
Distúrbios do sistema imune47:
- Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): condições alérgicas incluindo anafiláticas e anafilactoides e edema angioneurótico48.
Distúrbios do tecido subcutâneo49 e pele50:
- Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): urticária51, prurido12 e erupção52 cutânea53.
Distúrbios da mama45 e sistema reprodutivo:
- Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): dor pélvica54 (cólica), sensação de ardência genital, prurido12 genital feminino, irritação vaginal, corrimento vaginal (vaginite13).
Distúrbios gerais e do local de aplicação:
- Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): reações no local de aplicação.
Em casos de eventos adversos, notifique ao Sistema de Notificação de Eventos Adversos a Medicamentos – VIGIMED, ou para a Vigilância Sanitária Estadual ou Municipal.
SUPERDOSE
O uso excessivo de Gino-Mizonol pode ocasionar irritação local, que desaparece com a interrupção do tratamento. O nitrato de miconazol é destinado para aplicação local e não para uso oral. No caso de ingestão acidental de grandes quantidades do medicamento, caso necessário, deve-se utilizar um método apropriado de esvaziamento gástrico.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
Siga corretamente o modo de usar, não desaparecendo os sintomas36 procure orientação médica.
Registro M.S. nº 1.5423.0057
Farm. Resp.: Ronan Juliano Pires Faleiro - CRF-GO n° 3772
Geolab Indústria Farmacêutica S/A
VP. 1B QD.08-B MÓDULOS 01 A 08 - DAIA - ANÁPOLIS – GO
CNPJ: 03.485.572/0001-04
Indústria Brasileira
SAC 0800 701 6080