

Permese
EUROFARMA LABORATÓRIOS S.A.
IDENTIFICAÇÃO DO MEDICAMENTO
Permese
dipropionato de betamestasona + fosfato dissódico de betametasona
Injetável 5,0 mg/mL + 2,0 mg/mL
Medicamento similar equivalente ao medicamento de referência.
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Suspensão injetável
Embalagem contendo 1 ampola com 1 mL + 1 seringa1 esterilizada com sistema de segurança
USO INJETÁVEL (INTRAMUSCULAR, INTRA-ARTICULAR, PERIARTICULAR, INTRABÚRSICA, INTRADÉRMICA, INTRALESIONAL2 E EM TECIDOS MOLES)
USO ADULTO E PEDIÁTRICO ACIMA DE 15 ANOS
COMPOSIÇÃO:
Cada mL de Permese suspensão injetável contém:
| dipropionato de betametasona (equivalente a 5,0 mg de betametasona base) | 6,43 mg |
| fosfato dissódico de betametasona (equivalente a 2,0 mg de betametasona base) | 2,63 mg |
| veículo q.s.p. | 1 mL |
Veículo: edetato dissódico, carmelose sódica, macrogol, fosfato de sódio monobásico monoidratado, fosfato dissódico dibásico, polissorbato 80, cloreto de benzalcônio e água para injetáveis
INFORMAÇÕES AO PACIENTE
PARA QUÊ ESTE MEDICAMENTO É INDICADO?
Permese está indicado para o tratamento de doenças agudas e crônicas que respondem aos corticoides. A terapia hormonal com corticosteroide é coadjuvante3 e não substitui a terapêutica4 convencional.
Permese é indicado para os seguintes quadros clínicos:
Alterações osteomusculares e de tecidos moles – Artrite reumatoide5, doenças das articulações6 como: osteoartrite7, bursite8, espondilite anquilosante, espondilite radiculite9, dor no cóccix10, ciática, dor nas costas11, torcicolo12, exostose13, inflamação14 na planta dos pés (fascite).
Condições alérgicas – Asma15, rinite16 alérgica devida a pólen, edema angioneurótico17 (inchaço18 que pode afetar várias partes do organismo), bronquite alérgica, rinite16 alérgica persistente, hipersensibilidade a drogas, doença do soro19, picadas de insetos.
Condições dermatológicas – Dermatite20 atópica (doença alérgica da pele21), líquen simples crônico22, dermatite20 de contato, dermatite20 solar grave, urticária23, líquen plano hipertrófico, necrobiose lipoídica associada com diabetes mellitus24 (espécie de úlcera25 que afeta diabéticos), alopecia areata26 (queda de cabelo27), lúpus28 eritematoso29 discoide, psoríase30, queloides, pênfigo, dermatite20 herpetiforme.
Doenças do colágeno31 – Lúpus28 eritematoso29 sistêmico32, esclerodermia, dermatomiosite, poliarterite nodosa (tipos de doenças autoimunes33).
Tumores Malignos – Para o tratamento paliativo34 de leucemias e linfomas em adultos, leucemia35 aguda da infância.
Outras condições – Síndrome36 adrenogenital (alteração hormonal que pode masculinizar as mulheres), doenças gastrintestinais como: colite37 ulcerativa, ileíte38 regional, doença celíaca; afecções39 dos pés (bursite8, hallux40 rigidus, 5º dedo varo41), afecções39 necessitando de injeções subconjuntivais, transtornos hematológicos que respondem aos corticosteroides, alterações dos rins42 como: síndrome nefrítica43 e síndrome nefrótica44.
A insuficiência45 adrenocortical primária ou secundária poderá ser tratada com Permese, mas deverá haver suplementação46 com mineralocorticoides.
Permese é recomendado para:
- injeções intramusculares para doenças que respondem aos corticoides sistêmicos47;
- injeções diretamente nos tecidos moles afetados, quando indicado;
- injeções intra-articulares e periarticulares em artrites;
- injeções intralesionais para várias condições dermatológicas; e
- injeções locais para certos transtornos inflamatórios e císticos dos pés.
COMO ESTE MEDICAMENTO FUNCIONA?
Permese é uma associação de ésteres de betametasona que produzem efeito anti-inflamatório, antialérgico a antirreumático.
A ação imediata é fornecida pelo fosfato dissódico de betametasona, que é rapidamente absorvido após a administração. A ação prolongada é promovida pelo dipropionato de betametasona que, por ser de absorção lenta, controla os sintomas48 durante longo período de tempo. O tamanho reduzido do cristal de dipropionato de betametasona permite o uso de agulha de fino calibre (até calibre 25) para administração intradérmica e intralesional2.
Permese é uma suspensão aquosa injetável estéril de dipropionato de betametasona e fosfato dissódico de betametasona. Cada mL de Permese contém 5 mg de betametasona como dipropionato e 2 mg de betametasona como fosfato dissódico, em veículo estéril tamponado e conservado.
Os glicocorticoides, como a betametasona, causam profundos e variados efeitos metabólicos e modificam a resposta imunológica do organismo à diversos estímulos.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Este medicamento é contraindicado para pacientes49 que já tiveram qualquer alergia50 ou alguma reação incomum como hipersensibilidade ao dipropionato de betametasona, fosfato dissódico de betametasona, a outros corticoides ou a qualquer um dos componentes da fórmula. Também é contraindicado em pacientes com infecções51 sistêmicas por fungos.
Permese não deverá ser administrado por via intramuscular em pacientes com púrpura52 trombocitopência idiopática53.
Este medicamento é contraindicado para menores de 15 anos.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Permese NÃO deverá ser usado por via intravenosa ou subcutânea54. Técnica estritamente asséptica é mandatória com uso de Permese.
Agite antes de usar.
Por se tratar de uma suspensão injetável, o Permese deve ser aplicado por um profissional de saúde55.
Este medicamento contém dois ésteres de betametasona, um dos quais, o fosfato dissódico de betametasona, desaparece rapidamente do local da injeção56. O potencial para efeitos sistêmicos47 produzidos por esta porção solúvel de Permese deverá ser considerada pelo médico ao usar este preparado.
Após a administração intra-articular deverão ser tomadas precauções pelo paciente para evitar o uso excessivo da articulação57 na qual foi obtido benefício sintomático58.
A administração intramuscular de corticoides deverá ser feita profundamente em grandes massas musculares para evitar atrofia59 tissular60 local.
As injeções em tecidos moles, intralesionais e intra-articulares podem produzir efeitos sistêmicos47 e locais.
É necessário o exame do líquido sinovial61 para excluir um processo infeccioso. Deve-se evitar a injeção56 local em uma articulação57 previamente infectada. O aumento da dor e do edema62 local, restrição maior dos movimentos articulares, febre63 e mal-estar são sugestivos da artrite64 séptica. Se a infecção65 for confirmada, deverá ser instituída terapia antimicrobiana apropriada.
Corticosteroides não deverão ser injetados em articulações6 não estáveis, áreas infectadas ou espaços intervertebrais. Injeções repetidas em articulações6 com osteoartrite7 podem aumentar a destruição articular.
Evitar injetar corticosteroides diretamente nos tendões66 devido à relatos de ruptura tardia do tendão67.
Devido à ocorrência de raros casos de reações anafiláticas68 com o uso parenteral de corticoides, deverão ser tomadas medidas apropriadas de precaução antes da administração, especialmente se o paciente apresentar histórico de alergia50 medicamentosa.
Com o tratamento prolongado, deverá ser considerada a transferência da administração parenteral para a oral, depois da avaliação dos potenciais benefícios e riscos.
Reajustes posológicos poderão ser necessários para remissões ou exacerbações do processo patológico, conforme a resposta individual de cada paciente sob tratamento e quando ocorrer exposição do paciente a situações de estresse, isto é, infecção65 grave, cirurgia ou traumatismo69. Após o término de um tratamento prolongado com corticoides em altas doses, poderá ser necessária monitorização por até um ano.
Os corticoides podem mascarar sinais70 de infecção65 e novas infecções51 podem surgir durante o seu uso. Quando os corticoides são usados, pode ocorrer diminuição da resistência e dificuldade de localizar o sítio de uma nova infecção65.
O uso prolongado de corticoides pode produzir catarata71 subcapsular posterior, especialmente em crianças, glaucoma72 com possível dano ao nervo óptico, podendo ocorrer aumento da incidência73 de infecções51 oculares secundárias devidas à fungos ou vírus74.
Altas doses de corticoides podem causar elevação da pressão arterial75 e retenção hidrossalina, assim como aumento da excreção de potássio. Esses efeitos ocorrem com menos frequência com os derivados sintéticos, exceto quando usados em altas doses.
Deve ser considerada uma dieta com restrição de sal e suplementação46 de potássio. Todos os corticoides aumentam a excreção de cálcio.
Enquanto em tratamento com corticosteroide, os pacientes não deverão ser vacinados contra varíola.
Alguns procedimentos de imunização76 não deverão ser realizados em pacientes recebendo corticosteroides, principalmente em altas doses, devido ao provável risco de complicações neurológicas e falta de resposta por anticorpos77. Quando o corticosteroide estiver sendo utilizado como terapia de reposição (por exemplo, Doença de Addison), os procedimentos de imunização76 poderão ser realizados normalmente.
Pacientes em uso de doses imunossupressoras de corticosteroides deverão ser alertados a evitar a exposição à pessoas portadoras de varicela78 ou sarampo79, e, se forem expostas, deverão procurar orientação médica, principalmente no caso de crianças.
O tratamento com corticosteroides em pacientes com tuberculose80 ativa deverá ser restrito aos casos de tuberculose80 fulminante ou disseminada, nos quais o corticosteroide é usado em associação com um esquema antituberculoso apropriado.
Se os corticoides forem indicados em pacientes com tuberculose80 latente ou com reatividade tuberculina, será necessária uma observação cuidadosa, uma vez que poderá ocorrer reativação da doença. Durante tratamento prolongado, estes pacientes deverão receber quimioprofilaxia. O uso da rifampicina no programa de quimioprofilaxia, devido ao seu efeito de estimulação da depuração dos glicocorticoides, poderá impor um reajuste na dose empregada.
A menor dose possível de corticoide deverá ser usada para controlar a condição sob tratamento. Quando a redução da dose for possível, deverá ser gradual.
Insuficiência45 adrenocortical secundária, induzida pelo medicamento, poderá resultar da retirada muito rápida do corticoide, podendo ser minimizada pela redução gradual da dose. Essa insuficiência45 poderá persistir por meses após a descontinuação do tratamento, portanto, se ocorrer estresse durante este período, a corticoterapia deverá ser reinstituída. Se o paciente já estiver recebendo corticosteroides, a dose deverá ser aumentada. Uma vez que a secreção mineralocorticoide81 pode estar prejudicada, devem ser administrados sal e/ou mineralocorticosteroides concomitantemente.
Os efeitos dos corticoides são aumentados em pacientes com hipotireoidismo82 e em pacientes com cirrose83 hepática84. Aconselha-se cautela ao se usar corticoides em pacientes com herpes simples ocular devido à possibilidade de perfuração da córnea85.
Podem ocorrer transtornos psíquicos com a terapia corticosteroide. Os corticoides podem agravar instabilidade emocional ou tendências psicóticas pré-existentes.
Corticoides deverão ser usados com cautela em colite37 ulcerativa não especificada, quando houver probabilidade de perfuração iminente, abscesso86 ou outra infecção65 piogênica, em diverticulite87, anastomose88 intestinal recente, úlcera péptica89 ativa ou latente, insuficiência renal90, hipertensão arterial91, osteoporose92 e miastenia93 gravis.
Como as complicações do tratamento com corticosteroides são dependentes da dose e duração do tratamento, uma decisão baseada na relação risco/benefício deverá ser tomada para cada caso individual.
O crescimento e desenvolvimento de crianças e lactentes94 fazendo uso prolongado de corticoides deverão ser acompanhados cuidadosamente, pois pode haver distúrbio no crescimento e inibição da produção endógena de cortisol.
O tratamento com corticosteroides pode alterar a motilidade e o número de espermatozoides95.
A administração intra-articular e/ou intralesional2 pode produzir efeitos sistêmicos47 e locais, o que deverá ser levado em consideração em pacientes tratados concomitantemente com corticosteroides oral e/ou parenteral.
Gravidez96 e Lactação97
Como não foram feitos estudos controlados de reprodução98 humana com corticosteroides, o uso de dipropionato de betametasona + fosfato dissódico de betametasona durante a gravidez96 ou em mulheres em idade fértil exige que os possíveis benefícios do fármaco99 sejam pesados contra os potenciais riscos para a mãe, o feto100 e o lactente101. Crianças nascidas de mães que receberam doses substanciais de corticoides durante a gestação deverão ser observadas cuidadosamente para a detecção de sinais70 de hipoadrenalismo.
Devido à possibilidade de surgirem efeitos adversos indesejáveis com o uso do dipropionato de betametasona + fosfato dissódico de betametasona em lactentes94, deverá ser tomada a decisão de descontinuar a amamentação102 ou o tratamento, levando-se em consideração a importância do medicamento para a mãe.
Informe seu médico a ocorrência de gravidez96 na vigência do tratamento ou após o seu término. Informe ao médico se você estiver amamentando.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião- dentista.
Este medicamento pode causar doping.
Interações Medicamentosas
Interações medicamento-medicamento:
O uso concomitante de fenobarbital, rifampicina, fenitoína ou efedrina pode aumentar o metabolismo103 do corticosteroide, reduzindo, assim, seus efeitos terapêuticos.
Pacientes que estejam recebendo corticosteroides e estrogênios concomitantemente deverão ser observados devido à possível ocorrência de exacerbação dos efeitos dos corticosteroides.
O uso concomitante de corticosteroides com diuréticos104 depletores de potássio pode aumentar a hipocalemia105 (diminuição de potássio no sangue106).
O uso concomitante de corticoides com glicosídeos cardíacos pode aumentar a possibilidade de arritmias107 ou intoxicação digitálica associada à hipocalemia105.
Os corticoides podem aumentar a depleção108 de potássio causada pela anfotericina B. Em todos os pacientes em uso de digitálicos, diuréticos104 depletores de potássio e anfotericina B, as concentrações dos eletrólitos109 séricos, principalmente os níveis de potássio, deverão ser monitorizadas cuidadosamente.
O uso concomitante de corticosteroides com anticoagulantes110 cumarínicos pode aumentar ou diminuir os efeitos anticoagulantes110, havendo necessidade de ajustes posológicos.
Os corticosteroides podem diminuir as concentrações sanguíneas dos salicilatos. O ácido acetilsalicílico deve ser utilizado com cuidado em associação aos corticosteroides em pacientes com hipoprotrombinemia (alteração sanguínea que altera a coagulação111 do sangue106). Quando os corticosteroides forem administrados à diabéticos, poderão ser necessários reajustes posológicos dos hipoglicemiantes orais112 e da insulina113.
Terapia concomitante com glicocorticoides pode inibir a resposta à somatotropina.
Interações medicamento-álcool: Os efeitos combinados de anti-inflamatórios não esteroides ou álcool com corticoides podem resultar em aumento da ocorrência ou da gravidade de ulcerações114 gastrintestinais.
Interações medicamento-exames laboratoriais: Os corticoides podem afetar o teste de “nitroblue tetrazolium” para infecção65 bacteriana e produzir resultados falso- negativos.
Informe ao seu médico ou cirurgião-dentista se você estiver fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para sua saúde55.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Conservar em temperatura ambiente (15–30°C). Proteger da luz.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Suspensão homogênea branca, contida em ampola de vidro, isenta de partículas estranhas.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Para administração intramuscular, intra-articular, periarticular, intrabúrsica, intradérmica, intralesional2 e em tecidos moles.
Não está indicado para uso intravenoso ou subcutâneo115.
Este produto só poderá ser injetado por via intramuscular profunda na região glútea116 usando exclusivamente agulha calibre 30/7.
Por se tratar de uma suspensão injetável, o Permese deve ser aplicado por um profissional de saúde55.
Agite antes de usar. Técnica estritamente asséptica é mandatória para o uso do produto.
As necessidades posológicas são variáveis e deverão ser individualizadas com base na doença específica, na gravidade do quadro e na resposta do paciente ao tratamento.
A dose inicial deverá ser mantida ou ajustada até que uma resposta satisfatória seja obtida. Se uma resposta clínica satisfatória não ocorrer após um período de tempo razoável, o tratamento com Permese deverá ser descontinuado e deverá ser iniciada outra terapia apropriada.
Administração sistêmica: para o tratamento sistêmico32, Permese deverá ser iniciado com 1 a 2 mL na maioria das condições, repetindo-se a terapia, quando necessário. A administração é através de injeção intramuscular117 (IM) profunda na região glútea116. A dosagem e a frequência das administrações irão depender da gravidade da condição do paciente e da resposta terapêutica4. Em doenças graves, como lúpus28 eritematoso29 sistêmico32 ou estado de mal asmático já controlados por medidas de emergência118, 2 mL poderão ser necessários inicialmente.
Grande variedade de condições dermatológicas respondem à administração IM de corticoides. Uma injeção56 de 1 mL, repetida de acordo com a resposta terapêutica4, foi considerada como eficaz.
Em doenças do trato respiratório, o início da melhora dos sintomas48 ocorre dentro de poucas horas após a injeção intramuscular117 de dipropionato de betametasona + fosfato dissódico de betametasona. O controle efetivo dos sintomas48 com 1 a 2 mL é obtido na asma15 brônquica, febre do feno119, bronquite alérgica e rinite16 alérgica.
No tratamento da bursite8 aguda ou crônica, resultados excelentes foram obtidos com 1 a 2 mL de dipropionato de betametasona + fosfato dissódico de betametasona administrados por via intramuscular, repetidos se necessário.
Administração local – o uso de anestésicos locais raramente é necessário. Se isto for desejável, Permese poderá ser misturado (na seringa1 e não no frasco) com lidocaína ou procaína 1% a 2% ou anestésicos locais similares. Devem ser evitadas formulações que contenham metilparabeno, propilparabeno e fenol.
A dose necessária de Permese é transferida para a seringa1 e, em seguida, o anestésico. A mistura na seringa1 deve ser agitada levemente.
Em bursites agudas subdeltoides, subcromiais, olecraniais e pré-patelares, uma injeção56 intrabúrsica de 1 a 2 mL de Permese poderá aliviar a dor e restaurar a completa movimentação dentro de poucas horas. A bursite8 crônica poderá ser tratada com doses reduzidas, assim que os sintomas48 agudos estejam controlados. Em tenossinovite aguda, tendinite120 e peritendinite, uma injeção56 de Permese poderá trazer alívio. Em formas crônicas destas doenças, poderão ser necessárias injeções repetidas, de acordo com as necessidades do paciente. Após administração intra-articular de 0,5 mL a 2 mL de Permese ocorre alívio da dor, da sensibilidade e rigidez associadas à osteoartrite7 e à artrite reumatoide5 dentro de 2 a 4 horas. A duração do alívio, que varia amplamente nas duas condições, é de 4 semanas ou mais, na maioria dos casos.
Uma injeção56 intra-articular de Permese é bem tolerada pela articulação57 e pelos tecidos periarticulares. As doses recomendadas para injeção56 intra-articular são:
- Grandes articulações6 (joelho, bacia, ombro): 1 – 2 mL
- Médias articulações6 (cotovelo, punho, tornozelo121): 0,5 – 1 mL
- Pequenas articulações6 (pé, mão122, tórax123) 0,25 – 0,5 mL
Afecções39 dermatológicas poderão responder à administração intralesional2 de Permese. A resposta de algumas lesões124 não tratadas diretamente poderá ser devida à um leve efeito sistêmico32 do fármaco99. No tratamento intralesional2, é recomendada uma dose intradérmica de 0,2 mL/cm² de Permese distribuída igualmente com uma seringa1 do tipo tuberculina e agulha de calibre 26. A quantidade total de Permese aplicada em todas as áreas não deverá exceder 1 mL por semana.
Permese poderá ser usado eficazmente em afecções39 do pé que sejam suscetíveis aos corticoides. Bursite8 sob heloma (espessamento de uma das camadas da pele21) duro ou mole poderá ser controlada com duas injeções sucessivas, de 0,25 mL cada. Em algumas condições, como hallux40 rigidus, 5º dedo varo41 e artrite64 gotosa aguda, a melhora dos sintomas48 poderá ser rápida. Uma seringa1 do tipo tuberculina e uma agulha de calibre 25 são adequadas para a maioria das injeções. As doses recomendadas, em intervalos de aproximadamente uma semana, são: bursite8 sob heloma duro ou mole, 0,25 mL – 0,5 mL; bursite8 sob esporão de calcâneo125, 0,5 mL; bursite8 sobre hallux40 rigidus, 0,5 mL; bursite8 sobre o 5º dedo varo41, 0,5 mL; cisto sinovial, 0,25 mL – 0,5 mL; neuralgia126 de Morton (metatarsalgia), 0,25 mL – 0,5 mL; tenossinovite, 0,5 mL; periostite do cuboide, 0,5 mL; artrite64 gotosa aguda, 0,5 mL – 1 mL.
Depois de obtida uma resposta favorável, a dosagem de manutenção deverá ser determinada através da diminuição da dose inicial em decréscimos graduais, a intervalos apropriados, até que seja encontrada a dose mínima capaz de manter uma resposta clínica adequada.
A exposição do paciente a situações de estresse não relacionadas à doença em curso poderá necessitar de aumento da dose de Permese. Se for necessária a descontinuação do fármaco99 após tratamento prolongado, a dose deverá ser reduzida gradualmente.
Instruções de uso do conjunto seringa1 e agulha com sistema de segurança (vide figuras explicativas abaixo):
- Se a agulha já estiver previamente conectada, puxe para trás o dispositivo de segurança azul.
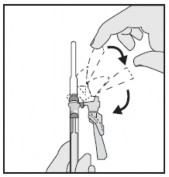
- Caso a agulha não esteja conectada, conecte-a à seringa1 com firmeza.
- Se precisar girar o dispositivo de segurança para orientar o bisel ou ler a escala, segure o dispositivo azul de segurança no ponto em que ele se conecta com a seringa1 com uma das mãos127 e gire a seringa1 com a outra mão122.
- Remova o protetor da agulha e realize o procedimento de aspiração da suspensão de Permese da ampola normalmente.
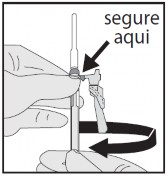
Atenção: Não use as duas mãos127 para fechar o dispositivo azul de segurança após aplicação.
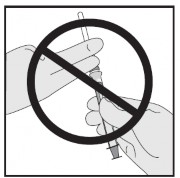
- Após aplicação, empurre o dispositivo azul com o dedo.
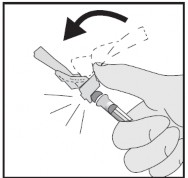
- Continue a apertar até que a agulha esteja totalmente coberta pelo dispositivo e o dispositivo esteja travado.
Você ouvirá um clique quando o dispositivo de segurança azul estiver travado. Confirme visualmente se a agulha está coberta.
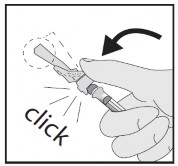
- Aperte o êmbolo128 para quebra-lo, impedindo assim a sua reutilização.
- Após o único uso, descarte o conjunto agulha + seringa1 imediatamente num recipiente aprovado para objetos cortantes, conforme normas de segurança.
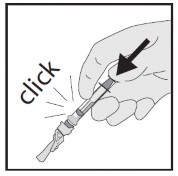
ADVERTÊNCIAS
A quebra do dispositivo pode causar respingos. Assegure-se de que a seringa1 esteja vazia antes de quebrar o êmbolo128. Para maior segurança, ao quebrar o êmbolo128, segure a seringa1 voltada para baixo, longe de si próprio e dos outros.
Caso o êmbolo128 quebre prematuramente durante a injeção56, continue a apertá-lo até que a dose seja completamente administrada.
Atenção: O produto depois de aberto não pode ser reutilizado. O conteúdo restante não deve ser utilizado em outras aplicações. Caso houver sobra, seu conteúdo deve ser descartado.
A seringa1 após a aplicação não deve ser reutilizada. Deve ser descartada em recipiente apropriado.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
Informe seu médico o aparecimento de reações desagradáveis, como alterações osteomusculares, gastrintestinais, dermatológicas, neurológicas, psiquiátricas, hiper ou hipopigmentação, atrofia59 cutânea129 e subcutânea54, abscessos130 estéreis, rubor local pós-injeção56 (em seguida ao uso intra-articular).
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Por se tratar de um corticosteroide de administração parenteral, que deve ser administrado por um profissional habilitado de saúde55, a possibilidade de esquecimento de dose é remota. Em caso de esquecimento, programe-se para administrar o medicamento assim que possível.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Reações adversas a dipropionato de betametasona + fosfato dissódico de betametasona, como aos demais corticosteroides, estão relacionadas com a posologia e a duração do tratamento. Geralmente estas reações podem reverter-se ao mínimo com a redução da posologia, o que é geralmente preferível à suspensão do tratamento farmacológico. Embora a incidência73 de reações adversas a dipropionato de betametasona + fosfato dissódico de betametasona seja baixa, a possível ocorrência de efeitos colaterais131 conhecidos dos corticoides deverá ser considerada.
As reações adversas relacionadas ao uso de dipropionato de betametasona + fosfato dissódico de betametasona, de acordo com a frequência de ocorrência e o sistema acometido são:
Reações comuns (ocorrem entre 1% e 10% dos pacientes que utilizam este medicamento):
- Sistema nervoso central132: insônia.
- Sistema gastrintestinal: dispepsia133; aumento de apetite.
- Organismo como um todo: aumento da incidência73 de infecções51
Reações incomuns (ocorrem entre 0,1% e 1% dos pacientes que utilizam este medicamento):
- Pele21: dificuldade de cicatrização; pequenos vasos superficiais visíveis; infecções51 subcutâneas; pele21 fina e frágil; inflamação14 do folículo piloso134; coceira.
- Sistema endócrino135: diabetes mellitus24; síndrome de Cushing136 (estado decorrente do excesso de corticoide). Sistema musculoesquelético: osteoporose92 Sistema gastrintestinal: sangramento digestivo.
- Sistema geniturinário: redução de potássio no sangue106; retenção de sódio e água; irregularidade menstrual.
Reações raras (ocorrem entre 0,01% e 0,1% dos pacientes que utilizaram este medicamento):
- Pele21: estrias; hematomas137; reação de hipersensibilidade; espinhas; urticária23; sudorese138 excessiva; rash139 cutâneo140; vermelhidão da face141 e pescoço142 após aplicação; sintomas48 e sinais70 no local de aplicação; aumento de pelos; diminuição da pigmentação cutânea129.
- Sistema nervoso central132: depressão; convulsões; tontura143; cefaleia144; confusão mental; euforia; distúrbio de personalidade; alteração de humor.
- Sistema gastrintestinal: úlcera péptica89 com possível perfuração e hemorragia145; aumento do tamanho do fígado146; distensão abdominal; alteração em exames do fígado146.
- Sistema geniturinário: diminuição da contagem de espermatozoides95.
- Sistema musculoesquelético: lesão147 muscular induzida por corticoide; fraqueza muscular; dor muscular.
- Olhos148: aumento de pressão intraocular149; catarata71.
- Sistema cardiovascular150: pressão alta; arritmias107 cardíacas; insuficiência cardíaca congestiva151; edema62 agudo152 do pulmão153; trombose venosa profunda154; vasculite155.
- Organismo como um todo: ganho de peso; infecção65 por fungos.
Reações cuja incidência73 não está determinada: soluços, alcalose156 hipocalêmica (aumento do pH do sangue106 por falta de potássio), perda de massa muscular, fraturas, necrose157 asséptica da cabeça158 do fêmur159 e do úmero160, fratura161 patológica dos ossos longos162, ruptura de tendão67, instabilidade articular decorrente de repetidas injeções intra- articulares, pancreatite163, esofagite164 ulcerativa, adelgaçamento cutâneo140, petéquias165 e equimose166, eritema167 (vermelhidão) facial, diminuição ou supressão da reação aos testes cutâneos, edema angioneurótico17, aumento da pressão intracraniana com edema de papila168 (pseudotumor cerebral), diminuição do crescimento na infância e no período intrauterino, falta de resposta adrenocortical e pituitária, diminuição da tolerância aos carboidratos, manifestações clínicas de diabetes mellitus24 latente, aumento das necessidades diárias de insulina113 ou agentes hipoglicemiantes orais112 em diabéticos, glaucoma72, balanço nitrogenado negativo devido ao catabolismo169 proteico, manifestações psicóticas, reações anafiláticas68, hipotensão170, choque171, dermatite20 alérgica, exoftalmia, agravamento dos sintomas48 na miastenia93 gravis.
Reações adversas relacionadas ao tratamento corticoide parenteral incluem: casos raros de cegueira associados ao tratamento intralesional2 da face141 e da cabeça158; hiper ou hipopigmentação, atrofia59 cutânea129 e subcutânea54; abscessos130 estéreis; área de rubor pós-injeção56 (em seguida ao uso intra-articular); artropatia172 do tipo Charcot.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Sintomas48
A superdose aguda de corticosteroides não leva à situações de risco de vida. Exceto nos casos de doses muito elevadas, alguns dias de dosagem excessiva não parecem produzir resultados prejudiciais na ausência de contraindicações específicas, como em pacientes com diabetes mellitus24, glaucoma72, úlcera péptica89 ativa ou em pacientes que estejam fazendo uso de medicamentos como digitálicos, anticoagulantes110 cumarínicos ou diuréticos104 depletores de potássio.
Tratamento
Complicações resultantes dos efeitos metabólicos dos corticosteroides ou dos efeitos deletérios da doença de base, ou concomitante, ou resultante de interações medicamentosas deverão ser tratadas apropriadamente.
Manter ingestão adequada de líquidos e monitorizar os eletrólitos109 séricos e urinários, com especial atenção ao balanço de sódio e potássio. Tratar o desequilíbrio eletrolítico, se necessário.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
M.S.: 1.0043.1357
Farm. Resp.: Dra. Ivanete A. Dias Assi CRF-SP 41.116
Fabricado e Registrado por:
EUROFARMA LABORATÓRIOS S.A.
Rod. Pres. Castello Branco, 3.565 Itapevi - SP
CNPJ: 61.190.096/0001-92
Indústria Brasileira
SAC 0800 703 1550






