Prosigne
CRISTÁLIA PRODUTOS QUÍMICOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Prosigne®
toxina1 botulínica A
APRESENTAÇÕES
Pó liófilo injetável – 50 e 100 U
Embalagens contendo 1 frasco-ampola.
USO INTRAMUSCULAR E INTRADÉRMICO
USO ADULTO E PEDIÁTRICO ACIMA DE 2 ANOS DE IDADE
COMPOSIÇÃO
|
Cada frasco-ampola contém: |
50 U |
100 U |
|
toxina1 botulínica A |
50 U |
100 U |
|
excipiente qsp |
1 frasco-ampola |
1 frasco-ampola |
|
(excipientes: gelatina, dextrana 20 e sacarose) |
||
O Prosigne® é uma forma liofilizada2 estéril da toxina1 botulínica A purificada, produzida a partir da toxina1 bruta da cultura de cepas3 Hall de Clostridium botulinum, cultivada em um meio contendo tripsina, caseína e extrato de levedura. Uma série de procedimentos de purificação foi realizada para obter um complexo cristalino4 consistindo de proteína toxina1 ativa de alto peso molecular e uma hematoglutinina associada. Após a redissolução e diálise5, uma quantidade precisa da toxina1 estéril filtrada (0,2 micron) é adicionada a uma solução contendo gelatina, dextrana e sacarose, e liofilizada2.
Cada frasco de Prosigne® contém 50U ou 100 U de toxina1 de Clostridium botulinum A, 5mg de gelatina, 25 mg de dextrana e 25 mg de sacarose. Diluir com solução salina normal antes do uso. O produto branco liofilizado6 torna-se uma solução incolor ou amarela transparente após a reconstituição.
Uma unidade (U) de Prosigne® corresponde a 1 DL50 da toxina1 botulínica A quando injetada intraperitonealmente (interior da cavidade abdominal7) no camundongo.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Este medicamento é indicado no tratamento da sintomatologia de doenças tais como: estrabismo8 (defeito no alinhamento dos olhos9), blefaroespasmo10 (fechamento repetitivo e involuntário da pálpebra provocado por contrações dos músculos11 orbiculares dos olhos9), espasmo12 hemifacial (contração involuntária13 e repetitiva de metade da face14), torcicolo15 espasmódico (contração involuntária13 e repetitiva dos músculos do pescoço16), distonia17 cervical (contração involuntária13 dos músculos do pescoço16), espasticidade18 (rigidez muscular que dificulta ou impossibilita o movimento), paralisia19 cerebral, reabilitação muscular, linhas faciais hipercinéticas (rugas de expressão da testa, glabela, ao redor dos olhos9, boca20 e platisma) e hiperidrose21 em adultos (produção excessiva de suor).
COMO ESTE MEDICAMENTO FUNCIONA?
Prosigne® promove a paralisação temporária dos músculos11, evitando a repetição dos movimentos causadores das rugas e linhas de expressão. Essa paralisação temporária impede que o músculo se contraia. A toxina1 botulínica também é usada para o tratamento de determinadas condições do músculo ocular causada por distúrbios nervosos.
Início da ação:
No tratamento do blefaroespasmo10 (fechamento repetitivo e involuntário da pálpebra provocado por contrações dos músculos11 orbiculares dos olhos9), o efeito inicial das injeções é notado em 3 dias, alcançando um pico entre 1 a 2 semanas após o tratamento.
No tratamento do estrabismo8, as doses iniciais caracteristicamente produzem paralisia19 dos músculos11 injetados começando 1 ou 2 dias após a injeção22, e aumentando a intensidade durante a primeira semana.
Duração da ação:
No tratamento de blefaroespasmo10, cada tratamento dura aproximadamente 3 meses.
No tratamento do estrabismo8, a paralisia19 dura de 2 a 6 semanas e diminui gradualmente em 2 a 6 semanas adicionais.
No tratamento das linhas hipercinéticas (rugas de expressão), o início de ação começa nas primeiras 24-72 horas com duração média aproximada entre 3-6 meses dependendo de cada paciente.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
O Prosigne® é contraindicado em indivíduos com histórico de reações anafiláticas23, distúrbios do sangramento, hipersensibilidade conhecida a esta formulação e na presença de infecção24 no local da injeção22.
Gravidez25:
CATEGORIA C
Não há estudos adequados bem controlados sobre a administração da toxina1 botulínica em mulheres durante a gravidez25. Considerando que nem sempre são preditivos de resposta humana, a toxina1 botulínica somente deve ser administrada durante a gravidez25 se os potenciais benefícios justificarem o risco potencial para o feto26. Se este medicamento for utilizado durante a gestação ou se a mulher engravidar durante o tratamento, a paciente deve ser advertida quanto aos potenciais riscos, incluindo abortamento27 ou malformações28 fetais.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Informe seu médico sobre a ocorrência de gravidez25 na vigência do tratamento ou após seu término.
Informar ao médico se está amamentando.
Este medicamento é contraindicado para menores de 2 anos de idade.
Atenção diabéticos: contém açúcar29.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
As dosagens recomendadas e a frequência de administração não devem ser ultrapassadas. Não foram relatados casos de toxicidade30 sistêmica resultante de injeção22 ou ingestão oral acidentais. Se algum desses eventos ocorrer, o paciente deve ser acompanhado por um médico por vários dias, em ambulatório ou consultório, para a observação de sinais31 ou sintomas32 de debilidade sistemática ou paralisia19 muscular. O conteúdo total de uma ampola é inferior à dose estimada de toxidade sistêmica em seres humanos que pesam 6 quilos ou mais.
Injeções de toxina1 botulínica devem ser feitas somente por profissionais médicos treinados, mesmo quando usado para fins cosméticos.
Gravidez25:
CATEGORIA C
Não há estudos adequados bem controlados sobre a administração da toxina1 botulínica em mulheres durante a gravidez25. Considerando que nem sempre são preditivos de resposta humana, a toxina1 botulínica somente deve ser administrada durante a gravidez25 se os potenciais benefícios justificarem o risco potencial para o feto26. Se este medicamento for utilizado durante a gestação ou se a mulher engravidar durante o tratamento, a paciente deve ser advertida quanto aos potenciais riscos, incluindo abortamento27 ou malformações28 fetais.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Carcinogenicidade:
Não foram realizados estudos em longo prazo para avaliação do potencial de carcinogenicidade da toxina1 botulínica A.
Lactação33:
Não existem dados disponíveis sobre a excreção da toxina1 botulínica no leite humano. Como muitas drogas são excretadas pelo leite humano, devem ser tomadas as devidas precauções quando a toxina1 botulínica for administrada a mulheres durante a lactação33.
Uso Pediátrico:
Ficou comprovado a segurança e eficácia em crianças com menos de 12 anos de idade que utilizaram Prosigne® em diversas patologias (espasticidade18, paralisia19 cerebral e reabilitação muscular) atráves de ensaios clínicos34 controlados, multicêntricos internacionais e estudos clínicos (fases I, II e III).
Pacientes idosos:
Estudos apropriados relacionando a idade aos efeitos da toxina1 botulínica A não foram realizados na população geriátrica. Contudo, não foram documentados problemas geriátricos específicos.
Efeitos na habilidade de dirigir veículos ou operar máquinas:
Desconhecem-se, até o momento, os efeitos sobre o ato de dirigir ou operar máquinas.
O efeito da toxina1 botulínica pode ser potencializado por antibióticos aminoglicosídicos (amicacina, gentamicina, estreptomicina); ciclosporina; cloroquina; hidroxicloroquina; D-penicilamina ou quaisquer outras substâncias que interfiram com a transmissão neuromuscular. Os pacientes que fazem uso desses fármacos devem ser cuidadosamente observados quando utilizarem a toxina1 botulínica. Também devem ser tomadas precauções quando a toxina1 botulínica for utilizada no tratamento de pacientes com miastenia35 gravis, síndrome36 de Eaton Lambert, esclerose37 amiotrófica ou distúrbios que produzam disfunção neuromuscular periférica.
Pacientes que utilizam anticoagulantes38 orais; derivados do ácido acetilsalicílico; derivados de vitamina39 E ou ginkgo biloba podem apresentar risco de formação de hematomas40 e equimoses41 no local de aplicação.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde42.
Atenção diabéticos: contém açúcar29.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Conservar o produto refrigerado em geladeira, em temperatura entre 2 e 8ºC, protegido da luz. A solução reconstituída deve ser armazenada sob refrigeração, entre 2 e 8ºC, e deve ser utilizada em até quatro horas após a reconstituição.
O prazo de validade do produto é de 24 meses a partir da data de fabricação, impressa na embalagem. Não utilize medicamento vencido.
Número de lote e datas de fabricação e validade: videm embalagem. Não use medicamento com o prazo de validade vencido.
Guarde-o em sua embalagem original.
Após o preparo, manter este medicamento sob refrigeração, em temperatura entre 2º e 8ºC, por até quatro horas. Após esse período ele não deve ser mais utilizado.
Anteriormente à reconstituição, Prosigne® apresenta-se como um grânulo branco liofilizado6, isento de partículas estranhas. A solução reconstituída em solução salina é incolor ou amarelo transparente.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
COMO DEVO USAR ESTE MEDICAMENTO?
A posologia e método de administração dependem do paciente, da localização e da extensão do comprometimento dos grupos musculares envolvidos. A injeção22 deve ser intramuscular ou intradérmica. O uso em pacientes idosos não requer adaptação da posologia, recomendando-se as mesmas doses do adulto. Em crianças a posologia deve ser calculada em função do peso corporal.
Espasticidade18:
Espasticidade18 associada ao acidente vascular cerebral43: a dose exata e o número dos locais de injeção22 devem ser titulados individualmente pelo seu médico. As doses não devem exceder a 360 U divididas entre os músculos11 selecionados.
Para tratamento da espasticidade18 relacionada à paralisia19 cerebral (pediátrica): Prosigne® é injetado por via intramuscular para o tratamento da marcha normal devida ao tônus muscular44 aumentado. As doses de 4 a 8 U/kg podem ser administradas em duas injeções em intervalos de quatro semanas,. A repetição da dose deve ser feita quando o efeito clínico da injeção22 anterior diminui, mas a frequência não deve ser inferior a dois meses. A dose máxima recomendada em uma única sessão de tratamento é de 200 U.
Distonias45:
Para tratamento das distonias45: as doses variam conforme o caso e a extensão do processo.
Espasmo12 hemifacial:
Pacientes com espasmo12 hemifacial devem ser tratados do mesmo modo descrito para o blefaroespasmo10 unilateral. Injeções adicionais podem ser necessárias a critério do médico.
Para o tratamento da distonia17 cervical:
A dose deve ser titulada individualmente baseando-se na posição da cabeça46 e do pescoço47 do indivíduo, da localização da dor, da hipertrofia48 muscular, do peso do paciente, e da resposta do paciente em caso de repetição do procedimento. As doses de Prosigne® (toxina1 botulínica A) reconstituído variaram entre 95U e 360 U (com média aproximada de 240 U). Não se recomenda o uso de injeções de reforço. O intervalo entre as doses não deve ser menor do que dois meses.
O número ideal de injeções depende do tamanho do músculo a ser desnervado quimicamente.
Hiperidrose21:
Hiperidrose21 axilar
A área a ser injetada deve ser definida utilizando técnicas padrão de coloração.
O Prosigne® (toxina1 botulínica A) reconstituído é injetado por via intradérmica, em cada axila, na dose de 50 U distribuídas uniformemente em vários locais de aproximadamente 1 a 2 cm cada um.
A repetição das injeções para hiperidrose21 axilar deve ser feita quando os efeitos das injeções prévias diminuírem, mas usualmente não deve ser feita com frequência maior que a cada dois meses.
Hiperidrose21 palmar49:
O Prosigne® reconstituído é injetado por via intradérmica nas palmas das mãos50.
As doses podem variar de 50 a 150 unidades por palma, distribuídas uniformemente em vários locais de aproximadamente 1 a 2 cm cada um, na área hiperidrótica. A dose total por palma pode ser modificada com base no tamanho da mão51.
A repetição das injeções para a hiperidrose21 palmar49 deve ser feita quando os efeitos clínicos das injeções prévias diminuírem, mas usualmente não são mais frequentes do que a cada dois meses.
Linhas hipercinéticas de expressão:
O Prosigne® reconstituído é administrado em cada um dos 5 locais: 2 em cada músculo corrugador e 1 no músculo piramidal52, com dose total de 20 U.
Para reduzir a incidência53 de ptose54 (queda das pálpebras55 superiores) como complicação, evitar a injeção22 próxima do músculo elevador da pálpebra superior. A resposta clínica subótima ou a curta duração da ação podem ser resultados de subdose, aplicação em locais indevidos ou uso da toxina1 botulínica diluída por tempo prolongado. Além disso, é fundamental uma boa avaliação clínica das rugas hipercinéticas, excluindo-se outros fatores envolvidos com a formação das rugas e considerando as variações anatômicas individuais. Como em qualquer outro tratamento de rejuvenescimento facial, devem ser consideradas as expectativas irreais por parte do paciente.
Duração do tratamento: de 3 a 6 meses.
Espasmos56 musculares, Síndromes de compressão nervosa, Desordem do VII Par e TCE (trauma crânio57 encefálico):
Utilizar 10 U – 100 U divididos entre os principais pontos gatilhos musculares comprometidos. Sendo em média 10 U por ponto gatilho do músculo comprometido. É importante ressaltar que as doses podem sofrer variações dependen do do paciente, da intensidade dos sintomas32 e da experiência do médico respectivamente.
Duração do tratamento: 3 meses.
Doses:
As doses variam de acordo com a avaliação individual de cada paciente e, portanto, sugere-se:
1. Para blefaroespasmo10 e espasmo12 hemifacial: A dose inicial de cada ponto é 2,5 U/0,05 mL ou 2,5 U/0,1 mL. Se o tratamento inicial for considerado insuficiente uma semana após, uma injeção22 suplementar pode ser administrada.
Dose dupla de 5 U/0,5 mL pode ser dada para pacientes58 recrudescentes. Porém, a limitação da dose total em 55 U para uma injeção22 e 200 U para um mês não deve ser excedida.
2. Para estrabismo8: para estrabismo8 muscular vertical horizontal e vertical de menos de 20 dioptrias, a dose inicial em cada músculo é de 1,25 a 2,5 U; para estrabismo8 horizontal de 20 a 40 dioptrias, a dose inicial em cada músculo é de 2,5 U; para estrabismo8 horizontal de 40 a 50 dioptrias, a dose inicial em cada músculo é de 2,5 U e pode ser aumentada (em 5,0 U cada vez) dependendo da resposta: para paralisia19 persistente do 6º nervo cranial durando mais de um mês, dose de 1,25 a 2,5 U pode ser injetada no músculo reto59 medial.
O volume de injeção22 em cada músculo não deve exceder 0,1 mL.
Podem ser administradas injeções complementares para pacientes58 tendo resposta insuficiente.
Para pacientes58 recrudescentes, a dose pode ser repetida ou aumentada irregularmente, porém para cada músculo a dose máxima deve ser menor que 5 U por injeção22.
3. Em crianças a posologia deve ser calculada em função do peso corporal. Cada unidade U corresponde à dose intraperitonial letal média (DL-50) de Prosigne® (toxina1 botulínica A), reconstituída, conforme cálculo60 em camundongos.
4. Nas linhas hipercinéticas (rugas de expressão) as doses por músculo sugeridas são: orbicular dos olhos9 (pés-de-galinha) – 2 U em cada ponto assinalado; ventre do músculo frontal – 4 U em cada ponto assinalado; corrugador – 5 U em cada ponto assinalado; prócero –5 U no ponto assinalado.
Diluição do Prosigne®
A diluição do Prosigne® com solução salina estéril normal deve ser feita cuidadosamente com base nas necessidades reais. A seguir, uma tabela de referência é apresentada com as diluições recomendadas:
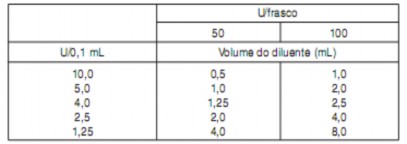
Agitar o frasco suavemente após a adição da solução salina estéril normal para completar a dissolução.
A solução reconstituída deve ser usada imediatamente ou armazenada em refrigerador entre 2 e 8ºC e usada dentro de 4 horas. O frasco e a seringa61 usados com o medicamento, assim como a solução residual de Prosigne® devem ser descartados após utilização.
Siga a orientação do seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa e o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
A toxina1 botulínica A possui efeito temporário, sendo administrada em intervalos espaçados de tempo.
Em caso de dúvidas, procure orientação do farmacêutico ou de se médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Reações adversas que podem ocorrer em pacientes recebendo terapia com Prosigne® para blefaroespasmo10, espasmo12 hemifacial e no tratamento das rugas de expressão:
Comum (> 1% e ≤ 10%): fraqueza dos músculos faciais62, ardência nos olhos9, dor local, lacrimejamento, Ptose54 palpebral leve.
Rara (> 0,01% e ≤ 0,1%): astenia63, diplopia64, ptose54 temporária da pálpebra, redução da pálpebra inferior, redução dos movimentos de piscar os olhos9, fechamento incompleto da pálpebra.
Contudo, todos os sintomas32 desaparecem sem qualquer terapia depois de 3 a 8 semanas.
Pacientes recebendo terapia com Prosigne® para estrabismo8, podem apresentar:
Rara (> 0,01% e ≤ 0,1%): ptose54 palpebral temporária e de graus diferentes, desvios verticais, midríase65 relacionada com a difusão da toxina1 para os músculos11 adjacentes.
Os sintomas32 desaparecem sem qualquer terapia dentro de algumas semanas.
Foram relatados casos de erupção66 difusa na pele67 e casos de edema68 local na pálpebra logo após a aplicação e que se prolongaram durante vários dias.
Não foi encontrado nenhum efeito clínico adverso da toxina1 botulínica A em pacientes que receberam doses baixas da toxina1 botulínica, como < 20 U.
A análise por eletromiografia69 de fibra isolada mostrou que a injeção22 de quantidades relativamente altas de toxina1 botulínica (140 a 165 U) conduz a difusão da toxina1, fraqueza de músculos11 distantes e efeitos subclínicos não caracterizados. Porém, isso pode ser resolvido com melhora na técnica de injeção22 e padronização consistente da atividade biológica do produto final.
Em indivíduos tratados com Prosigne® para o torcicolo15 espasmódico, podem ocorrer: Comum (> 1% e ≤ 10%): dispneia70, disfagia71 leve e transitória.
Vários pacientes apresentaram obstrução das vias aéreas superiores após tratamento com doses relativamente altas de toxina1 botulínica (> 150 U).
Desde a introdução da toxina1 botulínica A em uso clínico, a possibilidade de desenvolvimento de anticorpos72 neutralizantes é uma das mais temidas consequências de injeções repetidas. Isto parece ocorrer quando doses relativamente altas são empregadas, especificamente no tratamento de torcicolo15 e distonia17 de extremidade, e não foi encontrado no tratamento de blefaroespasmo10 e espasmo12 hemifacial. Portanto, é recomendável que os médicos empreguem as menores doses possíveis ao tratar dessas condições.
Reações gerais:
Conforme esperado para qualquer injeção intramuscular73, podem ocorrer as reações:
Comum (> 1% e ≤ 10%): hematomas40, astenia63, edema68 no local da injeção22, equimoses41, sensibilidade anormal à compressão e/ou ferimento no local.
Rara (> 0,01% e ≤ 0,1%): dor no local da injeção22.
A flacidez local representa a ação farmacológica esperada da toxina1 botulínica.
Em < 0,01% foram relatados os seguintes eventos adversos desde que a droga foi introduzida no mercado e a relação causal com a toxina1 botulínica é desconhecida: erupção66 cutânea74 (incluindo eritema multiforme75, urticária76 e erupção66 psoriásica), prurido77 e reação alérgica78. Foram também relatados casos raros e eventos adversos envolvendo o sistema cardiovascular79, incluindo arritmia80 e infarto do miocárdio81, em alguns casos fatais. Alguns destes pacientes apresentavam fatores de risco, incluindo doença cardiovascular. A relação causal com a toxina1 botulínica é desconhecida.
Informe ao seu médico, cirurgião-centista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu Serviço de Atendimento.
Os pacientes sedentários devem ser advertidos no sentido de reassumirem suas atividades lenta e cuidadosamente após a administração da toxina1 botulínica.
Em caso de qualquer dificuldade para engolir, falar ou respirar, o médico deve ser contatado imediatamente.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Na rara possibilidade de superdosagem ou aplicação no músculo errado, pode ser considerada a administração de antitoxina botulínica, no mesmo local, assim que possível, e no máximo dentro de 21 horas, para reduzir ou bloquear o local afetado pela toxina1 botulínica. A antitoxina (antitoxina botulínica trivalente, equina, tipos A, B e E) é uma proteína estranha, com risco significativo de efeitos colaterais82 sistêmicos83 e capacidade imunizante84. Os riscos de seu uso devem ser considerados em relação aos resultados adversos da toxina1 botulínica.
Os sinais31 ou sintomas32 de superdosagem não são evidentes imediatamente após a injeção22. Se ocorrer a injeção22 ou ingestão oral acidental, o paciente deve ter supervisão médica por vários dias para sinais31 ou sintomas32 de fraqueza sistêmica ou paralisia19 muscular.
Pode ser necessário suporte respiratório se houver aplicação de doses excessivas que provoquem paralisia19 dos músculos respiratórios85.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001 se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Nº lote, data de fabricação e prazo de validade: vide cartucho/rótulo.
MS nº 1.0298.0317
Farm. Resp.: Dr. José Carlos Módolo – CRF/SP nº 10.446
Fabricado por:
Lanzhou Institute of Biological Products
888#, Yanchang Road, Lanzhou, Gansu, República Popular da China
Registrado e Importado por:
Cristália Produtos Químicos Farmacêuticos Ltda.
Rodovia Itapira-Lindóia, km 14 – Itapira – SP
CNPJ nº 44.734.671/0001-51
Indústria Brasileira
SAC 0800 7011918