

Plasmafundin
LABORATÓRIOS B. BRAUN S/A
IDENTIFICAÇÃO DO MEDICAMENTO
Plasmafundin®
cloreto de sódio + cloreto de potássio + cloreto de magnésio hexaidratado + acetato de sódio tri-hidratado + gliconato de sódio
Injetável
FORMA FARMACÊUTICA E APRESENTAÇÃO:
solução injetável estéril, límpida, incolor e isentas de partículas visíveis a olho1 nu em frascos ampolas plásticos transparentes – Ecoflac® plus (Sistema fechado)
Embalagens contendo: 20 unidades de 500 mL por caixa.
VIA INTRAVENOSA
USO ADULTO e PEDIÁTRICO
COMPOSIÇÃO:
Plasmafundin® contém em sua formulação:
| cloreto de sódio | 0,526 g |
| cloreto de potássio | 0,037 g |
| cloreto de magnésio hexaidratado | 0,030 g |
| acetato de sódio tri-hidratado | 0,368 g |
| gliconato de sódio | 0,502 g |
| ajuste de pH água para injetáveis q.s.p. | 100 mL |
|
Conteúdo eletrolítico |
|
|
Sódio |
140,0 mEq/L |
|
Potássio |
5,0 mEq/L |
|
Magnésio |
3,0 mEq/L |
|
Cloreto |
98,0 mEq/L |
|
Acetato |
27,0 mEq/L |
|
Gliconato |
23,0 mEq/L |
pH= 7,4 (6,5–8,0)
Osmolaridade2: 294 mOsmol/L
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Plasmafundin® é fonte de água e eletrólitos3, sendo indicado para restauração de volume intravascular4, reposição eletrolítica ou como agente alcalinizante em casos de acidose metabólica5.
Plasmafundin® é compatível com sangue6 ou componentes sanguíneos e sua administração não causa perturbações na homeostase eletrolítica e no equilíbrio ácido-base.
COMO ESTE MEDICAMENTO FUNCIONA?
Plasmafundin® é uma solução com osmolalidade7, pH e concentrações de eletrólitos3, semelhantes àquelas encontradas no plasma8 humano normal.
Plasmafundin® é usado para corrigir perdas de água e eletrólitos3 visando restaurar e manter as condições osmóticas normais nos espaços intra e extracelular.
O padrão aniônico da solução representa uma combinação balanceada de cloreto, acetato e gliconato, que neutralizam acidose metabólica5.
As propriedades farmacocinéticas e farmacodinâmicas dos componentes de Plasmafundin® são semelhantes ao seu comportamento fisiológico9.
Uma vez que Plasmafundin® é administrado por via intravenosa sua biodisponibilidade é de 100 %.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
- Hipervolemia;
- Bloqueio cardíaco10;
- Insuficiência renal11;
- Edema12 geral grave;
- Hipercloremia;
- Hipernatremia13;
- Hipercaliemia;
- Hipersensibilidade aos componentes da formulação;
- É contraindicado o uso concomitante com diuréticos14 poupadores de potássio;
- Alcalose15 metabólica ou respiratória.
Compostos formadores de bicarbonato não devem ser administrados a pacientes com alcalose15 metabólica ou respiratória, hipocalcemia16, ou hipocloridria. Durante o tratamento da acidose17, a monitorização frequente das concentrações séricas de eletrólitos3 e equilíbrio ácido-base é essencial. Como o Plasmafundin® contém acetato e gliconato como componentes formadores de bicarbonato, é contraindicado em pacientes com alcalose15 respiratória ou metabolica, hipocalcemia16, ou hipocloridria.
Categoria de risco na gravidez18: C.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião- dentista.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Advertências e Precauções
Pacientes com insuficiência19 pulmonar ou cardíaca suave à moderada devem ser especificamente monitorados em caso de infusões de grandes volumes.
Plasmafundin® deve ser administrado com cautela em pacientes com:
- Insuficiência cardíaca20, insuficiência renal11, insuficiência hepática21, edema pulmonar22 ou periférico ou hiperidratação extracelular.
- Hipernatremia13, hipercloremia, desidratação23 hipertônica24, hipertensão25, função renal26 diminuída, eclampsia27 presente ou iminente, aldosteronismo ou outras condições ou tratamento (por exemplo, corticoides/esteroides) associados à retenção de sódio.
É necessária a monitoração dos eletrólitos3 séricos, do balanço de fluidos e do pH.
Não use se houver turvação, depósito ou violação do recipiente. Não utilizar o produto após a data de vencimento.
Risco de uso por via de administração não recomendada: Não há estudos dos efeitos de Plasmafundin® caso seja administrado por vias não recomendadas. Portanto, para segurança e eficácia deste medicamento, a administração deve ser realizada somente por via intravenosa.
Gravidez18 e Lactação28
Não existem dados sobre o uso de Plasmafundin® em mulheres grávidas e mulheres em período de amamentação29. Na indicação pretendida ainda não são conhecidos riscos, quando volume, níveis de ácido/base e eletrólitos3 são monitorados cuidadosamente. Plasmafundin® deve ser usado com cautela em toxemia30 da gravidez18. Plasmafundin® deve ser administrado a gestantes somente se necessário.
Categoria de risco na gravidez18: categoria C.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Populações especiais
Pacientes Idosos: Não há advertências e recomendações especiais sobre o uso adequado desse medicamento em pacientes idosos. Deve-se ajustar a dose levando em consideração a maior probabilidade de danos hepáticos, renais e cardíacos de pacientes dessa faixa etária.
Pacientes pediátricos: A segurança e a efetividade na população pediátrica estão baseadas na similaridade da resposta clínica entre adultos e crianças. Por isso, não há na atual literatura trabalhos que limitem a idade mínima para uso da solução. Em neonatos31 e em crianças pequenas, o volume de fluido pode afetar o balanço hidroeletrolítico32, especialmente nos neonatos31 prematuros, cuja função renal26 pode estar imatura e cuja habilidade de excretar cargas do liquido e do soluto pode estar limitada.
As advertências, precauções e reações adversas identificadas em outros grupos etários devem ser observadas para uso pediátrico.
Efeitos na habilidade de dirigir e usar máquinas
Não há informações sobre os efeitos de Plasmafundin® sobre a capacidade de dirigir ou operar automóveis e máquinas pesadas.
Interações medicamentosas
A administração conjunta de Plasmafundin® e fármacos que contêm carbonatos, fosfatos, sulfatos ou tartaratos pode produzir precipitado. Em caso de transfusão33 sanguínea concomitante, não se deve administrar a solução através do mesmo equipo de infusão.
Interações relacionadas com o sódio: Os esteroides/corticoides e a carbenoxolona podem estar associados à retenção de sódio e de água (com edema12 e retenção).
Interações relacionadas com o potássio: Estes medicamentos listados a seguir podem aumentar a concentração de potássio no plasma8 e conduzir a uma hipercalemia34 fatal, particularmente no caso de insuficiência renal11 aumentando o efeito hipercalêmico.
- Suxametônio;
- Diuréticos14 poupadores de potássio (amilorida, espironolactona, triantereno, em terapia singular ou em associação);
- Tacrolimus e ciclosporina.
Interações relacionadas com o acetato e gliconato: O uso de bicarbonato de sódio ou precursor aumenta alcalinização da urina35 e conduz a um aumento da excreção renal26 de fármacos ácidos tais como salicilatos, tetraciclinas, e barbituratos. Por outro lado, prolonga a meia-vida de drogas básicas.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde36.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Plasmafundin® deve ser mantido em sua embalagem original. Conservar em temperatura ambiente (15–30°C). Evitar calor excessivo.
Prazo de validade: 24 meses, a partir da data de fabricação, desde que a embalagem original esteja íntegra.
Número de Lote e datas de fabricação e validade: Vide embalagem.
Não use medicamento com prazo de validade vencido. Guarde-o em sua embalagem original.
Usar imediatamente depois de aberto e descartar qualquer produto não utilizado.
O produto é apresentado em recipientes de dose única. Não utilizar quaisquer conteúdos remanescentes, tampouco armazenar para utilização posterior.
Não guardar a solução contendo aditivos.
Características físicas e organolépticas do produto
Plasmafundin® é uma solução límpida. Usar somente se a solução estiver límpida, praticamente livre de partículas e o recipiente intacto, ou seja, recipiente não violado.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO? Posologia
A dosagem deve ser ajustada de acordo com as necessidades específicas de cada paciente.
Adultos, idosos, adolescentes e crianças: a dosagem depende da idade, condições clínicas e biológicas dos pacientes e terapia concomitante.
Posologia (todas as indicações)
Adultos, idosos e adolescentes: O requerimento de fluido de adultos geralmente é atendido com volumes de 30 a 40 mL/kg de peso corporal/dia. Além disso, perdas anormais de volume, por exemplo, causada por vômitos37, diarreia38 e sudorese39 excessiva devem ser considerados, ao determinar fluido e terapia eletrolítica.
População pediátrica: As recomendações para dosagem de manutenção dos requerimentos de fluidos em crianças estão representadas na tabela abaixo:
|
Manutenção dos requerimentos de fluidos |
|
|
Peso corporal |
Requerimento diário de fluidos |
|
0–10 kg |
4 mL/kg peso corporal/hora |
|
10–20 kg |
40 mL/h + 2 mL/kg peso corporal/hora acima 10 kg |
|
>20 kg |
60 mL/h + 1 mL/kg peso corporal/hora acima 20 kg |
As recomendações acima indicadas devem ser geridas pela administração de líquidos isotônicos. Além disso, recomenda-se que um plano de gerenciamento de fluido para qualquer criança deve abordar três questões fundamentais: qualquer déficit de fluido presente, os requisitos de manutenção de fluidos e quaisquer perdas decorrentes de cirurgia, por exemplo, perda de sangue6, as perdas de espaço. A hipovolemia40 deve ser corrigida com um bolus41 de fluido inicial de 10–20 mL/kg de peso corporal de um fluido isotônico42 (por exemplo, solução salina isotônica43, solução de Hartmann/solução de Ringer).
Reposição de líquidos intraoperatória
As estratégias de fluido intraoperatório prevalecentes pode implicar na administração de 10–18 mL/kg de peso corporal/hora. De 12–15 mL/kg peso corporal durante a primeira hora e 6–10 mL/kg de peso corporal para as próximas 2 horas. O fluido é administrado para manter a produção de urina35 em 1 mL/kg de peso corporal/hora ou de 50–100 mL/kg de peso corporal/hora para uma operação maior da terceira hora em diante. As anormalidades preexistentes, fluidos e eletrólitos3, devem ser corrigidas antes da operação, a administração de fluido deve manter o volume de urina35 entre 0,5 e 1 mL/kg de peso corporal/hora. A estabilidade renal26 e cardiovascular é muito melhor quando cristaloides são dados a uma taxa de 10–15 mL/kg de peso corporal/hora intraoperatória.
Em estado de choque44 hemorrágico45 e condições clínicas que exigem transfusão33 de sangue6 rápida
A quantidade estimada de líquido necessário para a reposição é de 3 mL para cada 1 mL de perda de sangue6, porque parte do fluido administrado é perdido para o espaço intersticial46 e espaço intracelular.
A dosagem de Plasmafundin® depende da idade, peso, condições biológicas e clínicas do paciente e da terapia concomitante. Recomenda-se um máximo de 40 mL/kg de peso corporal/dia para adultos. No entanto, no tratamento da deficiência aguda de volume, doses mais elevadas podem ser aplicadas. A taxa máxima de infusão depende das necessidades do paciente em relação ao fluido e eletrólitos3, seu peso, sua condição clínica e seu estado biológico. Uma dose máxima de 500 mL a 3 litros por 24 horas, observando-se a velocidade de infusão máxima de 126 mL/h. A duração do tratamento dependerá das necessidades do paciente, segundo avaliação médica.
Em pacientes pediátricos, taxas de infusão especificadas nessa faixa etária variam com a idade; 6–8 mL/kg de peso corporal/hora para bebês47, 4–6 mL/kg de peso corporal/h para crianças pequenas, e 2–4 mL/kg de peso corporal/h crianças em idade escolar.
Modo de Usar
Via de administração exclusivamente intravenosa. Administrar conforme orientação médica.
Se for necessária medicação suplementar, seguir as instruções descritas a No preparo e administração das Soluções Parenterais (SP), devem ser seguidas as recomendações da Comissão de Controle de Infecção48 em Serviços de Saúde36 quanto a: desinfecção49 do ambiente e de superfícies, higienização das mãos50, uso de EPIs e desinfecção49 de ampolas, frascos, pontos de adição dos medicamentos e conexões das linhas de infusão.
- Fazer a assepsia51 da embalagem primária utilizando álcool 70%. Retirar o lacre de um dos sítios de administração da tampa.
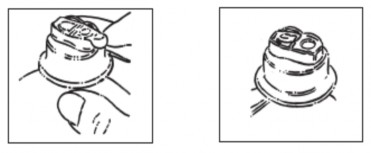
- Introduzir a ponta perfurante do equipo até o final, sem realizar movimentos giratórios.
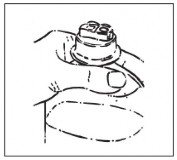
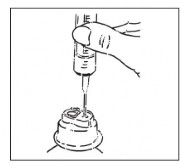
- Durante a introdução do equipo, a pinça rolete e a entrada de ar, se houver, devem estar fechadas.
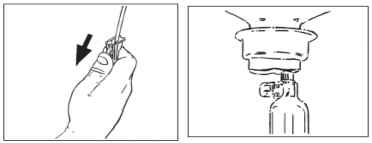
- Pendurar o frasco ampola Ecoflac® plus pela sua alça de sustentação, ajustar o nível da solução na câmara gotejadora e realizar o preenchimento do equipo.
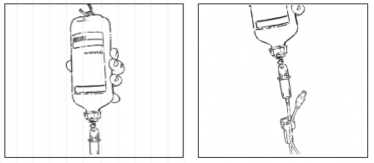
- Consultar as instruções de uso do equipo para mais informações.
- Conectar o equipo de infusão ao acesso do paciente. Abrir a pinça rolete e administrar a solução por gotejamento contínuo, conforme prescrição médica.
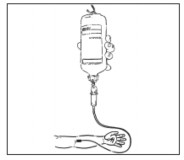
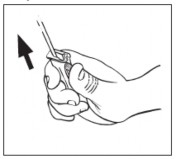
Para adição de medicamentos
Atenção: Verificar se há incompatibilidade entre o medicamento e a solução e, quando for o caso, se há incompatibilidade entre os medicamentos.
Apenas as embalagens que possuem dois sítios, um sítio para o equipo e um sítio próprio para a administração de medicamentos, poderão permitir a adição de medicamentos nas soluções parenterais.
Risco de uso por via de administração não recomendada: Não há estudos dos efeitos de Plasmafundin® caso seja administrado por vias não recomendadas. Portanto, para segurança e eficácia deste medicamento, a administração deve ser realizada somente por via intravenosa.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Em caso de dúvidas, procure a orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
As reações adversas a medicamentos podem ocorrer por causa da solução (por exemplo, a partir de contaminação) ou técnica de administração, incluindo febre52, infecção48 no local da injeção53, dor, trombose54 venosa ou flebite55 estendendo desde o local da injeção53 e extravasamento. Hipervolemia ou sintomas56 que resultam de um excesso ou déficit de um ou mais íon57 presentes na solução pode também ocorrer. Reações adversas podem estar associadas a outras medicações adicionadas à solução; a natureza do aditivo poderá determinar a probabilidade de quaisquer outros efeitos indesejáveis.
Foram descritas ocasionalmente reações de hipersensibilidade caracterizadas por urticária58, após a administração intravenosa de sais de magnésio. Em caso de reações adversas, deve-se suspender a infusão e aplicar as contramedidas apropriadas.
Medidas para tratamento da reação anafilática59 preconizados pela força tarefa em parâmetros práticos e recomendados pela American Academy of Allergy, Asthma and Immunology; The American College of Allergy, Asthma and Immunology, Consenso de alergia60, asma61 e imunologia, e European Academy of Allergy and Clinical Immunology:
- Administrar adrenalina62 intramuscular na face63 anterolateral do glúteo como medida inicial tão logo o diagnostico64 de anafilaxia65 seja feito;
- Colocar o paciente em posição supina para evitar o colapso66 circulatório;
- Administrar oxigênio;
- Administrar soluções de cristaloide nos pacientes com instabilidade ou em colapso66 circulatório;
Plasmafundin® contém agentes formadores de bicarbonato, acetato e gliconato. Portanto, existe a possibilidade de desenvolver alcalose15 metabólica associada a administração Plasmafundin®. Alcalose15, por sua vez, podem desencadear convulsões.
Alcalose15 metabólica ou respiratória, hipocalcemia16 ou hipocloridria
Compostos formadores de bicarbonato, acetato e gliconato desenvolvem alcalose15 metabólica, não devem ser administrados a pacientes com alcalose15 metabólica ou respiratória, hipocalcemia16 ou hipocloridria. Durante o tratamento da acidose17, a monitorização frequente das concentrações séricas de eletrólitos3 e equilíbrio ácido-base é essencial. Como Plasmafundin® contém acetato e gliconato como componentes formadores de bicarbonato, é contraindicado em pacientes com alcalose15 metabólica, hipocalcemia16, ou hipocloridria. Plasmafundin® não contém cálcio, a administração a um paciente com hipocalcemia16, diminuiria ainda mais os níveis séricos de cálcio e agravaria esta condição.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
O uso excessivo ou a administração demasiadamente rápida de Plasmafundin® pode originar sobrecarga de água e eletrólitos3 com o risco de edema12 e alcalose15 metabólica.
A administração excessiva pode causar: hipernatremia13, hipercaliemia, hipermagnesemia e hipercloremia. Quando a superdose está relacionada com qualquer medicação associada à solução infundida, os sinais67 e sintomas56 observáveis estarão diretamente relacionados com a natureza dos fármacos aditivados. Na eventualidade de uma infusão excessiva acidental, o tratamento deve ser interrompido e o paciente deve ser examinado no sentido de identificar os sinais67 e sintomas56 relacionados com o fármaco68 administrado. Devem ser tomadas as medidas sintomáticas e de suporte relevantes, consoante as necessidades apresentadas.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível.
Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
USO RESTRITO A HOSPITAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.0085.0147
Farm. Resp.: Sônia M. Q. de Azevedo – CRF RJ nº: 4.260
Fabricado por:
Laboratórios B. Braun S.A.
Av. Eugênio Borges, 1092 e Av. Jequitibá, 09 Arsenal - CEP: 24751–000
São Gonçalo - RJ - Brasil CNPJ: 31.673.254/0001–02
Indústria Brasileira
SAC 0800 0227286






