

Criscy
CRISTÁLIA PRODUTOS QUÍMICOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Criscy
somatropina
Injetável 4 UI, 12 UI, 16 UI e 30 UI
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Pó Liofilizado1 para Solução Injetável
Embalagem com 1 frasco-ampola de pó liofilizado1 para solução injetável e 1 frasco-ampola de solução diluente
USO SUBCUTÂNEO2
USO ADULTO E PEDIÁTRICO
COMPOSIÇÃO:
Cada frasco-ampola do produto contém:
|
|
4 UI |
12 UI |
16 UI |
30 UI |
|
somatropina |
1,33 mg |
4,00 mg |
5,33 mg |
10,13 mg |
Cada frasco-ampola da solução diluente contém:
|
|
1,0 mL |
1,9 mL |
|
álcool benzílico |
0,0086 mL |
0,01634 mL |
|
veículo q.s.p. |
1,0 mL |
1,9 mL |
Veículo: água para injetáveis.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Este medicamento é indicado:
- No tratamento de longo prazo de crianças com distúrbios de crescimento devido às seguintes condições: secreção insuficiente do hormônio3 de crescimento, síndrome4 de Turner (doença genética que só acomete mulheres), crianças nascidas pequenas para a idade gestacional que não recuperaram a altura nos primeiros quatro anos de vida e síndrome4 de Prader-Willi (doença genética que acomete ambos os sexos).
- No tratamento de baixa estatura idiopática5 (sem causa identificada).
- Na terapia de reposição em adultos com deficiência de hormônio3 de crescimento.
COMO ESTE MEDICAMENTO FUNCIONA?
A somatropina é um hormônio3 que age no metabolismo6 de lípides (gorduras do sangue7), carboidratos e proteínas8. Estimula o crescimento e aumenta a velocidade de crescimento em crianças que têm deficiência de hormônio3 de crescimento (GH) endógeno (produzido pelo organismo). Em adultos, assim como em crianças, a somatropina mantém a composição corpórea normal através do estímulo do crescimento dos músculos9 e ossos e distribuição da gordura10 corpórea. A gordura10 dos órgãos é bastante responsiva ao GH. Além do aumento da quebra das gorduras, a somatropina diminui os estoques de gordura10 corporal.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
A somatropina é contraindicada:
- A pacientes que apresentam hipersensibilidade (reação alérgica11) à somatropina ou a qualquer componente da fórmula.
- A pacientes que possuam evidência de atividade neoplásica12 (câncer13), pacientes com crescimento não controlado de tumores intracranianos (dentro do crânio14) benignos.
- Pacientes aguda e criticamente doentes por complicações após a cirurgia cardíaca (do coração15), cirurgia abdominal, trauma acidental múltiplo ou insuficiência respiratória aguda16 (diminuição aguda da respiração).
- Para promover o crescimento em crianças com epífises17 (áreas de crescimento dos ossos) fechadas.
- A pacientes com retinopatia diabética18 (doença da retina19 causada por diabetes20) proliferativa ativa ou não proliferativa grave.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião dentista.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Criscy é um medicamento biossimilar (produto biológico desenvolvido pela via da comparabilidade). E seu produto biológico comparador é o medicamento Genotropin®.
A somatropina pode induzir resistência à insulina21 e hiperglicemia22 (aumento da glicose23 no sangue7) em alguns pacientes. Raramente, pode ocorrer diabetes20. Nos pacientes diabéticos em tratamento com somatropina pode ser necessário ajustar a dose dos hipoglicemiantes24 (medicamentos que reduzem a glicose23 no sangue7).
A somatropina também pode interferir nos níveis sanguíneos dos hormônios da tireoide25. É recomendado dosar estes hormônios no sangue7 antes do início e toda vez que ajustar a dose do Criscy.
Em pacientes com deficiência do hormônio3 de crescimento devido a tratamento de doenças malignas, é recomendado monitorar a recorrência26 dos sintomas27 durante o uso de Criscy.
Se a criança apresentar dificuldade para andar durante o tratamento com somatropina, ela deve ser avaliada.
Pacientes que apresentarem dor de cabeça28 grave ou frequente, alterações visuais, náuseas29 e/ou vômitos30, devem fazer exame de fundo de olho31. Em caso de alteração neste exame, o diagnóstico32 de hipertensão33 intracraniana (aumento da pressão do cérebro34) benigna deve ser considerado. A experiência clínica mostra que pacientes que já apresentaram hipertensão33 craniana benigna podem ser tratados novamente com somatropina e não apresentam recorrência26 desta doença; os sintomas27 devem ser monitorados cuidadosamente. A experiência com a somatropina em pacientes acima de 60 anos é limitada.
Em crianças com síndrome4 de Prader-Willi, o tratamento com Criscy deve ser acompanhado de dieta com restrição calórica. Ocorrendo piora da escoliose35 (curvatura lateral da coluna vertebral36) durante o uso de Criscy, o médico deverá ser consultado.
A experiência com tratamentos prolongados em pacientes adultos ou com síndrome4 de Prader-Willi é limitada.
Antes de iniciar o tratamento com somatropina para crianças nascidas pequenas para a idade gestacional (PIG), outras razões que possam explicar o distúrbio do crescimento devem ser descartadas. Não é recomendado o início do tratamento com somatropina em crianças nascidas PIG em idade próxima ao início da puberdade. Se o tratamento com somatropina for interrompido antes de a criança atingir a altura final, o ganho em altura pode ficar prejudicado. Aumento da mortalidade37 em pacientes com doença crítica aguda devido a complicações após cirurgia cardíaca aberta, cirurgia abdominal ou trauma acidental múltiplo, ou aqueles com insuficiência respiratória aguda16 foi relatado após o tratamento com quantidades de somatropina (vide questão “3. Quando não devo usar este medicamento?”) e portanto, o potencial benefício da continuação do tratamento com somatropina em pacientes com doenças críticas agudas deve ser ponderado em relação ao risco potencial.
Quando não ocorre aumento da velocidade de crescimento, particularmente no 1° ano de tratamento, em pacientes pediátricos com baixa estatura idiopática5, é necessário avaliar a adesão ao tratamento e outras causas de falha de crescimento, como hipotireoidismo38, subnutrição, idade óssea avançada e anticorpos39 contra o rhGH.
Podem ocorrer reações graves de hipersensibilidade sistêmica, incluindo reações anafiláticas40 e angioedema41 com a utilização de somatropina e, portanto, caso ocorra uma reação alérgica11, deve ser solicitado atendimento médico imediato.
Informe ao seu médico a ocorrência de gravidez42 na vigência do tratamento ou após o seu término.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista. Não se sabe se a somatropina é excretada no leite materno, mas a absorção do hormônio3 pelo estômago43 e intestino do lactente44 (bebê em fase de amamentação45) é extremamente improvável. Informe ao seu médico se estiver amamentando. Caso ocorra obstrução das vias aéreas superiores (nariz46 e garganta47) incluindo início ou aumento de ronco durante o tratamento com Criscy, consulte o médico.
Efeitos na habilidade de dirigir e usar máquinas
Não foi observado efeito na habilidade de dirigir veículos ou operar máquinas com o uso de Criscy.
Este medicamento pode causar doping.
O tratamento concomitante com glicocorticoides inibe os efeitos promotores do crescimento dos medicamentos contendo somatropina. Pacientes com deficiência de hormônio3 adrenocorticotrófico (ACTH) devem ter sua terapia de reposição de glicocorticoides cuidadosamente ajustada para evitar qualquer efeito inibitório sobre o crescimento. E devem ter seu crescimento cuidadosamente monitorado para avaliar o impacto potencial do tratamento com glicocorticoides no crescimento. A administração de somatropina pode aumentar a eliminação de substâncias que sofrem metabolização pelo citocromo P450 3A4 (ex., esteroides sexuais, corticosteroides, anticonvulsivantes e ciclosporina). O aumento da eliminação destes compostos pode resultar na diminuição dos níveis plasmáticos (sanguíneos) dos mesmos. Ainda não se conhece a importância deste fato.
Informe seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde48.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
As concentrações de 4 UI, 12 UI,16 UI e 30 UI possuem prazo de validade de 24 meses a partir da data de fabricação impressa na embalagem.
Antes da reconstituição: Possui prazo de validade de 24 meses a partir da data de fabricação impressa na embalagem.
O Criscy deve ser mantido em sua embalagem original, deve ser conservado fechado sob refrigeração entre 2 a 8°C, protegido da luz. Não congelar.
A solução diluente deve ser conservada em sua embalagem original, fechado, junto ao produto, nas prateleiras da geladeira. Não congelar.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Após a reconstituição: Deve ser conservado sob refrigeração (2–8°C), protegido da luz. Não congelar.
ESTE MEDICAMENTO, DEPOIS DE RECONSTITUÍDO, DEVERÁ SER UTILIZADO EM NO MÁXIMO 28 DIAS (4 SEMANAS).
Características físicas e organolépticas do produto
- Antes da reconstituição: O Criscy apresenta-se como um pó liofilizado1 branco ou quase branco.
- Após a reconstituição: O Criscy reconstituído apresenta-se como uma solução límpida, com todo o conteúdo dissolvido, isenta de partículas e incolor a levemente amarelada
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o médico ou o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
A dose e o esquema de administração devem ser individualizados e estabelecidos somente pelo médico. A dose semanal de Criscy deve ser dividida em 6-7 injeções subcutâneas devendo-se variar o local de aplicação para evitar a ocorrência de lipoatrofia49 (diminuição da gordura10 corporal localizada).
Tabela 1. Doses recomendadas para crianças
|
Indicação |
Dose diária |
|||
|
mg/kg de peso corpóreo |
UI/kg de peso corpóreo |
mg/m2 área da superfície corpórea |
UI/m2 área da superfície corpórea |
|
|
Deficiência do hormônio3 de crescimento em crianças1 |
0,025 – 0,035 |
0,07 – 0,10 |
0,7 – 1,0 |
2,1 – 3,0 |
|
Síndrome4 de Turner |
0,045 – 0,050 |
0,14 |
1,4 |
4,3 |
|
Síndrome4 de Prader-Willi2 |
0,035 |
0,10 |
1,0 |
3,0 |
|
Crianças nascidas pequenas para a idade gestacional3 |
0,035 |
0,10 |
1,0 |
3,0 |
|
Baixa estatura idiopática5 |
Até 0,067 |
Até 0,2 |
Até 2,0 |
Até 6,0 |
- Doses maiores podem ser utilizadas.
- A dose diária não deve ultrapassar 2,7 mg. O tratamento não deve ser utilizado em crianças com velocidade de crescimento menor que 1 cm por ano e próximo ao fechamento das epífises17 (área de crescimento dos ossos). Em pacientes com distúrbio de crescimento o tratamento pode ser realizado até que a altura final seja atingida. O tempo de tratamento para melhora da composição corpórea deve ser avaliado pelo médico responsável pelo tratamento.
- Esta dose geralmente é recomendada até se atingir a altura final. O tratamento deve ser descontinuado se a velocidade de crescimento em altura for <2 cm/ ano e, se a idade óssea for >14 anos (meninas) ou >16 anos (meninos), correspondendo ao fechamento das placas50 de crescimento epifisário.
Baixa estatura idiopática5 (sem causa identificada): iniciar o tratamento com 0,15 UI/kg/dia, ajustando a dose de acordo com a resposta clínica e com as concentrações de IGF-1 no sangue7. A dosagem periódica do IGF-1 no sangue7, durante o tratamento com o Criscy, é útil na avaliação da eficácia, segurança e da aderência à medicação, auxiliando no ajuste da melhor dose para cada paciente.
Tabela 2. Doses recomendadas para pacientes51 adultos
|
Indicação |
UI/dia dose inicial |
mg/dia dose inicial |
UI/ dia dose de manutenção que raramente excede |
mg/ dia dose de manutenção que raramente excede |
|
Deficiência do hormônio3 de crescimento em adultos1 |
0,45 – 0,90 |
0,15 – 0,30 |
4 |
1,33 |
- A dose deve ser aumentada gradualmente de acordo com as necessidades individuais do paciente, conforme determinado pela concentração de IGF-I (substância produzida por estímulo do GH - hormônio3 do crescimento). O objetivo do tratamento deve ser atingir concentrações de IGF-I dentro de 2 DP (desvio padrão) a partir da média corrigida pela idade. Pacientes com concentrações normais de IGF-I no início do tratamento devem receber o Criscy até atingir, no máximo, nível normal de IGF-I, não excedendo 2 DP. A resposta clínica e os efeitos colaterais52 podem ser utilizados como parâmetros de determinação da dose. A dose diária de manutenção raramente excede 1,0 mg ao dia. Mulheres podem necessitar de doses maiores que os homens, sendo que os homens têm demonstrado aumento da sensibilidade ao IGF-I no decorrer do tempo. Isto significa que existe um risco de as mulheres, especialmente aquelas em tratamento de reposição oral de estrógeno53 (hormônio3 sexual feminino), sejam subtratadas, enquanto que há o risco dos homens serem supertratados. A exatidão da dose do Criscy deve ser controlada, portanto, a cada 6 meses. As doses podem ser reduzidas visto que a produção fisiológica54 normal do hormônio3 de crescimento diminui com a idade. Deve ser utilizada a menor dose efetiva.
Reconstituição: O produto deve ser reconstituído com a solução diluente.
Instruções para reconstituição: Para reconstituir o produto deve-se retirar exatamente 1,0 mL (para Criscy 4 UI, 12 UI e 16 UI) ou 1,9 mL (para Criscy 30 UI) da solução diluente com uma seringa55 estéril, injetando-o dentro do frasco de Criscy, direcionando o jato para a parede do frasco, fazendo movimentos leves e circulares no frasco. Não agitar vigorosamente. Soluções turvas ou com partículas não devem ser utilizadas.
Após o pó liofilizado1 ter sido dissolvido em 1,0 mL (para Criscy 4UI, 12 UI e 16 UI) ou 1,9 mL (para Criscy 30 UI) da solução diluente, as soluções finais terão 1,33 mg (4 UI), 4,0 mg (12 UI), 5,33 mg (16 UI) e 10,13 mg (30 UI) de somatropina por mL, respectivamente.
Utilize somente a quantidade recomendada da solução diluente (1,0 mL – para o Criscy 4 UI, 12 UI e 16 UI, ou 1,9 mL – para o Criscy 30 UI). O diluente restante no frasco-ampola da solução diluente deverá ser descartado.
Uso em pacientes idosos: A segurança e eficácia do Criscy em pacientes com 60 anos ou mais não foram avaliadas em estudos clínicos. Pacientes idosos podem ser mais sensíveis à ação do Criscy e ser mais propensos a desenvolver reações adversas.
Instruções para preparo e aplicação com a seringa55:
*Importante: recomenda-se utilizar seringas para insulina56 de 1 mL sem volume morto (espaço residual).
O produto deve ser administrado por indivíduos devidamente treinados e familiarizados com seu uso.
Reúna todo o material (frascos, seringas, algodão, álcool 70% e agulhas) necessário e lave as mãos57 antes de iniciar o processo.
- Retirar a tampa plástica do frasco-ampola da solução diluente e limpar a tampa de borracha com algodão umedecido com álcool 70% antes de introduzir a agulha*.

- Pegar o frasco-ampola da solução diluente:
Para Criscy 4 UI, 12 UI ou 16 UI: Introduzir a agulha da seringa55 através da tampa de borracha e retirar 1,0 mL do diluente. Para Criscy 30 UI: Introduzir a agulha da seringa55 através da tampa de borracha e retirar 1,9 mL do diluente.
Virar o frasco-ampola de ponta cabeça28 para retirar o diluente com a seringa55 reta.

- Pode ser necessário fazer um movimento na diagonal para completar a quantidade recomendada na seringa55.

- Certifique-se de que a quantidade de diluente na seringa55 está conforme a recomendação do menisco58 (Para Criscy 4 UI, 12 UI e 16 UI: 1,0 mL e para Criscy 30 UI: 1,9 mL).
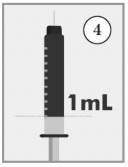
- Assegurar-se que as bolhas de ar foram retiradas segurando a seringa55 com a agulha virada para cima e dando pequenos toques na seringa55 com o dedo indicador até que todas as bolhas se juntem no topo. Empurrar lentamente o êmbolo59 da seringa55 para retirar todas as bolhas de ar até que haja uma pequena gota60 de líquido na extremidade da agulha.
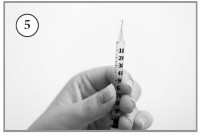
- Retirar a tampa plástica do frasco-ampola do Criscy e limpar a tampa de borracha com algodão umedecido de álcool 70% antes de introduzir a agulha.
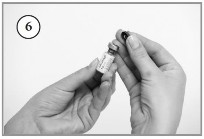
- Introduzir a agulha com o diluente através da tampa de borracha do frasco-ampola de Criscy e injetar o diluente lentamente contra a parede de vidro para evitar a formação de espuma.

- Diluir a solução através de movimentos rotativos suaves, até o conteúdo estar completamente dissolvido.
NÃO AGITAR VIGOROSAMENTE.
Se a solução estiver turva ou contiver partículas, não utilizar. O conteúdo deve ser límpido, isento de partículas e incolor a levemente amarelado após a preparação.
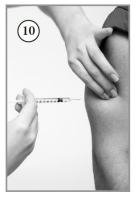
- Com seringa55 e agulha novas*, retirar a dose calculada para o paciente.
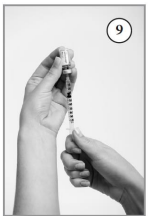
Repetir os passos da etapa 5, agora para a solução já diluída de Criscy. - Limpar a pele61 no local de aplicação com novo algodão umedecido com álcool 70%, fazendo movimento circular de dentro para fora. Esperar secar e pinçar a pele61 formando uma dobra, introduzir a agulha em um ângulo reto62 (90 graus), como indicado na figura, e injetar lentamente o medicamento. Contar 5 segundos antes de retirar a agulha.

Repetir os passos da etapa 5, agora para a solução já diluída de Criscy.
- Uma vez reconstituída, a solução de Criscy pode ser armazenada por 28 dias, seguindo instruções dos cuidados de armazenamento contido em bula.
- Não congelar ou expor ao sol. E não usar o medicamento após o prazo de validade.
- A cada nova administração deve-se utilizar uma nova seringa55 com agulha e repetir o processo a partir da etapa 9, até que o frasco-ampola já preparado não tenha mais conteúdo para novas administrações.
- Variar o local de aplicação para evitar a ocorrência de lipoatrofia49 (diminuição localizada da gordura10 corporal).
- Utilizar sempre a dose prescrita em todas as aplicações, conforme orientação do seu médico.
- Caso haja dificuldade em retirar volume suficiente do frasco com medicação reconstituída, pode ser necessária a abertura de um novo frasco para completar a dose. Neste caso, contatar um profissional de saúde48 para instruções.
- Coloque todas as seringas e agulhas usadas, bem como os frascos-ampola vazios, em um local seguro para evitar
- acidentes. Pode ser utilizado um recipiente de “perfuro-cortantes” apropriado.
- Pacientes com deficiência visual devem utilizar o Criscy somente com a ajuda de alguém treinado para preparo e aplicação do medicamento.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
- Se você esquecer de aplicar o Criscy no horário estabelecido, deve fazê-lo assim que lembrar. Entretanto, se já estiver perto do horário de administrar a próxima dose, você deve desconsiderar a dose esquecida e utilizar a próxima.
- Neste caso, você não deve utilizar a dose duplicada para compensar doses esquecidas. O esquecimento de dose pode comprometer a eficácia do tratamento.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
A seguir são apresentadas as reações adversas listadas de acordo as categorias de frequência:
Reações adversas descritas na bula de Genotropin® (produto comparador)
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento):
- Adultos: artralgia63 (dor nas articulações64) e edema65 periférico (inchaço66 nas extremidades do corpo).
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento):
- Crianças: artralgia63 (dor nas articulações64) e reação no local da injeção67;
- Adultos: parestesia68 (dormência69 e formigamento), mialgia70 (dor muscular) e rigidez muscular.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento):
- Crianças: parestesia68 (dormência69 e formigamento), erupção71 cutânea72, prurido73, urticária74 e edema65 periférico (inchaço66 nas extremidades do corpo).
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento):
- Crianças: leucemia75, hipertensão33 intracraniana benigna (aumento da pressão dentro do crânio14) e mialgia70 (dor muscular).
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): não conhecido.
Frequência desconhecida (não foi possível estimar com os dados disponíveis):
- Crianças: diabetes tipo 276, rigidez muscular, edema65 facial e diminuição do cortisol no sangue7;
- Adultos: diabetes tipo 276, hipertensão33 intracraniana benigna (aumento da pressão dentro do crânio14), erupção71 cutânea72, prurido73, urticária74, reação no local da injeção67, edema65 facial e diminuição do cortisol no sangue7.
Pós-comercialização
Na experiência pós-comercialização, casos raros de morte súbita foram relatados em pacientes portadores de síndrome4 de Prader-Willi tratados com Genotropin®, embora nenhuma relação causal tenha sido demonstrada.
Foram relatadas ocorrências de deslizamento da epífise femoral proximal77 e de síndrome4 de Legg-Calvé-Perthes (osteonecrose/necrose78 avascular, ocasionalmente associada a deslizamento da epífise femoral proximal77) em crianças tratadas com hormônio3 de crescimento. Casos foram relatados com Genotropin®.
Reações adversas registradas no estudo de fase III (Estudo Ceres)
Ao longo do estudo, foram registrados efeitos adversos (EAs) em um total de 85 participantes, sendo a percentagem de participantes com pelo menos um EA semelhante entre os grupos de tratamento: 87,8 % no grupo Cristália e 87,5 % no grupo Genotropin®. Não se verificaram diferenças estatisticamente significantes entre os grupos face79 à incidência80 global de EAs, número mediano de EAs ou incidência80 de EAs com relação possível, provável ou definida com a medicação. A intensidade dos EAs foi também semelhante entre os grupos de tratamento, sendo a maioria dos EAs reportados de intensidade moderada (79,8 % no grupo Cristália e 73,3 % no grupo Genotropin®). Apesar de uma alta incidência80 de EAs no presente estudo, pode observar-se que a relação causal da maioria dos EAs reportados em ambos os grupos foi classificada como "improvável" (49,4 % no grupo Cristália vs. 62,0 % no grupo Genotropin®). Adicionalmente, é de salientar que a grande maioria de EAs foram resolvidos sem sequelas81 (94,0 % no grupo Cristália vs. 92,0 % no grupo Genotropin®), apenas 1,7 % conduziram à hospitalização (grupo Cristália) e nenhuma morte ou descontinuação devido a EAs foram observadas durante o estudo. Cinco EAGs (2,1 %) foram observados no grupo Cristália, sendo 3 em uma paciente com craniofaringioma em que foi relatada a progressão da porção cística do tumor82 em 3 ocasiões. Apesar destes relatos terem sido considerados de relação possível com a medicação, a progressão desse tumor82 benigno pode acontecer mesmo sem o uso concomitante do hormônio3 do crescimento e os dados da literatura são inconclusivos quanto à relação causal entre progressão de um craniofaringioma e uso do hormônio3 de crescimento. Quanto à imunogenicidade, não foram encontradas diferenças estatisticamente significantes entre os grupos de tratamento em termos da incidência80 de anticorpos39 durante o período de tratamento. Em nenhum grupo se observou a presença de anticorpos39 neutralizantes. A tabela 13 mostra as reações adversas registradas no Estudo Ceres classificadas de acordo com a classe de sistema de órgãos e frequência para crianças e adultos separadamente, usando a seguinte convenção: muito comum (≥1/10); comum (≥1/100 a <1/10); incomum (≥1/1.000 a <1/100); raro (≥1/10.000 a <1/1.000); muito raro (<1/10.000); não conhecido (não pode ser estimado a partir dos dados disponíveis).
Tabela 3. Reações adversas com causalidade relacionada (possível, provável ou definida) com o produto Criscy
|
Classe de sistema de órgãos |
Muito comum |
Comum |
Incomum |
Raro |
Muito raro |
|
Doenças do sistema nervoso83 |
|
Cefaleia84 |
|
|
|
|
Afecções85 musculoesqueléticas e dos tecidos conjuntivos |
|
|
Dores nas extremidades, artralgia63, dor cervical, dorsalgia |
|
|
|
Doenças endócrinas |
|
|
Hiperglicemia22 |
|
|
|
Doenças gastrointestinais |
|
|
Náusea86, dor abdominal, vômito87 |
|
|
|
Afecções85 oculares |
|
Edema65 palpebral |
|
|
|
|
Perturbações gerais e alterações no local da administração |
|
|
Dor no local da aplicação |
|
|
|
Doenças renais e urinárias |
|
|
Infecção88 do trato urinário89 |
|
|
|
Doenças do sangue7 e do sistema linfático90 |
|
|
Trombocitose91 |
|
|
Informe seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
A superdose aguda poderia resultar inicialmente em hipoglicemia92 (diminuição da glicose23 no sangue7) e, subsequentemente, em hiperglicemia22 (aumento da glicose23 no sangue7). A superdose em longo prazo poderia resultar em sinais93 e sintomas27 compatíveis com efeitos conhecidos de excesso de hormônio3 de crescimento.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
SÓ PODE SER VENDIDO COM RETENÇÃO DA RECEITA
Reg. MS nº 1.0298.0509
Farmacêutico Responsável: Dr. José Carlos Módolo - CRF-SP nº 10.446
CRISTÁLIA Produtos Químicos Farmacêuticos Ltda.
Rodovia Itapira-Lindóia, km 14 - Itapira / SP
CNPJ 44.734.671/0001-51
Indústria Brasileira
SAC 0800 701 1918






