Glargilin (Caneta descartável) (Bula do profissional de saúde)
BIOMM SA
IDENTIFICAÇÃO DO MEDICAMENTO
Glargilin®
insulina glargina1
Caneta descartável com solução injetável 100 U/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Embalagem contendo 1 caneta descartável preenchida com 3 mL de solução injetável
USO SUBCUTÂNEO2
USO ADULTO E PEDIÁTRICO ACIMA DE 2 ANOS
COMPOSIÇÃO:
Cada mL de Glargilin® contém:
| unidades de insulina glargina1 derivada de DNA recombinante (equivalente a 3,64 mg) | 100 |
| veículo q.s.p. | 1 mL |
Veículo: metacresol, glicerol, cloreto de zinco, água para injetáveis, ácido clorídrico3 (ajuste de pH) e hidróxido de sódio (ajuste de pH).
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE4
INDICAÇÕES
Glargilin® é indicada para o tratamento de diabetes mellitus5 tipo 2 em adultos e para o tratamento de diabetes mellitus5 tipo 1 em adultos e crianças com 2 anos de idade ou mais que necessitem de insulina6 basal (longa duração) para o controle da hiperglicemia7.
RESULTADOS DE EFICÁCIA
Glargilin® é um medicamento biológico desenvolvido pela via de comparabilidade (biossimilar). O programa de desenvolvimento clínico do produto foi projetado para mostrar comparabilidade entre Glargilin® e o medicamento comparador Lantus®, com base em:
- Estudo de Fase I de clamp euglicêmico hiperinsulinêmico, cruzado, de dose única, randomizado8, duplo-cego que avaliou o perfil farmacocinético (PK) e farmacodinâmico (PD) da injeção9 de insulina glargina1 da Gan & Lee (Glargilin®) em comparação com o medicamento comparador - Lantus® com 41 pacientes DM1.
- Estudo de fase 3 de não-inferioridade de Eficácia e Segurança, realizado em 278 pacientes diabéticos do tipo 2, no qual 139 receberam Glargilin®.
- Um terceiro estudo, também tendo como desfechos eficácia e segurança em pacientes diabéticos do tipo 2, coletou dados sobre imunogenicidade, comparativos entre Glargilin® e o medicamento comparador Lantus®.
Estudo de Fase I realizado com o produto Glargilin®
Foi realizado entre 2015 e 2016 um estudo de Fase I de clamp euglicêmico hiperinsulinêmico, cruzado, de dose única, randomizado8, duplo-cego que avaliou o perfil farmacocinético (PK) e farmacodinâmico (PD) da injeção9 de insulina glargina1 da Gan & Lee (Glargilin®) em comparação com o medicamento comparador - Lantus®. Quarenta e um (41) pacientes DM1 foram incluídos e receberam ambas as insulinas em desenho cruzado. O desenho cruzado foi escolhido para reduzir a variabilidade entre os indivíduos, permitindo que cada paciente servisse como seu próprio controle. A dose do medicamento de estudo administrada (0,4 U/kg) provoca uma resposta robusta em indivíduos com DM1 [Heise et al. 2004] e é consistente com as informações de prescrição para Lantus®.
O estudo de clamp é a técnica padrão-ouro para avaliação de biossimilaridade de insulinas, conforme determinado pelo Guia da EMA para o desenvolvimento de insulinas biossimilares e recomendado pela ANVISA.
Os desfechos primários deste estudo foram escolhidos com base na orientação da EMA e ANVISA [EMA 2015; ANVISA 2015], indicando que a AUC10 e Cmáx são parâmetros- chave para estabelecer a bioequivalência de PK e PD e a similaridade dos produtos foi satisfatoriamente comprovada.
Neste estudo, a bioequivalência foi definida como o IC de 90% ou 95% da razão da média geométrica do LS para cada parâmetro de PK ou PD, respectivamente, estando totalmente contido dentro do intervalo de 0,8 a 1,25.
Notavelmente, a bioequivalência da PK foi demonstrada para a AUC100-24, AUC100-inf e Cmax. Com base na relação dos valores da AUC10 de 0-12 e 12-24 horas para a concentração sérica de insulina6 e GIR, respectivamente, os perfis de PK e PD de Glargilin® sustentam um perfil PK / PD comparativamente uniforme.
Com base na razão dos valores da AUC10 de 0-12 e 12-24 horas para a concentração sérica de insulina6 e o GIR, respectivamente, os perfis de PK e PD de Glargilin® foram verificados acima da duração do período de observação, suportando um perfil de PK/PD relativamente sem pico.
Em resumo, no estudo de fase 1 de PK e PD, Glargilin® demonstrou bioequivalência em relação à Lantus® para ambos os desfechos primários de PK (AUC10ins e Cmax) e no desfecho primário de PD (GIRmax).
Os perfis médios de PK/PD foram similares entre Glargilin® e Lantus®. Glargilin® foi bem tolerada, sem maiores achados de segurança.
Estudos de Fase III realizados com o produto Glargilin®
Diabetes tipo 211
O estudo de fase 3 de não-inferioridade comparativo, aberto, randomizado8 em grupos paralelos para avaliar eficácia e segurança de Glargilin® versus Lantus® em pacientes com diabetes mellitus5 tipo 2 não controlada com terapia com antidiabéticos orais12, comprovou a não inferioridade de Glargilin®. Após concluída a visita de recrutamento, 278 sujeitos entraram no estudo comparativo de 24 semanas e foram randomizados para o grupo Glargilin® ou grupo Lantus® em razão 1:1. O critério primário de eficácia neste estudo foi comparar a alteração no HbA1c13 do basal para o período de tratamento de 24 semanas nos dois grupos de tratamento. Critérios secundários de eficácia incluíram comparação da glicose sanguínea14 média nos dois grupos (8 pontos de tempo de valor de glicose sanguínea14 em 24 horas), comparação da glicose sanguínea14 em jejum do basal para o desfecho nos dois grupos de tratamento e comparação da taxa de incidência15 de hipoglicemia16 nos dois grupos de tratamento.
Com relação à variável primária de eficácia, ao final da semana 24, HbA1c13 teve uma redução significativa de 0,72% no grupo Glargilin® e 0,64% no grupo Lantus®, sem diferença estatisticamente significativa entre os dois grupos na população por protocolo. Resultados similares foram observados para a população total de análise. Para determinar não-inferioridade, um intervalo de confiança unilateral de 95% sobre a diferença de HbA1c13 de Lantus®-Glargilin® foi calculado. Como o limite inferior do intervalo de confiança sobre a diferença em HbA1c13 em Lantus® - Glargilin® é maior que o valor clinicamente significativo de ~0,5, concluiu-se que Glargilin® é não inferior à Lantus®. Com relação aos parâmetros secundários de eficácia, a glicose sanguínea14 em jejum teve redução significante de 20,1% no grupo Glargilin® e 19,7% no grupo Lantus® ao final da semana 24 do período de tratamento, sem diferença estatisticamente significativa entre os dois grupos. A mudança na glicose sanguínea14 do basal para o período de tratamento de 24 semanas foi calculada em cada um dos 8 pontos de tempo. Perfil de glicose sanguínea14 mostrou que a terapia com Glargilin® em Lantus® reduziu glicose sanguínea14 em todos os pontos de tempo, sem diferença estatisticamente significativa entre os dois grupos. 8,8% dos sujeitos no grupo Lantus® tiveram eventos de hipoglicemia16, significativamente mais comparados com os 2,4% no grupo Glargilin® ao final da semana 2 de tratamento. Ao final da semana 12, os eventos hipoglicêmicos foram significativamente maiores no grupo Lantus® (13,6%) do que no Glargilin® (5,5%). Ao final da semana 20 e 24, as proporções de casos de eventos hipoglicêmicos foram maiores no grupo Lantus® do que no Glargilin® porém sem significância estatística.
A eficácia de Glargilin® foi ainda avaliada por meio de um estudo clínico multicêntrico aberto, randomizado8, comparativo com duplo cruzamento em 70 pacientes com diabetes tipo 211 e com duração de 28 semanas.
Dados de eficácia primária são valores de HbA1c13 no basal e no desfecho (16 semanas e 28 semanas de tratamento). Valor inicial de hemoglobina glicada17 na população por protocolo foi de 9,0 ± 1,6% (mediana 9,0% e faixa interquartil 7,8-10,7%). Após 4 meses de terapia, independentemente do tipo de insulina6 administrado, o nível de hemoglobina glicada17 diminuiu de maneira estatisticamente significativa para 7,9 ± 1,4% (mediana 7,7% faixa interquartil 6,8-8,8%) p=0,000001, sem mudanças significativas no mês 7 de terapia após troca da insulina6 – 8,2 ± 1,6% (mediana 7,9% faixa interquartil 6,8-9,5%) p=0,214. No desfecho (28ª semana de terapia) valores de hemoglobina glicada17 nos pacientes do grupo 1 (troca de Glargilin® pra Lantus®) constituíam 8,1 ±1,5% (mediana 7,7 faixa interquartil 6,8-9,0%), enquanto no grupo 2 (troca de Lantus® para Glargilin®) 8,3 ± 1,7% (mediana 8,0% faixa interquartil 6,1±11,0%); estes valores foram significativamente melhores que os obtidos “antes do tratamento” (p<0,001), mas não houve diferenças (p=0,356).
Não houve diferenças entre os grupos em relação à produção de anticorpos18 anti-insulina6 (p = 0,492) e sequência de administração (p = 0,114). A dose de insulina6 ao final do período de titulação foi de 28,6 ± 11,9 U/d no grupo que iniciou com Glargilin® e 31,7 ± 14,1 U/d no grupo que iniciou com Lantus® (p = 0,031). A troca entre os grupos não acarretou ajuste da dose (p = 0,699). Não houve diferenças nos episódios de hipoglicemia16 sintomática19 ou confirmada entre os grupos.
Os estudos descritos a seguir foram realizados com o produto comparador Lantus® e constam na bula de Glargilin® de acordo com a nota de esclarecimento da ANVISA 002/2016.
A eficácia geral da insulina glargina1 administrada uma vez ao dia no controle metabólico foi comparada à eficácia da insulina6 humana NPH administrada uma ou duas vezes ao dia, em estudos abertos randomizados, ativo-controles, paralelos envolvendo 2327 pacientes com diabetes mellitus5 tipo 1 e 1563 pacientes com diabetes mellitus5 tipo 2. Em geral, a insulina glargina1 manteve ou melhorou o nível de controle glicêmico medido pela glicohemoglobina e glicemia de jejum20. Adicionalmente, menor número de pacientes utilizando insulina glargina1 relataram episódios hipoglicêmicos comparado com pacientes utilizando insulina6 humana NPH.
Diabetes tipo 121 – adulto (vide tabela 1)
Em estudos de fase III, voluntários com diabetes tipo 121 (n=1119) foram randomizados para o tratamento basal-bolus22 com Lantus® uma vez ao dia ou insulina6 humana NPH uma ou duas vezes ao dia e tratados por 28 semanas. Insulina6 humana regular foi administrada antes de cada refeição. Lantus® foi administrada antes de se deitar. A insulina NPH23 foi administrada uma vez ao dia ao se deitar ou de manhã e ao se deitar quando utilizada duas vezes por dia. Lantus® apresentou maior efeito na redução da glicose24 de jejum do que a insulina6 humana NPH administrada duas vezes ao dia, porém foi comparável com a insulina6 humana NPH administrada duas vezes ao dia, em seu efeito na glicohemoglobina e na incidência15 de hipoglicemia16 noturna e severa. Comparada à insulina6 humana NPH administrada uma vez ao dia, Lantus® apresentou efeito semelhante na glicemia de jejum20 e glicohemoglobina. Entretanto, poucos voluntários recebendo Lantus® relataram episódios de hipoglicemia16 severa após a titulação inicial, do mês 2 do estudo em diante, (0,9% vs. 5,6%, p<0,05) e poucos pacientes relataram episódio de hipoglicemia16 noturna (11,0% vs. 21,3%, p < 0,05). Foi relatada hipoglicemia16 com frequência semelhante durante o primeiro mês dos estudos após o início do tratamento com Lantus® comparado à insulina6 humana NPH (data on file, sanofi-aventis).
Em outro estudo fase III, voluntários com diabetes tipo 121 (n = 619) foram tratados por 16 semanas com um regime de insulina6 basal-bolus22 onde a insulina lispro25 foi usada antes de cada refeição. Lantus® foi administrada uma vez ao dia ao se deitar e a insulina6 humana NPH foi administrada uma ou duas vezes ao dia. Lantus® apresentou maior efeito na redução da glicemia de jejum20 do que a insulina6 humana NPH administrada duas vezes ao dia. Lantus® e insulina NPH23 apresentaram efeito semelhante na glicohemoglobina, com número semelhante de pacientes relatando episódio de hipoglicemia16 (Raskin et al, 2000).
Diabetes tipo 211 (vide tabela 1)
Em um estudo fase III (n=570), Lantus® foi avaliada por 52 semanas como parte de um regime de terapia combinada26 com insulina6 e agentes antidiabéticos orais12 (sulfonilureia, metformina27, acarbose28 ou combinação destes fármacos). Lantus® administrada uma vez ao dia ao se deitar foi tão efetiva quanto a insulina6 humana NPH administrada uma vez ao dia ao se deitar na redução da glicohemoglobina e da glicemia de jejum20. Entretanto, poucos voluntários tratados com Lantus® relataram episódios de hipoglicemia16 noturna após início da titulação, do mês 2 do estudo em diante. O benefício de Lantus® foi mais pronunciado no subgrupo de pacientes que não foram tratados previamente com insulina6 [Lantus®: 9,5%, insulina6 humana NPH: 22,8%; p < 0,05] (Massi-Benedetti et al, 2003).
Em outro estudo fase III, em pacientes com diabetes tipo 211 que não estavam usando agentes antidiabéticos orais12 (n=518), um regime basal-bolus22 de Lantus®, uma vez ao dia ao deitar ou insulina6 humana NPH administrada uma ou duas vezes ao dia foi avaliada por 28 semanas. Insulina6 humana regular foi usada antes das refeições conforme a necessidade. Lantus® apresentou efetividade semelhante para administrações de insulina6 humana NPH uma ou duas vezes ao dia na redução da glicohemoglobina e glicose24 de jejum. Entretanto, poucos voluntários tratados com Lantus® relataram hipoglicemia16 noturna do mês 2 do estudo em diante em relação a voluntários tratados com insulina NPH23 duas vezes por dia (29,8% versus 37,9%, p=0,0582) (Rosenstock et al. 2001).
Diabetes tipo 121 – pediátrico (vide tabela 2)
Em um estudo clínico, randomizado8, controlado, em crianças (faixa etária de 6 a 15 anos) (estudo 3003) com diabetes tipo 121 (n=349), os pacientes foram tratados por 28 semanas com regime de insulina6 basal-bolus22 em que a insulina6 humana regular foi utilizada antes de cada refeição. Lantus® foi administrada uma vez ao dia ao deitar e a insulina6 humana NPH foi administrada uma ou duas vezes por dia. Efeitos semelhantes na glicohemoglobina e na incidência15 de hipoglicemia16 foram observados em ambos os grupos de tratamento (Schober E et al. 2002).
Diabetes tipo 121 – pediátrico (1 a 6 anos)
Um estudo de 24 semanas de grupo paralelo foi conduzido em 125 crianças com diabetes mellitus5 tipo 1, com idades entre 1 a 6 anos (61 crianças de 2 a 5 anos no grupo da insulina glargina1 e 64 crianças de 1 a 6 anos no grupo insulina NPH23), comparando insulina glargina1 administrada uma vez ao dia pela manhã à insulina NPH23 administrada uma ou duas vezes ao dia como insulina6 basal. Ambos os grupos receberam insulina6 em bolus22 antes das refeições.
O objetivo primário do estudo foi comparar os dois regimes de tratamento em termos de hipoglicemia16. O resultado composto primário consistiu em: monitoramento contínuo das excursões de glicose24 abaixo de 70mg/dL confirmadas por medições da glicose24 no sangue29 por punção digital (FSBG); outras medições FSBG <70mg/dL e episódios sintomáticos de hipoglicemia16.
A taxa de eventos sintomáticos de hipoglicemia16 é o componente mais comumente usado e clinicamente relevante do resultado composto. As taxas de eventos sintomáticos de hipoglicemia16 foram numericamente inferiores no grupo da insulina glargina1, tanto no geral (25,5 episódios por paciente-ano, versus 33,0 para NPH) quanto durante a noite (2,38 episódios por paciente-ano, versus 3,65 para NPH).
As variabilidades de hemoglobina glicada17 e glicose24 foram comparáveis em ambos os grupos de tratamento. Não foram observados novos alertas de segurança neste estudo.
Resumo dos principais efeitos terapêuticos dos estudos clínicos Tabela 1: Diabetes mellitus5 tipo 1 – adulto
|
População diabética |
Tratamento |
na |
Média do final do estudo (alteração média do basal) |
% de voluntários |
||
|
Hemoglobina glicosilada30 (%) |
Glicemia de jejum20 (mg/dL31)b |
Hipoglicemia16 noturnac |
Hipoglicemia16 severad |
|||
|
Uso prévio de regime com insulina6 basal uma vez ao dia |
||||||
|
Com insulina6 humana regular |
1 x Lantus® |
222 |
7,98 (0,01) |
152,8 (- 16,7) |
11,0%g |
0,9%g |
|
1 x insulina6 humana NPH |
218 |
7,95 (-0,05) |
147,6 (- 21,8) |
21,3% |
5,6% |
|
|
Com insulina lispro25 |
1 x Lantus® |
73 |
7,11 (-0,25) |
144,2 (- 26,5) |
6,8% |
2,7% |
|
1 x insulina6 humana NPH |
69 |
7,46 (-0,23) |
155,9 (-17,1) |
9,0% |
4,5% |
|
|
Uso prévio de regime com insulina6 basal mais de uma vez ao dia |
||||||
|
Com insulina6 humana regular |
1 x Lantus® |
334 |
7,77 (0,06) |
143,1 (23,6)g |
18,9% |
3,4% |
|
2 x insulina6 humana NPH |
345 |
7,69 (-0,05) |
155,9 (- 13,0) |
21,6% |
4,4% |
|
|
Com insulina lispro25 |
1 x Lantus® |
237 |
7,66 (-0,03) |
144,4 (- 30,6)g |
9,9% |
0,9% |
|
2 x insulina6 humana NPH |
240 |
7,64 (-0,05) |
162,9 (- 9,9) |
10,0% |
0,4% |
|
Diabetes mellitus5 tipo 2
|
População diabética |
Tratamento |
na |
Média do final do estudo (alteração média do basal) |
% de voluntários |
||
|
Hemoglobina glicosilada30 (%) |
Glicemia de jejum20 (mg/dL31)b |
Hipoglicemia16 noturnae |
Hipoglicemia16 severaf |
|||
|
Insulina6 em combinação com agentes antidiabéticos orais12 |
||||||
|
Sem uso prévio de insulina6 |
1 x Lantus® |
222 |
8,34 (- 0,65) |
126,5 (- 59,4) |
9,5%g |
1,8% |
|
1 x insulina6 humana NPH |
204 |
8,24 (- 0,63) |
129,4 (- 56,0) |
22,8% |
0,5% |
|
|
Uso prévio de insulina6 |
1 x Lantus® |
67 |
9,05 (0,31) |
128,0 (- 19,6) |
19,4% |
0,0% |
|
1 x insulina6 humana NPH |
77 |
9,10 (0,42) |
129,7(- 20,0) |
23,7% |
2,6% |
|
|
Insulina6 sem agentes antidiabéticos orais12 |
||||||
|
Uso prévio de insulina6 basal uma vez ao dia |
1 x Lantus® |
52 |
8,07 (- 0,34) |
153,0 (- 15,1) |
13,7% |
0,0% |
|
1 x insulina6 humana NPH |
48 |
7,92 (- 0,45) |
142,9(- 22,3) |
25,0% |
0,0% |
|
|
Uso prévio de insulina6 basal mais de uma vez ao dia |
1 x Lantus® |
207 |
8,15 (- 0,44) |
138,8 (- 25,4) |
29,8% |
0,5% |
|
2 x insulina6 humana NPH |
211 |
7,96 (- 0,61) |
144,9 (- 20,3) |
37,9% |
2,4% |
|
a = Número de voluntários randomizados e tratados
b = Conversão de glicemia de jejum20, mmol/L32 x 18 = mg/dL31
c = Porcentagem de voluntários com diabetes tipo 121 com experiência de hipoglicemia16 noturna; definida como eventos ocorridos enquanto adormecidos, entre a administração de insulina6 ao deitar-se até a glicemia de jejum20; com a glicemia33 < 36 mg/dL31 (2,0 mmol/L32); do mês 2 ao final do estudo
d = Porcentagem de voluntários com diabetes tipo 121 com experiência de hipoglicemia16 severa; definida como eventos que necessitaram de outra pessoa para assistência; com glicemia33 < 36 mg/dL31 (2,0 mmol/L32); do mês 2 ao final do estudo
e = Porcentagem de voluntários com diabetes tipo 211 com experiência de hipoglicemia16 noturna; definida como eventos ocorridos enquanto adormecidos, entre a administração de insulina6 ao deitar-se até a glicemia de jejum20; do mês 2 ao final do estudo
f = Porcentagem de voluntários com diabetes tipo 211 com experiência de hipoglicemia16 severa; definida como eventos que necessitaram de outra pessoa para assistência; do mês 2 ao final do estudo
g = p < 0,05; Lantus® comparada à insulina6 humana NPH
Tabela 2: Diabetes mellitus5 tipo 1 – pediátrica
|
População diabética |
Tratamento |
na |
Média do final do estudo (alteração média do basal) |
% de voluntários |
||
|
Hemoglobina glicosilada30 (%) |
Glicemia de jejum20 (mg/dL31)b |
Hipoglicemia16 noturnae |
Hipoglicemia16 severaf |
|||
|
Uso prévio de regime com insulina6 basal uma vez ao dia |
||||||
|
Com insulina6 humana regular |
1 x Lantus® |
106 |
9,15 (0,52) |
179,8 (- 23,2) |
3,8%g |
8,6% |
|
1 x insulina6 humana NPH |
98 |
9,26 (0,41) |
189,2 (- 14,0) |
6,5% |
4,3% |
|
|
Uso prévio de regime com insulina6 basal mais de uma vez ao dia |
||||||
|
Com insulina6 humana regular |
1 x Lantus® |
68 |
8,55 (0,05) |
159,7 (- 22,1) |
5,9% g |
10,3% g |
|
1 x insulina6 humana NPH |
77 |
8,86 (0,21) |
171,0 (- 6,3) |
1,8% |
7,0% |
|
Flexibilização da dose diária
A segurança e eficácia da Lantus® administrada antes do café da manhã, antes do jantar, ou antes de dormir, foram avaliadas em um estudo clínico amplo, controlado e randomizado8. Nesse estudo em pacientes com diabetes tipo 121 (estudo G) (Hamann, A. 2003) (n= 378), que foram também tratados com insulina lispro25 às refeições, Lantus® administrada em diferentes horários do dia, resultou em controle glicêmico equivalente àquele obtido quando administrado antes de dormir.
A segurança e eficácia da Lantus®, administrada antes do café da manhã ou na hora de dormir, também foram avaliadas em um estudo clínico amplo, controlado e randomizado8 (estudo H) (Fritsche, A. 2003) (n=697) em pacientes com diabetes tipo 211 não mais adequadamente controlados com tratamento oral. Todos os pacientes nesse estudo também receberam glimepirida34 3 mg diariamente. Lantus® administrada antes do café da manhã foi no mínimo tão efetivo na redução da hemoglobina glicosilada30 A1c35 (HbA1c13) quanto Lantus® administrada antes de dormir ou insulina6 humana NPH administrada antes de dormir. Vide tabela 3 a seguir.
Tabela 3: Flexibilização da dose diária de Lantus® em diabetes mellitus5 tipo 1 (estudo G) e tipo 2 (estudo H)
|
Duração do tratamento |
Estudo G – 24 semanas |
Estudo H – 24 semanas |
||||
|
Lantus® |
Lantus® |
Lantus® |
Lantus® |
Lantus® |
NPH |
|
|
Número de indivíduos tratados (ITT*) |
112 |
124 |
128 |
234 |
226 |
227 |
|
HbA1c13 |
||||||
|
Média Basal Média Final |
7,56 |
7,53 |
7,61 |
9,13 |
9,07 |
9,09 |
|
Alteração média do basal |
7,39 |
7,42 |
7,57 |
7,87 |
8,12 |
8,27 |
|
Alteração média do basal |
- 0,17 |
- 0,11 |
- 0,04 |
- 1,26 |
- 0,95 |
- 0,82 |
|
Dose de insulina6 basal (U) |
||||||
|
Média Final |
27,3 |
24,6 |
22,8 |
40,4 |
38,5 |
36,8 |
|
Alteração média do basal |
5,0 |
1,8 |
1,5 |
NA** |
NA** |
NA** |
|
Dose de insulina6 total (U) |
|
|
|
|||
|
Média Final |
53,3 |
54,7 |
51,5 |
|||
|
Alteração média do basal |
1,6 |
3,0 |
2,3 |
|||
* Intenção de tratamento
** Não aplicável
Diabetes tipo 211 – adulto (controle glicêmico)
Em um estudo clínico randomizado8, aberto, paralelo, de 24 semanas (estudo J) em pacientes com diabetes tipo 211 (n=756) com HbA1c13 > 7,5% (média de 8,6%) com um ou dois agentes antidiabéticos orais12, adicionou-se ao regime anterior Lantus® ou insulina NPH23, uma vez ao dia, ao se deitar. Para alcançar o objetivo de glicemia de jejum20 ≤ 100 mg/dL31 (5,5 mmol/L32), as doses da Lantus® e NPH foram ajustadas de acordo com a titulação de dose descrita na tabela 4 a seguir (Riddle, M. C. 2003).
Tabela 4: Titulação de dose no estudo J:
|
Período |
Dose ou ajuste de dose |
|
Início do tratamento |
10 U/dia |
|
Ajuste a cada 7 dias baseado na glicemia de jejum20 como descrito a seguir: |
|
|
Média da glicemia de jejum20 ≥ 180 mg/dL31 (10 mmol/L32) nos dois últimos dias consecutivos e sem episódios de hipoglicemia16 severa ou sem glicemia33 < 72 mg/dL31 (4,0 mmol/L32) |
Aumente a dose diária em 8 U |
|
Média da glicemia de jejum20 ≥ 140 mg/dL31 (7,8 mmol/L32) e < 180 mg/dL31 (10 mmol/L32) nos dois últimos dias consecutivos e sem episódios de hipoglicemia16 severa ou sem glicemia33 < 72 mg/dL31 (4,0 mmol/L32) |
Aumente a dose diária em 6 U |
|
Média da glicemia de jejum20 ≥ 120 mg/dL31 (6,7 mmol/L32) e < 140 mg/dL31 (7,8 mmol/L32) nos dois últimos dias consecutivos e sem episódios de hipoglicemia16 severa ou sem glicemia33 < 72 mg/dL31 (4,0 mmol/L32) |
Aumente a dose diária em 4 U |
|
Média da glicemia de jejum20 > 100 mg/dL31 (5,5 mmol/L32) e < 120 mg/dL31 ( 6,7 mmol/L32) nos dois últimos dias consecutivos e sem episódios de hipoglicemia16 severa ou sem glicemia33 < 72 mg/dL31 (4,0 mmol/L32) |
Aumente a dose diária em 2 U |
|
Então manter o objetivo de glicemia de jejum20 ≤ 100 mg/dL31 (5,5 mmol/L32) |
|
Utilizando-se este esquema de titulação de dose, a HbA1c13 foi reduzida a uma média de 6,96% com Lantus® e a 6,97% com insulina NPH23. Mais da metade dos pacientes em cada grupo alcançou um valor de HbA1c13 ≤ 7,0% (Lantus®, 58%; insulina NPH23, 57,3%; a dose média no desfecho do estudo foi de 47,2 U para Lantus® e 41,8 U para NPH). No grupo tratado com Lantus®, 33,2% dos pacientes alcançaram a eficácia do desfecho primário (valor de A1c35 ≤ 7,0% na ausência de hipoglicemia16 noturna confirmada ≤ 72 mg/dL31 [4 mmol/L32]), comparada a 26,7% no grupo tratado com NPH (p = 0,0486).
Um número menor de pacientes tratados com Lantus® apresentou hipoglicemia16 noturna comparado com pacientes tratados com insulina NPH23. Outros estudos clínicos em pacientes com diabetes tipo 211 (estudo E, F e G) mostraram resultados semelhantes com menor incidência15 de hipoglicemia16 noturna em pacientes tratados com Lantus® comparados aos tratados com NPH.
Retinopatia diabética36
Os efeitos da Lantus® na retinopatia diabética36 foram avaliados num estudo amplo de 5 anos, NPH-controlado, em que a progressão da retinopatia foi investigada por fotografia do fundo de olho37 utilizando um protocolo de classificação derivado do Estudo de Retinopatia Diabética36 de Tratamento Precoce (ETDRS). O resultado primário neste estudo foi a progressão de 3 ou mais etapas na escala ETDRS do desfecho do estudo. Os resultados desta análise estão demonstrados na tabela a seguir para ambas as populações pré-protocolo (primário) e intenção ao tratamento (ITT) e indicam não inferioridade da Lantus® à NPH na progressão da retinopatia diabética36 conforme avaliado neste resultado.
Número (%) de pacientes com 3 ou mais etapas de progressão na escala ETDRS do desfecho
|
|
Lantus® (%) |
NPH (%) |
Diferençaa,b (SE) |
95% IC para a diferença |
|
Pré-protocolo |
53/374 (14,2%) |
57/363 (15,7%) |
- 1,98% (2,57%) |
- 7,02% a 3,06% |
|
Intenção ao tratamento |
63/502 (12,5%) |
71/487 (14,6%) |
- 2,10 (2,14%) |
- 6,29% a 2,09% |
a: Diferença = Lantus® - NPH
b: utilizando um modelo linear generalizado (SAS GENMOD) com tratamento e estado basal HbA1c13 estratificada conforme classificação das variáveis independentes e com distribuição binomial e identificação da função de ligação (Rosenstock et al. 2009).
Efeitos psicológicos de satisfação com o tratamento
Pacientes com diabetes mellitus5 tipo 1 tratados com regimes que incluíram insulina glargina1 demonstraram significativa melhora de satisfação com o tratamento quando comparados a pacientes com regimes de insulina NPH23. (Questionário de Satisfação do Tratamento de Diabetes38) (Witthaus E et al. 2001).
Estudo ORIGIN (Estudo 4032)
ORIGIN (Outcome Reduction with Initial Glargine Intervention – Desfecho da redução com intervenção inicial com glargina) foi um estudo internacional multicêntrico, randomizado8, com desenho fatorial 2x2 conduzido com 12.537 participantes com glicose24 de jejum alterada (GJA), com tolerância a glicose24 alterada (TGA) ou início de diabetesmellitus tipo 2 e evidência de doença cardiovascular. Os pacientes foram distribuídos aleatoriamente para receber Lantus® (n = 6264), com valor titulado de 95 mg/dl31 ou menos na glicemia de jejum20, ou tratamento padrão (n = 6.273). Os pacientes tinham a idade média de 63,5 anos, com duração média do diabetes38 de 5,8 anos naqueles com diabetes38 pré-existente, e média de HbA1c13 de 6,4%. A duração média do acompanhamento foi de 6,2 anos. Ao final do estudo 81% dos pacientes distribuídos para tomar Lantus® ainda continuavam com o tratamento. Durante o tratamento a média de valores de HbA1c13 variou entre 5,9 e 6,4% no grupo Lantus®, e 6,2 e 6,6% no grupo de tratamento padrão durante o período de acompanhamento. A média de glicemia de jejum20 no grupo Lantus® esteve conforme o objetivo (< 95mg/dL) seguindo o valor titulado para o período do estudo. As taxas de hipoglicemia16 severa (participantes afetados por 100 participantes-/ano de exposição) foi de 1,05 para insulina glargina1 e de 0,30 para o grupo com tratamento padrão. Em geral, a hipoglicemia16 severa foi relatada por 3,7% destes participantes durante os 6 anos de estudo (aproximadamente 0,6% por ano/participante). A média de alteração de peso corpóreo desde o início até a última consulta do tratamento foi 2,2kg maior no grupo Lantus® do que no grupo com tratamento padrão.
O objetivo primário deste estudo foi examinar o efeito do Lantus® em dois desfechos de eficácia coprimários compostos. O primeiro foi o tempo para primeira ocorrência de morte por doença cardiovascular, infarto39 não-fatal do miocárdio40 ou acidente vascular41 não- fatal, e o segundo foi o tempo para a primeira ocorrência de qualquer primeiro evento coprimário, ou procedimento de revascularização (cardíaco, carotídeo ou periférico), ou hospitalização por insuficiência cardíaca42.
Os desfechos secundários foram:
- mortalidade43 por todas as causas
- desfecho microvascular composto
- desenvolvimento de diabetes tipo 211, em participantes com GJA e/ou TGA no início do estudo
Os resultados dos desfechos primários e secundários, bem como os resultados de cada componente dos desfechos coprimários, são disponibilizados nas duas tabelas a seguir.
Tabela 5: ORIGIN: Hazard Ratio para os desfechos primários e secundários
|
|
Lantus® n = 6264 |
Tratamento padrão |
Lantus® x Tratamento padrão |
|
|
Participantes com eventos N (%) |
Participantes com eventos N (%) |
Hazard Ratio (95% CI) |
|
Desfechos primários |
|||
|
Morte cardiovascular, infarto39 não-fatal do miocárdio40 (MI) ou acidente vascular41 não- fatal |
1041 (16,6) |
1013 (16,1) |
1,02 (0,94 – 1,11) |
|
Morte cardiovascular, infarto39 não-fatal do miocárdio40 (MI) ou acidente vascular41 não- fatal ou hospitalização por insuficiência cardíaca42 ou procedimento de revascularização |
1792 (28,6) |
1727 (27,5) |
1,04 (097 – 1,11) |
|
Desfechos secundários |
|||
|
Mortalidade43 por todas as causas |
951 (15,2) |
965 (15,4) |
0,98 (0,90, 1,08) |
|
Desfecho microvascular composto* |
1323 (21,1) |
1363 (21,7) |
0,97 (0,90, 1,05) |
|
Componentes de desfecho coprimário |
|||
|
Morte cardiovascular |
580 (9,3) |
576 (9,2) |
1,00 (0,89, 1,13) |
|
MI (fatal ou não-fatal) |
336 (5,4) |
326 (5,2) |
1,03 (0,88, 1,19) |
|
Acidente vascular41 (fatal ou não-fatal) |
331 (5,3) |
319 (5,1) |
1,03 (0,89, 1,21) |
|
Revascularizações |
908 (14,5) |
860 (13,7) |
1,06 (0,96, 1,16) |
|
Hospitalizações por insuficiência cardíaca42 |
310 (4,9) |
343 (5,5) |
0,90 (0,77, 1,05) |
* com componentes de: fotocoagulação por laser ou vitrectomia ou cegueira por retinopatia diabética36; albuminúria44 progressiva; duplicação da creatinina45 sérica ou desenvolvimento da necessidade de transplante renal46.
Tabela 6: Taxa de incidência15 de diabetes38 ao final do estudo pelo Teste Oral de Tolerância à Glicose24 (TOTG47) *
|
Tratamento (N) |
Lantus® (6264) |
Tratamento padrão (6273) |
|
Número de participantes** |
737 |
719 |
|
Número de participantes que desenvolveram diabetes38 (%) |
182 (24,7) |
224 (31,2) |
|
Odds Ratio (95% CI) |
|
0,72 (0,58–0,91) |
* TOTG47 ao final do estudo aconteceu após 3–4 semanas da descontinuação de Lantus®.
** Participantes com pré-diabetes48 (GJA ou TGA) no início do estudo, baseado na performance de TOTG47.
Não foram encontradas diferenças estatisticamente significantes entre os grupos de tratamento na incidência15 global de câncer49 (todos os tipos combinados) ou morte por câncer49. O tempo para o primeiro evento de qualquer tipo de câncer49 ou um novo câncer49 durante o estudo foi similar entre os dois grupos com hazard ratio de 0,99 (0,88, 1,11) e 0,96 (0,85, 1,09) respectivamente.
A participação em ORIGIN por uma média de 6,2 anos demonstrou que o tratamento com Lantus® não altera o risco de eventos cardiovasculares, mortalidade43 por todas as causas ou câncer49, quando comparado com a terapia padrão de redução de glicose24. Adicionalmente, controle metabólico foi mantido em baixo nível de glicemia33 com a diminuição da porcentagem de participantes desenvolvendo diabetes38, ao custo de um modesto aumento em hipoglicemia16 e ganho de peso.
Os seguintes estudos demonstraram a flexibilidade de dose: Estudo G: “A randomized clinical trial comparing breakfast, dinner, or bedtime administration of insulin glargine in patients with type 1 diabetes38.” (Hamann, A. 2003) e Estudo H: “Glimepiride combined with morning insulin glargine, bedtime neutral protamine hagedorn insulin, or bedtime insulin glargine in patients with type 2 diabetes38. A randomized, controlled trial.” (Fritsche, A. 2003).
Outros estudos também demonstraram a eficácia da Lantus®: “The Treat to Target Trial. Randomized addition of glargine or human NPH insulin to oral therapy of type 2 diabetic patients.” (Riddle, M. C. 2003); “Less hypoglycemia with insulin glargine in intensive insulin therapy for type 1 diabetes38.” (Ratner, R.E. 2000); “Less nocturnal hypoglycemia and better post-dinner glucose control with bedtime insulin glargine compared with bedtime NPH insulin during insulin combination therapy in type 2 diabetes38.” (Yki- Jarvinen, H. 2000); “Glycemic control with insulin glargine in patients with type 2 diabetes38 is safely maintained in long-term exposure.” (Karacovsky-Bielesc, G. 2002); “Basal insulin therapy in type 2 diabetes38: 28-week comparison of insulin glargine (HOE 901) and NPH insulin.” (Rosenstock, J. 2001); “Improved metabolic control with type 1 and type 2 diabetes38 following the initiation/switching to insulin glargine in clinical practice.” (Schreiber, S.A. 2002).
CARACTERÍSTICAS FARMACOLÓGICAS
Propriedades Farmacodinâmicas
Glargilin® é um antidiabético que contém insulina glargina1. A insulina glargina1 é uma insulina6 humana análoga produzida por tecnologia de DNA-recombinante, utilizando Escherichia coli (cepa50 K12) como organismo produtor.
Glargilin® é uma insulina6 humana análoga desenhada para ter baixa solubilidade em pH neutro. Em pH 4 [como na solução injetável de Glargilin®], é completamente solúvel. Após ser injetada no tecido subcutâneo51, a solução ácida é neutralizada, levando a formação de micro-precipitados do qual pequenas quantidades de insulina glargina1 são liberadas continuamente, levando a um perfil de concentração / tempo previsível, sem pico e suave, com duração de ação prolongada, que suporta a administração uma vez ao dia.
A insulina glargina1 é metabolizada em dois metabólitos52 ativos M1 e M2 (vide “Propriedades Farmacocinéticas”). Ligação ao receptor de insulina6: os estudos in vitro indicam que a afinidade da insulina glargina1 e de seus metabolitos52 M1 e M2 ao receptor da insulina6 em humanos é similar àquela da insulina6 humana.
Ligação ao receptor IGF-1: a afinidade da insulina glargina1 ao receptor IGF-1 humano é aproximadamente 5 a 8 vezes maior que a da insulina6 humana (mas aproximadamente 70 a 80 vezes menor que àquela do IGF-1), enquanto que M1 e M2 se ligam ao receptor IGF- 1 com uma afinidade um pouco menor comparada a insulina6 humana.
A concentração terapêutica53 total de insulina6 (insulina glargina1 e seus metabólitos52) encontrada em pacientes com diabetes tipo 121 foi acentuadamente menor que aquela que seria requerida para ocupação máxima de metade dos receptores IGF-1 e a subsequente ativação da via proliferativa mitogênica iniciada pelo receptor IGF-1. As concentrações fisiológicas54 do IGF-1 endógeno podem ativar a via proliferativa mitogênica; entretanto, as concentrações terapêuticas encontradas na terapia com insulina6, incluindo a terapia com insulina glargina1, são consideravelmente menores que as concentrações farmacológicas requeridas para ativar a via IGF-1.
A atividade fundamental da insulina6, incluindo insulina glargina1, é a regulação do metabolismo55 da glicose24. A insulina6 e seus análogos diminuem os níveis glicêmicos estimulando a captação da glicose24 periférica, especialmente pelo músculo esquelético56 e tecido adiposo57, e pela inibição da produção da glicose24 hepática58. Insulina6 inibe a lipólise no adipócito, inibe a proteólise e aumenta a síntese proteica.
Propriedades Farmacocinéticas
O t1/2 de Glargilin® é de alguns minutos, similar a outras insulinas.
As características de ação da insulina6 dependem da sua taxa de liberação. Dentre sujeitos sadios ou diabéticos para os quais insulina glargina1 é subcutaneamente injetada, ela é liberada mais lentamente e tem duração mais prolongada da ação que insulina NPH23, e não apresenta um pico pronunciado, portanto, insulina glargina1 tem função estável e de longa duração na redução dos níveis de glicose24 sanguíneos, seu tempo de ação pode alcançar até 24 horas.
Se administrada subcutaneamente uma vez ao dia, as concentrações séricas de insulina6 podem alcançar estado estável 2~4 dias após a primeira injeção9.
A absorção de insulina glargina1 é afetada pela tecnologia de injeção9, dieta, exercício ou doenças. Portanto, o efeito de redução de glicose24 pode variar entre indivíduos e/ou no próprio indivíduo.
O estudo de fase 1, de clamp euglicêmico comparativo de farmacocinética e farmacodinâmica de Glargilin® versus o produto biológico comparador (Lantus®, Sanofi- Aventis), foi realizado em 16 voluntários sadios. A técnica de clamp euglicêmico utilizou dose de 0,4U/kg de cada insulina6. As concentrações plasmáticas de ambas as insulinas mostraram atividade metabólica constante durante 24h (P <0,.05). Não houveram diferenças significativas entre as INS-AUC0-24h, INS-Cmax e INSTmax entre as duas preparações de glargina (P >0.05). Os resultados mostraram que Glargilin® e Lantus® são bioequivalentes.
Dados pré-clínicos de segurança: dados pré-clínicos não mostram risco para humanos baseado em estudos convencionais de farmacodinâmica primária, farmacologia59 de segurança, toxicidade60 de dose única e toxicidade60 de dose repetida, assim como imunogenicidade.
Toxicidade60 genética
A insulina glargina1 não foi mutagênica em testes para detecção de mutações genéticas em bactérias e células61 de mamíferos (teste de Ames e HGPRT) e em testes para detecção de aberrações cromossômicas (citogenética in vitro em células61 V79 e in vivo em hamsters chineses).
Toxidade reprodutiva
Ratas receberam insulina glargina1 subcutânea62 (SC) antes do acasalamento para a gravidez63, a dose atingiu 0,36 mg/kg/d. Coelhas grávidas receberam 0,072 mg/kg/d SC durante a organogênese, que é respectivamente cerca de 7 vezes e 2 vezes a dose inicial subcutânea62 recomendada em humanos de 10U/d (0,008mg/kg/d). O efeito da insulina glargina1 em ratos e coelhos não é significativamente diferente da insulina6 humana. No grupo da dosagem alta, duas de cinco ninhadas de coelhos apresentaram dilatação ventricular. A fertilidade e o desenvolvimento embrionário inicial não foram anormais. No teste combinado de fertilidade do rato, pré-natal e pós-parto, os ratos receberam insulina glargina1 SC 0,36 mg/kg/d, calculada em mg/m2, que é 7 vezes a dose inicial humana subcutânea62 recomendada de 10U/d (0,008 mg/kg/d). Neste teste pode-se observar toxicidade60 materna relacionada à dose causada pela hipoglicemia16, incluindo morte. Consequentemente, uma redução da taxa de procriação ocorreu apenas no grupo de alta dose. Efeitos semelhantes foram observados com insulina NPH23.
Carcinogênese
Em camundongos e ratos, estudos padrão de carcinogenicidade de dois anos com insulina glargina1 foram realizados em doses de até 0,455 mg/kg, que foi aproximadamente 5 e 10 vezes a dose inicial humana SC recomendada de 10U/dia (0,008 mg/kg/d). Os histiocitomas foram encontrados nos locais de injeção9 em ratos e camundongos machos em grupos contendo veículos ácidos e são considerados uma resposta à irritação e inflamação64 crônica do tecido65 em roedores. Estes tumores não foram encontrados em animais fêmeas, em grupos de controle de solução salina ou comparadores de insulina6 usando um veículo diferente.
CONTRAINDICAÇÕES
Glargilin® é contraindicada para pacientes66 com hipersensibilidade à insulina glargina1 ou a qualquer componente da fórmula.
ADVERTÊNCIAS E PRECAUÇÕES
Geral
A terapia com insulina6 geralmente requer habilidades apropriadas para o autocontrole do diabetes38, incluindo monitorização da glicemia33, técnicas de injeção9 adequadas, medidas para o reconhecimento e controle de aumentos ou reduções nos níveis glicêmicos (hipoglicemia16 ou hiperglicemia7). Adicionalmente, os pacientes devem aprender como lidar com situações especiais como administração de doses de insulina6 inadvertidamente aumentadas, doses inadequadas ou esquecidas, ingestão inadequada de alimentos ou perda de refeições. O grau de participação do paciente no próprio controle do diabetes38 é variável e é geralmente determinado pelo médico.
O tratamento com insulina6 requer constante vigilância para a possibilidade de hiper e hipoglicemia16. Os pacientes e seus familiares devem saber quais passos devem tomar se ocorrer ou houver suspeita de hiperglicemia7 ou hipoglicemia16 e devem saber quando informar o médico.
Na ocorrência de controle de glicemia33 insuficiente ou tendência de ocorrência de episódios hipo ou hiperglicêmicos, outros fatores como, a aderência do paciente ao tratamento prescrito, a escolha do local de injeção9 e técnicas de manuseio de aparelhagem para injeção9 e todos os outros fatores relevantes devem ser revistos antes de considerar um ajuste de dose.
As doenças intercorrentes, particularmente a infecção67, geralmente resultam no aumento da dose de insulina6.
Os pacientes devem ser instruídos a realizar a rotação contínua do local da injeção9 para reduzir o risco de desenvolver lipodistrofia68 (alteração na distribuição de gordura69 no subcutâneo2, neste caso, causado pela aplicação da medicação repetidas vezes no mesmo local) e amiloidose70 cutânea71 localizada (depósito de amiloide, uma substância que surge de lesões72 na pele73). Há um risco potencial de absorção retardada de insulina6 e piora do controle glicêmico após injeções de insulina6 em locais com essas reações. Foi relatado que uma mudança repentina no local da injeção9 para uma área não afetada resultou em hipoglicemia16 (diminuição da taxa de açúcar74 no sangue29). O monitoramento da glicose24 no sangue29 é recomendado após a mudança no local da injeção9, e o ajuste da dose dos medicamentos antidiabéticos pode ser considerado (vide “9. Reações adversas”).
Hipoglicemia16
O tempo para a ocorrência da hipoglicemia16 depende do perfil de ação das insulinas usadas e pode, portanto, alterar quando o tratamento é substituído.
Assim como com todas as insulinas, deve ser exercido cuidado particular e a monitoração intensificada da glicemia33 é aconselhável, em pacientes nos quais sequelas75 de episódios hipoglicêmicos podem ser de particular relevância clínica. Por exemplo, podem ser pacientes com estenoses76 significativas das artérias coronárias77 ou das veias78 sanguíneas que suprem o cérebro79 (risco de complicações cardíacas ou cerebrais da hipoglicemia16), bem como pacientes com retinopatia proliferativa80, particularmente quando não tratados com fotocoagulação (risco de cegueira transitória após hipoglicemia16).
Em um estudo clínico, sintomas81 de hipoglicemia16 ou respostas hormonais contra- regulatórias foram similares após administração intravenosa de insulina glargina1 e insulina6 humana tanto em voluntários sadios quanto em pacientes com diabetes tipo 121. Contudo, sob certas circunstâncias, assim como com todas as insulinas, os sintomas81 iniciais que indicam o início da hipoglicemia16 ("sintomas de aviso") podem se alterar, ser menos pronunciados ou ausentes, por exemplo, nas seguintes situações: controle glicêmico acentuadamente melhor, hipoglicemia16 de desenvolvimento gradual, idade avançada, na presença de neuropatia autonômica82, em pacientes com história longa de diabetes38, em pacientes com doenças psiquiátricas ou que estejam sob uso concomitante de outros medicamentos (vide “6. Interações Medicamentosas”). Nestas circunstâncias, a hipoglicemia16 severa (ou mesmo a perda de consciência) pode desenvolver-se sem que o paciente perceba.
O efeito prolongado da insulina glargina1 subcutânea62, pode atrasar a recuperação de hipoglicemia16. Se valores normais ou diminuídos de hemoglobina glicosilada30 forem notados, a possibilidade de episódios de hipoglicemia16 periódicos ou desconhecidos (especialmente noturnos) devem ser considerados.
A aderência do paciente com a dose prescrita e restrições na dieta, o procedimento correto para a administração da insulina6 e o reconhecimento dos sintomas81 da hipoglicemia16 são essenciais na redução do risco de hipoglicemia16.
A presença de fatores que aumentam a susceptibilidade83 à hipoglicemia16 requer monitoração particularmente cuidadosa e pode necessitar ajuste da dose. Estes incluem:
- alteração da área da injeção9;
- aumento na sensibilidade à insulina6 (por exemplo: remoção dos fatores de stress);
- atividade física aumentada ou prolongada ou falta de hábito no exercício físico;
- doenças intercorrentes (por exemplo: vômito84 ou diarreia85);
- ingestão inadequada de alimentos;
- consumo de álcool;
- certos distúrbios endócrinos não compensados;
- uso concomitante de outros medicamentos (vide “6. Interações Medicamentosas”).
Hipoglicemia16 pode ser corrigida geralmente pela ingestão imediata de carboidrato86. Pelo fato de a ação corretiva inicial ter que ser tomada imediatamente, os pacientes devem transportar consigo pelo menos 20 g de carboidrato86 durante todo o tempo, bem como alguma informação que os identifique como diabéticos.
Doenças intercorrentes
O médico deve ser informado caso ocorram doenças intercorrentes, uma vez que a situação necessita da intensificação da monitoração metabólica. Em muitos casos, testes de urina87 para cetonas são indicados e frequentemente é necessário ajuste de dose da insulina6. A necessidade de insulina6 é frequentemente aumentada. Em pacientes com diabetes tipo 121, o suprimento de carboidrato86 deve ser mantido mesmo se os pacientes forem capazes de comer ou beber apenas um pouco ou nenhum alimento, ou estiverem vomitando, etc.; em pacientes com diabetes38 do tipo 1 a insulina6 não deve nunca ser omitida completamente.
Precauções ao viajar
Antes de viajar, o paciente deve ser informado sobre:
- a disponibilidade da insulina6 no local de destino;
- o suprimento de insulina6, seringas, etc.;
- a correta armazenagem da insulina6 durante a viagem;
- o ajuste das refeições e a administração de insulina6 durante a viagem;
- a possibilidade da alteração dos efeitos em diferentes tipos de zonas climáticas;
- a possibilidade de novos riscos à saúde4 nas cidades que serão visitadas.
Gravidez63 e Lactação88
Não há nenhum estudo clínico controlado com o uso de insulina glargina1 em mulheres grávidas. Um amplo número (mais de 1000 resultados de gravidez63 retrospectiva e prospectiva) de gestantes expostas ao produto referência Lantus®, determinado por dados de Farmacovigilância pós-comercialização, indicam que não há efeitos adversos específicos da insulina glargina1 em gestantes ou na saúde4 de fetos ou recém-nascidos. Além disso, uma meta-análise de oito estudos clínicos observacionais incluindo 331 mulheres utilizando insulina glargina1 (Lantus®) e 371 mulheres utilizando insulina NPH23 foi realizada para avaliar a segurança da insulina glargina1 e da insulina NPH23 em diabetes gestacional89 e preexistente. Não foram observadas diferenças com relação à segurança materna ou neonatal entre a insulina glargina1 e a insulina NPH23 durante a gravidez63.
Estudos em animais, com doses de até 6-40 vezes a dose humana, não indicam efeitos prejudiciais diretos na gravidez63.
Mulheres com diabetes38 preexistente ou gestacional devem manter um bom controle metabólico durante a gravidez63 para prevenir resultados adversos associados com a hiperglicemia7. Insulina glargina1 pode ser utilizada durante a gravidez63, se clinicamente necessário.
Nos três primeiros meses, as necessidades de insulina6 podem diminuir e geralmente aumentam durante o segundo e terceiro trimestres. Imediatamente após o parto, as necessidades de insulina6 diminuem rapidamente (aumento do risco de hipoglicemia16). Portanto, monitoração cuidadosa da glicemia33 é essencial nessas pacientes.
Ajustes das doses de insulina6, dieta ou ambos podem ser necessários em mulheres que estão amamentando.
Categoria de risco na gravidez63: C. Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Populações especiais
Pacientes idosos: recomenda-se que as doses iniciais, os aumentos de dose e doses de manutenção sejam conservadoras para se evitar as reações hipoglicêmicas.
Crianças: Glargilin® pode ser administrada em crianças com 2 anos de idade ou mais. Ainda não foi estudada a administração de insulina glargina1 em crianças abaixo de 2 anos de idade. O perfil de segurança para pacientes66 menores de 18 anos é semelhante ao perfil de segurança para pacientes66 maiores de 18 anos.
Não há dados clínicos de segurança disponíveis em pacientes com idade abaixo de 2 anos de idade.
Insuficiência renal90: em pacientes com insuficiência renal90, as necessidades de insulina6 podem ser menores devido ao metabolismo55 de insulina6 reduzido.
Em idosos, a deterioração progressiva da função renal46 pode levar a uma redução estável das necessidades de insulina6.
Insuficiência hepática91: em pacientes com insuficiência hepática91 severa, as necessidades de insulina6 podem ser menores devido à capacidade reduzida para gliconeogênese92 e ao metabolismo55 de insulina6 reduzido.
Efeitos na habilidade de dirigir e operar máquinas
Como resultado de hipoglicemia16, hiperglicemia7 ou visão93 prejudicada (vide “9. Reações Adversas”), a habilidade de concentração e reação pode ser afetada, possivelmente constituindo risco em situações onde estas habilidades são de particular importância.
Os pacientes devem ser aconselhados a tomarem precauções para evitarem hipoglicemia16 enquanto dirigem. Isso é particularmente importante naqueles que reduziram ou que não conhecem os "sintomas de aviso" de hipoglicemia16 ou que têm episódios frequentes de hipoglicemia16. A prudência no dirigir deve ser considerada nessas circunstâncias.
Este medicamento pode causar doping.
INTERAÇÕES MEDICAMENTOSAS
Várias substâncias afetam o metabolismo55 da glicose24 e podem requerer ajuste da dose de insulina6 e particularmente monitorização cuidadosa.
Um aumento no efeito de redução de glicemia33 e na susceptibilidade83 à hipoglicemia16 pode ocorrer no uso concomitante de, por exemplo: antidiabéticos orais12, inibidores da ECA, salicilatos, disopiramida, fibratos, fluoxetina, inibidores da MAO94, pentoxifilina, propoxifeno e antibióticos sulfonamídicos.
Uma diminuição no efeito de redução de glicemia33 pode ocorrer com o uso concomitante de corticosteroides, danazol, diazóxido, diuréticos95, agentes simpatomiméticos (como epinefrina, salbutamol96, terbutalina), glucagon97, isoniazida, derivados da fenotiazina, somatropina, hormônios da tireoide98, estrógenos e progestágenos (por exemplo: em contraceptivos orais), inibidores da protease99 e medicações antipsicóticas atípicas (por exemplo, olanzapina e clozapina).
Os betabloqueadores, clonidina, sais de lítio e álcool podem tanto potencializar ou diminuir o efeito de redução da glicemia33 da insulina6. A pentamidina pode causar hipoglicemia16, que pode algumas vezes ser seguida por hiperglicemia7.
Além disso, sob a influência de medicamentos simpatolíticos como, por exemplo, beta- bloqueadores, clonidina, guanetidina e reserpina, os sinais100 de contra regulação adrenérgica podem ficar reduzidos ou ausentes.
Casos de insuficiência cardíaca42 com pioglitazona foram relatados quando utilizada em combinação com insulina6, especialmente em pacientes com fatores de risco para o desenvolvimento de insuficiência cardíaca42.
Se a pioglitazona for usada em combinação com a injeção9 de insulina glargina1 recombinante, devem ser observados sintomas81 e sinais100 de insuficiência cardíaca42, como ganho de peso e edema101. Se algum sinal102 de doença cardíaca piorar, a pioglitazona deve ser descontinuada.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Canetas não abertas:
Glargilin® caneta descartável deve ser armazenada em temperatura entre 2 e 8°C e não deve ser congelada ou mantida próxima da bandeja de gelo do refrigerador. Este produto deve ser mantido longe da luz e calor. Antes de utilizar a caneta, mantê-la à temperatura ambiente por 1 a 2 horas.
Prazo de validade: 24 meses após a data de fabricação
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Canetas em uso:
Após aberto, válido por 4 semanas (28 dias), protegido da luz e do calor.
Conservar em temperatura ambiente até 30°. As canetas em uso não devem ser armazenadas sob refrigeração.
Descartar o produto caso tenha congelado. Descartar as canetas mantidas fora da refrigeração após 28 dias.
Características físicas e organolépticas
Solução incolor estéril.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Glargilin® é administrada por injeção9 tecidual subcutânea62. Não deve ser administrada intravenosamente.
Dentro de uma determinada área de injeção9 (abdome103, coxa104 ou deltoide105), deve ser escolhido um local diferente para cada injeção9, para reduzir o risco de lipodistrofia68 e amiloidose70 cutânea71 localizada. Não aplicar em áreas com lipodistrofia68 ou amiloidose70 cutânea71 localizada (vide “5. Advertências e precauções” e “9. Reações adversas”). A absorção de insulina glargina1 não é diferente entre as áreas de injeção subcutânea106 do abdome103, coxa104 ou deltoide105. Assim como para todas as insulinas, a taxa de absorção e consequentemente o início e duração da ação podem ser afetados por exercício e outras variáveis.
A prolongada duração de ação da insulina glargina1 é dependente da injeção9 no espaço subcutâneo2. A administração intravenosa da dose subcutânea62 usual pode resultar em hipoglicemia16 severa.
Instruções para uso da caneta descartável Glargilin®
Por favor, leia completamente estas instruções de uso e siga as instruções cuidadosamente antes de utilizar sua caneta descartável Glargilin®, mesmo que você tenha usado um dispositivo de caneta de injeção9 semelhante anteriormente.
Só utilize a caneta conforme indicação do seu médico.
Glargilin® apresenta-se em refis lacrados nas canetas injetoras descartáveis.
Inspecionar a caneta antes do uso. Somente utilizar se a solução estiver clara, incolor, sem a presença de partículas visíveis e se estiver com a consistência de água. Por não ser suspensão, não é necessária a ressuspensão antes do uso.
Glargilin® não deve ser misturada ou diluída com qualquer outra insulina6, pois existe risco de alterar o perfil de tempo/ação de Glargilin® ou causar a sua precipitação.
Não use qualquer outro tipo de insulina6 sem a orientação médica.
Recomenda-se anotar a data do primeiro uso da caneta.
A caneta preenchida de Glargilin libera dosagens de 1 a 60 unidades, de 1 em 1 unidade. Cada caneta contém múltiplas doses.
Informação importante
- Só use a caneta depois de ter recebido treinamento adequado do seu profissional de saúde4.
- Sempre descarte a caneta em conformidade com os regulamentos locais depois de tê-la usado.
- Utilize sempre uma nova agulha na caneta para cada injeção9.
- Mantenha sempre a caneta tampada quando não estiver utilizando-a.
- Sempre verifique a data de validade antes de usar.
- Esta é uma caneta de injeção9 descartável preenchida de dose múltipla e de dose variável.
- Para limpar a caneta, um pano úmido é suficiente.
- Substitua a agulha da caneta após cada utilização e não guarde a caneta com a agulha conectada.
- Guarde este folheto para consulta futura.
Características técnicas
Cada caneta contém um total de 300 unidades de insulina6. Você pode ajustar dosagens de 1 a 60 unidades de 1 em 1 unidade. Cada caneta contém múltiplas doses.
Contato
Se você tiver quaisquer dúvidas ou problemas relacionados com a caneta, consulte o seu médico e/ou entre em contato com o Serviço de Atendimento ao Consumidor da BIOMM S.A. 0800-057-2466.
Desenho
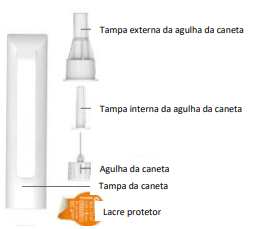

Advertências
Informações importantes de risco
Se as seguintes instruções não forem observadas, há o risco de receber uma dose incorreta de medicação. Se você tiver alguma dúvida sobre a sua saúde4, consulte o seu médico imediatamente.
Para garantir a manipulação correta
- As crianças somente devem utilizar a caneta para auto-injeção9 se tiverem atingido a idade de 7 anos e estiverem sendo supervisionadas por adultos treinados com experiência em seu uso.
- A caneta não deve ser usada por pacientes cegos ou deficientes visuais sem a assistência de pessoas com treinamento adequado.
- Armazenar a caneta fora do alcance das crianças e quaisquer outras pessoas que não estão familiarizadas com o manuseio adequado.
- Se você não entender ou não for capaz de executar um passo que é descrito no manual de instruções, entre em contato com seu médico ou o Serviço de Atendimento ao Consumidor da BIOMM S.A. através do telefone 0800-057- 2466.
Para assegurar o uso correto
- Só utilize a caneta com o tratamento que foi prescrito pelo seu médico. Siga as instruções dadas pelo seu médico sobre as partes adequadas do seu corpo para a injeção9. Quaisquer alterações devem ser feitas sob a supervisão de um médico.
- Antes de usar a caneta, verifique visualmente a caneta, para garantir que não esteja danificada.
- Evite a transmissão de doenças, usando a caneta e agulhas da caneta apenas por uma pessoa.
- Evite dobrar ou quebrar a agulha da caneta. Uma vez que a agulha da caneta foi inserida na pele73, não mude o ângulo da injeção9. Alterar o ângulo pode dobrar ou quebrar a agulha da caneta. Uma agulha da caneta dobrada ou quebrada pode ficar presa no corpo ou ficar completamente sob a pele73. Se uma agulha quebrada da caneta ficar presa no corpo ou ficar sob a pele73, procure ajuda médica imediatamente.
- Nunca submeta a caneta a temperaturas extremas, luz solar direta e condições de muito frio (por exemplo: dentro de um carro ou um congelador).
- Não deixe cair a caneta e não bata contra superfícies duras. Caso contrário, um teste funcional deve ser realizado antes da utilização da caneta novamente.
- Não mergulhe a caneta na água ou em qualquer outro líquido. Manuseie a caneta com cuidado.
- Nunca use a caneta se você tiver dúvidas sobre o seu adequado manuseio.
- Nunca aplique força excessiva na caneta. Nunca tente ultrapassar uma interrupção induzida pelo dispositivo através da aplicação de força. A caneta pode ser danificada e não funcionar adequadamente.
- Nunca tente você mesmo, reparar uma caneta danificada. Se a caneta estiver danificada, contate o Serviço de Atendimento ao Consumidor da BIOMM S.A. 0800-057-2466
Informações Adicionais
Indicadores sonoros e táteis: Sua caneta apresenta indicadores sonoros e táteis ao definir a dose. Para cada unidade do medicamento que é adicionada à dose ou corrigida, é percebido um clique audível e tátil de resistência.
Agulhas compatíveis da caneta: Compatível com as principais agulhas disponíveis no mercado.
Descarte: Descarte a agulha de forma segura, conforme regulamentações locais e como orientado pelo médico.
Descarte a caneta após o carpule (refil) estar vazio. Você pode descartar a caneta de acordo com os regulamentos locais sobre resíduos ou juntamente com o lixo doméstico.
Como Aplicar o Medicamento Glargilin® em Canetas Descartáveis
1ª etapa: Verificação da insulina6
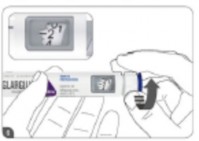
- Verifique o rótulo da caneta para certificar-se de que você está com a insulina6 correta.
- Remova a tampa da caneta.
- Verifique a aparência da insulina6. Glargilin® é uma insulina6 límpida, incolor, se partículas sólidas e com consistência aquosa. Não use a caneta se a insulina6 estiver turva, com cor ou com partículas.
2ª etapa: Conectando a agulha na caneta
Use sempre uma agulha estéril nova para cada aplicação. Isso ajuda a prevenir contaminação e possíveis entupimentos da agulha.
Antes de utilizar a agulha, leia cuidadosamente as “Instruções de uso” que acompanham as agulhas.
As agulhas mostradas nas figuras são ilustrativas.
Limpe o lacre de borracha com álcool.
- Retirar a tampa da caneta.
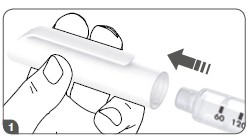
- Retirar a película de proteção sobre a agulha.
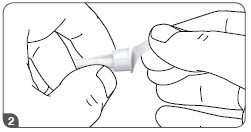
- Encaixar a agulha na caneta mantendo-a em linha reta.
Nota: O encaixe firme está assegurado quando aparafusado, mesmo sem um limite de parada perceptível.
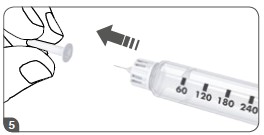
- Retirar a tampa exterior da agulha inserida na caneta e guardá-la para uso após a injeção9.

- Retirar a proteção interior da agulha da caneta e descartá-la.
3ª etapa: Teste funcional Importante:
- Antes da primeira injeção9, a caneta deve ser preparada de modo a remover as bolhas de ar do carpule (refil) para a dosagem exata e/ou para assegurar que a agulha não se encontre obstruída.
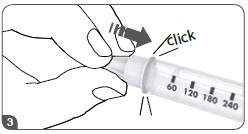
- Selecionar uma dose de 2 unidades girando o botão de dose no sentido horário (2 cliques). Se necessário, a dose selecionada pode ser corrigida girando o botão de dose no sentido anti-horário.
- Segurar a caneta na posição vertical (agulha da caneta apontada para cima). Tocar levemente com seu dedo no suporte do refil para permitir que subam as potenciais bolhas de ar de dentro do refil.
Nota: As bolhas de ar não estão sempre presentes. No entanto, este passo deve ser realizado para verificar o fluxo de medicamento através da agulha antes de cada injeção9.
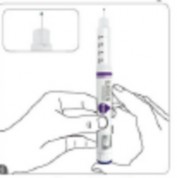
- Pressionar o botão de pressão por todo o caminho até que uma resistência dura seja sentida para liberar a dose. O número '0' é visível no visor de exibição e se alinha com o indicador de dose.
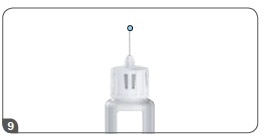
- Verificar se uma gotícula de líquido aparece na ponta da agulha inserida na caneta. Se não aparecerem gotas, repita as etapas 6-9 (teste funcional) até que uma gota107 apareça.
Importante: Caso nenhuma gota107 apareça depois de 5 tentativas, substitua a agulha da caneta (ver o passo 13) e repita o teste de funcionamento (ver as etapas de 6 -9).
4ª etapa: Seleção da dose
Você pode selecionar as dosagens de 1 em 1 unidade, sendo o mínimo 1 unidade e o máximo 60 unidades. Se você precisar de uma dosagem superior a 60, será necessário aplicar duas ou mais injeções.
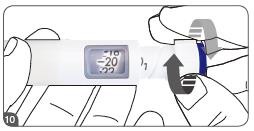
- Girar o botão de dose no sentido horário até que a dose prescrita se alinhe com o indicador de dose no visor. Se necessário, a dose pode ser corrigida girando o botão de dose no sentido anti-horário.
Importante: Certifique-se de não apertar o botão de pressão durante o ajuste da dose para evitar a perda do medicamento.
Notas:
- Uma dose maior do que a quantidade de medicamento que existe na caneta não pode ser marcada.
- Se a dose for maior do que o volume existente de medicamento no carpule (refil), uma nova caneta deve ser usada para a dose remanescente.
5ª etapa: Injetando a dose
Ler as etapas 11 e 12, antes de proceder com a injeção9.
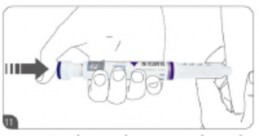
- Limpe a pele73 com um algodão embebido em álcool para limpar o local da injeção9. Deixe o local da injeção9 secar antes de injetar a sua dose.
- Segure a caneta de modo que o visor de exibição esteja visível durante a injeção9. Aplique a agulha da caneta na pele73 e pressione o botão de pressão em todo o caminho até que uma parada dura seja sentida e o número '0' fique visível no visor de exibição e se alinhe com o indicador de dose.
Nota: Utilize a técnica de injeção9 recomendada pelo seu médico ou profissional de saúde4.
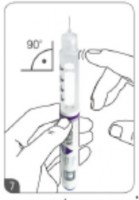
6ª etapa: Segurando o botão injetor após a injeção9
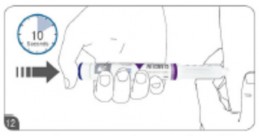
Assim que a dose completa tenha sido aplicada, mantenha o botão pressionado por mais 10 segundos. Em seguida, remova lentamente a caneta do local da injeção9 em um ângulo de 90°.
Nota: Manter o botão pressionado garante uma descarga completa da dose do medicamento.
Importante: Não inclinar a caneta durante a injeção9 e remoção da pele73 para evitar danos pela agulha da caneta.
7ª etapa: Remoção e descarte da agulha
Sempre remova a agulha após cada aplicação e guarde a caneta sem nenhuma agulha afixada. Isto ajuda a prevenir:
- Contaminação e/ou infecção67.
- Entrada de ar no reservatório da insulina6 e vazamento da insulina6, o que pode provocar imprecisão da dosagem.
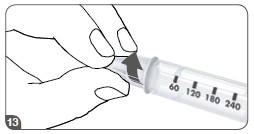
Substituir a tampa exterior da agulha com cuidado.
Desparafusar a agulha da caneta no sentido anti-horário e eliminar a agulha da caneta em segurança de acordo com os regulamentos locais ou orientação de seu médico.
Nota para profissionais de saúde4: Sempre aderir aos regulamentos específicos que se aplicam a você em relação à substituição da tampa da agulha (recapeamento) e eliminação.
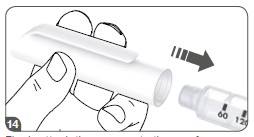
8ª etapa: Instalação da tampa da caneta
- Fixar firmemente a tampa da caneta na caneta para proteção entre as administrações.
Perguntas mais frequentes
1. É necessário realizar o teste funcional antes de cada injeção9?
- Sim. O teste funcional deve ser realizado para remover as bolhas de ar que se formam no carpule (refil) e para verificar o fluxo do medicamento através da agulha.
- Como em cada injeção9 uma nova agulha tem de ser usada, o teste funcional deve ser realizado antes de cada injeção9.
2. Como eu sei que a injeção9 está completa?
- O botão está pressionado com firmeza em todo o caminho até que ele pare.
- O número '0' é visível no centro do visor do mostrador (display).
- Você lentamente contou até 10, enquanto você ainda está segurando o botão de pressão e a caneta-agulha ainda está em sua pele73.
3. Por que eu tenho que contar até 10, mantendo o botão de pressão?
- Algumas gotas podem aparecer após o botão atingir a posição final.
- Segurando o botão por 10 segundos, a dose completa é injetada.
4. E se o botão de dose não puder ser conectado à dose necessária?
- O carpule (refil) da caneta pode não ter medicamento suficiente para aplicar a dose necessária.
- A caneta não permite uma dose maior ser pré-ajustada do que a que resta no carpule (refil).
- Injetar o medicamento residual e completar a dose com uma nova caneta, ou aplicar a dose completa com uma nova caneta.
Instruções para conservação
Se a sua caneta estive sob refrigeração, retire-a da refrigeração de 1 a 2 horas antes da injeção9 para que atinja a temperatura ambiente. A injeção9 de insulina6 fria é mais dolorosa. Mantenha sua caneta fora do alcance das crianças.
Conservar em local frio (temperatura entre 2° e 8°C) até o primeiro uso. Não congelar. Evitar contato direto do produto com o compartimento do congelador ou pacotes congelados.
Após a retirada da caneta do ambiente frio para uso ou para reserva, você poderá utilizá- la por 28 dias. Durante esse período, a caneta pode ser armazenada seguramente à temperatura ambiente (até 30°C) e não deve ser armazenada em geladeira. Não utilize a caneta após esse período.
Não utilize a caneta após a data de vencimento gravada no rótulo da caneta ou no cartucho.
Proteja a caneta da luz e do calor.
Descarte sua caneta como orientado pelas autoridades sanitárias em local apropriado.
Manutenção
Projeta sua caneta do pó e sujeira.
Você pode limpar a parte externa da sua caneta esfregando-a com um pano úmido. Não molhe, lave ou lubrifique a caneta, pois pode danificá-la.
A caneta foi desenvolvida para funcionar precisa e seguramente. Ela deve ser manuseada com cuidado. Evite situações em que a caneta possa ser danificada. Se estiver preocupado com a possibilidade da caneta estar danificada, descarte-a e use uma nova.
POSOLOGIA
Insulina glargina1 é uma nova insulina6 humana recombinante análoga, equipotente à insulina6 humana.
Devido ao perfil de redução de glicose24 sem pico com duração de ação prolongada de Glargilin®, a dose é administrada por via subcutânea62 uma vez ao dia. Pode ser administrada a qualquer hora do dia, entretanto, no mesmo horário todos os dias. Os níveis desejados de glicemia33, bem como as doses e intervalos das medicações antidiabéticas devem ser determinadas e ajustadas individualmente.
Os ajustes na dose podem também ser necessários, por exemplo, se houver alterações de peso, estilo de vida, planejamento da dose de insulina6 dos pacientes, ou outras circunstâncias que possam promover aumento na susceptibilidade83 à hipoglicemia16 ou hiperglicemia7 (vide “5. Advertências e Precauções”). Qualquer alteração de dose deve ser feita somente sob supervisão médica.
Em regimes de injeção9 basal em bolus22, geralmente 40-60% da dose diária é administrada como insulina glargina1 para cobrir os requerimentos de insulina6 basal. Num estudo clínico do produto Lantus® com pacientes diabéticos tipo 2, sob tratamento com antidiabético oral108, foi iniciada terapia com dose de 10 U de insulina glargina1, 1 vez ao dia, e subsequentemente o tratamento foi ajustado individualmente.
Glargilin® não é a insulina6 de escolha para o tratamento de cetoacidose diabética109. Insulina6 intravenosa de curta duração deve ser o tratamento preferido.
Quando ocorrer a alteração de um tratamento com insulina6 intermediária ou uma insulina6 de longa-duração para um tratamento com Glargilin®, pode ser necessário ajuste na quantidade e intervalo da insulina de curta duração110 ou da insulina6 análoga de ação rápida ou da dose de qualquer antidiabético oral108.
Para reduzir o risco de hipoglicemia16, quando os pacientes são transferidos de insulina glargina1 300 U/mL uma vez ao dia, para insulina glargina1 100U/mL uma vez ao dia, a dose inicial recomendada de insulina glargina1 100 U/mL é de 80% da dose de insulina glargina1 300 U/ml que será descontinuada.
Nos estudos clínicos realizados com o produto Lantus® quando os pacientes foram transferidos de insulina NPH23 uma vez ao dia ou insulina6 ultralenta para Lantus® (insulina glargina1) administrada uma vez ao dia, a dose inicial utilizada foi geralmente inalterada (por exemplo: quantidade de unidades, U, da Lantus® por dia foi igual às U de insulina NPH23). Para aqueles que foram transferidos de insulina NPH23 duas vezes ao dia para Lantus® uma vez ao dia, a dose inicial (U) foi geralmente reduzida em aproximadamente 20% (comparada com a dose total diária em U de insulina NPH23) e então ajustada com base na resposta do paciente, de forma a reduzir o risco de hipoglicemia16.
Um programa de monitorização metabólica cuidadosa, sob supervisão médica, é recomendado durante a transferência, e nas semanas iniciais subsequentes. Assim como com todas as insulinas análogas, isso é particularmente verdadeiro para pacientes66 que, devido aos anticorpos18 à insulina6 humana, necessitam de altas doses de insulina6 e podem apresentar uma resposta acentuadamente melhor com insulina glargina1.
Um controle metabólico melhor pode resultar em aumento da sensibilidade à insulina6 (necessidades reduzidas de insulina6) podendo ser necessário posterior ajuste das doses de Glargilin® e outras insulinas ou antidiabéticos orais12.
A monitorização da glicemia33 é recomendada para todos os pacientes com diabetes38.
Populações especiais
Crianças (acima de 2 anos): assim como nos pacientes adultos, a dose de Glargilin® em pacientes pediátricos deve ser individualizada pelo médico baseada nas necessidades metabólicas e na monitorização frequente dos níveis de glicose24. O perfil de segurança para pacientes66 ≤ 18 anos é semelhante ao perfil de segurança para pacientes66 maiores de 18 anos. Não há dados clínicos de segurança disponíveis em pacientes com idade abaixo de 2 anos de idade.
Uso em idosos: recomenda-se que as doses iniciais, os aumentos de dose e doses de manutenção sejam conservadoras para se evitar as reações hipoglicêmicas.
População com falência/comprometimento renal46: a dose de insulina6 do paciente com comprometimento renal46 pode precisar ser reduzida devido ao metabolismo55 reduzido da insulina6. A dose de insulina6 do paciente com falência renal46 pode precisar ser reduzida.
População com comprometimento hepático: a dose de insulina6 do paciente com comprometimento hepático pode precisar ser reduzida devido à baixa habilidade para gliconeogênese92 e metabolismo55 reduzido da insulina6.
Conduta necessária caso haja esquecimento de administração
Caso tenha sido esquecida a administração de uma dose de Glargilin® ou caso tenha sido administrada uma dose muito baixa de Glargilin®, o nível glicêmico pode se elevar demasiadamente. Checar o nível glicêmico frequentemente.
REAÇÕES ADVERSAS
Hipoglicemia16 (muito comum > 1/10): pode ocorrer hipoglicemia16 (em geral a reação adversa mais frequente da terapia com insulina6), caso a dose de insulina6 seja muito alta em relação às necessidades de insulina6 e/ou haja dieta e exercícios não-controlados em relação às necessidades de insulina6. Assim como com todas as insulinas, ataques hipoglicêmicos severos, especialmente se recorrentes, podem levar a distúrbios neurológicos. Episódios hipoglicêmicos severos ou prolongados podem ser de risco à vida. Em muitos pacientes, os sinais100 e sintomas81 de neuroglicopenia são precedidos por sinais100 de contra regulação adrenérgica. Geralmente, quanto mais rápido e maior o declínio na glicemia33, mais acentuados são os fenômenos de contra regulação e os sintomas81.
Reações do tecido65 cutâneo111 e subcutâneo2 (comum > 1/100 e ≤ 1/10): Assim como com todas as terapias com insulina6, pode ocorrer lipodistrofia68 no local da injeção9 e retardo da absorção da insulina6. Em estudos clínicos, em tratamentos que incluíam insulina glargina1, foi observada que a lipo-hipertrofia112 pode ocorrer em 1 a 2% dos pacientes, enquanto a lipoatrofia113 era incomum.
Amiloidose70 cutânea71 localizada ocorreu no local da injeção9 com insulinas. Hiperglicemia7 foi relatada com injeções repetidas de insulina6 em áreas de amiloidose70 cutânea71 localizada; hipoglicemia16 foi relatada com uma mudança repentina para um local de injeção9 não afetado.
A rotação contínua do local de injeção9 dentro de determinada área pode ajudar a reduzir ou evitar essas reações (vide “5. Advertências e Precauções”).
Local da injeção9 (comum > 1/100 e ≤ 1/10) e reações alérgicas (rara > 1/10.000 e ≤ 1.000): em estudos clínicos usando tratamentos que incluíam insulina glargina1, reações no local das injeções foram observadas em 3 a 4% dos pacientes. Assim como com qualquer terapia com insulina6, tais reações incluem rubor, dor, coceira, urticária114, inchaço115 e inflamação64. A maioria das pequenas reações geralmente é resolvida em poucos dias ou poucas semanas.
Reações alérgicas do tipo imediata são raras. Tais reações à insulina6 (incluindo insulina glargina1) ou aos excipientes podem, por exemplo, ser associadas com reações cutâneas116 generalizadas, angioedema117, broncoespasmo118, hipotensão119 e choque120, podendo ser de risco à vida.
Visão93 (rara > 1/10.000 e ≤ 1.000): uma alteração acentuada nos níveis glicêmicos pode causar distúrbios visuais temporários, devido à alteração temporária na turgidez e índice de refração das lentes. O controle glicêmico melhorado a longo prazo diminui o risco de progressão de retinopatia diabética36. Contudo, como com todos os tratamentos com insulina6, a terapia intensificada com insulina6 com melhora repentina nos níveis de glicemia33 pode estar associada com a piora temporária da retinopatia diabética36. Em pacientes com retinopatia proliferativa80, particularmente se não forem tratados com fotocoagulação, episódios hipoglicêmicos severos podem causar amaurose.
Outras reações (raras > 1/10.000 e ≤ 1.000 ou muito raras ≤ 0,01%): a administração de insulina6 pode causar a formação de anticorpos18. Em estudos clínicos, os anticorpos18 que têm reação cruzada com insulina6 humana e insulina glargina1 foram observados tanto nos grupos de tratamento com NPH quanto nos grupos com insulina glargina1, com incidências similares. Em casos raros (Pode acometer até 1 em 100 pessoas), a presença de tais anticorpos18 pode necessitar ajuste de dose da insulina6 para corrigir a tendência à hiperglicemia7 ou hipoglicemia16.
Raramente, a insulina6 pode causar retenção de sódio e edema101, particularmente após melhora significativa do controle metabólico em associação com a terapia intensificada por insulina6.
Foram relatados erros de medicação nos quais outras insulinas, particularmente insulinas de ação curta, foram administradas acidentalmente ao invés de insulina glargina1.
População pediátrica
Em geral, o perfil de segurança para pacientes≤ 18 anos é semelhante ao perfil de segurança para pacientes66 maiores de 18 anos.
As reações adversas reportadas no pós-comercialização do medicamento comparador (Lantus®) incluem relativamente com maior frequência em crianças e adolescentes (≤ 18 anos) que nos adultos: reações no local da injeção9 e reações na pele73 (rash121, urticária114).
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Sintomas81: a superdose com insulina6, relacionada com a ingestão de alimentos, consumo de energia ou ambos, pode levar a hipoglicemia16 severa e algumas vezes prolongada e apresentar risco de vida.
Checar a glicemia33 frequentemente.
Tratamento: episódios leves de hipoglicemia16 podem geralmente ser tratados com carboidratos por via oral Os ajustes da dose, padrões de alimentação, ou atividade física podem ser necessários.
Episódios mais severos culminando em coma122, convulsões ou danos neurológicos podem ser tratados com glucagon97 (intramuscular ou subcutâneo2) ou solução de glicose24 intravenosa concentrada. A ingestão sustentada de carboidrato86 e observação podem ser necessárias devido à possibilidade de recorrência123 de hipoglicemia16 após aparente recuperação clínica.
Em caso de intoxicação ligue para 0800-722-6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS: 1.3348.0001
Farmacêutico responsável: Herbert Silva Bathemarque CRF-MG: 20.253
Fabricado e embalado por:
Gan & Lee Pharmaceuticals Pequim, China.
Registrado e importado por:
BIOMM S/A
Avenida Regent, nº 705, Alphaville Lagoa dos Ingleses, Nova Lima – MG, Brasil. CEP: 34018-000
Ou
Fabricado por:
Gan & Lee Pharmaceuticals, Pequim, China.
Registrado, importado e embalado por:
BIOMM S/A
Avenida Regent, nº 705, Alphaville Lagoa dos Ingleses, Nova Lima – MG, Brasil. CEP: 34018-000
CNPJ : 04.752.991/0001-10
Indústria Brasileira
SAC 0800 057 2466