

Mercilon (Bula do profissional de saúde)
MERCK SHARP & DOHME FARMACEUTICA LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Mercilon®
desogestrel + etinilestradiol
Comprimidos 150 mcg + 20 mcg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Comprimidos
Embalagem com 21 ou 63 comprimidos
USO ORAL
USO ADULTO
COMPOSIÇÃO:
Cada comprimido de Mercilon® contém:
| desogestrel | 150 mcg |
| etinilestradiol | 20 mcg |
| excipiente q.s.p. | 1 comprimido |
Excipientes: amido, povidona, ácido esteárico, dióxido de silício, racealfatocoferol, estearato de magnésio e lactose1.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE2
INDICAÇÃO
Anticoncepção.
RESULTADOS DE EFICÁCIA
Em 1736 mulheres que receberam Mercilon® por até 48 ciclos, um total de 5 casos de gravidez3 ocorreu durante o tratamento.1 O índice de Pearl4 total foi de 0,22, considerando uma taxa de falha do método de 0,04 e uma taxa de falha por paciente de 0,18.
Referência bibliográfica:
- Scientific Development Group Release Report 2727. Dieben TOM, Voerman JWA. Evaluation of a new oral contraceptive combination containing 0.150 mg Org 2969 plus 0.020 mg ethinyloestradiol.
CARACTERÍSTICAS FARMACOLÓGICAS
Propriedades farmacodinâmicas
Classificação ATC G03A A09.
O efeito anticonceptivo dos anticoncepcionais hormonais combinados orais (AHCOs) é baseado na interação de vários fatores, sendo que os mais importantes são observados sobre a inibição da ovulação5 e as alterações do muco cervical. Assim como a proteção contra a gravidez3, os AHCOs apresentam várias propriedades positivas que, juntamente com as propriedades negativas (veja itens “5. ADVERTÊNCIAS E PRECAUÇÕES” e “9. REAÇÕES ADVERSAS”), podem ser úteis para decidir sobre o método de planejamento reprodutivo. O ciclo é mais regular, a menstruação6 é frequentemente menos dolorosa e o sangramento menos intenso. Este último pode resultar na redução da ocorrência de deficiência de ferro. Além disso, com os AHCOs de doses mais elevadas (50 mcg de etinilestradiol), há evidência de redução de risco de tumores fibrocísticos das mamas7, cistos ovarianos, doença inflamatória pélvica8, gravidez ectópica9 e câncer10 de endométrio11 e de ovário12. Ainda não foi confirmado se isso se aplica aos AHCOs de baixa dose.
Propriedades farmacocinéticas
– desogestrel
Absorção: o desogestrel administrado por via oral é rápida e completamente absorvido e convertido em etonogestrel. Concentrações plasmáticas máximas são atingidas em cerca de 1,5 hora. A biodisponibilidade é de 62% a 81%.
Distribuição: o etonogestrel se liga à albumina13 plasmática e à globulina14 transportadora de hormônio15 sexual (SHBG). Apenas 2% a 4% das concentrações plasmáticas totais do fármaco16 estão presentes como esteroide livre e 40% a 70% são ligados especificamente à SHBG. O aumento de SHBG induzido pelo etinilestradiol influencia a distribuição nas proteínas17 séricas, causando um aumento da fração ligada à SHBG e uma diminuição da fração ligada à albumina13. O volume de distribuição aparente do desogestrel é de 1,5 L/kg.
Metabolismo18: o etonogestrel é completamente metabolizado pelas vias conhecidas do metabolismo18 de esteroides. A taxa de depuração metabólica do plasma19 é de cerca de 2 mL/min/kg. Não foi encontrada qualquer interação com o etinilestradiol administrado concomitantemente.
Eliminação: as concentrações séricas do etonogestrel diminuem em duas fases. A fase final de eliminação é caracterizada por uma meia-vida de aproximadamente 30 horas. O desogestrel e seus metabólitos20 são excretados na proporção urinária/biliar de cerca de 6:4.
Condições no estado de equilíbrio: a farmacocinética do etonogestrel é influenciada pelas concentrações de SHBG, que são aumentadas em três vezes pelo etinilestradiol. Após a ingestão diária, as concentrações séricas do fármaco16 aumentam em cerca de duas a três vezes, atingindo as condições de estado de equilíbrio durante a segunda metade do ciclo de tratamento.
– etinilestradiol
Absorção: o etinilestradiol administrado por via oral é rápida e completamente absorvido. Concentrações plasmáticas máximas são atingidas dentro de 1 a 2 horas. A biodisponibilidade absoluta resultante da conjugação pré-sistêmica e do metabolismo18 de primeira passagem é de aproximadamente 60%.
Distribuição: o etinilestradiol é altamente, mas não especificamente, ligado à albumina13 sérica (aproximadamente 98,5%) e induz um aumento nas concentrações plasmáticas de SHBG. Foi determinado um volume de distribuição aparente de cerca de 5 L/kg.
Metabolismo18: o etinilestradiol é submetido à conjugação pré-sistêmica tanto na mucosa21 do intestino delgado22 quanto no fígado23. O etinilestradiol é principalmente metabolizado pela hidroxilação aromática, mas é formada uma ampla variedade de metabólitos20 hidroxilados e metilados, e estes estão presentes como metabólitos20 livres e conjugados com glucoronídeos e sulfato. O índice de depuração metabólica é de cerca de 5 mL/min/kg.
Eliminação: as concentrações séricas de etinilestradiol diminuem em duas fases de eliminação, sendo que a fase final é caracterizada por uma meia-vida de aproximadamente 24 horas. O fármaco16 inalterado não é excretado; os metabólitos20 do etinilestradiol são excretados na proporção urinária/biliar de 4:6. A meia-vida de excreção de metabólitos20 é de cerca de 1 dia.
Condições no estado de equilíbrio: as concentrações no estado de equilíbrio são atingidas após 3 a 4 dias quando as concentrações séricas do fármaco16 são maiores que 30% a 40% em comparação com a dose única.
Dados de segurança pré-clínicos
Os dados pré-clínicos não revelaram risco especial para humanos quando os AHCOs são utilizados conforme recomendado. Isso se baseia nos estudos convencionais de toxicidade24 de doses repetidas, genotoxicidade, potencial carcinogênico e toxicidade24 reprodutiva. Entretanto, deve-se considerar que os esteroides sexuais podem proporcionar o crescimento de determinados tecidos e tumores dependentes de hormônios.
CONTRAINDICAÇÕES
Os AHCs não devem ser utilizados na presença de quaisquer das condições relacionadas a seguir. Se alguma dessas condições aparecer pela primeira vez durante o uso do AHC, o produto deve ser descontinuado imediatamente.
Este medicamento é contraindicado para uso por mulheres nas seguintes condições:
- Presença ou antecedentes de trombose25 venosa (trombose venosa profunda26, embolia27 pulmonar).
- Presença ou antecedentes de trombose25 arterial (infarto do miocárdio28, acidente vascular cerebral29) ou condições prodrômicas (por exemplo: crise isquêmica transitória, angina30 pectoris).
- Predisposição conhecida para tromboses31 venosas ou arteriais, tais como resistência à proteína C ativada (PCA), deficiência de antitrombina-III, deficiência de proteína C, deficiência de proteína S, hiperomocisteinemia e anticorpos32 antifosfolípides.
- Antecedentes de enxaqueca33 com sintomas34 neurológicos focais (veja item “5. ADVERTÊNCIAS E PRECAUÇÕES”).
- Diabetes melito35 com envolvimento vascular36.
- A presença de fator(es) de risco grave(s) ou múltiplo(s) para trombose25 venosa ou arterial também pode constituir uma contraindicação (veja item “5. ADVERTÊNCIAS E PRECAUÇÕES”).
- Cirurgia de grande porte com imobilização prolongada (ver item “5. ADVERTÊNCIAS E PRECAUÇÕES”).
- Pancreatite37 ou antecedentes de pancreatite37, se associada com hipertrigliceridemia grave.
- Presença ou antecedentes de distúrbios hepáticos graves, enquanto os resultados dos testes de função hepática38 não retornarem ao normal.
- Presença ou antecedentes de tumores hepáticos (benignos ou malignos).
- Conhecidos ou suspeitos tumores dependentes de esteroides sexuais (por exemplo: dos órgãos genitais ou das mamas7).
- Sangramento vaginal sem diagnóstico39.
- Hipersensibilidade a quaisquer das substâncias ativas de Mercilon® ou a quaisquer dos excipientes.
Mercilon® é contraindicado para uso com o regime combinado dos medicamentos para o vírus40 da hepatite41 C ombitasvir/paritaprevir/ritonavir, com ou sem dasabuvir (veja item “5. ADVERTÊNCIAS E PRECAUÇÕES”).
Gravidez3 e Lactação42
Este medicamento é contraindicado para uso durante a gravidez3 ou suspeita de gravidez3.
Mercilon® não é indicado durante a gravidez3. Se ocorrer gravidez3 durante o tratamento com Mercilon®, a administração dos comprimidos deve ser interrompida. A maioria dos estudos epidemiológicos mostrou que não há aumento do risco de malformações43 nas crianças nascidas de mães que usaram AHCOs antes da gestação, nem efeitos teratogênicos44 quando o AHCO foi administrado inadvertidamente durante o início da gestação.
ADVERTÊNCIAS E PRECAUÇÕES
Se alguma das condições/fatores de risco relacionados a seguir estiver presente, os benefícios do uso do AHC devem ser avaliados contra os possíveis riscos para cada mulher individualmente e discutidos com a paciente antes dela decidir iniciar o uso do medicamento. Em caso de piora, exacerbação ou primeira ocorrência de alguma dessas condições ou fatores de risco, a mulher deve contatar o seu médico. O médico, então, deve decidir se o uso do AHC deve ser descontinuado.
Neste item da bula, o termo anticoncepcional hormonal combinado (AHC) é empregado quando existem dados para anticoncepcionais orais e não orais. O termo anticoncepcional hormonal combinado oral (AHCO) é empregado quando existem dados apenas para anticoncepcionais orais.
Distúrbios circulatórios
- Estudos epidemiológicos demonstram associação entre o uso de AHCs e aumento do risco de doenças tromboembólicas e trombóticas45 venosas ou arteriais, tais como infarto do miocárdio28, acidente vascular cerebral29, trombose venosa profunda26 e embolia27 pulmonar. Esses eventos ocorrem raramente.
- O uso de qualquer AHC é associado com um aumento do risco de tromboembolia venosa (TEV) manifestada por trombose venosa profunda26 e/ou embolia27 pulmonar. O risco é maior durante o primeiro ano em que a mulher inicia o uso de um AHC. O risco é também aumentado após o início do uso de AHC ou reinício de uso, do mesmo ou de diferente AHC, após uma interrupção de quatro semanas ou mais.
- Alguns estudos epidemiológicos sugeriram que as mulheres que utilizaram AHCOs de baixa dose com progestagênios de terceira geração, incluindo o desogestrel, apresentaram aumento do risco de tromboembolia venosa quando comparadas com aquelas que utilizaram AHCOs de baixa dose com o progestagênio levonorgestrel. Esses estudos indicaram aumento no risco de aproximadamente duas vezes, o que poderia corresponder a 1 ou 2 casos adicionais de tromboembolia venosa por 10.000 mulheres-ano de uso. Entretanto, os dados de outros estudos não mostraram esse aumento de duas vezes no risco.
- De modo geral, considera-se que a incidência46 de tromboembolia venosa em usuárias de AHCs de baixas doses de estrogênios (< 0,05 mg de etinilestradiol) é de 3 a 12 casos por 10.000 mulheres-ano em comparação com 1 a 5 casos por 10.000 mulheres-ano em não usuárias. A incidência46 de tromboembolia venosa que ocorre durante o uso de AHC é menor do que a incidência46 associada com a gestação (isto é, 5 a 20 casos por 10.000 mulheres-ano). A tromboembolia venosa é fatal em 1-2% dos casos.
- A figura a seguir mostra o risco de desenvolvimento de tromboembolia venosa para mulheres não grávidas e que não usam AHCs, para mulheres que usam AHCs, para mulheres grávidas e para mulheres em período pós-parto. Para colocar em perspectiva o risco de desenvolvimento de tromboembolia venosa: se 10.000 mulheres que não estão grávidas e não usam AHCs são acompanhadas por um ano, entre 1 e 5 delas irão desenvolver tromboembolia venosa.
- Probabilidade de desenvolvimento de tromboembolia venosa:
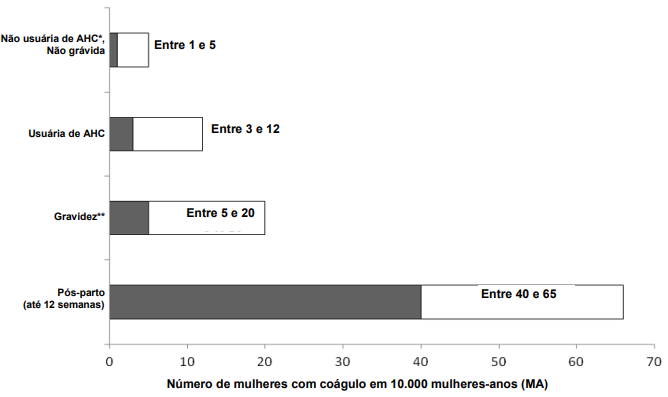
*AHC = anticoncepcional hormonal combinado
**Dados de gravidez3 baseados na duração real da gravidez3 em estudos de referência. Com base na suposição modelo que a gravidez3 tenha duração de nove meses, a taxa é de 7 a 27 por 10.000 mulheres-anos. - Há relatos extremamente raros da ocorrência de trombose25 em outros vasos sanguíneos47 em usuárias de AHCs, como veias48 e artérias49 hepáticas50, mesentéricas51, renais, cerebrais ou retinianas.
- Os sintomas34 de eventos trombóticos52/tromboembólicos venosos ou arteriais ou de acidente vascular cerebral29 podem incluir: dor e/ou edema53 unilateral na perna; dor torácica intensa súbita, irradiada ou não para o braço esquerdo; dispneia54 súbita; súbito início de tosse; cefaleia55 atípica, intensa e prolongada; perda de visão56 súbita parcial ou completa; diplopia57; dificuldade de fala ou afasia58; vertigem59; colapso60 com ou sem convulsão61 focal; fraqueza ou insensibilidade muito acentuada afetando subitamente um dos lados ou uma parte do corpo; distúrbios motores; abdome62 “agudo”.
- O risco de tromboembolia venosa aumenta com: aumento da idade; antecedentes familiares positivos (isto é, tromboembolia venosa em irmãos ou pais em idade relativamente precoce). Se houver suspeita de predisposição hereditária, a mulher deve ser encaminhada a um especialista para aconselhamento antes de decidir sobre o uso de qualquer anticoncepcional hormonal; obesidade63 (índice de massa corporal64 acima de 30 kg/m2); imobilização prolongada, cirurgia de grande porte, qualquer cirurgia nas pernas ou grande trauma. Nessas situações, é recomendável descontinuar o uso do AHCO (no caso de cirurgia eletiva65, com pelo menos com 4 semanas de antecedência) e não reiniciar o uso antes de duas semanas após completa remobilização. Ver também item “4. CONTRAINDICAÇÕES”; e possivelmente também com tromboflebite66 superficial e veias48 varicosas. Não há consenso sobre o possível papel dessas condições na etiologia67 da tromboembolia venosa.
- O risco de complicações tromboembólicas arteriais aumenta com: aumento da idade; tabagismo (com tabagismo intenso e aumento da idade, o risco também aumenta, especialmente em mulheres acima dos 35 anos de idade); antecedentes familiares positivos (isto é, trombose25 arterial em irmãos ou pais em idade relativamente precoce). Se houver suspeita de predisposição hereditária, a mulher deve ser encaminhada a um especialista para aconselhamento antes de decidir sobre o uso de qualquer anticoncepcional hormonal; obesidade63 (índice de massa corporal64 acima de 30 kg/m2); dislipoproteinemia; hipertensão68; enxaqueca33; doença cardíaca valvular; fibrilação atrial.
- O aumento do risco de tromboembolia no puerpério69 deve ser considerado (veja itens “4. CONTRAINDICAÇÕES - Gravidez” e “5. ADVERTÊNCIAS E PRECAUÇÕES - Lactação”).
- Outras condições médicas associadas com eventos adversos circulatórios incluem diabetes melito35, lúpus70 eritematoso71 sistêmico72, síndrome73 hemolítica urêmica, doença intestinal inflamatória crônica (colite74 ulcerativa ou doença de Crohn75) e anemia falciforme76.
- Um aumento na intensidade ou frequência de enxaqueca33 durante o uso de AHCO (que pode ser prodrômico77 de um evento vascular36 cerebral) pode ser uma razão para interrupção imediata do AHCO.
- Fatores bioquímicos que podem ser indicativos de predisposição hereditária ou adquirida para trombose25 venosa ou arterial incluem resistência à proteína C ativada (APC), hiperhomocisteinemia, deficiência de antitrombina-III, deficiência de proteína C, deficiência de proteína S, anticorpos32 antifosfolípides (anticorpos32 anticardiolipina, anticoagulante78 lúpico).
- Ao considerar a relação risco/benefício, o médico deve levar em conta que o tratamento adequado de uma condição pode diminuir o risco associado de trombose25.
Tumores
- O fator de risco79 mais importante para câncer10 de colo80 de útero81 é a infecção82 persistente pelo papilomavírus humano (HPV). Estudos epidemiológicos indicaram que o uso prolongado de AHCOs contribui para o aumento de risco, mas há incertezas sobre em que extensão esse achado é atribuível a outros fatores, assim como exames mais frequentes do colo do útero83, diferenças no comportamento sexual incluindo o uso de métodos anticoncepcionais de barreira, ou a uma associação causal.
- A meta-análise de 54 estudos epidemiológicos relatou que há aumento discreto do risco relativo (RR = 1,24) de ocorrer câncer10 de mama84 diagnosticado em mulheres usuárias de AHCOs. O aumento do risco desaparece gradativamente durante o curso de 10 anos após a descontinuação do uso do AHCO. Uma vez que o câncer10 de mama84 é raro em mulheres abaixo de 40 anos de idade, o número de cânceres de mama84 diagnosticados em usuárias atuais e recentes de AHCO é pequeno em relação ao risco global de câncer10 de mama84. O câncer10 de mama84 diagnosticado em mulheres que usaram AHCOs tende a ser clinicamente menos avançado do que o câncer10 diagnosticado em mulheres que nunca os usaram.
- Em outro estudo epidemiológico com 1,8 milhões de mulheres dinamarquesas acompanhadas por 10,9 anos em média, o RR relatado de câncer10 de mama84 em usuárias de AHCO aumentou com o uso de longa duração quando comparado com mulheres que nunca usaram AHCOs (RR geral = 1,19; RR variou de 1,17 a 1 para uso por menos de 5 anos e para 1,46 após o uso por mais de 10 anos). A diferença relatada de risco absoluto (número de casos de câncer10 de mama84 comparados entre não-usuárias e usuárias atuais e recentes de AHCOs) foi pequena: 13 para 100.000 mulheres/ano.
- Estudos epidemiológicos não proporcionam evidência de causalidade. O aumento de risco observado pode ser devido ao diagnóstico39 mais precoce do câncer10 de mama84 em usuárias de AHCO, aos efeitos biológicos dos AHCOs ou à combinação de ambos.
- Foram relatados, raramente, em usuárias de AHCOs, tumores hepáticos benignos, e ainda mais raramente, tumores hepáticos malignos. Em casos isolados, esses tumores causaram hemorragia85 intra-abdominal potencialmente fatal. Portanto, quando ocorrer dor abdominal superior intensa, hepatomegalia86 ou sinais87 de hemorragia85 intra-abdominal em mulheres usando AHCOs a presença de tumor88 hepático deve ser considerada no diagnóstico39 diferencial.
Hepatite41 C
- Durante os ensaios clínicos89 com alguns regimes de combinação de HCV, foram observadas elevações da ALT em mulheres usando medicamentos contendo etinilestradiol (ver item “6. INTERAÇÕES MEDICAMENTOSAS”). Por exemplo, o regime combinado dos medicamentos para o vírus40 da hepatite41 C ombitasvir/paritaprevir/ritonavir, com ou sem dasabuvir, elevações da ALT para valores acima de 5 vezes o limite superior da normalidade foram significativamente mais frequentes em mulheres em uso de medicamentos que contêm etinilestradiol, como os AHCOs. Mercilon® deve ser descontinuado ao se iniciar terapia com o regime combinado dos medicamentos ombitasvir/paritaprevir/ritonavir, com ou sem dasabuvir (veja itens “4. CONTRAINDICAÇÕES” e “6. INTERAÇÕES MEDICAMENTOSAS”). Mercilon® pode ser reiniciado aproximadamente 2 semanas após o término do tratamento deste regime combinado de medicamentos.
Outras condições
- Mulheres portadoras ou com antecedentes familiares de hipertrigliceridemia podem apresentar aumento do risco de pancreatite37 ao usarem AHCOs.
- Os estrogênios exógenos podem induzir ou exacerbar os sintomas34 de angioedema90 hereditário e adquirido.
- Embora pequenos aumentos da pressão sanguínea tenham sido relatados em muitas mulheres usando AHCOs, aumentos clinicamente relevantes são raros. Não foi estabelecida a relação entre o uso do AHCO e a hipertensão68 clínica. Entretanto, se hipertensão68 sustentada clinicamente significativa se desenvolver durante o uso de AHCO, é prudente o médico suspender o AHCO e tratar a hipertensão68. Se for considerado apropriado, o uso do AHCO pode ser reintroduzido quando forem obtidos valores normais de pressão com o tratamento anti-hipertensivo.
- A ocorrência ou deterioração das seguintes condições foi relatada tanto durante a gestação quanto no uso de AHCO, mas a evidência de associação com o uso de AHCO não é conclusiva: icterícia91 e/ou prurido92 relacionado com colestase93; formação de cálculos biliares; porfiria94; lúpus70 eritematoso71 sistêmico72; síndrome73 hemolítica urêmica; coreia de Sydenham95; herpes gestacional; perda de audição relacionada à otosclerose96.
- Distúrbios agudos ou crônicos da função hepática38 podem necessitar da descontinuação do uso do AHCO até que os exames da função hepática38 retornem ao normal. A recorrência97 de icterícia91 colestática que ocorreu pela primeira vez durante a gestação ou ao uso prévio de esteroides sexuais obriga a descontinuar o uso dos AHCOs.
- Embora os AHCOs possam apresentar efeitos sobre a resistência periférica98 à insulina99 e tolerância à glicose100, não há evidências da necessidade de alterar o esquema terapêutico em mulheres com diabetes101 usando AHCOs de baixas doses (contendo < 0,05 mg de etinilestradiol). Entretanto, as mulheres com diabetes101 devem ser cuidadosamente monitoradas durante o tratamento com AHCOs.
- Doença de Crohn75 e colite74 ulcerativa foram associadas ao uso de AHCO.
- Ocasionalmente pode ocorrer cloasma102, especialmente em mulheres com antecedentes de cloasma102 gravídico. As mulheres com tendência a apresentar cloasma102 devem evitar a exposição ao sol ou à radiação ultravioleta enquanto estiverem utilizando AHCOs.
- Mercilon® contém < 80 mg de lactose1 por comprimido. Pacientes com o raro problema hereditário de intolerância à galactose103, a deficiência de lactase de Lapp ou má absorção de glicose100-galactose103 que estiverem sendo submetidas à dieta sem lactose1 devem levar essa quantidade em consideração.
Ao aconselhar na escolha de método(s) anticonceptivo(s), todas as informações acima devem ser levadas em consideração.
Exames e consultas médicas
Antes de iniciar ou reinstituir o uso de Mercilon®, deve-se fazer anamnese104 completa (incluindo antecedentes familiares) e deve- se excluir a presença de gestação. A pressão arterial105 deve ser aferida e, se clinicamente indicado, deve ser feito exame físico voltado para as contraindicações (veja item “4. CONTRAINDICAÇÕES”) e advertências (veja item “5. ADVERTÊNCIAS E PRECAUÇÕES”) mencionadas nesta bula. As mulheres também devem ser orientadas a ler cuidadosamente a bula com as informações para as pacientes em uso de Mercilon® e respeitar suas recomendações. A frequência e natureza das avaliações periódicas adicionais devem se basear em normas práticas estabelecidas e adaptadas individualmente. As mulheres devem ser advertidas de que os anticoncepcionais orais não protegem contra infecções106 pelo HIV107 (AIDS) e outras doenças sexualmente transmissíveis.
Eficácia reduzida
A eficácia de Mercilon® pode ser reduzida quando, por exemplo, houver esquecimento da administração de comprimidos (veja item “8. POSOLOGIA E MODO DE USAR - Conduta se a mulher esquecer-se de tomar o comprimido”); ocorrerem distúrbios gastrintestinais (veja item “8. POSOLOGIA E MODO DE USAR - Conduta em caso de distúrbios gastrintestinais”) ou administração concomitante com outros medicamentos que diminuam a concentração plasmática de etonogestrel, o metabólito108 ativo do desogestrel (veja item “6. INTERAÇÕES MEDICAMENTOSAS”).
Redução do controle do ciclo
Com todos os AHCOs, pode ocorrer sangramento irregular (spotting ou sangramento inesperado), especialmente durante os primeiros meses de uso. Portanto, a avaliação de qualquer sangramento irregular é apenas importante após um intervalo de adaptação de cerca de três ciclos.
Se a irregularidade dos sangramentos persistir ou ocorrer após ciclos previamente regulares, então, devem ser consideradas causas não hormonais e medidas diagnósticas adequadas devem ser adotadas para excluir malignidade ou gestação. Essas medidas podem incluir a curetagem109.
Em algumas mulheres, o sangramento de privação pode não ocorrer durante o intervalo sem tratamento. Se o AHCO foi usado de acordo com as instruções recomendadas (veja item “8. POSOLOGIA E MODO DE USAR”), é improvável que a mulher esteja grávida. Entretanto, se o AHCO não foi usado adequadamente antes da primeira ausência de sangramento de privação ou se ocorrerem duas ausências de sangramento de privação seguidas, a presença de gestação deve ser descartada antes de continuar o uso do AHCO.
Lactação42
A lactação42 pode ser influenciada pelos AHCOs, uma vez que eles podem reduzir a quantidade e alterar a composição do leite materno. Portanto, o uso dos AHCOs geralmente não deve ser recomendado até que a lactante110 tenha completado o desmame. Pequenas quantidades de esteroides anticoncepcionais e/ou seus metabólitos20 podem ser excretadas pelo leite, mas não há evidência de que isso afete adversamente a saúde2 do lactente111.
Populações especiais
Pacientes idosas: Mercilon® é um medicamento de uso exclusivo em pacientes em idade reprodutiva. Não se destina a uso em pacientes com idade ≥ 60 anos.
Efeitos sobre a habilidade de dirigir e operar máquinas
Não foram observados efeitos sobre a habilidade de dirigir e operar máquinas.
INTERAÇÕES MEDICAMENTOSAS
Nota: As bulas dos medicamentos de uso concomitante devem ser consultadas para identificação de interações potenciais.
Poderá ocorrer sangramento inesperado e/ou falha anticonceptiva quando os anticoncepcionais orais forem administrados concomitantemente com outros medicamentos. As seguintes interações foram relatadas na literatura:
Metabolismo18 hepático: podem ocorrer interações com medicamentos ou produtos à base de ervas medicinais que induzem as enzimas microssomais, principalmente as enzimas do citocromo P450 (CYP), o que pode resultar em aumento da depuração e redução da concentração plasmática dos hormônios sexuais podendo causar diminuição da eficácia dos anticoncepcionais orais combinados, incluindo Mercilon®. Esses produtos incluem fenitoína, fenobarbital, primidona, bosentana, carbamazepina, rifampicina e, possivelmente, também, a oxcarbazepina, topiramato, felbamato, griseofulvina, alguns inibidores da protease112 do vírus40 HIV107 (por ex., ritonavir) e inibidores não nucleosídeos da transcriptase reversa (por ex., efavirenz) e produtos contendo a erva medicinal erva de São João ou St. John's wort.
A indução enzimática pode ocorrer após alguns dias de tratamento. A indução enzimática máxima é observada geralmente em algumas semanas. Após a descontinuação da terapia, a indução enzimática pode durar por cerca de 28 dias. Quando coadministrados com anticoncepcionais hormonais, muitas combinações de inibidores de protease do vírus40 HIV107 (por ex., nelfinavir) e inibidores não nucleosídeos da transcriptase reversa (por ex., nevirapina), e/ou combinações com medicamentos utilizados para o tratamento da hepatite41 C (por ex., boceprevir, telaprevir), podem aumentar ou diminuir a concentração plasmática de progestagênios, incluindo o etonogestrel, o metabólito108 ativo do desogestrel, ou estrogênios. O efeito líquido dessas alterações pode ser clinicamente relevante em alguns casos.
Mulheres tratadas com algum dos medicamentos ou produtos à base de ervas medicinais citados acima deverão ser informadas de que pode ocorrer redução de eficácia de Mercilon®. Deve ser usado algum método de barreira combinado com Mercilon® durante a administração de medicamentos indutores das enzimas hepáticas113 e por 28 dias após a descontinuação. Se a administração concomitante continuar após o término dos comprimidos do blíster, o próximo blíster deverá ser iniciado imediatamente a seguir, sem o intervalo usual sem comprimidos. Para mulheres em terapia prolongada com fármacos indutores de enzimas microssomais, deve ser considerada a escolha de um método anticonceptivo alternativo, o qual não seja afetado por esses fármacos.
A administração concomitante de inibidores fortes (por ex., cetoconazol, itraconazol, claritromicina) ou moderados (por ex., fluconazol, diltiazem, eritromicina) de CYP3A4 pode aumentar a concentração sérica de estrogênios e progestagênios, incluindo o etonogestrel, o metabólito108 ativo do desogestrel.
Os anticoncepcionais orais podem afetar o metabolismo18 de outros fármacos. Da mesma forma, as concentrações plasmáticas e tissulares podem tanto aumentar (por exemplo: ciclosporina) quanto diminuir (por exemplo: lamotrigina).
Durante os ensaios clínicos89 com o regime combinado dos medicamentos para o vírus40 da hepatite41 C ombitasvir/paritaprevir/ritonavir, com ou sem dasabuvir, elevações da ALT para valores acima de 5 vezes o limite superior da normalidade foram significativamente mais frequentes em mulheres em uso de medicamentos que contêm etinilestradiol, como os AHCOs. Mercilon® deve ser descontinuado ao se iniciar terapia com o regime combinado dos medicamentos ombitasvir/paritaprevir/ritonavir, com ou sem dasabuvir (veja itens “4. CONTRAINDICAÇÕES” e “5. ADVERTÊNCIAS E PRECAUÇÕES”). Mercilon® pode ser reiniciado aproximadamente 2 semanas após o término do tratamento deste regime combinado de medicamentos.
O uso concomitante com alguns outros medicamentos antivirais para o HCV, como os que contêm glecaprevir/pibrentasvir, pode aumentar o risco de elevações da ALT (ver item “5. ADVERTÊNCIAS E PRECAUÇÕES - Hepatite41 C”).
Exames laboratoriais
O uso de esteroides anticoncepcionais pode influenciar os resultados de determinados exames laboratoriais, incluindo parâmetros bioquímicos da função hepática38, tireoidiana, adrenal e renal114, concentrações plasmáticas de proteínas17 (carreadoras), como por exemplo, a globulina14 ligadora de corticosteroides e de frações de lípides/lipoproteínas, parâmetros do metabolismo18 de carboidratos e da coagulação115 e fibrinólise116. As alterações geralmente permanecem dentro dos limites da normalidade.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar em temperatura ambiente (entre 15 e 30°C). Proteger da luz e umidade. O prazo de validade do medicamento é de 36 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Os comprimidos de Mercilon® são brancos, biconvexos, redondos e possuem 6 mm de diâmetro. Cada comprimido possui de um lado a marca TR/4 e do outro a marca Organon.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Como tomar Mercilon®
Os comprimidos devem ser tomados na ordem orientada na cartela, com um pouco de líquido, conforme necessário. Um comprimido é tomado diariamente no mesmo horário, sem interrupção durante 21 dias, seguindo-se de uma pausa de 7 dias. Cada cartela subsequente é iniciada após o término dessa pausa de 7 dias sem comprimidos, durante a qual normalmente ocorre o sangramento de privação. Este, em geral, inicia-se no 2º ou 3º dia após a ingestão do último comprimido e pode não terminar antes do início da cartela seguinte.
Como iniciar o uso de Mercilon®
Sem ter utilizado qualquer anticoncepcional hormonal (no último mês): A administração do comprimido precisa iniciar no 1º dia do ciclo menstrual natural da mulher (isto é, no primeiro dia da menstruação6). Também é permitido iniciar entre o 2º e o 5º dia, e, neste caso, recomenda-se utilizar também um método de barreira nos primeiros 7 dias de tratamento.
Troca de um anticoncepcional hormonal combinado [anticoncepcional hormonal combinado oral (AHCO), anel vaginal ou adesivo transdérmico]: A mulher deve iniciar Mercilon® preferivelmente no dia seguinte ao da administração do último comprimido ativo (o último comprimido contendo substâncias ativas) do AHCO utilizado anteriormente, e no mais tardar, no dia seguinte ao do intervalo habitual sem tratamento ou do comprimido placebo117 do seu tratamento prévio com AHCO. No caso do anel vaginal ou do adesivo transdérmico, a mulher deve iniciar o uso de Mercilon® preferivelmente no dia da retirada do anel ou do adesivo, mas no mais tardar no dia em que a próxima inserção/aplicação seria realizada.
Se a mulher estiver utilizando o método anterior consistentemente e corretamente e se houver certeza de que não está grávida, ela também pode substituir seu método anticoncepcional combinado hormonal anterior em qualquer dia do ciclo.
O intervalo sem tratamento hormonal do método anterior nunca deve ser estendido além do tempo recomendado.
Troca de um medicamento à base de progestagênio isolado (minipílula, injeção118, implante119) ou sistema intrauterino liberador de progestagênio (SIU): A troca da minipílula por Mercilon® pode ser feita em qualquer dia. No caso de implante119 ou SIU, a troca deve ser feita no dia da retirada dos mesmos e, no caso de medicamento injetável, no dia em que seria administrada a próxima injeção118. Nesses casos, a mulher também deve ser advertida de que é necessária a utilização de um método anticoncepcional de barreira durante os primeiros 7 dias de tratamento com Mercilon®.
Após aborto no primeiro trimestre de gestação: Pode-se iniciar imediatamente. Nesse caso, não há necessidade da utilização de um método anticoncepcional adicional.
Após o parto ou pós-aborto no segundo trimestre de gestação: Para lactantes120, veja item “5. ADVERTÊNCIAS E PRECAUÇÕES - Lactação”.
As mulheres devem ser orientadas a iniciar Mercilon® nos dias 21 a 28 após o parto ou aborto no segundo trimestre de gestação. Quando iniciar depois desse período, a mulher também deve ser orientada a utilizar durante os primeiros 7 dias de tratamento, um método de barreira adicional. No entanto, se a mulher já teve alguma relação sexual antes de iniciar o tratamento, deve-se descartar a possibilidade de gravidez3 antes de iniciar o uso do AHCO, ou então, deve-se esperar que ocorra a primeira menstruação6 para iniciar o tratamento anticoncepcional.
O aumento de risco de tromboembolia venosa durante o período de pós-parto deve ser considerado ao reiniciar Mercilon® (ver item “5. ADVERTÊNCIAS E PRECAUÇÕES”).
Conduta se a mulher esquecer de tomar o comprimido
Se a mulher estiver menos de 12 horas atrasada para tomar qualquer comprimido, a proteção anticoncepcional não é reduzida. A mulher deve tomar o comprimido assim que lembrar e o próximo deve ser tomado no horário habitual. Caso a mulher esteja atrasada mais de 12 horas para tomar qualquer comprimido, a proteção anticoncepcional pode estar reduzida. A conduta em caso de esquecimento pode ser orientada pelas seguintes duas normas básicas:
- A administração dos comprimidos nunca deve ser descontinuada por mais de 7 dias.
- Os 7 dias de administração ininterrupta são requeridos para atingir supressão adequada do eixo hipotalâmico-hipofisário- ovariano.
As seguintes recomendações podem ser fornecidas na prática diária:
Primeira semana: a mulher deve tomar o comprimido esquecido assim que lembrar, mesmo se isso significar a ingestão de dois comprimidos ao mesmo tempo. Ela deve, então, continuar a tomar os comprimidos seguintes no horário habitual. Além disso, deve ser usado um método de barreira, como por exemplo, a "camisinha", durante os 7 dias seguintes. Se a mulher teve uma relação sexual nos 7 dias prévios ao esquecimento, a possibilidade de gravidez3 deve ser considerada. Quanto maior o número de comprimidos esquecidos e quanto mais próximo estiver o intervalo regular sem tratamento, maior o risco de gravidez3.
Segunda semana: a mulher deve tomar o último comprimido esquecido assim que lembrar, mesmo se isso significar a ingestão de dois comprimidos ao mesmo tempo. Ela deve, então, continuar tomando os comprimidos seguintes no horário habitual. Se ela tomou os comprimidos corretamente nos 7 dias antes do primeiro comprimido esquecido, não há necessidade de usar precauções anticoncepcionais adicionais. Entretanto, se esse não for o caso ou se ela se esqueceu de tomar mais de um comprimido, a mulher deve ser advertida a usar precauções adicionais durante 7 dias.
Terceira semana: o risco de confiabilidade reduzida é iminente por causa da proximidade com o intervalo sem tratamento. Entretanto, ajustando o esquema de administração dos comprimidos, a proteção anticoncepcional reduzida ainda pode ser evitada. Aderindo a qualquer das duas opções a seguir, não há necessidade de usar precauções anticoncepcionais adicionais, desde que nos 7 dias prévios ao primeiro comprimido esquecido, a mulher tenha tomado todos os comprimidos corretamente. Se esse não for o caso, a mulher deve ser orientada a seguir a primeira dessas duas opções e também usar precauções adicionais durante os 7 dias seguintes.
- A mulher deve tomar o último comprimido esquecido assim que lembrar, mesmo se isso significar a ingestão de dois comprimidos ao mesmo tempo. Ela deve, então, continuar tomando os comprimidos seguintes no horário habitual. A próxima cartela deve ser iniciada assim que a cartela em uso terminar, sem fazer intervalo entre as cartelas. É improvável que a mulher apresente sangramento de privação até o final da segunda cartela, mas ela pode apresentar spotting ou sangramento inesperado durante os dias em que estiver tomando os comprimidos.
- A mulher pode também ser orientada a interromper o uso dos comprimidos da cartela que estiver usando. Ela deve, então, ficar sem tomar os comprimidos durante 7 dias, contando o dia do comprimido esquecido e, subsequentemente, iniciar a próxima cartela.
Caso a mulher esqueça de tomar os comprimidos e, subsequentemente, não apresente sangramento de privação no primeiro intervalo normal sem tratamento, a possibilidade de gravidez3 deve ser considerada.
Conduta em caso de distúrbios gastrintestinais
Em caso de distúrbios gastrintestinais graves, a absorção pode não ter sido completa e devem ser adotados métodos anticoncepcionais adicionais.
Se ocorrer vômito121 dentro de 3 a 4 horas após a ingestão do comprimido, a recomendação para comprimidos esquecidos é aplicável (veja item “8. POSOLOGIA E MODO DE USAR - Conduta se a mulher esquecer de tomar o comprimido”). Se a mulher não quiser alterar seu esquema atual de administração, ela precisa tomar comprimidos adicionais de outra cartela.
Conduta para alterar ou atrasar a menstruação6
Para atrasar a menstruação6, a mulher deve continuar o tratamento com outra cartela de Mercilon® sem fazer o intervalo sem comprimido. A mulher pode continuar com essa segunda cartela durante o tempo que quiser, até que ela esteja completamente vazia. A mulher pode apresentar sangramento inesperado ou spotting durante o período em que estiver tomando os comprimidos. O uso regular de Mercilon® é, então, retomado após o intervalo habitual de 7 dias sem comprimido.
Para alterar o início da menstruação6 para outro dia da semana diferente daquele ao qual está acostumada, a mulher pode ser orientada a encurtar o próximo intervalo sem comprimido em quantos dias ela quiser. Quanto mais curto o intervalo, maior o risco de não apresentar sangramento de privação e de apresentar sangramento inesperado e spotting durante o uso da segunda cartela (logo que ela atrasar a menstruação6).
REAÇÕES ADVERSAS
As reações adversas possivelmente relacionadas ao tratamento, que foram relatadas em estudos clínicos ou estudos observacionais com Mercilon® ou usuárias de AHCs em geral, são mencionadas a seguir1:
|
Classe de órgãos e sistemas |
Comuns |
Incomuns |
Raros |
|
Distúrbios do sistema imune122 |
|
|
Hipersensibilidade |
|
Distúrbios metabólicos e nutricionais |
|
Retenção de líquidos |
|
|
Distúrbios psiquiátricos |
Humor deprimido Humor alterado |
Libido123 diminuída |
Libido123 aumentada |
|
Distúrbios do sistema nervoso124 |
Cefaleia55 |
Enxaqueca33 |
|
|
Distúrbios oculares |
|
|
Intolerância a lentes de contato |
|
Distúrbios vasculares125 |
|
|
Tromboembolismo126 venoso2 Tromboembolismo126 alterial2 |
|
Distúrbios gastrintestinais |
Náusea127, dor abdominal |
Vômito121, diarreia128 |
|
|
Distúrbios da pele129 e do tecido subcutâneo130 |
|
Exantema131, urticária132 |
Eritema nodoso133, eritema multiforme134 |
|
Distúrbios do sistema reprodutor e das mamas7 |
Dor mamária, sensibilidade mamária |
Aumento mamário |
Secreção vaginal secreção mamária |
|
Investigações |
Aumento do peso |
|
Diminuição do peso |
1 O termo MedDRA mais apropriado para descrever determinada reação adversa foi listado. Os sinônimos ou condições relacionadas não são listados, mas também devem ser considerados.
2 A incidência46 em estudos de coorte135 observacionais é de ? 1/10.000 a < 1/1.000 mulheres-anos.
Vários efeitos indesejáveis relatados por mulheres utilizando anticoncepcionais orais combinados são abordados em detalhes no item “5. ADVERTÊNCIAS E PRECAUÇÕES”. Eles incluem: distúrbios tromboembólicos venosos; distúrbios tromboembólicos arteriais; hipertensão68; tumores dependentes de hormônios (por exemplo, tumores hepáticos e câncer10 de mama84); exacerbações de angioedema90 hereditário e adquirido; cloasma102.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Não há relatos de danos graves decorrentes de superdose. Os sintomas34 que podem ocorrer nesse caso incluem: náusea127, vômito121 e, em meninas jovens, leve sangramento vaginal. Não há antídotos e o tratamento deve ser sintomático136.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS 1.0029.0220
Farm. Resp.: Marcos C. Borgheti - CRF-SP nº 15.615
Registrado por:
Organon Farmacêutica Ltda.
Rua 13 de Maio, 815 - Sousas, Campinas/SP
CNPJ: 45.987.013/0001-34 - Indústria Brasileira
Fabricado por:
Eurofarma Laboratórios S.A.
Itapevi/SP
SAC 0800 0000149



