

TORLÓS
Torrent do Brasil Ltda.
TORLÓS
losartana potássica
I – IDENTIFICAÇÃO DO PRODUTO
Nome do produto: TORLÓS®
Nome genérico: losartana potássica
Forma Farmacêutica e Apresentação de Torlós
TORLÓS® 25 mg: embalagens contendo 28 comprimidos revestidos.TORLÓS® 50 mg: embalagens contendo 14 ou 28 comprimidos revestidos.
TORLÓS® 100 mg: embalagens contendo 10 ou 30 comprimidos revestidos.
Composição de Torlós
Cada comprimido revestido de TORLÓS® 25 mg contém:
losartana potássica........................................ 25 mg
Excipientes: lactose1 monoidratada, amido, hiprolose, talco, estearato de magnésio, TRC coat A e óxido de ferro vermelho.
Cada comprimido revestido de TORLÓS® 50 mg contém:
losartana potássica........................................ 50 mg
Excipientes: lactose1 monoidratada, amido, hiprolose, talco, estearato de magnésio, TRC coat A e óxido de ferro vermelho.
Cada comprimido revestido de TORLÓS® 100 mg contém:
losartana potássica......................................100 mg
Excipientes: lactose1, amido, estearato de magnésio, celulose microcristalina, talco, dióxido de silício coloidal, hipromelose, hiprolose e dióxido de titânio.
II - INFORMAÇÕES AO PACIENTE
Ação esperada do medicamento:
TORLÓS® age dilatando os vasos sanguíneos2 para ajudar o coração3 a bombear o sangue4 para todo o corpo com mais facilidade. Essa ação ajuda a reduzir a pressão alta. Em muitos pacientes com insuficiência cardíaca5, TORLÓS® irá auxiliar no melhor funcionamento do coração3. TORLÓS® também diminui o risco de doenças do coração3 e dos vasos sanguíneos2, tal como derrame6 (acidente vascular cerebral7) em pacientes com pressão alta e espessamento das paredes do ventrículo esquerdo do coração3 (hipertrofia8 ventricular esquerda). Além desses efeitos sobre a pressão arterial9, TORLÓS® também ajuda a proteger os rins10 se o paciente tiver diabetes tipo 211 e proteinúria12 (perda de proteína na urina13 por comprometimento dos rins10).
Cuidados de armazenamento:
Manter em temperatura ambiente (15° a 30°C) e protegido da umidade.
Prazo de validade:
O prazo de validade encontra-se impresso na embalagem. Não utilize este ou qualquer outro medicamento com o prazo de validade vencido.
Gravidez14 e lactação15:
Informe seu médico da ocorrência de gravidez14 na vigência do tratamento ou após o término. Informar ao médico se está amamentando.
Pare de tomar TORLÓS® se estiver grávida ou engravidar durante o tratamento e procure o seu médico o mais rápido possível.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez14.
Cuidados na administração:
Siga a orientação do seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Interrupção do tratamento:
Não interrompa o tratamento sem o conhecimento do seu médico.
Reações adversas:
Informe seu médico o aparecimento de reações desagradáveis.
Alguns pacientes podem apresentar tontura16, fadiga17, aturdimento, exantema18 ou urticária19 (para mais informações vide “Reações Adversas” em “Informações Técnicas”). Informe ao seu médico imediatamente se você apresentar esses sintomas20 ou outros sintomas20 incomuns.
Alguns pacientes, especialmente pacientes com diabetes tipo 211 e proteinúria12, também podem apresentar aumento dos níveis de potássio no sangue4. Informe ao seu médico se você apresentar doença renal21 e diabetes tipo 211 e proteinúria12 e/ou estiver tomando suplementos de potássio, medicamentos poupadores de potássio ou substitutos do sal da dieta que contêm potássio.
Se apresentar uma reação alérgica22 com inchaço23 da face24, dos lábios, da garganta25 e/ou da língua26 que possa dificultar sua respiração ou capacidade de engolir, pare de tomar o medicamento e procure seu médico imediatamente.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS
Ingestão concomitante com outras substâncias:
Em geral, a losartana potássica não interage com alimentos ou outros medicamentos. É importante informar ao seu médico se estiver tomando suplementos de potássio, medicamentos poupadores de potássio ou substitutos do sal da dieta que contêm potássio.
Contraindicações e precauções:
Este medicamento é contraindicado em pacientes com alergia27 a qualquer componente da formulação. Informe ao seu médico se tiver apresentado recentemente episódios de vômito28 ou diarreia29 excessivos. É muito importante informar problemas dos rins10 ou fígado30.
Informe seu médico sobre qualquer medicamento que esteja usando, antes do início ou durante o tratamento.
NÃO TOME REMÉDIO SEM O CONHECIMENTO DO SEU MÉDICO, PODE SER PERIGOSO PARA A SAÚDE31.
III – INFORMAÇÕES TÉCNICAS
Características de Torlós
A losartana potássica é um antagonista32 do receptor (tipo AT1) da angiotensina II. A losartana potássica também reduz o risco combinado de morte cardiovascular, acidente vascular cerebral7 e infarto do miocárdio33 em pacientes hipertensos com hipertrofia8 ventricular esquerda e oferece proteção renal21 para pacientes34 com diabetes tipo 211 e proteinúria12.Mecanismo de ação: a angiotensina II, um potente vasoconstritor, é o principal hormônio35 ativo do sistema renina-angiotensina e o maior determinante da fisiopatologia36 da hipertensão37. A angiotensina II liga-se ao receptor AT1 encontrado em muitos tecidos (por exemplo, músculo liso vascular38, glândulas39 adrenais, rins10 e coração3) e desencadeia várias ações biológicas importantes, incluindo vasoconstrição40 e liberação de aldosterona. A angiotensina II também estimula a proliferação de células musculares41 lisas. Foi identificado um segundo receptor da angiotensina II subtipo AT2, cuja função na homeostase cardiovascular é desconhecida.
A losartana é um composto sintético potente, ativo por via oral. Em bioensaios de ligação e farmacológicos, liga-se seletivamente ao receptor AT1. In vitro e in vivo, tanto a losartana quanto seu metabólito42 ácido carboxílico farmacologicamente ativo (E-3174) bloqueiam todas as ações fisiologicamente relevantes da angiotensina II, independentemente da fonte ou via de síntese. Diferentemente de alguns antagonistas peptídicos da angiotensina II, a losartana não apresenta efeitos agonistas.
A losartana liga-se seletivamente ao receptor AT1 e não se liga ou bloqueia outros receptores de hormônios ou canais iônicos importantes na regulação cardiovascular. Além disso, a losartana não inibe a ECA (cininase II), a enzima43 que degrada a bradicinina44. Consequentemente, os efeitos não relacionados diretamente ao bloqueio do receptor AT1, como a potencialização dos efeitos mediados pela bradicinina44 ou o desenvolvimento de edema45 (losartana: 1,7%; placebo46: 1,9%), não estão associados à losartana.
Absorção: após a administração oral, a losartana é bem absorvida e sofre metabolismo47 de primeira passagem, formando um metabólito42 ácido carboxílico ativo e outros metabólitos48 inativos. A biodisponibilidade sistêmica dos comprimidos de losartana é de aproximadamente 33%. As concentrações máximas médias de losartana e de seu metabólito42 ativo são atingidas em 1 hora e em 3 a 4 horas, respectivamente. Não houve efeito clinicamente significativo no perfil da concentração plasmática de losartana quando o fármaco49 foi administrado com uma refeição-padrão.
Distribuição: tanto a losartana como seu metabólito42 ativo apresentam taxa de ligação à proteínas50 plasmáticas > 99%, principalmente com a albumina51. O volume de distribuição da losartana é de 34 litros. Estudos em ratos indicam que a losartana praticamente não atravessa a barreira hematoencefálica.
Metabolismo47: aproximadamente 14% da dose de losartana administrada por via intravenosa ou oral são convertidos ao seu metabólito42 ativo. Após a administração intravenosa ou oral de losartana potássica marcado com 14C, a radioatividade plasmática circulante principal é atribuída à losartana e ao seu metabólito42 ativo. Observou-se conversão mínima de losartana ao seu metabólito42 ativo em aproximadamente 1% dos indivíduos estudados. Além do metabólito42 ativo, são formados metabólitos48 inativos, incluindo dois principais formados por hidroxilação da cadeia lateral butílica e um secundário, um glucuronídeo N-2 tetrazol.
Eliminação: a depuração plasmática da losartana e de seu metabólito42 ativo é de aproximadamente 600 mL/min e 50 mL/min, respectivamente. A depuração renal21 da losartana e de seu metabólito42 ativo é de aproximadamente 74 mL/min e 26 mL/min, respectivamente. Quando a losartana é administrada por via oral, aproximadamente 4% da dose é excretada inalterada na urina13 e 6%, na forma de metabólito42 ativo. As farmacocinéticas da losartana e de seu metabólito42 ativo são lineares com doses de losartana potássica de até 200 mg, administradas por via oral.
Após a administração oral, as concentrações plasmáticas de losartana e de seu metabólito42 ativo diminuem poliexponencialmente, com meia-vida final de aproximadamente 2 horas e de 6 a 9 horas, respectivamente. Durante a administração da dose única diária de 100 mg, a losartana e seu metabólito42 ativo não se acumulam significativamente no plasma52.
Tanto a excreção biliar como a urinária contribuem para a eliminação de losartana e seus metabólitos48. Após dose oral de losartana potássica marcada com 14C em humanos, aproximadamente 35% da radioatividade é recuperada na urina13 e 58%, nas fezes. Após dose intravenosa de losartana potássica marcada com 14C em humanos, aproximadamente 43% da radioatividade é recuperada na urina13 e 50% nas fezes.
Indicações de Torlós
Hipertensão37
TORLÓS® é indicado para o tratamento da hipertensão37.
TORLÓS® é indicado para o tratamento da insuficiência cardíaca5, quando o tratamento com inibidor da ECA não é mais considerado adequado. Não é recomendada a troca do tratamento para TORLÓS® em pacientes com insuficiência cardíaca5 que estejam estabilizados com inibidores da ECA.
Redução do Risco de Morbidade53 e Mortalidade54 Cardiovascular em Pacientes Hipertensos com Hipertrofia8 Ventricular Esquerda
TORLÓS® é indicado para reduzir o risco de morbidade53 e mortalidade54 cardiovascular avaliado pela incidência55 combinada de morte cardiovascular, acidente vascular cerebral7 e infarto do miocárdio33 em pacientes hipertensos com hipertrofia8 ventricular esquerda (vide “Raça” em “Precauções e Advertências”).
Proteção Renal21 em Pacientes com Diabetes Tipo 211 e Proteinúria12
TORLÓS® é indicado para retardar a progressão da doença renal21 avaliada pela redução da incidência55 combinada de duplicação da creatinina56 sérica, insuficiência renal57 terminal (necessidade de diálise58 ou transplante renal21) ou morte; e para reduzir a proteinúria12.
Contraindicações de Torlós
O medicamento é contraindicado a pacientes com hipersensibilidade conhecida à losartana potássica ou a outros componentes da formulação.Precauções e Advertências de Torlós
Hipersensibilidade.
Angioedema59 (vide “Reações Adversas”).
Hipotensão60 e desequilíbrio hidroeletrolítico61: em pacientes que apresentam depleção62 de volume intravascular63 (por exemplo, aqueles tratados com altas doses de diuréticos64), pode ocorrer hipotensão60 sintomática65. Essas situações devem ser corrigidas antes da administração da losartana potássica, ou deve-se utilizar dose inicial mais baixa (vide “Posologia”).
Desequilíbrios eletrolíticos são comuns em pacientes com comprometimento renal21, com ou sem diabetes66, e devem ser corrigidos. Em um estudo clínico que envolveu pacientes com diabetes tipo 211 e proteinúria12, a incidência55 de hipercalemia67 foi mais alta no grupo tratado com a losartana potássica quando comparado ao grupo placebo46; entretanto, poucos pacientes descontinuaram o tratamento em razão de hipercalemia67 (vide “Reações Adversas”).
Insuficiência hepática68: com base nos dados de farmacocinética que demonstram aumentos significativos das concentrações plasmáticas de losartana em pacientes com cirrose69, deve-se considerar doses mais baixas para pacientes34 com histórico de insuficiência hepática68 (vide “Posologia”).
Insuficiência renal57: como consequência da inibição do sistema renina-angiotensina, foram relatadas, em indivíduos susceptíveis, alterações na função renal21, inclusive insuficiência renal57; essas alterações podem ser reversíveis com a descontinuação do tratamento.
Outros fármacos que afetam o sistema renina-angiotensina podem aumentar as taxas de ureia70 sanguínea e de creatinina56 sérica em pacientes com estenose71 da artéria renal72 bilateral ou estenose71 da artéria73 de rim74 único. Foram relatados efeitos semelhantes com a losartana potássica; essas alterações da função renal21 podem ser reversíveis com a descontinuação do tratamento.
Insuficiência cardíaca5: o uso concomitante de losartana potássica e inibidores da ECA não foi adequadamente estudado.
Raça: com base no estudo LIFE (Losartan Intervention For Endpoint reduction in hypertension - Intervenção com losartana para redução de desfechos na hipertensão37), os benefícios de losartana potássica na morbidade53 e mortalidade54 cardiovascular comparados aos do atenolol não se aplicam a pacientes negros com hipertensão37 e hipertrofia8 ventricular esquerda, embora os dois esquemas terapêuticos reduzam efetivamente a pressão arterial9 em pacientes negros. Na população total do estudo LIFE (n= 9.193), o tratamento com a losartana potássica comparado ao atenolol reduziu em 13% (p= 0,021) o risco do desfecho primário composto de morte cardiovascular, acidente vascular cerebral7 e infarto do miocárdio33. Nesse estudo, a losartana potássica reduziu o risco de morbidade53 e mortalidade54 cardiovascular comparado ao atenolol em pacientes hipertensos com hipertrofia8 ventricular esquerda que não eram negros (n= 8.660) conforme avaliado pelo desfecho primário composto (incidência55 combinada de morte cardiovascular, acidente vascular cerebral7 e infarto do miocárdio33) (p= 0,003). Nesse estudo, entretanto, o risco de os pacientes negros que receberam atenolol apresentarem o desfecho primário composto foi menor quando comparado ao risco daqueles que receberam losartana potássica (p= 0,03). No subgrupo de pacientes negros (n= 533; 6% dos pacientes do Estudo LIFE), ocorreram 29 desfechos primários entre os 263 pacientes que receberam atenolol (11%, 25,9 por 1.000 pacientes/ano) e 46, entre os 270 pacientes que receberam losartana potássica (17%, 41,8 por 1.000 pacientes/ano).
Gravidez14: quando utilizados durante o segundo e o terceiro trimestres da gravidez14, os fármacos que atuam diretamente no sistema renina-angiotensina podem causar danos e até morte do feto75 em desenvolvimento. Quando houver confirmação de gravidez14, o tratamento com a losartana potássica deve ser suspenso o mais rapidamente possível.
Embora não haja experiência com a utilização de losartana potássica em mulheres grávidas, estudos realizados com losartana potássica em animais demonstraram danos e morte do feto75 e do recém-nascido; acredita-se que isto ocorra por um mecanismo farmacologicamente mediado pelos efeitos no sistema renina-angiotensina. Em humanos, a perfusão renal21 fetal, que depende do desenvolvimento do sistema renina-angiotensina, começa no segundo trimestre; assim, o risco para o feto75 aumenta se a losartana potássica for administrada durante o segundo ou o terceiro trimestre da gravidez14.
Categoria de risco na gravidez14: C (primeiro trimestre) - Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Categoria de risco na gravidez14: D (segundo e terceiro trimestres) - Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez14.
Lactação15: não se sabe se a losartana é excretada no leite humano. Uma vez que muitos fármacos são excretados no leite humano e por causa do potencial de efeitos adversos para o lactente76, deve-se optar por suspender a amamentação77 ou o tratamento com a losartana potássica, levando-se em consideração a importância do medicamento para a mãe.
Pediatria: a segurança e a eficácia em crianças ainda não foram estabelecidas.
Pacientes idosos: nos estudos clínicos, não houve diferença relacionada à idade nos perfis de eficácia e segurança de losartana.
Interações Medicamentosas de Torlós
Nos estudos clínicos de farmacocinética realizados com hidroclorotiazida, digoxina, varfarina, cimetidina, fenobarbital, cetoconazol e eritromicina, não foram identificadas interações medicamentosas de importância clínica. Houve relatos de redução dos níveis do metabólito42 ativo pela rifampicina e pelo fluconazol. Não foram avaliadas as consequências clínicas dessas interações. A exemplo do que ocorre com outros fármacos que bloqueiam a angiotensina II ou os seus efeitos, o uso concomitante de diuréticos64 poupadores de potássio (por exemplo, espironolactona, triantereno, amilorida), suplementos de potássio ou substitutos do sal que contêm potássio pode resultar em aumento do potássio sérico.O efeito anti-hipertensivo da losartana, a exemplo do que ocorre com outros anti-hipertensivos, pode ser atenuado pelo anti-inflamatório não esteróide indometacina.
Reações Adversas de Torlós
Em estudos clínicos controlados de hipertensão37, verificou-se que a losartana potássica, em geral, é bem tolerada; os efeitos adversos foram em geral de natureza leve e transitória e não requereram a descontinuação do tratamento. A incidência55 geral de efeitos colaterais78 relatados com a losartana potássica foi comparável à do placebo46. Em estudos clínicos controlados de hipertensão37 essencial, tontura16 foi o único efeito adverso relatado como relacionado à medicação com incidência55 superior à do placebo46, em 1% ou mais dos pacientes tratados com losartana potássica. Além disso, efeitos ortostáticos relacionados à dose foram observados em menos de 1% dos pacientes. Raramente foi relatada erupção79 cutânea80, embora a incidência55 em estudos clínicos controlados tenha sido menor do que a do placebo46.
Nesses estudos clínicos duplo-cegos e controlados sobre hipertensão37 essencial, as seguintes experiências adversas relatadas com a losartana potássica ocorreram em 1% dos pacientes, independentemente da relação com a medicação:

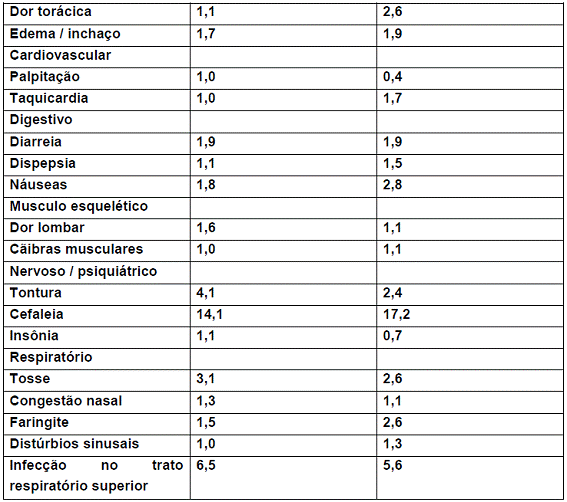
A losartana potássica foi geralmente bem tolerada em estudos clínicos controlados sobre insuficiência cardíaca5. Os efeitos adversos mais comuns relacionados à medicação foram tontura16 e hipotensão60.
A losartana potássica foi geralmente bem tolerada em um estudo clínico que envolveu pacientes com hipertrofia8 ventricular esquerda. As reações adversas relacionadas à medicação mais comuns foram tontura16, astenia81/fadiga17 e vertigem82.
No estudo LIFE (Losartan Intervention For Endpoint reduction in hypertension), dentre os pacientes sem diabetes66 no período basal, a incidência55 de novos casos de diabetes mellitus83 com a losartana potássica foi mais baixa quando comparada àquela observada com o atenolol (242 pacientes versus 320 pacientes, respectivamente, p<0,001). Como não foi incluído no estudo um grupo com placebo46, não se sabe se isso representa efeito benéfico da losartana potássica ou reação adversa ao atenolol.
A losartana potássica foi geralmente bem tolerada em um estudo clínico controlado que envolveu pacientes com diabetes tipo 211 e proteinúria12. As reações adversas relacionadas à medicação mais comuns foram astenia81/fadiga17, tontura16, hipotensão60 e hipercalemia67 (vide “Hipotensão e Desequilíbrio hidroeletrolítico” em “Precauções e Advertências”).
Após a comercialização da losartana potássica, foram relatados os seguintes efeitos adversos: - Hipersensibilidade: reações anafiláticas84, angioedema59, incluindo edema45 de laringe85 e glote86, com obstrução das vias aéreas e/ou edema45 de face24, lábios, faringe87 e/ou língua26, foram relatados raramente em pacientes tratados com losartana; alguns desses pacientes apresentaram anteriormente angioedema59 com outros medicamentos, entre eles os inibidores da ECA. Vasculite88, incluindo púrpura89 de Henoch-Schoenlein, foi raramente relatada.
- Gastrintestinais: anormalidades da função hepática90, hepatite91 (relatada raramente).
- Hematológico: anemia92.
- Musculoesquelético: mialgia93.
- Sistemas nervoso/psiquiátrico: enxaqueca94.
- Respiratório: tosse.
- Pele95: urticária19, prurido96.
Alterações em exames laboratoriais: em estudos clínicos controlados sobre hipertensão37 essencial, alterações clinicamente importantes dos parâmetros laboratoriais-padrão foram raramente associadas com a administração de losartana potássica. Hipercalemia67 (potássio sérico >5,5 mEq/L) ocorreu em 1,5% dos pacientes nos estudos clínicos sobre hipertensão37. Em um estudo clínico conduzido em pacientes com diabetes tipo 211 e proteinúria12, 9,9% dos pacientes tratados com a losartana potássica e 3,4% dos pacientes que receberam placebo46 desenvolveram hipercalemia67 (vide “Hipotensão e Desequilíbrio hidroeletrolítico” em “Precauções e Advertências”). Raramente ocorreram aumentos de ALT que, em geral, desapareceram com a descontinuação do tratamento.
Posologia de Torlós
TORLÓS® pode ser administrado com ou sem alimentos.TORLÓS® pode ser administrado com outros agentes anti-hipertensivos.
Hipertensão37
A dose usual inicial e de manutenção é de 50 mg uma vez ao dia para a maioria dos pacientes. O efeito anti-hipertensivo máximo é alcançado 3 a 6 semanas após o início do tratamento. Alguns pacientes podem obter benefício adicional se a dose for aumentada para 100 mg uma vez ao dia.
Para pacientes34 com depleção62 de volume intravascular63 (por exemplo, pacientes tratados com altas doses de diuréticos64), deve ser considerada uma dose inicial de 25 mg uma vez ao dia (vide “Precauções e Advertências”).
Não há necessidade de ajuste posológico inicial para pacientes34 idosos ou para pacientes34 com insuficiência renal57, inclusive para pacientes34 sob diálise58. Deve ser considerada a utilização de uma dose mais baixa para pacientes34 com histórico de insuficiência hepática68 (vide “Precauções e Advertências”).
Redução do risco de morbidade53 e mortalidade54 cardiovascular em pacientes hipertensos com hipertrofia8 ventricular esquerda
A dose usual inicial de TORLÓS® é de 50 mg uma vez ao dia. Uma dose baixa de hidroclorotiazida deve ser adicionada e/ou a dose de TORLÓS® deve ser elevada para 100 mg uma vez ao dia, com base na resposta da pressão arterial9.
Insuficiência cardíaca5
A dose inicial de TORLÓS® para pacientes34 com insuficiência cardíaca5 é de 12,5 mg uma vez ao dia. Geralmente, a dose deve ser titulada a intervalos semanais (isto é, 12,5 mg/dia, 25 mg/dia, 50 mg/dia) até a dose usual de manutenção de 50 mg uma vez ao dia, de acordo com a tolerabilidade do paciente.
Proteção Renal21 em Pacientes com Diabetes Tipo 211 e Proteinúria12
A dose usual inicial é de 50 mg uma vez ao dia. Essa dose pode ser aumentada para 100 mg uma vez ao dia, com base na resposta da pressão arterial9. TORLÓS® pode ser administrado com outros agentes anti-hipertensivos (por exemplo, diuréticos64, bloqueadores dos canais de cálcio, alfa ou betabloqueadores e agentes de ação central) e também com insulina97 e outros agentes hipoglicemiantes98 comumente utilizados (por exemplo: sulfonilureias99, glitazonas e inibidores da glucosidase).
Superdosagem de Torlós
Os dados disponíveis sobre superdose em humanos são limitados. As manifestações mais prováveis de superdose seriam hipotensão60 e taquicardia100; bradicardia101 poderia ocorrer por estimulação parassimpática (vagal). Se ocorrer hipotensão60 sintomática65, deve-se instituir tratamento de suporte.
Nem a losartana, nem o seu metabólito42 ativo podem ser removidos da circulação102 por hemodiálise103.
Pacientes Idosos de Torlós
Nos estudos clínicos não houve diferença relacionada à idade nos perfis de eficácia e segurança da losartana.
IV – DIZERES LEGAIS
Registro MS 1.0525.0005
Farmacêutico Responsável:
Dr. Ricardo Magela Rocha - CRF-SP: 7.907
Importado por:
Torrent do Brasil Ltda.
Avenida Tamboré, 1180 - Módulo A5
Barueri - SP
CNPJ 33.078.528/0001-32
Fabricado por:
Torrent Pharmaceuticals Ltd.
Baddi – Índia
SAC: 0800.7708818
VENDA SOB PRESCRIÇÃO MÉDICA.
n° do lote, data de fabricação e data de validade: vide cartucho
TORLÓS - Laboratório
Torrent do Brasil Ltda.
Av. Tamboré, 1180, Módulo A5.
Baurueri - SP/SP
Tel: 0800-7708818
Site: http://www.torrent.com.br
Ver outros medicamentos do laboratório "Torrent do Brasil Ltda."






