

Actemra SC
PRODUTOS ROCHE QUÍMICOS E FARMACÊUTICOS S.A.
IDENTIFICAÇÃO DO MEDICAMENTO
Actemra® SC
tocilizumabe
Injetável 162 mg/0,9 mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável para administração subcutânea1 162 mg/0,9 mL
Caixa com 4 seringas preenchidas de uso único com dispositivo de segurança da agulha.
VIA SUBCUTÂNEA1
USO ADULTO
COMPOSIÇÃO:
Cada 0,9 mL de Actemra® SC contém:
| tocilizumabe | 162 mg |
| veículo q.s.p. | 0,9 mL |
Excipientes: polissorbato 80, L-arginina, cloridrato de L-arginina, L-metionina, L-histidina, cloridrato de L-histidina mono-hidratada e água para injetáveis.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Actemra® SC em associação com metotrexato (MTX) é indicado no tratamento da artrite reumatoide2 (AR) grave, ativa e progressiva em pacientes adultos não tratados previamente com MTX. Neste grupo de pacientes, Actemra® SC pode ser usado em monoterapia em caso de intolerância a MTX ou quando o uso continuado de MTX é inapropriado.
Actemra® SC é indicado para o tratamento de artrite reumatoide2 ativa, moderada a grave em pacientes adultos, quando tratamento anterior adequado com, pelo menos, um medicamento antirreumático modificador da doença (DMARD) não tenha trazido os benefícios esperados:
- Após falha de esquema combinado com DMARDs convencionais, incluindo, necessariamente, o metotrexato, utilizados nas doses e pelo tempo indicados na bula de cada agente específico; ou
- Após falha do agente anti-TNF, utilizado na dose e pelo tempo indicados na bula de cada agente específico.
Neste grupo de pacientes, Actemra® SC pode ser usado isoladamente ou em combinação com metotrexato (MTX) e/ou outros DMARDs.
Actemra® SC está indicado para o tratamento de arterite de células gigantes3 (ACG) em pacientes adultos.
COMO ESTE MEDICAMENTO FUNCIONA?
Actemra® SC faz parte dos novos medicamentos antirreumáticos biológicos modificadores da doença (DMARDs). É considerado um DMARD biológico, porque organismos vivos estão envolvidos na sua produção, o que não ocorre com DMARDs sintéticos, como o metotrexato, por exemplo.
Actemra® SC é um anticorpo4 (substância que ajuda na defesa do organismo) humanizado que bloqueia a ação da interleucina 6 (IL-6), uma proteína que promove a inflamação5 crônica na AR. Em pacientes com AR, observam-se níveis elevados de IL-6 na articulação6, e seus níveis no sangue7 correlacionam-se bem com a atividade da doença.
Tocilizumabe (TCZ) neutraliza a ação da IL-6, o que resulta em melhora significativa e clinicamente superior quando comparado ao tratamento com DMARDs tradicionais (como o metotrexato [MTX] e outros) em populações estudadas com AR ativa moderada a grave.
A eficácia de Actemra® SC subcutâneo8 foi avaliada em um estudo que incluiu pacientes com artrite reumatoide2 ativa que não haviam respondido bem a outros tratamentos. O estudo avaliou se havia diferença na proporção de pacientes que obtiveram melhora na semana 24 de estudo em tratamento com Actemra® intravenoso ou subcutâneo8. Esse estudo demonstrou que Actemra® SC foi equivalente a Actemra® IV, de acordo com a avaliação de diversos tipos de respostas dos pacientes. Foi também realizado estudo para verificar se Actemra® SC poderia inibir a progressão radiográfica em pacientes com artrite reumatoide2 moderada a severa. Os resultados foram compatíveis com os obtidos com Actemra® IV, isto é, os pacientes com Actemra® SC apresentaram progressão muito menor em 24 semanas que os pacientes tratados com placebo9.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Actemra® SC é contraindicado a pacientes com hipersensibilidade (alergia10) conhecida a tocilizumabe ou aos componentes da fórmula.
O tratamento com Actemra® SC não deve ser iniciado em pacientes com infecções11 graves ativas.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Este medicamento deverá ser prescrito por médicos com experiência no tratamento da AR que tenham conhecimento suficiente sobre o produto.
A substituição por qualquer outro medicamento biológico requer o consentimento do médico prescritor.
Geral
Infecções11: Foram relatadas infecções11 sérias e, em alguns casos, fatais em pacientes em tratamento com agentes imunossupressores que incluem tocilizumabe.
Pacientes com infecções11 ativas (em que o agente causal esteja presente e se multiplicando) não devem iniciar tratamento com Actemra® SC, e sua administração deve ser interrompida se o paciente desenvolver infecção12 grave, até que seja resolvida. Informe a seu médico se você tem história de infecções11 recorrentes ou alguma condição subjacente (por exemplo, diverticulite13 – inflamação5 do intestino delgado14 ou grosso ou diabetes15) que possa predispô-lo(a) a infecções11.
Procure imediatamente seu médico caso apareça qualquer sinal16 / sintoma17 sugestivo de infecção12 para garantir a detecção rápida de infecções11 potencialmente graves e instituição de tratamento apropriado.
Complicações da diverticulite13 (divertículos são sacos que surgem na parede do intestino grosso18): foram relatados eventos de perfuração diverticular como complicação de diverticulite13 em pacientes tratados com Actemra®. Tocilizumabe deve ser usado com cautela em pacientes com histórico de úlceras19 intestinais ou doença diverticular. Pacientes que apresentam sintomas20 potencialmente indicativos de complicações de doença diverticular, tais como dor abdominal, devem ser avaliados prontamente para que haja identificação precoce de perfuração gastrintestinal.
Tuberculose21: embora os estudos clínicos não tenham demonstrado risco aumentado de tuberculose21, não se pode descartar a possibilidade de reativação da tuberculose21. Portanto, médicos e seus pacientes com histórico de infecção12 por tuberculose21 devem estar atentos quanto à manifestação de sintomas20 da doença e realizar periodicamente radiografia de tórax22. Todos os pacientes devem ser avaliados para infecção12 latente por tuberculose21 antes do início da terapia com tocilizumabe. Pacientes com tuberculose21 latente devem ser tratados com terapia antimicobacteriana padrão antes do início do tratamento com tocilizumabe.
Vacinas
Vacinas vivas e / ou vivas atenuadas não devem ser administradas a pacientes que estão em tratamento com Actemra® SC.
Não existem dados sobre a transmissão secundária de infecções11 de pessoas que receberam vacinas vivas para pacientes23 em uso de Actemra®.
Em um estudo aberto randomizado24, pacientes adultos com AR tratados com tocilizumabe e MTX conseguiram produzir resposta às vacinas contra pneumonia25 [vacina26 antipneumocócica 23-valente (polissacarídea)] e tétano27 (toxoide tetânico), comparáveis com a resposta de pacientes tratados apenas com MTX.
Recomenda-se que todos os pacientes, particularmente pacientes pediátricos e idosos, se possível, sejam vacinados de acordo com as recomendações atuais, antes do início do tratamento com Actemra® SC. O intervalo de administração entre vacinas vivas e a terapia com Actemra® deve estar de acordo com as recomendações de vacinação relativas a agentes que alteram a função do sistema imunológico28 (conhecidos como imunossupressores).
Reações de hipersensibilidade
Reações graves de hipersensibilidade (inclusive anafilaxias – reação alérgica29 grave) foram relatadas em associação a tocilizumabe. As reações de hipersensibilidade clinicamente significativas que necessitaram de interrupção permanente de Actemra® foram tratadas com sucesso com corticosteroides injetáveis (medicamentos que podem ser utilizados em casos de alergia10), epinefrina e outras medicações sintomáticas.
Na fase de pós-comercialização, eventos de hipersensibilidade grave e anafilaxia30 ocorreram em pacientes tratados com uma variedade de doses de tocilizumabe, com ou sem terapias concomitantes, pré-medicações e/ou reação de hipersensibilidade prévia.
Se ocorrer uma reação anafilática31 ou outra reação de hipersensibilidade séria, interrompa imediatamente a administração e procure seu médico.
Doença hepática32 ativa e insuficiência hepática33
Informe ao seu médico se você possui alguma doença ativa no fígado34 ou insuficiência hepática33.
Reativação viral
Reativação viral (por exemplo, vírus35 da hepatite36 B) tem sido relatada com terapias biológicas para artrite reumatoide2. Em estudos clínicos com tocilizumabe, os pacientes recrutados com resultados positivos para o vírus35 da hepatite36 foram excluídos do estudo.
Distúrbios desmielinizantes37
Os médicos devem estar vigilantes quanto a sintomas20 potencialmente indicativos de início de distúrbios de desmielinização central. O potencial para a desmielinização central com Actemra® é desconhecido até o momento, mas esclerose múltipla38 e polineuropatia desmielinizante39 inflamatória crônica foram relatadas raramente em estudos clínicos para artrite reumatoide2.
Risco cardiovascular
Pacientes com artrite reumatoide2 tem um risco elevado de doenças cardiovasculares40 e devem ter os fatores de risco (como hipertensão41 e hiperlipidemia42) acompanhados e controlados como parte do seguimento de rotina.
Exames laboratoriais
Neutropenia43 (diminuição do número de um dos tipos de glóbulos brancos no sangue7) O tratamento com tocilizumabe associa-se a maior incidência44 de neutropenia43.
No entanto, não se observou associação entre neutropenia43 relacionada ao tratamento de infecções11 sérias nos estudos clínicos.
Deve-se ter cuidado ao considerar a introdução de tratamento com tocilizumabe em pacientes com neutropenia43. O tratamento não é recomendado quando o número absoluto de glóbulos brancos (neutrófilos45) estiver abaixo de 500/mm3 (0,5 x 109/L). Na AR e ACG, a contagem de neutrófilos45 deve ser monitorada de quatro a oito semanas após o início do tratamento e regularmente após esse período.
Trombocitopenia46 (redução do número de plaquetas47, células48 responsáveis pela coagulação49 do sangue7)
O tratamento com tocilizumabe associa-se à redução do número de plaquetas47.
No entanto, não se observou associação entre redução do número de plaquetas47 relacionada ao tratamento e casos graves de sangramento nos estudos clínicos.
Deve-se ter cautela ao considerar a introdução de tratamento com tocilizumabe em pacientes com número reduzido de plaquetas47. O tratamento não é recomendado a pacientes com número de plaquetas47 inferior a 50.000/mm3 (50 x 103/µL).
Na AR e ACG, a contagem de plaquetas47 deve ser monitorada de quatro a oito semanas após o início do tratamento e regularmente após esse período.
Elevação das transaminases hepáticas50 (substâncias existentes no fígado34, responsáveis pela sua função)
Nos estudos clínicos, foi observada elevação leve a moderada das transaminases hepáticas50 associada ao tratamento com tocilizumabe, sem progressão para danos no fígado34. Os aumentos nas transaminases hepáticas50 foram mais frequentemente observados quando medicamentos com potencial hepatotóxico (que são tóxicos para o fígado34, tais como metrotexato) foram administrados concomitantemente com tocilizumabe.
Deve-se ter cuidado ao considerar a introdução de tratamento com tocilizumabe em pacientes com elevação das transaminases ALT ou AST. O tratamento não é recomendado a pacientes com ALT ou AST acima de 5 x o limite superior da normalidade (LSN) (TGP ou TGO > 5 x LSN).
Na AR e ACG, as transaminases devem ser monitoradas de quatro a oito semanas após o início do tratamento e regularmente após esse período.
Parâmetros lipídicos (quantidade de gordura51)
Foram observadas elevações nos níveis de lipídios, tais como colesterol52, triglicérides53 e / ou lipoproteína de baixa densidade LDL54 popularmente conhecido como mau colesterol52.
Em pacientes tratados com tocilizumabe, os níveis de lipídios devem ser monitorados de quatro a oito semanas após o início do tratamento com tocilizumabe. Os pacientes devem ser tratados de acordo com os protocolos clínicos locais para o tratamento de hiperlipidemia42.
Gravidez55 e amamentação56
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Não existem dados adequados sobre o uso de Actemra® SC em gestantes. Um estudo em macacos não demonstrou risco potencial de dismorfogênese (malformações57), mas demonstrou número maior de aborto espontâneo / óbito58 com dose elevada. A relevância desses dados para humanos é desconhecida.
Actemra® SC só deve ser usado se os potenciais benefícios clínicos provenientes de seu uso para a mãe excederem os potenciais riscos à saúde59 do feto60.
Não se sabe se tocilizumabe é excretado no leite materno. Embora alguns tipos de anticorpos61 passem para o leite humano, a absorção de tocilizumabe pela criança por meio do aleitamento é improvável, por causa da rápida desintegração dessas proteínas62 no estômago63. A decisão em se manter / interromper o aleitamento materno64 ou manter / interromper a terapia com Actemra® SC deve ser adotada levando em consideração o benefício do aleitamento materno64 para a criança e o benefício da terapia com tocilizumabe para a paciente.
Advertências para populações especiais
Pacientes com doença nos rins65 (insuficiência66 dos rins65), doença no fígado34 (insuficiência66 do fígado34), crianças e idosos: vide item “6. Como devo usar este medicamento? – Instruções especiais de administração”.
Efeitos sobre a capacidade de dirigir e operar máquinas
Não foram realizados estudos específicos sobre os efeitos de Actemra® SC na capacidade de dirigir e operar máquinas. No entanto, não existem evidências, a partir dos dados disponíveis, de que tocilizumabe afete a capacidade de dirigir e operar máquinas.
Abuso e dependência
Não foram realizados estudos sobre efeitos potenciais de dependência causados por tocilizumabe. No entanto, não existem evidências de que o tratamento com tocilizumabe resulte em dependência ou abuso.
Até o momento não há informações de que tocilizumabe possa causar doping. Em caso de dúvidas, consulte seu médico.
Principais interações medicamentosas
O metotrexato, anti-inflamatórios gerais (não esteroidais) e corticosteroides não influenciaram a farmacocinética (etapas de transformação do medicamento dentro do organismo, desde sua ingestão até eliminação) de tocilizumabe em pacientes com AR.
Em pacientes com ACG, não foi observado efeito acumulativo da dose de corticosteroide sobre a exposição a tocilizumabe.
Não há experiência do uso de tocilizumabe em combinação com outros antagonistas de TNF ou outros tratamentos biológicos em pacientes com artrite reumatoide2. O uso de Actemra® SC com outros agentes biológicos não é recomendado.
Ao introduzir ou interromper tratamento com tocilizumabe em pacientes tratados com atorvastatina, bloqueadores dos canais de cálcio, teofilina, varfarina, fenitoína, ciclosporina ou benzodiazepínicos, deve-se monitorar as doses desses medicamentos, pois podem requerer ajuste, a fim de manter o efeito terapêutico.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde59.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Actemra® SC seringa67 preenchida deve ser armazenado no refrigerador, em temperatura entre 2 e 8°C. O produto não deve ser congelado. Mantenha o produto no cartucho para proteger da luz.
Após removido do refrigerador, Actemra® SC deve ser administrado dentro de 8 horas e não deve ser mantido a temperatura maior que 30°C.
Actemra® SC não deve ser usado depois do prazo de validade mostrado na seringa67 preenchida e na embalagem.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Actemra® SC é um líquido amarelado e não contém conservantes.
Não use se o medicamento estiver turvo ou contiver partículas ou se apresentar qualquer cor exceto incolor a amarelada ou se alguma parte da seringa67 preenchida parecer danificada.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Descarte de seringas / perfurocortantes
É indispensável obedecer rigorosamente às normas de uso e descarte da seringa67 preenchida:
- seringas nunca podem ser reutilizadas;
- coloque todas as seringas usadas em um recipiente para perfurocortantes (recipiente à prova de furos);
- mantenha esse recipiente fora do alcance das crianças;
- evite colocar os recipientes de perfurocortantes no lixo doméstico;
- descarte o recipiente inteiro de acordo com a legislação local ou conforme orientação do seu profissional da saúde59.
Os pacientes devem ter um recipiente resistente para descartar todas as seringas usadas.
Descarte de medicamento não utilizado / com prazo de validade vencido
A liberação de produtos farmacêuticos no meio ambiente deve ser reduzida ao máximo. Os medicamentos não podem ser desprezados no esgoto doméstico e deve-se evitar desprezá-los no lixo doméstico. Use os “sistemas de coleta”, se disponíveis na sua região.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Dose
Artrite reumatoide2: A dose recomendada de Actemra® SC a pacientes adultos com AR é de 162 mg, administrada uma vez por semana em injeção subcutânea68. Actemra® SC pode ser usado isoladamente ou associado com metotrexato ou outras DMARDs sintéticos.
Arterite de Células Gigantes3: A dose recomendada de tocilizumabe para pacientes23 adultos com ACG é de 162 mg administrada uma vez por semana em injeção subcutânea68 em combinação com um tratamento com redução gradual de dose de glicocorticoides. Tocilizumabe pode ser usado isoladamente depois da descontinuação dos glicocorticoides. Caso os sintomas20 da ACG reapareçam durante o tratamento com tocilizumabe, seu médico poderá considerar a reintrodução e / ou aumento gradual da dose dos glicocorticoides concomitantes.
Geral: Informações limitadas estão disponíveis sobre a substituição de Actemra® intravenoso por Actemra® SC em dose fixa.
Pacientes que estiverem trocando a terapia intravenosa (IV) pela terapia subcutânea1 (SC) de Actemra® devem substituir a próxima dose IV programada pela primeira injeção69 SC, sob supervisão de profissional da saúde59 qualificado.
As formulações subcutâneas de Actemra® SC não podem ser aplicadas por via intravenosa.
Para que você possa utilizar Actemra® SC em casa, é necessário que esteja seguro(a) sobre a aplicação do medicamento e sempre atento(a) em relação a possíveis reações alérgicas, que devem ser informadas imediatamente a um profissional da saúde59, antes da aplicação da dose seguinte. Você também deve saber onde buscar atendimento imediato se surgirem sintomas20 de uma reação alérgica29 grave.
Se seus exames laboratoriais mostrarem alterações do fígado34, do número de glóbulos brancos ou de plaquetas47 no sangue7, o seu médico precisará ajustar a dose de Actemra® SC de acordo com esquemas estabelecidos ou até mesmo suspender a medicação até que o resultado do exame volte para níveis aceitáveis.
Instruções especiais de administração
Crianças: a segurança e a eficácia de tocilizumabe SC não foram estabelecidas em pacientes menores de 18 anos.
Idosos: não é necessário ajuste de dose em pacientes com idade superior a 65 anos.
Insuficiência66 dos rins65: não é necessário ajuste de dose em pacientes com insuficiência66 leve ou moderada dos rins65. Actemra® SC não foi estudado em pacientes com insuficiência66 grave dos rins65.
Insuficiência66 do fígado34: a segurança e eficácia de tocilizumabe não foram estudadas em pacientes com insuficiência66 do fígado34.
Modo de uso
A formulação subcutânea1 de Actemra® SC é aplicada usando a seringa67 preenchida com dispositivo de segurança da agulha. A primeira injeção69 precisa ser realizada sob a supervisão de um profissional da saúde59. Você deverá ser instruído(a) por seu médico quanto à técnica correta de autoaplicação. Não aplique o medicamento até que você tenha segurança de que compreendeu corretamente as instruções. Os locais recomendados para aplicação da injeção69 (abdome70, coxa71 e parte superior do braço) devem ser rodiziados, e nunca se deve aplicar o medicamento em pintas, verrugas, cicatrizes72 ou áreas de pele73 dolorosas, com manchas roxas, vermelhas ou com alguma lesão74.
Como administrar Actemra® SC em seringa67 preenchida de uso único com dispositivo de segurança da agulha:
Primeiro passo: verifique visualmente a seringa67
- Retire da geladeira a caixa que contém a seringa67 e abra a caixa. Não toque o gatilho da seringa67, pois isso pode danificá-la.
- Remova a seringa67 da caixa e examine-a visualmente, bem como o medicamento nela contido. Isso é importante para garantir que a seringa67 e o medicamento estejam em condições seguras de uso.
- Verifique a data de validade na caixa e na seringa67 (Vide Fig. A) para garantir que não esteja vencida. Não utilize a seringa67 caso a data de validade tenha expirado. Isso é importante para garantir que a seringa67 e o medicamento estejam em condições seguras de uso.
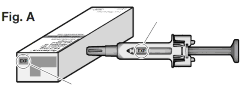
Data de validade na seringa67
Data de validade na caixa
Descarte a seringa67 e não a utilize caso:
- o medicamento esteja turvo;
- o medicamento apresente partículas;
- o medicamento apresente qualquer coloração além de incolor a amarelado;
- qualquer parte da seringa67 tenha aparência danificada.
Segundo passo: deixe que a seringa67 atinja a temperatura ambiente
- Não remova a tampa da agulha antes do quinto passo.
- Coloque a seringa67 em uma superfície plana limpa e deixe que ela atinja a temperatura ambiente por 25 a 30 minutos. Não permitir que a seringa67 atinja a temperatura ambiente pode resultar em desconforto na injeção69 e pode ser difícil pressionar o êmbolo75. Não aqueça a seringa67 de nenhuma outra maneira.
Terceiro passo: limpe suas mãos76.
- Lave suas mãos76 com água e sabão.
Quarto passo: escolha e prepare um local de injeção69
- Os locais de injeção69 recomendados são na frente e no meio de suas coxas77, e na parte inferior do seu abdome70, abaixo do umbigo78, com exceção da área de cinco centímetros diretamente ao redor do umbigo78. (Vide Fig. B)
- Caso um cuidador esteja administrando a injeção69, a área externa da parte superior dos braços também pode ser utilizada. (Vide Fig. B)
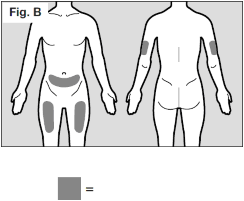
(Locais de injeção69 em destaque) - Você deve usar um local diferente cada vez que for administrar uma injeção69 em você mesmo, pelo menos três centímetros da área que você utilizou na última injeção69. Não injete em áreas que possam causar incômodo por um cinto ou faixa abdominal.
- Não injete em verrugas, cicatrizes72, hematomas79 ou áreas onde a pele73 estiver sensível, avermelhada, endurecida ou não intacta.
- Limpe a área de injeção69 escolhida utilizando um lenço umedecido com álcool, para reduzir o risco de infecções11.
- Permita que a pele73 seque por, aproximadamente, 10 segundos.
- Certifique-se de não tocar a área limpa, antes da injeção69. Não abane ou sopre a área limpa.
Quinto passo: remova a tampa da agulha
- Não segure a seringa67 pelo êmbolo75 enquanto estiver retirando a tampa da agulha.
- Segure o revestimento da agulha da seringa67 firmemente com uma das mãos76 e puxe a tampa da agulha com a outra mão80. (Vide Fig. D).
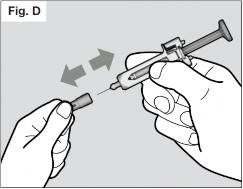
- Não toque na agulha nem deixe que ela toque em qualquer superfície.
- É possível que você veja uma gota81 de líquido na ponta da agulha. Isso é normal.
- Descarte a tampa da agulha em um recipiente apropriado para objetos pontiagudos ou cortantes.
OBSERVAÇÃO: uma vez que a tampa da agulha tiver sido removida, a seringa67 deve ser utilizada imediatamente.
- Caso não seja usada dentro de 5 minutos, a seringa67 deve ser descartada em um recipiente apropriado para objetos pontiagudos ou cortantes e uma nova seringa67 deve ser utilizada.
- Nunca recoloque a tampa da agulha após sua remoção.
Sexto passo: administre a injeção69
- Segure a seringa67 confortavelmente em sua mão80.
- Para assegurar-se de que a agulha pode ser inserida corretamente sob a pele73, belisque uma prega de pele73 na área de injeção69 limpa com sua mão80 livre. Beliscar a pele73 é importante para garantir que você está injetando sob a pele73 (no tecido adiposo82), e não mais profundamente (no músculo). Injeção69 no músculo pode resultar em uma injeção69 desconfortável.
- Não segure ou empurre o êmbolo75 enquanto estiver inserindo a agulha na pele73.
- Insira a agulha até o fim na prega de pele73 em um ângulo entre 45° e 90° com um movimento rápido e firme.
É importante escolher o ângulo correto para garantir que o medicamento seja injetado sob a pele73; do contrário, a injeção69 pode ser dolorosa e o medicamento pode não funcionar.
- Então mantenha a seringa67 na posição e solte a prega de pele73.
- Injete lentamente todo o medicamento empurrando suavemente o êmbolo75 até o fim (vide Fig. F). Você deve pressionar o êmbolo75 até o final para garantir que esteja recebendo a dose completa do medicamento e para garantir que o gatilho esteja completamente afastado para o lado. Se o êmbolo75 não estiver completamente pressionado, o revestimento da agulha não se estenderá para cobrir a agulha quando ela for removida. Caso a agulha não esteja coberta, proceda com cautela e coloque a seringa67 em um recipiente apropriado para objetos pontiagudos, para evitar ferimentos com a agulha.
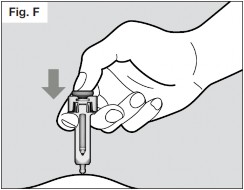
- Uma vez que o êmbolo75 estiver totalmente pressionado, continue pressionando-o para ter certeza de que todo o medicamento foi injetado antes de retirar a agulha da pele73.
- Continue pressionando o êmbolo75 enquanto você retira a agulha da pele73 no mesmo ângulo que o de inserção. (Vide Fig. G).
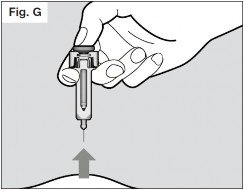
- Uma vez que a agulha tiver sido removida completamente da pele73, você pode liberar o êmbolo75, permitindo que o revestimento da agulha a proteja. (Vide Fig. H)
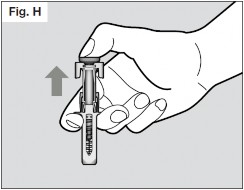
- Caso você veja gotas de sangue7 no local da injeção69, você pode pressionar uma bola de algodão ou gaze estéril sobre o local da injeção69 por, aproximadamente, 10 segundos.
- Não esfregue o local da injeção69.
Sétimo passo: descarte a seringa67
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
É muito importante o uso de Actemra® SC exatamente como prescrito por seu médico. Mantenha o controle de sua próxima dose.
Se você perder a sua dose semanal no prazo de sete dias, não aplique-a assim que se lembrar. Aguarde até o próximo dia programado.
Se você estiver utilizando Actemra® SC em semanas alternadas (em caso de modicações de dose sugeridas pelo seu médico) e perder a sua dose quinzenal no prazo de sete dias, aplique uma dose assim que se lembrar e aplique a sua próxima dose no dia regular previsto.
Se você perder a sua dose semanal ou quinzenal por mais que sete dias ou não tiver certeza de quando utilizar Actemra® SC, contate o seu médico.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Estudos clínicos
O perfil de segurança nesta seção foi baseada em 4458 pacientes expostos a tocilizumabe em estudos clínicos; a maior parte desses pacientes estava participando de estudos sobre AR (n = 4009), enquanto que o restante da experiência vem de estudos sobre pAIJ (n = 188), sAIJ (n = 112) e ACG (n = 149). O perfil de segurança de tocilizumabe nessas indicações continua semelhante e não diferenciada.
Artrite reumatoide2
A segurança de tocilizumabe subcutâneo8 na AR foi avaliada no estudo (SC-I). O estudo comparou a eficácia e segurança de tocilizumabe 162 mg administrado por via subcutânea1 semanalmente versus 8 mg/kg de tocilizumabe administrado por via intravenosa, em 1.262 indivíduos adultos com AR. Todos os pacientes do estudo receberam DMARD(s) não biológicos. A segurança e a imunogenicidade observadas para tocilizumabe administrado por via SC foi consistente com o perfil de segurança conhecido de tocilizumabe administrado por via IV, e nenhuma nova ou inesperada reação adversa foi observada. A maior frequência de reação no local da aplicação foi observada para Actemra® SC.
Arterite de Células Gigantes3
A segurança de tocilizumabe subcutâneo8 foi estuada em um estudo Fase III (WA28119) incluindo 251 pacientes com ACG. A duração total em pacientes anos na população total exposta foi de 138,5 pacientes anos durante a fase de 12 meses duplo-cega controlada com placebo9 do estudo. O perfil de segurança total observado nos grupos de tratamento com tocilizumabe foi compatível com o perfil de segurança conhecido de tocilizumabe. A taxa de eventos de infecção12 / infecção12 grave foi equilibrada entre os grupos de tocilizumabe semanal (200,2/9,7 eventos por 100 pacientes-anos) versus placebo9 mais 26 semanas de redução gradual de prednisona (156,0/4,2 eventos por 100 pacientes-anos) e placebo9 mais 52 semanas de redução gradual (210,2/12,5 eventos por 100 pacientes-anos).
Reações no local de aplicação
Nos estudos de Actemra® SC, as reações no local de aplicação (que incluem vermelhidão, prurido83, dor e hematoma84) foram leves a moderadas em gravidade. A maioria foi resolvida, sem nenhum tratamento, e nenhuma necessitou suspensão da medicação.
Imunogenicidade
No SC-I, 625 pacientes tratados com 162 mg de tocilizumabe semanalmente foram testados quanto à presença de anticorpos61 antitocilizumabe nos estudos controlados de 6 meses. Cinco pacientes (0,8%) desenvolveram anticorpos61 antitocilizumabe positivos; desses, todos desenvolveram anticorpos61 neutralizantes.
Um total de 1.454 pacientes expostos a tocilizumabe SC foi testado para anticorpos61 antitocilizumabe, 13 pacientes (0,9%) desenvolveram anticorpos61 antitocilizumabe positivos, e, desses, 12 pacientes (0,8%) desenvolveram anticorpos61 neutralizantes antitocilizumabe.
Nenhuma correlação entre o desenvolvimento de anticorpos61 e resposta clínica ou eventos adversos foi observada.
Os principais efeitos colaterais85 ocorridos durante o tratamento com tocilizumabe foram:
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam esse medicamento): infecções11 de vias aéreas superiores.
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam esse medicamento): celulite86 (inflamação5 dos tecidos abaixo da pele73), pneumonia25, herpes simples oral (tipo de erupção87 com vesículas88 causada por vírus35), herpes-zóster (reativação do vírus35 da varicela89 em uma raiz nervosa, provocando dor geralmente intensa e vesículas88 na pele73 da região correspondente àquele nervo, popularmente conhecido como “cobreiro”), dor na região da barriga, ulcerações90 na boca91 (aftas), gastrite92, erupções (nome genérico para lesões93 de pele73, geralmente avermelhadas), coceira, urticária94 (erupção87 cutânea95, com coceira, caracterizada por placas96 salientes), dor de cabeça97, tonturas98, aumento de enzimas do fígado34, aumento da pressão sanguínea, leucopenia99 e neutropenia43 (redução dos glóbulos brancos no sangue7), aumento de colesterol52, aumento de peso, edema100 periférico, reações alérgicas, reações no local da aplicação, tosse, falta de ar e conjuntivite101.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam esse medicamento): diverticulite13 (inflamação5 do intestino delgado14 ou grosso), estomatite102 (aftas), úlcera gástrica103, aumento da bilirrubina104 total (pigmento produzido pelo fígado34 a partir da hemoglobina105 e que pode se acumular em casos de lesão74 do próprio fígado34 ou das vias biliares106 por onde é eliminado), aumento de triglicérides53 (tipo de gordura51 dosada no sangue7), nefrotilíase (condição na qual um ou mais cálculos estão presentes na pélvis ou nos cálices do rim107 ou no ureter108), hipotireoidismo109 (diminuição da função da tireoide110).
Artrite reumatoide2 inicial – não tratado previamente com metotrexato
O perfil de segurança global observado nos pacientes com artrite reumatoide2 inicial, moderada a grave, que não haviam recebido tratamento prévio com MTX e agentes biológicos e que foram tratados com Actemra®, foi consistente com o perfil de segurança conhecido para tocilizumabe.
Alterações laboratoriais
As alterações em exames laboratoriais encontradas nos estudos clínicos referem-se a alterações de células sanguíneas111 (número baixo de plaquetas47 e de neutrófilos45), do figado34 (elevação de enzimas do fígado34) e dos parâmetros lipídicos (elevação de colesterol52 total, LDL54, HDL112, triglicérides53). Seu médico avaliará as possíveis alterações laboratoriais.
Pós-comercialização
O perfil de segurança no período pós-comercialização da formulação intravenosa é consistente com os dados dos estudos clínicos, com exceção de relatos de anafilaxia30 fatal durante o tratamento com tocilizumabe intravenoso. Síndrome de Stevens-Johnson113 (tipo de reação alérgica29, com descamação114 da pele73 e mucosas115 e formação de bolhas) tem sido relatada durante o tratamento com a formulação intravenosa de tocilizumabe.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
Atenção: este produto é um medicamento que possui nova indicação terapêutica116 no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidas. Nesse caso, informe seu médico.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Os dados disponíveis sobre superdose com Actemra® SC são limitados. Um caso de superdose acidental foi relatado em um paciente com mieloma117 múltiplo (câncer118 de um dos tipos de células48 do sangue7, os plasmócitos, em que podem ocorrer também lesões93 nos ossos) que recebeu uma dose única de 40 mg/kg IV. Apesar da dose elevada, não foram observados efeitos colaterais85.
Não foram observados efeitos colaterais85 graves ao medicamento em voluntários saudáveis que receberam dose única de até 28 mg/kg IV. Nesses indivíduos, observou-se queda do número de glóbulos brancos, que foi limitante da dose.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.0100.0655
Farm. Resp.: Tatiana Tsiomis Díaz - CRF-RJ nº 6942
Fabricado por
Vetter Pharma-Fertigung GmbH & Co. KG, Ravensburg, Alemanha
Embalado por
F. Hoffmann-La Roche Ltd., Kaiseraugst, Suíça
Importado por:
Produtos Roche Químicos e Farmacêuticos S.A.
Est. dos Bandeirantes, 2.020 – CEP 22775-109 – Rio de Janeiro – RJ
CNPJ: 33.009.945/0023-39
SAC 0800 7720 289






