Prelone (Solução oral) (Bula do profissional de saúde)
Aché Laboratórios Farmacêuticos S.A
DENTIFICAÇÃO DO MEDICAMENTO
Prelone
fosfato sódico de prednisolona
Solução oral 3 mg/ml
APRESENTAÇÕES
Frasco com 60 ml + pipeta dosadora em ml
Frasco com 120 ml + pipeta dosadora em ml
USO ORAL
USO ADULTO E PEDIÁTRICO
COMPOSIÇÃO
Cada ml de Prelone solução oral contém:
| fosfato sódico de prednisolona (equivalente a 3 mg de prednisolona) | 4,02 mg |
| excipiente q.s.p. | 1 ml |
Excipientes: aroma de cereja, ciclamato de sódio, edetato dissódico di-hidratado, fosfato de sódio monobásico monoidratado, fosfato de sódio dibásico dodecaidratado, metilparabeno, sacarina1 sódica di-hidratada, sorbitol2 e água purificada.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE3
INDICAÇÕES
Prelone é indicado como agente anti-inflamatório e imunossupressor4 em patologias cujos mecanismos fisiopatológicos envolvam processos inflamatórios e/ou autoimunes5; para o tratamento de condições endócrinas; e em composição de esquemas terapêuticos em algumas neoplasias6:
Distúrbios Endócrinos:
Insuficiência7 adrenocortical primária ou secundária (sendo que corticosteroides naturais como cortisona ou hidrocortisona são de primeira escolha). Análogos sintéticos podem ser utilizados em conjunto com mineralocorticoides, quando necessário (na infância a suplementação8 de mineralocorticoides é especialmente importante); hiperplasia9 adrenal congênita10; tireoidite não-supurativa; hipercalcemia associada ao câncer11.
Distúrbios Reumáticos:
Como terapia adjuvante para administração a curto prazo (para reverter paciente em episódio agudo12 ou exacerbado) em: artrite13 psoriática, artrite reumatoide14, incluindo artrite reumatoide14 juvenil (em casos particulares serão utilizadas terapias de manutenção de baixas doses); espondilite anquilosante; bursite15 aguda e subaguda16; tenossinovite aguda inespecífica; artrite13 gotosa aguda; osteoartrite17 pós-traumática; sinovites osteoartríticas; epicondilites.
Colagenoses:
Durante exacerbação ou como terapia de manutenção em casos particulares de lúpus18 eritematoso19 sistêmico20, cardite reumática aguda.
Doenças Dermatológicas:
Pênfigo; dermatite21 herpetiforme bolhosa; eritema multiforme22 grave (Síndrome de Stevens-Johnson23); dermatite21 esfoliativa; micoses fungoides; psoríase24 grave; dermatite21 seborréica grave.
Estados Alérgicos:
Controle de condições alérgicas graves ou incapacitantes refratárias25 aos meios adequados de tratamentos convencionais; rinite26 alérgica perene ou sazonal; dermatite21 de contato; dermatite21 atópica; doenças do soro27; reações de hipersensibilidade a drogas.
Doenças Oftálmicas:
Processos inflamatórios e alérgicos agudos e crônicos graves: envolvendo o olho28 e seus anexos29 como úlceras30 marginais alérgicas da córnea31; herpes zoster32 oftálmico; inflamação33 do segmento anterior; coroidite e uveíte34 posterior difusa; oftalmia simpática; conjuntivite35 alérgica; ceratite; coriorretinite; neurite36 óptica; irites e iridociclites.
Doenças Respiratórias:
Sarcoidose37 sintomática38; Síndrome39 de Löefler não-tratável por outros meios; beriliose40; tuberculose41 pulmonar fulminante ou disseminada quando usado concomitantemente à quimioterapia42 antituberculose apropriada; pneumonite43 por aspiração; asma44 brônquica.
Distúrbios Hematológicos:
Púrpura45 trombocitopênica idiopática46 em adultos; trombocitopenia47 secundária em adultos; anemia hemolítica48 adquirida (autoimune49); eritroblastopenia (anemia50 eritrocítica); anemia50 hipoplásica congênita10 (eritroide).
Doenças Neoplásicas51:
Para o tratamento paliativo52 de leucemia53 e linfomas em adultos; leucemia53 aguda infantil.
Estados Edematosos:
Para indução de diurese54 ou remissão da proteinúria55 na síndrome nefrótica56 idiopática46 ou devida ao lúpus18 eritematoso19, sem uremia57.
Doenças Gastrintestinais:
Manutenção do paciente após um período crítico da doença em colite58 ulcerativa e enterite regional.
Doenças Neurológicas:
Exacerbações agudas da esclerose múltipla59.
RESULTADOS DE EFICÁCIA
Foram compilados resultados do tratamento de todas as crianças com anemia50 de Diamond-Blackfan registradas na Sociedade Japonesa de Hematologia Pediátrica entre 1988 e 1998. Cinquenta e quatro crianças foram identificadas. O tratamento de 1a linha instituído para todas as crianças foi a prednisolona (2 mg/kg/dia); em 17 crianças, houve necessidade de iniciar tratamento com ciclosporina A (CsA). A probabilidade de remissão sem necessidade de medicamento foi significantemente maior para as crianças tratadas somente com prednisolona em comparação com aquelas que necessitaram uso de CsA.
Foram randomizados 359 pacientes pediátricos com leucemia53 linfoblástica aguda (LLA) para receber prednisolona (60 mg/m² na indução e 40 mg/m² nas intensificações) ou dexametasona (8 mg/m² na indução e 6 mg/m² nas intensificações). A sobrevida60 livre de eventos após 8 anos de seguimento foi de 81,1 ±3,9% para a dexametasona e 84,4 ±5,2% para a prednisolona, no grupo de risco61 básico (P=0,217), e de 84,9 ±4,6% para a dexametasona e 80,4 ±5,1% para a prednisolona, no grupo de risco61 intermediário (P=0,625). Embora o número absoluto de pacientes que apresentaram toxicidade62 grave tenha sido maior no grupo dexametasona, não se observou diferença estatisticamente significativa.
Estudo avaliou a eficácia e a segurança de um esquema de 6 ciclos (repetidos a cada 21 dias) com mitoxantrona (14 mg/m²; D1), clorambucil (10 mg/d; D1 a D10 e prednisolona (25 mg/m²; D1 a D10) no tratamento de 130 portadores de linfoma63 não-Hodgkin (LNH) (88 com baixo grau e 42 com alto grau). No grupo de LNH de baixo grau, observou-se 86% de resposta (50%, resposta completa; 36%, resposta parcial), e no grupo de alto grau, a taxa de resposta foi de 64% (33%, resposta completa; 31%, resposta parcial). A toxicidade62 foi considerada baixa.
O esquema de melfalano com prednisolona (MP) foi comparado com a associação de mitoxantrona, vincristina e prednisolona (NOP) em um estudo fase III envolvendo 151 portadores de mieloma64 múltiplo (MM). No esquema MP, a dose de prednisolona usada foi de 100-200 mg/dia, do D1 ao D4, repetidos a cada 4 semanas, e no esquema NOP a dose de prednisolona foi de 250 mg do D1 ao D4 e do D17 ao D20. Os dois esquemas estavam programados para serem repetidos por até 1 ano. A taxa de resposta nos pacientes tratados com MP e NOP foram de 60% e 64% (P =NS) e o tempo para progressão foi de 16 meses (IC95%, 14-51 meses) e 21 meses (IC95%, 15-27 meses; P =NS), respectivamente. A mediana da sobrevida60 foi superior nos pacientes tratados com MP (31 meses [IC95%, 21-43 meses] vs. 14 meses [IC95%, 7-21 meses]; P =0,02), indicando superioridade do esquema MP.
Foram comparados dois esquemas de prednisolona oral no tratamento da púrpura45 trombocitopênica idiopática46 (PTI): dose baixa (0,5 mg/kg/dia) e dose convencional (1,0 mg/kg/dia). Cinquenta e nove pacientes adultos foram randomizados para cada um dos tratamentos, não se observando diferença estatística para as taxas de remissão entre os grupos (35% no grupo “dose baixa” e 39% no grupo “dose convencional”). Entretanto, o tempo médio de hospitalização foi menor no grupo “dose baixa” (20 dias vs. 50 dias; P < 0,001). Em conclusão, o tratamento da PTI com prednisolona oral em dose baixa tem a mesma eficácia da dose alta, mas se associa a menor tempo de permanência intra-hospitalar.
A prednisolona foi comparada com outros corticosteroides no tratamento da artrite reumatoide14 (AR). Foi conduzido estudo com 142 pacientes para comparar, durante 12 semanas, a prednisolona (7,5 mg/dia) com budesonida em cápsulas de liberação ileal (3 mg ou 9 mg) e placebo65. A prednisolona e a budesonida 9 mg tiveram eficácia semelhante na melhora da artrite13, resposta esta que teve magnitude superior ao placebo65 e à budenosida 3 mg. O critério de resposta ACR20 foi atingido em 25% dos pacientes tratados com placebo65, 22% com budesonida 3 mg, 42% com budesonida 9 mg e 56% com prednisolona 7,5 mg. Eventos adversos atribuíveis aos glicocorticoides foram semelhantes nos grupos tratados com os mesmos. Não se observou rebote dos sintomas66 após a suspensão dos tratamentos.
Foi observada melhora nas seguintes variáveis após tratamento com prednisolona (na dose de 0,4 mg/kg/dia) durante 10 dias, em comparação com o placebo65 em pacientes com artrite reumatoide14 juvenil: grau de fraqueza muscular; fadiga67; avaliação subjetiva global; avaliação global pelo médico; índices articulares de articulações68 comprometidas.
Foram comparados dois esquemas de corticosteroides para o tratamento da crise asmática: 65 pacientes adultos foram randomizados para tratamento parenteral (hidrocortisona, 100 mg IV a cada 6 horas por 72 horas) ou oral (prednisolona, 100 mg VO uma vez ao dia por 72 horas). Todos os pacientes receberam corticosteroides inalatórios e broncodilatadores69. Observou-se melhora significativa dos sintomas66 e do pico de fluxo expiratório (PEF) nos dois braços de tratamento, sem que houvesse diferença entre eles. A tolerabilidade também foi igual nos dois grupos, indicando que a prednisolona é uma alternativa eficaz e segura à corticoterapia parenteral no tratamento da exacerbação asmática em adultos.
Estudo duplo-cego70 controlado com placebo65 avaliou o impacto clínico e radiológico de um tratamento curto com prednisolona em pacientes com polipose nasal. Quarenta pacientes foram randomizados para prednisolona (50 mg/dia por 14 dias) ou placebo65. A eficácia do tratamento foi avaliada pela avaliação médica, questionário de sintomas66, rinoscopia e ressonância magnética71 (RM). Ao final de duas semanas, observou-se melhora dos sintomas66 nasais somente nos pacientes tratados com prednisolona, e tanto a MR quanto a rinoscopia mostraram redução do tamanho dos pólipos72 somente após o corticosteroide. O tratamento com prednisolona foi bem tolerado, sendo a insônia o único evento adverso relatado com frequência superior ao grupo placebo65.
Resultados positivos foram obtidos em um estudo tailandês com 105 pacientes randomizados para prednisolona (50 mg/dia) ou placebo65 durante 14 dias. A resposta clínica foi avaliada pelo escore de sintomas66 nasais, índice de pico de fluxo e escore de pólipos72 nasais. Além disso, foi realizada rinoscopia e exames radiográficos para avaliar o tamanho dos pólipos72. Observou-se melhora clínica e redução do tamanho dos pólipos72 apenas nos pacientes tratados com prednisolona (P<0,001 para todas as variáveis). A presença de pólipos72 grau 3 ou superior foi um preditor de menor resposta ao tratamento.
Um estudo controlado com placebo65 conduzido na Turquia avaliou a associação de prednisolona (20 mg, duas vezes ao dia) nos primeiros 40 dias de tratamento com esquema antituberculoso em pacientes HIV73-negativos com TBP. Em comparação com o grupo placebo65, os pacientes tratados com o corticosteroide apresentaram resolução mais rápida da febre74, maior ganho de peso corporal, maior elevação da albumina75 sérica, melhora radiológica e negativação do escarro mais rápida e menor tempo de permanência no hospital. Nenhum evento adverso significativo foi observado.
Foram acompanhados 280 pacientes com sarcoidose37 pulmonar estágios I e II, sem manifestações extrapulmonares, que foram randomizados para tratamento com prednisolona por 6 meses, 12 meses ou para observação somente. A dose de prednisolona prescrita foi de 40 mg/dia, com redução gradual de 5 mg a cada semana até a dose de manutenção de 10 mg/dia. Observou-se regressão radiológica mais significativa nos pacientes tratados com prednisolona.
Foram comparadas duas estratégias anti-inflamatórias em 40 pacientes com uveíte34 que seriam submetidos a facoemulsificação e implante76 de lente acrílica intraocular: grupo 1, dose única de metilprednisolona IV (15 mg/kg), 30 minutos antes da cirurgia; grupo 2, prednisolona VO (0,5 mg/kg/dia), iniciada duas semanas antes da cirurgia, com desmame gradual após o procedimento. A flarefotometria (que mede o número de partículas em suspensão no humor aquoso77) mostrou maior aumento no número do “flare” e de células78 na câmara anterior79 nos pacientes que receberam o corticosteroide IV, em comparação com a prednisolona VO, indicando que o último foi mais eficaz em preservar a integridade da barreira hemato-aquosa.
Foi avaliado se o prolongamento da corticoterapia além das 8 semanas do esquema convencional poderia diminuir a taxa de recidivas80. Quarenta e cinco crianças no primeiro episódio de SNI foram randomizadas para o tratamento convencional de 8 semanas ou tratamento prolongado de 16 semanas (2,0 mg/kg/dia por 4 semanas → 1,5 mg/kg/dia por 4 semanas → 1,5 mg/kg em dias alternados por 4 semanas → 1,0 mg/kg em dias alternados por 4 semanas). O tempo até a primeira recidiva81 foi maior nos pacientes tratados com o esquema prolongado (média, 222,2 dias; mediana, 120 dias) em comparação com o esquema convencional (média, 134,3 dias; mediana, 96,5 dias). A porcentagem de pacientes sem recidivas80 6 e 12 meses após a interrupção do corticosteroide foi de 40,9% e 27,3%, para o tratamento prolongado e 21,7% e 8,7% para o tratamento convencional, respectivamente.
Foi comparada a budesonida oral com a prednisolona no tratamento da colite58 ulcerativa, em 72 pacientes, durante 9 semanas. A dose utilizada de prednisolona foi de 40 mg/dia, com desmame gradual. Observou-se equivalência dos dois tratamentos em relação ao escore endoscópico, mas em relação ao escore histopatológico, a prednisolona foi superior. Por ter baixa biodisponibilidade por via oral, a budesonida não interferiu na secreção endógena de cortisol, ao contrário da prednisolona.
Referências:
Ohga, S. et al. Diamond-Blackfan anemia50 in Japan: clinical outcomes of prednisolone therapy and hematopoietic stem cell transplantation. International Journal of Hematology. v. 79, p. 22-30, 2004. Igarashi, S. et al. No advantage of dexamethasone over prednisolone for the outcome of standard- and intermediate-risk childhood acute lymphoblastic leukemia in the Tokyo Children's Cancer11 Study Group L95-14 protocol. Journal of the American Society of Clinical Oncology, v. 23, p. 6489-6498, 2005. Bernard, T. et al. Mitoxantrone, chlorambucil and prednisolone in the treatment of non-Hodgkin's lymphoma. Leukemia & Lymphoma, v. 15, p. 481-485, 1994.
Keldsen, N. et al. Multiple myeloma treated with mitoxantrone in combination with vincristine and prednisolone (NOP regimen) versus melphalan and prednisolone: a phase III study. Nordic Myeloma Study Group (NMSG). European Journal of Hematology, v. 51, p. 80-85, 1993.
Ohmine, K. et al. Low-dose prednisolone therapy for idiopathic thrombocytopenic purpura45. Rinsho Ketsueki. The Japanese journal of Clinical Hematology, v. 41, p. 8-11, 2000.
Kirwan, J.R. et al. A randomised placebo65 controlled 12 week trial of budesonide and prednisolone in rheumatoid arthritis. Annals of the rheumatic diseases, v. 63, p. 688-695, 2004.
Wallace, C.A. et al. Trial of early aggressive therapy in polyarticular juvenile idiopathic arthritis. Arthritis and Rheumatism, v. 64, p. 2012-2021, 2012.
Dembla, G. et al. Oral versus intravenous steroids in acute exacerbation of asthma--randomized controlled study. The Journal of the Association of Physicians of India, v. 59, p. 621-623, 2011.
Hissaria, P. et al. Short course of systemic corticosteroids in sinonasal polyposis: a double-blind, randomized, placebo65-controlled trial with evaluation of outcome measures. The Journal of Allergy and Clinical Immunology, v. 118, p.128-133, 2006.
Kirtsreesakul, V. et al. Clinical efficacy of a short course of systemic steroids in nasal polyposis. Rhinology, v. 49, p. 525-532, 2011.
Bilaceroglu, S. et al. Prednisolone: a beneficial and safe adjunct to antituberculosis treatment? A randomized controlled trial. The international journal of tuberculosis and lung disease. The Official Journal of the International Union against Tuberculosis and Lung Disease, v. 3, p. 47-54, 1999.
Eule, H. et al. Corticosteroid therapy of intrathoracic sarcoidosis stages I and II--results of a controlled clinical trial. Zeitschrift fur Erkrankungen der Atmungsorgane 149, 142-147, 1977.
Meacock, W.R. et al. Steroid prophylaxis in eyes with uveitis undergoing phacoemulsification. The British Journal of Ophthalmology, v. 88, p. 1122-1124, 2004.
Bagga, A. et al. Prolonged versus standard prednisolone therapy for initial episode of nephrotic syndrome. Pediatric Nephrology, v. 13, p. 824-827, 1999.
Lofberg, R. et al. Oral budesonide versus prednisolone in patients with active extensive and left-sided ulcerative colitis. Gastroenterology, v. 110, p. 1713-1718, 1996.
CARACTERÍSTICAS FARMACOLÓGICAS
A prednisolona é rapidamente absorvida pelo trato gastrintestinal quando administrada oralmente. A ligação da prednisolona às proteínas82 plasmáticas é de 70 a 90% e sua meia-vida é de 2 a 4 horas. A metabolização é hepática83 e é excretada na urina84 como conjugados de sulfato e glicuronídeos.
A prednisolona é um análogo sintético adrenocorticosteroide; é um esteroide sob a forma de álcool livre ou esterificado85, com propriedades predominantes dos glicocorticoides. Pode reproduzir alguns efeitos dos glicocorticoides endógenos, mas após a administração de altas doses terapêuticas podem surgir efeitos que necessariamente não se assemelham aos dos hormônios adrenocorticais.
A prednisolona pode causar alguns efeitos metabólicos baseados em sua propriedade glicocorticoide: estímulo da gliconeogênese86; aumento do depósito de glicogênio87 no fígado88; inibição da utilização da glicose89; diminuição da tolerância a carboidratos; atividade anti-insulínica; aumento do catabolismo90 proteico; aumento da lipólise; estímulo da síntese e armazenamento de gordura91; aumento da taxa de filtração glomerular (aumento na excreção urinária de urato sem alteração na excreção de creatinina92); excreção aumentada de cálcio.
A produção de eosinófilos93 e linfócitos é diminuída e há estímulo da eritropoiese94 e da produção de leucócitos polimorfonucleares95. Há inibição dos processos inflamatórios (edema96, deposição de fibrina97, dilatação capilar98, migração de leucócitos99 e fagocitose100), e de estágios tardios da cicatrização (proliferação capilar98, deposição de colágeno101 e cicatrização).
Com o uso de prednisolona, a corticotrofina tem a sua produção inibida e isso leva à supressão da produção de corticosteroides andrógenos102. Pode haver alguma atividade mineralocorticoide103, ocorrendo estímulo da perda de potássio intracelular e entrada de sódio nas células78. Esse efeito é evidente nos rins104, e pode levar ao aumento da retenção de sódio e à hipertensão105.
CONTRAINDICAÇÕES
Este medicamento é contraindicado para uso por pacientes alérgicos à prednisolona ou a qualquer outro componente da fórmula; e para pacientes106 com infecções107 fúngicas108 sistêmicas ou infecções107 não controladas.
ADVERTÊNCIAS E PRECAUÇÕES
Em pacientes sob terapia com corticosteroides submetidos a situações incomuns de estresse (trauma, cirurgia, etc.), recomenda-se que a dosagem de corticosteroides seja aumentada rapidamente, antes, durante e após a situação estressante.
Os corticosteroides podem mascarar alguns sinais109 de infecção110 e novas infecções107 podem aparecer durante o tratamento.
Durante o uso de corticosteroides pode haver diminuição da resistência e dificuldade na localização de infecções107.
O uso prolongado de corticosteroides pode produzir catarata111 subcapsular posterior, glaucoma112 com possível lesão113 dos nervos ópticos e pode aumentar a ocorrência de infecções107 secundárias oculares devido a fungos e viroses.
Doses médias e elevadas de hidrocortisona e cortisona podem causar elevação da pressão arterial114, retenção de sódio e água e aumento da excreção de potássio. Esses efeitos ocorrem menos frequentemente com os derivados sintéticos, a não ser quando utilizados em altas doses.
Altas doses de corticosteroides, bem como doses habituais, podem causar elevação da pressão arterial114, retenção de sal e água e aumento da excreção de potássio. Todos os corticosteroides aumentam a excreção de cálcio. Considerar a possibilidade de dieta hipossódica e suplementação8 de potássio, quando os corticosteroides forem utilizados.
Quando em terapia com corticosteroides, os pacientes não devem ser vacinados contra varíola. Outras imunizações não devem ser feitas em pacientes sob corticoterapia, especialmente em altas doses, devido aos possíveis riscos de complicações neurológicas e a ausência de resposta imune.
Crianças e adultos sob terapia imunossupressora são mais sensíveis a infecções107 do que indivíduos saudáveis. Varicela115 e sarampo116, por exemplo, podem ter um curso mais grave e até fatal em crianças e adultos não-imunes sob corticoterapia. Em crianças e adultos que não tiveram infecções107 causadas por esses agentes, deve-se ter o cuidado especial de evitar a exposição aos mesmos. Desconhece-se como a dose, via e duração de administração de corticosteroides podem afetar o risco de desenvolvimento de infecção110 disseminada. A contribuição da causa da doença e/ou tratamento prévio com corticosteroides a este risco também é desconhecida. Se o paciente for exposto à varicela115, pode ser indicada a profilaxia com imunoglobulina117 específica para varicela115. Se o paciente for exposto ao sarampo116, pode ser indicada a profilaxia com pool de imunoglobulinas118 intramuscular. Caso ocorra o desenvolvimento da varicela115, deve-se considerar o tratamento com agentes antivirais.
Medicamentos imunossupressores podem ativar focos primários de tuberculose41. Os médicos que acompanham pacientes sob imunossupressão119 devem estar alertas quanto à possibilidade de surgimento de doença ativa, tomando, assim todos os cuidados para o diagnóstico120 precoce e tratamento.
O uso de prednisolona em tuberculose41 ativa deve ser restrito a casos de tuberculose41 fulminante ou disseminada, nas quais o corticosteroide é usado para o controle da doença associado a um regime antituberculoso apropriado.
Quando os corticosteroides forem indicados a pacientes com tuberculose41 latente ou com reatividade à tuberculina é necessária rigorosa observação, pois pode haver reativação da doença. Durante corticoterapia prolongada, estes pacientes devem receber quimioprofilaxia.
As crianças que utilizam esteroides, em longo prazo, devem ser cuidadosamente observadas em relação ao aparecimento de reações adversas graves potenciais, como: obesidade121, retardo no crescimento, osteoporose122 (diminuição da densidade óssea) e supressão adrenal.
Há risco de insuficiência7 adrenal em função de retirada súbita do fármaco123 após terapia prolongada, podendo ser evitada mediante redução gradativa da dose.
Em casos de insuficiência7 adrenocortical induzida por prednisolona, pode-se minimizar o quadro por redução gradual da dosagem. Devido à possibilidade de persistência desse quadro após a interrupção do tratamento por algum tempo, pode ser necessário reiniciar a corticoterapia em situações de estresse. Como a secreção de mineralocorticoide103 pode estar reduzida, deve-se administrar concomitantemente sais ou mineralocorticoides.
Nos pacientes com insuficiência hepática124, pode ser necessária uma redução da dose. No tratamento de doenças hepáticas125 crônicas ativas com prednisolona, as principais reações adversas, como: fratura126 vertebral, hiperglicemia127, diabete, hipertensão105, catarata111 e síndrome de Cushing128, ocorreram em cerca de 30% dos pacientes.
Em pacientes portadores de hipotireoidismo129 ou com cirrose130, existe aumento do efeito do corticosteroide. Pacientes portadores de herpes simples ocular devem utilizar corticosteroides com cautela pois pode haver possível perfuração de córnea31.
A menor dose possível de corticosteroide deve ser utilizada a fim de se controlar as condições sob tratamento. Quando a redução da dosagem for possível, esta deve ser feita gradualmente.
Podem aparecer distúrbios psíquicos quando do uso de corticosteroides, variando desde euforia, insônia, alteração do humor, alteração de personalidade, depressão grave até manifestações de psicose131 ou instabilidade emocional. Tendências psicóticas preexistentes podem ser agravadas pelos corticosteroides.
Em hipoprotrombinemia, o ácido acetilsalicílico deve ser utilizado com cautela quando associado à corticoterapia.
Deve haver cuidado na utilização de esteroides em casos de colite58 ulcerativa não-específica, caso haja possibilidade de perfuração iminente (já que há risco de perfuração gastrointestinal), abscesso132 ou outras infecções107 piogênicas; diverticulite133; anastomoses134 de intestino; úlcera péptica135 ativa ou latente; insuficiência renal136; hipertensão105; osteoporose122 (diminuição da densidade óssea) e miastenia137 gravis.
O crescimento e desenvolvimento de crianças sob corticoterapia prolongada devem ser observados cuidadosamente.
Embora estudos clínicos controlados tenham demonstrado a efetividade dos corticosteroides em aumentar a rapidez da resolução do problema das exacerbações agudas da esclerose múltipla59, eles não demonstraram que os corticosteroides afetam o resultado final do histórico natural da doença. Os estudos mostram que doses relativamente maiores de corticosteroides são necessárias para alcançar um efeito significativo.
Pressão arterial114, peso corporal, dados rotineiros de laboratório, incluindo glicose89 pós-prandial de 2 horas e potássio sérico, raio-x de tórax138 e partes superiores devem ser obtidos a intervalos regulares.
Gravidez139 e Lactação140
Como estudos adequados de reprodução141 humana não foram feitos com corticosteroides, o uso de prednisolona na gravidez139, lactação140 ou em mulheres com potencial de engravidar, requer que os possíveis benefícios da droga justifiquem o risco potencial para a mãe, embrião ou feto142.
Categoria de risco na gravidez139: C – Não há estudos adequados em mulheres. Em experiências animais ocorreram alguns efeitos colaterais143 no feto142, mas o benefício do produto pode justificar o risco potencial durante a gravidez139.
Lactação140: a prednisolona é excretada no leite materno em baixos níveis (menos de 1% da dose administrada). Medidas de cautela devem ser tomadas quando a prednisolona é administrada a lactantes144.
Recém-nascidos e crianças de mães que receberam doses altas de corticosteroides, durante a gravidez139, devem ser observados quanto a sinais109 de hipoadrenalismo.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
INTERAÇÕES MEDICAMENTOSAS
Interação Medicamento-Medicamento:
Severidade maior
- Efeito da interação: risco de ulceração145 gastrintestinal ou hemorragia146 pode ser aumentado quando estas substâncias são utilizadas concomitantemente com glicocorticoides, entretanto o uso concomitante de anti-inflamatórios não-esteroidais no tratamento de artrite13 deve promover benefício terapêutico aditivo e permitir redução de dosagem de glicocorticoide.
- Medicamento: Álcool ou drogas anti-inflamatórias não-esteroidais
Severidade moderada
- Efeito da interação: o uso concomitante a longo prazo com glicocorticoides pode aumentar a pressão intraocular147.
- Medicamento: anticolinérgicos, especialmente atropina e compostos relacionados.
- Efeito da interação: os efeitos dos derivados cumarínicos ou da indandiona geralmente diminuem (mas podem aumentar em alguns pacientes), quando estes medicamentos são utilizados concomitantemente com glicocorticoides. Ajustes de dose baseados na determinação do tempo de protrombina148 podem ser necessários durante e após a terapia com glicocorticoide. O potencial de ocorrência de ulceração145 gastrintestinal ou hemorragia146 durante terapia com glicocorticoide e os efeitos dos glicocorticoides na integridade vascular149, podem apresentar-se aumentados em pacientes que recebem terapia com anticoagulante150 ou trombolítico.
- Medicamento: anticoagulantes151, derivados cumarínicos ou indandionas, heparina, estreptoquinase ou uroquinase.
- Efeito da interação: os glicocorticoides podem aumentar as concentrações de glicose89 no sangue152. Ajuste de dose de um ou ambos agentes pode ser necessário quando a terapia com glicocorticoide é descontinuada.
- Medicamento: agentes antidiabéticos, sulfonilureia ou insulina153.
- Efeito da interação: alterações na condição da tireoide154 do paciente podem ocorrer como um resultado de administração, alteração na dosagem ou descontinuação de hormônios da tireoide154 ou agentes antitireoidianos, podendo necessitar de ajuste de dosagem de corticosteroide, uma vez que a depuração metabólica de corticosteroides diminui em pacientes com hipotireoidismo129 e aumenta em pacientes com hipertireoidismo155. Os ajustes de dose devem ser baseados em resultados de testes de função da tireoide154.
- Medicamento: agentes antitireoidianos ou hormônios da tireoide154.
- Efeito da interação: estrogênios podem alterar o metabolismo156, levando à diminuição da depuração, aumentando a meia-vida de eliminação e aumentando os efeitos terapêuticos e toxicidade62 dos glicocorticoides. O ajuste de dose dos glicocorticoides pode ser requerido durante e após o uso concomitante.
- Medicamento: Estrogênios ou contraceptivos orais contendo estrogênios.
- Efeito da interação: o uso concomitante de glicocorticoides pode aumentar a possibilidade de arritmias157 ou toxicidade62 digitálica associada com hipocalemia158.
- Medicamento: glicosídios digitálicos.
- Efeito da interação: efeitos de natriuréticos e diuréticos159 podem diminuir as ações de retenção de sódio e fluidos de corticosteroides e vice-versa. O uso concomitante de diuréticos159 depletores de potássio com corticosteroides pode resultar em hipocalemia158. A monitoração da concentração de potássio sérico e função cardíaca é recomendada. Efeito de diuréticos159 no potássio excessivo e/ou corticosteroide nas concentrações de potássio sérico pode ser diminuído durante uso concomitante. A monitoração das concentrações de potássio sérico é recomendada.
- Medicamento: diuréticos159
- Efeito da interação: inibição do crescimento em resposta ao somatrem ou somatropina pode ocorrer com uso terapêutico crônico160 de doses diárias (por m2 de superfície corporal) que excedam 2,5 – 3,75 mg de prednisolona oral ou 1,25 - 1,88 mg de prednisolona parenteral. É recomendado que estas doses não sejam excedidas durante a terapia com somatrem ou somatropina. Se doses maiores forem necessárias, a administração de somatrem ou somatropina deve ser postergada.
- Medicamento: somatropina.
- Efeito da interação: drogas que induzem a atividade das enzimas metabólicas hepáticas125 da fração microssomal podem aumentar o metabolismo156 da prednisolona, requerendo, em terapias concomitantes, o aumento da dosagem de prednisolona.
- Medicamento: barbituratos e drogas indutoras enzimáticas.
Severidade menor
- Efeito da interação: glicocorticoides, especialmente prednisolona, podem aumentar o metabolismo156 hepático e/ou excreção de isoniazida, levando à diminuição das concentrações plasmáticas e eficácia da isoniazida, especialmente em pacientes que sofrem acetilação rápida. O ajuste de dose de isoniazida pode ser necessário durante e após o uso concomitante.
- Medicamento: isoniazida
Interação Medicamento – Exame laboratorial:
Severidade menor
- Efeito da interação: a prednisolona pode resultar em falso aumento dos níveis de digoxina.
- Medicamento: digoxina.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Conservar em temperatura ambiente (entre 15 e 30°C). Proteger da luz e umidade. Desde que respeitados os cuidados de armazenamento, o medicamento apresenta uma validade de 24 meses a contar da data de sua fabricação.
Número de lote e datas de fabricação e validade: vide embalagem. Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Prelone solução 3mg/mL é uma solução límpida, incolor, pouco viscosa com odor de cereja.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
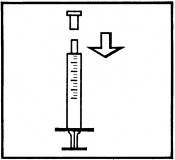
Instruções de uso da pipeta dosadora em ml:
- Encaixar a pipeta dosadora no adaptador do frasco (fig. 1).

- Virar o frasco e aspirar a medida desejada. Puxar cuidadosamente o êmbolo161, medindo a quantidade exata em ml (fig. 2).

- Retirar a pipeta dosadora (fig. 3).

- Esvaziar a pipeta dosadora lentamente na boca162, com a cabeça163 inclinada para trás (fig. 4).

- Tampar o frasco (fig. 5).

- Lavar bem a pipeta dosadora com água corrente e fechá-la com sua respectiva tampa (fig. 6).
Observações:
A pipeta dosadora é de uso exclusivo para administração de Prelone por via oral. O manuseio deve ser feito somente por adultos.
POSOLOGIA
ATENÇÃO: utilizar a pipeta exclusiva que acompanha o produto. esta pipeta está graduada de ml em ml. em caso de dúvida consulte seu médico (1 ml de solução equivale a 3 mg prednisolona. cada mg de prednisolona equivale a 1,34 mg de fosfato sódico de prednisolona).
A dosagem inicial de Prelone pode variar de 5 a 60 mg por dia, dependendo da doença específica que está sendo tratada. As doses de Prelone requeridas são variáveis e devem ser individualizadas de acordo com a doença em tratamento e a resposta do paciente. Para bebês164 e crianças, a dosagem recomendada deve ser controlada pela resposta clínica e não pela adesão estrita ao valor indicado pelos fatores idade e peso corporal. Iniciar a terapia com a menor dose da posologia em idosos.
A dosagem deve ser reduzida ou descontinuada gradualmente quando a droga for administrada por mais do que alguns dias.
Crianças: A dose pediátrica inicial pode variar de 0,14 a 2 mg/kg de peso por dia, ou de 4 a 60 mg por metro quadrado de superfície corporal por dia, administrados de 3 a 4 vezes por dia. Posologias para recém-nascidos e crianças devem ser orientadas segundo as mesmas considerações feitas para adultos, ao invés de se adotar rigidez estrita aos índices para idade ou peso corporal. Na Síndrome Nefrótica56 utiliza-se 60mg/m2/dia em 3 vezes ao dia por 4 semanas, seguidas de 40mg/m2 em dias alternados, por 4 semanas.
Em situações de menor gravidade, doses mais baixas, geralmente, são suficientes, enquanto que para alguns pacientes, altas doses iniciais podem ser necessárias. A dose inicial deve ser mantida ou ajustada até que a resposta satisfatória seja notada. Depois disso deve-se determinar a dose de manutenção por pequenos decréscimos da dose inicial a intervalos de tempo determinados, até que se alcance a dose mais baixa para se obter uma resposta clínica adequada. Deve-se ter em mente que é necessária uma constante observação em relação à dosagem de Prelone. Se por um período razoável de tempo não ocorrer resposta clínica satisfatória, o tratamento com Prelone deve ser interrompido e o paciente transferido para outra terapia apropriada.
Incluem-se as situações nas quais pode ser necessário ajuste na dose: mudança no estado clínico secundário por remissão ou exacerbação no processo da doença, a suscetibilidade individual do paciente à droga e o efeito da exposição do paciente a situações estressantes não-diretamente relacionadas à doença em tratamento; se for necessário que o tratamento seja interrompido, é recomendado que a retirada seja gradual e nunca abrupta.
REAÇÕES ADVERSAS
As reações adversas de Prelone têm sido do mesmo tipo das relatadas para outros corticosteroides e normalmente podem ser revertidas ou minimizadas com a redução da dose, sendo isto preferível à interrupção do tratamento com o fármaco123.
Ocorrem efeitos tóxicos com todas as preparações de corticosteroides e sua incidência165 eleva-se se a dose aumenta muito acima de 8 mg/dia de prednisolona ou seu equivalente.
Reações comuns (> 1/100 e < 1/10):
- Gastrintestinais: Aumento do apetite; indisgestão; úlcera péptica135 (ulceração145 do estômago166 e/ou duodeno167) com possível perfuração e hemorragia146; pancreatite168 e esofagite169 ulcerativa.
- Neurológicas: Nervosismo, fadiga67 e insônia.
- Dermatológicas: Reações alérgicas locais.
- Oftálmicas: Catarata111; glaucoma112 e exoftalmia. O estabelecimento de infecções107 secundárias por fungos ou vírus170 dos olhos171 pode também ser intensificado.
- Endócrinas: Redução da tolerância aos carboidratos (pré-diabetes172), manifestação de diabetes173 mellitus latente e aumento das necessidades de insulina153 ou hipoglicemiantes orais174 em diabéticos. O tratamento com doses elevadas de corticosteroides pode induzir o aumento acentuado dos triglicérides175 no sangue152, com plasma176 leitoso.
Reações incomuns (> 1/1.000 e < 1/100):
- Dermatológicas: Retardo da cicatrização, atrofia177 cutânea178; petéquias179 e equimoses180; eritema181/rubor facial; sudorese182 excessiva; supressão a reações de alguns testes cutâneos; urticária183, edema angioneurótico184 (edema96 nos olhos171 e lábios) e dermatite21 alérgica. Facilidade em ter hematoma185, acne186 na face187, peito188 e costas189 e estrias avermelhadas nas coxas190, nádegas191 e ombros.
- Neurológicas: Convulsões, aumento da pressão intracraniana com papiledema (pseudotumor cerebral), usualmente após tratamento; cefaleia192; vertigem193; atividade motora aumentada, alterações isquêmicas de nervos, alterações no eletroencefalograma194 e crises.
- Psiquiátricas: Euforia, depressão grave com manifestações psicóticas, alterações da personalidade, hiperirritabilidade e alterações do humor.
- Endócrinas: Irregularidades menstruais; desenvolvimento de estado cushingoide; supressão do crescimento fetal ou infantil; ausência de resposta secundária adrenocortical e hipofisária, especialmente em situações de estresse, como trauma, cirurgia ou doença. Em alguns homens, o uso de corticosteroides resultou em aumento ou diminuição da motilidade e do número de espermatozoides195.
- Gastrintestinais: Distensão abdominal; diarreia196 ou constipação197; náuseas198; vômitos199; perda do apetite (que pode resultar em perda de peso), irritação do estômago166.
- Hidroeletrolíticas: Retenção de sódio; retenção de líquido; insuficiência cardíaca congestiva200 em pacientes suscetíveis; alcalose201 hipocalêmica e aumento da pressão arterial114.
- Musculoesqueléticas: Miopatia202 (fraqueza muscular); perda de massa muscular; osteoporose122, necrose203 asséptica da cabeça163 umeral e femoral; fratura126 patológica de ossos longos204 e das vértebras; agravamento dos sintomas66 da miastenia137 gravis e ruptura do tendão205.
- Metabólicas: Balanço negativo de nitrogênio devido ao catabolismo90 proteico.
Durante a experiência pós-comercialização, foram observadas as seguintes reações adversas sem incidência165 definida: arritmias157 (taquicardia206 ou bradicardia207); albuminúria208; aumento de peso; dor no peito188; dorsalgia; mal estar geral; palidez; sensação de calor ou de frio; descoloração da língua209; sensibilidade dos dentes; sialorreia210; soluço; xerostomia211; dispneia212; rinite26; tosse; frequência miccional aumentada; isquemia213 de origem periférica; perda ou alteração do paladar214; parosmia; hipertonia215; nistagmo216; paralisia217 facial; tremor; aumento da libido218; confusão; distúrbio do sono e sonolência.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária - NOTIVISA ou para a Vigilância Sanitária Estadual ou Municipal.
Sintomas66
Não foram relatados os efeitos de ingestão acidental de grandes quantidades de prednisolona em um curto período de tempo.
O que fazer antes de procurar socorro médico?
Devem-se evitar a provocação de vômitos199 e a ingestão de alimentos ou bebidas. O mais indicado é procurar um serviço médico, tendo em mãos219 a embalagem do produto e, de preferência sabendo-se a quantidade exata de medicamento ingerida. Pode-se, alternativamente, solicitar auxílio ao Centro de Assistência Toxicológica da região, o qual deve fornecer as orientações para a superdose em questão. Superdose aguda com glicocorticoides, incluindo prednisolona, não deve levar a situações de risco de morte. Exceto em doses extremas, poucos dias em regime de alta dose com glicocorticoides torna improvável que a produção de resultados nocivos, na ausência de contraindicações específicas, como em pacientes com diabetes mellitus220, glaucoma112 ou úlcera péptica135 ativa, ou em pacientes que estejam fazendo uso de medicações, como: digitálicos, anticoagulantes151 cumarínicos ou diuréticos159 depletores de potássio. O seu tratamento inclui a indução de emese221 ou através de lavagem gástrica222. As possíveis complicações associadas devem ser tratadas especificamente. Este medicamento deve ser usado somente na dose recomendada. Se você utilizar grande quantidade deste medicamento, procure imediatamente socorro médico, levando a bula do produto.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.0573.0330
Farmacêutica Responsável: Gabriela Mallmann - CRF-SP nº 30.138
Fabricado por:
Aché Laboratórios Farmacêuticos S.A.
Guarulhos - SP
Registrado por:
Aché Laboratórios Farmacêuticos S.A.
Av. Brigadeiro Faria Lima, 201 - 20º andar
São Paulo - SP
CNPJ 60.659.463/0029-92
Indústria Brasileira
SAC 0800 701 6900