Valpakine (Solução oral)
SANOFI-AVENTIS FARMACÊUTICA LTDA
INFORMAÇÕES AO PACIENTE
Valpakine®
valproato de sódio
Solução oral
APRESENTAÇÃO
Solução oral
Frasco com 40 mL + seringa1 graduada
USO ORAL
USO PEDIÁTRICO
COMPOSIÇÃO
Cada mL de Valpakine solução oral contém:
| valproato de sódio | 200 mg |
| excipiente q.s.p. | 1 mL |
Excipientes: ureia2, hidróxido de sódio e água purificada.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Valpakine é destinado ao tratamento das epilepsias generalizadas ou parciais.
Generalizadas primárias: pequeno mal, grande mal, epilepsias mioclônicas3.
Generalizadas secundárias: West (síndrome4 epilética), Lennox-Gastaut.
Parciais: de sintomatologia simples e/ou complexa (formas psicossensoriais, psicomotoras), bem como as epilepsias parciais benignas.
Formas mistas: Valpakine também é indicado nos distúrbios do comportamento ligados à epilepsia5, no tratamento das convulsões febris na infância, em casos de alto risco e que já tenham apresentado convulsões.
COMO ESTE MEDICAMENTO FUNCIONA?
Valpakine é um medicamento que possui em sua fórmula o valproato de sódio, substância que atua na eliminação dos sintomas6 da epilepsia5.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Valpakine é contraindicado nas seguintes situações:
- Tratamento da epilepsia5
- na gravidez7, a menos que não exista tratamento alternativo adequado (vide “ O que devo saber antes de usar este medicamento? ”).
- em mulheres com potencial para engravidar, a menos que as condições do programa de prevenção da gravidez7 sejam cumpridas (vide “O que devo saber antes de usar este medicamento?”).
Todas as indicações
Valpakine não deve ser utilizado caso:
- Você seja alérgico ao valproato de sódio;
Este medicamento é contraindicado para uso por pacientes com:
- Hepatite8 (inflamação9 do fígado10) aguda ou crônica;
- antecedente pessoal ou familiar de hepatite8 severa (inflamação9 do fígado10), especialmente medicamentosa;
- doença rara chamada porfiria11 hepática12;
- doença mitocondrial causada por mutações no gene nuclear que codifica a enzima13 mitocondrial polimerase ? (POLG, por exemplo, síndrome4 Alpers-Huttenlocher) e em crianças menores de dois anos de idade com suspeita de ter um distúrbio relacionado com POLG (vide “O que devo saber antes de usar este medicamento? - Advertências”);
- distúrbio conhecido do ciclo da ureia2 (ciclo de reações das enzimas do organismo) (vide “O que devo saber antes de usar este medicamento? - Precauções”).
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
ADVERTÊNCIAS
Programa de Prevenção da Gravidez7
O valproato tem um alto potencial teratogênico14 e as crianças expostas in utero15 ao valproato têm um alto risco de malformações16 congênitas17 e distúrbios do neurodesenvolvimento (vide “Gravidez”).
Valpakine está contraindicado nas seguintes situações:
Tratamento da epilepsia5
- na gravidez7, a menos que não haja tratamento alternativo adequado (vide “Contraindicação” e “Gravidez”).
- em mulheres com potencial para engravidar, a menos que as condições do programa de prevenção da gravidez7 sejam cumpridas (vide “Contraindicação” e “Gravidez”).
Condições do Programa de Prevenção da Gravidez7
O prescritor deve assegurar que:
- circunstâncias individuais são avaliadas em cada caso e discutidas com o paciente. Isso é para garantir o envolvimento do paciente e a compreensão das opções terapêuticas, juntamente com os riscos e as medidas necessárias para mitigar18 os riscos.
- o potencial de gravidez7 é avaliado para todos os pacientes do sexo feminino.
- o paciente compreende e reconhece os riscos de malformações16 congênitas17 e distúrbios do neurodesenvolvimento, incluindo a magnitude desses riscos em crianças expostas ao valproato no útero15.
- o paciente compreende a necessidade de se submeter a um teste de gravidez7 antes do início do tratamento e durante o tratamento, conforme necessário.
- o paciente é aconselhado em relação à contracepção19, e que o paciente é capaz de cumprir a necessidade de usar contracepção19 efetiva (ver subseção contracepção19 deste aviso), sem interrupção durante toda a duração do tratamento com valproato.
- o paciente compreende a necessidade de uma revisão regular (pelo menos anual) do tratamento por um especialista com experiência no tratamento da epilepsia5 ou distúrbios bipolares.
- a paciente compreende a necessidade de consultar seu médico assim que ela estiver planejando a gravidez7, para garantir uma discussão oportuna e mudar para opções alternativas de tratamento antes da concepção20, e antes que a contracepção19 seja interrompida.
- o paciente compreende a necessidade de consultar urgentemente seu médico em caso de gravidez7.
- o paciente recebeu o guia do paciente.
- o paciente reconheceu que entendeu os perigos e as precauções necessárias associadas ao uso de valproato (Formulário Anual de Reconhecimento de Risco).
Estas condições também dizem respeito a mulheres que não são sexualmente ativas, a menos que o prescritor considere que existem razões convincentes para indicar que não há risco de gravidez7.
O farmacêutico ou outro profissional de saúde21 deve assegurar que:
- o cartão do paciente é fornecido com todas as dispensas de valproato e os pacientes compreendem seu conteúdo.
- os pacientes são aconselhados a não interromper a medicação com valproato e a contactar imediatamente um especialista em caso de gravidez7 planeada ou suspeita.
Crianças do sexo feminino
- Os prescritores devem assegurar que os pais / cuidadores de crianças do sexo feminino compreendam a necessidade de contatar o especialista, uma vez que a criança do sexo feminino usando valproato experimenta a menarca22.
- O prescritor deve assegurar que os pais / cuidadores de crianças do sexo feminino que experimentaram a menarca22 recebam informações abrangentes sobre os riscos de malformações16 congênitas17 e distúrbios do neurodesenvolvimento, incluindo a magnitude desses riscos em crianças expostas ao valproato no útero15.
- Em pacientes que experimentaram a menarca22, o especialista em prescrição deve reavaliar a necessidade de terapia com valproato anualmente e considerar opções alternativas de tratamento. Se o valproato for o único tratamento adequado, deve-se discutir a necessidade de usar contraceptivos eficazes e todas as outras condições do programa de prevenção da gravidez7. Todo esforço deve ser feito pelo especialista para mudar as crianças do sexo feminino para um tratamento alternativo antes que elas atinjam
Teste de gravidez7
A gravidez7 deve ser excluída antes do início do tratamento com valproato. O tratamento com valproato não deve ser iniciado em mulheres com potencial para engravidar sem um teste de gravidez7 negativo (teste de gravidez7 plasma23), confirmado por um prestador de cuidados de saúde21, para excluir o uso não intencional na gravidez7.
Contracepção19
As mulheres em idade fértil que recebem valproato prescrito devem usar contraceptivos eficazes, sem interrupção durante toda a duração do tratamento com valproato. Estes pacientes devem receber informações abrangentes sobre a prevenção da gravidez7 e devem ser encaminhados para orientação contraceptiva se não estiverem usando métodos contraceptivos eficazes. Deve ser utilizado pelo menos um método de contracepção19 eficaz (preferencialmente uma forma independente do usuário, como um dispositivo intra-uterino ou implante24) ou duas formas complementares de contracepção19, incluindo um método de barreira. Circunstâncias individuais devem ser avaliadas em cada caso, ao escolher o método de contracepção19 envolvendo o paciente na discussão, para garantir seu engajamento e cumprimento das medidas escolhidas. Mesmo que ela tenha amenorréia25, ela deve seguir todos os conselhos sobre contracepção19 eficaz.
Revisões anuais de tratamento por um especialista:
O especialista deve, pelo menos, revisar anualmente se o valproato é o tratamento mais adequado para o paciente. O especialista deve discutir o formulário anual de reconhecimento de riscos, no início e durante cada revisão anual e garantir que o paciente entendeu seu conteúdo.
Planejamento da gravidez7.
Para a indicação de epilepsia5, se uma mulher estiver planejando engravidar, um especialista com experiência no tratamento da epilepsia5 deve reavaliar a terapia com valproato e considerar opções alternativas de tratamento. Todo esforço deve ser feito para mudar para tratamento alternativo apropriado antes da concepção20, e antes que a contracepção19 seja descontinuada (vide “Gravidez”). Se a mudança não for possível, a mulher deve receber mais aconselhamento sobre os riscos do valproato para o feto26, para apoiar sua tomada de decisão informada em relação ao planejamento familiar.
Para a indicação do transtorno bipolar, se uma mulher está planejando engravidar, um especialista com experiência no manejo do transtorno bipolar deve ser consultado. O tratamento com valproato deve ser descontinuado antes da concepção20 e antes da descontinuação da contracepção19. Se necessário, opções alternativas de tratamento devem ser consideradas.
Em caso de gravidez7:
Se uma mulher usando valproato engravidar, ela deve ser imediatamente encaminhada a um especialista para reavaliar o tratamento com valproato e considerar opções alternativas. Os pacientes com uma gravidez7 exposta a valproato e os seus parceiros devem ser encaminhados para um especialista com experiência em teratologia / medicina pré-natal para avaliação e aconselhamento sobre a gravidez7 exposta (vide “Gravidez”).
Materiais educativos:
Para ajudar os profissionais de saúde21 e os pacientes a evitar a exposição ao valproato durante a gravidez7, a empresa detentora do registro forneceu materiais educativos para reforçar as advertências e fornecer orientações relativamente à utilização de valproato em mulheres com potencial para engravidar e os detalhes do programa de prevenção da gravidez7. Um guia do paciente e um cartão do paciente devem ser fornecidos a todas as mulheres em idade fértil usando valproato.
Um formulário de reconhecimento de risco precisa ser usado no momento do início do tratamento e durante cada revisão anual do tratamento com valproato pelo especialista, e quando uma mulher estiver planejando uma gravidez7 ou está grávida
Lesões27 graves no fígado10
Condições de ocorrência:
- Lesões27 severas no fígado10 foram excepcionalmente relatadas.
- A experiência demonstra que, especialmente em casos de terapia anticonvulsivante múltipla, neonatos28 e crianças com menos de 3 anos de idade com epilepsia5 grave, principalmente epilepsia5 associada a lesões27 cerebrais, retardo mental e/ou doença metabólica congênita29 ou degenerativa30, possuem maior risco de lesões27 hepáticas31 severas. A partir de 3 anos de idade, a incidência32 diminui de forma significativa, progressivamente com a idade.
Na grande maioria dos casos, esses comprometimentos hepáticos foram observados durante os 6 primeiros meses de tratamento.
Sinais33 sugestivos:
O diagnóstico34 precoce de dano hepático ou pancreático baseia-se principalmente nos sintomas6 clínicos. Particularmente convém considerar (especialmente nos pacientes que apresentam risco), dois tipos de manifestações que podem preceder a icterícia35 (pele36 amarelada):
- Sintomas6 não específicos, geralmente de aparecimento súbito, como astenia37 (fraqueza), anorexia38 (redução ou perda do apetite), letargia39 (torpor40 ou entorpecimento), sonolência, são geralmente acompanhados de vômitos41 repetidos e dores abdominais.
- Em pacientes com epilepsia5, recorrência42 de crises epilépticas.
Caso você apresente esses sintomas6 procure o médico imediatamente para que ele possa fazer além do exame clínico, a execução imediata de uma avaliação laboratorial da função do seu fígado10.
Detecção:
Antes do início e durante os primeiros 6 meses de tratamento, o acompanhamento da função do fígado10 deverá ser feito periodicamente.
Inflamação9 no pâncreas43
Inflamação9 severa do pâncreas43 foi raramente reportada. As crianças possuem um risco particular que diminui com o aumento da idade. Crises epilépticas severas, problemas neurológicos ou terapia anticonvulsivante podem ser fatores de risco. Disfunções hepáticas31 com pancreatite44 aumentam o risco de consequências fatais.
Caso você apresente dor abdominal aguda você deve procurar imediatamente avaliação médica. Em caso de pancreatite44 diagnosticada, Valpakine deve ser descontinuado.
Medicamentos contendo estrógeno45
O valproato não reduz a eficácia dos contraceptivos hormonais. No entanto, os medicamentos contendo estrógeno45, incluindo os contraceptivos hormonais que contenham estrógeno45, podem resultar na diminuição da concentração no sangue46 do valproato e potencialmente na diminuição da eficácia do valproato. Os médicos prescritores devem monitorar a resposta clínica (controle de convulsões ou controle de humor) ao iniciar ou descontinuar medicamentos contendo estrógeno45 (vide “Interações Medicamentosas”).
Comportamentos e intenções suicidas
Os pacientes que apresentam sinais33 de comportamentos ou intenções suicidas devem ser monitorados, e tratamento apropriado deve ser considerado. Os pacientes (e seus responsáveis) devem a procurar orientação médica imediatamente caso surjam sinais33 de comportamentos ou intenções suicidas.
Agentes carbapenêmicos (uma classe de antibióticos de uso hospitalar)
O uso concomitante de valproato de sódio e agentes carbapenêmicos não é recomendado (vide “Interações Medicamentosas”).
Pacientes com doença mitocondrial conhecida ou suspeita
O valproato pode desencadear ou agravar sinais33 clínicos de doenças mitocondriais subjacentes causadas por mutações do DNA mitocondrial, bem como o gene nuclear codificado POLG. Em particular, insuficiência hepática47 aguda e as mortes relacionadas com o fígado10 têm sido associados ao tratamento com valproato numa taxa mais elevada em pacientes com síndromes neurometabólicas hereditárias causadas por mutações no gene da enzima13 mitocondrial polimerase γ (POLG; por exemplo, Síndrome4 de Alpers-Huttenlocher).
Distúrbios relacionados ao POLG devem ser investigados em pacientes com histórico familiar ou sintomas6 sugestivos deste distúrbio, incluindo, mas não limitado a encefalopatia48 sem explicação, epilepsia5 refratária (focal, mioclônica49), estado epiléptico, atrasos de desenvolvimento, regressão psicomotora50, neuropatia51 axonal sensitivo-motora, ataxia52 cerebelar (miopatia53), oftalmoplegia, ou enxaqueca54 complicada com aura occipital. Teste de mutação55 POLG deve ser realizado de acordo com a prática clínica atual para a avaliação diagnóstica de tais distúrbios (vide “Quando não devo usar este medicamento”?).
Agravamento das convulsões
Assim como ocorre com outros medicamentos antiepilépticos, alguns pacientes podem apresentar, em vez de uma melhora, um agravamento reversível da frequência e da severidade das convulsões (incluindo o estado epiléptico), ou o aparecimento de novos tipos de convulsões com uso de valproato. No caso de agravamento das convulsões, você deve consultar imediatamente o seu médico (vide “Quais os males que este medicamento pode me causar?”).
PRECAUÇÕES
Antes do início e durante os primeiros 6 meses de tratamento, o acompanhamento da função do fígado10 deverá ser feito periodicamente, principalmente em pacientes com risco (vide “Contraindicações”). Deve-se assinalar que, como ocorre com a maior parte dos antiepiléticos, pode surgir no início do tratamento uma leve elevação, isolada e transitória das enzimas hepáticas56, sem sinais33 clínicos. Nesse caso, recomenda-se realizar uma avaliação mais completa.
Aconselha-se efetuar exame de sangue46 (contagem de células sanguíneas57, inclusive plaquetas58, tempo de sangramento e tempo de coagulação59) antes de iniciar o tratamento, antes de qualquer cirurgia e na ocorrência de hematoma60 ou sangramento espontâneo (vide “Quais os males que este medicamento pode causar”?).
Antes de iniciar o tratamento com Valpakine verifique com seu médico caso:
- Você tenha uma doença chamada lúpus61 (lúpus61 eritematoso62 sistêmico63).
- Você apresente deficiência enzimática no ciclo da ureia2, levando ao risco de hiperamonemia (excesso de amônia no organismo) com valproato (vide “Quando não devo usar este medicamento”?).
Seu médico irá orientá-lo sobre o risco de ganho de peso no início da terapia, e estratégias, já que ganho de peso é um fator de risco64 para síndrome4 do ovário65 policístico e estratégias apropriadas devem ser adotadas para minimizar esse risco (vide “Quais os males que esse medicamento pode me causar”?).
Alterações no ciclo menstrual também devem ser monitoradas.
Se você tiver deficiência basal de carnitina palmitoil transferase (CPT) tipo II seu médico deve adverti-lo sobre o risco maior de rabdomiólise66 (lesão67 muscular que pode levar a insuficiência renal68 aguda) quando estiverem em tratamento com Valpakine.
A ingestão de álcool não é recomendada durante o tratamento com valproato de sódio.
Gravidez7 e amamentação69
O valproato é contraindicado como tratamento para o transtorno bipolar durante a gravidez7. O valproato é contra- indicado como tratamento para a epilepsia5 durante a gravidez7, a menos que não haja alternativa adequada para tratar a epilepsia5. O valproato é contraindicado para uso em mulheres com potencial para engravidar, a menos que as condições do programa de prevenção da gravidez7 sejam cumpridas (Vide “Contraindicações” e “Advertências”).
Teratogenicidade e Efeitos no Desenvolvimento: Exposição à Gravidez7 Risco relacionado ao valproato.
Tanto a monoterapia com valproato como a politerapia com valproato, incluindo outros antiepilépticos, estão associadas a resultados anormais da gravidez7. Os dados disponíveis sugerem que a politerapia antiepiléptica, incluindo o valproato, pode estar associada a um maior risco de malformações16 congénitas do que a monoterapia com valproato.
Dados de uma meta-análise (incluindo registros e estudos de coorte70) mostraram que 10,73% dos filhos de mulheres epilépticas expostas à monoterapia com valproato durante a gravidez7 sofrem de malformações16 congênitas17 (95% CI: 8,16-13,29). Esta é um maior risco de malformações16 maiores do que para a população em geral, para quem o risco é de cerca de 2-3%. O risco é dependente da dose, mas uma dose limiar abaixo da qual não existe risco não pode ser estabelecida.
Malformações16 congênitas17
Dados disponíveis mostram um aumento na incidência32 de malformações16 no feto26. Os tipos mais comuns de malformações16 , incluindo, defeitos do tubo neural71, dismorfismo facial, lábio leporino72 palato73, craniostenosa, defeitos cardíacos, renais e urogenitais, dos defeitos dos membros (incluindo aplasia bilateral do rádio74)e múltiplas anomalias envolvendo vários sistemas corporais.
Transtornos de desenvolvimento
Os dados mostraram que a exposição ao valproato no útero15 pode ter efeitos adversos sobre o desenvolvimento mental e físico das crianças expostas. O risco parece ser dependente da dose, mas uma dose limiar menor, que não ofereça risco, não pode ser estabelecida com base nos dados disponíveis. O período gestacional exato de risco para estes efeitos é incerto e a possibilidade de um risco ao longo de toda a gravidez7 não pode ser excluída.
Estudos em crianças com idade pré-escolar expostas ao valproato no útero15 mostram que até 30-40% apresentaram atrasos no início do desenvolvimento, tais como falar e andar mais tarde, habilidades intelectuais mais baixas, competência linguística pobre (falar e entender) e problemas de memória.
O quociente de inteligência75 (QI76) medido em crianças em idade escolar (de 6 anos), com uma história de exposição ao valproato no útero15 foi em média de 7-10 pontos mais baixo do que as crianças expostas a outros antiepilépticos. Embora a função dos fatores de confusão não possa ser excluída, existem evidências em crianças expostas ao valproato de que o risco de comprometimento intelectual pode ser independente do QI76 materno. Há dados limitados sobre os resultados a longo prazo.
Há dados que mostram que crianças expostas ao valproato no útero15 estão em maior risco de transtorno do espectro autista (aproximadamente de 3 vezes), incluindo autismo infantil (aproximadamente 5 vezes em comparação com a população geral).
Dados limitados sugerem que as crianças expostas ao valproato no útero15 podem ser mais propensas a desenvolver sintomas6 de déficit de atenção / hiperatividade (TDAH).
Se uma mulher planeja uma gravidez7: para a indicação de epilepsia5, se uma mulher estiver planejando engravidar, um especialista com experiência no tratamento da epilepsia5 deve reavaliar a terapia com valproato e considerar opções alternativas de tratamento. Todo esforço deve ser feito para mudar para tratamento alternativo apropriado antes da concepção20, e antes que a contracepção19 seja descontinuada (vide “O que devo saber antes de usar este medicamento ?). Se a mudança não for possível, a mulher deve receber mais aconselhamento sobre os riscos do valproato para o feto26, para apoiar sua tomada de decisão informada em relação ao planejamento familiar.
Para a indicação do transtorno bipolar, se uma mulher está planejando engravidar, um especialista com experiência no manejo do transtorno bipolar deve ser consultado. O tratamento com valproato deve ser descontinuado antes da concepção20 e antes da descontinuação da contracepção19. Se necessário, opções alternativas de tratamento devem ser consideradas.
Mulheres grávidas: o valproato como tratamento para transtorno bipolar é contraindicado para uso durante a gravidez7. O valproato como tratamento para a epilepsia5 é contraindicado na gravidez7, a menos que não exista tratamento alternativo adequado (vide “Contraindicações” e “O que devo saber antes de usar este medicamento ?).
Se uma mulher usando valproato engravidar, ela deve ser imediatamente encaminhada a um especialista para considerar opções alternativas de tratamento. Durante a gravidez7, as crises tónicas clónicas maternas e o estado epiléptico com hipoxia77 podem acarretar um risco particular de morte para a mãe e o feto26.
Se, apesar dos riscos conhecidos de valproato durante a gravidez7 e após uma análise cuidadosa de um tratamento alternativo, em circunstâncias excepcionais, uma mulher grávida deve receber valproato para a epilepsia5, recomenda-se: use a menor dose efetiva e divida a dose diária de valproato em várias doses pequenas a serem tomadas ao longo do dia. A utilização de uma formulação de libertação prolongada pode ser preferível a outras formulações de tratamento, de modo a evitar concentrações plasmáticas de pico elevado.
Todos os pacientes com uma gravidez7 exposta a valproato e os seus parceiros devem ser encaminhados para um especialista com experiência em teratologia / medicina pré-natal para avaliação e aconselhamento sobre a gravidez7 exposta. A monitoração pré-natal especializada deve ocorrer para detectar a possível ocorrência de defeitos do tubo neural71 ou outras malformações16. A suplementação78 com folato (5 mg por dia) antes da gestação pode diminuir o risco de defeitos do tubo neural71 que podem ocorrer em todas as gestações. No entanto, a evidência disponível não sugere que ela previna defeitos congênitos79 ou malformações16 devido à exposição ao valproato.
O valproato não reduz a eficácia dos contraceptivos hormonais. No entanto, os medicamentos contendo estrógeno45, incluindo os contraceptivos hormonais que contenham estrógeno45, podem resultar na diminuição da concentração no sangue46 do valproato e potencialmente na diminuição da eficácia do valproato. Os médicos prescritores devem monitorar a resposta clínica (controle de convulsões ou controle de humor) ao iniciar ou descontinuar medicamentos contendo estrógeno45 (vide “Interações Medicamentosas”).
Mulheres em idade fértil devem ser informadas sobre os riscos e benefícios do tratamento com valproato durante a gravidez7.
Em uma mulher epiléptica em tratamento com valproato de sódio, a ocorrência de gravidez7 deve levar em conta a relação risco-benefício.
Se a gravidez7 é programada, ou se a mulher engravidar durante o tratamento, o uso de valproato de sódio deve ser reavaliado qualquer que seja sua indicação:
- Em epilepsia5, a terapia com valproato não deve ser descontinuada sem a reavaliação dos riscos-benefícios. Se, após cuidadosa avaliação dos riscos e benefícios, o tratamento não for interrompido durante a gravidez7, convém administrar a dose diária mínima eficaz dividida em diversas tomadas. O uso de uma formulação de liberação prolongada é mais indicado.
- Adicionalmente, se necessário, deve-se administrar suplemento de folato antes da gravidez7 e na dose pertinente (5 mg/dia) para diminuir o risco de anomalias do tubo neural71. Entretanto, a evidência disponível não sugere que isto previna os defeitos congênitos79 ou malformações16 devido à exposição ao valproato.
- Um acompanhamento pré-natal especializado deve ser instituído para registrar o eventual aparecimento de anomalias do tubo neural71 ou outras malformações16.
Risco no neonato80
Casos excepcionais de síndrome4 hemorrágica81 foram relatados em neonatos28 cujas mães utilizaram valproato de sódio durante a gravidez7. Essa síndrome4 hemorrágica81 está relacionada com hipofibrinogenemia e afribinogenemia e pode ser fatal. Essas hipofibrinogenemias (alterações de uma proteína, fibrinogênio82, envolvida na coagulação59 do sangue46) possivelmente estão associadas com a diminuição de fatores de coagulação59. O médico deve fazer uma investigação em neonatos28.
Então, deve-se investigar a contagem de plaquetas58, níveis de fibrinogênio82 plasmático, testes de coagulação59 e os fatores de coagulação59 em neonatos28.
Foram reportados casos de hipoglicemia83 em neonatos28 cujas mães utilizaram valproato durante o terceiro trimestre da gravidez7.
Casos de hipotireoidismo84 foram reportados em neonatos28 cujas mães utilizaram o valproato durante a gravidez7.
Síndrome4 de abstinência [tais como, em particular, agitação, irritabilidade, hiperexcitabilidade, nervosismo, hipercinesia85 (presença de movimentos excessivos, intensos), distúrbios de tonicidade, tremor, convulsão86 e distúrbios nutricionais] pode ocorrer em neonatos28 cujas mães estavam em tratamento com valproato durante o último trimestre da gravidez7.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez7.
Fertilidade
Amenorreia25, ovários87 policísticos e aumento dos níveis de testosterona têm sido relatados em mulheres que usam valproato (vide “Quais os males que este medicamento pode me causar?”). Administração de valproato também pode comprometer a fertilidade em homens88 (vide “Quais os males que este medicamento pode me causar?”). Relatos de casos indicam que as disfunções da fertilidade são reversíveis após a descontinuação do tratamento.
A excreção do valproato no leite materno é pequena, atingindo concentrações de 1 a 10% do nível sérico.
Com base na literatura e na experiência clínica, a amamentação69 pode ser considerada, levando-se em conta o perfil de segurança de Valpakine, especialmente os distúrbios hematológicos (vide “Quais os males que este medicamento pode me causar?”).
POPULAÇÕES ESPECIAIS
Crianças:
Nas crianças com menos de 3 anos aconselha-se utilizar Valpakine em monoterapia. Antes do início do tratamento, o médico avaliará o benefício terapêutico em relação ao risco de danos no fígado10 ou inflamação9 no pâncreas43 nos pacientes dessa idade.
O uso concomitante de salicilatos deve ser evitado em crianças com menos de 3 anos de idade devido ao risco de toxicidade89 no fígado10.
Pacientes com problema nos rins90:
Caso você apresente algum problema nos rins90 o médico poderá prescrever uma dose menor de Valpakine.
Alterações na capacidade de dirigir veículos e operar máquinas
Os pacientes que sofrem de epilepsia5 não devem dirigir veículos ou operar máquinas perigosas. Para Valpakine essas recomendações são reforçadas, pois alguns pacientes podem apresentar confusão mental ou aumento das crises convulsivas. Informe seu médico caso você faça parte deste grupo de risco91.
Precaução especial
Consulte seu médico antes de tomar Valpakine caso você seja portador do vírus92 HIV93 (AIDS).
INTERAÇÕES MEDICAMENTOSAS
Associações que necessitam precauções de uso: Interações com medicamentos:
- Neurolépticos94; inibidores da MAO95; antidepressivos e benzodiazepínicos.
- O valproato de sódio pode potencializar a ação de outros psicotrópicos96 como os neurolépticos94, inibidores da MAO95, antidepressivos e benzodiazepínicos.
- Lítio: não apresenta efeito sobre os níveis séricos de lítio;
- Fenobarbital: Valpakine aumenta as concentrações plasmáticas de fenobarbital, com aparecimento de sedação97, particularmente em crianças;
- Primidona: Valpakine aumenta os níveis plasmáticos da primidona, com acentuação dos seus efeitos indesejáveis (como sedação97). Após uso prolongado, esses efeitos cessam;
- Fenitoína: Valpakine diminui a concentração plasmática total da fenitoína. Além disso, o valproato de sódio aumenta a concentração da forma livre de fenitoína, podendo produzir sinais33 de superdosagem;
- Carbamazepina: foi relatada toxicidade89 clínica após administração de valproato de sódio em conjunto com carbamazepina. O valproato pode potencializar o efeito tóxico da carbamazepina;
- Etosuximida: aumento da concentração plasmática de etosuximida. Recomenda-se monitorização da concentração plasmática da etosuximida durante terapia combinada98 com valproato;
- Nimodipina: o tratamento concomitante de nimodipino com ácido valproico pode aumentar a concentração plasmática de nimodipino em 50%;
- Lamotrigina: Valpakine reduz o metabolismo99 da lamotrigina e aumenta sua meia-vida em quase duas vezes. Esta interação pode levar ao aumento da toxicidade89 da lamotrigina, particularmente em relação ao “rash” cutâneo100;
- Zidovudina: o valproato pode aumentar a concentração plasmática de zidovudina levando a um aumento de sua toxicidade89;
- Felbamato: o ácido valproico pode diminuir o “clearance” médio de felbamato em até 16%;
- Olanzapina: o ácido valproico pode diminuir a concentração plasmática da olanzapina.
- Rufinamida: o ácido valproico pode levar a um aumento no nível plasmático da rufinamida. Este aumento depende da concentração do ácido valproico. Deve-se ter cuidado, em particular nas crianças, já que este efeito é maior nesta população.
- Propofol: o ácido valproico pode levar a um aumento do nível sanguíneo de propofol. Quando coadministrado com valproato, deve ser considerada a redução da dose de propofol.
A monitorização clínica é recomendável e o ajuste de dose deve ser realizado sempre que necessário.
Efeito dos outros antiepilépticos sobre o valproato de sódio: Os antiepilépticos com efeito indutor enzimático (incluindo fenitoína, fenobarbital, carbamazepina) diminuem as concentrações séricas do ácido valproico. Em caso de terapia combinada98, deve-se ajustar as doses de acordo com a resposta clínica e níveis sanguíneos.
- A combinação de felbamato e valproato diminui o “clearance” de ácido valproico entre 22 e 50% e, consequentemente, aumenta sua concentração plasmática. Portanto, a dose de valproato deve ser monitorizada.
- O nível de metabólitos101 do ácido valproico pode aumentar em caso de administração concomitante com fenitoína ou fenobarbital. Assim, os pacientes tratados com esses dois medicamentos devem ser cuidadosamente monitorados quanto aos sinais33 e sintomas6 de hiperamonemia (excesso de amônia no organismo).
- Mefloquina aumenta o metabolismo99 do ácido valproico e tem um efeito convulsivo. Por isso, crises epiléticas podem ocorrer em casos de terapia combinada98.
- Em caso de uso concomitante de valproato e agentes de alta ligação proteica (ácido acetilsalicílico), pode ocorrer o aumento dos níveis séricos de ácido valproico livre.
- Monitorização da taxa de protrombina102 deve ser executada em caso de uso concomitante de fator anticoagulante103 dependente de vitamina104 K.
- Em caso de uso concomitante com cimetidina ou eritromicina, os níveis séricos de ácido valproico podem aumentar (como resultado da redução do metabolismo99 hepático).
- Clonazepam: existem alguns relatos de crises de ausência após uso concomitante de clonazepam e valproato de sódio.
- Carbapenêmicos (panipenem, meropenem, imipenem etc.): diminuições nos níveis sanguíneos de ácido valproico foram reportadas quando coadministrados com agentes carbapenêmicos, algumas vezes associada às convulsões. Devido ao início rápido e à extensão da diminuição, deve ser evitada administração concomitante de agentes carbapenêmicos em pacientes estabilizados com ácido valproico.
- A rifampicina pode diminuir os níveis do ácido valproico no sangue46 resultando em uma deficiência do efeito terapêutico. Portanto, o ajuste da posologia de Valpakine pode ser necessário quando coadministrado com rifampicina.
- Os inibidores de protease: os inibidores de protease, tais como lopinavir, ritonavir, diminuem o nível plasmático de valproato, quando coadministrados.
- Colestiramina: a colestiramina pode levar a uma diminuição no nível plasmático de valproato, quando coadministrados.
- Medicamentos contendo estrógeno45: os medicamentos contendo estrógeno45, incluindo os anticonceptivos hormonais que contenham estrógeno45, podem resultar na diminuição da concentração no sangue46 do valproato e potencialmente na diminuição da eficácia do valproato. O valproato não reduz a eficácia de agentes estroprogestativos em mulheres recebendo contraceptivos hormonais.
Outras interações
Informe seu médico se você estiver em tratamento com topiramato ou acetazolamida uma vez que o uso concomitante desse medicamento com Valpakine está associado com encefalopatia48 e/ou hiperamonemia.
Quetiapina: a coadministração de valproato e quetiapina pode aumentar o risco de neutropenia105/leucopenia106 (diminuição do número de neutrófilos107 no sangue46/ redução dos glóbulos brancos no sangue46).
Interações com substâncias químicas
Álcool: o valproato de sódio pode potencializar os efeitos sedativos de substâncias que afetam o Sistema Nervoso Central108.
Interações em testes laboratoriais e de diagnóstico34
Uma vez que o valproato é excretado principalmente através dos rins90, em parte, sob a forma de corpos cetônicos, o teste de excreção de corpos cetônicos nos pacientes diabéticos pode gerar resultados falsos positivos.
Informe ao seu médico se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para sua saúde21.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Valpakine solução oral deve ser mantido em temperatura ambiente (entre 15 e 30ºC). Proteger da luz.
Número de lote e datas de fabricação e validade: vide embalagem. Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas
Líquido límpido com coloração incolor a levemente amarelada.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
COMO DEVO USAR ESTE MEDICAMENTO?
Valpakine deve ser ingerido preferencialmente durante ou logo após as refeições para reduzir as chances de ocorrer náusea109. Valpakine solução oral deve ser diluído em água não gasosa ou suco de frutas.
|
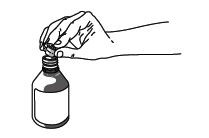
1º passo: Coloque a tampa interna que acompanha a seringa1 dosadora no frasco de Valpakine |
 |
|
2º passo: Encaixe a seringa1 dosadora no orifício da tampa interna do frasco, vire o frasco de cabeça110 para baixo e puxe o êmbolo111 até a marca correspondente à quantidade indicada pelo seu médico. |
 |
|
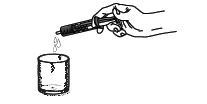
3º passo: Colocar, vagarosamente, a quantidade do líquido correspondente em um copo. |
 |
|
4º passo: Diluir em um pouco de água ou suco de fruta não gasoso |
 |
|
5º passo: Após a administração, lave a seringa1 com água e guarde-a na respectiva caixa para que possa ser utilizada novamente. |
|
Posologia
A posologia diária deve ser ajustada de acordo com a idade e peso corporal. A correlação entre a dose diária, concentração no sangue46 e eficácia não foi totalmente estabelecida e a dose ideal deve ser baseada principalmente na resposta clínica.
A dose diária deve ser dividida em 2 ou mais vezes de preferência durante as refeições:
Uso em lactentes112 e crianças
Valpakine solução oral 200 mg/mL: a dose diária é de 30 mg/kg. A dose deve ser calculada em mg ou em mL. A solução deverá ser diluída em água ou suco de fruta não gasosos.
Início do tratamento com Valpakine:
No início do tratamento você receberá uma dose pequena. Isso porque alguns pacientes necessitam de doses menores de Valpakine que outros pacientes para controlar suas convulsões. Seu médico aumentará a dose até que sua condição esteja controlada e a dose ótima seja obtida em aproximadamente uma semana.
Caso você já esteja em tratamento com outro antiepiléptico, seu médico irá orientá-lo a iniciar progressivamente o uso de Valpakine de modo a atingir a dose ótima em aproximadamente duas semanas. A seguir, reduzir as terapêuticas associadas de acordo com o controle obtido.
Em se tratando de paciente que não esteja tomando outro antiepiléptico à ascensão da posologia deverá ser feita por aumentos sucessivos a cada 2 ou 3 dias de maneira a obter a dose ótima em aproximadamente uma semana.
IMPORTANTE: não interrompa o tratamento com Valpakine sem primeiro conversar com o seu médico, mesmo se você estiver se sentindo melhor, uma vez que a interrupção repentina pode ocasionar a volta das convulsões.
Não há estudos dos efeitos de Valpakine administrado por vias não recomendadas. Portanto, por segurança e para garantir a eficácia deste medicamento, a administração deve ser somente por via oral conforme recomendado pelo médico.
Populações especiais
Em pacientes com insuficiência renal68, seu médico poderá prescrever uma dose menor de Valpakine.
Crianças e adolescentes do sexo feminino, mulheres em idade fértil e gestantes
Valpakine deve ser iniciado e supervisionado por um médico com experiência no tratamento de epilepsia5. O tratamento só deve ser iniciado se outros tratamentos forem ineficazes ou não tolerados (vide “O que devo saber antes de usar este medicamento?”) e os benefícios e riscos devem ser cuidadosamente reconsiderados nas consultas de acompanhamento do tratamento. Preferencialmente, Valpakine deve ser prescrito em monoterapia e na dose eficaz mais baixa. A dose diária deve ser dividida em pelo menos duas doses únicas durante a gravidez7.
Medicamentos contendo estrógeno45
O valproato não reduz a eficácia dos contraceptivos hormonais.
No entanto, os medicamentos contendo estrógeno45, incluindo os contraceptivos hormonais que contenham estrógeno45, podem resultar na diminuição da concentração no sangue46 do valproato e potencialmente na diminuição da eficácia do valproato. Os médicos prescritores devem monitorar a resposta clínica (controle de convulsões ou controle de humor) ao iniciar ou descontinuar medicamentos contendo estrógeno45 (vide “Interações Medicamentosas”).
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento de seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Caso esqueça de administrar uma dose, administre-a assim que possível. No entanto, se estiver próximo do horário da dose seguinte, espere por este horário, respeitando sempre o intervalo determinado pela posologia. Nunca devem ser administradas duas doses ao mesmo tempo.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Informe seu médico sobre o aparecimento de reações desagradáveis com o uso de Valpakine. As frequências das reações adversas estão listadas a seguir de acordo com a seguinte convenção: Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento).
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento).
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento).
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento).
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento).
Reação desconhecida (não pode ser estimada pelos dados disponíveis)
Distúrbios congênitos113, familiares e genéticos (vide “O que devo saber antes de tomar este medicamento? – Gravidez”).
Distúrbios do sangue46 e sistema linfático114
- Comum: anemia115 (diminuição do número de glóbulos vermelhos no sangue46), trombocitopenia116 (redução do número de plaquetas58 no sangue46) (vide “O que devo saber antes de tomar este medicamento? – Precauções”).
- Incomum: pancitopenia117 (diminuição global de elementos celulares no sangue46 – glóbulos brancos, vermelhos e plaquetas58), leucopenia106 (diminuição do número de glóbulos brancos no sangue46).
- Rara: deficiência na medula óssea118, incluindo aplasia (falta de desenvolvimento) pura de glóbulos vermelhos, agranulocitose119 (diminuição acentuada na contagem de células brancas do sangue120 como basófilos, eosinófilos121 e neutrófilos107), anemia115 macrocítica (diminuição da quantidade e aumento do tamanho dos glóbulos vermelhos), macrocitose (aumento no tamanho dos glóbulos vermelhos).
Investigações
- Rara: redução dos fatores de coagulação59 (pelo menos um), testes anormais de coagulação59 (como aumento do tempo da protrombina102, aumento do tempo da tromboplastina122 parcial, aumento no tempo da trombina123, aumento do INR) (vide “O que devo saber antes de tomar este medicamento? - Precauções e Gravidez”), deficiência de biotina/deficiência de biotinidase (biotina é uma vitamina104 do complexo B).
Distúrbios do sistema nervoso124
- Muito comum: tremor.
- Comum: distúrbios extrapiramidais (relacionados à coordenação e controle dos movimentos), torpor40* (sensibilidade reduzida), sonolência, convulsão86* (contrações involuntárias dos músculos125 secundárias a descargas elétricas cerebrais), comprometimento da memória, dor de cabeça110, nistagmo126 (movimento involuntário, rápido e repetitivo do globo ocular127). Incomum: coma128* (estado mórbido de sonolência profunda ou de inconsciência129), encefalopatia48* (disfunção do sistema nervoso central108), letargia39* (sonolência), parkinsonismo reversível, ataxia52 (falta de coordenação dos movimentos), parestesia130 (sensação anormal como ardor131, formigamento e coceira, percebidos na pele36 e sem motivo aparente), agravamento das convulsões (vide “O que devo saber antes de usar este medicamento?”).
- Rara: demência132 reversível associada à atrofia133 cerebral reversível, distúrbios cognitivos134 (alterações de conhecimento).
*Torpor40 e letargia39 (sonolência) podendo levar ao coma128 transitório (encefalopatia48).
Distúrbios oculares:
- Desconhecida: diplopia135 (visão136 dupla).
Distúrbios do labirinto137 e audição
- Comum: surdez.
Distúrbios respiratórios, torácicos e mediastinais
- Incomum: derrame138 pleural (acúmulo de líquido na pleura139).
Distúrbios gastrintestinais (do estômago140 e do intestino)
- Muito comum: náusea109 (enjoo).
- Comum: vômito141, distúrbio da gengiva (principalmente hiperplasia142 gengival), estomatite143, dor na parte superior do abdome144 e diarreia145 ocorrem frequentemente em alguns pacientes no início do tratamento, mas desaparecem em geral, em alguns dias, mesmo sem interrupção do tratamento.
- Incomum: pancreatite44 (inflamação9 no pâncreas43), algumas vezes letal (vide “O que devo saber antes de tomar este medicamento? – Advertências”).
Distúrbios renais e urinários Comum: incontinência urinária146. Incomum: insuficiência renal68.
- Rara: enurese147 (incontinência urinária146), nefrite148 tubulointersticial, (inflamação9 do rim149), Síndrome4 de Fancioni (distúrbio raro da função excretora renal150) reversível, mas o mecanismo de ação não é conhecido.
Distúrbios da pele36 e tecidos subcutâneos
- Comum: hipersensibilidade (reações alérgicas), alopecia151 (queda de cabelo152) transitória e/ou dose relacionada, alterações no leito ungueal153 (parte abaixo das unhas154) e unhas154.
- Incomum: angioedema155 (inchaço156 em região subcutânea157 ou em mucosas158, geralmente de origem alérgica), “rash” (erupção159 cutânea160), distúrbio capilar161 (tais como textura capilar161 anormal, alteração na cor do cabelo152, crescimento anormal do cabelo152).
- Rara: necrólise epidérmica tóxica162 (doença grave na pele36), síndrome de Stevens-Johnson163 (doença grave na pele36), eritema multiforme164 (reação imunológica das mucosas158 e da pele36), síndrome4 DRESS (síndrome4 relacionada ao medicamento caracterizada por sintomas6 cutâneos e sistêmicos165).
Distúrbios musculoesqueléticos e do tecido conjuntivo166
- Incomum: diminuição da densidade óssea podendo levar a osteopenia ou osteoporose167 e fraturas em pacientes com terapia prolongada com Valpakine. O mecanismo pelo qual o valproato afeta o metabolismo99 ósseo não está elucidado.
- Rara: lúpus61 sistêmico63 eritematoso62 (doença multissistêmica autoimune168) (vide “O que devo saber antes de tomar este medicamento? – Precauções”), rabdomiólise66 [lesão67 muscular que pode levar a insuficiência renal68 aguda (redução da função dos rins90)] (vide “O que devo saber antes de tomar este medicamento? – Precauções”).
Distúrbios endócrinos (conjunto de glândulas169 que produzem hormônios)
- Incomum: Síndrome4 da Secreção Inapropriada de ADH (hormônio170 antidiurético que promove reabsorção de água no rim149) – SIADH, hiperandrogenismo [hirsutismo171 (crescimento excessivo de pelos), virilismo (aparecimento de características masculinas, como por exemplo, pelo em mulheres nas áreas características de distribuição masculina), acne172, alopecia151 (perda de cabelos e pelos) com padrão masculino e/ou aumento de andrógeno173].
- Rara: hipotireoidismo84 (produção insuficiente de hormônio170 pela glândula174 tireoide175) (vide “O que devo saber antes de tomar este medicamento? – Gravidez”).
Distúrbios do metabolismo99 e nutrição176
- Comum: hiponatremia177 (desequilíbrio na concentração de sódio), ganho de peso. O aumento de peso deve ser cuidadosamente monitorado uma vez que é um fator de risco64 para a síndrome4 de ovário65 policístico (vide “O que devo saber antes de tomar este medicamento? – Precauções”).
- Rara: hiperamonemia (aumento dos níveis de amônia no sangue46) (vide “O que devo saber antes de tomar este medicamento? – Precauções”), obesidade178.
Neoplasmas179 (tumores) benignos, malignos e inespecíficos (incluindo cistos e pólipos180)
- Rara: síndrome4 mielodisplástica (grupo de doenças que apresentam redução de uma ou mais linhagens de células181 do sangue46).
Distúrbios vasculares182
- Comum: hemorragia183 (perda de sangue46) (vide “O que devo saber antes de tomar este medicamento? – Precauções e Gravidez”).
- Incomum: vasculite184 (inflamação9 nos vasos sanguíneos185).
Distúrbios gerais
- Incomum: hipotermia186 (baixa temperatura corporal), edema187 (inchaço156) periférico não severo.
Distúrbios do fígado10
- Comum: lesão67 do fígado10 (vide “O que devo saber antes de tomar este medicamento? - Advertências”).
Distúrbios do sistema reprodutivo e mamário
- Comum: dismenorreia188 (cólica menstrual). Incomum: amenorreia25 (ausência de menstruação189).
- Rara: infertilidade190 masculina, ovários87 policísticos.
Distúrbios psiquiátricos
- Comum: estado confusional, alucinação191, agressividade*, agitação*, distúrbio de atenção*.
- Rara: comportamento anormal*, hiperatividade psicomotora50*, distúrbio de aprendizagem*.
*Estas reações adversas são principalmente observadas na população pediátrica.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também a empresa através do seu sistema de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Os seguintes efeitos podem ocorrer: coma128, com hipotonia192 muscular (músculos125 fracos), hiporreflexia (reflexos lentos), miose193 (diminuição do tamanho da pupila), problemas respiratórios e problemas de metabolismo99, hipotensão194 (pressão baixa) e colapso195/choque196 circulatório. Também foram reportados crises epiléticas e casos de hipertensão197 intracraniana relacionados a edema187 cerebral.
A presença de sódio nas formulações de valproato pode levar a hipernatremia198 (excesso de sódio no sangue46) quando administrados em superdose.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
SÓ PODE SER VENDIDO COM RETENÇÃO DA RECEITA
MS 1.1300.1053
Farm. Resp: Silvia Regina Brollo - CRF-SP 9.815
Registrado por:
Sanofi-Aventis Farmacêutica Ltda.
Av. Mj. Sylvio de M. Padilha, 5200 – São Paulo – SP
CNPJ 02.685.377/0001-57
Fabricado por:
Sanofi-Aventis Farmacêutica Ltda.
Rua Conde Domingos Papaiz, 413 – Suzano – SP
CNPJ 02.685.377/0008-23
Indústria Brasileira
SAC 0800 703 0014