

Atroveran Composto (Gotas) (Bula do profissional de saúde)
COSMED INDUSTRIA DE COSMETICOS E MEDICAMENTOS S.A.
IDENTIFICAÇÃO DO MEDICAMENTO
Atroveran Composto
cloridrato de papaverina + dipirona monoidratada + Atropa belladonna L. + Hyoscyamus niger L. + Peumus boldus Molina
Gotas
APRESENTAÇÃO
Solução Gotas
Embalagem contendo 1 frasco com 30mL
VIA DE ADMINISTRAÇÃO: ORAL
USO ADULTO E PEDIÁTRICO ACIMA DE 12 ANOS
COMPOSIÇÃO
Cada mL de Atroveran Composto solução gotas contém:
| cloridrato de papaverina | 10 mg |
| dipirona monoidratada | 333 mg |
| extrato de Atropa belladonna Linné (contém 0,075mg/mL de sulfato de hiosciamina) |
6 mg |
| extrato de Hyoscyamus niger Linné (contém 0,0135mg/mL de bromidrato de escopolamina) |
6 mg |
| extrato de Peumus boldus Molina (contém 0,0142mg/mL de boldina) |
12 mg |
| veículo q.s.p. | 1 mL |
Veículo: óleo essencial de Illicim verum Hook. F., álcool etílico, metilparabeno, propilparabeno, ciclamato de sódio, sacarina1 sódica di-hidratada, propilenoglicol e água.
*Cada mL da solução contém 40 gotas e cada gota2 da solução contém:
- 0,25mg de cloridrato de papaverina
- 8,325mg de dipirona monoidratada
- 0,15mg de extrato de Atropa belladonna Linné
- 0,15mg de extrato de Hyoscyamus niger Linné
- 0,30mg de extrato de Peumus boldus Molina
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE3
INDICAÇÕES
O presente estudo teve como objetivo avaliar a eficácia e a tolerabilidade da associação de papaverina, dipirona sódica e extrato fluido de Atropa belladonna, (Atroveran Composto) comparado com a associação de dipirona sódica e brometo de N-butilescopolamina ("Medicamento B") no tratamento da cólica menstrual. Foi realizado um estudo clínico mascarado, multicêntrico, fase III, aleatorizado de caráter prospectivo4, comparativo, no qual foi avaliada a eficácia (pela paciente e pelo médico) através da escala visual analógica. A avaliação da tolerabilidade foi realizada através da observação dos eventos adversos, em um episódio de cólica menstrual. Participaram do estudo 82 pacientes do sexo feminino, subdivididas em quatro grupos: medicamento A comprimido (Atroveran Composto); medicamento A solução (Atroveran Composto); medicamento B comprimido, medicamento B solução. Devido à diferença de intensidade da dor de cada paciente, o médico seguiu os seguintes critérios para determinar cada dose individual: para episódios de intensidade leve foram recomendadas 40 gotas ou dois comprimidos de A, ou 20 gotas ou um comprimido de B. Para episódios de intensidade moderada foram recomendadas 60 gotas ou três comprimidos de A, ou 30 gotas ou dois comprimidos de B. Para casos de dor de intensidade severa foram recomendadas 80 gotas ou três comprimidos de A, ou 40 gotas ou dois comprimidos de B. A significância estatística demonstrada entre o grupo tratado com o medicamento A comprimido e o grupo tratado com o medicamento B comprimido sugere que os dois tratamentos são terapeuticamente equivalentes. O grupo tratado com o medicamento B solução apresentou eficácia descritivamente maior que o grupo tratado com o medicamento A solução (Atroveran Composto), sem significância estatística. O grupo tratado com o medicamento A comprimido demonstrou eficácia significativamente maior do que o grupo tratado com o medicamento A solução. Entre os grupos tratados com o medicamento B comprimido e o medicamento B solução, a significância estatística demonstrada sugere que os dois tratamentos são terapeuticamente equivalentes. A eficácia no grupo tratado com medicamento B solução foi descritivamente maior quando comparada ao tratamento com medicamento A comprimido, não demonstrando significância estatística entre os grupos. Não foi estatisticamente significativa a diferença observada na eficácia entre o grupo tratado com medicamento B comprimido e o grupo tratado com o medicamento A solução. Os quatro medicamentos apresentaram boa tolerabilidade, porém, o tratamento com o medicamento A solução apresentou uma tolerabilidade significativamente maior que o tratamento com o medicamento A comprimido.
Referência bibliográfica:
Kaari C, Lopes CMC, Hime LFCC, et al. Avaliação clínica da eficácia e segurança da associação de papaverina, dipirona sódica e extrato fluido de Atropa belladonna* comparado com a associação de dipirona sódica e brometo de N-butilescopolamina no tratamento de cólicas5 menstruais. Rev Bras Med. 2006; 63(8): 418-26.
CARACTERÍSTICAS FARMACOLÓGICAS
cloridrato de papaverina – é o mais importante derivado do grupo benzílico quinolínico dos alcaloides do ópio. Exerce ação antiespasmódica enérgica sobre a musculatura lisa, aliviando o fenômeno dor nos espasmos6 do piloro, do esôfago7, da bexiga8, dos canais hepáticos, da vesícula biliar9, dos ureteres10 e do útero11. dipirona – a dipirona, quimicamente o fenil-dimetil-pirazolona-metilaminometanossulfonato sódico, é um agente analgésico12 e antipirético13 de largo uso clínico, tanto isolado como combinado a outros medicamentos.
Atropa belladonna – possui alcaloides de ação sobre atividade motora excessiva, como peristalse14, pilorospasmos, e espasticidade15 reflexa do cólon16.
Propriedades farmacodinâmicas
A dipirona tem ações analgésica, antipirética e anti-inflamatória. Atua inibindo a síntese das ciclooxigenases e também tem ação periférica e central.
A papaverina tem efeito relaxante direto sobre a musculatura lisa, especialmente quando esta musculatura está em estado de contração.
Causa relaxamento dos vasos sanguíneos17, coronarianos, cerebrais, pulmonares e artérias18 periféricas. Causa relaxamento dos brônquios19, trato gastrintestinal e sistema biliar.
A ação principal dos alcaloides da belladonna é um efeito potente anticolinérgico
Propriedades farmacocinéticas
Estudos farmacocinéticos revelam que a meia-vida da dipirona é de 6 a 8 horas, sendo sua eliminação por via renal20. Cerca de 90% da dose oral tem absorção gastrintestinal sob forma inalterada e sob forma do metabólito21 4-aminoantipirina. A concentração plasmática máxima ocorre entre 60 a 90 minutos.
A papaverina é rapidamente absorvida pelo trato gastrintestinal. A biodisponibilidade oral é de aproximadamente 54%. O pico máximo plasmático é atingido em cerca de 2 horas após administração de dose única oral. É metabolizada pelo fígado22 e eliminada pela urina23 sob forma inativa
Não existem estudos farmacocinéticos específicos dos alcaloides presentes na belladonna. Existem evidências que estes alcaloides são completamente absorvidos pelo trato gastrintestinal e que a ligação às proteínas24 plasmáticas destes alcaloides está entre 30 a 60%. A meia-vida dos alcaloides da belladonna varia entre 13 a 38 horas. Os alcaloides da belladonna atravessam a barreira placentária e a barreira hematoencefálica. A eliminação é feita pela urina23.
CONTRAINDICAÇÕES
O produto é contraindicado para pacientes25 que apresentarem antecedentes de hipersensibilidade a qualquer um dos componentes da fórmula.
Contraindicado em pacientes portadores de glaucoma26 de ângulo agudo27, de hipertrofia28 prostática, o uso de dipirona, em casos de amigdalite ou qualquer outra afecção29 da bucofarínge, deve merecer cuidado redobrado: esta afecção29 preexistente pode mascarar os primeiros sintomas30 de agranulocitose31 (angina32 agranulocítica), ocorrência rara, mas possível, quando se faz uso de produto que contenha dipirona. Seu uso deve ser evitado nos primeiros três meses e nas últimas seis semanas da gestação e, mesmo fora destes períodos, dipirona somente deve ser administrada a gestantes em casos de absoluta necessidade. Pacientes com asma33 ou infecções34 respiratórias crônicas, bem como pacientes com hipersensibilidade a qualquer tipo de substância, podem desenvolver choque35. Em pacientes com distúrbios hematopoiéticos, dipirona somente deve ser administrada sob controle médico.
Pacientes idosos: Não foram relatadas restrições quanto ao uso do produto em pacientes com mais de 65 anos de idade.
ADVERTÊNCIAS E PRECAUÇÕES
A administração do produto deve ser cuidadosa em pacientes portadores de doenças crônicas, sob rigorosa supervisão médica.
O produto não deve ser administrado a pacientes que façam uso de medicação entorpecente, hipnótica e barbitúrica
Durante o tratamento, recomenda-se evitar a ingestão de bebidas alcoólicas.
INTERAÇÕES MEDICAMENTOSAS
Ainda não foram totalmente relacionadas às interações do produto com outras drogas e/ou medicamentos.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar em temperatura ambiente (entre 15 e 30ºC). Proteger da luz e umidade.
O prazo de validade deste medicamento é de 24 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem. Não use medicamento com o prazo de validade vencido.
Para sua segurança, mantenha o medicamento na embalagem original.
Características físicas
ATROVERAN COMPOSTO apresenta-se como solução límpida, castanho esverdeado, sabor amargo característico de Anis e isento de partículas estranhas.
Antes de usar, observar o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Para uma melhor eficácia ATROVERAN COMPOSTO deve ser usado logo aos primeiros sintomas30.
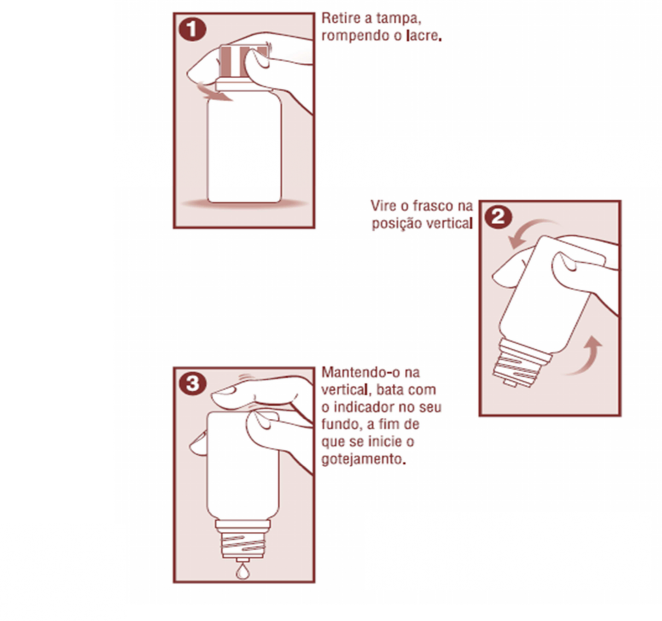
Solução Gotas - 40 gotas em um cálice d'água, 10 minutos antes das refeições, por duas a três vezes ao dia. Em casos especiais, serão aumentadas as doses, que podem ser de 40 a 80 gotas de cada vez. As crianças acima de 12 anos tomarão a metade ou o terço da dose indicada, conforme o caso.
REAÇÕES ADVERSAS
Quando usado em doses acima das recomendadas, o produto poderá ocasionar náuseas36, taquicardia37, tontura38 e congestão facial. A papaverina base frequentemente causa elevação da fosfatase alcalina39 no plasma40, indicativo da hepatotoxicidade41. Em pacientes sensíveis, independentemente da dose, a dipirona pode provocar reações de hipersensibilidade. As mais graves, embora bastante raras, são choques e discrasias sanguíneas (agranulocitose31, leucopenia42 e trombocitopenia43), que é sempre um quadro muito grave. Pacientes com história de reação de hipersensibilidade a outras drogas ou substâncias podem constituir um grupo de maior risco e apresentar efeitos colaterais44 mais intensos, até mesmo choque35. Neste caso, o tratamento deve ser imediatamente suspenso e tomadas as providências médicas adequadas. Em situações ocasionais, principalmente em pacientes com histórico de doença renal20 preexistente ou em casos de superdoagem, houve distúrbios renais transitórios com oligúria45 ou anúria46, proteinúria47 e nefrite48 intersticial49. Podem ser observados ataques de asma33 em pacientes pré-dispostos a tal condição.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA ou à Vigilância Sanitária Estadual ou Municipal.
SUPERDOSE
A lavagem gástrica50 e outras medidas para limitar a absorção intestinal devem ser procedidas sem demora.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
Siga corretamente o modo de usar, não desaparecendo os sintomas30 procure orientação médica.
Registro M.S. nº 1.7817.0042
Farm. Responsável: Fernando Costa Oliveira - CRF-GO nº 5.220
Registrado por:
Cosmed Indústria de Cosméticos e Medicamentos S.A.
Avenida Ceci, nº 282, Módulo I - Tamboré - Barueri - SP - CEP 06460-120
C.N.P.J.: 61.082.426/0002-07 – Indústria Brasileira
Fabricado por:
Brainfarma Indústria Química e Farmacêutica S.A.
VPR 1 - Quadra 2-A - Módulo 4 - DAIA - Anápolis - GO - CEP 75132-020
SAC 0800 97 99 900






