Fanhdi
GRIFOLS BRASIL LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Fanhdi®
Fator VIII
Injetável 250 UI, 500 UI, 1000 UI, 1500 UI
FORMAS FARMACÊUTICAS E APRESENTAÇÕES
Pó liófilo injetável
Apresentado em frasco com injetável liofilizado1 + seringa2 pré-carregada com diluente de 10 ml para as apresentações de 250, 500 e 1000 UI ou 15 ml para a apresentação de 1500 UI
USO ENDOVENOSO
USO PEDIÁTRICO E ADULTO
COMPOSIÇÃO
Cada frasco de Fanhdi® 250 UI contém:
| Fator VIII | 250 UI |
| (proteínas3 totais) | ≤ 90 mg |
| excipiente q.s.p. | 10 mL |
Excipientes: albumina4 humana, arginina histidina, água para injeção5.
Cada frasco de Fanhdi® 500 UI contém:
| Fator VIII | 500 UI |
| (proteínas3 totais) | ≤ 90 mg |
| excipiente q.s.p. | 10 mL |
Excipientes: albumina4 humana, arginina histidina, água para injeção5.
Cada frasco de Fanhdi® 1000 UI contém:
| Fator VIII | 1000 UI |
| (proteínas3 totais) | ≤ 90 mg |
| excipiente q.s.p. | 10 mL |
Excipientes: albumina4 humana, arginina histidina, água para injeção5.
Cada frasco de Fanhdi® 1500 UI contém:
| Fator VIII | 1500 UI |
| (proteínas3 totais) | ≤ 135 mg |
| excipiente q.s.p. | 15 mL |
Excipientes: albumina4 humana, arginina histidina, água para injeção5.
INFORMAÇÕES AO PACIENTE
PARA QUÊ ESTE MEDICAMENTO É INDICADO?
Fanhdi® é indicado na prevenção e controle de hemorragias6 em pacientes com déficit moderado ou grave de fator VIII devido à hemofilia7 A.
COMO ESTE MEDICAMENTO FUNCIONA?
Fanhdi® é o fator VIII da coagulação8 sanguínea que favorece a adesão de plaquetas9 ao endotélio vascular10 e desempenha um papel importante na agregação plaquetária.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Utilizar este medicamento com precaução em pacientes com reações alérgicas conhecidas aos componentes da preparação.
O QUE DEVO SABER ANTES DE UTILIZAR ESTE MEDICAMENTO?
Se aparecerem reações alérgicas ou anafiláticas, deverá suspender-se imediatamente a infusão (devem-se seguir os procedimentos do tratamento de choque11).
Após a administração repetida de concentrados de fator VIII humano, o nível de inibidores no plasma12 deve ser determinado.
Quando os medicamentos são feitos a partir do sangue13 ou plasma12 humano, algumas medidas são realizadas para prevenir infecções14 que podem ser passadas para os pacientes. Estas medidas incluem a seleção cuidadosa dos doadores de sangue13 e plasma12 para se garantir a exclusão de doadores com risco de padecer de infecções14, e da análise de cada doação e pools de plasma12 para sinais15 de vírus16/infecções14. Os fabricantes destes produtos incluem também etapas no processamento do sangue13 ou plasma12 que podem inativar ou remover vírus16. Apesar destas medidas, quando os medicamentos preparados a partir de sangue13 ou plasma12 humano são administrados, a possibilidade de transmissão de infecção17 não pode ser totalmente excluída. Isso se aplica a vírus16 desconhecidos ou emergentes ou outros tipos de infecções14.
As medidas adotadas são consideradas eficazes para os vírus16 encapsulados como o vírus16 da imunodeficiência18 humana (HIV19), o vírus16 da hepatite20 B e o vírus16 da hepatite20 C, e para o vírus16 não encapsulado da hepatite20 A. As medidas tomadas podem ter um valor limitado para vírus16 não encapsulados tais como o parvovírus B19.
A infecção17 por parvovírus B19 pode ser grave para uma mulher grávida (infecção17 fetal) e para pessoas cujo sistema imunológico21 esteja deprimido ou que padeçam de algum tipo de anemia22 (Exemplo: com anemia hemolítica23).
Seu médico pode lhe recomendar que seja considerada a vacinação contra hepatite20 A e B caso seja administrado regularmente concentrados de fator VIII obtidos de plasma12 humano.
É altamente recomendável que cada vez que se administre Fanhdi® a um paciente, seja registrado o nome do medicamento e nº de lote administrado a fim de manter uma relação entre o paciente e o lote do produto.
Interações medicamentosas
Não foram descritas.
Não use medicamento sem consultar o seu médico. Pode ser perigoso para sua saúde24.
Informe ao seu médico ou cirurgião dentista se você está fazendo uso de algum outro medicamento.
Informe seu médico sobre a ocorrência de gravidez25 durante o tratamento ou após seu término.
Informe ao médico ou cirurgião-dentista o aparecimento de reações indesejáveis. Informe ao médico se você estiver amamentando.
Fanhdi® é de uso restrito a hospitais.
ONDE, COMO, E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Este produto é válido por um período de até 3 (três) anos após sua data de fabricação desde que conservado adequadamente como descrito na embalagem. Conservar a temperatura não superior a 30 °C.
Não Congelar
Após a reconstituição o produto é estável química e fisicamente durante 12 horas a 25°C. Do ponto de vista microbiológico26, o produto deve ser utilizado imediatamente. Caso não seja utilizado imediatamente, o tempo e as condições de conservação antes de seu uso são responsabilidade do usuário e, normalmente não será mais que 24 horas à 2°C - 8°C, a menos que a reconstituição tenha sido realizada em condições assépticas controladas e validadas. Em nenhuma hipótese a fração não utilizada poderá ser aproveitada, nem mesmo se guardada sob refrigeração.
Número de lote e datas de fabricação e validade: vide embalagem. Não use medicamento com o prazo de validade vencido.
Para sua segurança, mantenha o medicamento na embalagem original. Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
O produto deve ser levado à temperatura ambiente (sem ultrapassar os 30°C) antes de sua administração. Administre Fanhdi® unicamente por via intravenosa. A velocidade de administração não deve ultrapassar os 10 ml/min.
Cada frasco de Fanhdi® vai acompanhado da seringa2 pré-carregada com diluente e dos acessórios necessários para sua reconstituição e administração: microfiltro, 2 toalhas com álcool, adaptador de frasco e equipo de infusão.
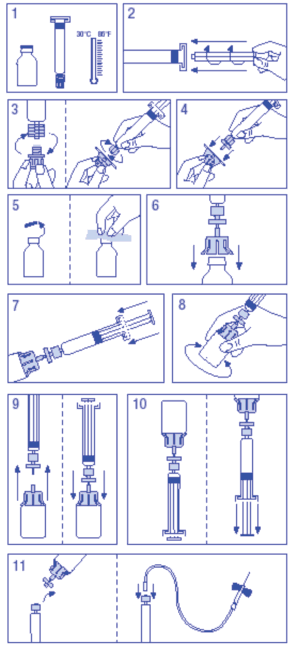
Preparação da solução
- Aquecer o frasco e a seringa2 de dissolvente sem ultrapassar os 30°C.
- Acoplar o êmbolo27 à seringa2 de dissolvente.
- Remover o lacre do filtro da embalagem. Remover o protetor da ponta da seringa2 do dissolvente e acoplá-la ao filtro.
- Remover o lacre do adaptador do frasco e acoplá-lo ao conjunto seringa2/filtro.
- Remover o lacre do frasco, desinfetando a tampa com o lenço anti-séptico.
- Introduzir o perfurador do adaptador no frasco.
- Transferir todo o dissolvente da seringa2 para o frasco.
- Agitar o frasco através de giros suaves até a total dissolução. Como todos os produtos de administração parenteral, não utilizar se a dissolução for incompleta ou apresentar partículas.
- Separar o conjunto filtro/seringa2 do restante momentaneamente a fim de remover o vácuo.
- Inverter o frasco e aspirar o conteúdo para a seringa2.
- Preparar o local da injeção5 no paciente, separar a seringa2 do restante e injetar o produto utilizando a agulha borboleta com cânula fornecida ou com uma agulha estéril a uma velocidade de 3 ml/min por via intravenosa. A velocidade de administração não deve ultrapassar os 10 ml/min a fim de evitar reações vasomotoras.
Não reutilizar os equipos de administração.
A dose e a duração do tratamento com Fanhdi® deve ajustar-se às necessidades individuais de cada paciente.
A dose necessária pode ser calculada utilizando-se a seguinte fórmula como guia:
|
N° de unidades de fator VIII requeridas (UI) = Peso corporal (Kg) × Aumento desejado de FVIII (%) × 0,5 |
Este cálculo28 está baseado no fato de que 1 UI de FVIII por kg de peso corporal aumenta a atividade plasmática de FVIII em aproximadamente 2% (ou seja: são necessários 0,5 UI/kg peso para aumentar em 1% o nível de FVIII no plasma12).
Os níveis de FVIII plasmáticos do paciente devem ser determinados e monitorizados durante o tratamento com Fanhdi®. Isto é particularmente importante no caso de intervenções cirúrgicas.
|
Tipo de hemorragia29 |
Nível plasmático de atividade de FVIII terapeuticamente necessário |
Período durante o qual é necessário manter tal nível plasmático de atividade de FVIII |
|
Hemorragias6 menores:
|
30% |
Pelo menos 1 dia, dependendo da gravidade da hemorragia29 |
|
Hemorragias6 maiores:
|
40 - 50% |
3 - 4 dias ou até alcançar uma recuperação adequada |
|
Hemorragias6 que representam risco de vida:
|
60 - 100% |
Tratamento durante 7 dias. A partir de então, terapia durante pelo menos outros 7 dias |
Pacientes com inibidores
Se o fator VIII plasmático não alcançar os níveis esperados no paciente, ou se não for possível controlar a hemorragia29 após uma dose adequada, deve-se suspeitar da presença de um inibidor.
Os hemofílicos com anticorpos33 contra o fator VIII (inibidores) requerem uma terapia específica.
Pode-se obter imunotolerância mediante o tratamento com o concentrado de fator VIII de coagulação8 do plasma12 humano.
Profilaxia
Para a profilaxia a longo prazo de hemorragias6 em pacientes com hemofilia7 A grave, deve-se administrar Fanhdi® em doses de 10 - 50 UI/kg, em intervalos de 2 - 3 dias. Em alguns casos, esp ecialmente em pacientes jovens, podem ser necessários intervalos mais curtos ou doses maiores.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Consulte imediatamente seu médico ou farmacêutico e siga suas instruções
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE CAUSAR?
Como outros medicamentos Fanhdi® pode causar alguns efeitos secundários raros como:
- reações alérgicas ou anafiláticas;
- aumento da temperatura;
- Desenvolvimento de anticorpos33 contra o fator VIII;
- Apesar do baixo conteúdo em isoaglutininas, existe algum risco de hemólise34 intravascular35;
- Não é possível excluir-se totalmente a transmissão de agentes infecciosos (ver item “4. O que devo saber antes de usar este medicamento?”).
Não existem dados robustos sobre a frequência dos efeitos indesejáveis dos ensaios clínicos36 e experiência pós-comercialização.
Informe seu médico sobre qualquer medicamento que esteja usando, antes do início, ou durante o tratamento.
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento.
Informe a empresa sobre o aparecimento de reações indesejáveis e problemas com este medicamento, entrando em contato através do Sistema de Atendimento ao Consumidor (SAC) através do 0800 709 2444.
Fanhdi® destina-se a administração intravenosa. No caso de aparecerem reações alérgicas, a infusão deverá ser imediatamente interrompida.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Não se conhecem suas consequências, visto que não foram descritos casos de superdosagem.
Fanhdi® é de uso restrito a hospitais.
DIZERES LEGAIS
USO RESTRITO A HOSPITAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Registro MS: 1.3641.0003.003-4 - 250 UI
Registro MS: 1.3641.0003.002-6 - 500 UI
Registro MS: 1.3641.0003.001-8 - 1000 UI
Registro MS: 1.3641.0003.004-2 - 1500 UI
Responsável técnico: Luiz C. de Almeida CRF/PR: 012968
Fabricado por:
Instituto Grifols, S.A.
Can Guasch, 2 - Parets del Vallès
08150 Barcelona - ESPANHA
Importado e Distribuído por:
Grifols Brasil, Ltda.
Av. Gianni Agnelli, 1909
Fazendinha 83607-430
Campo Largo - PR
CGC: 02513899/0001-71
SAC 0800 709 2444