

Aricilina
BLAU FARMACÊUTICA S.A.
IDENTIFICAÇÃO DO MEDICAMENTO
Aricilina®
benzilpenicilina potássica
Injetável 5.000.000 UI
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Pó injetável
Embalagem contendo 50 frascos-ampola de 5.000.000 UI
VIA DE ADMINISTRAÇÃO: INTRAVENOSA OU INTRAMUSCULAR
USO ADULTO OU PEDIÁTRICO
COMPOSIÇÃO:
Cada frasco-ampola de Aricilina® contém:
| benzilpenicilina potássica | 5.000.000 UI |
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE1
INDICAÇÕES
A Aricilina® está indicada no tratamento de infecções2 ocasionadas por bactérias sensíveis à penicilina G e sua ação é bactericida. A terapêutica3 deverá ser orientada por estudos bacteriológicos (incluindo testes de sensibilidade) e pela resposta clínica.
Nas seguintes situações clínicas, ocorrem usualmente respostas a doses adequadas de Aricilina®:
- Infecções2 estreptocócicas (grupo A, sem bacteremia4).
- Infecções2 leves e moderadas do trato respiratório superior e da pele5.
- Infecções2 venéreas: sífilis6, bouba, bejel (sífilis6 endêmica) e pinta.
- Profilaxia da glomerulonefrite7 aguda e doença reumática.
- Profilaxia de recorrências8 da febre reumática9 e/ou coreia.
CARACTERÍSTICAS FARMACOLÓGICAS
Farmacocinética e Farmacodinâmica
A Aricilina® (penicilina G potássica ou benzilpenicilina potássica) é uma penicilina natural, do grupo dos beta-lactâmicos que exerce ação bactericida durante o estágio de multiplicação ativa dos microrganismos sensíveis. Atua por inibição da biossíntese do mucopeptídeo da parede celular. Aproximadamente 60% das benzilpenicilinas administradas se ligam às proteínas10 plasmáticas e se distribuem amplamente pelos vários tecidos do organismo. Os níveis mais elevados são encontrados nos rins11 e, em menores concentrações, no fígado12, pele5 e intestinos13; a presença da benzilpenicilina ocorre em menor grau no líquor14.
Com função renal15 normal, a droga é rapidamente excretada pelos túbulos renais. Em recém-nascidos e crianças pequenas, como em indivíduos com função renal15 comprometida, a excreção encontra-se consideravelmente retardada.
A benzilpenicilina desempenha elevada atividade “in vitro” contra estafilococos (exceto as cepas16 produtoras de penicilinase), estreptococos (grupos A, C, G, H, L e M) e pneumococos.
Outros microrganismos sensíveis à atividade terapêutica3 da benzilpenicilina são: Neisseria gonorrhoeae, Corynebacterium diphtheriae, Bacillus anthracis, Clostridium sp., Actinomyces bovis, Streptobacillus moniliformis, Listeria monocytogenes e Leptospira.
O Treponema pallidum é extremamente sensível à ação bactericida da benzilpenicilina.
CONTRAINDICAÇÕES
A Aricilina® está contraindicada para pacientes17 com hipersensibilidade as penicilinas e cefalosporinas.
Em caso de dúvida, é essencial que o médico esteja presente durante a primeira administração, para tratar qualquer possível reação anafilática18. É possível a ocorrência de reação de sensibilidade cruzada em pacientes alérgicos a penicilinas ou a outros antibióticos beta- lactâmicos.
ADVERTÊNCIAS E PRECAUÇÕES
Para a prescrição de Aricilina®, é necessário realizar anamnese19 preliminar, buscando identificar um passado alérgico, particularmente, relacionado com hipersensibilidade aos antibióticos beta-lactâmicos.
Caso ocorra uma reação de hipersensibilidade, o tratamento deve ser interrompido.
A utilização de Aricilina® deve ser realizada com extremo cuidado em pacientes sensíveis, devido à possibilidade de ocorrência de hipersensibilidade cruzada entre penicilinas e cefalosporinas em 5 a 10% dos casos; uma monitoração cuidadosa é necessária na primeira administração. Reações de hipersensibilidade que ocorram com estas duas famílias de antibióticos podem ser sérias ou mesmo fatais.
Devem-se realizar culturas ao término do tratamento para detectar se os estreptococos foram totalmente erradicados, caso contrário, as sequelas20 da doença estreptocócica poderão surgir.
Em tratamentos prolongados com penicilinas, particularmente quando são utilizados regimes de altas doses, recomendam-se avaliações periódicas das funções renal15 e hematopoiética. O uso de antibióticos poderá resultar em proliferação de microrganismos resistentes, assim é essencial uma constante observação do paciente. Se aparecerem novas infecções2 por bactérias ou fungos durante a terapia, devem-se tomar medidas apropriadas.
Durante a administração intramuscular do medicamento, devem-se evitar acidentes, incluindo injeção21 intra-arterial direta ou próxima às artérias22, que podem resultar em danos neuromusculares graves, como a mielite23 transversa com paralisia24 permanente, a necrose25 e gangrena26 de porções mais próximas das extremidades e nos locais de injeção21. Pode também ocorrer palidez imediata, cianose27 ou lesões28 musculares nas extremidades distal29 e proximal30 do local de injeção21 seguidas de formação de vesículas31, edema32 intenso, requerendo fasciotomia anterior e /ou posterior na extremidade inferior. As reações descritas ocorrem com maior frequência em crianças pequenas. Injeções em nervos ou próximas a nervos podem resultar em lesões28 permanentes.
Uso durante a gravidez33
As penicilinas atravessam a barreira placentária, mas não existem relatos de problemas para o feto34.
Categoria de risco na gravidez33: B.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Uso durante a amamentação35
Aricilina® é excretada para o leite materno, podendo ocasionar diarreia36 e candidíase37, no lactente38. A presença de reações alérgicas ou alguma outra alteração no lactente38 pode estar relacionada com a eliminação do medicamento, através do leite.
Uso pediátrico
A Aricilina® oferece segurança para o uso em crianças e em neonatos39. O uso de penicilinas, nesse grupo de pacientes, deve ser acompanhado de avaliações frequentes devido ao desenvolvimento renal15 incompleto, o que pode diminuir a taxa de eliminação do medicamento.
Uso em pacientes com comprometimento renal15
A eliminação do medicamento está diminuída em pacientes com comprometimento da função renal15.
Uso em idosos, crianças e outros grupos de risco
Seguir orientações anteriores. Não há contraindicações relativas à pacientes idosos.
INTERAÇÕES MEDICAMENTOSAS
A administração concomitante ou subsequente de drogas potencialmente nefrotóxicas (como os aminoglicosídeos) exige uma estreita
monitoração da função renal15, através de dados clínicos e dos níveis sanguíneos da creatinina40 e / ou pela medida da depuração da creatinina40 endógena. Na presença de diminuição da função renal15 por agressão tóxica poderá ocorrer a diminuição da depuração da creatinina40 endógena e / ou elevação dos níveis sanguíneos da creatinina40. Por inibir a secreção renal15, a administração simultânea de probenecida aumenta a concentração sérica da penicilina e prolonga a sua duração de ação.
A tetraciclina, um antibiótico bacteriostático41, pode antagonizar o efeito bactericida da penicilina. Os antibióticos do grupo dos aminoglicosídeos não devem ser misturados com as penicilinas na mesma solução para uso parenteral, devido ao risco de inativação substancial do aminoglicosídeo. O uso concomitante de penicilina e bloqueadores beta-adrenérgicos42 pode aumentar o risco e a gravidade de reações anafiláticas43. Pacientes em tratamento com beta-bloqueadores são menos sensíveis a epinefrina e, portanto, é mais difícil tratar quadros de anafilaxia44 nestes indivíduos. O uso concomitante de cloranfenicol pode diminuir o efeito da penicilina e aumentar a meia-vida do cloranfenicol.
A utilização de altas doses de penicilina, por via intravenosa, em pacientes que estejam usando heparina e anticoagulantes45 orais, pode causar alterações na coagulação46 do sangue47, aumentando o risco de sangramento.
Interferências em exames laboratoriais
As penicilinas podem interferir com a medida da glicosúria48 realizada pelo método do sulfato de cobre, ocasionando resultados falso-positivos ou mesmo falso-negativos. Esta interferência não ocorre com o método da glicose49-oxidase.
Incompatibilidades
Não se recomenda a mistura de Aricilina® com outras medicações. A mistura de antibacterianos beta-lactâmicos (penicilinas e cefalosporinas) e aminoglicosídeos podem resultar em inativação de ambas as substâncias. Se houver indicação clínica, elas devem ser administradas por vias separadas (não misturá-las no mesmo frasco ou numa mesma bolsa para infusão intravenosa).
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar o medicamento em temperatura ambiente entre 15°C e 30°C e proteger da umidade.
Prazo de validade: 36 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Pó cristalino50 branco ou cristais brancos a incolores, praticamente inodoro e moderadamente higroscópico.
Aspecto após reconstituição: Solução límpida, incolor a levemente amarelada, isenta de partículas visíveis.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Reconstituição
O profissional da saúde1, antes da reconstituição do medicamento, deve verificar a aparência do pó, no interior do frasco-ampola, buscando identificar alguma partícula que possa interferir na integridade e na qualidade do medicamento.
Para a reconstituição da solução de Aricilina®, utilizam-se 2 mL de água para injetáveis para cada 1 milhão de UI de penicilina, ou seja, para a reconstituição do frasco-ampola de Aricilina®, são necessários 10 mL de água para injetáveis, resultando em um volume final de 12 mL. Para a completa homogeneização da solução, recomenda-se agitar o frasco-ampola vigorosamente antes da retirada da dose a ser injetada, conforme figura abaixo:
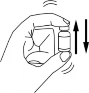
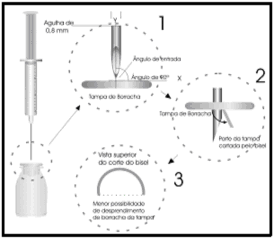
Com a finalidade de evitar o aparecimento de partículas de borracha após a inserção de agulha no frasco-ampola, proceder da seguinte forma:
- Encaixar uma agulha de injeção21 de no máximo 0,8 mm de calibre;
- Encher a seringa51 com o diluente apropriado;
- Segurar a seringa51 verticalmente à borracha;
- Perfurar a tampa dentro da área marcada, deixando o frasco-ampola firmemente na posição vertical;
- É recomendado não perfurar mais de 4 vezes a área demarcada (ISO 7864).
Veja abaixo o procedimento:
Após a reconstituição, o profissional da saúde1 deverá inspecionar cuidadosamente, antes de sua utilização, se a solução no interior do frasco- ampola de vidro incolor está na forma líquida, livre de fragmentos52 ou de alguma substância que possa comprometer a eficácia e a segurança do medicamento. O profissional não deverá utilizar o produto ao verificar qualquer alteração que possa prejudicar a saúde1 do paciente.
Para evitar problemas de contaminação, deve-se tomar cuidado durante a reconstituição para assegurar assepsia53.
Administração
Para infusão intravenosa, diluir com soro54 fisiológico55 a 0,9% ou soro54 glicosado a 5%, a solução inicialmente reconstituída, observando-se uma concentração final de 50.000 UI/mL. Infundir durante 30 a 60 minutos.
Deve-se considerar que cada milhão de unidades desse medicamento contém 1 mEq de potássio e que a infusão de 10 mEq ou mais de potássio por hora necessita de acompanhamento adequado das concentrações séricas desse eletrólito56 e / ou acompanhamento eletrocardiográfico.
Para crianças, a velocidade máxima da infusão de potássio deve ser de 0,25 mEq/kg/hora (a posologia total em 24 horas deve ser de 50.000 a 250.000 UI/ kg, que pode ser dividida em quatro etapas, isto é, de 6 em 6 horas).
A injeção21 intravenosa deve ser extremamente cuidadosa e lenta. Nos casos de infecções2 por estreptococos, o período de tratamento deve ser de, no mínimo, 10 dias.
A via intramuscular está praticamente reservada para uso em crianças menores, devido ao menor volume do produto a ser administrado, considerando-se o menor peso corporal nessa faixa etária e a posologia recomendada.
Nos casos de administração do medicamento, por via intramuscular, a aplicação deve ser realizada profundamente no quadrante superior lateral da nádega ou na face57 lateral da coxa58. Para doses repetidas, recomenda-se variar o local da injeção21. A injeção21 deve ser feita lentamente. Interrompa a administração se o paciente queixar-se de dor intensa no local ou se, em crianças, ocorrerem sinais59 e sintomas60 que sugiram dor intensa.
Posologia
A dose e a via de administração depende do tipo e da severidade da infecção61. A dosagem varia de 0,6 a 2,4 g de Penicilina G potássica diárias, divididas em 2 ou 4 vezes.
Adultos: A dose usual é de 1.000.000 a 5.000.000 UI diárias, divididas em 4 intervalos de 2 a 6 horas, geralmente administradas por infusão intravenosa.
Doses mais altas, atingindo 10.000.000 e 30.000.000 UI diários, poderão ser necessárias para o tratamento de casos de endocardite62, meningite63 meningocócica e pneumocócica.
Crianças: A dose usual é de 100.000 a 250.000 UI/kg/dia, dividida em intervalos a cada 6 horas. Para as crianças recém-nascidas, com menos de sete dias: com peso menor que 2 kg, a dose é de 50.000 UI/kg/dia, dividida em intervalos de 12 horas, e as, com peso maior que 2 kg, a dose é de 75.000 UI/kg/dia, dividida em intervalos de 8 horas.
Para as crianças maiores de sete dias, com peso menor que 2 kg, a dose é de 75.000 UI/kg/dia, dividida em intervalos de 8 horas e para as com peso maior que 2 kg a dose é de 100.000 UI/kg/dia, dividida em intervalos de 6 horas.
Nos casos de meningite63: em neonatos39, a dose é de 150.000 a 250.000 UI/kg/dia, por via intravenosa, administrada a intervalos de 4 a 6 horas e em crianças maiores, a dose é de 250.000 UI/kg/dia, por via intravenosa ou intramuscular, administrada a intervalos de 3 a 6 horas.
Conduta necessária caso haja esquecimento de administração
Caso haja esquecimento de administração de uma dose, esta deverá ser feita assim que possível, respeitando-se, a seguir, o intervalo determinado pela posologia.
NUNCA DEVEM SER ADMINISTRADAS DUAS DOSES AO MESMO TEMPO.
REAÇÕES ADVERSAS
As reações de hipersensibilidade são as mais comuns e independem da dose. Incluem urticária64, prurido65, edema angioneurótico66, laringoespasmo, broncoespasmo67, hipotensão68, colapso69 vascular70, erupções cutâneas71 desde a forma maculopapulosa até a dermatite72 esfoliativa, eritema multiforme73, reações semelhantes à doença do soro54 (febre74, calafrios75, edema32, artralgia76 e mialgia77), edema32 de laringe78; miocardite79, cujas reações iniciais caracterizam-se por erupções, febre74 e eosinofilia80. Reações anafiláticas43 fatais têm sido relatadas.
Podem também ocorrer reações adversas envolvendo o sistema linfático81 e hematopoiético, incluindo as alterações na coagulação46 sanguínea, nefropatias82, neuropatias, eosinofilia80, trombocitopenia83 e anemia hemolítica84 em consequência de altas doses por via intravenosa, no entanto estas geralmente são reversíveis após a interrupção do tratamento.
Pode ocorrer um aumento transitório na creatinina40 sérica, especialmente quando coadministrado com aminoglicosídeos e raramente pode ocorrer nefrite85 intersticial86.
A administração de altas doses de antibióticos beta-lactâmicos, particularmente em pacientes com insuficiência renal87, pode resultar em encefalopatia88 (com prejuízo da consciência, movimentos anormais e convulsão89). Em doses maiores que 10.000.000 UI, por via intravenosa, pode ocorrer intoxicação por potássio principalmente em pacientes com insuficiência renal87. Os sintomas60 incluem: hiper-reflexia, convulsão89, coma90, arritmia91 cardíaca e parada cardíaca. Convulsões, parestesias92 e irritabilidade neuromuscular podem ser observadas com altas doses. As reações locais mais comuns são: irritação inflamatória, dor no local da aplicação, equimose93, trombose94 e hematoma95.
Como ocorre com a utilização de outros antibióticos, o uso prolongado de Aricilina® pode resultar em crescimento excessivo de organismos não susceptíveis.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA ou à Vigilância Sanitária Estadual ou Municipal.
SUPERDOSE
Em casos de administração de altas doses de Aricilina®, não existe antídoto96 específico.
O tratamento é sintomático97 e deve ser acompanhado das medidas de apoio ao estado geral do paciente.
Aos primeiros sinais59 de choque anafilático98 (transpiração99, náusea100, cianose27) interromper imediatamente a administração, mantendo ou providenciando uma via de acesso venoso. Além das medidas usuais de emergência101, colocar o paciente na posição horizontal com as pernas elevadas e as vias aéreas desobstruídas. De acordo com o quadro clínico do paciente, pode ser necessária a utilização de epinefrina, de expansores plasmáticos e de corticosteroides. Outras medidas terapêuticas como: respiração artificial102, inalação de oxigênio, administração de anti-histamínicos podem ser empregadas, a critério médico.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Reg. M.S. nº 1.1637.0108
Farm. Resp.: Eliza Yukie Saito - CRF-SP n° 10.878
Registrado por:
Blau Farmacêutica S.A.
CNPJ 58.430.828/0001-60
Rodovia Raposo Tavares Km 30,5 n° 2833 - Prédio 100
CEP 06705-030 - Cotia – SP
Indústria Brasileira
Fabricado por:
Blau Farmacêutica S.A.
CNPJ 58.430.828/0013-01
Rua Adherbal Stresser, 84
CEP 05566-000 - São Paulo – SP
Indústria Brasileira
SAC 0800 701 6399






