Enbrel PFS
LABORATÓRIOS PFIZER LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Enbrel® PFS
etanercepte
Injetável 50 mg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Cartucho contendo 4 seringas preenchidas com solução injetável contendo 50 mg de etanercepte e 4 lenços umedecidos com álcool.
USO SUBCUTÂNEO1
USO ADULTO E PEDIÁTRICO ACIMA DE 8 ANOS DE IDADE
COMPOSIÇÃO:
Cada seringa2/caneta de aplicação plástica de Enbrel® PFS contém:
| etanercepte | 50 mg |
| excipiente q.s.p. | 1 seringa2 |
Excipientes: fosfato de sódio dibásico diidratado, fosfato de sódio monobásico diidratado, cloridrato de arginina, cloreto de sódio, sacarose (açúcar3) e água para injetáveis.
Não contém conservante.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Adultos com artrite reumatoide4
Enbrel® PFS está indicado para redução dos sinais5 e sintomas6 e inibição da progressão do dano estrutural em pacientes com artrite reumatoide4 ativa moderada a grave.
Enbrel® PFS pode ser iniciado em associação ao metotrexato ou em monoterapia.
Enbrel® PFS está indicado no tratamento da artrite reumatoide4 ativa moderada a grave, quando a resposta a um ou mais DMARDs (drogas modificadoras da doença artrite reumatoide4) se mostrar insatisfatória.
Adultos com artrite7 psoriásica
Enbrel® PFS é indicado na inibição do dano estrutural e na redução de sinais5 e sintomas6 de pacientes com artrite7 psoriásica.
Adultos com espondilite anquilosante
Enbrel® PFS é indicado para redução dos sinais5 e sintomas6 em pacientes com espondilite anquilosante ativa.
Adultos com espondiloartrite axial não radiográfica
Enbrel® PFS é indicado para o tratamento de adultos com espondiloartrite axial não radiográfica grave com sinais5 de inflamação8, conforme indicado pela elevação de proteína C reativa (PCR9) e/ou alteração à ressonância magnética10, que tenham apresentado uma resposta inadequada ou que são intolerantes à terapia convencional11.
Adultos com psoríase12 em placas13
Enbrel® PFS é indicado para o tratamento de pacientes adultos (18 anos ou mais) com psoríase12 crônica em placas13 moderada a grave que são candidatos a terapia sistêmica ou fototerapia.
Pacientes pediátricos com psoríase12 em placas13
Enbrel® PFS é indicado para o tratamento de psoríase12 crônica grave em placas13 em crianças e adolescentes a partir de 8 anos de idade que estão inadequadamente controlados ou são intolerantes a outra terapia sistêmica ou fototerapia.
COMO ESTE MEDICAMENTO FUNCIONA?
Enbrel® PFS é um medicamento antirreumático, obtido por biotecnologia. Age diminuindo a dor e o inchaço14 das articulações15 e retardando o dano causado pela doença ativa moderada a grave, que pode resultar em comprometimento da função da articulação16.
Enbrel® PFS age ligando-se a uma substância conhecida como TNF (fator de necrose17 tumoral), bloqueando sua atividade e reduzindo a dor e a inflamação8 associadas à artrite reumatoide4, artrite7 psoriásica, espondilite anquilosante e psoríase12 crônica.
O tempo médio estimado para início de ação de Enbrel® PFS é de 2 semanas, podendo se modificar a depender da gravidade dos sintomas6.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Enbrel® PFS é contraindicado em pessoas com alergia18 conhecida a qualquer um de seus componentes.
Enbrel® PFS é contraindicado em pacientes com infecção19 generalizada ou em risco de desenvolvê-la.
O tratamento com Enbrel® PFS não deve ser iniciado em pacientes com infecções20 ativas sérias, incluindo infecções20 crônicas ou localizadas.
Este medicamento é contraindicado para menores de 4 anos de idade.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Procure seu médico imediatamente se desenvolver uma nova infecção19 durante o tratamento com Enbrel® PFS. Se você desenvolver uma infecção19 séria durante o tratamento, este deverá ser descontinuado, sob a orientação do seu médico.
O uso de Enbrel® PFS e anakinra não é recomendado.
O uso de Enbrel® PFS em pacientes para o tratamento da hepatite21 alcoólica não é recomendado. Médicos devem ter cuidado quando o Enbrel® PFS for usado em pacientes que apresentem hepatite21 alcoólica moderada a grave.
A tampa das agulhas da seringa2 e da caneta de aplicação plástica contém látex (borracha natural seca). Os pacientes ou seus cuidadores devem entrar em contato com o médico antes de usar o Enbrel® PFS se a tampa da agulha for manuseada ou se o Enbrel® PFS for administrado a alguém com hipersensibilidade (alergia18) conhecida ou possível ao látex.
Foram relatadas reações alérgicas associadas à administração de Enbrel® PFS. Caso ocorra alguma reação alérgica22, procure o seu médico imediatamente.
Existe a possibilidade das terapias anti-TNF, incluindo o Enbrel® PFS, comprometerem a defesa do paciente contra infecções20 e doenças malignas, pois o TNF é responsável pela mediação da inflamação8 e pela resposta imunológica celular. Casos de leucemia23 têm sido reportados em pacientes tratados com antagonistas do TNF.
Doenças malignas (particularmente linfomas de Hodgkin e não Hodgkin), algumas fatais, foram relatadas entre crianças e adolescentes que receberam tratamento com antagonistas do TNF, incluindo Enbrel® PFS. A maioria dos pacientes recebeu imunossupressores concomitantemente.
A qualquer sinal24 de infecção19 ou comprometimento das funções de coagulação25 e defesa do organismo (por ex.: febre26 persistente, dor de garganta27, hematomas28, sangramento, palidez), comunique seu médico imediatamente. Ele tomará as providências necessárias.
Recomenda-se ao médico uma avaliação cuidadosa da relação risco/benefício ao prescrever este medicamento a pacientes com doença neurológica degenerativa29 (por ex.: diagnóstico30 conhecido de esclerose múltipla31) preexistente ou de início recente.
O médico deve ter cautela ao utilizar este medicamento em pacientes que também sofrem de insuficiência cardíaca congestiva32.
Foi relatada hipoglicemia33 após iniciação de Enbrel® PFS em pacientes recebendo medicação para diabetes34, sendo necessária redução da medicação antidiabetes em alguns desses pacientes.
Gravidez35 e Lactação36
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião- dentista.
Não deve ser utilizado durante a gravidez35 e amamentação37, exceto sob orientação médica. Informe ao seu médico ou cirurgião-dentista se ocorrer gravidez35 ou iniciar amamentação37 durante o uso deste medicamento.
Efeitos na habilidade de dirigir e usar máquinas
Não foram realizados estudos dos efeitos do uso de Enbrel® PFS sobre a capacidade de dirigir veículos e operar máquinas.
Atenção: Este medicamento contém açúcar3, portanto, deve ser usado com cautela em portadores de Diabetes34.
Interações Medicamentosas
Não utilizar o produto em associação ao anakinra. Pode-se utilizar Enbrel® PFS com glicocorticoides, anti- inflamatórios não esteroides (AINEs), analgésicos38 ou metotrexato, desde que sob orientação de seu médico.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde39.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Conservar a solução injetável sob refrigeração (temperatura entre 2–8°C). Após refrigeração, a solução deverá atingir a temperatura ambiente antes da injeção40.
Manter a seringa2 e a caneta de aplicação plástica na embalagem para proteger da luz.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Enbrel® PFS é uma solução injetável límpida a levemente opalescente e incolor a levemente amarelada, e o líquido pode conter traços de partículas amorfas translúcidas a brancas. Na caneta de aplicação plástica , a solução pode ser visualizada pela janela de inspeção41.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Somente para uso subcutâneo1.
Instruções para Preparo e Administração da Seringa2 Preenchida
Este item está dividido nos seguintes subitens:
Introdução
- Passo 1: Preparo antes da administração
- Passo 2: Escolha do local da administração
- Passo 3: Administração da solução de Enbrel® PFS
- Passo 4: Descarte dos materiais
Introdução: As orientações a seguir explicam como preparar e administrar Enbrel® PFS. Estas orientações devem ser lidas com atenção e seguidas passo a passo. O médico ou seu assistente irão orientá-lo sobre as técnicas de administração do medicamento em si mesmo (autoadministração) ou em uma criança. Não tente aplicar a injeção40 sem estar certo de que compreendeu como preparar e administrar o medicamento.
A solução de Enbrel® PFS não deve ser misturada com nenhum outro medicamento antes do uso.
Passo 1: Preparo antes da administração
- Escolha uma superfície de trabalho plana, limpa e bem-iluminada.
- Retire do refrigerador a embalagem com as seringas preenchidas do Enbrel® PFS e coloque-a sobre a superfície de trabalho plana. Retire uma seringa2 preenchida e um lenço umedecido com álcool e coloque-os sobre a superfície de trabalho. Não agite a seringa2 preenchida de Enbrel® PFS. Recoloque a embalagem com as seringas preenchidas que não serão utilizadas de volta no refrigerador (2°C a 8°C). Se tiver dúvidas quanto ao armazenamento do produto, entre em contato com o médico, o enfermeiro ou o farmacêutico para mais orientações.
- Verifique a data de validade na seringa2 preenchida. Se a data de validade estiver vencida, não use a seringa2 preenchida e entre em contato com o farmacêutico para orientações.
- Espere 15 a 30 minutos para permitir que o Enbrel® PFS na seringa2 preenchida atinja a temperatura ambiente.
NÃO remova a tampa da agulha enquanto a seringa2 estiver em repouso. Aguardar até que a solução atinja a temperatura ambiente faz com que a injeção40 seja mais confortável para você. Não aqueça o Enbrel® PFS de nenhuma outra forma (por exemplo, não use forno de microondas ou água quente). - Reúna os outros materiais que você precisará para a injeção40. Entre eles estão o lenço umedecido com álcool fornecido no cartucho do Enbrel® PFS e um chumaço de algodão ou gaze.
- Lave as mãos42 com sabão e água quente.
- Examine a solução na seringa2 preenchida. Ela deve estar límpida a levemente opalescente e incolor a levemente amarelada, e o líquido pode conter traços de partículas amorfas translúcidas a branca. Esta aparência é normal para Enbrel® PFS. Não utilize a solução se estiver desbotada, turva, ou se outras partículas além das descritas acima estiverem presentes. Se você estiver preocupado com a aparência da solução, entre em contato com o farmacêutico para orientações.
Passo 2: Escolha do local da administração
- Os três locais recomendados para a administração do Enbrel® PFS usando a seringa2 preenchida são: (1) a face43 anterior da parte média da coxa44; (2) o abdome45, com exceção da área de 5 cm ao redor do umbigo46 e (3) a região externa do braço (ver imagem). Para a autoinjeção não se deve usar a região externa do braço.

- A cada nova aplicação, escolha um local diferente, a pelo menos 3 cm de distância do local de aplicação anterior. Não aplique a injeção40 em áreas em que a pele47 esteja sensível, com hematoma48, avermelhada ou endurecida. Evitar áreas com cicatrizes49 ou estrias.
- Se você ou a criança tem psoríase12, deve tentar não administrar diretamente o produto em nenhuma placa50 cutânea51 saliente, espessa, avermelhada ou com descamação52 (“lesões cutâneas53 da psoríase”).
Passo 3: Injeção40 da solução do Enbrel® PFS
- Limpe o local onde o Enbrel® PFS será injetado com um lenço umedecido com álcool fazendo movimentos circulares. NÃO toque mais nessa região antes da aplicação da injeção40.
- Pegue a seringa2 preenchida da superfície de trabalho plana. Retire a tampa da agulha puxando firmemente em linha reta (ver imagem). Tenha cuidado para não dobrar ou torcer a tampa da agulha durante a sua retirada evitando danos à agulha.
Quando a tampa da agulha é removida, pode haver uma gota54 da solução no fim da agulha; isso é normal. Não toque na agulha nem deixe que ela toque em nenhuma superfície. Não toque nem empurre o êmbolo55. Isso pode provocar extravasamento do líquido.

- Faça uma prega na área limpa da pele47 quando estiver seca e segure-a firmemente com uma mão56. Com a outra mão56, segure a seringa2 como um lápis.
- Com um movimento rápido e curto, empurre a agulha toda na pele47 em um ângulo entre 45° e 90° (ver imagem). Com a experiência, você encontrará o ângulo que é mais confortável para você. Tenha cuidado para não empurrar a agulha na pele47 muito lentamente, ou com muita força.

- Quando a agulha estiver completamente inserida na pele47, solte a pele47. Com a mão56 livre, segure a seringa2 próxima à base para estabilizar. Então empurre lentamente o êmbolo55 para injetar toda a solução em uma velocidade estável (ver imagem).

- Quando a seringa2 estiver vazia, retire a agulha da pele47 tendo o cuidado de mantê-la no mesmo ângulo em que foi inserida. Pode ocorrer um pequeno sangramento no local da administração. Você pode pressionar um chumaço de algodão ou gaze sobre o local da administração por 10 segundos. NÃO esfregue o local da administração. Se necessário você pode cobrir o local da administração com um curativo.
Passo 4: Descarte dos materiais
- A seringa2 preenchida é para administração única. A seringa2 e a agulha NUNCA devem ser reutilizadas.
NUNCA reencapar a agulha. Descarte a agulha e a seringa2 conforme orientação do médico, enfermeiro ou farmacêutico.
Todas as dúvidas devem ser esclarecidas por um médico, enfermeiro ou farmacêutico que estejam familiarizados com Enbrel® PFS.
Instruções para Preparo e Administração da Caneta de aplicação plástica
Este item está dividido nos seguintes subitens:
- Passo 1: Preparo antes da administração de Enbrel® PFS
- Passo 2: Escolha do local de administração
- Passo 3: Administração da solução de Enbrel® PFS
- Passo 4: Descarte da caneta MYCLIC® usada
Introdução: As instruções abaixo explicam como usar a caneta MYCLIC® para administrar Enbrel® PFS. Leia cuidadosamente as instruções e siga o passo a passo. Seu médico ou enfermeiro dirá como você deve administrar o Enbrel® PFS. Não tente administrar a injeção40 até ter certeza de que você entendeu como usar a caneta MYCLIC® de forma adequada. Caso tenha dúvidas sobre como aplicar a injeção40, peça ajuda ao médico ou enfermeiro.
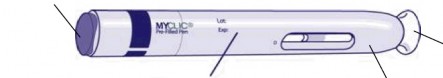
Passo 1: Preparo antes da administração de Enbrel® PFS
- Escolha um local limpo, plano e bem iluminado.
- Reúna os itens que você precisará para sua administração e coloque-os no local escolhido:
- Uma caneta de aplicação plástica e um lenço umedecido com álcool (pegue esses itens na embalagem da caneta de aplicação plástica que você mantém no refrigerador). Não agite a caneta.
- Um chumaço de algodão ou gaze.
- Confira a data de validade (mês/ano) na caneta. Se a data estiver ultrapassada, não use a caneta e entre em contato com seu farmacêutico para assistência.
- Inspecione a solução da caneta olhando através da janela de inspeção41 transparente. A solução deve ser límpida ou levemente opalescente, incolor ou amarela clara, e pode conter pequenas partículas de proteína brancas ou quase transparentes. Esta aparência é normal para Enbrel® PFS. Não utilize a solução se estiver desbotada, turva, ou se outras partículas além das descritas acima estiverem presentes. Se você estiver preocupado com a aparência da solução, contate seu farmacêutico para assistência.
- Deixe a tampa da agulha no lugar e espere aproximadamente 15 a 30 minutos para permitir que a solução de Enbrel® PFS na caneta alcance a temperatura ambiente. Não aqueça de outra forma. Aguardar até que a solução atinja a temperatura ambiente faz com que a injeção40 seja mais confortável para você. Sempre deixe a caneta fora do alcance e da visão57 de crianças.
Enquanto espera a solução da caneta alcançar a temperatura ambiente, leia o Passo 2 (abaixo) e escolha um local para a administração.
Passo 2: Escolha do local de administração
- O local recomendado para a administração é no meio da parte frontal das coxas58. Caso prefira, você poderá usar como alternativa a área da barriga, mas certifique-se de escolher um local com pelo menos 5 cm de distância do umbigo46. Caso outra pessoa esteja aplicando a injeção40, a área externa na parte superior do braço pode ser usada.

- Cada nova injeção40 deve ser administrada a pelo menos 3 cm de distância de onde você aplicou na última vez.
Não injete em locais moles, com machucados ou duros. Evite locais com cicatrizes49 ou estrias. (Pode ser útil manter um registro dos locais de administração anteriores). - Caso tenha psoríase12, você deve tentar não aplicar a injeção40 diretamente em qualquer local que apresente elevações, espessamento, vermelhidão ou esteja com aparência escamosa59.
Passo 3: Administração da solução de Enbrel® PFS
- Depois de esperar aproximadamente 15 a 30 minutos para a solução na caneta alcançar a temperatura ambiente, lave suas mãos42 com água e sabão.
- Limpe o local da administração com o lenço umedecido com álcool com movimentos circulares e deixe secar. Não toque novamente essa área até a administração.
- Pegue a caneta e remova a tampa branca puxando-a até que saia completamente (ver imagem). Para evitar dano à agulha que está dentro da caneta, não dobre a tampa branca da agulha enquanto estiver removendo a tampa e não a coloque de volta depois de removida. Após a retirada da tampa da agulha, você verá uma proteção de segurança roxa da agulha estendendo-se levemente no final da caneta. A agulha permanecerá protegida dentro da caneta até que esta seja ativada. Não use a caneta se ela cair no chão sem a tampa da agulha.

- Beliscar levemente a pele47 ao redor do local de aplicação entre o polegar e o dedo indicador da mão56 livre pode tornar a injeção40 mais fácil e confortável.
- Segure a caneta em um ângulo reto60 (90°) no local de administração e pressione firmemente a abertura da caneta contra a pele47 para que a proteção de segurança da agulha seja empurrada completamente para dentro da caneta. Será observada uma leve depressão na pele47 (ver imagem). A caneta pode apenas ser ativada quando a proteção da agulha for completamente empurrada para dentro da caneta.

- Enquanto empurra firmemente a caneta contra a pele47 para garantir que a proteção de segurança da agulha esteja completamente dentro da caneta, com o polegar pressione o centro do botão verde no topo da caneta para iniciar a injeção40. Observação: se você não conseguir iniciar a aplicação conforme descrito, pressione a caneta mais firmemente contra sua pele47, então pressione o botão verde novamente.

- Ao ouvir um segundo clique (ou , se você não ouvir o segundo click, após terem passado 10 segundos) sua administração estará completa (ver Diagrama 6). A partir deste momento, você poderá levantar a caneta de sua pele47. Conforme você levantar a caneta, a proteção de segurança roxa da agulha irá automaticamente se estender para cobrir a caneta (ver imagem).

- A janela de inspeção41 da caneta deverá estar completamente roxa, confirmando que a dose foi injetada corretamente (ver Diagrama 8). Caso a janela não esteja completamente roxa, contate o enfermeiro ou o farmacêutico para assistência, uma vez que a caneta pode não ter injetado completamente a solução de Enbrel® PFS. Não tente usar a caneta novamente e não tente usar outra caneta sem o consentimento do enfermeiro ou farmacêutico.

- Caso você observe um pouco de sangue61 no local de administração, você deverá pressionar o local da administração com um chumaço de algodão ou gaze durante 10 segundos. Não esfregue o local da administração.
Passo 4: Descarte da caneta MYCLIC® usada
A caneta deve ser usada apenas uma vez – ela nunca deverá ser reutilizada. Descarte a caneta usada conforme as instruções de seu médico, enfermeiro ou farmacêutico. Não tente tampar a caneta.
Em caso de dúvida, converse com um médico, enfermeiro ou farmacêutico que estejam familiarizados com Enbrel® PFS.
POSOLOGIA
Pacientes adultos (≥18 anos) com artrite reumatoide4
A dose recomendada para pacientes62 adultos com artrite reumatoide4 é de 50 mg de Enbrel® PFS por semana, administrada uma vez por semana (em uma injeção subcutânea63 utilizando uma seringa2 de 50 mg).
Pacientes adultos (≥18 anos) com artrite7 psoriásica, espondilite anquilosante e espondiloartrite axial não radiográfica
A dose recomendada para pacientes62 adultos é de 50 mg de Enbrel® PFS por semana, administrada uma vez por semana (em uma injeção subcutânea63 utilizando uma seringa2 de 50 mg).
O uso de metotrexato, glicocorticoides, salicilatos, anti-inflamatórios não esteroides (AINEs) ou analgésicos38 pode ser mantido durante o tratamento com Enbrel® PFS em adultos.
Os dados disponíveis sugerem que uma resposta clínica é normalmente atingida em 12 semanas de tratamento. Deve ser cuidadosamente reconsiderado o tratamento contínuo em pacientes que não respondem neste período de tempo.
Pacientes adultos com psoríase12 em placas13
A dose de Enbrel® PFS é de 50 mg uma vez por semana (em uma injeção subcutânea63 utilizando uma seringa2 de 50 mg). Respostas maiores podem ser obtidas com tratamento inicial com a dose de 50 mg duas vezes por semana por até 12 semanas seguido, se necessário, por uma dose de 50 mg uma vez por semana.
Pacientes adultos podem ser tratados intermitente64 ou continuamente, baseado no julgamento do médico e nas necessidades individuais do paciente. O tratamento deve ser descontinuado em pacientes que não apresentarem resposta após 12 semanas. No uso intermitente64, os ciclos de tratamento subsequentes ao ciclo inicial devem usar dose de 50 mg uma vez por semana.
Na indicação de retratamento, a dose deve ser de 50 mg uma vez por semana.
Uso pediátrico
A dose de Enbrel® PFS para pacientes62 pediátricos é baseada no peso corporal. Pacientes com menos de 62,5 kg devem receber doses precisas na base de mg/kg usando a apresentação de Enbrel® 25 mg em frasco-ampola (pó liófilo e solução diluente para injeção40) (ver abaixo posologia para indicação específica). Pacientes com 62,5 kg ou mais podem receber dose fixa utilizando as apresentações de Enbrel® PFS em seringa2 preenchida ou caneta de aplicação plástica.
Glicocorticoides, anti-inflamatórios não esteroidais (AINEs) ou analgésicos38 podem ser mantidos durante o tratamento com Enbrel® PFS. O uso concomitante de metotrexato e doses mais altas de Enbrel® PFS não foram estudados em pacientes pediátricos.
Enbrel® PFS não foi estudado em crianças com menos de 4 anos de idade.
Psoríase12 em placas13 pediátrica
Uso em menores (>8 e <18 anos): A dose recomendada para pacientes62 pediátricos de 8 a 17 anos com psoríase12 em placas13 é de 0,8 mg/kg (máximo de 50 mg por dose) administrada uma vez por semana durante um período máximo de 24 semanas. O tratamento deve ser descontinuado em pacientes que não apresentarem resposta após 12 semanas. Se o retratamento for indicado, as referidas orientações sobre a duração do tratamento devem ser seguidas. A dose deve ser de 0,8 mg/kg (até um máximo de 50 mg por dose) uma vez por semana.
Uso em pacientes idosos (≥ 65 anos) e em pacientes com insuficiência renal65 e/ou hepática66: Não é necessário ajuste de dose.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Caso o paciente tenha esquecido de aplicar uma dose de Enbrel® PFS, deve-se aplicar a próxima dose assim que se lembrar. Depois, deve-se continuar o tratamento de Enbrel® PFS de acordo com a prescrição. Não se deve aplicar uma dose dupla de Enbrel® PFS para compensar a dose que foi esquecida.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR? PACIENTES ADULTOS
A proporção de descontinuação do tratamento devido a reações adversas nos estudos clínicos em pacientes com artrite reumatoide4 foi semelhante, tanto no grupo que recebeu Enbrel® PFS, como no grupo placebo67 (substância sem ação terapêutica68).
Reações no local da administração: Podem ocorrer reações no local da administração (eritema69 (vermelhidão) e/ou prurido70 (coceira), dor ou inchaço14).
A frequência de reações no local da administração foi maior no primeiro mês, diminuindo posteriormente. Em estudos clínicos, estas reações foram geralmente transitórias com duração média de 4 dias.
Na experiência pós-comercialização, também foram observados sangramentos e hematomas28 no local da administração do tratamento com Enbrel® PFS.
Infecções20: Foram relatadas infecções20 sérias e fatais. Entre os microrganismos mencionados estão bactérias, micobactérias (incluindo a da tuberculose71), vírus72, fungos e parasitas (incluindo protozoários73). Infecções20 oportunistas também foram relatadas (incluindo a listeriose e legionelose) (ver item “4. O que devo saber antes de usar este medicamento?”).
Nos estudos em pacientes com artrite reumatoide4, as taxas relatadas de infecções20 sérias (fatais, que resultaram em risco de vida ou que necessitaram de hospitalização ou antibioticoterapia intravenosa) e não sérias foram semelhantes para os grupos tratados com Enbrel® PFS e placebo67, quando ajustadas de acordo com a duração da exposição. Infecções20 do trato respiratório superior foram às infecções20 não sérias mais frequentemente relatadas.
Câncer74: A frequência e incidência75 de novas doenças malignas observadas nos estudos clínicos com Enbrel® PFS foram semelhantes às esperadas nas populações estudadas (ver item“1. Para que este medicamento é indicado?”ba). Durante o período de pós-comercialização, foram recebidos relatos de doenças malignas afetando diversos locais.
Formação de autoanticorpos: Não se sabe qual o impacto do tratamento a longo prazo com Enbrel® PFS sobre o desenvolvimento de doenças autoimunes76.
Abaixo listamos as reações observadas com a utilização desse medicamento:
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento): Infecções20 (incluindo infecções20 do trato respiratório superior, bronquite, cistite77, infecções20 da pele47) e reações no local da aplicação (incluindo eritema69 (vermelhidão), coceira, dor e inchaço14).
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): reações alérgicas, formação de autoanticorpo, prurido70 (coceira), rash78 (erupção79 avermelhada da pele47), febre26.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento): infecções20 sérias (incluindo pneumonia80, celulite81, artrite7 bacteriana, sepse82 e infecção19 parasitária), câncer74 de pele47 não melanoma83, diminuição de plaquetas84, anemia85 (diminuição da quantidade de células86 vermelhas do sangue61: hemácias87), diminuição de leucócitos88 e neutrófilos89 (células86 de defesa do organismo), vasculite90 (incluindo vasculite90 ANCA positiva), uveíte91, esclerite92 (inflamação8 da parte branca dos olhos93), piora da insuficiência cardíaca congestiva32, enzimas hepáticas94 elevadas, angioedema95 (inchaço14 das partes mais profundas da pele47 ou da mucosa96, geralmente de origem alérgica), psoríase12 (recorrência97 ou exacerbação; incluindo todos os subtipos), urticária98 e erupção79 psoriásica.
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento): tuberculose71, infecção19 oportunista (incluindo infecções20 fúngica99 invasiva, bacteriana micobacteriana atípica, viral e por Legionella), melanoma83 maligno, linfoma100, leucemia23, diminuição de hemácias87, plaquetas84 e leucócitos88 conjuntamente, reações alérgicas/anafiláticas sérias - incluindo broncoespasmo101 (chiado no peito102), sarcoidose103 (doença autoimune104 que forma nódulos inflamatórios nos órgãos), eventos desmielinizantes105 do sistema nervoso central106, incluindo esclerose múltipla31 e condições desmielinizantes105 localizadas, como neurite107 (inflamação8 de um nervo) óptica e mielite108 transversa, eventos desmielinizantes105 periféricos, incluindo síndrome109 de Guillain-Barré, polineuropatia desmielinizante110 inflamatória crônica, polineuropatia desmielinizante110 e neuropatia111 motora multifocal, convulsão112, novo início de insuficiência cardíaca congestiva32 (incapacidade do coração113 bombear a quantidade adequada de sangue61), doença pulmonar intersticial114 (incluindo fibrose115 (endurecimento do órgão ou estrutura) pulmonar e pneumonite116), hepatite21 autoimune104, Síndrome de Stevens-Johnson117, vasculite90 cutânea51 (incluindo vasculite90 de hipersensibilidade), eritema multiforme118, lúpus119 eritematoso120 cutâneo121, lúpus119 eritematoso120 cutâneo121 subagudo122, síndrome109 do tipo lúpus119.
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento): anemia85 aplástica (diminuição da produção de células86 vermelhos do sangue61), necrólise epidérmica tóxica123 (camada superior da pele47 desprende-se em camadas).
Reação com frequência não conhecida: reativação da hepatite21 B, Listeria, carcinoma124 de célula125 de Merkel, histiocitose hematofágica (síndrome109 de ativação macrofágica).
Pacientes pediátricos
Em geral, os eventos adversos em pacientes pediátricos apresentaram frequência e tipo semelhantes aos observados em adultos.
Infecção19 foi o evento adverso mais comum em pacientes pediátricos tratados com Enbrel® PFS, tendo ocorrido com incidência75 semelhante à observada no grupo placebo67.
Atenção: este produto é um medicamento que possui nova indicação terapêutica68 no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Se acidentalmente você aplicar mais Enbrel® PFS do que o indicado pelo seu médico, entre em contato com um médico ou dirija-se com urgência126 ao hospital mais próximo. Leve sempre consigo a embalagem ou o frasco de Enbrel® PFS, mesmo que estejam vazios.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS – 1.0216.0250
Farmacêutica Responsável: Adriana L. N. Heloany – CRF-SP nº 21250
Registrado e importado por:
Laboratórios Pfizer Ltda.
Rodovia Presidente Castelo Branco, nº 32501, km 32,5 CEP 06696-000 – Itapevi – SP
CNPJ nº 46.070.868/0036-99
Fabricado por:
Pfizer Manufacturing Belgium NV Puurs, Bélgica
Embalado por:
Wyeth Pharmaceuticals Havant, Reino Unido
SAC 0800 7701575