

Phosfoenema (Bula do profissional de saúde)
CRISTÁLIA PRODUTOS QUÍMICOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Phosfoenema®
fosfato de sódio monobásico monoidratado + fosfato de sódio dibásico heptaidratado
Enema1
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Enema1 pronto para uso
Frasco plástico descartável, com cânula retal previamente lubrificada, dotada de válvula de segurança, contendo 130 mL
USO RETAL
USO ADULTO E PEDIÁTRICO ACIMA DE 12 ANOS
COMPOSIÇÃO:
Cada 100 mL de Phosfoenema® solução (volume aplicado) contém:
| fosfato de sódio monobásico monoidratado | 16 g |
| fosfato de sódio dibásico heptaidratado | 6 g |
| veículo q.s.p. | 100 mL |
Veículo: benzoato de sódio, metilparabeno, hidróxido de sódio, água para injetáveis.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE2
INDICAÇÕES
Este medicamento é destinado para alívio da prisão de ventre e como laxativo3 para a obstipação4/constipação5 intestinal e intestino preso.
RESULTADOS DE EFICÁCIA
Enemas6 de sódio-fosfatados são amplamente utilizados para tratar a constipação5, e são raramente associados com efeitos colaterais7. Uma revisão sistemática da literatura foi realizada para identificar os efeitos adversos mais comuns de enemas6 de fosfato de sódio e fatores de risco associados. A busca sistemática foi realizada no MEDLINE, e da base de dados Cochrane, compreendendo o período de janeiro 1957 a março de 2007. Trinta e nove trabalhos relevantes foram selecionados. As indicações terapêuticas mais comuns incluíram constipação5 intestinal (63%). Sessenta e oito por cento dos pacientes com efeitos adversos associados apresentava comorbidades8, sendo as mais comuns os distúrbios da motilidade gastrointestinal, doenças cardíacas e insuficiência renal9. Praticamente todos os efeitos secundários foram devidos a distúrbios hidroeletroliticos. A maioria dos pacientes era menor de 18 anos de idade (66%) ou com idade acima de 65 anos (25%). Um total de 12 mortes foram relatadas. Os principais efeitos colaterais7 causados pelos enemas6 de fosfato de sódio são os distúrbios de água e eletrólitos10. Os principais fatores de risco são idade extrema e comorbidades8 associadas. A faixa etária compreendida entre 2 e 18 anos de idade foi representada por um grupo de 14 pacientes, sendo 50% de cada sexo. As comorbidades8 mais comuns foram os distúrbios de motilidade intestinal. A indicação mais frequente do enema1 para estes pacientes foi para tratamento da constipação5 intestinal. Todos os pacientes sofreram distúrbios hidroeletrolíticos, no entanto, apenas um foi a óbito11 por causa da própria comorbidade12. Observou-se que apesar dos efeitos adversos experimentados, o método com solução fosfatada não traz risco à vida em pacientes sadios.1
Com o objetivo de determinar a segurança e eficácia do enema1 de leite e melaço (ELM) em comparação com enemas6 de fosfato de sódio para o tratamento da constipação5 no departamento de emergência13 pediátrica, foi feita revisão de prontuários de pacientes que se apresentaram à emergência13 com queixa de constipação5 intestinal, e receberam ou ELM ou enema1 fosfatado para tratamento, entre 1º de novembro de 2007 e 1º de Novembro de 2008. Foram identificados e revisados os prontuários para a coleta de dados. A idade variou desde os dois anos (dose de 59 mL do enema1 fosfatado) até pacientes maiores de 11 anos (os quais receberam dose de enema1 fosfatado equivalente à dose de adultos). Os seguintes dados foram coletados para determinar a segurança e a eficácia: dados basais, queixa principal, história médica, imagens radiográficas, tipo de enema1, dose do tratamento, efeitos adversos, melhora dos sintomas14, o tempo até a defecação, falha da terapia inicial a necessidade de intervenção adicional, e o tempo de tratamento até a disposição. Ambos grupos de tratamento apresentavam características basais semelhantes. Não houve diferenças estatísticas de efeito do tratamento entre ELM e enemas6 fosfatados de sódio. Várias tendências clinicamente significativas foram observadas, incluindo a necessidade de tratamento adicional retal após a administração de enemas6 de fosfato de sódio versus terapia oral após ELM. Além disso, houve 6 casos de falha do tratamento com enemas6 de fosfato de sódio contra um caso com o ELM. Não foram encontradas diferenças estatisticamente significativas entre ELM e enemas6 fosfatados de sódio. Com base nos resultados, ambos tratamentos foram igualmente eficazes e seguros.2
Referências Bibliográficas:
- Mendoza J, Legido J, Rubio S, Gisbert JP. Systematic review: the adverse effects of sodium phosphate enema1. Aliment Pharmacol Ther 2007; 26, 9-20.
- Hansen SE, Whitehill J,L, Goto CS, Quintero CA, Darling BE, Davis J. Safety and Efficacy of Milk and molasses Enemas6 Compared With Sodium Enemas6 for the Treatment of Constipation in a Pediatric Emergency Department. Pediatric Emergency care 2011; 27 (12): 1118-1120.
CARACTERÍSTICAS FARMACOLÓGICAS
Os fosfatos atuam como laxativos15 salinos quando administrados por via retal na forma de enema1 ou supositórios. O mecanismo de ação se baseia no fato dos fosfatos serem fracos e lentamente absorvidos, e devido às suas propriedades osmóticas aumentarem o volume de água na luz intestinal.
Cerca de dois terços do fosfato, quando ingerido, são absorvidos do trato gastrointestinal; o excesso de fosfato é excretado principalmente pela urina16, sendo o restante excretado pelas fezes.
O tempo médio estimado para o inicio da ação terapêutica17 do medicamento é em torno de 2 a 5 minutos após sua administração.
CONTRAINDICAÇÕES
Phosfoenema® não deve ser utilizado nos seguintes casos:
- Insuficência cardíaca congestiva;
- Presença de náusea18, vômitos19 ou dor abdominal;
- Hipersensibilidade aos componentes da fórmula;
- Insuficiência renal9 dialítica;
- Ascite20;
- Obstrução gastrointestinal suspeitada ou conhecida;
- Megacólon21 (congênito22 ou adquirido);
- Perfuração;
- Doença inflamatória intestinal ativa;
- Ânus23 imperfurado;
- Em casos de desidratação24 e em casos onde a capacidade de absorção está aumentada ou a capacidade de excreção está diminuída.
Este medicamento não é recomendado para menores de 12 anos.
ADVERTÊNCIAS E PRECAUÇÕES
Soluções laxativas devem ser utilizadas com cautela em pacientes com função renal25 comprometida ou com hiperfosfatemia.
Apesar da absorção pela via retal ser pequena, o fosfato pode reduzir a concentração de cálcio ionizado no plasma26. Alguma absorção de sódio pode não ser recomendada em pacientes com insuficiência cardíaca congestiva27 ou insuficiência renal9, pois o aumento de sódio e a diminuição dos níveis séricos de cálcio e potássio, devido ao aumento dos fosfatos, podem levar a hipernatremia28, hiperfosfatemia, hipocalemia29, hipocalcemia30, acidose metabólica31, insuficiência renal9, prolongamento do intervalo QT e em casos gravíssimos falência múltipla dos órgãos, arritmia32 cardíaca e morte.
Devido ao fato de ser uma solução hipertônica33, deve ser administrada com cautela em pacientes debilitados, desidratados ou em uso de medicação que aumente a filtração glomerular, pois a mesma pode agravar estas condições.
Todo o conteúdo intestinal34 deve ser expelido após a utilização desta medicação, e seu uso em pequenos intervalos de tempo repetidamente deve ser evitado.
Cautela ao utilizar em mulheres grávidas, assim como em idosos, pois eles são mais sensíveis aos efeitos dos enemas6.
Deve-se assegurar que o conteúdo do intestino seja evacuado após a administração deste medicamento.
Seu uso repetido em intervalos curtos deve ser evitado.
Este medicamento não deve ser utilizado em crianças menores de 12 anos de idade.
Gravidez35 e Lactação36
Categoria C – Não há estudos adequados em mulheres. Em experiências animais ocorreram alguns efeitos colaterais7 no feto37, mas o benefício do produto pode justificar o risco potencial durante a gravidez35.
Não é conhecido se o Phosfoenema® é eliminado pelo leite materno.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
INTERAÇÕES MEDICAMENTOSAS
Phosfoenema® não deve ser utilizado com nenhuma outra preparação de fosfato de sódio, incluindo soluções orais ou comprimidos, concomitantemente.
Não existem interações específicas conhecidas do Phosfoenema® com outros fármacos.
Cautela ao administrar Phosfoenema® com outros medicamentos que podem afetar os níveis de eletrólitos10.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
O prazo de validade do produto é de 36 meses a contar da data de fabricação. Após este prazo, o produto pode não mais apresentar efeitos terapêuticos.
Conservar o produto em temperatura ambiente (15–30°C), protegido da luz.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use o medicamento com prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Liquido límpido incolor a levemente amarelado, isento de partículas estranhas.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
A Embalagem
Phosfoenema® possui embalagem especialmente desenvolvida, com ponta anatômica, lubrificada, com capa protetora e válvula de segurança para controlar o fluxo e evitar o refluxo.

- Capa protetora, evita contaminação.
- Ponta anatomicamente correta assegura facilidade de inserção.
- Válvula de segurança, uni-direcional, controla o fluxo e evita o refluxo.
- Frasco redondo, fácil de segurar e comprimir.
Modo de usar:
- Antes de usar, retire a capa protetora da cânula retal.
- Com o frasco para cima, segure com os dedos a tampa sulcada. Com a outra mão38, segure a capa protetora, retirando-a suavemente.
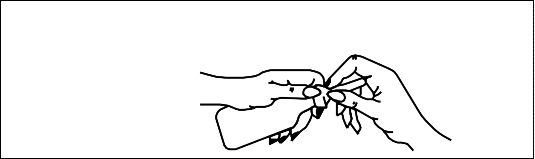
- Escolher a posição mais conveniente, entre as citadas nas ilustrações.
LADO ESQUERDO: Deitar sobre o lado esquerdo, com os joelhos em flexão e braços relaxados.

JOELHO – TÓRAX39: Ajoelhar-se e, em seguida, baixar a cabeça40 e o tórax39 para a frente, até que o lado esquerdo da face41 repouse na superfície, deixando os braços em posição confortável.
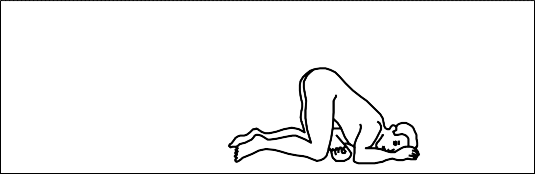
AUTO – ADMINISTRAÇÃO: O processo mais simples é assumir a posição indicada, deitado sobre uma toalha, colocada de preferência no piso do banheiro.

Com pressão firme, inserir suavemente a cânula no reto42, comprimindo o frasco até ser expelido quase todo o líquido. Retire a cânula do reto42.
Nota: Não é necessário esvaziar completamente o frasco porque ele contém quantidade de líquido superior à necessária para uso eficaz.
Não forçar o enema1, poderá resultar em perfuração e/ou abrasão do reto42. Após a compressão, uma pequena quantidade ficará no frasco.
Manter a posição até sentir forte vontade de evacuar (geralmente 2 a 5 minutos).
Posologia
Phosfoenema® deve ser administrado por via retal.
Adultos e crianças acima de 12 anos:
- A dose usual de Phosfoenema é de 100 mL em 24 horas.
- A dose máxima diária não deve exceder os 100mL em 24 horas.
Uso em idosos, crianças e outros grupos de risco: Os idosos são mais sensíveis aos efeitos dos enemas6. Não utilizar em crianças menores de 12 anos de idade e em portadores de insuficiência hepática43 ou renal25. Verificar os itens CONTRAINDICAÇÕES e ADVERTÊNCIAS E PRECAUÇÕES.
REAÇOES ADVERSAS
As frequências das reações adversas estão listadas a seguir, de acordo com a seguinte convenção:
|
Categoria |
Frequência |
|
Muito comum |
≥ 10% |
|
Comum |
≥ 1% e < 10% |
|
Incomum |
≥ 0,1% e < 1% |
|
Raro |
≥ 0,01% e < 0,1% |
|
Muito raro |
< 0,01% |
|
Desconhecida |
Não pode ser estimada pelos dados disponíveis |
|
Sistema |
Evento Adverso |
Detalhes |
|
Muito Comum |
||
|
Endócrino44/Metabólico |
Hiperfosfatemia |
Incidência45 93 a 96% |
|
Hipopotassemia46 |
Incidência45 18 a 22% |
|
|
Gastrointestinal |
Edema47 abdominal |
Incidência45 31 a 41% |
|
Dor abdominal |
Incidência45 23 a 25% |
|
|
Náuseas48 |
Incidência45 26 a 37% |
|
|
Comum |
||
|
Gastrointestinal |
Vômitos19 |
Incidência45 4 a 10% |
|
Sério/Grave |
||
|
Cardiovascular |
Prolongamento do intervalo QT |
Raro |
|
Neurológico |
Convulsão49 tônico-clônica |
Raro |
|
Renal25 |
Nefropatia50 aguda pelo fosfato |
Raro |
|
Falência renal25 |
Raro |
|
Reações desagradáveis podem ocorrer. Este medicamento pode causar distúrbios hidroeletrolíticos, cólicas51, irritação da pele52 próxima à região retal, queimação, prurido53, dor ou sangramento retal.
Observar alterações do hábito intestinal que persistam por mais de duas semanas.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA ou à Vigilância Sanitária Estadual ou Municipal.
A superdosagem (mais de um enema1 em um período de 24 horas), ausência de retorno da solução de enema1, tempo de retenção maior do que 10 minutos ou ausência de movimento intestinal dentro de 30 minutos após o uso do enema1, podem levar a graves distúrbios eletrolíticos, incluindo a hipernatremia28, hiperfosfatemia, hipocalcemia30 e hipocalemia29, bem como a desidratação24 e hipovolemia54, além de acidose metabólica31, insuficiência renal9, prolongamento do intervalo QT e/ou, em casos mais graves, falência de múltiplos órgãos, arritmia32 cardíaca e morte.
O paciente que recebeu uma superdosagem ou que apresenta tempo de retenção do produto por mais de 10 minutos deve ser cuidadosamente monitorizado.
Se o paciente desenvolver vômitos19 e/ou sinais55 de desidratação24, deverão ser realizados exames laboratoriais (dosagem sérica de cálcio, potássio, sódio, creatinina56 e ureia57). O tratamento do distúrbio hidroeletrolítico58 exige intervenção médica imediata com reposição de eletrólitos10 apropriados e terapia de reposição de fluidos.
Em caso de aplicações de doses acima das preconizadas ou ingestão acidental deste medicamento, recomenda-se adotar medidas habituais de controle das funções vitais.
Em caso de intoxicação, ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
Siga corretamente o modo de usar, não desaparecendo os sintomas14 procure orientação médica.
Registro M.S.: 1.0298.0040
Farm. Resp.: Dr. José Carlos Módolo - CRF-SP Nº 10.446
Cristália Produtos Químicos Farmacêuticos Ltda.
Rod. Itapira-Lindóia, km 14 – Itapira – SP
CNPJ nº 44734.671/0001-51
Indústria Brasileira
SAC 0800 7011918






