

Propovan (Bula do profissional de saúde)
CRISTÁLIA PRODUTOS QUÍMICOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Propovan®
propofol
Injetável 10 mg/mL
Medicamento similar equivalente ao medicamento de referência.
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Emulsão Injetável Intravenosa
Caixa com 10 ampolas de 10 mL. Caixa com 10 frascos-ampola de 20 mL.
USO INTRAVENOSO
USO ADULTO E PEDIÁTRICO ACIMA DE 3 ANOS
COMPOSIÇÃO:
Cada mL de Propovan® contém:
| propofol | 10 mg |
| veículo estéril q.s.p. | 1 mL |
Veículo: óleo de soja, lecitina de ovo1, glicerol, hidróxido de sódio, água para injetáveis.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE2
INDICAÇÕES
Propovan® é indicado para indução e manutenção de anestesia3 geral em procedimentos cirúrgicos. Isto significa que Propovan® faz com que o paciente fique inconsciente ou sedado durante operações cirúrgicas ou outros procedimentos.
Propovan® pode também ser usado para a sedação4 de pacientes adultos ventilados que estejam recebendo cuidados de terapia intensiva5.
Propovan® pode também ser usado para sedação4 consciente para procedimentos cirúrgicos e de diagnóstico6.
RESULTADOS DE EFICÁCIA
Agente anestésico de curta duração: indução e manutenção
Em estudos comparativos de óxido nitroso-sevoflurano com óxido nitroso-propofol para indução e manutenção da anestesia3, foi determinada a taxa de recuperação para cada anestésico. Cinquenta pacientes, P 1 ou 2 na faixa etária de 18 a 70 anos, submetidos a procedimentos cirúrgicos eletivos7 com duração de 1 a 3 horas, foram distribuídos de maneira randomizada e receberam sevoflurano (grupo A) ou propofol (grupo B). Para a indução da anestesia3: no grupo A o sevoflurano foi administrado em concentrações crescentes (até 3,5%) com o paciente em respiração espontânea, no grupo B o propofol foi administrado na dose de 2–2,5 mg/kg em 60 segundos com o paciente em respiração espontânea com oxigênio a 100%. A manutenção da anestesia3 no grupo A foi realizada com sevoflurano 0,3% a 1,8% e no grupo B com infusão de 50 a 200 mcg/kg/min de propofol. O óxido nitroso 60–70% foi administrado em todos os pacientes e fentanila na dose de 1–3 mcg/kg foi administrado em bolus8 como suplemento anestésico nos dois grupos. Ao final da cirurgia foi interrompida a administração dos agentes anestésicos e instaurado um fluxo de oxigênio a 100% (6 L/min). Os resultados demonstraram que indução no grupo B foi mais rápida quando comparada com o grupo A (0,8 vs. 2,0 minutos respectivamente). A facilidade de indução e o tempo necessário para o despertar foram similares nos dois grupos. Dentre os efeitos indesejáveis, no grupo A, 13 pacientes apresentaram náuseas9 e 5 apresentaram vômitos10, enquanto que no grupo B a incidência11 de náuseas9 foi de 3 pacientes. A incidência11 de tremores e dor foi similar nos dois grupos. (Lien CA et. al. Journal of Clinical Anesthesia 1996; 8(8):639).
Reves et al., descrevem o uso do propofol como agente anestésico para indução-manutenção da anestesia3, assim como o seu uso em sedação4 para procedimentos cirúrgicos e em pacientes sob ventilação12 mecânica em UTI devido a sua eficácia e segurança. (Reves JG et al. Anesthesia Fourth Edition 1994, 1(11): 272).
Estudos comparativos do uso do propofol em infusão manual com o uso pela bomba de infusão alvo controlada (IAC) foram realizados em 160 pacientes (paciente grau ASA 1–3 com idade ≥ a 18 anos), submetidos a procedimentos cirúrgicos. Os dados analisados foram: aceitabilidade da técnica, eficácia e segurança. O grupo IAC apresentou doses de indução menores e taxa de infusão de manutenção maiores. Na avaliação dos anestesistas envolvidos, a facilidade de controle e o uso da bomba de IAC foi considerada melhor.
Foi concluído que o sistema de IAC é efetivo e seguro, tendo melhor aceitabilidade do que a técnica de infusão manual. (Mazzarella B et al. Minerva Anestesiologica 1999;65 (10):701).
Sedação4 para procedimentos cirúrgicos/diagnósticos
Charles J. Coté estabelece o uso de propofol em pediatria para sedação4 intermitente13 ou em infusão constante nos procedimentos radiológicos devido à sua eficácia na prática clínica. (Coté CJ. Anesthesia Fourth Edition 1994, 2(63):2104).
Foi reportado um estudo prospectivo14 e randomizado15, comparando propofol e midazolam para sedação4 em colangiopancreatografia retrógrada via endoscópica. Foram selecionados 200 pacientes P 3 e 4 com idade entre 28–88 anos. Estes pacientes receberam de forma randomizada midazolam 2,5 mg para indução seguido de doses repetidas de acordo com a necessidade ou propofol 40–60 mg de dose inicial conforme o peso corporal seguido de 20 mg em doses repetidas. Do total dos pacientes, três foram excluídos devido a presença de carcinoma16 (2 pacientes no grupo midazolam e 1 paciente no grupo propofol). Os resultados demonstraram um tempo de início médio de ação da sedação4 menor no grupo propofol do que no grupo midazolam (3 min vs. 6 min), assim como um tempo médio de recuperação menor no grupo tratado com propofol em relação ao grupo tratado com midazolam (19 min vs. 29 min). Foi concluído que a sedação4 endovenosa com propofol para colangiopancreatografia retrógrada via endoscópica é mais efetiva que midazolam, associada com recuperação rápida e segura desde que haja monitorização adequada (Wehrmann T et al. Gastrointestinal Endoscopy 1999).
Sedação4 UTI
Barrientos et al., realizaram um estudo comparativo entre propofol 2% e midazolam, onde analisaram a eficácia, tempo para extubação e custo. Neste estudo foram selecionados 78 pacientes submetidos à cirurgia que necessitaram de ventilação12 controlada mecânica e sedação4 prolongada na unidade de terapia intensiva5. Após distribuição randomizada, 40 pacientes receberam propofol 2% e 38 midazolam. A dose média de propofol 2% foi de 1–6 mg/kg/h e de midazolam 0,05–0,4 mg/kg/h. Nenhum bloqueador neuromuscular foi utilizado e a duração média da sedação4 foi de 141,2 h para o grupo propofol 2% e 140,5 h para o grupo midazolam. Os resultados demonstraram que a eficácia foi similar nos dois grupos, sendo que, no grupo propofol 2%, 2,5% dos pacientes apresentaram hipertrigliceridemia. O tempo necessário para extubação foi significativamente menor no grupo propofol 2% quando comparado com o grupo midazolam, o que levou os autores a acreditarem que o custo benefício do propofol 2% é melhor. (Barrientos – Vega R et al. Intensive Care Medicine 1997: 23 (suppl): S176, Abs149).
CARACTERÍSTICAS FARMACOLÓGICAS
Grupo farmacoterapêutico: anestésicos gerais
Propriedades Farmacodinâmicas
O propofol (2,6-diisopropilfenol) é um agente de anestesia3 geral de curta duração com rápido início de ação de aproximadamente 30 segundos. A recuperação da anestesia3 geralmente é rápida. O mecanismo de ação, assim como com todos os anestésicos gerais, é pouco conhecido. Entretanto, propofol é conhecido por produzir efeito sedativo e anestésico pela modulação positiva da função inibitória do neurotransmissor GABA17 através do receptor GABAA ativado por ligante.
Em geral, queda na pressão arterial18 e leves mudanças na frequência cardíaca são observadas quando propofol é administrado para indução e manutenção da anestesia3. Entretanto, os parâmetros hemodinâmicos normalmente permanecem relativamente estáveis durante a manutenção e a incidência11 de alterações hemodinâmicas adversas é baixa.
Apesar da possibilidade de ocorrência de depressão ventilatória após administração de Propovan®, quaisquer efeitos são qualitativamente similares àqueles causados por outros agentes anestésicos intravenosos e são facilmente gerenciáveis na prática clínica.
Propofol reduz o fluxo sanguíneo cerebral, a pressão intracraniana e o metabolismo19 cerebral. A redução na pressão intracranial é maior em pacientes com uma linha de base elevada para pressão intracranial.
A recuperação da anestesia3 geralmente é rápida e sem efeitos residuais, com baixa incidência11 de dor de cabeça20, náusea21 e vômitos10 pós-operatórios.
Em geral, há menos náusea21 e vômitos10 pós-operatórios após anestesia3 com propofol que com agentes anestésicos inalatórios. Há evidência de que isso possa estar relacionado ao efeito antiemético22 do propofol.
Nas concentrações atingidas clinicamente, propofol não inibe a síntese de hormônios adrenocorticais.
Propriedades Farmacocinéticas
O declínio das concentrações de propofol após uma dose em bolus8 ou após o final de uma infusão pode ser descrito por um modelo tricompartimental aberto. A primeira fase é caracterizada por uma distribuição muito rápida (meia-vida de 2–4 minutos), seguido por rápida eliminação (meia-vida de 30 a 60 minutos) e uma fase final mais lenta, representativa da redistribuição do propofol por tecidos pouco perfundidos.
O propofol é amplamente distribuído e rapidamente eliminado do corpo (depuração total: 1,5–2 L/minuto). A depuração ocorre através de processos metabólicos, principalmente no fígado23, para formar conjugados inativos de propofol e seu quinol correspondente, os quais são excretados na urina24. Quando Propovan® é usado para manter a anestesia3, as concentrações sanguíneas de propofol aproximam-se assintoticamente do valor do estado de equilíbrio para a dada velocidade de administração. A farmacocinética de propofol é linear ao longo da faixa recomendada de velocidades de infusão.
Dados de segurança pré-clínica
O propofol é um fármaco25 com extensa experiência clínica.
CONTRAINDICAÇÕES
Propovan® é contraindicado nas seguintes situações:
- Hipersensibilidade conhecida ao propofol ou a qualquer componente de sua fórmula;
- Sedação4 em crianças menores de 3 anos de idade com infecção26 grave do trato respiratório, recebendo tratamento intensivo;
- Sedação4 de crianças de todas as idades com difteria27 ou epiglotite recebendo tratamento intensivo (ver item Advertências e Precauções).
Este medicamento é contraindicado para menores de 3 anos. Categoria de risco na gravidez28: B.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
ADVERTÊNCIAS E PRECAUÇÕES
Propovan® deve ser administrado por profissional de saúde2 treinado em técnicas de anestesia3 (ou quando for o caso, por médicos treinados em cuidados de pacientes em terapia intensiva5). Os pacientes devem ser constantemente monitorados e devem estar disponíveis instalações para manutenção das vias aéreas abertas, ventilação12 artificial, enriquecimento de oxigênio, além de instalações ressuscitatórias.
Propovan® não deve ser administrado pela pessoa que conduziu o procedimento diagnóstico6 ou o procedimento cirúrgico.
Quando Propovan® é administrado para sedação4 consciente, procedimentos cirúrgicos e de diagnóstico6, os pacientes devem ser continuamente monitorados para sinais29 precoces de hipotensão30, obstrução das vias aéreas e dessaturação de oxigênio.
Assim como outros agentes sedativos, quando Propovan® é usado para sedação4 durante procedimentos cirúrgicos, podem ocorrer movimentos involuntários dos pacientes. Durante procedimentos que requerem imobilidade, esses movimentos podem ser perigosos para o local da cirurgia.
Um período adequado é necessário antes da alta do paciente para garantir a recuperação total após a anestesia3 geral. Muito raramente o uso de propofol pode estar associado ao desenvolvimento de um período de inconsciência31 pós-operatória, o qual pode ser acompanhado por um aumento no tônus muscular32. Isto pode ou não ser precedido por um período de vigília. Apesar da recuperação ser espontânea, deve-se ter um cuidado apropriado ao paciente inconsciente.
Assim como com outros agentes anestésicos intravenosos, deve-se tomar cuidado em pacientes com insuficiência cardíaca33, respiratória, renal34 ou hepática35 e em pacientes hipovolêmicos ou debilitados.
Propovan® não possui atividade vagolítica e tem sido associado com relatos de bradicardia36 (ocasionalmente profunda) e também assistolia. Deve-se considerar a administração intravenosa de um agente anticolinérgico antes da indução ou durante a manutenção da anestesia3, especialmente em situações em que haja probabilidade de predominância do tônus vagal ou quando Propovan® for associado a outros agentes com potencial para causar bradicardia36.
Quando Propovan® for administrado a um paciente epiléptico, pode haver risco de convulsão37.
Deve-se dispensar cuidado especial aos pacientes com disfunções no metabolismo19 de gordura38 e em outras condições que requeiram cautela na utilização de emulsões lipídicas.
Caso se administre Propovan® a pacientes que estejam sob risco de acumular gordura38, recomenda-se que os níveis sanguíneos de lipídeos sejam controlados. A administração de Propovan® deve ser ajustada adequadamente se o controle indicar que a gordura38 não está sendo bem eliminada. Se o paciente estiver recebendo concomitantemente outro lipídeo39 por via intravenosa, sua quantidade deve ser reduzida, levando-se em consideração que a fórmula de Propovan® contém lipídeos (1,0 mL de Propovan® contém aproximadamente 0,1 g de lipídeo39).
Foram recebidos relatos muito raros de acidose metabólica40, de rabdomiólise41, de hipercalemia42, alterações no ECG* e/ou de falha cardíaca, em alguns casos com um resultado fatal, em pacientes gravemente acometidos recebendo propofol para sedação4 na UTI. Os principais fatores de risco para o desenvolvimento destes eventos são: diminuição na liberação de oxigênio para os tecidos; lesão43 neurológica grave e/ou sepse44; altas doses de um ou mais agentes farmacológicos: vasoconstritores, esteroides, inotrópicos e/ou propofol. Todos os sedativos e agentes terapêuticos usados na UTI (incluindo Propovan®) devem ser titulados para manter uma liberação de oxigênio ideal e parâmetros hemodinâmicos.
*elevação do segmento ST (similar às alterações de ECG na síndrome45 de Brugada).
Propovan® não é recomendado para uso em neonatos46 para a indução e manutenção da anestesia3.
Não há dados que dão suporte ao uso de Propovan® em sedação4 para neonatos46 prematuros, recebendo tratamento intensivo.
Não há dados de estudos clínicos que dão suporte ao uso de propofol em sedação4 de crianças com difteria27 ou epiglotite, recebendo tratamento intensivo.
Efeitos na habilidade de dirigir e usar máquinas
Os pacientes devem ser alertados de que o desempenho para tarefas que exijam atenção, tais como dirigir veículos e operar máquinas pode estar comprometido durante algum tempo após o uso de Propovan®.
Gravidez28 e Lactação47
Categoria de risco na gravidez28: B.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
A segurança para o neonato48, quando do uso de Propovan® em mulheres que estejam amamentando, não foi estabelecida.
Propovan® não deve ser usado durante a gravidez28.
Propovan® atravessa a placenta e pode estar associado à depressão neonatal. O produto não deve ser utilizado em anestesia3 obstétrica.
INTERAÇÕES MEDICAMENTOSAS
Propofol foi usado em associação com anestesia3 espinhal e epidural49, com pré-medicação normalmente usada, bloqueadores neuromusculares, agentes inalatórios e agentes analgésicos50. Nenhuma incompatibilidade farmacológica foi encontrada.
Entretanto, recomenda-se que os bloqueadores neuromusculares atracúrio e mivacúrio, não devem ser administrados na mesma via IV antes de se eliminar os indícios de propofol.
Doses menores de Propovan® podem ser necessárias em situações em que a anestesia3 geral é utilizada como um adjunto às técnicas anestésicas regionais.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar o produto em temperatura ambiente, entre 15 e 30°C, protegido da luz. O produto não deve ser congelado.
O prazo de validade é de 18 meses a partir da data de fabricação impressa na embalagem.
Agitar antes do uso.
Deve ser usado em até 6 horas após diluição. Não diluído, usar em até 12 horas.
Qualquer porção remanescente deve ser descartada, pois o produto não contém conservantes antimicrobianos.
A porção restante do conteúdo do frasco-ampola não deve ser reutilizada, devendo ser descartada ao final do procedimento.
Não use o produto se o frasco estiver aberto ou com visível separação de fases da emulsão. Durante o manuseio, devem ser mantidas técnicas assépticas estritas.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
emulsão homogênea, isenta de partículas estranhas, branca a quase branca.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Modo de usar
Propovan® é uma emulsão homogênea para injeção51 intravenosa.
Geralmente, além de Propovan®, são necessários agentes analgésicos50 suplementares.
Propofol tem disso usado em associação com anestesia3 espinhal e epidural49, com pré-medicação normalmente usada, bloqueadores neuromusculares, agentes inalatórios e agentes analgésicos50. Nenhuma incompatibilidade farmacológica foi encontrada. Doses menores de Propovan® podem ser necessárias em situações em que a anestesia3 geral é utilizada como um adjunto às técnicas anestésicas regionais.
Propovan® não contém conservantes antimicrobianos.
Assim sendo, imediatamente após a abertura da ampola ou frasco-ampola, a aspiração do produto deve ser feita assepticamente para uma seringa52 estéril ou para o equipamento de infusão. A administração de Propovan® deve ser iniciada sem demora. Os cuidados de assepsia53 devem ser observados até o término da infusão, tanto na manipulação de Propovan® como do equipamento em uso. Quaisquer infusões de fluídos adicionados à linha de infusão de Propovan® devem ser administrados próximo do local da cânula.
Propovan® não deve ser administrado através de filtro microbiológico54. As ampolas e os frascos- ampola de Propovan® devem ser agitados antes do uso e qualquer porção não utilizada deve ser descartada.
Propovan®, e qualquer seringa52 contendo Propovan®, destina-se a um único uso em apenas um paciente.
De acordo com as orientações para a administração de outras emulsões lipídicas, uma infusão única (não diluída) de Propovan® não deve exceder 12 horas. No final do procedimento cirúrgico ou após o término da estabilidade (6 horas após diluição e 12 horas sem diluição), o que ocorrer primeiro, tanto o reservatório de Propovan® como o equipamento de infusão devem ser descartados e substituídos de maneira apropriada.
Propovan® pode ser usado para infusão, sem diluição, em seringas plásticas ou frascos de vidro para infusão. Quando Propovan® é usado sem diluição na manutenção da anestesia3, recomenda-se que seja sempre utilizado um equipamento tal como bomba de seringa52 ou bomba volumétrica para infusão, a fim de controlar as velocidades de infusão.
Propovan® pode também ser administrado diluído somente em infusão intravenosa de dextrose55 a 5%, em bolsas de infusão de PVC ou frascos de vidro de infusão. As diluições, que não devem exceder a proporção de 1:5 (2 mg de propofol/mL), devem ser preparadas assepticamente imediatamente antes da administração. A mistura é estável por até 6 horas.
A diluição pode ser usada com várias técnicas de controle de infusão, porém um determinado tipo de equipo usado sozinho não evitará o risco de infusão acidental incontrolada de grandes volumes de Propovan® diluído. Uma bureta, contador de gotas ou uma bomba volumétrica devem ser incluídos na linha de infusão.
O risco de infusão incontrolada deve ser considerado durante a decisão da quantidade máxima de diluição na bureta.
Propovan® pode ser administrado via equipo em Y próximo ao local da injeção51, em infusões intravenosas de dextrose55 a 5%, em infusão intravenosa de cloreto de sódio a 0,9% ou de dextrose55 a 4% com infusão intravenosa de cloreto de sódio a 0,18%.
Propovan® pode ser pré-misturado com injeções contendo 500 mcg/mL de alfentanila na velocidade de 20:1 a 50:1 v/v. As misturas devem ser preparadas usando técnicas estéreis e devem ser usadas dentro de 6 horas após a preparação.
A fim de reduzir a dor da injeção51 inicial, Propovan® usado para indução pode ser misturado com injeção51 de lidocaína em uma seringa52 plástica na proporção de 20 partes de Propovan® com até 1 parte de injeção51 de lidocaína 0,5% ou 1% (ver tabela de diluições) imediatamente antes da administração.
Propovan® 1% pode ser misturado com glicose56 5% em bolsas de infusão de PVC ou frascos de vidro para infusão ou injeção51 de lidocaína ou alfentanila em seringas plásticas.
Diluição e co-administração de Propovan® com outros fármacos ou fluidos de infusão (ver item Advertências e Precauções)
|
Técnica de co-administração |
Aditivo ou diluente |
Preparação |
Precauções |
|
Pré-mistura |
Infusão intravenosa de dextrose55 a 5% |
Misturar 1 parte de propofol 1% com até 4 partes de infusão intravenosa de dextrose55 a 5% em bolsas de infusão de PVC ou em frascos de infusão de vidro. Quando diluído em bolsas de PVC, recomenda-se utilizar uma bolsa cheia e que a diluição seja preparada retirando um volume do fluído de infusão e substituindo-o por um volume igual ao de propofol 1%. |
Preparar a mistura de forma asséptica imediatamente antes da administração. A mistura é estável por até 6 horas. |
|
Injeção51 de cloridrato de lidocaína (0,5% ou 1,0%, sem conservantes) |
Misturar 20 partes de propofol 1% com até 1 parte de injeção51 de cloridrato de lidocaína a 0,5% ou 1,0%. |
Preparar a mistura de forma asséptica imediatamente antes da administração. Usar apenas para indução. |
|
|
Injeção51 de alfentanila (500 mcg/mL) |
Misturar propofol 1% com injeção51 de alfentanila na proporção de 20:1 a 50:1 v/v. |
Preparar a mistura de forma asséptica; usar dentro de 6 horas da preparação. |
|
|
Co-administração com equipo em Y |
Infusão intravenosa de dextrose55 a 5% |
Co-administrar através de um equipo em Y. |
Colocar o conector em Y perto do local da injeção51. |
|
Infusão intravenosa de cloreto de sódio a 0,9% |
Conforme acima. |
Conforme acima. |
|
|
Infusão intravenosa de dextrose55 a 4% com cloreto de sódio a 0,18% |
Conforme acima. |
Conforme acima. |
IMPORTANTE: ampola com ponto de corte. Veja instruções abaixo:
Segure a ampola com o ponto de corte marcado no gargalo voltado para sua direção e quebre no sentido oposto (ver ilustrações abaixo).
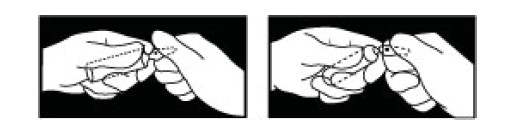
Orientação sobre as concentrações alvo de propofol é fornecida a seguir. Em razão da variabilidade da farmacocinética e farmacodinâmica do propofol, tanto em pacientes pré-medicados quanto nos pacientes não pré-medicados, a concentração alvo de propofol deve ser titulada de acordo com a resposta do paciente, a fim de se atingir a profundidade de anestesia3 ou sedação4 consciente desejada.
POSOLOGIA
Sistema de Classificação do Estado Físico de acordo com a Sociedade Americana de Anestesiologistas (ASA):
|
GRAU |
CLASSIFICAÇÃO |
|
1 |
Paciente normal |
|
2 |
Paciente com doença sistêmica de leve a moderada |
|
3 |
Paciente com doença sistêmica grave |
|
4 |
Paciente com doença sistêmica grave que limita atividades diárias |
|
5 |
Paciente moribundo que não é esperada a sobrevivência57 sem cirurgia |
|
6 |
Paciente com morte cerebral58 declarada cujos órgãos serão removidos para propósitos de doação |
Adultos
Indução de anestesia3 geral: Propovan® 1% pode ser usado para induzir anestesia3 através de infusão ou injeção51 lenta em bolus8.
Em pacientes com ou sem pré-medicação, recomenda-se que Propovan® seja titulado de acordo com a resposta do paciente. Administrar aproximadamente 40 mg a cada 10 segundos em adulto razoavelmente saudável por injeção51 em bolus8 ou por infusão, até que os sinais29 clínicos demonstrem o início da anestesia3. A maioria dos pacientes adultos com menos de 55 anos possivelmente requer de 1,5 a 2,5 mg/kg de propofol. A dose total necessária pode ser reduzida pela diminuição da velocidade de administração (20–50 mg/min). Acima desta idade, as necessidades serão geralmente menores. Em pacientes de Graus ASA 3 e 4 deve-se usar velocidade de administração menor (aproximadamente 20 mg a cada 10 segundos).
Manutenção de anestesia3 geral: A profundidade requerida da anestesia3 pode ser mantida pela administração de Propovan® por infusão contínua ou por injeções repetidas em bolus8.
- Infusão contínua – A velocidade adequada de administração varia consideravelmente entre pacientes, mas velocidades na faixa de 4 a 12 mg/kg/h, normalmente mantêm a anestesia3 satisfatoriamente.
- Injeções repetidas em bolus8 – recomenda-se que apenas Propovan 1% seja utilizado. Se for utilizada a técnica que envolve injeções repetidas em bolus8, podem ser administrados aumentos de 25 mg (2,5 mL) a 50 mg (5 mL), de acordo com a necessidade clínica.
Sedação4 na UTI: Quando utilizado para promover sedação4 em pacientes adultos ventilados na UTI, recomenda-se que Propovan® seja administrado por infusão contínua. As taxas de infusão entre 0,3 e 4,0 mg/kg/h atingem a sedação4 de forma satisfatória na maioria dos pacientes adultos. A administração de Propovan® para sedação4 na UTI em pacientes adultos não deve exceder a 4 mg/kg/h, a menos que os benefícios para o paciente superem os riscos.
Sedação4 consciente para cirurgia e procedimentos de diagnóstico6: Para promover a sedação4 em procedimentos cirúrgicos e de diagnóstico6, as velocidades de administração devem ser individualizadas e tituladas de acordo com a resposta clínica. A maioria dos pacientes necessitará de 0,5 a 1 mg/kg por aproximadamente 1 a 5 minutos para iniciar a sedação4.
A manutenção da sedação4 pode ser atingida pela titulação da infusão de Propovan® até o nível desejado de sedação4 – a maioria dos pacientes irá necessitar de 1,5 a 4,5 mg/kg/h. Adicional à infusão, a administração em bolus8 de 10 a 20 mg pode ser usada se for necessário um rápido aumento na profundidade da sedação4. Em pacientes de graus ASA 3 e 4, a velocidade de administração e a dosagem podem necessitar de redução.
Crianças
Não se recomenda o uso de Propovan® em crianças menores de 3 anos de idade.
Indução de anestesia3 geral: Quando usado para induzir anestesia3 em crianças, recomenda-se que Propovan® seja administrado lentamente, até que os sinais29 clínicos demonstrem o início da anestesia3.
A dose deve ser ajustada em relação à idade e/ou ao peso. A maioria dos pacientes com mais de 8 anos provavelmente irá necessitar de aproximadamente 2,5 mg/kg de propofol para a indução da anestesia3. Entre 3 e 8 anos de idade, a necessidade pode ser ainda maior. Doses mais baixas são recomendadas para crianças com graus ASA 3 e 4.
Manutenção da anestesia3 geral: A profundidade necessária de anestesia3 pode ser mantida pela administração de Propovan® por infusão ou por injeções repetidas em bolus8. É recomendado que somente Propovan 1% seja usado se forem usadas injeções repetidas em bolus8. A velocidade necessária de administração varia consideravelmente entre os pacientes, no entanto, a faixa de 9 a 15 mg/kg/h normalmente produz anestesia3 satisfatória.
Sedação4 consciente para procedimentos de diagnóstico6 e cirúrgicos: Propovan® não é recomendado para sedação4 consciente em crianças uma vez que a segurança e eficácia não foram demonstradas.
Sedação4 na UTI: Propovan® não é recomendado para sedação4 em crianças, uma vez que a segurança e a eficácia não foram demonstradas. Apesar de não ter sido estabelecida nenhuma relação causal, reações adversas sérias (incluindo fatalidades) foram observadas através de relatos espontâneos sobre o uso não aprovado em UTI. Esses eventos foram mais frequentes em crianças com infecções59 do trato respiratório e que receberam doses maiores que aquelas recomendadas para adultos.
Idosos
Em pacientes idosos, a dose de Propovan® necessária para a indução de anestesia3 é reduzida. Esta redução deve levar em conta a condição física e a idade do paciente. A dose reduzida deve ser administrada mais lentamente e titulada conforme a resposta. Quando Propovan® é usado para manutenção da anestesia3 ou sedação4, a taxa de infusão ou “concentração alvo” também deve ser diminuída. Pacientes com graus ASA 3 e 4 necessitarão de reduções adicionais na dose e na velocidade de administração. A administração rápida em bolus8 (única ou repetida) não deve ser utilizada no idoso, pois pode levar à depressão cardiorrespiratória.
REAÇÕES ADVERSAS
A indução da anestesia3 com Propovan® é geralmente suave, com evidência mínima de excitação. As reações adversas mais comumente reportadas são efeitos adversos farmacologicamente previsíveis de um agente anestésico, como a hipotensão30. Dada a natureza anestésica e os pacientes que recebem cuidado intensivo, eventos relatados em associação com anestesia3 e cuidado intensivo também podem estar relacionados aos procedimentos utilizados ou às condições do paciente.
Resumo tabelado de reações adversas
A seguinte convenção foi utilizada para a classificação de frequência: Muito comum (>1 / 10), comum (>1 / 100 e ≤1/10), incomum (>1 / 1000 e ≤1/100), rara (>1 / 10.000 e ≤1/1000), muito rara (≤1 / 10.000) e desconhecida (não pode ser estimado a partir dos dados disponíveis).
|
Frequência |
Sistema de classificação (SOC) |
Reações adversas |
|
Muito Comum |
Distúrbios gerais e condições do local de aplicação |
Dor local em indução (1) |
|
Comum |
Distúrbios vasculares60 |
Hipotensão30 (2); Ruborização em crianças (4) |
|
Distúrbios cardíacos |
Bradicardia36 (3) |
|
|
Distúrbios respiratórios, torácicos e do mediastino61 |
Apneia62 transitória durante a indução |
|
|
Distúrbios gastrointestinais |
Náusea21 e vômito63 durante a fase de recuperação |
|
|
Distúrbios do sistema nervoso64 |
Dor de cabeça20 durante a fase de recuperação |
|
|
Distúrbios gerais e no local de aplicação |
Sintomas65 de abstinência em crianças (4) |
|
|
Incomum |
Distúrbios vasculares60 |
Trombose66 e flebite67 |
|
Rara |
Distúrbios do sistema nervoso64 |
Movimentos epileptiformes, incluindo convulsões e opistótono68 durante a indução, manutenção e recuperação. |
|
Distúrbios psiquiátricos |
Euforia |
|
|
Muito Rara |
Distúrbios músculoesqueléticos e do tecido conjuntivo69 |
Rabdomiólise41 (5) |
|
Distúrbios gastrointestinais |
Pancreatite70 |
|
|
Lesões71, envenenamento e complicações de procedimento |
Febre72 pós-operatória |
|
|
Distúrbios renais e urinários |
Descoloração da urina24 após administração prolongada |
|
|
Distúrbios do sistema imune73 |
Anafilaxia74 - pode incluir angioedema75, broncoespasmo76, eritema77 e hipotensão30. |
|
|
Distúrbios do sistema reprodutivo e mamário |
Desinibição sexual |
|
|
Distúrbios cardíacos |
Edema pulmonar78 |
|
|
Distúrbios do sistema nervoso64 |
Inconsciência31 pós-operatória |
|
|
Desconhecida |
Sistema reprodutivo e distúrbios mamários |
Priapismo79 |
- Pode ser minimizada usando veias80 maiores do antebraço81 e da fossa antecubital. Com Propovan® a dor local também pode ser minimizada pela co-administração de lidocaína (ver item Modo de Usar).
- Ocasionalmente, hipotensão30 pode requerer o uso de fluidos intravenosos e redução da velocidade de administração de Propovan®.
- Bradicardias graves são raras. Houve relatos isolados de progressão a assistolia.
- Após interrupção abrupta de propofol durante cuidado intensivo.
- Raros relatos de rabdomiólise41 foram recebidos onde propofol foi administrado em doses superiores a 4 mg/kg/h para sedação4 em UTI.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
É possível que a superdosagem acidental acarrete depressão cardiorrespiratória. A depressão respiratória deve ser tratada através de ventilação12 artificial com oxigênio. A depressão cardiovascular requer a inclinação da cabeça20 do paciente e, se for severa, o uso de expansores plasmáticos e agentes vasopressores.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
SÓ PODE SER VENDIDO COM RETENÇÃO DA RECEITA
USO RESTRITO A HOSPITAIS
MS nº 1.0298.0134
Farm. Resp.: Dr. José Carlos Módolo - CRF-SP nº 10.446
Registrado por:
Cristália Prod. Quím. Farm. Ltda.
Rodovia Itapira-Lindoia, km 14 – Itapira – SP
CNPJ n.º 44.734.671/0001–51 – Indústria Brasileira
Fabricado por:
Cristália Prod. Quím. Farm. Ltda.
Av. Nossa Senhora da Assunção, 574 – Butantã – São Paulo – SP
CNPJ nº 44.734.671/0008–28 – Indústria Brasileira
SAC 0800 7011918






