

Vagifem
BESINS HEALTHCARE BRASIL COMERCIAL E DISTRIBUIDORA DE MEDICAMENTOS LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Vagifem
estradiol hemi-hidratado
Comprimidos vaginais 10 mcg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Comprimido vaginais
Embalagem com 18 comprimidos acompanhados de aplicadores individuais
VIA VAGINAL
USO ADULTO
COMPOSIÇÃO:
Cada comprimido vaginal de Vagifemcontém:
| estradiol hemi-hidratado | 10 mcg |
| excipiente q.s.p. | 1 comprimido |
Excipientes: Interior do comprimido: hipromelose, lactose1 monoidratada, amido, estearato de magnésio. Película de revestimento: hipromelose, macrogol.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Vagifem® é destinado ao tratamento de atrofia2 vaginal devido à deficiência de estrogênio em mulheres na pós-menopausa3.
COMO ESTE MEDICAMENTO FUNCIONA?
Vagifem® tem como princípio ativo o hormônio4 estradiol, que é idêntico ao estradiol produzido pelos ovários5 das mulheres. Vagifem® pertence a um grupo de medicamentos chamados de Terapia de Reposição Hormonal (TRH) local. É utilizado para aliviar os sintomas6 da menopausa3 na vagina7, tal como ressecamento ou irritação. Em termos médicos, isso é conhecido como ‘atrofia vaginal’, que é causada por uma queda nos níveis de estrogênio em seu corpo. Isto acontece naturalmente após a menopausa3.
Vagifem® funciona substituindo o estrogênio, que normalmente é produzido nos ovários5 das mulheres. É utilizado por via vaginal, para que o hormônio4 seja liberado no local onde é necessário, o que pode aliviar o desconforto na vagina7.
A experiência no tratamento de mulheres acima de 65 anos é limitada.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Você não deve utilizar Vagifem® nas seguintes condições:
- se você tem, teve ou suspeita que tem câncer8 de mama9;
- se você tem, teve ou suspeita que tem câncer8 sensível a estrogênio, tal como câncer8 na parede interna do útero10 (endométrio11);
- se você tem sangramento vaginal sem causa definida;
- se você tem crescimento excessivo da parede interna do útero10 (hiperplasia endometrial12) não tratada;
- se você tem ou teve um coágulo13 em algum vaso sanguíneo (trombose14), como nas pernas (trombose venosa profunda15) ou pulmões16 (embolia17 pulmonar);
- se você tem uma desordem trombolítica (ex.: deficiência de proteína C, proteína S ou antitrombina);
- se você tem ou teve recentemente uma doença causada por coágulos nas artérias18, tais como angina19, derrame20 ou ataque do coração21;
- se você tem ou se teve uma doença do fígado22 e seus valores de função hepática23 nos testes ainda não retornaram ao normal;
- se é alérgica (hipersensível) ao componente ativo ou a qualquer um dos excipientes (vide item “Composição”);
- se você tem uma doença rara do sangue24 chamada “porfiria” que pode ser de origem hereditária.
Este medicamento é contraindicado para uso por lactantes25.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Precauções e advertências
Para o tratamento de sintomas6 pós-menopausa3, a TRH só deve ser iniciada para sintomas6 que afetem negativamente a qualidade de vida. Em todos os casos, uma avaliação cuidadosa dos riscos e benefícios deve ser realizada pelo menos anualmente e a TRH somente deve ser continuada enquanto o benefício compensar o risco.
As evidências sobre os riscos associados à TRH no tratamento da menopausa3 prematura são limitadas. Devido ao baixo nível de risco absoluto em mulheres mais jovens, no entanto, o equilíbrio de riscos e benefícios para estas mulheres pode ser mais favorável do que em mulheres mais velhas.
Exames/acompanhamento médico
Antes de iniciar ou retomar a terapia hormonal, deve ser obtido um histórico médico pessoal e familiar completo. Exames físicos (incluindo pélvico26 e de mama9) devem ser orientados nesse sentido e pelas contraindicações e advertências de uso. Durante o tratamento, são recomendados exames periódicos, de frequência e natureza adaptados à mulher individualmente. As mulheres devem estar cientes que as mudanças em seus seios27 devem ser comunicadas ao seu médico. As investigações incluindo ferramentas apropriadas de imagem, como por exemplo, mamografias, devem ser efetuadas de acordo com as práticas atualmente aceitas de rastreio, modificadas para as necessidades clínicas de cada paciente.
O perfil farmacocinético de Vagifem® mostra que a entrada na corrente sanguínea (absorção sistêmica) do estradiol é muito baixa durante o tratamento, no entanto, sendo um produto de TRH, o seguinte precisa ser considerado, especialmente para o uso a longo prazo ou repetido deste produto.
Condições que necessitam acompanhamento
Se qualquer uma das seguintes condições estiverem presentes, tiver ocorrido anteriormente, e/ou tiver sido agravada durante a gravidez28 ou tratamento hormonal anterior, a paciente deve ser supervisionada de perto. Deve ser considerado que estas condições podem reaparecer ou serem agravadas durante o tratamento com estrogênio, em particular:
- Leiomioma29 (miomas uterinos) ou endometriose30 (presença de tecido31 uterino fora do interior do útero10);
- Fatores de risco para distúrbios tromboembólicos (risco para desenvolvimento de coágulos sanguíneos);
- Fatores de risco para tumores dependentes de estrógeno32, ex.: 1º grau de hereditariedade33 para câncer8 de mama9 (como ter mãe, irmã ou avó com câncer8 de mama9, por exemplo);
- Hipertensão34 (pressão alta);
- Distúrbios hepáticos (desordens na função do fígado22, como por ex.: tumor35 benigno no fígado22);
- Diabetes mellitus36;
- Colelitíase37 (cálculo38 biliar ou pedra na vesícula39);
- Enxaqueca40 ou dor de cabeça41 severa;
- Lúpus42 eritematoso43 sistêmico44 (doença do sistema imunológico45 que afeta vários órgãos do corpo);
- Histórico de hiperplasia endometrial12 (crescimento excessivo da parede interna do útero10);
- Epilepsia46;
- Asma47;
- Otosclerose48 (doença que afeta tímpano49 e ouvido).
O perfil farmacocinético de Vagifem® mostra que há muito baixa absorção de estradiol durante o tratamento. Devido a isto, a recorrência50 ou agravamento das condições acima mencionadas é menos provável do que com o tratamento sistêmico44 com estrogênio.
Interrompa imediatamente a utilização e consulte o seu médico
A terapia com Vagifem® deve ser interrompida caso ocorra alguma das seguintes situações:
- Icterícia51 (presença de cor amarelada na pele52 ou na parte branca dos olhos53), isto pode ser um sinal54 de uma doença do fígado22;
- Aumento significativo da pressão arterial55 (sintomas6 podem ser dor de cabeça41, cansaço, tontura56);
- Aparecimento de dor de cabeça41 tipo enxaqueca40 pela primeira vez;
- Gravidez28.
Vagifem® é uma preparação de estradiol de dose baixa e ação local e, portanto, a ocorrência das condições abaixo mencionadas é menos provável do que com o tratamento sistêmico44 de estrogênio.
Hiperplasia endometrial12 (crescimento excessivo da parede interna do útero10) e carcinoma57 (câncer8) Mulheres com útero10 intacto com sangramento anormal de causa desconhecida ou mulheres com útero10 intacto que tenham sido previamente tratadas com estrogênios isolados (ex.: sem o uso de progesterona associada) devem ser examinadas com cuidado especial, de forma a excluir estimulação aumentada/risco de câncer8 do endométrio11 antes do início do tratamento com Vagifem®.
Em mulheres com útero10 intacto os riscos de hiperplasia endometrial12 (crescimento excessivo da parede interna do útero10) e câncer8 são aumentados quando os estrogênios são administrados sozinhos por períodos prolongados. O aumento relatado no risco de câncer8 endometrial entre usuárias de estrogênio isolado sistêmico44 varia de 2 a 12 vezes em comparação com as não usuárias, dependendo da duração do tratamento e da dose de estrogênio. Após a interrupção do tratamento, o risco pode permanecer elevado por pelo menos 10 anos.
Durante o tratamento com Vagifem®, um menor grau de entrada na corrente sanguínea pode ocorrer em algumas pacientes, especialmente durante as duas primeiras semanas de administração uma vez ao dia. No entanto, as concentrações médias plasmáticas permanecem dentro da faixa de normalidade na pós-menopausa3 em todas as pacientes.
A segurança endometrial a longo prazo (mais de um ano) ou o uso repetido de estrogênio administrado localmente via vaginal é incerta. Portanto, se repetido, o tratamento deve ser avaliado pelo menos anualmente, com especial atenção dada a quaisquer sintomas6 de hiperplasia endometrial12 (crescimento excessivo da parede interna do útero10) ou carcinoma57 (câncer8).
Como regra geral, a terapia de reposição de estrogênio não deve ser prescrita por mais de um ano sem realizar outro exame físico, incluindo os ginecológicos.
Se sangramento ou sangramento de escape (sangramento mínimo) aparecerem a qualquer momento durante a terapia, a razão deve ser investigada, o que pode incluir biópsia58 endometrial para excluir risco de câncer8 endometrial.
A mulher deve ser aconselhada a contatar o seu médico caso ocorra sangramento ou sangramento de escape (sangramento mínimo) durante o tratamento com Vagifem®.
O uso de estrogênio isolado (ex.: sem o uso de progesterona associada) pode levar à transformação pré-maligna ou maligna (risco de câncer8) nos focos residuais da endometriose30. Portanto, é aconselhável ter cuidado ao usar este produto em mulheres que sofreram histerectomia59 (remoção de parte ou totalidade do útero10) por causa de endometriose30, especialmente se são conhecidas por terem endometriose30 residual.
Câncer8 de mama9
A evidência geral sugere um risco aumentado de câncer8 de mama9 em mulheres que utilizam estrogênio e progestágeno combinados e possivelmente também TRH de estrogênio isolado (ex.: sem o uso de progesterona associada), dependente da duração da TRH.
O ensaio WHI não constatou aumento no risco de câncer8 de mama9 em mulheres histerectomizadas (remoção de parte ou totalidade do útero10) usando TRH de estrogênio isolado. Estudos observacionais relataram, em sua maioria, um pequeno aumento no risco de ter câncer8 de mama9 diagnosticado, o que é substancialmente menor do que o encontrado em usuárias de combinações de estrogênio e progestágeno.
O risco adicional torna-se aparente dentro de alguns anos de uso, mas retorna à taxa normal dentro de poucos anos (no máximo cinco) após a interrupção do tratamento.
Uma relação entre o risco de câncer8 de mama9 e a terapia local de baixa dose de estrogênio vaginal é incerta.
A TRH, especialmente o tratamento combinado de estrogênio e progestágeno, aumenta a densidade das imagens mamográficas, o que pode afetar adversamente a detecção radiológica do câncer8 de mama9.
Câncer8 de ovário60
O câncer8 de ovário60 é muito mais raro do que o câncer8 de mama9. O uso prolongado (pelo menos de 5 a 10 anos) de produtos de TRH de estrogênio isolado tem sido associado a um risco ligeiramente aumentado de câncer8 de ovário60. Alguns estudos, incluindo o ensaio WHI, sugerem que o uso a longo prazo de TRH combinada pode proporcionar um risco semelhante ou um pouco menor.
Uma relação entre o risco de câncer8 de ovário60 e a terapia local de baixa dose de estrogênio vaginal é incerta.
Tromboembolismo61 venoso (coágulos sanguíneos na veia)
A TRH está associada a um risco de 1,3 a 3 vezes de desenvolver tromboembolismo61 venoso (TEV), ou seja, trombose venosa profunda15 ou embolia17 pulmonar. A ocorrência de tal evento é mais provável no primeiro ano de TRH do que mais tarde.
As pacientes com estados trombofílicos conhecidos têm um maior risco de TEV e a TRH pode aumentar esse risco. A TRH é, portanto, contraindicada para estas pacientes.
Fatores de risco geralmente reconhecidos para TEV incluem o uso de estrogênios, idade avançada, cirurgia de grande porte, imobilização prolongada, obesidade62 (IMC63 > 30kg/m²), período de gravidez28/pós-parto, lúpus42 eritematoso43 sistêmico44 (LES) e câncer8. Não há consenso sobre o possível papel das veias64 varicosas na TEV. Uma relação entre tromboembolismo61 venoso e terapia local de baixa dose de estrogênio vaginal é incerta.
Como em todas as pacientes no pós-operatório, medidas profiláticas devem ser consideradas para prevenir TEV após cirurgia. Caso seja prevista uma imobilização prolongada devido a uma cirurgia programada, é recomendado parar temporariamente a TRH de 4 a 6 semanas antes. O tratamento não deve ser reiniciado até que a mulher esteja completamente móvel.
Em mulheres sem histórico pessoal de TEV, mas com familiar de primeiro grau com histórico de trombose14 em idade jovem, o exame pode ser oferecido após aconselhamento cuidadoso sobre suas limitações (apenas uma proporção de problemas trombofílicos é identificada pelo exame).
Se for identificado um problema trombofílico que segregue com trombose14 em membros da família, ou se o problema for 'grave' (por exemplo, deficiência de antitrombina, proteína S ou proteína C, ou uma combinação de problemas) a TRH é contraindicada.
As mulheres já em tratamento crônico65 com anticoagulante66 requerem uma análise cuidadosa do risco-benefício do uso da TRH.
Caso se desenvolva TEV após iniciar a terapia, o medicamento deve ser descontinuado. As pacientes devem entrar imediatamente em contato com seus médicos quando perceberem um potencial sintoma67 tromboembólico (por exemplo, inchaço68 doloroso de uma perna, dor súbita no peito69, dispneia70).
Doença arterial coronária (DAC)
Não há evidências de ensaios clínicos71 randomizados controlados de proteção contra infarto do miocárdio72 em mulheres com ou sem DAC existente, que receberam terapia combinada73 de estrogênio e progestágeno ou de estrogênio isolada (ex.: sem o uso de progesterona associada).
Os dados controlados randomizados não indicaram risco aumentado de DAC em mulheres histerectomizadas usando a terapia de estrogênio isolada.
Acidente vascular cerebral74 isquêmico75 (derrame20)
As terapias combinadas de estrogênio e progestágeno e de estrogênio isolada (ex.: sem o uso de progesterona associada), estão associadas a um aumento de até 1,5 vez no risco de AVC isquêmico75. O risco relativo não muda com a idade ou o tempo desde a menopausa3. No entanto, como o risco normal de incidência76 de AVC é fortemente dependente da idade, o risco geral de AVC em mulheres que usam a TRH aumenta com a idade. Uma relação entre AVC isquêmico75 e a terapia local de baixa dose de estrogênio vaginal é incerta.
Outras condições
Estrogênios podem causar retenção de líquidos, e, portanto, as pacientes com disfunção cardíaca ou renal77 devem ser cuidadosamente observadas.
Mulheres com hipertrigliceridemia (níveis elevados de gordura78/triglicérides79 no sangue24) preexistente devem ser seguidas de perto durante a terapia de reposição estrogênica ou de reposição hormonal, uma vez que raros casos de grandes aumentos de triglicérides79 plasmáticos levando à pancreatite80 foram relatados com a terapia de estrogênio nesta condição.
A relação entre a hipertrigliceridemia (níveis elevados de gordura78/triglicérides79 no sangue24) preexistente e a terapia local de baixa dose de estrogênio vaginal é desconhecida.
Os estrogênios podem aumentar os níveis de proteínas81 transportadoras no sangue24 tais como a globulina82 ligadora de tiroxina (TBG), globulina82 ligadora de corticosteroide (CBG), globulina82 ligadora de hormônios sexuais (SHBG) e outras proteínas81 do plasma83 (substrato de angiotensina/renina, alfa-1 antitripsina, ceruloplasmina), ocasionando aumento dos níveis circulantes de hormônios tireoidianos T3 ou T4, corticosteroides e esteroides sexuais, mas não a concentração livre ou biologicamente ativa destes.
É provável que estes efeitos estejam menos pronunciados devido a entrada mínima do estradiol na corrente sanguínea com a administração vaginal local.
A TRH não melhora a função cognitiva84. Há algumas evidências do ensaio WHI do aumento do risco de provável demência85 em mulheres que começam a utilizar a TRH contínua combinada ou de estrogênio isolada após a idade de 65 anos.
O aplicador intravaginal pode causar pequenos traumas locais, especialmente em mulheres com atrofia2 vaginal grave.
Efeitos na habilidade de dirigir e operar máquinas
Não há efeitos conhecidos.
Gravidez28 e Lactação86
Vagifem® não é indicado durante a gravidez28. Caso ocorra a gravidez28 durante tratamento com Vagifem®, o tratamento deve ser retirado imediatamente. Os resultados da maioria dos estudos epidemiológicos até a atualidade relevantes para a exposição fetal inadvertida aos estrogênios não indicam efeitos teratogênicos87 (malformação88 fetal) ou fetotóxicos (tóxicos para o feto89)
Este medicamento não deve ser utilizado por mulheres grávidas ou que possam ficar grávidas durante o tratamento.
Vagifem® não é indicado durante a lactação86.
Interações Medicamentosas
Como o estrogênio no Vagifem® é administrado de forma intravaginal e, devido aos baixos níveis de estradiol liberados, é improvável que quaisquer interações medicamentosas clinicamente relevantes ocorram com Vagifem®.
No entanto, o metabolismo90 de estrogênios pode ser aumentado pelo uso concomitante de substâncias conhecidas por induzir enzimas metabolizadoras de medicamentos, especificamente as enzimas do citocromo P450, tais como anticonvulsivantes (por exemplo, fenobarbital, fenitoína, carbamazepina) e anti-infecciosos (por exemplo, rifampicina, rifabutina, nevirapina, efavirenz).
Ritonavir e nelfinavir, embora conhecidos como fortes inibidores, por contraste apresentam propriedades indutoras quando utilizados concomitantemente com hormônios esteroides. As preparações à base de plantas contendo erva de São João (Hypericum perforatum) podem induzir o metabolismo90 dos estrogênios.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde91.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Vagifem® deve ser conservado em temperatura ambiente (15–30°C). Não refrigerar.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Comprimido branco, biconvexo, revestido por película, gravado com NOVO 278 em um dos lados. Diâmetro de 6 mm.
Cada comprimido individual está contido em um aplicador descartável, de uso único, de polietileno/polipropileno. Os aplicadores são embalados separadamente em blisters de PVC/folha de alumínio.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Posologia
Dose inicial: Um comprimido vaginal de 10 mcg diariamente por 2 semanas.
Dose de manutenção: Um comprimido vaginal duas vezes por semana.
O tratamento pode ser iniciado em qualquer dia, que seja conveniente.
Para o início e continuidade do tratamento de sintomas6 da pós-menopausa3, deve-se utilizar a mínima dose eficaz, pelo período mais curto.
Vagifem® é uma terapia vaginal local e em mulheres com um útero10 intacto, não é necessário tratamento progestagênico (tratamento com hormônio4 do tipo progestágeno) adicional.
Vagifem® pode ser utilizado em mulheres com ou sem útero10 intacto.
Infecções92 vaginais devem ser tratadas antes do início da terapia com Vagifem®. A experiência no tratamento de mulheres acima de 65 anos é limitada.
Siga a orientação do seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
Este medicamento não deve ser partido, aberto ou mastigado.
Modo de Usar
- Vagifem® é administrado de forma intravaginal, como terapia local de estrogênio com uso de aplicador.
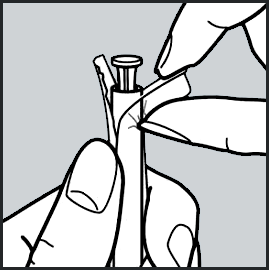
- Rasgue uma única embalagem do blister.
- Abra a extremidade do êmbolo93, como mostrado na figura.
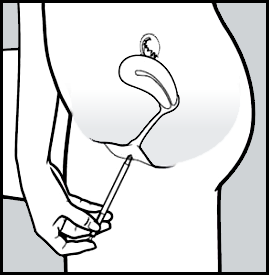
- Introduza o aplicador cuidadosamente na vagina7.
- Pare quando puder sentir alguma resistência (8 a 10 cm).
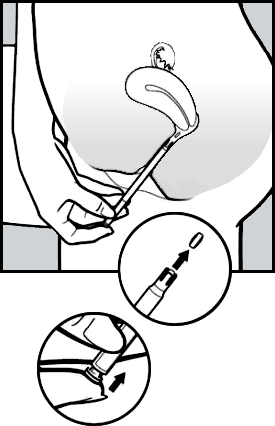
- Para liberar o comprimido, pressione suavemente o botão até sentir um clique.
O comprimido irá, imediatamente, aderir na parede da vagina7. Não cairá se você ficar de pé ou andar.

- Retire o aplicador e jogue-o fora.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Em caso de esquecimento, utilize o medicamento assim que se lembrar. Não dobre a dose para repor a que foi esquecida.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Reações adversas
Eventos adversos relacionados ao estrogênio, como dor na mama9, edema94 periférico e sangramentos pós- menopausa3 foram relatados em taxas muito baixas, semelhantes ao placebo95, com Vagifem® 10 microgramas, mas se ocorrerem, estão geralmente presentes apenas no início do tratamento. Os eventos adversos observados com maior frequência em pacientes tratadas com Vagifem® 10 microgramas, em comparação com o placebo95, e que possivelmente estão relacionados ao tratamento são apresentados abaixo.
|
Classe de órgão do sistema |
Comum |
Incomum |
Raro |
|
Infecções92 e infestações |
|
Infecção96 micótica vulvovaginal |
|
|
Distúrbios do sistema nervoso97 |
Dor de cabeça41 |
|
|
|
Distúrbios gastrointestinais |
Dor de estômago98 |
Náuseas99 (Enjoo) |
|
|
Distúrbios do sistema reprodutivo e da mama9 |
Sangramento vaginal, corrimento vaginal ou desconforto vaginal |
|
|
|
Distúrbios de pele52 e do tecido subcutâneo100 |
|
Lesões101 na pele52 |
|
|
Investigações |
|
Aumento de peso |
|
|
Distúrbios vasculares102 |
|
Ondas de calor Pressão alta |
|
Reações Adversas Medicamentosas de fontes de pós-comercialização
Além das reações adversas medicamentosas mencionadas acima, aquelas apresentadas a seguir têm sido relatadas espontaneamente para pacientes103 tratadas com Vagifem® 25 microgramas e são consideradas como possivelmente relacionadas ao tratamento. A taxa de relatos destas reações adversas espontâneas é muito rara (< 1/10.000 paciente-anos).
- Neoplasmas104 benignos e malignos (incluindo cistos e pólipos105): câncer8 de mama9, câncer8 de endométrio11;
- Distúrbios do sistema imunológico45: reações de hipersensibilidade generalizada (por exemplo, reação/choque anafilático106);
- Distúrbios do metabolismo90 e nutrição107: retenção de líquidos;
- Transtornos psiquiátricos: insônia;
- Distúrbios do sistema nervoso97: enxaqueca40 agravada;
- Distúrbios vasculares102: trombose venosa profunda15;
- Distúrbios gastrointestinais: diarreia108;
- Distúrbios de pele52 e do tecido subcutâneo100: urticária109 (pele52 irritada), erupção110 cutânea111 eritematosa112 (lesão113 vermelha na pele52), erupção110 cutânea111 pruriginosa (lesão113 na pele52 que coça), prurido114 genital (coceira na vagina7);
- Distúrbios do sistema reprodutivo e da mama9: hiperplasia endometrial12 (crescimento excessivo da parede interna do útero10), irritação vaginal, dor vaginal, vaginismo, ulceração115 vaginal;
- Distúrbios gerais e condições do local de administração: ineficácia terapêutica116;
- Investigações: aumento de peso, aumento do estrógeno32 sanguíneo.
Outras reações adversas foram relatadas em associação com o tratamento de estrogênio. As estimativas de risco foram delineadas a partir da exposição sistêmica e não se sabe como estas se aplicam aos tratamentos locais:
- Infarto do miocárdio72, doença cardíaca congestiva;
- Acidente vascular cerebral74;
- Doença da vesícula biliar117;
- Distúrbios de pele52 e subcutâneos: cloasma118 (manchas descoloridas na pele52, em especial na face119), eritema multiforme120 ou nodoso (manchas avermelhadas doloridas ou castanhas na pele52), púrpura121 vascular122 (manchas arroxeadas na pele52);
- Aumento no tamanho de miomas;
- Epilepsia46;
- Desordens da libido123;
- Deterioração da asma47;
- Provável demência85 acima dos 65 anos.
Risco de câncer8 de mama9
As estimativas de risco foram delineadas a partir da exposição sistêmica e não se sabe como estas se aplicam aos tratamentos locais.
Relata-se aumentado em até 2 vezes o risco de ter câncer8 de mama9 diagnosticado em mulheres que utilizam a terapia combinada73 de estrogênio e progestágeno por mais de 5 anos.
Qualquer risco aumentado em usuárias de terapia de estrogênio isolado é substancialmente mais baixo do que a observada em usuárias de terapia combinada73 de estrogênio e progestágeno.
O nível de risco é dependente da duração do uso.
São apresentados os resultados do maior ensaio aleatorizado controlado por placebo95 (estudo WHI) e maior estudo epidemiológico (MWS).
Estudo de um Milhão de Mulheres – Risco adicional estimado de câncer8 de mama9 após 5 anos de uso
|
Faixa etária (anos) |
Incidência76 por 1.000 nunca usuárias de TRH durante um período mais de 5 anos* |
Taxa de risco e IC 95% # |
Casos adicionais por 1.000 usuárias TRH por mais de 5 anos (IC 95%) |
|
TRH de estrogênio isolado |
|||
|
50–65 |
9–12 |
1,2 |
1–2 (0–3) |
|
Estrogênio-progestagênio combinados |
|||
|
50–65 |
9–12 |
1,7 |
6 (5–7) |
* Considerado das taxas de incidência76 basais nos países desenvolvidos.
# Taxa de risco geral. A taxa de risco não é constante, mas aumentará com o aumento da duração do uso. Nota: Visto que a incidência76 de antecedentes de câncer8 de mama9 difere por país da UE, o número de casos adicionais de câncer8 de mama9 também irá mudar proporcionalmente.
Estudos de WHI nos EUA – risco adicional de câncer8 de mama9 após uso de 5 anos
|
Faixa etária (anos) |
Incidência76 por 1.000 mulheres no braço placebo95 por mais de 5 anos |
Taxa de risco e 95% CI |
Casos adicionais por 1.000 usuárias de TRH por mais de 5 anos (IC 95%) |
|
CEE estrogênio isolado |
|||
|
50 – 79 |
21 |
0,8 (0,7 – 1,0) |
-4 (-6 – 0)* |
|
CEE+MPA estrogênio e progestagênio‡ |
|||
|
50 – 79 |
17 |
1,2 (1,0 – 1,5) |
+4 (0 – 9) |
* Estudo de WHI em mulheres sem útero10, que não mostraram um aumento no risco de câncer8 de mama9.
‡Quando a análise se restringiu à mulheres que não haviam utilizado TRH anteriormente ao estudo não houve risco aumentado aparente durante os primeiros 5 anos de tratamento: após 5 anos o risco era maior do que em não usuárias.
Risco de câncer8 endometrial
Mulheres na pós-menopausa3 com útero10
O risco de câncer8 endometrial é de cerca de 5 em cada 1.000 mulheres com útero10 não utilizando TRH.
Em mulheres com útero10, o uso de TRH sistêmica de estrogênio isolado não é recomendado, porque aumenta o risco de câncer8 endometrial.
Dependendo da duração do uso de terapia sistêmica de estrogênio isolado e da dosagem de estrogênio, o aumento no risco de câncer8 endometrial em estudos epidemiológicos variou entre 5 e 55 casos extras diagnosticados em cada 1.000 mulheres entre idades de 50 e 65 anos.
A adição de um progestágeno à terapia sistêmica de estrogênio isolado durante pelo menos 12 dias por ciclo pode evitar este risco aumentado. No Estudo de um Milhão de Mulheres, a utilização de cinco anos da TRH combinada (sequencial ou contínua) não aumentou o risco de câncer8 endometrial (RR de 1,0 (0,8-1,2)).
Câncer8 de ovário60
As estimativas de risco foram delineadas a partir da exposição sistêmica e não se sabe como estas se aplicam aos tratamentos locais.
O uso prolongado de TRH de estrogênio isolado e estrogênio e progestágeno combinados tem sido associado a um risco ligeiramente aumentado de câncer8 de ovário60. No Estudo de um Milhão de Mulheres, 5 anos de TRH resultou em 1 caso extra a cada 2.500 usuárias.
Risco de tromboembolismo61 venoso (coágulos sanguíneos na veia)
As estimativas de risco foram delineadas a partir da exposição sistêmica e não se sabe como estas se aplicam aos tratamentos locais.
A TRH está associada a um risco relativo aumentado de 1,3 a 3 vezes de desenvolver tromboembolismo61 venoso (TEV), ou seja, trombose venosa profunda15 ou embolia17 pulmonar. A ocorrência de tal evento é mais provável no primeiro ano do uso de TRH. Os resultados dos estudos de WHI são apresentados:
Estudos de WHI – Risco adicional de TEV com uso por mais de 5 anos
|
Faixa etária (anos) |
Incidência76 por 1.000 mulheres no braço placebo95 por mais de 5 anos |
Taxa de risco e IC 95% |
Casos adicionais por 1.000 usuárias de TRH |
|
Estrogênio isolado oral* |
|||
|
50–59 |
7 |
1,2 (0,6–2,4) |
1 (-3–10) |
|
Estrogênio-progestagênio orais combinados |
|||
|
50 – 59 |
4 |
2,3 (1,2 – 4,3) |
5 (1 – 13) |
* Estudo em mulheres sem útero10.
Risco de doença arterial coronariana
As estimativas de risco foram delineadas a partir da exposição sistêmica e não se sabe como estas se aplicam aos tratamentos locais.
O risco de doença arterial coronariana é ligeiramente aumentado em usuárias de TRH combinada de estrogênio e progestágeno em idade superior a 60 anos.
Risco de AVC isquêmico75 (derrame20 cerebral)
As estimativas de risco foram delineadas a partir da exposição sistêmica e não se sabe como estas se aplicam aos tratamentos locais.
O uso de terapia de estrogênio isolado e de estrogênio e progestágeno está associado com um aumento de risco relativo de até 1,5 vezes de acidente vascular cerebral74 isquêmico75. O risco de AVC hemorrágico124 não é aumentado durante o uso da TRH.
Este risco relativo não é dependente da idade ou duração do uso, mas como o risco basal é fortemente dependente da idade, o risco geral de acidente vascular cerebral74 em mulheres que usam TRH irá aumentar com a idade.
Estudos combinados de WHI – Risco adicional de AVC isquêmico75* com uso por mais de 5 anos
* Considerado das taxas de incidência76 basais nos países desenvolvidos. # Taxa de risco geral. A taxa de risco não é constante, mas aumentará com o aumento da duração do uso. Nota: Visto que a incidência76 de antecedentes de câncer8 de mama9 difere por país da UE, o número de casos adicionais de câncer8 de mama9 também irá mudar proporcionalmente.|
Faixa etária (anos) |
Incidência76 por 1.000 mulheres no braço placebo95 por mais de 5 anos |
Taxa de risco e IC 95% |
Casos adicionais por 1.000 usuárias de TRH por mais de 5 anos |
|
50 – 59 |
8 |
1,3 (1,1 – 1,6) |
3 (1 – 5) |
* Nenhuma diferenciação foi feita entre AVC isquêmico75 e hemorrágico124.
População pediátrica
Não há dados clínicos sobre uso em crianças.
Atenção: este produto é um medicamento que possui nova forma farmacêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
A superdose de estradiol por via oral pode causar: náuseas99 e vômitos125.
Vagifem® destina-se ao uso intravaginal e a dose de estradiol é muito baixa. A superdose, portanto, é improvável, mas se isso ocorrer, o tratamento consiste na suspensão do medicamento e cuidados sintomáticos.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Reg. MS. 1.8759.0007
Farm. Resp.: Talita Tonelato Menezes - CRF/SP 74.229
Registrado e importado por:
Besins Healthcare Brasil Com. Dist. Med. Ltda.
Rua Alexandre Dumas, 1658 - São Paulo/SP
CNPJ: 11.082.598/0001-21
Fabricado e embalado por:
Novo Nordisk A/S
Novo Allé - DK-2760
Maaloev - Dinamarca
SAC 0800 777 24 30






