Heptris (Bula do profissional de saúde)
MYLAN LABORATORIOS LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Heptris®
enoxaparina sódica
Injetável 20 mg/0,2 mL; 40 mg/0,4 mL; 60 mg/0,6 mL; 80 mg/0,8 mL; 100 mg/1,0 mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
seringas preenchidas com e sem sistema de segurança
USO SUBCUTÂNEO1 OU INTRAVENOSO (a via de administração varia de acordo com a indicação do produto).
USO ADULTO
COMPOSIÇÃO:
Cada seringa2 de Heptris® 20 mg contém:
| enoxaparina sódica | 20 mg |
| água para injetáveis q.s.p. | 0,2 mL |
Cada seringa2 de Heptris® 40 mg contém
| enoxaparina sódica | 40 mg |
| água para injetáveis q.s.p. | 0,4 mL |
Cada seringa2 de Heptris® 60 mg contém
| enoxaparina sódica | 60 mg |
| água para injetáveis q.s.p. | 0,6 mL |
Cada seringa2 de Heptris® 80 mg contém
| enoxaparina sódica | 80 mg |
| água para injetáveis q.s.p. | 0,8 mL |
Cada seringa2 de Heptris® 100 mg contém
| enoxaparina sódica | 100 mg |
| água para injetáveis q.s.p. | 1,0 mL |
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE3
INDICAÇÕES
- Tratamento da trombose venosa profunda4 com ou sem embolismo5 pulmonar;
- Tratamento da angina6 instável e infarto do miocárdio7 sem elevação do segmento ST, administrado concomitantemente ao ácido acetilsalicílico;
- Tratamento de infarto8 agudo9 do miocárdio10 com elevação do segmento ST, incluindo pacientes a serem tratados clinicamente ou com subsequente intervenção coronariana percutânea;
- Profilaxia do tromboembolismo11 venoso, em particular aqueles associados à cirurgia ortopédica ou à cirurgia geral;
- Profilaxia do tromboembolismo11 venoso em pacientes acamados devido a doenças agudas incluindo insuficiência cardíaca12, falência respiratória, infecções13 severas e doenças reumáticas;
- Prevenção da formação de trombo14 na circulação15 extracorpórea durante a hemodiálise16.
RESULTADOS DE EFICÁCIA
Heptris® é um medicamento biológico desenvolvido pela via da comparabilidade (biossimilar). O programa de desenvolvimento do produto foi projetado para demonstrar a comparabilidade entre Heptris® e o medicamento comparador Clexane.
DADOS DE Clexane
Cirurgia abdominal
Em um estudo duplo-cego17 em pacientes submetidos à cirurgia eletiva18 de tumores gastrointestinais, urológicos19, ou do trato ginecológico, um total de 1.116 pacientes foram incluídos e 1.115 receberam profilaxia de TEV.
Clexane 40 mg SC, uma vez ao dia, começando 2h antes da cirurgia e continuado por um período de no máximo 12 dias após a cirurgia, teve sua eficácia comparada a da heparina não fracionada (HNF) 5000 U SC a cada 8h na redução do risco de trombose venosa profunda4 (TVP). Os dados de eficácia são apresentados abaixo [ver tabela 1] (Bergqvist et al, 1997).
Tabela 1 - Eficácia de Clexane na profilaxia de TVP após cirurgia abdominal
|
Indicação |
Regime |
|
|
Clexane |
Heparina 5000 U SC cada 8h n (%) |
|
|
Todos os pacientes submetidos à cirurgia abdominal que receberam profilaxia |
555 (100) |
560 (100) |
|
TEV total1 (%) |
56 (10,1) |
63 (11,3) |
|
Somente TVP (%) |
54 (9,7) |
61 (10,9) |
1 TEV = tromboembolismo11 venoso incluíram TVP, EP e óbitos considerados de causa tromboembólica.
2 IC = Intervalo de Confiança
Em outro estudo duplo-cego17, Clexane 40 mg SC uma vez ao dia foi comparado com HNF 5000 U SC a cada 8h, em pacientes submetidos à cirurgia colorretal (um terço deles com câncer20). Um total de 1.347 pacientes foi incluído no estudo e todos receberam tratamento. A profilaxia foi iniciada aproximadamente 2h antes da cirurgia e continuada por aproximadamente 7 a 10 dias após a cirurgia. Os dados de eficácia são apresentados abaixo [ver tabela 2] (MacLeod RS et al, 2001).
Tabela 2 - Eficácia de Clexane na profilaxia de TVP após cirurgia de câncer20 colorretal
|
Indicação |
Regime |
|
|
Clexane |
Heparina |
|
|
Todos os pacientes submetidos à cirurgia colorretal que receberam profilaxia |
673 (100) |
674 (100) |
|
TEV total1 (%) |
48 (7,1) |
45 (6,7) |
| Somente TVP (%) |
47 (7,0) |
44 (6,5) |
1 TEV = tromboembolismo11 venoso incluíram TVP, EP e óbitos considerados de causa tromboembólica.
2 IC = Intervalo de Confiança
Cirurgia geral oncológica
Em estudo duplo cego17 randomizado21 multicêntrico conduzido com pacientes submetidos à cirurgia abdominal ou pélvica22 oncológica curativa, 332 pacientes receberam Clexane 40 mg uma vez ao dia, por 6 a 10 dias e após este período, foram randomizados para receber placebo23 ou manter a profilaxia com Clexane 40 mg uma vez ao dia por 19 a 21 dias adicionais, totalizando um período de tratamento de 25 a 31 dias. O desfecho primário de eficácia analisado foi a incidência24 de de tromboembolismo11 venoso diagnosticada à venografia entre os dias 25 e 31. Os resultados de eficácia são apresentados na tabela abaixo [ver tabela 3]. Todos os pacientes foram acompanhados por 3 meses. (Berqgvist, 2002).
Tabela 3 - Incidência24 de eventos tromboembólicos
|
Evento |
Placebo23 |
Enoxaparina |
Redução do risco |
P |
|
n= 167 |
n= 165 |
(95% IC)1 |
||
|
Nº(%) |
% |
|||
|
Durante o período duplo cego |
|
|||
|
TEV Total |
20(12,0) |
8(4,8) |
60(10-82) |
0,02 |
|
TVP Proximal25 |
3(1,8) |
1(0,6) |
|
|
|
TVP Distal26 |
17(10,2) |
7(4,2) |
|
|
|
Embolia27 pulmonar |
1(0,6)* |
0 |
|
|
|
No 3º mês |
|
|||
|
TEV Total |
23(13,8) |
9(5,5) |
60(17-81) |
0,01** |
|
TVP Proximal25 |
4(2,4) |
2(1,2) |
|
|
|
TVP Distal26 |
17(10,2) |
7(4,2) |
|
|
|
Embolia27 pulmonar |
2(1,2) |
0 |
|
|
1 Intervalo de confiança
*O paciente com embolia27 pulmonar também apresentou TVP distal26
** Um caso de TVP em membro superior distal26 no grupo placebo23 foi incluído, se este caso fosse excluído, P=0,02
Artroplastia de quadril
Em um estudo duplo-cego17, randomizado21, Clexane 40 mg SC uma vez ao dia foi comparado com HNF 5000 U SC a cada 8h, após artroplastia total de quadril. A profilaxia foi iniciada 12h antes da cirurgia, no caso da enoxaparina, e 2h antes da cirurgia, no caso da heparina. Um total de 237 pacientes foram randomizados no estudo e receberam profilaxia. Os resultados de eficácia são mostrados na tabela abaixo [ver tabela 3] (Planes et al 1988).
Tabela 4 - Eficácia de Clexane na profilaxia de TVP após artroplastia total de quadril
|
Indicação |
Regime |
|
|
Clexane |
Heparina |
|
|
TVP total |
12,5%1 |
25% |
|
TVP proximal25 (%) |
7,5%2 |
18,5% |
1 valor de p versus heparina = 0,03; redução de risco relativo de 50%
2 valor de p versus heparina = 0,014; redução de risco relativo de 59%
Um estudo duplo-cego17, multicêntrico, comparou três regimes de dose de Clexane em pacientes submetidos à artroplastia de quadril. Um total de 572 pacientes foram randomizados e 568 receberam a profilaxia proposta. Profilaxia com Clexane foi iniciada 2 dias após a cirurgia e continuou por 7 a 11 dias após a cirurgia. Os dados de eficácia são fornecidos abaixo [ver tabela 4] (Spiro et al, 1994).
Tabela 5 - Eficácia de Clexane na profilaxia de TVP após cirurgia de artroplastia de quadril
|
Indicação |
Regime |
||
|
10 mg SC cada 24h n (%) |
30 mg SC cada 12h n (%) |
40 mg SC cada 24h n (%) |
|
|
Todos os pacientes |
161 (100) |
208 (100) |
199 (100) |
|
TVP total (%) |
40 (25) |
22 (11)1 |
27 (14) |
|
TVP proximal25 (%) |
17 (11) |
8 (4)2 |
9 (5) |
1 valor de p versus Clexane 10 mg cada 24h = 0,0008
2 valor de p versus Clexane 10 mg cada 24h = 0,0168
Não houve diferença significativa entre os regimes de 30 mg cada 12h e 40 mg cada 24h.
Em um estudo de profilaxia estendida para pacientes28 submetidos à artroplastia de quadril, os pacientes receberam durante a internação, Clexane 40 mg SC iniciado 12h antes da cirurgia para prevenir TVP pós-operatória. Ao final do período perioperatório, todos os pacientes foram submetidos à venografia bilateral. Seguindo um desenho duplo- cego, todos os pacientes sem evidência de doença tromboembólica foram randomizados para um regime pós-alta de Clexane 40 mg (n = 90) por via SC, uma vez ao dia ou de placebo23 (n = 89) por 3 semanas. Nessa população de pacientes, a incidência24 de TVP durante a fase de profilaxia estendida foi significativamente mais baixa no grupo que recebeu Clexane comparado ao placebo23. Os dados de eficácia são apresentados na tabela abaixo [ver tabela 5] (Planes et al 1996).
Tabela 6 - Eficácia de Clexane na profilaxia estendida de TVP após artroplastia de quadril
|
Indicação (Pós-alta) |
Regime pós-alta |
|
|
Clexane |
Placebo23 |
|
|
Todos os pacientes com profilaxia estendida |
90 (100) |
89 (100) |
|
TVP total (%) |
6 (7)1 (95% IC2: 3 a 14) |
18 (20) |
|
TVP proximal25 (%) |
5 (6)3 |
7 (8) |
1 valor de p versus placebo23 = 0,008
2 IC= Intervalo de confiança
3 valor de p versus placebo23 = 0,537
Em um segundo estudo, pacientes submetidos à artroplastia de quadril receberam durante a hospitalização Clexane 40 mg SC, iniciado 12h antes da cirurgia. Todos os pacientes foram examinados em busca de sinais29 e sintomas30 de doença tromboembólica. Pacientes sem qualquer sinal31 de TEV foram randomizados para um regime pós-alta com Clexane 40 mg SC uma vez ao dia (n = 131) ou placebo23 (n = 131) por 3 semanas. Um total de 262 pacientes foram randomizados nessa fase duplo-cega. De modo semelhante ao primeiro estudo, a incidência24 de TVP durante a profilaxia estendida foi significativamente menor com Clexane quando comparado ao placebo23, com diferença estatisticamente significativa tanto na incidência24 TVP total (Clexane [16%] versus placebo23 45 [34%]; p = 0,001) quanto na de TVP proximal25 (Clexane 8 [6%] versus placebo23 28 [21%]; p = <0,001) (Bergqvist et al, 1996).
Artroplastia de joelho
Um total de 132 pacientes foram randomizados no estudo e 131 receberam profilaxia. Após hemostasia32, profilaxia foi iniciada 12 a 24h após a cirurgia e continuada por até 15 dias. A incidência24 de TVP total e proximal25 após cirurgia foi significativamente mais baixa no grupo que recebeu Clexane comparado ao placebo23. Os dados de eficácia são mostrados abaixo [ver tabela 6] (Leclerc et al, 1992).
Tabela 7 - Eficácia de Clexane na profilaxia de trombose venosa profunda4 após artroplastia total de Joelho
|
Indicação |
Regime |
|
|
Clexane 30 mg |
Placebo23 |
|
|
Todos os pacientes submetidos a artroplastia de joelho |
47 (100) |
52 (100) |
|
TVP Total (%) |
5 (11)1 |
32 (62) |
|
TVP proximal25 (%) |
0 (0)3 |
7 (13) |
1 valor de p versus placebo23 = 0,0001
2 IC = Intervalo de Confiança
3 valor de p versus placebo23 = 0,013
4 LC = Limite de Confiança
Ainda em artroplastia eletiva18 de joelho, outro estudo clínico aberto, de grupos paralelos, randomizado21, comparou Clexane 30 mg SC a cada 12h com heparina 5000 U SC a cada 8h. Um total de 453 pacientes foram randomizados e todos receberam profilaxia conforme o grupo designado. A profilaxia iniciou-se após a cirurgia e continuou até 14 dias. A incidência24 de trombose venosa profunda4 foi significativamente menor com Clexane, comparada com heparina (Cowell et al, 1995).
Profilaxia de tromboembolismo11 em pacientes clínicos com mobilidade reduzida durante doença aguda
Em um estudo multicêntrico, duplo-cego, de grupos paralelos, Clexane 20 mg ou 40 mg SC uma vez ao dia foi comparado com placebo23 na profilaxia de TVP em pacientes clínicos com mobilidade restrita durante uma doença aguda (definida como distância percorrida <10 metros em tempo ≤ 3 dias). Esse estudo incluiu pacientes com insuficiência cardíaca12 (NYHA Classe funcional III ou IV); insuficiência respiratória aguda33 ou insuficiência respiratória crônica34 complicada (sem necessidade de suporte ventilatório): infecção35 aguda (exceto choque36 séptico) ou doença reumatológica aguda. Um total de 1.102 pacientes foi incluído no estudo, e 1.073 pacientes receberam profilaxia. A terapia foi continuada por até 14 dias (média de duração de 7 dias). Quando administrado numa dose de 40 mg SC 1x/dia, Clexane reduziu significativamente a incidência24 de TVP comparado ao placebo23. Dados de eficácia são mostrados abaixo [ver tabela 7] (Samama et al, 1999).
Tabela 8 - Eficácia do Clexane em pacientes clínicos com mobilidade reduzida durante doença aguda
|
Indicação |
Regime |
||
|
Clexane |
Clexane |
Placebo23 |
|
|
n (%) |
n (%) |
n (%) |
|
|
Todos os pacientes clínicos que receberam profilaxia durante doença aguda |
351 (100) |
360 (100) |
362 (100) |
|
Falha terapêutica1 TEV Total2 (%) |
43 (12,3) |
16 (4,4) |
43 (11,9) |
|
TVP Total (%) |
43 (12,3) |
16 (4,4) |
41 (11,3) |
|
TVP proximal25 (%) |
13 (3,7) |
5 (1,4) |
14 (3,9) |
1 Falha terapêutica37 durante os dias 1 e 14.
2 TEV = Eventos tromboembólicos, os quais incluem TVP, EP e óbito38 considerado de origem embólica.
3 IC = Intervalo de Confiança
O tratamento profilático com Clexane 40 mg SC ao dia reduziu em 63% o risco de TEV. Em aproximadamente 3 meses após a inclusão, a incidência24 de tromboembolismo11 permaneceu significativamente mais baixa no grupo que recebeu Clexane 40 mg versus o grupo placebo23.
Tratamento de trombose venosa profunda4 (TVP) com ou sem embolia27 pulmonar (EP)
Em um estudo multicêntrico, de grupos paralelos, 900 pacientes com TVP aguda de membro inferior associada ou não à embolia27 pulmonar foram randomizados para tratamento hospitalar com Clexane 1,5 mg/kg SC 1x/dia, Clexane 1 mg/kg SC cada 12h ou heparina em bolus39 (5000 UI) seguido de infusão contínua (administrada até atingir um TTPa de 55 a 85 segundos). Todos os pacientes receberam tratamento. Todos os pacientes também receberam varfarina sódica (dose ajustada de acordo com o TP para atingir um RNI (relação normatizada internacional) entre 2 e 3), a partir de 72h do início da terapia com Clexane ou HNF. Clexane ou HNF foram administrados por no mínimo 5 dias e até que o RNI desejado fosse atingido. Ambos os regimes de Clexane foram equivalentes à terapia com HNF em reduzir o risco de TEV recorrente. Os dados de eficácia são mostrados abaixo [ver tabela 8] (Merli et al, 2001).
Tabela 9 - Eficácia de Clexane no tratamento da trombose venosa profunda4 com ou sem embolia27 pulmonar
|
Indicação |
Regime1 |
||
|
Clexane |
Clexane |
Heparina |
|
|
n (%) |
n (%) |
n (%) |
|
|
Todos os pacientes com TVP tratados (com ou sem EP) |
298 (100) |
312 (100) |
290 (100) |
|
TEV Total2 (%) |
13 (4,4)3 |
9 (2,9)3 |
12 (4,1) |
|
Somente TVP (%) |
11 (3,7) |
7 (2,2) |
8 (2,8) |
|
TVP Proximal25 (%) |
9 (3,0) |
6 (1,9) |
7 (2,4) |
|
EP (%) |
2 (0,7) |
2 (0,6) |
4 (1,4) |
1 Todos os pacientes também foram tratados com varfarina sódica a partir de 72h do início do tratamento com Clexane ou heparina padrão.
2 TEV = evento tromboembólico (trombose venosa profunda4 [TVP] e/ou embolia27 pulmonar [EP]).
Os intervalos de confiança de 95% para a diferença de tratamento no TEV total foram: Clexane 1x/dia versus heparina (-3,0 to 3,5) Clexane cada 12h versus heparina (-4,2 to 1,7).
Hemodiálise16
Em um estudo, pacientes com insuficiência renal40 terminal (n=36) fazendo hemodiálise16 3 vezes por semana, receberam Clexane ou HNF e depois foram trocados para o outro tratamento, a cada 12 semanas. Enoxaparina 1 mg/kg foi administrada na forma de bolus39 dentro da linha arterial antes da diálise41. Doses subsequentes de enoxaparina eram reduzidas para 0,2 mg/kg caso ocorresse sangramento. HNF 50 UI/kg foi administrada na forma de bolus39 dentro da linha arterial, seguida por uma dose de manutenção de 1000 UI/hora. As linhas e filtros de diálise41 ficaram significativamente mais limpas (sem coágulos) com Clexane em comparação com HNF (p<0,001) (Saltissi et al, 1999).
Tratamento de angina6 instável e infarto do miocárdio7 (IM) sem elevação do segmento ST (Cohen et al, 1997) Em um grande estudo multicêntrico, 3.171 pacientes incluídos na fase aguda de angina6 instável ou IM sem elevação do segmento ST foram randomizados para receber, em associação com ácido acetilsalicílico (100 a 325 mg, uma vez ao dia), 1 mg/kg de enoxaparina sódica em injeção subcutânea42 a cada 12 horas, ou HNF por administração IV, ajustada com base no tempo de tromboplastina43 parcial ativada (TTPa). Os pacientes foram tratados em ambiente hospitalar por um período mínimo de 2 e máximo de 8 dias, até estabilização clínica, procedimentos de revascularização ou alta hospitalar. Os pacientes foram acompanhados por 30 dias. A enoxaparina sódica, em comparação à HNF, diminuiu significativamente a incidência24 de angina6 recorrente, IM e óbito38, com redução do risco relativo de 16,2% no 14º dia, sustentado durante o período de 30 dias. Além disto, um número menor de pacientes do grupo tratado com enoxaparina sódica foi submetido à revascularização por angioplastia44 coronariana transluminal percutânea (ACTP) ou por enxerto45 de ponte arterial coronariana (15,8% de redução do risco relativo no 30º dia).
Tratamento do IM com elevação do segmento ST
(Antman et al, 2006)
Em um grande estudo multicêntrico, 20.479 pacientes diagnosticados com IM com elevação do segmento ST, elegíveis para receber terapia fibrinolítica, foram randomizados para receber: 1) enoxaparina sódica em bolus39 IV único de 30 mg acompanhado de 1 mg/kg por via SC, seguido de doses SC de 1 mg/kg a cada 12 horas; ou, 2) HNF por administração IV, ajustada com base no tempo de TTPa por 48 horas. Todos os pacientes também foram tratados com ácido acetilsalicílico por um período mínimo de 30 dias. A estratégia posológica de enoxaparina foi ajustada para pacientes28 acometidos por insuficiência renal40 severa e para pacientes28 idosos com idade maior ou igual a 75 anos. As injeções SC de enoxaparina foram administradas por um período máximo de 8 dias ou até que o paciente recebesse alta do hospital (considerando o que ocorresse primeiro).
Em um subgrupo deste mesmo estudo, 4.716 pacientes foram submetidos à intervenção coronariana percutânea (ICP) recebendo suporte antitrombótico com fármaco46 do estudo de modo cego. Portanto, para pacientes28 que utilizaram a enoxaparina, a ICP foi realizada com enoxaparina (sem troca) utilizando-se o regime estabelecido em estudos prévios, ou seja, caso a última dose SC tenha sido administrada há menos de 8 horas antes de o balão ser inflado, não se administra dose adicional e caso a última dose subcutânea47 tenha sido administrada há mais de 8 horas antes de o balão ser inflado, administra-se uma dose adicional de 0,3 mg/kg através de bolus39 intravenoso.
A enoxaparina sódica quando comparada com a HNF reduziu significativamente a incidência24 do desfecho primário, uma combinação de morte por qualquer causa ou reinfarto do miocárdio10 nos primeiros 30 dias após a randomização [9,9% no grupo tratado com enoxaparina, comparado a 12,0% no grupo tratado com heparina não fracionada] com uma redução relativa do risco igual a 17% (P<0,001).
Os benefícios do tratamento com enoxaparina, evidenciados por uma série de resultados de eficácia, surgiram em 48 horas, tempo no qual houve uma redução de 35% do risco relativo de reinfarto do miocárdio10, quando comparado com o tratamento com HNF (P<0,001).
O efeito benéfico da enoxaparina no desfecho primário foi consistente entre os subgrupos principais do estudo, incluindo idade, sexo, local do infarto8, histórico de diabetes48, histórico de infarto do miocárdio7 anterior, tipo do fibrinolítico administrado e tempo para tratamento com o fármaco46 em estudo.
Houve um benefício significativo do tratamento com enoxaparina, quando comparado com o tratamento com HNF, em pacientes submetidos à ICP dentro de 30 dias após a randomização (23% de redução do risco relativo) ou em pacientes tratados com terapia medicamentosa (15% de redução do risco relativo, P = 0,27 para interação).
A incidência24 do desfecho composto de morte, reinfarto do miocárdio10 ou hemorragia49 intracraniana (uma medida do benefício clínico líquido), considerando-se os 30 primeiros dias, foi significativamente menor (p<0,0001) no grupo tratado com enoxaparina (10,1%) quando comparado com o grupo tratado com HNF (12,2%), representando uma redução de 17% do risco relativo em favor do tratamento com Clexane.
O efeito benéfico da enoxaparina no desfecho primário, observado durante os primeiros 30 dias, foi mantido por um período de acompanhamento de 12 meses.
REFERÊNCIAS BIBLIOGRÁFICAS
- Antman EM et al. for the ExTRACT-TIMI 25 Investigators. Enoxaparin versus UFH with Fibrinolysis for STElevation Myocardial Infarction. N Engl J Med 2006;354:1477-88.
- Bergqvist D et al. Low-molecular-weight heparin (enoxaparin) as prophylaxis against venous thromboembolism after total hip replacement. N Engl J Med. 1996;335(10):696-700.
- Bergqvist et al. for the ENOXACAN Study Group. Efficacy and safety of enoxaparin versus unfractionated heparin for prevention of deep vein thrombosis in elective cancer20 surgery: A double-blind randomized multicentre trial with venographic assessment. Br J Surg. 1997;84:1099-1103.
- Bergqvist D et al; ENOXACAN II Investigators. Duration of prophylaxis against venous thromboembolism with enoxaparin after surgery for cancer20. N Engl J Med. 2002 Mar 28;346(13):975-80.
- Cohen M el al. A comparison of low-molecular-weight heparin with UFH for unstable coronary artery disease. N Engl J Med. 1997;337:447-452.
- Colwell CW et al for the Enoxaparin Clinical Trial Group. Efficacy and safety of enoxaparin versus unfractionated heparin for prevention of deep venous thrombosis after elective knee arthroplasty. Clin Orthop. 1995; 321:19-27.
- Leclerc JR et al. Prevention of deep vein thrombosis after major knee surgery. A randomized, double-blind trial comparing a low molecular weight heparin fragment (enoxaparin) to placebo23. Thromb Haemost. 1992; 67:417- 423.
- MacLeod RS et al. Subcutaneous heparin versus low-molecular-weight heparin as thromboprophylaxis in patients undergoing colorectal surgery: results of the Canadian Colorectal DVT Prophylaxis Trial: a randomized, double-blind trial. Ann Surg 2001; 233: 438-444.
- Merli G et al. Subcutaneous enoxaparin once or twice daily compared with intravenous UFH for treatment of venous thromboembolic disease. Ann Intern Med 2001;134,191-202.
- Planès A et al. Prevention of postoperative venous thrombosis: A randomized trial comparing unfractionated heparin with low molecular weight heparin in patients undergoing total hip replacement. Thromb Haemost. 1988; 60:407-410.
- Planes A et al. Risk of deep-venous thrombosis after hospital discharge in patients having undergone total hip replacement: double-blind randomised comparison of enoxaparin versus placebo23. Lancet. 1996; 348:224-8.
- Saltissi D, Morgan C, Westhuyzen J, et al: Comparison of low-molecular-weight heparin (enoxaparin sodium) and standard unfractionated heparin for haemodialysis anticoagulation. Nephrol Dial Transplant 1999; 14:2698-2703.
- Samama MM et al. Comparison of enoxaparin with placebo23 for the prevention of venous thromboembolism in acutely ill medical patients. N Engl J Med 1999; 341: 793-800.
- Spiro T et al. Efficacy and Safety of Enoxaparin to Prevent Deep Venous Thrombosis after Hip Replacement Surgery Ann Intern Med 1994; 121;2; 81-89.
- Clinical Overview “Enoxaparin And History Of Heparin-Induced Thrombocytopenia” M. Berthon, PharmD (09- Feb-2017 / GPE-CL-2017-00111)
Dados comparativos de Clexane x Heptris®
Foi realizado um estudo randomizado50, multicêntrico, paralelo e aberto para a comprovação da não-inferioridade de Heptris® referente à incidência24 de eventos de sangramento durante o período de tratamento, comparação da segurança de Heptris® versus Clexane e da eficácia dos medicamentos na prevenção de tromboembolismo11 venoso em pacientes cirúrgicos. Foi planejada a avaliação de 300 indivíduos para recebimento de Heptris® 40 mg/0,4 mL ou Clexane 40 mg/0,4 mL na proporção 1:1. Foram analisados 299 indivíduos: Heptris® 40 mg/0,4 mL (n=153) com Clexane 40 mg/0,4 mL (n=146). Os indivíduos foram tratados por 14 dias, com uma injeção51 diária de enoxaparina sódica 40 mg/0,4 mL administrada via subcutânea47. O objetivo primário foi avaliar a incidência24 de pacientes com eventos de sangramento até 24 horas após a descontinuação do tratamento. Os objetivos secundários do estudo estavam relacionados à segurança/eficácia. Para o objetivo primário, em ambas as análises de população ITT e PP, a não-inferioridade de Heptris® em relação ao Clexane foi comprovada. Os resultados de ambas as análises estão em conformidade e confirmam mutuamente a não-inferioridade de Heptris® em relação ao Clexane. Para o objetivo de segurança analisado neste estudo, não foi detectada uma diferença significativa entre a incidência24 deste endpoint particular no grupo de referência de Clexane e Heptris® (enoxaparina sódica 40 mg/mL). Além disso, os resultados obtidos na análise com base na população ITT estão em conformidade com os resultados obtidos na análise com base na população PP e levam à conclusão de que não há diferenças significativas entre Heptris® e Clexane no que diz respeito à incidência24 de qualquer endpoint de segurança. Os desfechos de eficácia foram avaliados não tendo sido detectada nenhuma diferença significativa entre Heptris® e Clexane. Além disso, os resultados obtidos na análise com base na população ITT estão de acordo com os resultados obtidos na análise com base na população PP e levam à conclusão de que não há diferenças significativas entre ambos.
CARACTERÍSTICAS FARMACOLÓGICAS
Propriedades farmacodinâmicas
O princípio ativo de Heptris® é a enoxaparina sódica. Trata-se de uma heparina de baixo peso molecular com peso médio de 4.500 dáltons. A enoxaparina sódica é um sal de sódio. A distribuição do peso molecular é:
< 2000 dáltons ≤ 20%
2000 a 8000 dáltons ≥ 68%
> 8000 dáltons ≤ 18%
A enoxaparina sódica é obtida pela despolimerização alcalina do éster benzil heparina derivado da mucosa intestinal52 suína. Sua estrutura é caracterizada por um grupo ácido 2-O-sulfo-4-enepiranosurônico no final não redutor da cadeia e um 2-N, 6-O-dissulfo-D-glicosamina no final redutor da cadeia. Aproximadamente 20% (variando entre 15% e 25%) da estrutura da enoxaparina contêm um derivado 1,6 anidro no final redutor da cadeia polissacarídica.
Em um sistema purificado in vitro, a enoxaparina sódica apresenta alta atividade anti-Xa (aproximadamente 100 UI/mg) e baixa atividade anti-IIa ou antitrombina (aproximadamente 28 UI/mg). Estas atividades anticoagulantes53 são mediadas por antitrombina III (ATIII) resultando em atividade antitrombótica em humanos.
Além da sua atividade anti-Xa/IIa, as propriedades antitrombótica e anti-inflamatória da enoxaparina foram identificadas em indivíduos saudáveis e em pacientes, bem como em modelos não clínicos.
Estes incluem inibição ATIII-dependente de outros fatores de coagulação54, como fator VIIa, indução da liberação do inibidor da Via do Fator Tecidual endógeno, assim como uma liberação reduzida de fator de von Willebrand do endotélio vascular55 para a circulação15 sanguínea. Estes fatores são conhecidos por contribuir para o efeito antitrombótico global da enoxaparina.
Propriedades farmacocinéticas
Características gerais: Os parâmetros farmacocinéticos da enoxaparina sódica foram estudados principalmente com relação ao tempo da atividade plasmática anti-Xa e também com relação à atividade anti-IIa, nos intervalos de dose recomendados após administrações subcutâneas únicas e repetidas e após administração intravenosa única.
A determinação quantitativa das atividades farmacocinéticas anti-Xa e anti-IIa foi realizada por métodos amidolíticos validados com substratos específicos e com a enoxaparina padrão calibrada contra o padrão internacional para heparinas de baixo peso molecular (NIBSC).
Biodisponibilidade e Absorção: A biodisponibilidade absoluta da enoxaparina sódica após administração subcutânea47, baseada na atividade anti-Xa, é próxima de 100%. Os volumes de injeção51 e concentração de doses no intervalo de 100–200 mg/mL não afetam os parâmetros farmacocinéticos em voluntários saudáveis.
A máxima atividade anti-Xa plasmática média é observada 3 a 5 horas após administração subcutânea47 alcançando, aproximadamente, 0,2; 0,4; 1,0 e 1,3 anti-Xa UI/mL após administração subcutânea47 de doses únicas de 20 mg, 40 mg, 1 mg/Kg e 1,5 mg/Kg, respectivamente.
Um bolus39 intravenoso de 30 mg seguido imediatamente por uma dose subcutânea47 de 1 mg/kg a cada 12 horas forneceu um pico inicial de níveis de fator anti-Xa igual a 1,16 UI/mL (n = 16) e uma exposição média correspondente a 88% dos níveis do estado de equilíbrio. O estado de equilíbrio é alcançado no segundo dia de tratamento.
A farmacocinética da enoxaparina parece ser linear nos intervalos de dose recomendados. A variabilidade intra e interpacientes é baixa. Após repetidas administrações subcutâneas não ocorre acumulação. Após repetidas administrações subcutâneas de 40 mg, uma vez ao dia, e de 1,5 mg/kg uma vez ao dia, em voluntários saudáveis, o estado de equilíbrio é alcançado no 2° dia, com uma taxa de exposição média aproximadamente 15% maior do que após a administração de dose única. O nível de atividade da enoxaparina no estado de equilíbrio é bem previsível pela farmacocinética de dose única. Após administrações subcutâneas repetidas de 1 mg/kg, num regime de 2 vezes ao dia, o estado de equilíbrio é alcançado entre o 3° e o 4° dia, com uma exposição média aproximadamente 65% maior do que após administração de dose única, e as concentrações máxima e mínima médias de aproximadamente 1,2 e 0,52 UI/mL, respectivamente. Baseada na farmacocinética da enoxaparina sódica, esta diferença no estado de equilíbrio é esperada e está dentro do intervalo terapêutico.
A atividade plasmática anti-IIa após a administração subcutânea47 é aproximadamente 10 vezes menor do que a atividade anti-Xa. A máxima atividade anti-IIa média é observada aproximadamente 3–4 horas após administração subcutânea47 e alcança 0,13 UI/mL e 0,19 UI/mL após administração repetida de 1 mg/kg, duas vezes ao dia e de 1,5 mg/kg, uma vez ao dia, respectivamente.
Dados comparativos PK/PD de Clexane e Heptris®
Foi realizado um estudo randomizado50, aberto, dose única, PK/PD comparativo cross-over de 2 vias (n=20) entre os medicamentos Heptris® 40 mg/0,4 mL versus Clexane 40 mg/0,4 mL após administração subcutânea47 em indivíduos saudáveis. O objetivo do estudo foi avaliar as propriedades PK / PD e investigar a bioequivalência de Heptris® com Clexane, bem como comparar a segurança e tolerabilidade dessas formulações. Nenhum indivíduo experimentou qualquer evento adverso e nenhum evento adverso sério (SAE) foi observado.
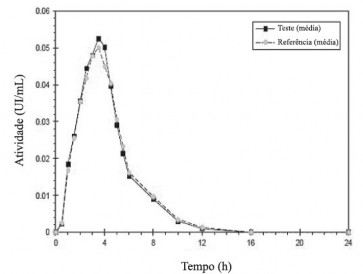
Perfil farmacocinético Anti-Xa:

Perfil farmacocinético Anti-IIa:
|
Parâmetro |
N |
Média Geométrica dos Mínimos Quadrados |
Taxa T/R (%) |
Limite de Confiança (%) |
||
|
Heptris® (T) |
Clexane (R) |
Inferior |
Superior |
|||
|
anti-Xa |
||||||
|
AUC56(0-t) (UI-h/mL) |
20 |
3.922 |
3.709 |
105.72 |
98.57 |
113.40 |
|
Amax (UI/mL) |
20 |
0.524 |
0.500 |
104.79 |
100.36 |
109.42 |
|
anti-IIa |
||||||
|
AUC56(0-t) (UI-h/mL) |
20 |
0.2144 |
0.2070 |
103.58 |
92.52 |
115.95 |
|
Amax (UI/mL) |
20 |
0.0563 |
0.0550 |
102.24 |
97.73 |
106.96 |
De acordo com o protocolo do estudo, os parâmetros AUC56 (0-t) e Amax para a atividade anti-Xa e anti-IIa foram usados para avaliar a bioequivalência. Os resultados confirmam que o intervalo de confiança 90% para as taxas T/R das razões das médias dos mínimos quadrados geométricos dos parâmetros avaliados estavam dentro da bioequivalência faixa de aceitação de 80,00 a 125,00%. A bioequivalência entre Heptris® e Clexane foi confirmada neste estudo.
Distribuição: O volume de distribuição da atividade anti-Xa da enoxaparina sódica é de aproximadamente 5 L e é próximo do volume sanguíneo.
Metabolismo57: A enoxaparina é metabolizada principalmente no fígado58 por dessulfatação e/ou despolimerização formando moléculas de peso menor, que apresentam potência biológica muito reduzida.
Eliminação: A enoxaparina sódica é um fármaco46 de baixa depuração, com média de clearance plasmático anti-Xa de 0,74 L/h após infusão intravenosa de 1,5 mg/kg em 6 horas.
A eliminação parece ser monofásica, com meia-vida de aproximadamente 5 4 horas após uma dose subcutânea47 única, e até aproximadamente 7 horas após doses repetidas.
O clearance renal59 dos fragmentos60 ativos representa aproximadamente 10% da dose administrada e a excreção renal59 total dos fragmentos60 ativos e não-ativos é de 40% da dose.
Características em populações especiais
Idosos: com base nos resultados da análise farmacocinética populacional, o perfil cinético de enoxaparina sódica não é diferente em voluntários idosos comparados a voluntários jovens quando a função renal59 é normal. Entretanto, como é conhecido que a função renal59 diminui com o aumento da idade, pacientes idosos podem apresentar retardo na eliminação de enoxaparina sódica (vide item “5. Advertências e Precauções - Populações Especiais”, “8. Posologia e modo de usar - Populações Especiais” e o item a seguir “Insuficiência renal”).
Insuficiência renal40: observou-se uma relação linear entre o clearance plasmático de anti-Xa e o clearance de creatinina61 no estado de equilíbrio, o que indica um decréscimo do clearance de enoxaparina sódica em pacientes com função renal59 reduzida. A exposição anti-Xa representada pela AUC56 (área sob a curva), no estado de equilíbrio, é levemente aumentada na insuficiência renal40 leve (clearance de creatinina61 50–80 mL/min) e moderada (clearance de creatinina61 30–50 mL/min) após repetidas doses subcutâneas de 40 mg, uma vez ao dia. Em pacientes com insuficiência renal40 severa (clearance de creatinina61 < 30 mL/min), a AUC56 no estado de equilíbrio é significativamente aumentada em média em 65% após repetidas doses únicas diárias subcutâneas de 40 mg (vide itens “5. Advertências e Precauções - Populações especiais” e “8. Posologia e modo de usar - Populações especiais”).
Peso: após repetidas doses subcutâneas de 1,5 mg/kg, uma vez ao dia, a AUC56 média de atividade anti-Xa é levemente maior no estado de equilíbrio em voluntários saudáveis obesos (IMC62 30–48 Kg/m2) em comparação aos voluntários controle não-obesos, embora a atividade máxima observada não tenha aumentado. Há menor clearance ajustado ao peso em voluntários obesos tratados com doses subcutâneas.
Quando se administram doses não ajustadas ao peso, a exposição da atividade anti-Xa é 52% maior em mulheres de peso baixo (< 45 Kg) e 27% maior em homens de peso baixo (< 57 Kg), após uma dose subcutânea47 única de 40 mg, quando comparada aos voluntários controle com peso normal (vide item “5. Advertências e Precauções - Populações especiais”).
Hemodiálise16: em um único estudo, a taxa de eliminação apresentou-se semelhante, porém a AUC56 foi duas vezes maior que na população controle, após uma dose intravenosa única de 0,25 ou 0,50 mg/kg.
Interações farmacocinéticas
Não foram observadas interações farmacocinéticas entre a enoxaparina e trombolíticos quando administrados concomitantemente.
Dados de Segurança Pré-Clínicos
Não foram realizados estudos de longa duração em animais para avaliar o potencial carcinogênico da enoxaparina.
A enoxaparina não se mostrou mutagênica em testes in vitro, incluindo o teste Ames, o teste de mutação63 de células64 de linfoma65 em camundongos, o teste de aberração cromossômica linfocítica em humanos e os testes in vivo de aberração cromossômica na medula óssea66 de ratos.
Demonstrou-se que a enoxaparina não tem nenhum efeito na fertilidade ou no desempenho reprodutivo de ratos machos e fêmeas em doses subcutâneas de até 20 mg/kg/dia. Estudos teratológicos foram conduzidos em ratas e coelhas prenhes em doses subcutâneas de enoxaparina de até 30 mg/kg/dia. Não houve nenhuma evidência de efeitos teratogênicos67 ou fetotoxicidade devido à enoxaparina.
Além dos efeitos anticoagulantes53 da enoxaparina, não houve evidência de efeitos adversos em doses de 15 mg/kg/dia em 13 semanas de estudos de toxicidade68 subcutânea47, ambos em ratos e cães e em doses de 10 mg/kg/dia em 26 semanas de estudos de toxicidade68 subcutânea47 e intravenosa ambos em ratos e macacos.
CONTRAINDICAÇÕES
- Hipersensibilidade à enoxaparina sódica, à heparina e seus derivados, inclusive outras heparinas de baixo peso molecular;
- História de trombocitopenia69 induzida pela heparina mediada por imunidade70 (TIH) nos últimos 100 dias ou na presença de anticorpos71 circulantes;
- Hemorragias72 ativas de grande porte e condições com alto risco de desenvolvimento de hemorragia49, incluindo acidente vascular cerebral73 hemorrágico74 recente, úlcera75 gastrointestinal, presença de neoplasia76 maligna com alto risco de sangramento cerebral recente, cirurgia espinhal ou oftálmica, varizes77 esofágicas conhecidas ou suspeitas, malformações78 arteriovenosas, aneurismas vasculares79 ou anomalias vasculares79 intra-espinhais ou intracerebrais importantes;
- Anestesia80 raquidiana ou epidural81 ou anestesia80 loco-regional quando a enoxaparina sódica é usada para tratamento nas 24 horas anteriores.
ADVERTÊNCIAS E PRECAUÇÕES
Não administrar Heptris® por via intramuscular.
Hemorragia49
Assim como com outros anticoagulantes53, pode ocorrer sangramento em qualquer local (vide item “9. Reações Adversas”). Se ocorrer sangramento, a origem da hemorragia49 deve ser investigada e tratamento apropriado deve ser instituído.
Heptris®, assim como qualquer outra terapia anticoagulante82, deve ser utilizado com cautela em condições com alto risco de hemorragia49, tais como:
- alterações na hemostasia32;
- histórico de úlcera péptica83;
- acidente vascular cerebral73 isquêmico84 recente;
- hipertensão arterial85 severa não controlada;
- retinopatia diabética86;
- neurocirurgia ou cirurgia oftálmica recente;
- uso concomitante de medicamentos que afetem a hemostasia32 (vide item “6. Interações Medicamentosas”).
Monitoramento da contagem plaquetária
O risco de trombocitopenia69 induzida por heparina (reação mediada por anticorpos71) também existe com heparinas de baixo peso molecular. Pode ocorrer trombocitopenia69, geralmente entre o 5º e 21º dia após o início do tratamento com Heptris®. Portanto, recomenda-se a realização de contagem plaquetária antes do início e regularmente durante o tratamento. Na prática, em caso de confirmação de diminuição significativa da contagem plaquetária (30 a 50% do valor inicial), o tratamento com Heptris® deve ser imediatamente interrompido e substituído por outra terapia.
Advertências Gerais
As diferentes classes de heparinas de baixo peso molecular (HBPM), por exemplo, enoxaparina, dalteparina, bemiparina e nadroparina não devem ser intercambiáveis (unidade por unidade), pois existem diferenças entre elas quanto ao processo de fabricação, peso molecular, atividade anti-Xa específica, unidade e dosagem. Isto ocasiona diferenças em suas atividades farmacocinéticas e biológicas associadas (por exemplo, a atividade antitrombina e a interação plaquetária). Portanto, é necessário obedecer às instruções de uso de cada medicamento.
Anestesia80 espinhal/peridural87
Foram relatados casos de hematoma88 intraespinhal com o uso concomitante de Heptris® e anestesia80 espinhal/peridural87, resultando em paralisia89 prolongada ou permanente. Estes eventos são raros com a administração de doses iguais ou inferiores a 40 mg/dia de Heptris®. O risco destes eventos pode ser aumentado com administração de doses maiores de Heptris®, uso de cateter epidural81 no pós-operatório ou em caso de administração concomitante de medicamentos que alteram a hemostasia32, tais como anti-inflamatórios não esteroidais (vide item “6. Interações Medicamentosas”). O risco parece também ser aumentado por traumatismo90 ou punções espinhais repetidas ou em pacientes com histórico de cirurgia ou deformidade espinhal.
Para reduzir o risco potencial de sangramento associado ao uso concomitante de Heptris® e anestesia80/analgesia peridural87 ou espinhal, deve-se considerar o perfil farmacocinético do fármaco46 (vide item “3. Características Farmacológicas - Propriedades Farmacocinéticas”). A introdução e remoção do cateter devem ser realizadas quando o efeito anticoagulante82 de Heptris® estiver baixo, no entanto, o momento exato para chegar a um efeito anticoagulante82 suficientemente baixo em cada paciente não é conhecido.
A introdução ou remoção do cateter deve ser postergada por pelo menos 12 horas após a administração de doses baixas de Heptris® (20 mg uma vez ao dia, 30 mg uma ou duas vezes ao dia, ou 40 mg uma vez ao dia) e, pelo menos, 24 horas após a administração de doses mais elevadas de Heptris® (0,75 mg/kg, duas vezes ao dia, 1 mg/kg duas vezes ao dia, ou 1,5 mg/kg uma vez ao dia). Níveis de anti-Xa ainda são detectáveis neste momento, e estes atrasos não são uma garantia de que um hematoma88 neuroaxial (espinhal) será evitado. Pacientes recebendo a dose de 0,75 mg/kg duas vezes ao dia, ou a dose de 1 mg/kg duas vezes ao dia não devem receber a segunda dose de enoxaparina no regime de duas vezes ao dia para permitir um atraso maior antes da colocação ou remoção do cateter. Da mesma forma, apesar de uma recomendação específica para o intervalo da dose subsequente de enoxaparina após a remoção do cateter não poder ser feita, considerar adiar esta dose seguinte por pelo menos quatro horas, com base numa avaliação do risco- benefício considerando tanto o risco de trombose91 como o risco de sangramento no contexto do procedimento e fatores de risco do paciente. Para pacientes28 com clearance de creatinina61 < 30 mL/minuto, são necessárias considerações adicionais porque a eliminação de enoxaparina é mais prolongada; considerar a duplicação do tempo de remoção de um cateter, pelo menos, 24 horas para a menor dose prescrita de enoxaparina (30 mg uma vez ao dia) e, pelo menos, 48 horas para a dose mais elevada (1 mg/kg/dia).
Caso o médico decida administrar anticoagulantes53 durante o uso de anestesia80 peridural87/espinhal ou punção lombar, deve-se empregar o monitoramento frequente para detectar qualquer sinal31 ou sintoma92 de lesão93 neurológica, tais como, dor na linha média da região dorsal, deficiências sensoriais e motoras (entorpecimento ou fraqueza dos membros inferiores), alterações intestinais e/ou urinárias. Os pacientes devem ser instruídos a informar imediatamente a seu médico caso apresentem qualquer sintoma92 ou sinal31 descrito acima. Em caso de suspeita de sinais29 ou sintomas30 de hematoma88 intraespinhal, devem ser efetuados o diagnóstico94 e tratamento, incluindo descompressão95 da medula espinhal96, com urgência97.
Trombocitopenia69 induzida pela heparina
A utilização de enoxaparina sódica em pacientes com história de HIT mediada por imunidade70 nos últimos 100 dias ou na presença de anticorpos71 circulantes está contraindicada. Os anticorpos71 circulantes podem persistir vários anos.
A enoxaparina sódica deve ser usada com extrema cautela em pacientes com história (mais de 100 dias) de trombocitopenia69 induzida por heparina sem anticorpos71 circulantes. A decisão de utilizar enoxaparina sódica neste caso, deve ser feita apenas após uma cuidadosa avaliação do risco benefício e após terem sido considerados tratamentos alternativos sem heparina.
Procedimentos de revascularização coronariana percutânea
Para minimizar o risco de sangramento após a instrumentação vascular98 durante o tratamento da angina6 instável, infarto do miocárdio7 sem elevação do segmento ST e infarto8 agudo9 do miocárdio10 com elevação do segmento ST, devem-se respeitar precisamente os intervalos entre as doses recomendadas de Heptris®. É importante estabelecer a hemostasia32 no local da punção após a intervenção coronariana percutânea. Caso tenha sido utilizado um dispositivo de fechamento, a bainha de acesso vascular98 pode ser removida imediatamente. Caso tenha sido utilizado um método de compressão manual, a bainha deve ser removida 6 horas após a última administração intravenosa ou subcutânea47 de Heptris®. Se o tratamento com Heptris® continuar, a próxima dose programada não deve ser administrada antes de 6 a 8 horas após a remoção da bainha. Deve-se ter atenção especial ao local do procedimento para detecção de sinais29 de sangramento ou formação de hematoma88.
Gravidez99 e Lactação100
Estudos em animais não demonstraram qualquer evidência de fetotoxicidade ou teratogenicidade. Em ratas prenhes, a passagem de 35 S-enoxaparina sódica através da placenta para o feto101 é mínima.
Em humanos, não existe evidência da passagem da enoxaparina sódica através da placenta durante o segundo trimestre da gravidez99. Ainda não existem informações disponíveis a este respeito durante o primeiro e terceiro trimestres da gravidez99.
Como não foram realizados estudos adequados e bem controlados em gestantes, e uma vez que os estudos realizados em animais nem sempre são bons indicativos da resposta humana, deve-se utilizar Heptris® durante a gravidez99 somente se o médico considerar como estritamente necessário.
Categoria de risco na gravidez99: B. Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Em ratas lactantes102, a concentração de 35 S-enoxaparina sódica ou de seus metabólitos103 marcados no leite é muito baixa. Não se sabe se a enoxaparina sódica inalterada é excretada no leite humano. A absorção oral da enoxaparina sódica é improvável, porém, como precaução, não se deve amamentar durante o tratamento com Heptris®.
Gestantes com próteses mecânicas valvulares cardíacas: Não foram realizados estudos adequados para avaliar a utilização de Heptris® na tromboprofilaxia em gestantes com próteses mecânicas valvulares cardíacas. Em um estudo clínico em gestantes com próteses mecânicas valvulares cardíacas, administrou-se enoxaparina (1 mg/kg duas vezes ao dia) para redução do risco de tromboembolismo11, 2 de 8 gestantes desenvolveram coágulos resultando em bloqueio da válvula, levando a óbitos materno e fetal. Houve relatos isolados pós-comercialização de trombose91 da valva em gestantes com próteses mecânicas valvulares cardíacas enquanto eram medicadas com enoxaparina para tromboprofilaxia. Gestantes com próteses mecânicas valvulares cardíacas podem apresentar maior risco de tromboembolismo11 (vide item “5. Advertências e Precauções - Próteses mecânicas valvulares cardíacas”).
Populações especiais
Pacientes idosos: não foi observado aumento na tendência de hemorragia49 em idosos com doses profiláticas.
Porém, pacientes idosos (especialmente pacientes com idade igual ou maior a 80 anos) podem ter um aumento no risco de complicações hemorrágicas104 com doses terapêuticas. Portanto, aconselha-se um monitoramento clínico cuidadoso (vide itens “3. Características Farmacológicas - Propriedades Farmacocinéticas” e 8. Posologia e modo de usar”).
Pacientes idosos podem apresentar retardo na eliminação da enoxaparina sódica. (vide item “8. Posologia e modo de usar”).
Crianças: a segurança e eficácia de Heptris® em crianças ainda não foram estabelecidas.
Próteses mecânicas valvulares cardíacas: o uso de Heptris® não foi adequadamente estudado para casos de tromboprofilaxia em pacientes com próteses mecânicas valvulares cardíacas. Foram relatados casos isolados de trombose91 com próteses valvulares cardíacas em pacientes com próteses mecânicas valvulares cardíacas que receberam enoxaparina para tromboprofilaxia. A avaliação destes casos é limitada devido aos fatores causais serem confusos, incluindo doenças anteriores e dados clínicos insuficientes. Alguns destes casos ocorreram em gestantes nas quais a trombose91 resultou em óbitos materno e fetal. Gestantes com próteses mecânicas valvulares cardíacas podem apresentar maior risco para tromboembolismo11 (vide item “5. Advertências e Precauções - Gestantes com próteses mecânicas valvulares cardíacas”).
Insuficiência renal40: em pacientes com insuficiência renal40, existe aumento da exposição ao Heptris®, aumentando também o risco de hemorragia49. Como a exposição ao Heptris® aumenta significativamente em pacientes com insuficiência renal40 severa (clearance de creatinina61 < 30 mL/min), o ajuste posológico é recomendado para dosagens terapêuticas e profiláticas. Embora não seja recomendado ajuste posológico em pacientes com insuficiência renal40 moderada (clearance de creatinina61 30-50 mL/min) e leve (clearance de creatinina61 50-80 mL/min), é aconselhável realizar um monitoramento clínico cuidadoso (vide itens “3. Características Farmacológicas- Propriedades Farmacocinéticas” e “8. Posologia e modo de usar”).
Peso baixo: um aumento na exposição ao Heptris® em doses profiláticas (não ajustadas ao peso) tem sido observado em mulheres e homens com baixo peso (< 45 kg e < 57 kg, respectivamente), que pode resultar em maior risco de hemorragia49. Portanto, é aconselhável realizar um monitoramento clínico cuidadoso nestes pacientes (vide item “3. Características Farmacológicas- Propriedades Farmacocinéticas”).
Pacientes obesos: pacientes obesos apresentam risco aumentado de tromboembolismo11. A segurança e a eficácia de doses profiláticas em pacientes obesos (IMC62 > 30 kg/m2) não foram totalmente determinadas e não há consenso para ajuste de dose. Estes pacientes devem ser observados cuidadosamente quanto aos sinais29 e sintomas30 de tromboembolismo11.
Efeitos na habilidade de dirigir e operar máquinas
A utilização de Heptris® não afeta a habilidade de dirigir ou operar máquinas.
INTERAÇÕES MEDICAMENTOSAS
Medicamento-medicamento
Recomenda-se a interrupção do uso de medicamentos que afetam a hemostasia32 antes do início do tratamento com Heptris®, a menos que seu uso seja estritamente indicado. Tais medicamentos incluem:
- salicilatos sistêmicos105, ácido acetilsalicílico e outros anti-inflamatórios não-esteroidais (AINEs), incluindo o cetorolaco;
- dextrana 40, ticlopidina e clopidogrel;
- glicocorticoides sistêmicos105;
- agentes trombolíticos e anticoagulantes53;
- outros agentes antiplaquetários, incluindo os antagonistas de glicoproteína IIb/IIIa;
Em caso de indicação do uso de qualquer uma destas associações, deve-se utilizar Heptris® sob cuidadoso monitoramento clínico e laboratorial, quando apropriado.
Medicamento-exame laboratorial
Nas doses utilizadas na profilaxia do tromboembolismo11 venoso, Heptris® não influencia significativamente o tempo de sangramento e os testes de coagulação54 sanguínea global, nem afeta a agregação plaquetária ou a ligação do fibrinogênio106 às plaquetas107.
Pode ocorrer aumento do tempo de tromboplastina43 parcial ativada (TTPa) e do tempo de coagulação54 ativada (TCA) com a administração de doses mais altas. Aumentos no TTPa e TCA não estão linearmente correlacionados ao aumento da atividade antitrombótica de Heptris®, sendo, portanto, inadequados e inseguros para monitoramento da atividade de Heptris®.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Heptris® deve ser mantida em temperatura ambiente (15–30°C).
Prazo de validade: 24 meses a partir da data de fabricação. Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Características físicas e organolépticas: Solução transparente, incolor ou amarela clara.
Após abertas, as seringas de enoxaparina sódica devem ser utilizadas imediatamente. Se houver solução remanescente após o uso, esta deverá ser descartada.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR MODO DE USAR
A via de administração de Heptris® varia dependendo da indicação do produto. Abaixo estão descritas as técnicas de injeção subcutânea42 e bolus39 intravenoso.
A injeção subcutânea42 aplicada corretamente é essencial para reduzir a dor e ferimento no local da injeção51.
Para evitar ferimentos acidentais com a agulha após a injeção51, as apresentações de seringas preenchidas com dispositivo de segurança são providas de um dispositivo de segurança automático.
Preparo do local para injeção51: O local recomendado para injeção51 é na gordura108 da parte inferior do abdômen, pelo menos 5 centímetros de distância do umbigo109 para fora e em ambos os lados.
Antes da injeção51, lavar as mãos110. Limpar (não esfregar) com álcool o local selecionado para injeção51. Selecionar um local diferente do abdômen inferior a cada aplicação.
Preparo da seringa2 antes da injeção51: Verifique se a seringa2 não está danificada e se o medicamento dentro está como uma solução límpida, sem partículas. Se a seringa2 estiver danificada ou o medicamento não for límpido, utilizar outra seringa2.
Técnica de injeção subcutânea42 de seringas preenchidas sem sistema de segurança
- Retirar cuidadosamente a capa protetora da agulha.
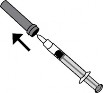
- Não pressionar o êmbolo111 antes de injetar para expelir bolhas de ar. Isso pode levar à perda da medicação. Depois de remover a tampa, não permitir que a agulha toque em nada de modo a garantir que a agulha permaneça estéril.
- As seringas com doses de 20 mg e 40 mg estão prontas para uso. Para as seringas com doses de 60 mg, 80 mg e 100 mg, ajustar a dose a ser injetada, se necessário. A quantidade do medicamento a ser injetada deve ser ajustada dependendo do peso corpóreo do paciente; consequentemente qualquer excesso do medicamento deve ser expelido antes da injeção51. Segure a seringa2 apontando para baixo (para manter a bolha112 de ar na seringa2) e expelindo o excesso do medicamento em um recipiente adequado.
- A injeção51 deve ser administrada por injeção subcutânea42 profunda, no tecido subcutâneo113 da parede abdominal114, com o paciente deitado ou sentado em posição confortável, alternando entre os lados esquerdo e direito a cada aplicação.
- A agulha deve ser introduzida perpendicularmente na espessura de uma prega cutânea115 feita entre os dedos polegar e indicador (verticalmente em um ângulo de 90º). Insira toda a extensão da agulha na dobra da pele116.
Pressionar o êmbolo111 para aplicar a injeção51. A prega deve ser mantida durante todo o período da injeção51.
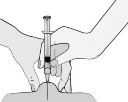
- Remover a agulha.
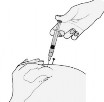
- Não esfregar o local da injeção51 após a administração.
Técnica de injeção subcutânea42 de seringas preenchidas com sistema de segurança:
Para as doses de 20 mg e 40 mg:
- Retire a capa protetora da agulha.

Uma gota117 pode aparecer na ponta da agulha. Caso isto ocorra, remova-a antes de injetar o medicamento através de batidas suaves no corpo da seringa2 com a agulha apontada para baixo. Não expelir qualquer bolha112 de ar da seringa2 antes de administrar a injeção51.
Para as doses de 60 mg, 80 mg e 100 mg:
- Retire a capa protetora da agulha.

- Ajuste a dose a ser injetada (se necessário):
A quantidade do medicamento a ser injetada deve ser ajustada dependendo do peso corpóreo do paciente; consequentemente qualquer excesso do medicamento deve ser expelido antes da injeção51. Segure a seringa2 apontando para baixo (para manter a bolha112 de ar na seringa2) e expelindo o excesso do medicamento em um recipiente adequado.
Nota: Caso o excesso de medicamento não seja expelido antes da aplicação, o dispositivo de segurança não será ativado ao final da injeção51.
Quando não houver a necessidade de ajuste da dose, a seringa2 preenchida está pronta para o uso. Não expelir qualquer bolha112 de ar da seringa2 antes de administrar a injeção51.
Uma gota117 pode aparecer na ponta da agulha. Se isso ocorrer, remova a gota117 antes da administração através de batidas no corpo da seringa2 com a agulha apontada para baixo.
Administração da injeção51:
- A seringa2 preenchida (20 mg/0,2 mL e 40 mg/0,4 mL) já está pronta para uso. Para evitar a perda da medicação, não pressione o êmbolo111 para expelir qualquer bolha112 de ar antes de administrar a injeção51.
- A injeção51 deve ser administrada por injeção subcutânea42 profunda, no tecido subcutâneo113 da parede abdominal114, com o paciente deitado ou sentado em posição confortável, alternando entre os lados esquerdo e direito a cada aplicação.
- A agulha deve ser introduzida perpendicularmente na espessura de uma prega cutânea115 feita entre os dedos polegar e indicador. A prega deve ser mantida durante todo o período da injeção51. Não esfregue o local da injeção51 após a administração.
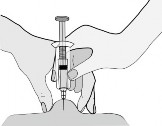
- O dispositivo de segurança é automaticamente ativado, quando o êmbolo111 é pressionado até o final, deste modo protegendo completamente a agulha usada e sem causar desconforto ao paciente. A ativação do dispositivo de segurança só é possível se o êmbolo111 for completamente abaixado.
Nota: o dispositivo de segurança somente poderá ser ativado com a seringa2 completamente vazia.
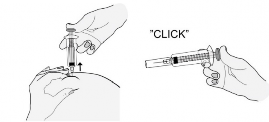
Técnica de injeção51 intravenosa (bolus39)
Apenas para a indicação de tratamento de infarto8 agudo9 do miocárdio10 com elevação do segmento ST
Heptris® deve ser administrado através de uma linha intravenosa e não deve ser misturado ou coadministrado com outros medicamentos. Para evitar a possibilidade de mistura de Heptris® com outros medicamentos, o acesso intravenoso escolhido deve ser lavado com quantidade suficiente de solução salina ou solução dextrose118 antes e imediatamente após a administração do bolus39 intravenoso de Heptris® para limpar o dispositivo de acesso do medicamento. Heptris® pode ser utilizado com segurança com solução salina normal 0,9% ou dextrose118 a 5% em água.
Bolus39 intravenoso inicial de 30 mg: utiliza-se uma seringa2 preenchida graduada de Heptris® e despreza- se o excesso do volume, obtendo apenas 30 mg (0,3 mL) na seringa2. Injeta-se, então, a dose de 30 mg diretamente na linha intravenosa.
Bolus39 adicional para pacientes28 submetidos à intervenção coronariana percutânea quando a última dose subcutânea47 de Heptris® foi administrada há mais de 8 horas antes de o balão ser inflado: para pacientes28 submetidos à intervenção coronariana percutânea, um bolus39 intravenoso adicional de 0,3 mg/kg deve ser administrado se a última dose subcutânea47 de Heptris® foi administrada há mais de 8 horas antes de o balão ser inflado (vide item “8. Posologia e modo de usar - Tratamento do infarto8 agudo9 do miocárdio10 com elevação do segmento ST”).
Para assegurar a precisão do pequeno volume a ser injetado, recomenda-se a diluição do medicamento para uma solução de 3 mg/mL.
Para obter uma solução a 3 mg/mL utilizando uma seringa2 preenchida de 60 mg de Heptris®, recomenda- se usar uma bolsa de infusão de 50 mL (contendo, por exemplo, solução salina normal 0,9% ou dextrose118 a 5% em água). Com o auxílio de uma seringa2, retira-se 30 mL da solução contida na bolsa e desprezasse este volume. Aos 20 mL restantes na bolsa de infusão, injeta-se o conteúdo total de uma seringa2 preenchida graduada de 60 mg. Mistura- se gentilmente a solução final. Retira-se com uma seringa2 o volume requerido da solução para administração na linha intravenosa. Recomenda-se que esta solução seja preparada imediatamente antes de sua utilização.
Após finalizada a diluição, o volume a ser injetado na linha intravenosa deve ser calculado utilizando-se a seguinte fórmula: [volume da solução diluída (mL) = peso do paciente (kg) x 0,1] ou utilizando a tabela abaixo.
|
Volume de solução a 3 mg/mL a ser injetado na linha intravenosa |
||
|
Peso do paciente (kg) |
Dose Requerida (0,3 mg/Kg) |
Volume a ser injetado (mL) após ser diluído para a concentração final de 3 mg/mL |
|
45 |
13,5 |
4,5 |
|
50 |
15 |
5 |
|
55 |
16,5 |
5,5 |
|
60 |
18 |
6 |
|
65 |
19,5 |
6,5 |
|
70 |
21 |
7 |
|
75 |
22,5 |
7,5 |
|
80 |
24 |
8 |
|
85 |
25,5 |
8,5 |
|
90 |
27 |
9 |
|
95 |
28,5 |
9,5 |
|
100 |
30 |
10 |
POSOLOGIA
A posologia de Heptris® é determinada pela predisposição individual de ocorrer o tromboembolismo11 venoso em situações desencadeantes como cirurgia, imobilização prolongada e trauma, entre outras. Dessa maneira, são considerados com risco moderado os indivíduos que apresentem os seguintes fatores predisponentes: idade superior a 40 anos, obesidade119, varizes77 dos membros inferiores, neoplasia76, doença pulmonar ou cardíaca crônica, estrogenioterapia, puerpério120, infecções13 sistêmicas, entre outros. São considerados com alto risco os indivíduos com histórico de tromboembolismo11 venoso prévio, neoplasia76 abdominal ou pélvica22, cirurgia ortopédica de grande porte dos membros inferiores, entre outros.
1. Profilaxia do tromboembolismo11 venoso em pacientes cirúrgicos
A duração e a dose do tratamento com Heptris® baseiam-se no risco do paciente. O risco de o paciente sofrer o evento tromboembólico pode ser estimado através de modelos de estratificação de risco validados.
Em pacientes que apresentam risco moderado de tromboembolismo11, a dose recomendada de Heptris® é de 20 mg ou 40 mg uma vez ao dia por via subcutânea47. Na cirurgia geral, a primeira injeção51 deve ser administrada 2 horas antes da intervenção cirúrgica.
O tratamento com Heptris® é geralmente prescrito por um período médio de 7 a 10 dias. Um tratamento mais prolongado pode ser apropriado em alguns pacientes e deve ser continuado enquanto houver risco de tromboembolismo11 venoso e até que o paciente seja ambulatorial.
Em pacientes com alto risco de tromboembolismo11, a dose recomendada de Heptris® administrada por via subcutânea47 é de 40 mg uma vez ao dia, iniciada 12 horas antes da cirurgia, ou de 30 mg, duas vezes ao dia, iniciada 12 a 24 horas após a cirurgia.
- Para os pacientes que se submetem à cirurgia ortopédica de grande porte com um risco elevado de tromboembolismo11 venoso, uma tromboprofilaxia de até 5 semanas é recomendada.
- Para pacientes28 submetidos à cirurgia oncológica com risco elevado de tromboembolismo11 venoso, recomenda-se uma tromboprofilaxia de até 4 semanas.
Para recomendações especiais sobre o intervalo entre as dosagens para anestesia80 espinhal/peridural87 e procedimentos de revascularização coronária percutânea: vide item “5. Advertências e Precauções”.
2. Profilaxia do tromboembolismo11 venoso em pacientes clínicos
A dose recomendada para pacientes28 clínicos é de 40 mg de Heptris®, uma vez ao dia, administrada por via subcutânea47. A duração do tratamento deve ser de no mínimo, 6 dias, devendo ser continuado até que o paciente recupere a capacidade plena de se locomover, por um período máximo de 14 dias.
3. Tratamento da trombose venosa profunda4 com ou sem embolismo5 pulmonar
A posologia de Heptris® recomendada para o tratamento da trombose venosa profunda4 é de 1,5 mg/kg, uma vez ao dia ou 1 mg/kg, duas vezes ao dia, administrado por via subcutânea47. Em pacientes com distúrbios tromboembólicos complicados, recomenda-se a administração da dose de 1 mg/kg, duas vezes ao dia.
O tratamento com Heptris® é geralmente prescrito por um período médio de 10 dias. A terapia anticoagulante82 oral deve ser iniciada quando apropriada e o tratamento com Heptris® deve ser mantido até que o efeito terapêutico do anticoagulante82 tenha sido atingido (International Normalisation Ratio 2 a 3).
4. Prevenção da formação de trombo14 no circuito de circulação15 extracorpórea durante a hemodiálise16
A dose recomendada é de 1 mg/kg de Heptris®.
Em pacientes com alto risco hemorrágico74, a dose deve ser reduzida para 0,5 mg/kg quando o acesso vascular98 for duplo ou 0,75 mg/kg quando o acesso vascular98 for simples.
Durante a hemodiálise16, Heptris® deve ser introduzido na linha arterial do circuito, no início da sessão de hemodiálise16. O efeito desta dose geralmente é suficiente para uma sessão com duração de 4 horas; entretanto, caso haja o aparecimento de anéis de fibrina121, por exemplo, após uma sessão mais longa que o normal, pode ser administrada dose complementar de 0,5 a 1,0 mg/kg de Heptris®.
5. Tratamento de angina6 instável e infarto do miocárdio7 sem elevação do segmento ST
A dose de Heptris® recomendada é de 1 mg/kg a cada 12 horas, por via subcutânea47, administrada concomitantemente com ácido acetilsalicílico oral (100 a 325 mg, uma vez ao dia).
Nestes pacientes, o tratamento com Heptris® deve ser prescrito por no mínimo 2 dias e mantido até estabilização clínica. A duração normal do tratamento é de 2 a 8 dias.
6. Tratamento do infarto8 agudo9 do miocárdio10 com elevação do segmento ST
A dose recomendada de Heptris® é de um bolus39 intravenoso único de 30 mg acompanhado de uma dose de 1 mg/kg por via subcutânea47, seguido por 1 mg/kg por via subcutânea47 a cada 12 horas (as duas primeiras doses subcutâneas devem ser de no máximo 100 mg cada dose e as demais doses 1 mg/kg por via subcutânea47). Para pacientes28 com 75 anos de idade ou mais, verifique instruções específicas descritas abaixo em “Populações Especiais – Idosos”.
Quando administrado em conjunto com um trombolítico (específico para fibrina121 ou não), Heptris® deve ser administrado entre 15 minutos antes e 30 minutos depois do início da terapia fibrinolítica. Todos os pacientes devem receber ácido acetilsalicílico tão logo seja diagnosticado o infarto8 agudo9 do miocárdio10 com elevação do segmento ST. Esta medicação deve ser mantida com dosagem de 75 a 325 mg uma vez ao dia, a menos que haja contraindicação para o seu uso.
A duração recomendada do tratamento com Heptris® é de 8 dias ou até que o paciente receba alta do hospital, considerando-se o que ocorrer primeiro.
Para pacientes28 submetidos à intervenção coronariana percutânea: se a última dose subcutânea47 de Heptris® foi administrada há menos de 8 horas antes de o balão ser inflado, não é necessária dose adicional deste medicamento. Entretanto, caso a última dose subcutânea47 tenha sido administrada há mais de 8 horas antes de o balão ser inflado, uma dose adicional de 0,3 mg/kg de Heptris® deve ser administrada através de bolus39 intravenoso.
Risco de uso por via de administração não recomendada
Não há estudos dos efeitos de Heptris® administrado por vias não recomendadas. Portanto, por segurança e para garantir a eficácia deste medicamento, a administração deve ser somente por via intravenosa ou subcutânea47 (dependendo da indicação terapêutica37).
Populações Especiais
Idosos: para o tratamento do infarto8 agudo9 do miocárdio10 com elevação do segmento ST em pacientes idosos (com idade igual ou maior a 75 anos), não deve ser administrado o bolus39 intravenoso inicial. A dose inicial é de 0,75 mg/kg por via subcutânea47 a cada 12 horas (as duas primeiras doses subcutâneas devem ser de no máximo 75 mg cada dose e as demais 0,75 mg/kg por via subcutânea47).
Para as demais indicações do produto, não é necessário realizar ajuste posológico em idosos, a menos que a função renal59 esteja prejudicada (vide itens “3. Características Farmacológicas - Propriedades farmacocinéticas”, “5. Advertências e Precauções” e “8. Posologia e modo de usar - Insuficiência122 renal”).
Insuficiência renal40: (vide itens “3. Características Farmacológicas - Propriedades farmacocinéticas” e “5. Advertências e Precauções”)
- Insuficiência renal40 severa: é necessário realizar ajuste posológico em pacientes com insuficiência renal40 severa (clearance de creatinina61 < 30 mL/min), de acordo com as tabelas a seguir, uma vez que a exposição ao Heptris® é significativamente aumentada nesta população de pacientes.
Para uso terapêutico os seguintes ajustes posológicos são recomendados:
|
Dose padrão |
Insuficiência renal40 severa |
|
1 mg/kg por via subcutânea47, duas vezes ao dia |
1 mg/kg por via subcutânea47, uma vez ao dia |
|
1,5 mg/kg por via subcutânea47, uma vez ao dia |
1 mg/kg por via subcutânea47, uma vez ao dia |
|
Tratamento do infarto8 agudo9 do miocárdio10 com elevação do segmento ST em pacientes com idade inferior a 75 anos |
|
|
30 mg em bolus39 intravenoso único acompanhado de uma dose de 1 mg/kg por via subcutânea47, seguido de 1 mg/kg por via subcutânea47 duas vezes ao dia (as duas primeiras doses subcutâneas devem ser de no máximo 100 mg cada) |
30 mg em bolus39 intravenoso único acompanhado de uma dose de 1 mg/kg por via subcutânea47, seguido de 1 mg/kg por via subcutânea47 uma vez ao dia (a primeira dose subcutânea47 deve ser de no máximo 100 mg) |
|
Tratamento do infarto8 agudo9 do miocárdio10 com elevação do segmento ST em pacientes idosos com idade maior ou igual a 75 anos |
|
| 0,75 mg/kg por via subcutânea47 duas vezes ao dia SEM bolus39 intravenoso inicial (as duas primeiras doses subcutâneas devem ser de no máximo 75 mg cada) | 1 mg/kg por via subcutânea47 uma vez ao dia SEM bolus39 intravenoso inicial (a primeira dose subcutânea47 deve ser de no máximo 100 mg) |
Para uso profilático, os seguintes ajustes posológicos são recomendados:
|
Dose padrão |
Insuficiência renal40 severa |
|
40 mg por via subcutânea47, uma vez ao dia |
20 mg por via subcutânea47, uma vez ao dia |
|
20 mg por via subcutânea47, uma vez ao dia |
20 mg por via subcutânea47, uma vez ao dia |
Estes ajustes posológicos não se aplicam à indicação em hemodiálise16.
Insuficiência renal40 leve e moderada: embora não seja recomendado realizar ajuste posológico em pacientes com insuficiência renal40 moderada (clearance de creatinina61 30-50 mL/min) e leve (clearance de creatinina61 50-80 mL/min), é aconselhável que se faça um monitoramento clínico cuidadoso.
Insuficiência hepática123: em decorrência da ausência de estudos clínicos, recomenda-se cautela em pacientes com insuficiência hepática123.
Anestesia80 espinhal/peridural87: para pacientes28 que recebendo anestesia80 espinhal/peridural87 vide item “5. Advertências e Precauções - Anestesia80 espinhal/peridural”.
REAÇÕES ADVERSAS
A enoxaparina foi avaliada em mais de 15.000 pacientes que receberam o medicamento em estudos clínicos. Estes estudos incluíram 1.776 pacientes para profilaxia de trombose venosa profunda4 seguida de cirurgia ortopédica ou abdominal em pacientes com risco de complicações tromboembólicas, 1.169 para profilaxia de TVP em pacientes intensamente doentes com mobilidade severamente restrita, 559 para tratamento de TVP com ou sem embolismo5 pulmonar, 1.578 para tratamento de angina6 instável e infarto do miocárdio7 sem elevação do segmento ST e 10.176 para tratamento de infarto8 agudo9 do miocárdio10 com elevação do segmento ST.
O regime de enoxaparina sódica administrada durante estes estudos clínicos varia dependendo da indicação. A dose de enoxaparina sódica foi de 40 mg por via subcutânea47 uma vez ao dia para profilaxia de TVP seguida de cirurgia ou em pacientes intensamente doentes com mobilidade severamente restrita. No tratamento da TVP com ou sem embolismo5 pulmonar, pacientes recebendo enoxaparina foram tratados também com uma dose de 1 mg/kg por via subcutânea47 a cada 12 horas ou uma dose de 1,5 mg/kg por via subcutânea47 uma vez ao dia. Nos estudos clínicos para o tratamento de angina6 instável e infarto do miocárdio7 sem elevação do segmento ST, as doses foram de 1 mg/kg por via subcutânea47 a cada 12 horas e no estudo clinico para tratamento de infarto8 agudo9 do miocárdio10 com elevação do segmento ST, o regime de enoxaparina sódica foi de 30 mg por via intravenosa em bolus39 seguida de 1 mg/kg por via subcutânea47 a cada 12 horas.
As frequências estão definidas como: muito comum (≥ 1/10); comum (≥ 1/100 a < 1/10); incomum (≥ 1/1.000 a < 1/100); rara (≥ 1/10.000 a < 1/1.000), muito rara (< 1/10.000) ou desconhecido (que não pode ser estimada a partir dos dados disponíveis). As reações adversas observadas após comercialização são classificadas como de “frequência desconhecida”.
Hemorragias72
Em estudos clínicos, hemorragias72 foram as reações mais comumente relatadas. Estas incluem hemorragias72 de grande porte, reportadas no máximo em 4,2% dos pacientes (pacientes cirúrgicos**). Alguns destes casos foram fatais.
Assim como com outros anticoagulantes53, pode ocorrer hemorragia49 na presença de fatores de risco associados, tais como: lesões124 orgânicas suscetíveis a sangramento, procedimentos invasivos ou uso concomitante de medicamentos que afetam a hemostasia32 (vide itens “5. Advertências e Precauções - Populações especiais” e “6. Interações Medicamentosas”).
Distúrbios vasculares79
Profilaxia em pacientes cirúrgicos:
- Muito comum: hemorragia49*
- Rara: hemorragia49 retroperitoneal125
Profilaxia em pacientes sob tratamento médico:
- Comum: hemorragia49*
Tratamento em pacientes com trombose venosa profunda4 com ou sem embolismo5 pulmonar:
- Muito comum: hemorragia49*
- Incomum: hemorragia49 intracraniana, hemorragia49 retroperitoneal125
Tratamento em pacientes com angina6 instável e infarto do miocárdio7 sem elevação do segmento ST:
- Comum: hemorragia49*
- Rara: hemorragia49 retroperitoneal125
Tratamento em pacientes com infarto8 agudo9 do miocárdio10 com elevação do segmento ST:
- Comum: hemorragia49*
- Incomum: hemorragia49 intracraniana, hemorragia49 retroperitoneal125
*como hematoma88, outras equimoses126 além do local da injeção51, ferimento com hematoma88, hematúria127, epistaxe128 e hemorragia49 gastrintestinal.
** em pacientes cirúrgicos as complicações hemorrágicas104 foram consideradas de grande porte: (1) se a hemorragia49 causou um evento clínico significativo, ou (2) se acompanhado por uma diminuição da hemoglobina129 ≥ 2 g/dL ou transfusão130 de 2 ou mais unidades de produto sanguíneo. As hemorragias72 retroperitoneal125 e intracraniana foram sempre consideradas de grande porte.
Trombocitopenia69 e trombocitose131
Distúrbios do sangue132 e sistema linfático133
Profilaxia em pacientes cirúrgicos
- Muito comum: trombocitose131 (aumento de plaquetas107 > 400.000/ mm3)
- Comum: trombocitopenia69
Profilaxia em pacientes sob tratamento médico
- Incomum: trombocitopenia69
Tratamento em pacientes com trombose venosa profunda4 com ou sem embolismo5 pulmonar
- Muito comum: trombocitose131
- Comum: trombocitopenia69
Tratamento em pacientes com angina6 instável e infarto do miocárdio7 sem elevação do segmento ST
- Incomum: trombocitopenia69
Tratamento em pacientes com infarto8 agudo9 do miocárdio10 com elevação do segmento ST
- Comum: trombocitose131, trombocitopenia69
- Muito rara: trombocitopenia69 imunoalérgica
Outras reações adversas clinicamente relevantes
Estas reações estão apresentadas abaixo, qualquer que sejam as indicações, por sistema órgão classe, frequência e ordem decrescente de gravidade.
Distúrbios do sistema imune134:
- Comum: reação alérgica135
- Rara: reação anafilática136/anafilactoide137 (ver também experiência pós-comercialização)
Distúrbios hepatobiliares138
- Muito comum: aumento das enzimas hepáticas139 (principalmente transaminases com níveis > 3 vezes o limite superior da normalidade)
Doenças da pele116 e do tecido subcutâneo113
- Comum: urticária140, prurido141, eritema142
- Incomum: dermatite143 bolhosa
Distúrbios gerais no local de administração
- Comum: hematoma88, dor e outras reações no local da injeção51 (como edema144, hemorragia49, hipersensibilidade, inflamação145, tumoração, dor ou reação não especificada)
- Incomum: irritação local, necrose146 da pele116 no local da injeção51
Investigação:
- Rara: Hipercalemia147
Experiência pós-comercialização
As reações adversas a seguir foram identificadas durante o período após a aprovação do uso do medicamento comparador Clexane. As reações adversas são derivadas de relatos espontâneos e, portanto, a frequência é desconhecida (não pode ser estimada a partir dos dados).
Distúrbios do sistema imunológico148
Reação anafilática136/anafilactóide incluindo choque36
- Distúrbios do sistema nervoso149
- Dor de cabeça150
Distúrbios vasculares79
Foram relatados casos de hematoma88 espinhal (ou hematoma88 neuroaxial) com o uso concomitante de enoxaparina sódica e anestesia80 espinhal/peridural87 ou punção espinhal. Estas reações resultaram em graus variados de lesão93 neurológica, incluindo paralisia89 por tempo prolongado ou permanente (vide item “5. Advertências e Precauções).
Distúrbios do sangue132 e linfáticos:
- Anemia151 hemorrágica152
- Casos de trombocitopenia69 imunoalérgica com trombose91:em alguns casos, a trombose91 foi complicada por infarto8 orgânico ou isquemia153 de extremidade (vide item “5. Advertências e Precauções”).
- Eosinofilia154
Distúrbios da pele116 e tecidos subcutâneos:
- Vasculite155 cutânea115, necrose146 cutânea115 geralmente ocorrendo no local da administração (estes fenômenos são geralmente precedidos por púrpura156 ou placas157 eritematosas158, infiltradas e dolorosas), devendo-se interromper o tratamento com Heptris®.
- Nódulos no local de injeção51 (nódulos inflamatórios que não são inclusões císticas de enoxaparina) que desaparecem após alguns dias e não devem ser motivo para interrupção do tratamento.
- Alopecia159
Distúrbios hepatobiliares138:
- Lesão93 hepatocelular
- Lesão93 colestática
Distúrbios musculoesqueléticos e de tecido conjuntivo160
- Osteoporose161 em terapia prolongada (acima de 3 meses)
Em caso de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Sintomas30 e severidade: a superdose acidental após administração intravenosa, extracorporal ou subcutânea47 de Heptris® pode causar complicações hemorrágicas104. A absorção de Heptris® após a administração oral, mesmo em altas doses, é improvável.
Tratamento e antídoto162: os efeitos anticoagulantes53 podem ser em grande parte, neutralizados pela administração intravenosa lenta de protamina. A dose de protamina depende da dose de Heptris® administrada, ou seja, 1 mg de protamina neutraliza o efeito anticoagulante82 de 1 mg de Heptris®, se Heptris® foi administrado nas primeiras 8 horas. Uma infusão de 0,5 mg de protamina para 1 mg de Heptris® pode ser administrado se Heptris® foi administrado há mais de 8 horas antes da administração da protamina, ou se tiver sido determinado que uma segunda dose de protamina seja necessária. Após 12 horas da injeção51 de Heptris®, a administração da protamina pode não ser necessária. Entretanto, mesmo com doses elevadas de protamina, a atividade anti-Xa de Heptris® nunca é completamente neutralizada (máximo de aproximadamente 60%).
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.8830.0076
Farm. Resp.: Dra. Marcia Yoshie Hacimoto - CRF-RJ: 13.349
Fabricado por:
Shenzhen Techdow Pharmaceutical Co., Ltd
No. 19, Gaoxinzhongyi Road, Nanshan District, Shenzhen Guangdong Province
República Popular da China
Importado por:
Mylan Laboratórios Ltda.
Estrada Dr. Lourival Martins Beda, 1118.
Donana - Campos dos Goytacazes - RJ - CEP: 28110-000
CNPJ: 11.643.096/0001-22
SAC: 0800 020 0817