

Syletyv (Bula do profissional de saúde)
ACCORD FARMACÊUTICA LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Syletyv
paricalcitol
Injetável 5 mcg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Embalagens contendo 5 ampolas de 1 mL ou 2 mL cada
USO INTRAVENOSO
USO ADULTO
COMPOSIÇÃO:
Cada mL de Syletyv contém:
| paricalcitol | 5,00 mcg |
| veículo q.s.p. | 1 mL |
Veículo: propilenoglicol, álcool etílico, água para injetáveis.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE1
INDICAÇÕES
Syletyv é destinado ao tratamento e prevenção do hiperparatireoidismo secundário, associado à insuficiência renal2 crônica.
RESULTADOS DE EFICÁCIA
Estudos em pacientes com insuficiência renal2 crônica (IRC) estágio 5 mostraram que paricalcitol suprime o paratormônio (PTHi) sem diferenças significativas na incidência3 de hipercalcemia ou hiperfosfatemia quando comparado com o placebo4. No entanto, os níveis séricos de fósforo, cálcio e o produto Ca x P podem aumentar quando paricalcitol é administrado.
Em três estudos placebo4-controlado1, Fase III, de 12 semanas, em pacientes com insuficiência renal2 crônica em diálise5, paricalcitol foi introduzido a 0,04 mcg/kg, três vezes por semana. A dose foi aumentada em 0,04 mcg/kg, a cada duas semanas até que os níveis de PTHi diminuíssem pelo menos 30% sobre o valor basal, ou até que o quinto aumento levasse a uma dose de 0,24 mcg/kg, ou que o PTHi caísse para menos que 100 pg/mL, ou ainda, o produto Ca x P fosse maior que 75, num período de duas semanas, ou o cálcio sérico ultrapasse 11,5 mg/dL6, em qualquer momento.
Os pacientes tratados com paricalcitol alcançaram uma redução média de PTHi de 30% em seis semanas. Nesses estudos, não houve diferença significativa na incidência3 de hipercalcemia ou de hiperfosfatemia entre pacientes tratados com paricalcitol e placebo4. Os resultados destes estudos estão resumidos abaixo (Tabela 1):
Tabela 1 - Resultado dos estudos1
|
|
Grupo (Número de Pacientes) |
Valor Basal Médio (faixa) |
Média (EP) de alteração do valor basal ao resultado final |
|
PTHi (pg/mL) |
Paricalcitol (n=40) Placebo4 (n=38) |
783 (291 - 2076) 745 (320 - 1671) |
-379 (43,7) -69,6 (44,8) |
|
Fosfatase alcalina7 (U/L) |
Paricalcitol (n=31) Placebo4 (n=34) |
150 (40 - 600) 169 (56 - 911) |
-41,5 (10,6) +2,6 (10,1) |
|
Cálcio (mg/dL6) |
Paricalcitol (n=40) Placebo4 (n=38) |
9,3 (7,2 - 10,4) 9,1 (7,8 - 10,7) |
+0,47 (0,1) +0,02 (0,1) |
|
Fósforo (mg/dL6) |
Paricalcitol (n=40) Placebo4 (n=38) |
5,8 (3,7 - 10,2) 6,0 (2,8 - 8,8) |
+0,47 (0,3) -0,47 (0,3) |
|
Produto Cálcio X Fósforo |
Paricalcitol (n=40) Placebo4 (n=38) |
54 (32 - 106) 54 (26 - 77) |
+7,9 (2,2) -3,9 (2,3) |
Em um estudo de 12 semanas2, Fase IV, duplo-cego, randomizado8, multicêntrico, paricalcitol foi administrado em uma dose inicial de 0,04 mcg/kg ou de PTHi basal/80, três vezes por semana, para pacientes9 com insuficiência renal2 crônica (IRC estágio 5) em diálise5. A dose foi aumentada em 2 mcg a cada 2 semanas até que os níveis de PTHi fossem reduzidos em 30% a 60% em relação aos níveis basais ou que o PTHi reduzisse para valores inferiores a 100 pg/dL, ou o produto Ca x P aumentasse para acima de 75 por duas mensurações consecutivas, ou o cálcio sérico se elevasse para níveis superiores a 11,5 mg/dL6 em qualquer momento. Os pacientes completariam o estudo se atingissem redução do PTH ≥ 30% em relação aos níveis basais em quatro mensurações consecutivas, ou se apresentassem um único episódio de hipercalcemia, ou completassem 12 semanas de tratamento. Não foram observados episódios de hipercalcemia em ambos os grupos de tratamento. Ambos os métodos de determinação da dose se mostraram seguros e efetivos. Os resultados estão apresentados abaixo (Tabela 2):
Tabela 2 - Resultados do estudo2:
|
Parâmetro |
PTH/80 |
0,04 mcg/kg |
|
Incidência3 de hipercalcemia |
0 |
0 |
|
Mediana de Dias para a Primeira de 4 Reduções do PTHi ≥ 30% |
31a |
45 |
|
Mediana do Número de Ajustes de Doseb |
2 |
3 |
|
Incidências de Ca x P > 75 |
5 (7,8%) |
2 (3,3%) |
a Estatisticamente significativo (p= 0,0306)
b Para a primeira redução de 4 ≥ 30% do PTHi.
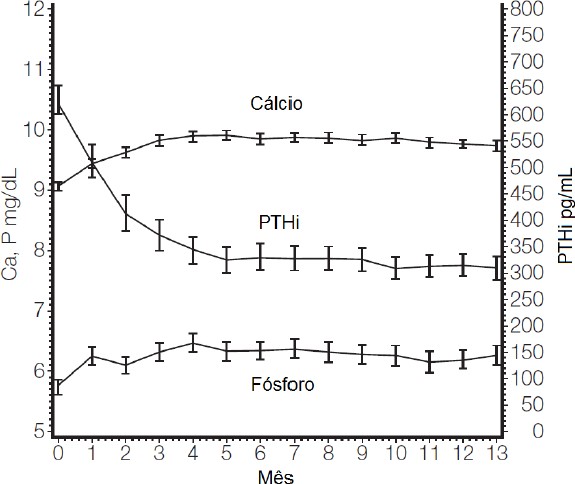
Um estudo de segurança aberto de longo prazo em 164 pacientes com insuficiência renal2 crônica estágio 5 (dose média de 7,5 mcg três vezes por semana) demonstrou que os níveis séricos médios de Ca, P e do produto Ca x P ficaram com faixas clinicamente apropriadas com a redução do PTH (redução média de 319 pg/mL no 13º mês).3
Referências Bibliográficas:
- Martin KJ, González EA, Gellens M, Hamm LL, Abboud H, Lindberg J. 19-Nor-1-α-25- Dihydroxyvitamin D2 (Paricalcitol) Safely and Effectively Reduces the Levels of Intact Parathyroid Hormone in Patients on Hemodialysis. J Am Soc Nephrol. 1998; 9:1427-1432.
- Martin KJ, González E, Lindberg JS, et al. Paricalcitol Dosing According to Body Weight or Severity of Hyperparathyroidism: a Double-Blind, Multicenter, Randomized Study. Am J Kid Dis. 2001 38(5):S57-63.
- Lindberg J, Martin KJ, Gonzáles EA, Acchiardo SR, et al. A long-term, multicenter study of the efficacy of paricalcitol in end-stage renal10 disease. Clin Nephrol.2001;56(4):315-323.
CARACTERÍSTICAS FARMACOLÓGICAS
Descrição
O paricalcitol é um análogo sintético do calcitriol, a forma metabolicamente ativa da vitamina11 D com modificações na cadeia lateral (D2) e A (19-nor) do anel. O paricalcitol é um pó branco e cristalino12 quimicamente denominado como 19-nor-1α,3β,25- trihidróxi-9,10 secoergosta-5(Z),7(E),22(E)-trieno(C27H44O3).
Propriedades Farmacodinâmicas
O hiperparatireoidismo secundário é caracterizado por uma elevação do hormônio13 paratireoidiano (PTH) associada a níveis inadequados de vitamina11 D ativa. A fonte de vitamina11 D no organismo é a síntese pela pele14 como vitamina11 D3 e a dieta com vitamina11 D2 ou D3. Ambas as vitaminas D2 e D3 necessitam de duas hidroxilações sequenciais no fígado15 e nos rins16 para se ligar e ativar o receptor de vitamina11 D (VDR). O ativador endógeno do VDR, calcitriol, é um hormônio13 que se liga aos VDRspresentes na glândula17 paratireoide, intestino, rins16 e ossos para manter o funcionamento da paratireoide e homeostase de cálcio e fósforo e aos VDRs que se encontram em muitos outros tecidos, incluindo próstata18, endotélio19 e células20 imunes. A ativação do VDR é essencial para a formação e manutenção óssea adequadas. Em rins16 deficientes, a ativação da vitamina11 D é diminuída, resultando no aumento de PTH e, consequentemente, levando ao hiperparatireoidismo secundário e a distúrbios na homeostase do cálcio e fósforo. A diminuição nos níveis de calcitriol e o aumento nos níveis de PTH precedem anormalidades de cálcio e fósforo séricos e afetam a taxa de turnover ósseo, o que pode resultar em osteodistrofia21 renal10. Em pacientes com insuficiência renal2 crônica, reduções no PTH estão associadas a um impacto favorável na fosfatase alcalina7 ósseo-específica, turnover ósseo e fibrose22 óssea. Além de reduzir os níveis de PTH e corrigir o turnover ósseo, a terapia com vitamina11 D ativa pode prevenir outras consequências da deficiência de vitamina11 D.
Mecanismo de ação
Estudos pré-clínicos e in vitro demonstraram que as ações biológicas do paricalcitol são mediadas pela ligação com o VDR, que resulta na ativação seletiva da via de resposta da vitamina11 D. Vitamina11 D e paricalcitol demonstraram reduzir os níveis do hormônio13 paratireoidiano através da inibição da síntese e secreção de PTH. Níveis reduzidos de 1,25 (OH)2D3 foram observados nos estágios iniciais da insuficiência renal2 crônica.
O tempo estimado para início da ação terapêutica23 do paricalcitol é dependente dos níveis de PTH basal e resposta individual de cada paciente.
No entanto, em 3 estudos clínicos Fase III, duplo-cego, placebo4-controlado, pacientes tratados com paricalcitol, com dose baseada no peso corporal, atingiram uma redução média de PTHi de 30% em 6 semanas. Adicionalmente, em um estudo Fase IV, duplo-cego, duração de 12 semanas, com dose baseada tanto nos níveis de PTHi basal quanto no peso corporal, o tempo médio para a primeira entre quatro reduções ≥ 30% de PTHi foi de 31 dias para a dose baseada no PTHi e 45 dias para a dose baseadano peso corporal.
Farmacocinética
Duas horas após a administração de doses que variam de 0,04 a 0,24 mcg/kg, as concentrações de paricalcitol diminuíram rapidamente; depois disso, as concentrações de paricalcitol declinaram loglinearmente, com meia-vida média de cerca de 15 horas. Nenhum acúmulo de paricalcitol foi observado após doses múltiplas.
Distribuição: paricalcitol é extensamente ligado a proteínas24 do plasma25 (>99%). Em voluntários sadios, o volume de distribuição no estado de equilíbrio (steady state) é de aproximadamente 23,8 L. Após uma dose de 0,24 mcg/kg de paricalcitol em pacientes com insuficiência renal2 crônica estágio 5 com necessidade de hemodiálise26 e diálise peritoneal27, a média do volume aparente de distribuição é de aproximadamente 31 a 35 L. A farmacocinética de paricalcitol foi investigada em pacientes com insuficiência renal2 crônica (IRC), com necessidade de hemodiálise26. O paricalcitol é administrado como injeção28 in bolus29 intravenosa.
Metabolismo30: muitos metabólitos31 foram detectados na urina32 e fezes. O paricalcitol não foi detectado na urina32. Dados in vitro sugerem que paricalcitol é metabolizado por várias enzimas hepáticas33 e não hepáticas34, incluindo CYP24 mitocondrial, assim como CYP3A4 e UGT1A4. Os metabólitos31 identificados incluem o produto da 24(R)-hidroxilação (presente em baixos níveis no plasma25), assim como 24,26- e 24,28-di-hidroxilação e glicuronidação direta. Paricalcitol não é um inibidor de CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 ou CYP3A em concentrações de até 50 nM (21ng/mL). Notou-se menos de duas induções com CYP2B6, CYP2C9 e CYP3A4 em concentrações semelhantes de paricalcitol.
Eliminação: paricalcitol é eliminado principalmente por excreção hepatobiliar35. Aproximadamente 63% da radioatividade foi eliminada nas fezes e 19% foi recuperada na urina32 em voluntários sadios. Nesses voluntários, a média de eliminação da meia- vida de paricalcitol é cerca de 5 a 7 horas na faixa da dose estudada de 0,04 a 0,16 mcg/kg.
Tabela 3 - Parâmetros Farmacocinéticos em pacientes com insuficiência renal2 crônica (IRC) estágio 5 (dose única de 0,24 mcg/kg in bolus29 intravenosa)
|
|
IRC estágio 5-HD (n=14) |
IRC estágio 5-PD (n=8) |
|
Cmáx (ng/mL) |
1,680 ± 0,511 |
1,832 ± 0,315 |
|
AUC36(0-∞) (ng.h/mL) |
14,51 ± 4,12 |
16,01 ± 5,98 |
|
β (1/h) |
0,050 ± 0,023 |
0,045 ± 0,026 |
|
t1/2 (h)a |
13,9 ± 7,3 |
15,4 ± 10,5 |
|
CL (L/h) |
1,49 ± 0,60 |
1,54 ± 0,95 |
|
Vdβ (L) |
30,8 ± 7,5 |
34,9 ± 9,5 |
HD: hemodiálise26
PD: diálise peritoneal27
a: média harmônica
±: pseudo desvio padrão
Populações especiais
Idosos: a farmacocinética de paricalcitol não foi estudada em pacientes idosos com idade superior a 65 anos.
Crianças: a farmacocinética de paricalcitol não foi estudada em pacientes com idade inferior a 18 anos.
Sexo: a farmacocinética de paricalcitol é independente do sexo.
Interações Medicamentosas
Um estudo in vitro indicou que paricalcitol não é um inibidor da CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 ou CYP3A em concentrações acima de 50 nM (21 ng/mL) (aproximadamente 20 vezes maior do que o obtido após a maior dose testada). Em culturas primárias frescas de hepatócitos, a indução observada em concentrações de paricalcitol maiores que 50 nM foi menor que duas induções para CYP2B6, CYP2C9 ou CYP3A, enquanto os controles positivos resultaram em indução de seis a nove vezes. Portanto, não é esperado que paricalcitol iniba ou induza a eliminação de drogas metabolizadas por estas enzimas. Interações de injeção28 de paricalcitol não foram estudados. O efeito de múltiplas doses de cetoconazol administradas como 200 mg duas vezes ao dia por cinco dias na farmacocinética de paricalcitol cápsulas foi estudada em indivíduos sadios. A Cmáx de paricalcitol foi minimamente afetada, porém a AUC360-∞ aproximadamente dobrou na presença de cetoconazol. A meia-vida média do paricalcitol foi de 17,0 horas na presença de cetoconazol comparado com 9,8 horas quando paricalcitol é administrado isoladamente.
CONTRAINDICAÇÕES
Syletyv não deve ser administrado a pacientes com evidência de toxicidade37 por vitamina11 D, hipercalcemia ou hipersensibilidade a algum componente deste produto.
ADVERTÊNCIAS E PRECAUÇÕES
Superdosagem aguda de paricalcitol pode produzir hipercalcemia e levar à necessidade de cuidados de emergência38. Durante o ajuste de dose, os níveis séricos de cálcio e fósforo devem ser cuidadosamente monitorados (ex., duas vezes por semana). Se hipercalcemia clinicamente significativa se desenvolver, a dose deverá ser reduzida ou interrompida. A administração crônica de paricalcitol pode expor os pacientes ao risco de hipercalcemia, à elevação do produto Ca x P e à calcificação39 metastática.
A hipercalcemia crônica pode levar a calcificação39 vascular40 generalizada e outras calcificações em tecidos moles.
O tratamento de pacientes com hipercalcemia clinicamente significativa consiste em redução imediata da dose ou sua interrupção e inclui uma dieta pobre em cálcio, suspensão de suplementos com cálcio, mobilização do paciente, atenção aos desequilíbrios de fluidos e eletrólitos41, avaliação das anormalidades eletrocardiográficas (crítico em pacientes recebendo digitálicos), e hemodiálise26 ou diálise peritoneal27 com um dialisato sem cálcio, se justificado. Os níveis séricos de cálcio devem ser monitorados até que se estabeleça a normocalcemia. Fosfatos ou compostos relacionados à vitamina11 D não devem ser ingeridos concomitantemente ao Syletyv.
A toxicidade37 por digitálicos é potencializada pela hipercalcemia de qualquer causa; desse modo, cautela deve ser tomada quando compostos digitálicos são prescritos concomitantemente ao Syletyv.
Lesões42 ósseas a dinâmicas podem se desenvolver se os níveis de PTH forem suprimidos em níveis anormais.
Gravidez43 e Lactação44
O paricalcitol demonstrou produzir diminuições mínimas na viabilidade fetal (5%) quando metade da dose humana de 0,24 mcg/kg (baseada na superfície corporal, mcg/m2) foi administrada diariamente em coelhos e quando 2 vezes a dose humana de 0,24 mcg/kg (baseada nos níveis plasmáticos de exposição) foi administrada em ratos. Na maior dose investigada (20 mcg/kg, três vezes por semana em ratos, 13 vezes a dose humana de 0,24 mcg/kg baseada na superfície corporal), houve um aumento significativo na mortalidade45 dos ratos recém-nascidos nas doses que foram maternalmente tóxicas (hipercalcemia). Nenhum outro efeito no desenvolvimento dos filhotes foi observado. O paricalcitol não foi teratogênico46 nas doses investigadas.
Não há estudos adequados e bem controlados em mulheres grávidas. O paricalcitol deve ser administrado durante a gravidez43 apenas se os benefícios justificarem o risco potencial ao feto47.
Categoria de risco: C – Não há estudos adequados em mulheres. Em experiências animais ocorreram alguns efeitos colaterais48 no feto47, mas o benefício do produto pode justificar o risco potencial durante a gravidez43.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Uso na lactação44: estudos em ratos demonstraram que paricalcitol está presente no leite. Não se sabe se o paricalcitol é excretado no leite humano. A decisão de descontinuar a amamentação49 ou descontinuar o medicamento deve ser tomada levando-se em consideração a importância do medicamento para a mãe.
Populações especiais
Uso Pediátrico: a segurança e a eficácia de paricalcitol em pacientes menores de 18 anos não foram estabelecidas. Há pouca experiência de uso do medicamento nesta população.
Uso em idosos: de 40 pacientes recebendo paricalcitol em um estudo Fase III, placebo4-controlado, de insuficiência renal2 crônica, 10 pacientes tinham idade superior a 65 anos. Nesses estudos, não houve grandes diferenças de eficácia e segurança entre pacientes com idade superior a 65 anos e pacientes mais jovens.
Testes laboratoriais
Durante o ajuste de dose e antes que a dose de paricalcitol seja estabelecida, testes laboratoriais devem ser realizados com mais frequência. Uma vez que a dosagem tenha sido estabelecida, cálcio e fósforo séricos devem ser medidos, no mínimo, mensalmente. Recomenda-se que a medição de PTH sérico ou plasmático seja realizada a cada três meses.
Insuficiência hepática50: a disposição do paricalcitol (0,24 mcg/kg) foi comparada em pacientes com insuficiência hepática50 leve (n=5) e moderada (n=5) (avaliados segundo critérios de Child-Pugh) e voluntários com função hepática51 normal (n=10). A farmacocinética de paricalcitol não ligado foi similar nos grupos avaliados neste estudo. Não é necessário ajuste de dose em pacientes com insuficiência hepática50 leve a moderada. A influência da insuficiência hepática50 grave na farmacocinética do paricalcitol não foi avaliada.
Insuficiência renal2: a farmacocinética de paricalcitol foi estudada em pacientes com insuficiência renal2 crônica (IRC) estágio 5 que necessitavam de hemodiálise26 e/ou diálise peritoneal27. O procedimento de hemodiálise26 não interfere na eliminação de paricalcitol. No entanto, em comparação a voluntários sadios, pacientes com IRC demonstraram uma diminuição na depuração e aumento na meia-vida.
Carcinogênese: em um estudo de carcinogênese de 104 semanas em camundongos CD-1, foi observado um aumento na incidência3 de leiomiossarcoma52 e leiomioma53 uterino a doses subcutâneas de 1, 3, 10 mcg/kg (2 a 15 vezes a AUC36 da dose humana de 14 mcg, equivalente a 0,24 mcg/kg baseado na AUC36). A taxa de incidência3 de leiomioma53 uterino foi significativamente diferente comparando-se ao grupo controle com uma dose máxima de 10 mcg/kg.
Em um estudo de carcinogênese de 104 semanas em ratos, foi observado um aumento na incidência3 de feocromocitoma54 adrenal benigno a doses subcutâneas de 0,15; 0,5; 1,5 mcg/kg (< 1 a 7 vezes a dose humana de 14 mcg, equivalente a 0,24 mcg/kg baseado na AUC36). O aumento na incidência3 do feocromocitoma54 em ratos pode estar relacionado à alteração da homeostase do cálcio causada pelo paricalcitol.
Mutagênese: o paricalcitol não apresentou toxicidade37 genética in vitro, com ou sem ativação metabólica, no ensaio de mutagênese microbiana (teste de Ames), no ensaio de mutagênese em linfoma55 de camundongo (L5178Y) ou no ensaio de aberrações cromossômicas em linfócito56 humano.
Também não houve evidência de toxicidade37 genética em um ensaio in vivo com micronúcleos de camundongos.
Prejuízo à Fertilidade: o paricalcitol não teve efeito sobre a fertilidade (em machos ou fêmeas) em ratos nas doses intravenosas de até 20 mcg/kg/dose [equivalente a 13 vezes a maior dose humana recomendada (0,24 mcg/kg), com base na área de superfície corporal, mcg/m2].
INTERAÇÕES MEDICAMENTOSAS
Estudos específicos de interação medicamentosa não foram conduzidos com paricalcitol injetável.
Um estudo de interação fármaco57-fármaco57 de múltiplas doses com cetoconazol e paricalcitol cápsulas demonstrou que cetoconazol praticamente dobrou a AUC36(0-∞) de paricalcitol (veja em “3.CARACTERÍSTICAS FARMACOLÓGICAS”). Como o paricalcitol é parcialmente metabolizado por CYP3A e sabe-se que o cetoconazol é um forte inibidor do citocromo P450 3A, deve-se ter cautela ao administrar paricalcitol com cetoconazol ou outro forte inibidor de P450 3A.
Prescrições baseadas em fosfatos ou produtos contendo vitamina11 D não devem ser utilizados concomitantemente a paricalcitol devido ao aumento do risco de hipercalcemia e elevação do produto Ca x P.
A coadministração de altas doses de preparações contendo cálcio ou diuréticos58 tiazídicos e paricalcitol podem aumentar o risco de hipercalcemia.
Preparações contendo magnésio (ex. antiácidos59) não devem ser utilizadas em combinação com preparações de vitamina11 D pois pode ocorrer hipermagnesemia.
Preparações contendo alumínio (ex. antiácidos59, aglutinantes de fosfato) não devem ser administrados cronicamente com produtos medicinais contendo vitamina11 D, pois pode ocorrer aumento dos níveis de alumínio no sangue60 e toxicidade37 de alumínio nos ossos. Não se espera que o paricalcitol iniba a depuração de fármacos metabolizados pelo citocromo P450, enzimas CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 ou CYP3A; e tampouco induza a depuração de fármacos metabolizados por CYP2B6, CYP2C9 ou CYP3A.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Syletyv deve ser armazenado em temperatura ambiente (temperatura entre 15 e 30°C).
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original. Depois de aberto, este medicamento deve ser utilizado imediatamente.
Observação: produtos parenterais devem ser inspecionados visualmente antes da administração quanto a material particulado e descoloração, sempre que a solução e o recipiente permitirem.
Soluções que não estejam límpidas e incolores não devem ser usadas. Descartar as porções não utilizadas.
Características físicas e organolépticas do produto
Syletyv apresenta-se como uma solução clara incolor, contida em uma ampola de vidro transparente, quando examinada sob condições de visibilidade ela é livre de partículas estranhas.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
A via de administração usual de Syletyv é pelo acesso para hemodiálise26. Para pacientes9 sem acesso para hemodiálise26, o Syletyv deve ser administrado por via intravenosa, com injeção28 lenta, com pelo menos 30 segundos de duração, para minimizar a dor.
Posologia
Há dois métodos para determinação da dose inicial de Syletyv. A dose máxima administrada com segurança nos estudos clínicos foi de 40 microgramas.
Dose inicial baseada na massa corpórea
A dose inicial recomendada de paricalcitol é de 0,04 mcg/kg a 0,1 mcg/kg (2,8- 7 mcg), administrada como dose in bolus29, não mais frequentemente do que em dias alternados, a qualquer momento durante a diálise5.
Dose inicial baseada nos níveis de PTHi
Ensaios de segunda geração para PTH [PTH intacto (PTHi)] foram utilizados para dosagem de PTH biologicamente ativo em pacientes com insuficiência renal2 crônica. A dose inicial é calculada pela fórmula abaixo e administrada por via intravenosa como dose in bolus29, não mais frequentemente do que em dias alternados a qualquer momento durante a diálise5:
Dose inicial (microgramas) = nível basal de PTHi (pg/mL) ÷ 80
Ajuste da dose
A faixa terapêutica23 atualmente aceita para os níveis de PTHi em pacientes com IRC no estágio final sob hemodiálise26 é de não mais do que 1,5 a 3 vezes o limite superior normal não-urêmico (150-300 pg/mL para PTHi). Acompanhamento próximo e doses tituladas individuais são necessários para alcançar parâmetros fisiológicos apropriados.
Durante qualquer período de ajuste de dose, o cálcio (corrigido para hipoalbuminemia61) e fósforo séricos devem ser monitorados mais frequentemente e, se um nível elevado de cálcio, aumento persistente de fósforo ou aumento persistente do produto Ca x P maior que 75 forem observados, a dose deve ser ajustada ou interrompida até que estes parâmetros sejam normalizados. Portanto, o Syletyv deve ser reiniciado a uma menor dose. Se o paciente está utilizando quelante de fosfato à base de cálcio, a dose deve ser diminuída ou interrompida, ou o paciente deve trocar para um quelante de fosfato não cálcico.
As doses poderão ser diminuídas quando os níveis de PTH começarem a diminuir em resposta à terapia. Assim a dosagem incremental deve ser individualizada.
Se uma resposta satisfatória não for observada, a dose poderá ser elevada em 2 a 4 mcg, a intervalos de duas a quatro semanas. Se, em qualquer momento, o nível de PTHi diminuir para menos de 150 pg/mL, a dosagem de Syletyv deve ser diminuída.
A Tabela 4 a seguir é uma abordagem sugerida para a titulação de dose:
Tabela 4 - Diretrizes de doses sugeridas
|
Nível de PTHi |
Dose de Syletyv |
|
o mesmo ou em elevação |
Aumentar em 2 ou 4 mcg |
|
em diminuição menor do que 30% |
Aumentar em 2 ou 4 mcg |
|
em diminuição maior do que 30% e menor do que 60% |
Manter |
|
em diminuição maior do que 60% |
Diminuir em 2 ou 4 mcg |
|
Menor do que 150 pg/mL |
Diminuir em 2 ou 4 mcg |
|
uma e meia a três vezes o limite superior normal (150 a 300 pg/mL) |
Manter |
REAÇÕES ADVERSAS
Reações adversas em estudos clínicos placebo4 ou ativo controlado Fase II a Fase IV
Duzentos e noventa pacientes foram tratados com paricalcitol em estudos clínicos placebo4 ou ativo controlado Fase II-IV. O evento adverso mais comum associado com a terapia de paricalcitol foi a hipercalcemia ocorrendo em 4,1% dos pacientes. Hipercalcemia é dependente dos níveis de supressão intensa do PTH e pode ser minimizado pela titulação da dose adequada.
As reações adversas e suas frequências pelo menos, possivelmente relacionadas ao paricalcitol são apresentadas a seguir:
Os seguintes agrupamentos por frequência foram utilizados: reação muito comum (> 1/10), reação comum (≥ 1/100 e < 1/10), reação incomum (≥ 1/1000 e < 1/100), reação rara (≥ 1/10000 e < 1/1000), reação muito rara (< 1/10000) e de frequência desconhecida (não foi possível estimar através dos dados disponíveis).
Reação comum (≥ 1/100 e < 1/10):
- Alterações do metabolismo30 e nutrição62: hipercalcemia.
- Alterações do sistema nervoso63: disgeusia64, cefaleia65.
- Alterações gastrointestinais: hemorragia66 gastrointestinal, diarreia67, constipação68.
- Alterações gerais e condições do local da administração: febre69, calafrios70, dor no local da injeção28.
Reação incomum (≥ 1/1000 e < 1/100):
- Infecções71 e infestações: pneumonia72, gripe73, infeção do trato respiratório superior, nasofaringite.
- Neoplasias74 benignas e malignas (incluindo cistos e pólipos75): câncer76 de mama77.
- Alterações do sistema linfático78 e hematológico: anemia79.
- Alterações endócrinas: hipoparatireoidismo.
- Alterações do metabolismo30 e nutrição62: hipocalcemia80, hiperfosfatemia, diminuição do apetite.
- Alterações psiquiátricas: delírio81, estado confusional, agitação, insônia, nervosismo, inquietação.
- Alterações do sistema nervoso63: acidente vascular cerebral82, síncope83, mioclonia84, vertigem85, hipoestesia86, parestesia87.
- Alterações visuais: conjuntivite88.
- Alterações cardíacas: parada cardíaca, flutter atrial, palpitação89.
- Alterações vasculares90: hipotensão91, hipertensão92.
- Alterações respiratórias, torácicas e do mediastino93: edema pulmonar94, dispneia95, ortopneia, tosse.
- Alterações gastrointestinais: isquemia96 intestinal, hemorragia66 retal, vômito97, desconforto abdominal, boca98 seca. Alterações de pele e tecido subcutâneo99: alopécia100, rash101 com prurido102, prurido102, sensação de queimação da pele14, bolhas. Alterações musculoesqueléticas, tecido conectivo103 e ósseo: artralgia104, rigidez articular, mialgia105, contrações musculares. Alterações no sistema reprodutivo: disfunção erétil, dor nas mamas106.
- Alterações gerais e condições do local da administração: alterações na marcha, inchaço107, astenia108, mal-estar, fadiga109, condições agravadas.
- Investigações: aumento da aspartato aminotransferase, teste laboratorial anormal, perda de peso.
- Palpitação89, hemorragia66 gastrointestinal, e calafrios70 são eventos adversos que foram observados em uma frequência maior que o placebo4.
Pós-comercialização
Reações adversas em estudos clínicos Fase IV, outros estudos clínicos ou pós comercialização:
- Infecções71 e infestações: sepse110, infecção111 vaginal.
- Alterações do sistema linfático78 e hematológico: linfoadenopatia112.
- Alterações do sistema imunológico113: hipersensibilidade, angioedema114, edema115 de laringe116.
- Alterações endócrinas: hiperparatireoidismo.
- Alterações do metabolismo30 e nutrição62: hipercalemia117.
- Alterações do sistema nervoso63: indiferença (sem resposta) ao estímulo.
- Alterações visuais: glaucoma118, hiperemia119 ocular. Alterações do ouvido e labirinto120: desconforto no ouvido. Alterações cardíacas: arritmia121.
- Alterações respiratórias, torácicas e do mediastino93: chiado.
- Alterações gastrointestinais: disfagia122, gastrite123, náusea124.
- Alterações de pele e tecido subcutâneo99: hirsutismo125, suores noturnos, rash101, urticária126.
- Alterações gerais e condições do local da administração: desconforto no peito127, dor no peito127, edema115, sensação anormal, extravasamento no local da injeção28, edema115 periférico, dor, sede.
- Investigações: tempo de sangramento prolongado, frequência cardíaca irregular.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
A superdosagem de paricalcitol pode produzir hipercalcemia, hipercalciúria128, hiperfosfatemia e supressão elevada de PTH.
O paricalcitol não é significativamente removido por diálise5. O tratamento de pacientes com hipercalcemia clinicamente significativa consiste em imediata redução de dose ou interrupção da terapia com Syletyv e inclui dieta com baixa ingestão de cálcio, descontinuação de suplementos de cálcio, mobilização do paciente, atenção aos desequilíbrios de fluidos e eletrólitos41, avaliação de anormalidades eletrocardiográficas (crítico em pacientes recebendo digitálicos) e hemodiálise26 ou diálise peritoneal27 com um dialisato sem cálcio, se justificado.
Quando os níveis plasmáticos de cálcio retornam ao limite da normalidade, a terapia com Syletyv pode ser reiniciada com baixas doses. Se os níveis séricos de cálcio continuarem persistentes e acentuados, uma variedade de alternativas terapêuticas deve ser considerada. Isto inclui o uso de drogas tais como fosfatos e corticosteroides bem como medidas para induzir a diurese129.
A solução de Syletyv contém 30% v/v de propilenoglicol como excipiente. Casos isolados de depressão do Sistema Nervoso Central130, hemólise131 e acidose132 lática133 foram reportados como efeitos tóxicos associados à administração de propilenoglicol em altas doses. Embora não sejam esperados com a administração de Syletyv, já que ocorre eliminação do propilenoglicol durante o processo de diálise5, deve-se considerar estes efeitos em situações de superdose.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.5537.0077
Farm. Resp.: Dra. Jarsonita Alves Serafim – CRF/SP 51512
Fabricado por:
Intas Pharmaceuticals Ltd.
Plot n° 457, 458 - Matoda 382 210, Dist. Ahmedabad – Índia
Importado por:
Accord Farmacêutica Ltda.
Av. Guido Caloi, 1985 – G.01 – Santo Amaro – São Paulo/SP
CNPJ: 64.171.697/0001-46
SAC 0800 723 9777






