Tobramina (Bula do profissional de saúde)
ANTIBIÓTICOS DO BRASIL LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Tobramina®
sulfato de tobramicina
Injetável 75 mg/1,5 mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Embalagem com 10 ampolas de 1,5 mL cada
USO INTRAVENOSO OU INTRAMUSCULAR
USO ADULTO E PEDIÁTRICO
COMPOSIÇÃO:
Cada mL de Tobramina contém:
| sulfato de tobramicina (equivalente a 50 mg de tobramicina) | 152,45 mg |
| veículo q.s.p. | 1 mL |
Veículo: bissulfito de sódio, edetato dissódico, fenol e água para injetáveis.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE1
INDICAÇÕES
Tobramina® está indicada no tratamento de infecções2 bacterianas graves causadas por cepas3 suscetíveis dos microrganismos descritos no item “Microbiologia” e mencionados abaixo:
Septicemia4 em pacientes pediátricos e adultos causada por: Pseudomonas aeruginosa, Escherichia coli e Klebsiella spp.
Infecções2 do trato respiratório inferior causadas por: Pseudomonas aeruginosa, Klebsiella spp., Enterobacter spp., Serratia spp., Escherichia coli, e Staphylococcus aureus (cepas3 produtoras e não produtoras de penicilinase).
Meningites5 causadas por: microrganismos suscetíveis.
Infecções2 intra-abdominais, incluindo peritonite6 causadas por: Escherichia coli, Klebsiella spp. e Enterobacter spp.
Infecções2 ósseas, da pele7 e de estruturas da pele7 causadas por: Pseudomonas aeruginosa, Proteus spp., Escherichia coli, Klebsiella spp., Enterobacter spp. e Staphylococcus aureus.
Infecções2 urinárias recorrentes e complicadas causadas por: Pseudomonas aeruginosa, Proteus spp. (indol positivo e indol negativo), Escherichia coli, Klebsiella spp., Enterobacter spp., Serratia spp., Providencia spp., Staphylococcus aureus e Citrobacter spp.
Os aminoglicosídeos, incluindo a tobramicina, não estão indicados em episódios iniciais não complicados de infecções2 do trato urinário8, a menos que o microrganismo causal não seja suscetível a outros antibacterianos com menor potencial de toxicidade9.
A tobramicina deve ser considerada em infecções2 estafilocócicas graves quando a penicilina ou outros medicamentos potencialmente menos tóxicos estão contraindicados, ou quando os testes de suscetibilidade bacteriana ou o julgamento clínico indicarem seu uso.
Culturas bacterianas devem ser realizadas antes e durante o tratamento. Se os testes de suscetibilidade demonstrarem que os microrganismos causais são resistentes à tobramicina, outro tratamento deve ser instituído.
Nos pacientes em que houver suspeita de infecção10 grave com risco de morte causada por Gram-negativo, incluindo aqueles em que o tratamento conjunto com penicilina ou cefalosporina e um aminoglicosídeo estiver indicado, o tratamento com tobramicina pode ser iniciado antes que os resultados dos testes de suscetibilidade estejam disponíveis. A decisão de continuar o tratamento com a tobramicina deve ser baseada nos resultados dos testes de suscetibilidade, gravidade da infecção10 e nas advertências e precauções para o uso do produto (ver item “5. ADVERTÊNCIAS E PRECAUÇÕES”).
RESULTADOS DE EFICÁCIA
Em estudos clínicos8 a tobramicina demonstrou boa ação contra infecções2 envolvendo microrganismos descritos no item “1. INDICAÇÕES”:
Trato respiratório inferior
Em estudos clínicos, dos 110 pacientes inclusos nesta categoria, 95 (85%) responderam ao tratamento com tobramicina.
Pele7, ossos e tecidos moles, incluindo queimaduras
Em estudos clínicos, dos 95 pacientes inclusos nesta categoria, 82 (86%) responderam ao tratamento com tobramicina.
Infecções2 urinárias recorrentes e complicadas
Em estudos clínicos, dos 348 pacientes diagnosticados com pielonefrite11, cistite12 e infecção10 urinária inespecífica, 333 (96%) responderam ao tratamento com tobramicina. Dos pacientes que responderem ao tratamento, 265 não tiveram recorrência13 após eliminação do patógeno. Os outros 65 pacientes, que responderam ao tratamento, apresentaram recorrência13 da infecção10 pelo mesmo patógeno (32 pacientes) ou por patógenos diferentes (36 pacientes).
A tobramicina também apresentou ação no combate à bacteriúria14. Em estudo com 34 pacientes que responderam ao tratamento com tobramicina, 26 não apresentaram recorrência13, 7 apresentaram recorrência13 do mesmo patógeno e 1 apresentou recorrência13 de patógeno diferente.
Infecção10 gastrintestinal, incluindo peritonite6
Em estudos clínicos, dos 35 pacientes inclusos nesta categoria, 29 (83%) responderam ao tratamento com tobramicina.
Infecções2 do Sistema Nervoso Central15, incluindo meningite16
Em estudos clínicos, 9 pacientes (8 deles crianças com pelo menos 1 doença grave de base, como hidrocefalia17 e mielomeningocele18) diagnosticados com infecção10 no sistema nervoso central15 foram tratados com tobramicina por no mínimo 10 dias seguidos e 7 (78%) pacientes responderam satisfatoriamente.
Septicemia4
Em estudos clínicos, dos 55 pacientes (46 recém-nascidos ou lactentes19 e 8 pacientes mais velhos) diagnosticados com septicemia4, 50 (93%) responderam ao tratamento com tobramicina.
CARACTERÍSTICAS FARMACOLÓGICAS
Descrição: o sulfato de tobramicina é um antibacteriano do grupo dos aminoglicosídeos, derivado do actinomiceto Streptomyces tenebrarius, solúvel em água, e apresenta-se como uma solução aquosa estéril, clara e incolor, para administração parenteral. A fórmula química do sulfato de tobramicina é (C18H37N5O9)2 • 5H2SO4 . O peso molecular é 1425,45.
Farmacocinética
Absorção: a tobramicina é pouco absorvida pelo trato gastrintestinal. Após administração intramuscular, no entanto, é rapidamente absorvida. As concentrações séricas de pico ocorrem entre 30 e 90 minutos após administração intramuscular. Após uma dose intramuscular de 1 mg/kg de peso corpóreo, as concentrações séricas máximas alcançam cerca de 4 mcg/mL, e níveis mensuráveis persistem por até 8 horas. Os níveis séricos terapêuticos geralmente variam de 4 a 6 mcg/mL. Quando a tobramicina é administrada por infusão intravenosa, durante um período de 1 hora, as concentrações séricas são similares às obtidas com a administração intramuscular.
Distribuição: em pacientes com a função renal20 normal, com exceção de neonatos21, a tobramicina administrada a cada 8 horas não acumula no soro22. Entretanto, nos pacientes com função renal20 reduzida e em neonatos21, a concentração sérica é normalmente mais alta e pode ser detectada por períodos de tempo mais longos que em adultos normais. Portanto, a posologia para tais pacientes deve ser ajustada. (ver item “8. POSOLOGIA E MODO DE USAR”).
A tobramicina pode ser detectada nos tecidos e nos fluidos corpóreos após administração parenteral. Concentrações na bile23 e nas fezes geralmente são baixas, sugerindo uma excreção biliar mínima. A tobramicina apareceu em baixas concentrações no líquido cefalorraquidiano24, após administração parenteral, e as concentrações são dependentes da dose, taxa de penetração e grau de inflamação25 meníngea26. Também foi encontrada no escarro, líquido peritoneal, líquido sinovial27 e fluidos de abscessos28. A tobramicina cruza a membrana placentária. As concentrações no córtex renal29 são muitas vezes superiores aos níveis séricos usuais.
Eliminação: após administração parenteral, ocorre pouca ou nenhuma transformação metabólica, e a tobramicina é eliminada quase que exclusivamente por filtração glomerular. O clearance renal20 é similar ao da creatinina30 endógena. Estudos de ultrafiltração demonstram que praticamente não ocorre ligação às proteínas31 séricas. Em pacientes com função renal20 normal, até 84% da dose são recuperáveis na urina32 em 8 horas e até 93% em 24 horas.
Concentrações urinárias de pico variando de 75 a 100 mcg/mL foram observadas após a administração intramuscular de uma dose única de 1 mg/kg. Após diversos dias de tratamento, a quantidade de tobramicina excretada na urina32 se aproxima da dose diária administrada. Quando a função renal20 está prejudicada, a excreção da tobramicina é mais lenta, podendo ocorrer níveis sanguíneos tóxicos.
A meia-vida sérica, em indivíduos normais, é de 2 horas. Existe uma relação inversa entre a meia-vida sérica e o clearance de creatinina30, e o esquema posológico deve ser ajustado de acordo com o grau de diminuição da função renal20 (ver item “8. POSOLOGIA E MODO DE USAR”).
Em pacientes submetidos à diálise33, 25% a 70% da dose administrada podem ser removidos dependendo da duração e do tipo de diálise33. A probenecida não afeta o transporte tubular renal20 da tobramicina.
Farmacodinâmica
A tobramicina age na inibição da síntese de proteínas31 nas células34 bacterianas por ligação irreversível às subunidades 30S dos ribossomos. Testes in vitro demonstraram que a tobramicina é bactericida.
Microbiologia: A tobramicina demonstrou ser ativa contra a maior parte das cepas3 dos seguintes microrganismos, tanto in vitro como em infecções2 clínicas, como descrito no item “1. INDICAÇÕES”.
Aeróbicos Gram-positivos:
- Staphylococcus aureus
Aeróbicos Gram-negativos:
- Citrobacter spp.
- Enterobacter spp.
- Escherichia coli
- Klebsiella spp.
- Morganella morganii
- Pseudomonas aeruginosa
- Proteus mirabilis
- Proteus vulgaris
- Providencia spp.
- Serratia spp.
Os aminoglicosídeos têm baixo grau de atividade contra a maioria dos microrganismos Gram-positivos, incluindo Streptococcus pyogenes, Streptococcus pneumoniae e enterococos.
Embora a maioria das cepas3 de enterococos demonstre resistência in vitro, algumas cepas3 deste grupo são suscetíveis. Estudos in vitro demonstraram que um aminoglicosídeo combinado com um antibiótico que interfere na síntese da parede celular, afeta sinergicamente algumas cepas3 de enterococos. A penicilina G e a tobramicina, associadas, apresentam um efeito bactericida sinérgico in vitro contra algumas cepas3 de Enterococcus faecalis. Entretanto, essa combinação não é sinérgica contra outros microrganismos com relação próxima, como o Enterococcus faecium. Não basta apenas classificar o enterococo por espécie para predizer a suscetibilidade. É necessário realizar testes de suscetibilidade e testes de sinergismo antibiótico.
Resistência cruzada entre aminoglicosídeos pode ocorrer.
Testes de Suscetibilidade
Técnicas de Difusão:
Métodos quantitativos baseados na medição dos diâmetros dos halos proporcionam uma estimativa de suscetibilidade ao antibacteriano. O método recomendado pelo Clinical and Laboratory Standards Institute (CLSI) para testar a suscetibilidade dos microrganismos à tobramicina emprega discos com 10 mcg de tobramicina. Os resultados dos testes de suscetibilidade devem ser interpretados de acordo com os seguintes critérios:
|
Diâmetro do Halo (mm) |
Interpretação |
|
≥ 15 |
(S) Suscetível |
|
13–14 |
(I) Intermediário |
|
≤ 12 |
(R) Resistente |
Um resultado “suscetível” indica que o patógeno provavelmente será inibido pelos níveis sanguíneos normalmente alcançados. Um resultado “intermediário” sugere que o microrganismo deve ser suscetível se for usada alta dose ou se a infecção10 estiver confinada nos tecidos e líquidos onde altos níveis do antibacteriano são atingidos. Um resultado “resistente” indica que as concentrações alcançadas não serão suficientes para inibir o microrganismo e outra terapia deve ser selecionada.
Cepas3-Controle:
Procedimentos padronizados pelo Clinical and Laboratory Standards Institute (CLSI) requerem o uso de cepas3-controle de microrganismos (cepas3 ATCC). Os discos de 10 mcg de tobramicina devem produzir o seguinte halo de inibição:
|
Microrganismo |
Diâmetro do Halo (mm) |
|
Escherichia coli |
18–26 |
|
Pseudomonas aeruginosa |
19–25 |
|
Staphylococcus aureus |
19–29 |
Técnicas de Diluição:
Usar o método de diluição padronizado pelo Clinical and Laboratory Standards Institute (CLSI), em caldo, ágar ou equivalente. Os valores de concentração inibitória mínima (CIM) para tobramicina obtidos devem ser interpretados de acordo com os seguintes critérios:
|
CIM (mcg/mL) |
Interpretação |
|
≤ 4 |
(S) Suscetível |
|
8 |
(I) Intermediário |
|
≥ 16 |
(R) Resistente |
Um resultado “suscetível” indica que o patógeno provavelmente será inibido pelos níveis sanguíneos normalmente alcançados. Um resultado “intermediário” sugere que o microrganismo deve ser suscetível se for usada alta dose ou se a infecção10 estiver confinada nos tecidos e líquidos onde altos níveis do antibacteriano são atingidos. Um resultado “resistente” indica que as concentrações alcançadas não serão suficientes para inibir o microrganismo e outra terapia deve ser selecionada.
Cepas3-Controle:
Os procedimentos de diluição também requerem o uso de cepas3-controle de microrganismos (cepas3 ATCC). A tobramicina padrão deve dar os seguintes valores de CIM com o método de diluição padronizado pelo Clinical and Laboratory Standards Institute (CLSI):
|
Microrganismos |
Variação de CIMs (mcg/mL) |
|
Enterococcus faecalis |
8–32 |
|
Escherichia coli |
0,25–1 |
|
Pseudomonas aeruginosa |
0,25–1 |
|
Staphylococcus aureus |
0,12–1 |
CONTRAINDICAÇÕES
Tobramina® é contraindicada para pacientes35 com hipersensibilidade a qualquer aminoglicosídeo, principalmente à tobramicina. História de hipersensibilidade ou reação tóxica grave aos aminoglicosídeos, pode também contraindicar o uso de qualquer outro aminoglicosídeo devido à conhecida hipersensibilidade cruzada a medicamentos desta classe.
Uso na Gravidez36 – categoria de risco D.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Os aminoglicosídeos podem causar dano fetal quando administrados a mulheres grávidas. Se a tobramicina for usada durante a gravidez36, ou se a paciente engravidar enquanto estiver sob tratamento com a tobramicina, deve-se notificar a mãe sobre o potencial dano para o feto37.
Os antibacterianos aminoglicosídeos cruzam a placenta e há diversos relatos de surdez congênita38 bilateral total e irreversível em crianças cujas mães receberam estreptomicina durante a gravidez36. Não foram relatados efeitos colaterais39 graves para a mãe, para o feto37 ou para o recém-nascido, no tratamento de mulheres grávidas com outro aminoglicosídeo.
ADVERTÊNCIAS E PRECAUÇÕES
Sensibilidade ao sulfito: Tobramina® contém bissulfito de sódio, um sulfito que pode causar reações do tipo alérgicas, incluindo sintomas40 anafiláticos e episódios asmáticos menos graves ou com risco de morte em indivíduos sensíveis. A prevalência41 total de hipersensibilidade ao sulfito na população geral é desconhecida e é provavelmente baixa. A sensibilidade ao sulfito tem sido observada mais frequentemente em pessoas asmáticas do que em não asmáticas.
Reações de hipersensibilidade: raramente foram relatadas reações alérgicas graves incluindo anafilaxia42 e reações dermatológicas incluindo dermatite43 esfoliativa, necrólise epidérmica tóxica44 e Síndrome de Stevens-Johnson45. Apesar de raras, algumas fatalidades foram reportadas. Se uma reação alérgica46 ocorrer, a droga deve ser descontinuada e uma terapia adequada deve ser instituída.
Ototoxicidade47: a tobramicina, assim como os aminoglicosídeos em geral, possui potencial inerente para causar ototoxicidade47. Pacientes tratados com esses medicamentos devem ficar sob observação clínica rigorosa.
O risco de ototoxicidade47 (coclear ou vestibular48) induzida por aminoglicosídeos aumenta com o grau de exposição a altos picos de concentração sérica ou concentrações séricas elevadas constantes. Pacientes que desenvolvem dano coclear podem não apresentar sintomas40, durante o tratamento, que os alertem sobre a toxicidade9 ao oitavo par craniano. A surdez bilateral, irreversível, parcial ou total, pode continuar a se desenvolver mesmo após a medicação ter sido interrompida. Quando possível, recomenda-se a realização de audiometrias seriadas, particularmente em pacientes de alto risco.
Nefrotoxicidade49: a nefrotoxicidade49 induzida por aminoglicosídeos é geralmente reversível. Em casos raros, a nefrotoxicidade49 se manifestou alguns dias após o término do tratamento.
Podem ocorrer danos em pacientes apresentando dano renal20 pré-existente e em pacientes com função renal20 normal para os quais os aminoglicosídeos são administrados por períodos mais longos ou em doses mais altas do que as recomendadas. Também há maior chance de nefrotoxicidade49 quando se associa um aminoglicosídeo a outra droga nefrotóxica (ver item “6. INTERAÇÕES MEDICAMENTOSAS”).
A função renal20 deve ser monitorada em pacientes com diminuição da função renal20 suspeita ou conhecida e em pacientes com função renal20 inicialmente normal que desenvolveram sinais50 de disfunção renal20 durante o tratamento.
A urina32 deve ser examinada para detectar diminuição da densidade específica e aumento da excreção de proteínas31, células34 e cilindros. Devem ser avaliados periodicamente a uremia51, a creatinina30 sérica e o clearance de creatinina30.
Evidências de prejuízos renais, vestibulares52 ou das funções auditivas requerem a interrupção do tratamento com o medicamento ou ajuste na posologia.
Neurotoxicidade: a neurotoxicidade pode ser manifestada tanto por ototoxicidade47 auditiva como vestibular48. As alterações auditivas são irreversíveis, geralmente bilaterais, podendo ser parciais ou totais. Podem ocorrer danos no oitavo par craniano (nervo vestibulococlear) principalmente em pacientes apresentando dano renal20 pré-existente e em pacientes com função renal20 normal para os quais os aminoglicosídeos são administrados por períodos mais longos ou em doses mais altas do que as recomendadas.
Outras manifestações de neurotoxicidade podem incluir: entorpecimento, sensação de picadas na pele7, contrações musculares e convulsões.
Desidratação53 e hipovolemia54: são fatores de risco para neurotoxicidade, ototoxicidade47 e nefrotoxicidade49 induzidas por tobramicina. Amostras do soro22 e da urina32 devem ser colhidas para exame para monitoramento de cálcio, magnésio e sódio séricos.
Deve-se corrigir a desidratação53, a hipovolemia54, a diminuição da perfusão renal20 e a insuficiência cardíaca congestiva55 antes da utilização de aminoglicosídeos.
Uso concomitante com outro medicamento nefrotóxico e/ou neurotóxico: o uso concomitante ou sequencial de outro antibacteriano nefrotóxico e/ou neurotóxico, particularmente outros aminoglicosídeos (amicacina, estreptomicina, neomicina, canamicina, gentamicina ou paramomicina), cefaloridina, viomicina, polimixina B, colistina, cisplatina e vancomicina deve ser evitado.
Uso concomitante com diuréticos56 potentes: a tobramicina não deve ser administrada concomitantemente a diuréticos56 potentes, tais como o ácido etacrínico e a furosemida. Alguns diuréticos56 por si só causam ototoxicidade47, e diuréticos56 administrados por via intravenosa aumentam a toxicidade9 dos aminoglicosídeos, incluindo a tobramicina, alterando sua concentração sérica e tecidual.
Uso concomitante com cefalosporina: foi relatado um aumento na incidência57 de nefrotoxicidade49 quando da administração concomitante de antibacterianos aminoglicosídeos e cefalosporinas (ex.: cefazolina e cefalotina).
Bloqueio neuromuscular e paralisia58 respiratória: bloqueio neuromuscular e paralisia58 respiratória foram relatados em gatos recebendo doses muito altas de tobramicina (40 mg/kg). A possibilidade de apneia59 prolongada ou secundária deve ser considerada se a tobramicina for administrada a pacientes anestesiados que também estejam recebendo agentes bloqueadores neuromusculares (succinilcolina, tubocurarina ou decametônio), ou a pacientes recebendo volumosas transfusões de sangue60 com citrato.
Se ocorrer o bloqueio neuromuscular, o mesmo pode ser revertido pela administração de sais de cálcio.
Pacientes com distúrbios musculares, tais como a miastenia61 gravis ou parkinsonismo: a tobramicina deve ser usada com cautela, uma vez que os aminoglicosídeos podem agravar a fraqueza muscular devido seu potencial efeito tipo curare na função neuromuscular.
Pacientes com extensas queimaduras ou fibrose cística62: a alteração da farmacocinética pode resultar em concentrações séricas reduzidas de aminoglicosídeos. Em tais pacientes, tratados com tobramicina, a determinação da concentração sérica é extremamente importante como base para a determinação da posologia adequada.
Absorção pela superfície corporal: aminoglicosídeos, incluindo a tobramicina, podem ser absorvidos em quantidades significativas pela superfície corpórea após irrigação ou aplicação, podendo causar neurotoxicidade e nefrotoxicidade49.
Uso intraocular e/ou subconjuntival: aminoglicosídeos não foram aprovados para uso intraocular e/ou subconjuntival. Existem relatos de necrose63 macular após administração de aminoglicosídeos, incluindo a tobramicina, por essas vias.
Hipersensibilidade cruzada: foi demonstrada hipersensibilidade cruzada entre os aminoglicosídeos. História de hipersensibilidade ou reação tóxica grave aos aminoglicosídeos pode contraindicar o uso de qualquer outro aminoglicosídeo devido à conhecida alergia64 cruzada a medicamentos desta classe.
Inativação da tobramicina por antibacterianos betalactâmicos: a inativação da tobramicina e outros aminoglicosídeos por antibacterianos betalactâmicos (penicilinas ou cefalosporinas) foi demonstrada in vitro e em pacientes com insuficiência renal65 grave.
Esta inativação não foi identificada em pacientes com função renal20 normal aos quais se administraram antibacterianos aminoglicosídeo e betalactâmico em locais separados.
Superinfecção66: o tratamento com tobramicina pode resultar em crescimento exagerado de microrganismos não suscetíveis. Nesses casos, tratamento adequado deve ser iniciado.
Monitoramento de níveis séricos de tobramicina: os níveis séricos devem ser medidos periodicamente durante o tratamento para assegurar níveis adequados e evitar níveis potencialmente tóxicos. Concentrações prolongadas acima de 12 mcg/mL devem ser evitadas. Níveis ascendentes (acima de 2 mcg/mL) podem indicar acumulação tecidual. Este acúmulo, idade avançada e doses acumulativas podem contribuir para a ototoxicidade47 e a nefrotoxicidade49. É de particular importância monitorizar de perto os níveis séricos de pacientes com conhecida diminuição da função renal20.
Estas avaliações de níveis séricos podem ser especialmente úteis para monitorar o tratamento de pacientes gravemente doentes com alterações de função renal20, pacientes infectados com microrganismos menos suscetíveis e pacientes recebendo doses máximas. Realizar a primeira coleta de material para avaliação do nível sérico de tobramicina 2 ou 3 doses após início do tratamento, assim a posologia poderá ser ajustada se necessário. Após a primeira avaliação do nível sérico, realizar coletas a intervalos de 3 a 4 dias durante o tratamento com tobramicina.
Para determinar o nível sérico de pico, retirar as amostras de soro22 cerca de 30 minutos após o término da infusão intravenosa ou 1 hora após uma injeção intramuscular67.
Para determinar o nível sérico de vale, retirar as amostras de soro22 cerca de 8 horas após administração de tobramicina ou logo antes da aplicação da próxima dose de tobramicina. Estes intervalos de tempo sugeridos devem ser entendidos apenas como orientação e podem variar de acordo com a conduta da instituição. É importante, porém, que haja consistência com o esquema individual do paciente, a menos que programas computadorizados de dosagem farmacocinética estejam disponíveis na instituição.
Na eventualidade de alteração na função renal20, aumentar a frequência de avalição dos níveis séricos e ajustar as doses ou o intervalo entre as doses de acordo com as instruções do item “8. POSOLOGIA E MODO DE USAR”.
Gravidez36 e Lactação68
Uso na Gravidez36: categoria de risco D – Há evidências de risco em fetos humanos. Só usar se o benefício justificar o risco potencial. Em situação de risco de vida ou em caso de doenças graves para as quais não se possa utilizar drogas mais seguras, ou se estas drogas não forem eficazes.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica.
Os aminoglicosídeos podem causar dano fetal quando administrados a mulheres grávidas. Se a tobramicina for usada durante a gravidez36, ou se a paciente engravidar enquanto estiver sob tratamento com a tobramicina, deve-se notificar a mãe sobre o potencial dano para o feto37.
Os antibacterianos aminoglicosídeos cruzam a placenta e há diversos relatos de surdez congênita38 bilateral total e irreversível em crianças cujas mães receberam estreptomicina durante a gravidez36. Não foram relatados efeitos colaterais39 graves para a mãe, para o feto37 ou para o recém-nascido, no tratamento de mulheres grávidas com outros aminoglicosídeos diferentes da estreptomicina.
Uso na Lactação68: a tobramicina é excretada no leite humano em baixas concentrações, contudo, os aminoglicosídeos são fracamente absorvidos pelo trato gastrintestinal. Não há relatos de problemas.
Populações especiais
Uso em crianças: a tobramicina deve ser usada com cautela em crianças prematuras e neonatas devido a sua imaturidade renal20 e consequente prolongamento da meia-vida sérica do medicamento.
Uso em idosos: idade avançada é um fator de risco69 para neurotoxicidade, ototoxicidade47 e nefrotoxicidade49 induzidas por tobramicina.
Os pacientes idosos podem ter função renal20 reduzida não detectada pelos exames de rotina, tais como uremia51 e creatinina30 sérica. A determinação do clearance de creatinina30 pode ser mais útil. O monitoramento da função renal20 nesses pacientes é particularmente importante.
INTERAÇÕES MEDICAMENTOSAS
A tobramicina:
- pode ter toxicidade9 aditiva com: outros medicamentos ototóxicos, nefrotóxicos e/ou neurotóxicos como outros aminoglicosídeos (ex.: amicacina, estreptomicina, neomicina, canamicina, gentamicina ou paramomicina), aciclovir70, anfotericina B, bacitracina, capreomicina, algumas cefalosporinas (ex.: cefalotina, cefaloridina), viomicina, polimixinas injetáveis (ex.: polimixina B), colistina, cisplatina, e vancomicina. Se possível, evitar o uso concomitante e/ou sequencial.
- pode ter sua ação diminuída (em pacientes com insuficiência renal65 importante) por: penicilina, cefalosporina.
- pode antagonizar os efeitos de: antimiastênicos.
- pode ter o risco de ototoxicidade47 aumentado com: diuréticos56 potentes como a furosemida ou ácido etacrínico.
- pode aumentar o bloqueio neuromuscular e causar paralisia58 respiratória com: medicamentos bloqueadores neuromusculares (ex.: succinilcolina, tubocurarina e decametônio) e anestésicos gerais (ex.: cetamina e etomidato).
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Tobramina® deve ser armazenada em sua embalagem original, em temperatura ambiente (15–30°C). Este medicamento tem validade de 24 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Após diluição manter em temperatura ambiente (15°C a 30°C) por até 24 horas (ver item “8. POSOLOGIA E MODO DE USAR”).
Características físicas e organolépticas do produto
Características da solução antes e após diluição: solução clara e incolor.
Tobramina® pode apresentar odor característico de formol.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Posologia
ATENÇÃO: as doses são dadas em termos de tobramicina.
Crianças
- Recém-nascidos até 1 semana de vida: até 2 mg por kg de peso cada 12 a 24 horas, administrados por via intramuscular ou por infusão intravenosa. Crianças acima de 1 semana de vida: 2 a 2,5 mg por kg de peso a cada 8 horas ou 1,5 a 1,9 mg por kg de peso a cada 6 horas, administrados por via intramuscular ou por infusão intravenosa.
Adultos com função renal20 normal
- Infecção10 grave: 1 mg por kg de peso a cada 8 horas, administrados por via intramuscular ou por infusão intravenosa.
- Infecção10 com risco de morte: 1,66 mg por kg de peso a cada 8 horas, administrados por via intramuscular ou por infusão intravenosa. A dose não deve ultrapassar 5 mg por kg de peso ao dia, a menos que os níveis séricos sejam monitorados.
Idosos
- Costumam ser mais sensíveis aos aminoglicosídeos; não exceder as doses (e mesmo baixá-las em função de idade muito avançada, condição renal20 ou perda de peso); monitorar função renal20 e auditiva (pode haver perda auditiva mesmo com função renal20 normal).
Duração do tratamento
É desejável limitar o tratamento a um período de tempo curto. A duração usual de tratamento é de 7 a 10 dias. Caso um tratamento mais longo seja necessário (infecções2 difíceis e complicadas), a monitorização das funções renais, auditivas e vestibulares52 é aconselhável, uma vez que a neurotoxicidade ocorre mais frequentemente quando o tratamento se estende por mais de 10 dias.
Instruções Posológicas Especiais
Pacientes com fibrose cística62: Em pacientes com fibrose cística62, alterações farmacocinéticas podem resultar em concentrações séricas reduzidas de aminoglicosídeos. A avaliação das concentrações séricas de tobramicina durante o tratamento é especialmente importante para a determinação de uma dose adequada. Em pacientes com fibrose cística62 grave, sugere-se um esquema posológico inicial de 2,5 mg /kg a cada 6 horas. Este esquema posológico é sugerido apenas como uma orientação. Os níveis séricos de tobramicina devem ser medidos diretamente durante o tratamento devido à ampla variabilidade entre os pacientes.
Pacientes com função renal20 diminuída: Sempre que possível as concentrações séricas de tobramicina devem ser determinadas durante o tratamento.
Após uma dose de ataque inicial de 1 mg/kg, a posologia deve ser ajustada, reduzindo-se as doses administradas a cada 8 horas (ver subitem “Posologia reduzida, em intervalos de 8 horas”) ou aumentando os intervalos entre as doses administradas (ver subitem “Posologia normal em intervalos prolongados”).
Ambos métodos são sugeridos como orientação para serem usados quando os níveis séricos de tobramicina não puderem ser medidos diretamente. Eles são baseados ou no clearance de creatinina30 ou no nível sérico de creatinina30 do paciente, uma vez que estes valores se correlacionam com a meia-vida da tobramicina.
Os esquemas posológicos derivados de ambos métodos devem ser usados conjuntamente com cuidadosas observações clínicas e laboratoriais do paciente e devem ser modificados segundo as necessidades. Nenhum desses métodos deve ser usado quando diálise33 estiver sendo realizada.
- Posologia reduzida, em intervalos de 8 horas: Para calcular a dose reduzida a ser administrada deve-se conhecer o clearance de creatinina30 ou o valor da creatinina30 sérica e consultar o NOMOGRAMA DA POSOLOGIA REDUZIDA abaixo.
Quando o clearance de creatinina30 for menor ou igual a 70 mL por minuto, ou quando o valor da creatinina30 sérica for conhecido, a dose reduzida pode ser calculada multiplicando-se a dose normalmente recomendada (indicada no item “8. POSOLOGIA E MODO DE USAR – subitem Adultos com função renal20 normal”) pelo percentual da dose normal encontrada no nomograma. A dose reduzida deve ser administrada a cada 8 horas.
NOMOGRAMA DA POSOLOGIA REDUZIDA*
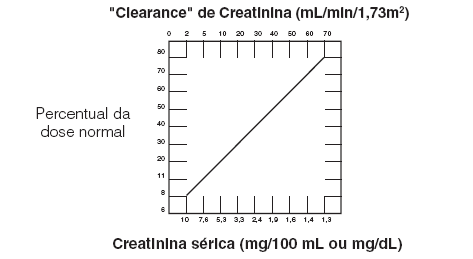
*As escalas foram ajustadas para facilitar os cálculos da dose.
Uma orientação alternativa aproximada para calcular a dose reduzida em pacientes cujos valores de creatinina30 sérica são conhecidos, é dividir a dose normalmente recomendada (indicada no item “8. POSOLOGIA E MODO DE USAR – subitem Adultos com função renal20 normal”) pela creatinina30 sérica do paciente. A dose reduzida deve ser administrada a cada 8 horas.
- Posologia normal em intervalos prolongados: Se o clearance de creatinina30 não estiver disponível e as condições do paciente forem estáveis, calcular a nova frequência das doses (em horas) multiplicando a creatinina30 sérica do paciente por 6.
Pacientes Obesos: A dose pode ser calculada estimando-se um peso ideal para o paciente, acrescido de 40% do excesso de peso. Por exemplo: um paciente com 120 kg, cujo peso ideal fosse 80 kg, terá o cálculo71 de dose como se tivesse 96 kg.
[80 kg + 40% de (120 kg – 80 kg)]
[80 kg + 16 kg = 96 kg]
MODO DE USAR
ATENÇÃO: medicamentos injetáveis devem ser bem inspecionados antes da administração. Se houver partículas, a solução deve ser descartada.
O produto preparado em capela de fluxo unidirecional (laminar) qualificado pode ser armazenado pelos tempos descritos a seguir. Para produtos preparados fora desta condição, recomenda-se o uso imediato.
– VIA INTRAMUSCULAR
Retirar a dose adequada diretamente da ampola.
Administração: injetar imediatamente em uma grande massa muscular, em adultos, nas nádegas72 (quadrante superior externo); em crianças, na face73 lateral da coxa74. A aspiração é necessária para evitar injetar inadvertidamente dentro de um vaso sanguíneo.
– INFUSÃO INTRAVENOSA
Retirar a dose adequada diretamente da ampola e realizar a diluição.
Diluição
- Diluente: Cloreto de Sódio 0,9% ou Glicose75 5%.
- Volume: 50 – 100 mL.
O volume e a concentração final da solução dependem da dose a ser administrada e o volume de diluente utilizado para a diluição.
Aspecto da solução após diluição: solução incolor.
Estabilidade após diluição com Cloreto de Sódio 0,9% ou Glicose75 5%:
Temperatura ambiente (15–30°C): 24 horas.
Tempo de infusão: 20 a 60 minutos.
Incompatibilidades: se clinicamente necessários, aminoglicosídeos e cefalosporinas devem ser administrados em locais separados para evitar uma possível inativação de ambas as substâncias. Não devem ser misturados na mesma seringa76 ou na mesma solução.
REAÇÕES ADVERSAS
Reações comuns (>1% e <10%):
Ototoxicidade47: efeitos adversos sobre os ramos auditivo e vestibular48 do oitavo par craniano (nervo vestibulococlear) foram observados, especialmente em pacientes recebendo altas doses, em tratamentos prolongados, em pacientes que receberam tratamento prévio com um medicamento ototóxico ou em casos de desidratação53. Os sintomas40 incluem: tontura77, vertigem78, zumbidos, rumor nos ouvidos e perda da audição.
A perda da audição geralmente é irreversível e se manifesta inicialmente por diminuição da acuidade para tons altos. A tobramicina e a gentamicina são bastante similares em relação ao potencial ototóxico.
Se um paciente desenvolver perda auditiva, tinido, vertigem78 ou nistagmo79, deve-se interromper a administração do aminoglicosídeo.
Nefrotoxicidade49: alterações da função renal20, evidenciadas por elevação da uremia51, do nitrogênio não proteico, da creatinina30 sérica e por oligúria80, cilindrúria, e aumento da proteinúria81, têm sido relatadas, especialmente em pacientes com história de insuficiência renal65 que foram tratados por períodos longos ou com doses mais altas que as recomendadas.
Efeitos adversos renais podem, entretanto, ocorrer mesmo em pacientes que antes tinham função renal20 normal. Estudos clínicos e com animais foram realizados, comparando os potenciais nefrotóxicos da tobramicina e da gentamicina. Em alguns estudos a tobramicina causou menos nefrotoxicidade49 que a gentamicina. Em outros estudos não foi encontrada diferença significativa entre a tobramicina e a gentamicina.
Reações incomuns (>0,1% e <1%): anemia82, granulocitopenia, trombocitopenia83, leucopenia84, leucocitose85, eosinofilia86, febre87, erupção88 na pele7, dermatite43 esfoliativa, coceira, urticária89, náusea90, vômitos91, diarreia92, cefaleia93, letargia94, dor no local da injeção95, confusão mental e desorientação, aumento das transaminases séricas (AST/TGO, ALT/TGP), aumento da desidrogenase láctica96 sérica e bilirrubinas97, diminuição de cálcio, magnésio, sódio e potássio séricos.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Sinais50 e Sintomas40
A gravidade das manifestações depende da dose administrada, da função renal20, do estado de hidratação, da idade do paciente e de outros medicamentos administrados concomitantemente. A toxicidade9 pode ocorrer em pacientes tratados por mais de 10 dias, em adultos recebendo mais que 5 mg por kg por dia, em pacientes pediátricos recebendo mais que 7,5 mg por kg por dia, ou em pacientes com função renal20 reduzida para os quais as doses não foram adequadamente ajustadas.
A nefrotoxicidade49 parece estar relacionada às concentrações sanguíneas de vale que não caem abaixo de 2 mcg/mL e é também proporcional à concentração sanguínea média. Pacientes idosos, com função renal20 anormal, que estão recebendo outro medicamento nefrotóxico ou com depleção98 de volume, correm maior risco de desenvolver necrose63 tubular aguda.
As toxicidades auditiva e vestibular48 têm sido associadas à superdosagem com aminoglicosídeos. Estas toxicidades ocorrem em pacientes tratados por mais de 10 dias, em pacientes com função renal20 anormal, em pacientes desidratados ou em pacientes recebendo medicamentos com toxicidades auditivas aditivas. Estes pacientes podem não apresentar sinais50 ou sintomas40, ou podem sentir tonturas99, zumbidos, vertigens100 ou perda da acuidade a tons altos, conforme a ototoxicidade47 progride. Os sintomas40 e sinais50 da ototoxicidade47 podem começar após longo período da interrupção do tratamento.
O bloqueio neuromuscular ou a paralisia58 respiratória pode ocorrer após a administração de aminoglicosídeos. Bloqueio neuromuscular, insuficiência respiratória101 e paralisia58 respiratória prolongada podem ocorrer mais frequentemente em pacientes com miastenia61 gravis ou doença de Parkinson102. A paralisia58 respiratória prolongada pode ocorrer também em pacientes recebendo decametônio, tubocurarina ou succinilcolina.
Se a tobramicina for ingerida, a toxicidade9 deve ser bem menor, uma vez que a absorção de aminoglicosídeos é bastante pobre no trato gastrintestinal íntegro.
Tratamento
Quando estiver tratando a superdosagem, considerar a possibilidade de superdoses de medicamentos múltiplos, interação entre medicamentos e/ou uma cinética103 fora do usual no paciente. A conduta inicial é manter o acesso das vias aéreas e assegurar a oxigenação e a ventilação104. Medidas de ressuscitação devem ser iniciadas prontamente se ocorrer a paralisia58 respiratória. Pacientes que receberam uma superdose de tobramicina, e que têm função renal20 normal, devem ser adequadamente hidratados para manter o débito urinário105 de 3 a 5 mL/kg/h. O balanço hídrico, o clearance de creatinina30 e os níveis séricos de tobramicina (concentração de vale) devem ser monitorizados cuidadosamente até que o nível sérico de tobramicina caia abaixo de 2 mcg/mL. Pacientes em que a meia-vida de eliminação for maior que 2 horas, ou aqueles em que a função renal20 for anormal, podem requerer tratamento mais agressivo. Em tais pacientes, a hemodiálise106 pode ser benéfica.
Se o bloqueio neuromuscular ocorrer, o mesmo pode ser revertido pela administração de sais de cálcio, mas o suporte mecânico pode ser necessário.
Em caso de intoxicação ligue para 0800 722 6001 se você precisar de mais orientações sobre como proceder.
Referências Bibliográficas
- Clinical and Laboratory Standards Institute. Performance Standards for Antimicrobial Disk Susceptibility Tests - 10th ed. Approved Standards CLSI Document M2–A10, Vol. 29, Nº 1, CLSI, Wayne, PA, 2009.
- Clinical and Laboratory Standards Institute. Methods for Dilution Antimicrobial Susceptibility Tests for Bacteria107 That Grow Aerobically - 8th ed. Approved Standards CLSI Document M7-A3, Vol. 29, Nº 2, CLSI, Wayne, PA, 2009.
- Clinical and Laboratory Standards Institute. Performance Standards for Antimicrobial Susceptibility Testing - 21st ed. Informational Supplement M100-S21, Vol. 31, Nº 1, CLSI, Wayne, PA, 2011.
- Cockcroft, D. W. and Gault, M. H.: Prediction of Creatinine Clearance from Serum Creatinine, Nephron 16:31-41, 1976.
- Handbook on Injectable Drugs, 16th Edition, 2011, Lawrence A. Trissel, American Society of Health-System Pharmacists.
- Physicians’ Desk Reference, 57th Edition, 2004, Thomson PDR at Montvale, NJ 07645-1742.
- Drug Information for the Health Care Professional – USP DI, 27 th Edition, 2007, Thomson –Micromedex.
- Clinical and Laboratorial studies of Nebcin® - tobramycin sulfate.
- Drug Information 2010 – American Society of Health-System Pharmacists.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
SÓ PODE SER VENDIDO COM RETENÇÃO DA RECEITA
Registro MS nº 1.5562.0010
Farm. Resp.: Sidnei Bianchini Junior - CRF-SP n° 63.058
Fabricado por:
Eurofarma Laboratórios S/A
Rodovia Presidente Castelo Branco, Km 35,6 n° 3565
Bairro Itaqui – Itapevi – São Paulo
Indústria Brasileira
Registrado por:
Antibióticos do Brasil Ltda
Rod. Professor Zeferino Vaz - SP-332, Km 135 – Cosmópolis – SP
CNPJ: 05.439.635/0001-03
Indústria Brasileira
SAC 0800 701 5456