
POSOLOGIA E MODO DE USAR DEPAKENE XAROPE
Convulsões parciais complexas (CPC)
Para adultos e crianças com 10 anos ou mais.
A dose inicial recomendada na monoterapia, conversão para monoterapia ou dose a ser acrescentada no tratamento adjuvante é de 10 a 15 mg/kg/dia, podendo ser aumentada, a cada semana, de 5 a 10 mg/kg/dia, até que se consiga o controle das convulsões. Normalmente a resposta clínica ideal é atingida com doses diárias abaixo de 60 mg/kg/dia. Se não for atingida resposta clínica satisfatória, devem-se medir os níveis plasmáticos para se determinar se eles estão ou não dentro da variação terapêutica1 aceitável (50 a 100 mcg/ml).
Monoterapia (tratamento inicial)
O ácido valproico não foi estudado sistematicamente como tratamento inicial. A probabilidade de ocorrer trombocitopenia2 aumenta significativamente com concentração plasmática total de valproato acima de 110 mcg/ml em mulheres e 135 mcg/ml em homens. O benefício de melhor controle das convulsões com doses mais elevadas deve ser pesado contra a possibilidade de maior incidência3 de reações adversas (ver “5. ADVERTÊNCIAS E PRECAUÇÕES – Trombocitopenia2”).
Conversão para monoterapia
A dose do medicamento antiepilépticos usado concomitantemente, comumente pode ser reduzida em aproximadamente 25% a cada duas semanas. Esta redução pode ser iniciada quando se começa o tratamento com ácido valproico, ou adiada em uma ou duas semanas se existir preocupação com a possibilidade de ocorrerem convulsões com a redução. A velocidade e a duração da retirada do medicamento antiepiléptico concomitante pode ser altamente variável e os pacientes devem ser monitorados durante este período quanto ao aumento da frequência de convulsões.
Tratamento adjuvante
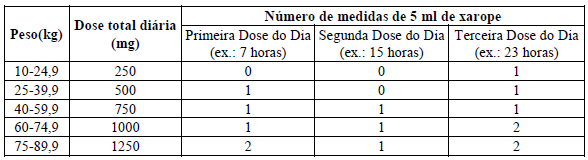
Se a dose total diária exceder 250 mg, ela deve ser administrada de forma fracionada.
Em um estudo de tratamento adjuvante de convulsões parciais complexas, no qual os pacientes estavam recebendo tanto carbamazepina quanto fenitoína além do divalproato sódico, não foi necessário ajuste das doses de carbamazepina ou de fenitoína. Entretanto, considerando que o valproato pode interagir com essas substâncias ou outros antiepilépticos comumente administrados, bem como com outros medicamentos, recomenda-se determinar periodicamente a concentração plasmática dos antiepilépticos concomitantes durante a fase inicial do tratamento (ver “6. INTERAÇÕES MEDICAMENTOSAS”).
Convulsões do tipo ausência simples e complexa
A dose inicial recomendada é de 15 mg/kg/dia, podendo ser aumentada em intervalos semanais, em 5 a 10 mg/kg/dia, até que as convulsões sejam controladas ou até que o aparecimento de efeitos colaterais4 impeça outros aumentos. A dose máxima recomendada é de 60 mg/kg/dia. Se a dose total diária exceder 250 mg, ela deve ser administrada de forma fracionada.
Não foi estabelecida uma boa correlação entre a dose diária, concentrações séricas e efeito terapêutico. Entretanto, as concentrações séricas terapêuticas do valproato para a maioria dos pacientes com convulsões tipo ausência devem variar de 50 a 100 mcg/ml. Alguns pacientes podem ser controlados com concentrações séricas mais baixas ou mais elevadas (ver “3. CARACTERÍSTICAS FARMACOLÓGICAS – Farmacocinética”).
Na medida em que a dose do ácido valproico é titulada para cima, as concentrações sanguíneas do fenobarbital e/ou fenitoína podem ser afetadas (ver “6. INTERAÇÕES MEDICAMENTOSAS”).
Medicamentos antiepilépticos não devem ser descontinuados bruscamente em pacientes nos quais o medicamento é administrado para impedir convulsões maiores, pois existe grande possibilidade de desencadeamento de estado epiléptico com hipóxia5 contínua e risco à vida.
O quadro a seguir é um guia para administração da dose diária inicial de DEPAKENE (valproato
de sódio) 15 mg/kg/dia considerando a administração a cada 8 horas:
Crianças e adolescentes do sexo feminino, mulheres em idade fértil e gestantes
A terapia com ácido valproico deve ser iniciada e supervisionada por um médico especialista no
tratamento de epilepsia6.
O tratamento somente deve ser iniciado se outros tratamentos alternativos forem ineficazes ou não tolerados pelas pacientes e o risco e o benefício devem ser cuidadosamente reconsiderados nas revisões do tratamento. Preferencialmente, o divalproato de sódio deve ser prescrito como monoterapia e na menor dose eficaz, se possível o uso da formulação de liberação prolongada deve ser preferível com o intuito de evitar altos picos de contrações plasmáticas. A dose diária deve ser dividida em, pelo menos, 2 doses individuais.
Recomendações gerais de dosagem
Pacientes idosos: devido a um decréscimo na depuração do valproato não ligado e possivelmente a uma maior sensibilidade à sonolência nos idosos, a dose inicial deverá ser reduzida nesses pacientes. A dosagem deverá ser aumentada mais lentamente e com regular monitorização da ingestão de alimentos e líquidos, desidratação7, sonolência e outros eventos adversos. Reduções de dose ou descontinuação do valproato devem ser consideradas em pacientes com menor consumo de alimentos ou líquidos e em pacientes com sonolência excessiva. A melhor dose terapêutica1 deverá ser alcançada com base na resposta clínica e na tolerabilidade (ver “5. ADVERTÊNCIAS E PRECAUÇÕES”).
Irritação gastrointestinal: pacientes que apresentam irritação gastrointestinal podem ser beneficiados com a administração do medicamento juntamente com a alimentação ou com uma
elevação gradativa da dose a partir de um baixo nível de dose inicial.
Efeitos adversos relacionados à dose: a frequência de efeitos adversos (particularmente a elevação de enzimas hepáticas8 e trombocitopenia2) pode estar relacionada à dose. A probabilidade de trombocitopenia2 parece aumentar significativamente em concentrações totais de valproato maior ou igual a 110 mcg/ml (mulheres) e 135 mcg/ml (homens) (ver “5. ADVERTÊNCIAS E PRECAUÇÕES – Trombocitopenia2”). O benefício de um melhor efeito terapêutico com doses mais altas deve ser avaliado contra a possibilidade de uma maior incidência3 de eventos adversos.
- 9. REAÇÕES ADVERSAS
Epilepsia6
Com base em um ensaio placebo9-controlado de terapia adjuvante para o tratamento de crises parciais complexas, o divalproato foi geralmente bem tolerado, sendo que a maioria dos eventos adversos foi considerada leve a moderada. A intolerância foi a principal razão para a descontinuação nos pacientes tratados com divalproato de sódio (6%), em relação aos pacientes tratados com placebo9 (1%). Como os pacientes foram também tratados com outros medicamentos antiepilépticos, não é possível, na maioria dos casos, determinar se os eventos adversos são associados ao divalproato de sódio somente ou à combinação deste com outros medicamentos antiepilépticos.
Na Tabela 3 são apresentadas as reações adversas relatadas por ≥ 5 % dos pacientes tratados com divalproato de sódio como terapia adjuvante para crises parciais complexas, com incidência3 maior do que no grupo placebo9.
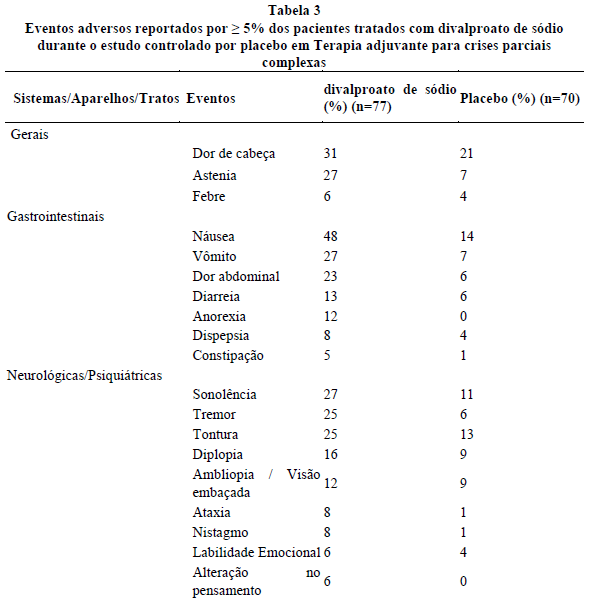

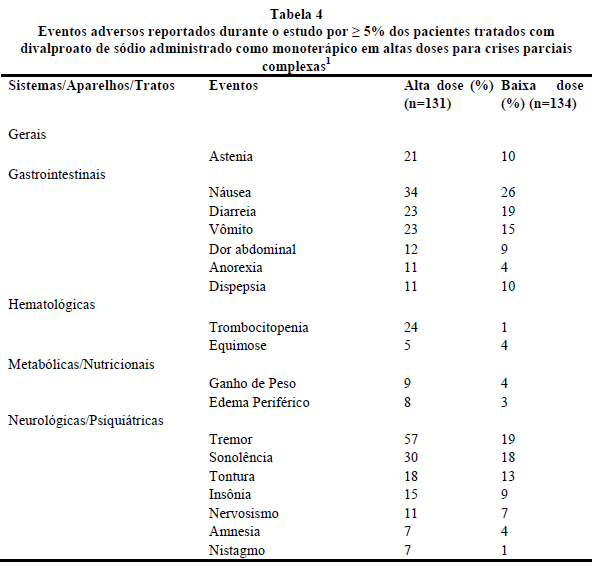
A Tabela 4 lista os eventos adversos ocorridos durante o tratamento emergencial reportados por ≥ 5% dos pacientes que ingeriram altas doses de divalproato de sódio, e para aqueles eventos adversos que ocorreram em maior proporção do que no grupo de baixa dose, em um estudo controlado de divalproato de sódio como monoterapia para crises parciais complexas.
Como os pacientes foram também tratados com outros medicamentos antiepilépticos, não é possível, na maioria dos casos, determinar se os efeitos adversos são associados ao divalproato de sódio somente ou à combinação deste com outros medicamentos antiepilépticos.

Os seguintes eventos adversos foram reportados por mais do que 1%, mas menos que 5% dos 358 pacientes tratados com divalproato de sódio nos estudos controlados para crises parciais complexas:
Gerais: dor nas costas10, dor no peito11 e mal estar.
Cardiovasculares: taquicardia12, hipertensão13 e palpitação14.
Gastrointestinais: aumento do apetite, flatulência, hematêmese15, eructação16, pancreatite17 e abcesso periodontal18.
Hematológicas: petéquia19.
Metabólicas/Nutricionais: AST e ALT aumentadas.
Musculoesqueléticas: mialgia20, contração muscular, artralgia21, cãibra na perna e miastenia22.
Neurológicas/Psiquiátricas: ansiedade, confusão, alteração na marcha, parestesia23, hipertonia24,
incoordenação, alteração nos sonhos e transtorno de personalidade.
Respiratórias: sinusite25, tosse aumentada, pneumonia26 e epistaxe27.
Dermatológicas: rash28 cutâneo29, prurido30 e pele31 seca.
Sensoriais: alteração no paladar32, na visão33 e audição, surdez e otite média34.
Urogenitais: incontinência urinária35, vaginite36, dismenorreia37, amenorreia38 e poliúria39.
Outras Populações de Pacientes
Os eventos adversos que foram relatados com todas as formas de dosagem de valproato em estudos clínicos sobre o tratamento de epilepsia6, ou em relatos espontâneos e de outras fontes, são listados a seguir:
Gastrointestinais: os efeitos colaterais4 mais frequentemente relatados no início do tratamento são náusea40, vômito41 e indigestão. São efeitos usualmente transitórios e raramente requerem interrupção do tratamento. Diarreia42, dor abdominal e constipação43 e distúrbios gengivais (principalmente hiperplasia44 gengival) foram relatados. Tanto anorexia45 com perda de peso, quanto aumento do apetite com ganho de peso também foram relatados. A administração de comprimidos revestidos de divalproato de sódio, de liberação entérica, pode resultar na redução dos eventos adversos gastrointestinais em alguns pacientes.
Obesidade46 foi relatada em raros casos durante a experiência pós-comercialização.
Neurológicas: foram observados efeitos sedativos em pacientes sob tratamento apenas com valproato; porém, esses são mais frequentes em pacientes recebendo terapias combinadas. A sedação47 geralmente diminui com a redução de outros medicamentos antiepilépticos administrados concomitantemente. Tremores (podem ser dose-relacionados), alucinações48, ataxia49, cefaleia50, nistagmo51, diplopia52, asterixis, escotomas53, disartria54, tontura55, confusão, hipoestesia56, vertigem57, incoordenação motora, comprometimento da memória, desordem cognitiva58 e parkinsonismo foram relatados com o uso do valproato. Raros casos de coma59 ocorreram em pacientes recebendo valproato isolado ou em combinação com fenobarbital. Em raros casos, encefalopatia60, com ou sem febre61 desenvolveu-se logo após a introdução da monoterapia com valproato, sem evidência de disfunção hepática62 ou níveis plasmáticos altos inadequados. Embora a recuperação tenha sido descrita após a suspensão do medicamento, houve casos fatais em pacientes com encefalopatia60 hiperamonêmica, particularmente em pacientes com distúrbios do ciclo da ureia63 subjacente (ver “5. ADVERTÊNCIAS E PRECAUÇÕES – Distúrbios do Ciclo da Ureia63 e Hiperamonemia e Encefalopatia60 associada ao uso concomitante de topiramato e Hiperamonemia”).
Houve relatos pós-comercialização de atrofia64 (reversível e irreversível) cerebral e cerebelar, temporariamente associadas ao uso de produtos que se dissociam em íon65 valproato. Em alguns
casos, porém, a recuperação foi acompanhada por sequelas66 permanentes. Foram observados prejuízo psicomotor67 e atraso no desenvolvimento em crianças com atrofia64 cerebral decorrente da exposição ao valproato quando em ambiente intrauterino. Más formações congênitas68 e transtornos de desenvolvimento também foram relatadas (ver “5. ADVERTÊNCIA E PRECAUÇÕES – Atrofia64 Cerebral/Cerebelar”).
Dermatológicas: perda temporária de cabelo69, distúrbios relacionados aos cabelos (como alterações de cor, anormalidades na textura e no crescimento dos cabelos), erupções cutâneas70,
fotossensibilidade, prurido30 generalizado, eritema multiforme71 e síndrome de Stevens-Johnson72. Casos raros de necrólise epidérmica tóxica73 foram relatados, incluindo um caso fatal num lactente74 de seis meses de idade recebendo valproato e vários outros medicamentos concomitantes. Um caso adicional de necrólise epidérmica tóxica73 resultante em óbito75 foi relatado num paciente com 35 anos de idade com AIDS, recebendo vários medicamentos concomitantes e com histórico de múltiplas reações cutâneas70 a medicamento.
Reações cutâneas70 sérias foram relatadas com o uso concomitante de lamotrigina e valproato (ver “6. INTERAÇÕES MEDICAMENTOSAS – Lamotrigina”).
Alterações das unhas76 e leito ungueal77 foram relatadas durante a experiência pós-comercialização.
Psiquiátricas: observaram-se casos de instabilidade emocional, depressão, psicose78, agressividade, hiperatividade psicomotora79, hostilidade, agitação, distúrbio de atenção, comportamento anormal, desordem do aprendizado e deterioração do comportamento.
Musculoesqueléticas: fraqueza - foi verificado em estudos, relatos de diminuição de massa óssea, levando potencialmente a osteoporose80 e osteopenia, durante tratamento por longo período com medicações anticonvulsivantes, incluindo o valproato. Alguns estudos indicaram que o suplemento de cálcio e vitamina81 D pode ser benéfico a pacientes crônicos em terapia com valproato.
Hematológicas: trombocitopenia2 e inibição da fase secundária da agregação plaquetária (ver “5. ADVERTÊNCIAS E PRECAUÇÕES – Geral” e “6. INTERAÇÕES MEDICAMENTOSAS – Varfarina”), que podem ser evidenciadas por alteração do tempo de sangramento, petéquias82, hematomas83, epistaxe27 e hemorragia84. Linfocitose relativa, macrocitose, hipofibrinogenemia, leucopenia85, eosinofilia86, anemia87 incluindo macrocítica com ou sem deficiência de folato, supressão da medula óssea88, pancitopenia89, anemia87 aplástica, agranulocitose90 e porfiria91 aguda intermitente92 foram observadas.
Hepáticas93: são frequentes pequenas elevações de transaminases (AST e ALT) e de DHL, que parecem estar relacionadas às doses. Ocasionalmente, os resultados de exames de laboratório incluem também aumentos de bilirrubina94 sérica e alterações de outras provas de função hepática62.
Tais resultados podem refletir hepatotoxicidade95 potencialmente grave (ver “5. ADVERTÊNCIAS
E PRECAUÇÕES – Hepatotoxicidade95”).
Endócrinas: menstruação96 irregular, amenorreia38 secundária, aumento das mamas97, galactorreia98 e
tumefação99 da glândula parótida100.
Hiperandrogenismo (hirsutismo101, virilismo, acne102, padrão masculino de alopecia103, e/ou aumento no nível de andrógenos104). Testes anormais da função da tireoide105, incluindo hipotireoidismo106 (ver “5. ADVERTÊNCIAS E PRECAUÇÕES – Geral”). Existem raros relatos espontâneos de doença
do ovário107 policístico. A relação causa e efeito não foi estabelecida.
Pancreáticas: foi relatada pancreatite17 aguda em pacientes recebendo valproato, incluindo raros
casos fatais (ver “5. Advertências e Precauções – Pancreatite17”).
Metabólicas: hiperamonemia (ver “5. Advertências e Precauções – Hiperamonemia”), hiponatremia108 e secreção de HAD alterada. Existem raros relatos de síndrome109 de Fanconi ocorrendo principalmente em crianças. Diminuição das concentrações de carnitina também foi observada, embora a relevância clínica deste achado seja desconhecida. Hiperglicinemia (elevada concentração plasmática de glicina) foi associada à evolução fatal em um paciente com hiperglicinemia não cetótica preexistente.
Urogenitais: enurese110, insuficiência renal111, nefrite112 tubulo-intersticial113 e infecção114 do trato urinário115.
Sensoriais: perda auditiva, irreversível ou reversível, foi relatada; no entanto, a relação causa e efeito não foi determinada. Otalgia116 também foi relatada. Neoplásicas117 benignas, malignas e inespecíficas (incluindo cistos e pólipos118): Síndrome109 mielodisplásica.
Respiratórias, torácicas e mediastinais: Efusão119 pleural.
Outras: reação alérgica120, anafilaxia121, edema122 de extremidades, lupus123 eritematoso124, rabdomiólise125, deficiência de biotina/biotinidase, dor nos ossos, tosse aumentada, pneumonia26, otite média34, bradicardia126, vasculite127 cutânea128, febre61 e hipotermia129.
Mania
Apesar da segurança e eficácia do ácido valproico não terem sido avaliadas no tratamento de episódios maníacos associados com distúrbio bipolar, os seguintes eventos adversos não listados anteriormente foram relatados por 1% ou mais dos pacientes em dois estudos clínicos placebocontrolados com divalproato de sódio em comprimidos.
Gerais: calafrios130, dor na nuca e rigidez do pescoço131.
Cardiovasculares: hipotensão132, hipotensão132 postural e vasodilatação.
Gastrointestinais: incontinência fecal133, gastroenterite134 e glossite135.
Musculoesqueléticas: artrose136.
Neurológicas: agitação, reação catatônica, hipocinesia, reflexo aumentado, discinesia tardia137 e
vertigem57.
Dermatológicas: furunculose, erupções maculopapulares e seborreia138.
Sensoriais: conjuntivite139, olho140 ressecado e dor ocular.
Urogenitais: disúria141.
Enxaqueca142
Apesar da segurança e eficácia do ácido valproico não terem sido avaliadas na profilaxia de enxaqueca142, os seguintes eventos adversos não listados anteriormente foram relatados por 1% ou mais dos pacientes em dois estudos clínicos placebo9-controlados com divalproato de sódio em comprimidos.
Gerais: edema122 facial.
Gastrointestinais: boca143 seca, estomatite144.
Urogenitais: cistite145, metrorragia146 e hemorragia vaginal147.
Notificação de suspeitas de reações adversas
Notificar as suspeitas de reações adversas após a aprovação do medicamento é importante, pois permite o monitoramento contínuo do risco-benefício do medicamento. Solicitamos a todos os profissionais de saúde148 que notifiquem qualquer suspeita de reação adversa à empresa e através do sistema de notificações da vigilância sanitária.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.
- 10. SUPERDOSE
Doses de valproato acima do recomendado podem resultar em sonolência, bloqueio cardíaco149, hipotensão132 e colapso150/choque151 circulatório e coma59 profundo. Fatalidades têm sido relatadas; no entanto, os pacientes tem se recuperado de níveis plasmáticos de valproato tão altos quanto 2120 mcg/ml.
A presença de teor de sódio nas formulações de DEPAKENE podem resultar em hipernatremia152
quando administradas em doses acima do recomendado.
Em situações de superdosagem, a fração da substância não ligada à proteína é alta e hemodiálise153 ou hemodiálise153 mais hemoperfusão podem resultar em uma significante remoção da substância. O benefício da lavagem gástrica154 ou emese155 varia com o tempo de ingestão. Medidas de suporte geral devem ser aplicadas, com particular atenção para a manutenção do fluxo urinário.
O uso de naloxona pode ser útil para reverter os efeitos depressores de elevadas doses de valproato sobre o SNC156. Como a naloxona pode teoricamente reverter os efeitos antiepilépticos do valproato, deve ser usada com cautela.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.


