
OUTRAS INTERAÇÕES MEDICAMENTOSAS TOPAMAX
Digoxina: Em um estudo de dose única, a administração concomitante de Topamax® provocou uma redução de 12% na área sob a curva de concentração plasmática (AUC1) da digoxina. A importância clínica desta observação não foi determinada. Quando o Topamax® for associado ou descontinuado em pacientes submetidos a tratamento com a digoxina, recomenda-se atenção à monitoração rotineira e cuidadosa das concentrações séricas de digoxina.
Depressores do SNC2/álcool: Não houve avaliação nos estudos clínicos, da administração concomitante de Topamax® e álcool ou outras drogas depressoras do SNC2. Recomenda-se que Topamax® não seja utilizado concomitantemente com bebidas alcoólicas ou com outros medicamentos depressores do SNC2.
Anticoncepcionais orais: Em um estudo de interação farmacocinética em voluntárias sadias, com administração concomitante de contraceptivo oral combinado contendo 1 mg de noretindrona e 35 mcg de etinilestradiol, Topamax® , administrado isoladamente nas doses de 50 a 200 mg/dia, não foi associado a alterações estatisticamente significantes na exposição média (AUC1) aos componentes do contraceptivo oral. Em outro estudo, a exposição ao etinilestradiol apresentou redução estatisticamente significante com doses de 200, 400 e 800 mg/dia (18%, 21% e 30% respectivamente) quando administrado como adjuvante em pacientes em uso de ácido valpróico. Em ambos os estudos, Topamax® (50 mg/dia a 800 mg/dia) não afetou significantemente a exposição à noretindrona. Entretanto, nas doses entre 200-800 mg/dia, houve uma redução dose-dependente na exposição ao etinilestradiol e, nas doses de 50-200 mg/dia, não houve alteração significante dose-dependente na exposição ao etinilestradiol.
A significância clínica das alterações observadas não é conhecida. A possibilidade de redução da eficácia do contraceptivo e aumento no sangramento de escape deve ser considerada em pacientes em uso de contraceptivos orais combinados e Topamax® . Deve-se solicitar a pacientes em uso de contraceptivos orais que relatem qualquer alteração em seus padrões menstruais. A eficácia contraceptiva pode ser reduzida, mesmo na ausência de sangramento de escape.
Lítio: Em voluntários saudáveis, foi observada uma redução (18% para AUC1) na exposição sistemática para o lítio durante a administração concomitante com topiramato 200 mg/dia. Nos pacientes com transtorno bipolar, a farmacocinética do lítio não foi afetada durante o tratamento com topiramato em doses de 200 mg/dia; entretanto, foi observado aumento na exposição sistêmica (26% para AUC1) depois de doses do topiramato de até 600 mg/dia. Os níveis do lítio devem ser monitorados quando co-administrados com topiramato.
Risperidona: os estudos de interação droga-droga conduzidos sob condições de dose única e múltipla em voluntários saudáveis e em pacientes com transtorno bipolar atingiram resultados similares. Quando administrado concomitantemente com topiramato em doses escaladas de 100, 250 e 400 mg/dia houve uma redução da risperidona (administrada em doses que variando de 1 a 6 mg/dia) na exposição sistêmica (16% e 33% para AUC1 no estado de equilíbrio nas 250 e 400 doses de mg/dia, respectivamente). Alterações mínimas na farmacocinética do total de partes ativas (risperidona mais 9-hidroxirisperidona) e nenhuma alteração para 9-hidroxirisperidona foi observada. Não houve mudança clínica significativamente na exposição sistemica do total de partes ativas da risperidona ou do topiramato, portanto esta interação não é provável ser de significância clínica.
Hidroclorotiazida: Um estudo de interação medicamentosa conduzido em voluntários sadios avaliou a farmacocinética no estado estacionário da hidroclorotiazida (25 mg a cada 24h) e do topiramato (96 mg a cada12h) quando administrados isolada ou concomitantemente. Os resultados deste estudo indicaram que a Cmáx do topiramato aumentou 27% e a AUC1 aumentou 29% quando a hidroclorotiazida foi associada ao topiramato. A significância clínica desta alteração é desconhecida. A associação de hidroclorotiazida ao tratamento com topiramato pode precisar de um ajuste da dose do topiramato. A farmacocinética da hidroclorotiazida no estado estacionário não foi influenciada significativamente pela administração concomitante do topiramato. Os resultados laboratoriais clínicos indicaram redução no potássio sérico após administração do topiramato ou da hidroclorotiazida, sendo maior quando a hidroclorotiazida e o topiramato foram administrados em combinação.
Metformina3: Um estudo de interação medicamentosa conduzido em voluntários sadios avaliou a farmacocinética da metformina3 e do topiramato no estado de equilíbrio no plasma4 quando a metformina3 foi administrada isolada e quando a metformina3 e o topiramato foram administrados simultaneamente. Os resultados do estudo indicaram que a Cmax média e a AUC0-12 h média da metformina3 aumentaram em 18% e 25%, respectivamente, enquanto que o “clearance” médio diminuiu 20% quando a metformina3 foi co-administrada com topiramato. O topiramato não afeta o Tmax da metformina3. A significância clínica do efeito do topiramato na farmacocinética da metformina3 não está clara. O “clearance” plasmático oral do topiramato parece ser reduzido quando administrado com metformina3. A extensão da alteração no “clearance” é desconhecida. A significância clínica do efeito da metformina3 na farmacocinética do topiramato não está clara. Quando Topamax® é administrado ou retirado em pacientes tratados com metformina3, deve-se ter especial atenção na monitorização rotineira para um controle adequado do diabetes5.
Pioglitazona: Um estudo de interação medicamentosa conduzido em voluntários sadios avaliou a farmacocinética no estado estacionário do topiramato e da pioglitazona quando administrados isolada ou concomitantemente. Uma redução de 15% na AUC1, ss de pioglitazona sem alteração na Cmáx, ss foi observada. Este achado não foi estatisticamente significante. Além disso, reduções de 13% na Cmáx, ss e de 16% na AUC1, ss do hidróxi-metabólito6 ativo foram observadas, assim como uma redução de 60% tanto na Cmáx, ss como na AUC1, ss do ceto-metabólito6 ativo foram observadas. A significância clínica destes achados é desconhecida. Quando Topamax® é associado ao tratamento com pioglitazona ou pioglitazona é associada ao tratamento com Topamax® , deve-se ter atenção especial à rotina de monitoramento dos pacientes para um controle adequado do estado diabético.
Gliburida: Um estudo de interação droga-droga conduzido nos pacientes com diabetes tipo 27 avaliou a farmacocinética no estado de equilíbrio da gliburida (5 mg/dia) isolada e concomitantemente com topiramato (150 mg/dia). Houve uma redução de 25% na AUC1 da gliburida durante a administração do topiramato. A exposição sistêmica dos metabolitos8 ativos, 4-trans-hidroxi-gliburida (M1) e 3-cis-hidróxi-gliburida (M2), também foram reduzidas em 13% e 15%, respectivamente. A farmacocinética no estado de equilíbrio do topiramato não foi afetada pela administração concomitante da gliburida. Quando o topiramato é adicionado a terapia da gliburida ou a gliburida é adicionada a terapia do topiramato, deve ser feita uma rotina de monitorização cuidadosa dos pacientes para o controle adequado do estado da sua doença diabética.
Outras Formas de Interação:
Agentes que predispõem à nefrolitíase
Topamax® pode aumentar o risco de nefrolitíase em pacientes em uso concomitante de outros agentes que predispõem à nefrolitíase. Durante o tratamento com Topamax® , tais agentes deverão ser evitados, uma vez que eles criam um ambiente fisiológico9 que aumenta o risco de formação de cálculo10 renal11.
Ácido valpróico
A administração concomitante do topiramato e do ácido valpróico foi associada com hiperamonemia com ou sem encefalopatia12 nos pacientes que toleraram uma ou outra droga isolada. Na maioria dos casos, os sintomas13 e os sinais14 cessaram com a descontinuação de uma ou outra droga. Este evento adverso não é devido a uma interação farmacocinética. Uma associação de hiperamonemia com monoterapia do topiramato ou do tratamento concomitante com outros antiepilépticos não foi estabelecida.
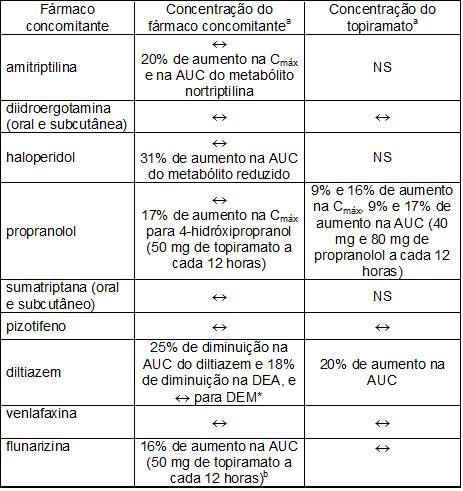
Estudos adicionais de interação medicamentosa farmacocinética: Estudos clínicos foram conduzidos para avaliar a interação medicamentosa farmacocinética potencial entre o topiramato e outros agentes. As alterações na Cmáx e na AUC1 como resultado das interações estão descritas a seguir. A segunda coluna (concentração do fármaco15 concomitante) descreve o que acontece com a concentração do fármaco15 concomitante listado na primeira coluna quando topiramato é associado. A terceira coluna (concentração do topiramato) menciona como a co-administração do fármaco15 listado na primeira coluna modifica a concentração do topiramato.
Resumo dos resultados dos estudos adicionais de interação medicamentosa farmacocinética
Reações Adversas a Medicamentos
Dados de estudos clínicos
A segurança de Topamax® foi avaliada a partir de um banco de dados de estudos clínicos composto de 4.111 pacientes (3.182 tratados com Topamax® e 929 com placebo16) que participaram de 20 estudos duplo-cegos e 2.847 pacientes que participaram de 34 estudos abertos, respectivamente, para o tratamento de convulsões tônico-clônicas generalizadas primárias, convulsões de início parcial, convulsões associadas à síndrome17 de Lennox-Gastaut, epilepsia18 ou enxaqueca19 de diagnóstico20 novo ou recente. As informações apresentadas neste item foram obtidas a partir de dados agrupados.
A maioria das reações adversas foi de gravidade leve a moderada.
Dados de estudos duplo-cegos, controlados por placebo16, de terapia adjuvante para epilepsia18 – Pacientes adultos.
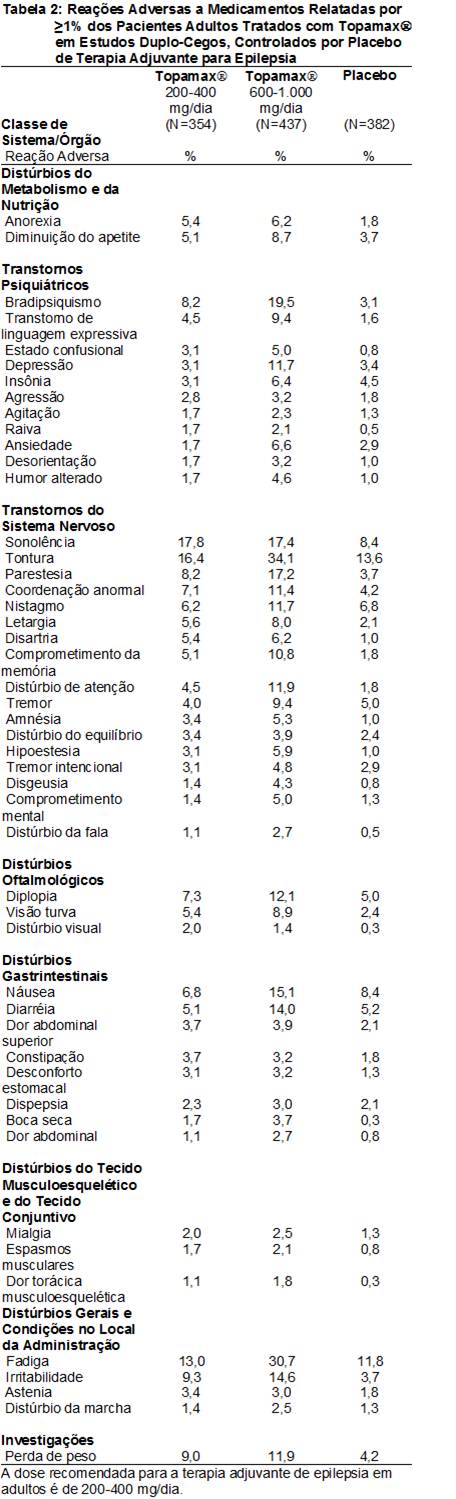
As Reações Adversas a Medicamentos (RAMs) relatadas em ≥1% dos pacientes adultos tratados com o Topamax® em estudos duplo-cegos, controlados por placebo16 de terapia adjuvante para epilepsia18 são apresentadas na Tabela 2. As RAMs com incidência21 >5% no intervalo de dose recomendado (200 a 400 mg/dia) em adultos em estudos duplo-cegos, controlados por placebo16 de terapia adjuvante para epilepsia18 em ordem decrescente de freqüência incluíram sonolência, tontura22, fadiga23, irritabilidade, perda de peso, bradipsiquismo, parestesia24, diplopia25, coordenação anormal, náusea26, nistagmo27, letargia28, anorexia29, disartria30, visão31 turva, diminuição do apetite, comprometimento de memória e diarréia32.
Dados de estudos duplo-cegos, controlados por placebo16, de terapia adjuvante para epilepsia18 – Pacientes pediátricos
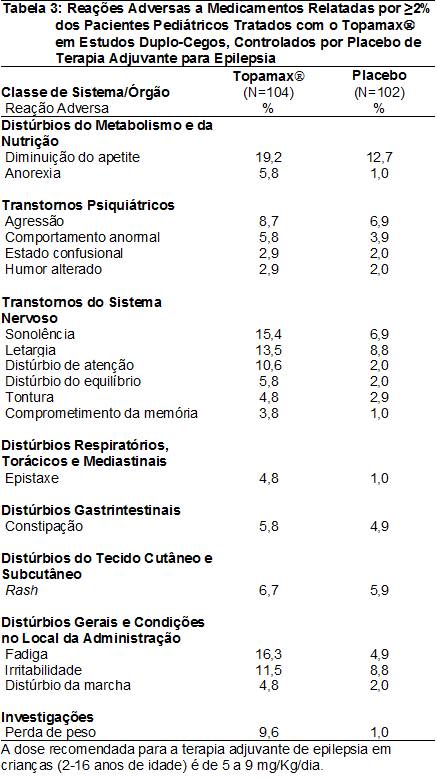
As RAMs relatadas em >2% dos pacientes pediátricos tratados com o Topamax® (2 a 16 anos de idade) em estudos duplo-cegos, controlados por placebo16 de terapia adjuvante para epilepsia18 são apresentadas na Tabela 3. As RAMs com incidência21 >5% no intervalo de dose recomendado (5 a 9 mg/Kg/dia) em ordem decrescente de frequência incluíram diminuição do apetite, fadiga23, sonolência, letargia28, irritabilidade, distúrbio de atenção, perda de peso, agressão, erupção33 cutânea34, comportamento anormal, anorexia29, distúrbio do equilíbrio e constipação35.
Dados dos estudos duplo-cegos, controlados e de monoterapia para epilepsia18 – Pacientes adultos
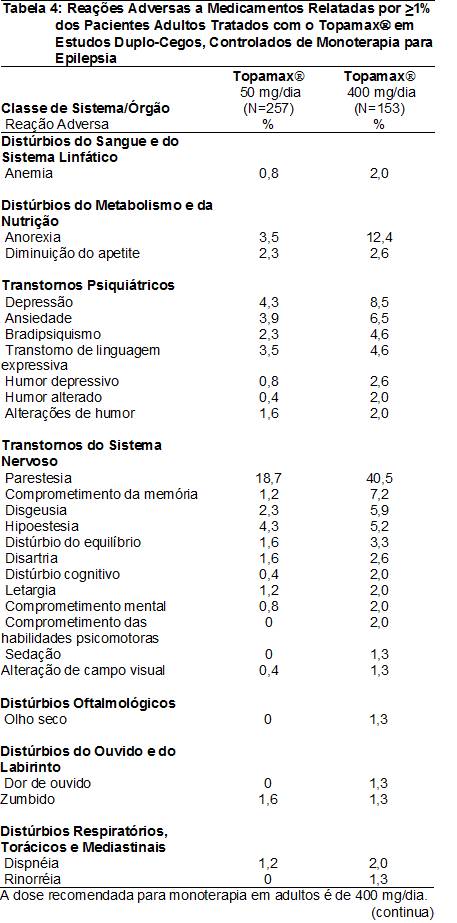
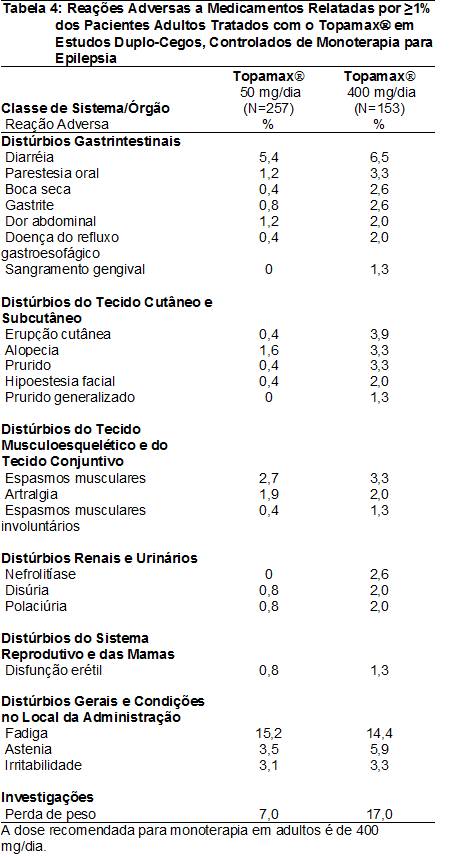
As RAMs relatadas em ≥1% dos pacientes adultos tratados com o TopamaxÒ em estudos duplo-cegos, controlados e de monoterapia para epilepsia18 são apresentadas na Tabela 4. As RAMs que apresentaram incidência21 >5% na dose recomendada (400 mg/dia) em ordem decrescente de freqüência incluíram parestesia24, perda de peso, fadiga23, anorexia29, depressão, comprometimento da memória, ansiedade, diarréia32, astenia36, disgeusia37 e hipoestesia38.
Dados de estudos duplo-cegos, controlados e de monoterapia para epilepsia18 – Pacientes pediátricos
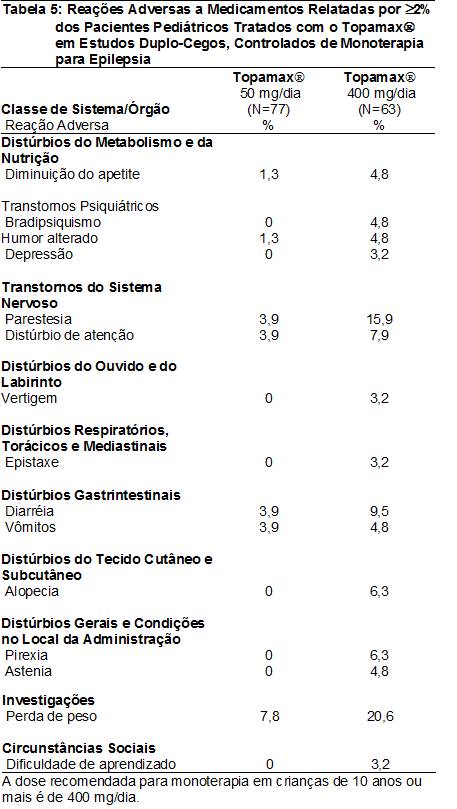
As RAMs relatadas em ≥2% dos pacientes pediátricos tratados com o Topamax® (10 a 16 anos de idade) em estudos duplo-cegos, controlados e de monoterapia para epilepsia18 são apresentadas na Tabela 5. As RAMs com incidência21 >5% na dose recomendada (400 mg/dia) em ordem decrescente de freqüência incluíram perda de peso, parestesia24, diarréia32, distúrbio de atenção, pirexia39, e alopecia40.
Dados de estudos duplo-cegos, controlados por placebo16, de profilaxia de enxaqueca19 – Pacientes adultos
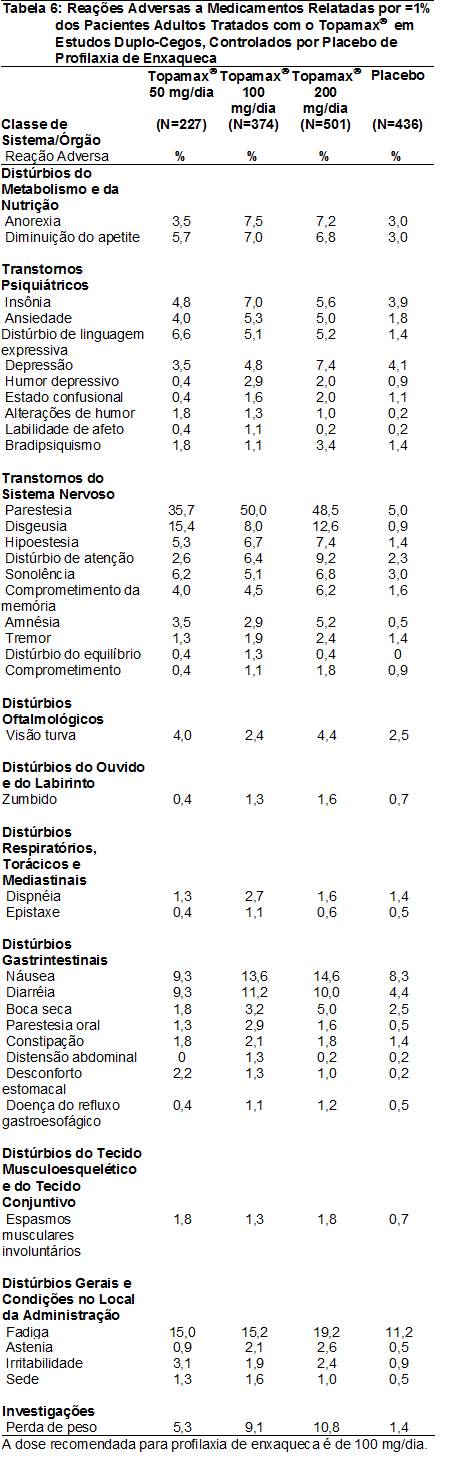
As RAMs relatadas em ≥1% dos pacientes adultos tratados com o Topamax® em estudos duplo-cegos, controlados por placebo16 de profilaxia de enxaqueca19 são apresentadas na Tabela 6. As RAMs com incidência21 >5% na dose recomendada (100 mg/dia) em ordem decrescente de freqüência incluíram parestesia24, fadiga23, náusea26, diarréia32, perda de peso, disgeusia37, anorexia29, diminuição do apetite, insônia, hipoestesia38, distúrbio de atenção, ansiedade, sonolência, e transtorno de linguagem expressiva.
Outros Dados de Estudos Clínicos
As RAMs relatadas em estudos clínicos duplo-cegos controlados em <1% dos pacientes adultos tratados com o Topamax® ou em qualquer taxa em estudos clínicos abertos em pacientes adultos tratados com o Topamax® são apresentadas na Tabela 7.

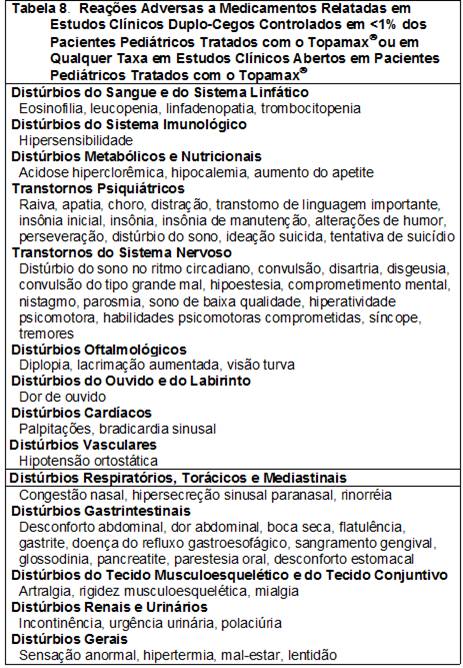
As RAMs relatadas em estudos clínicos duplo-cegos controlados em <1% dos pacientes pediátricos tratados com o Topamax® ou em qualquer taxa em estudos clínicos abertos em pacientes pediátricos tratados com o Topamax® são apresentadas na Tabela 8.
Dados Pós-Comercialização
Os eventos adversos primeiramente identificados como RAMs durante a experiência pós-comercialização com o Topamax® estão mencionados na Tabelas 9. Na tabela, as freqüências são apresentadas de acordo com a seguinte convenção:
| Muito comum | ≥1/10 |
| Comum | ≥1/100 a <1/10 |
| Incomum | ≥1/1.000 a <1/100 |
| Raro | ≥1/10.000 a <1/1.000 |
| Muito raro | <1/10.000, incluindo relatos isolados |

Superdose
Sinais14 e sintomas13
Superdose de topiramato tem sido relatada. Sinais14 e sintomas13 incluem convulsão41, sonolência, distúrbio da fala, visão31 borrada, diplopia25, atividade mental prejudicada, letargia28, coordenação anormal, estupor, hipotensão42, dor abdominal, agitação, vertigem43 e depressão. As conseqüências clínicas não foram graves na maioria dos casos, mas foram relatados casos de óbitos após superdoses com diversas drogas, incluindo o topiramato.
Superdose com topiramato pode resultar em acidose metabólica44 grave (ver item “Precauções e Advertências”).
A maior superdose relatada com topiramato foi calculada em 96-110 g e resultou em coma45 com duração de 20-24 horas seguido de recuperação total após 3 a 4 dias.
Tratamento
Medidas gerais de suporte são indicadas e uma tentativa deve ser feita para remover o fármaco15 não digerido do trato gastrintestinal utilizando lavagem gástrica46 ou carvão ativado. A hemodiálise47 é um método eficaz para a retirada do topiramato do organismo. O paciente deve ser bem hidratado.
Modo de Administrar Topamax® Cápsulas
As cápsulas de Topamax® podem ser tomadas inteiras ou podem ser abertas e seu conteúdo misturado com alimento, de acordo com as instruções abaixo.
 | Você deve espalhar o conteúdo da cápsula de Topamax® sobre uma pequena quantidade (uma colher das de chá) de alimento pastoso como purê de maçã, sorvete, mingau, pudim ou iogurte. |
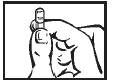 | Segure a cápsula na vertical, com a palavra “TOP” para cima. |
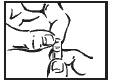 | Torça a porção clara da cápsula com cuidado, de preferência sobre o alimento que será administrado ao paciente. |
 | Espalhe todo o conteúdo da cápsula sobre a colher com o alimento pastoso, certificando-se que a dose prescrita tenha sido adicionada ao alimento. |
 | O alimento contendo o medicamento deve ser ingerido imediatamente, não devendo ser mastigado. A administração de líquidos ao paciente logo após a ingestão irá garantir que a mistura alimento/medicamento seja totalmente deglutida. IMPORTANTE: nunca guarde a mistura para uso posterior. |


