

Firmagon
LABORATÓRIOS FERRING LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Firmagon®
degarelix
Injetável 80 mg e 120 mg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável 120 mg: embalagens com 2 frascos-ampola de pó liofilizado1, 2 seringas com 3,0 mL de diluente, 2 adaptadores de frasco-ampola, 2 agulhas para injeção2 e 2 êmbolos.
Solução injetável 80 mg: embalagens com 1 frasco-ampola de pó liofilizado1, 1 seringa3 com 4,2 mL de diluente, 1 adaptador de frasco-ampola, 1 agulha para injeção2 e 1 êmbolo4.
USO SUBCUTÂNEO5
USO ADULTO
COMPOSIÇÃO:
Cada frasco-ampola de Firmagon® 120 mg contém:
| degarelix | 128 mg* |
| excipiente q.s.p. | 1 frasco-ampola |
Excipiente: manitol.
*É adicionado um excesso do ativo, de modo a garantir a administração da quantidade correta, considerando-se as perdas durante a preparação e administração do produto.
Cada frasco-ampola de Firmagon® 80 mg contém:
| degarelix | 88,2 mg* |
| excipiente q.s.p. | 1 frasco-ampola |
Excipiente: manitol
* É adicionado um excesso do ativo, de modo a garantir a administração da quantidade correta, considerando-se as perdas durante a preparação e administração do produto.
Cada seringa3 com líquido diluente contém: água para injetáveis
INFORMAÇÕES AO PACIENTE
Solicitamos a gentileza de ler cuidadosamente as informações abaixo. Caso não esteja seguro a respeito de determinado item, favor informar ao seu médico.
PARA QUE ESTE MEDICAMENTO É INDICADO?
Firmagon® é destinado ao tratamento de pacientes adultos do sexo masculino com câncer6 de próstata7 avançado dependente de hormônios.
COMO ESTE MEDICAMENTO FUNCIONA?
Firmagon® contém degarelix que é um hormônio8 sintético bloqueador da produção de testosterona utilizado no tratamento de câncer6 de próstata7. O degarelix mimetiza um hormônio8 natural (hormônio8 liberador de gonadotropina, GnRH) e bloqueia diretamente os seus efeitos. Com isso o degarelix reduz imediatamente o nível do hormônio8 masculino testosterona que estimula o câncer6 de próstata7.
O tempo médio para início da ação de Firmagon® é de 2 a 4 horas, pois neste período de tempo já ocorre a diminuição do nível de testosterona. A concentração mais baixa de testosterona ocorre em aproximadamente 24 a 36 horas após a administração de Firmagon®.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Contraindicações
Firmagon® não deve ser utilizado caso a resposta para a pergunta a seguir for “SIM”:
Você possui hipersensibilidade (reação alérgica9) conhecida aos componentes da fórmula?
Este medicamento é contraindicado para uso por crianças. Este medicamento é contraindicado para uso por mulheres.
Este medicamento não deve ser utilizado por mulheres grávidas ou que possam ficar grávidas durante o tratamento.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Advertências e precauções
Informar ao seu médico se você tem qualquer um dos seguintes problemas:
- Problemas com o ritmo cardíaco (arritmia10) ou está em tratamento com medicamentos para esta condição. O risco de problemas com o ritmo cardíaco pode aumentar com o uso de Firmagon®.
- Diabetes11 mellitus. Pode ocorrer a piora ou reestabelecimento da diabetes11, portanto se você tiver diabetes11, deve ser feito o monitoramento da glicose sanguínea12 com maior frequência.
As seguintes condições podem ocorrer com o uso de Firmagon®:
Hipersensibilidade:
Firmagon® não foi estudado em pacientes que apresentem histórico de asma13 severa não tratada, reações anafiláticas14 (reação alérgica9 grave) ou urticária15 severa ou angioedema16 (inchaço17 por baixo da pele18, principalmente na região dos lábios e olhos19).
Alterações na densidade óssea:
A literatura médica reporta casos de diminuição da densidade óssea em homens que sofreram orquiectomia20 (remoção cirúrgica dos testículos21) ou que foram tratados com agonistas de GnRH (hormônio8 liberador de gonadotropina). Pode-se dizer que tratamentos a longo prazo com supressores de testosterona em homens apresentarão efeitos na densidade dos ossos. A densidade óssea não foi avaliada durante tratamento com degarelix.
Devido à ausência de estudos, não é conhecido o risco de fraturas durante o tratamento com degarelix.
Prolongamento do intervalo QT (intervalo específico observado em exames de eletrocardiograma22):
A terapia de supressão de andrógenos23 a longo prazo pode prolongar o intervalo QT. Firmagon® não foi estudado em pacientes com histórico corrigido de intervalo QT acima de 450 mseg, em pacientes com histórico ou que apresentem fatores de risco de “torsades de pointes” (aceleração dos batimentos cardíacos ventriculares, acompanhados de intervalos QT ou QTU prolongados) e em pacientes que estejam recebendo tratamentos com outros medicamentos que possam prolongar o intervalo QT. Portanto, nesses pacientes o médico irá avaliar a razão risco/benefício para o tratamento com Firmagon®.
Tolerância a glicose24:
Uma redução na tolerância a glicose24 foi observada em homens que tiveram orquiectomia20 (remoção cirúrgica dos testículos21) ou que foram tratados com um agonista25 de GnRH (hormônio8 liberador de gonadotropina). Desenvolvimento ou agravamento da diabetes11 pode ocorrer; portanto, pacientes diabéticos podem exigir um monitoramento mais frequente de glicose sanguínea12 quando receberem terapia de privação do androgênio. O efeito de degarelix sobre os níveis de insulina26 e glicose24 não foi estudado.
Cuidados e advertências para populações especiais
Pacientes idosos, com comprometimento hepático ou renal27:
Não há necessidade de se ajustar a dose para idosos ou pacientes com comprometimento leve ou moderado da função hepática28 (do fígado29) ou renal27 (do rim30). Pacientes com comprometimento hepático ou renal27 grave não foram estudados, portanto aconselha-se ter cautela na utilização do produto.
Pacientes que apresentavam suspeita ou confirmação de problemas hepáticos não foram incluídos em estudos com degarelix. É recomendado que o médico monitore a função hepática28 nesses pacientes durante o tratamento com Firmagon®.
Estudos demonstraram que o velocidade com que o organismo elimina o degarelix em pacientes com comprometimento renal27 leve a moderado é reduzido aproximadamente em 20 a 30%. Portanto, o ajuste de doses nesses pacientes não é recomendado. Dados sobre pacientes com comprometimento renal27 grave são escassos, sendo aconselhável ter-se cuidado com essa população de pacientes. Já os pacientes com disfunção hepática28 grave não foram estudados, portanto o médico deve ter cautela com esse grupo.
Efeito na capacidade de dirigir veículos e operar máquinas
Nenhum estudo foi realizado com Firmagon® para avaliar a se existe efeito na capacidade de dirigir veículos ou operar máquinas. Entretanto, como a ocorrência de cansaço e tonturas31 são reações adversas comuns associadas ao tratamento ou são resultantes da doença, estas podem influenciar a capacidade dirigir veículos e operar máquinas.
Interações medicamentosas
Firmagon® pode interferir com alguns medicamentos utilizados no tratamento de problemas do ritmo cardíaco (por exemplo: quinidina, procainamida, amiodarona e sotalol) ou outros medicamentos que tenham efeito no ritmo cardíaco (por exemplo: metadona, cisaprida, moxifloxacino e antipsicóticos).
Interações com alimentos e álcool
Não há dados disponíveis até o momento sobre a interferência de Firmagon® com alimentos e álcool.
Alterações em exames laboratoriais e não laboratoriais
O tratamento com Firmagon® resulta na supressão do sistema pituitário gonadal (glândula32 hipófise33 e testículo34). Os resultados dos testes das funções pituitárias (hipófise33) e gonadais (testículos21) durante e após o tratamento com Firmagon® podem ser alterados.
As seguintes alterações podem ser observadas em pacientes que possuíam valores normais antes do tratamento:
- Valores acentuadamente anormais de enzimas do fígado29 (transaminase hepática28 – ALT, AST e GGT).
- Redução acentuada nos valores hematológicos, hematócritos e hemoglobina35 (resultados dos exames de sangue36).
- Valores acentuadamente anormais de potássio, creatinina37 e ureia38 (substâncias presentes em exames de urina39).
- As alterações nas medições de eletrocardiograma22 (Prolongamento do intervalo QT
- intervalo específico observado em exames cardíacos).
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde40.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Firmagon® deve ser conservado em temperatura ambiente (temperatura entre 15 e 30°C) e em local seco.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Pó liofilizado1: pastilha, branca ou quase branca. Solução injetável: líquido incolor e transparente.
A solução reconstituída deve ser transparente e livre de material não dissolvido. Após a reconstituição, a solução deve ser utilizada imediatamente.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Este medicamento normalmente é administrado por um(a) farmacêutico(a), um(a) enfermeiro(a) ou um(a) médico(a).
O Firmagon® deve ser injetado SOMENTE debaixo da pele18 (administração subcutânea41). Firmagon® NÃO deve ser administrado pela veia (administração intravenosa). Precauções devem ser realizadas para evitar injeção2 acidental na veia. O local de injeção2 deve variar na região abdominal.
As injeções devem ser administradas em áreas em que o paciente não será exposto a pressão, ou seja, não deve ser administrado na região em que é utilizado o cinto ou onde a calça é abotoada ou próximo às costelas42.
Modo de preparo
As instruções para reconstituição devem ser seguidas cuidadosamente. Observação: os frascos não devem ser agitados.
Após a reconstituição, a solução deve ser utilizada imediatamente.
A embalagem de Firmagon® 120 mg contém 2 conjuntos de pó e diluente que devem ser preparados em separado para injeção subcutânea43. Portanto, as instruções abaixo devem ser repetidas uma segunda vez.
|
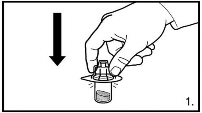 |
1. Remova a embalagem do adaptador de frasco-ampola. Insira o adaptador no frasco-ampola do pó pressionando o adaptador para baixo até que o tampão de borracha seja rompido e o adaptador fique preso. |
|
2. Prepare a seringa3 do diluente inserindo o êmbolo4. |
|
|
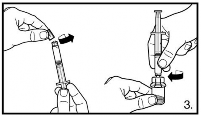 |
3. Remova a tampa da seringa3. Conecte e gire a seringa3 no adaptador do frasco-ampola do pó. Transfira todo o diluente para o frasco do pó. |
|
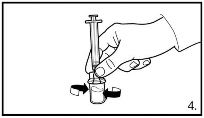 |
4. Com a seringa3 conectada ao adaptador, gire gentilmente até que o líquido fique transparente e sem pó ou partículas não dissolvidas. Caso o pó se prenda ao frasco acima da superfície líquida, o frasco pode ser levemente inclinado. EVITE AGITAR PARA PREVENIR A FORMAÇÃO DE ESPUMA. Um anel de pequenas bolhas de ar sobre a superfície do líquido é aceitável. O procedimento de reconstituição normalmente leva poucos minutos, porém pode demorar até 15 minutos. |
|
 Firmagon® 120 mg
 Firmagon® 80 mg |
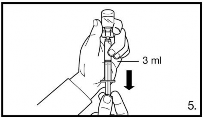
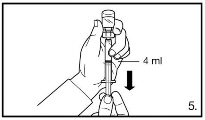
5. Vire o frasco de cabeça44 para baixo e retire a solução até a marca da linha da seringa3 para injeção2.
Tenha sempre certeza de que o volume exato foi retirado e tenha cuidado com a presença de bolhas de ar. |
|
6. Desconecte a seringa3 do adaptador do frasco-ampola e conecte a agulha de segurança para administração subcutânea41 profunda. Realize a administração do produto imediatamente após a reconstituição. |
|
|
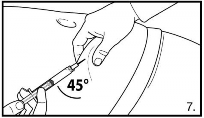 |
7. O produto deve ser administrado por injeção subcutânea43 profunda Aperte a pele18 do abdômen, eleve o tecido subcutâneo45. Insira a agulha profundamente em um ângulo de até 45 graus.
|
|
8. Firmagon 120 mg: Repita o procedimento de reconstituição para a segunda dose. Escolha um local diferente para a injeção2 e injete 3,0 mL. |
|
A reconstituição deve ser feita utilizando o líquido diluente que acompanha a embalagem.
O volume final da solução reconstituída que será administrada de Firmagon® 120 mg é de 3,0 mL e após a reconstituição, cada mL possui 40 mg de degarelix.
O volume final da solução reconstituída que será administrada de Firmagon® 80 mg é de 4,0 mL e após a reconstituição, cada mL possui 20 mg de degarelix.
Posologia
Firmagon® deve ser administrado pela via subcutânea41.
|
Dose inicial |
Dose de manutenção – administração mensal |
|||
|
240 mg administrados com duas injeções subcutâneas de 120 mg cada |
80 mg administrados subcutânea41 com uma injeção2 |
|||
A primeira dose de manutenção deve ser dada um mês após a dose inicial.
A injeção2 do líquido forma um gel em seu organismo que libera continuamente o degarelix por um período de 1 (um) mês.
O médico irá avaliar o efeito terapêutico de degarelix através do monitoramento de parâmetros clínicos e níveis sanguíneos de antígeno46 específico de próstata7 (PSA). Estudos clínicos demonstraram que a supressão da testosterona (T) ocorre imediatamente após a administração da dose inicial com 96% dos pacientes com níveis de testosterona correspondentes a castração47 médica (T?0,5 ng/mL) após três dias e 100% após um mês. O tratamento de longo prazo com a dose de manutenção de até 1 ano demonstra que 97% dos pacientes têm níveis de testosterona suprimidos mantidos (T?0,5 ng/mL).
Caso a reação clínica do paciente pareça abaixo do ideal, deve-se confirmar se os níveis séricos de testosterona permanecem suficientemente suprimidos.
Degarelix não induz a um aumento de testosterona, portanto, não é necessário adicionar um antiandrogênio como proteção contra aumento no início da terapia.
Firmagon® é um medicamento que deve ser administrado mensalmente.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Caso ocorra esquecimento de administração, entrar em contato com o médico.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
As reações adversas mais observadas durante a terapia de degarelix devidas aos efeitos fisiológicos esperados da supressão de testosterona, incluindo rubores e aumento do peso (relatados em 25% e 7%, respectivamente, dos pacientes que receberam tratamento por um ano), ou eventos adversos no local da injeção2.
Os eventos adversos no local da injeção2 relatados foram principalmente dor e eritema48, relatados em 28% e 17% dos pacientes, respectivamente, menos frequentemente relatados foram inchaço17 (6%), enrijecimento (4%) e nódulo49 (3%). Esses eventos ocorreram principalmente com a dose inicial, enquanto durante a terapia de manutenção com dose de 80 mg a incidência50 desses eventos por 100 injeções foi de: 3 para dor e <1 para eritema48, inchaço17, nódulo49 e enrijecimento. Os eventos relatados foram, em sua maioria, transitórios, de intensidade leve a moderada, e levaram a poucas descontinuações (<1%). Reações sérias no local da injeção2 foram muito raramente reportadas, como por exemplo infecção51, abcesso ou necrose52 no local da injeção2, que necessitassem procedimentos cirúrgicos ou drenagem53.
A frequência de efeitos indesejáveis listada abaixo se encontra definida usando-se a seguinte convenção: muito comum (≥ 1/10); comum (≥ 1/100 para <1/10); não-comuns (≥1/1.000 para < 1/100). Dentro de cada grupo de frequência, os efeitos indesejáveis são apresentados em ordem de gravidade decrescente.
|
Classificação Sistema-Órgão – MedDRA |
Muito Comum (≥ 1/10) |
Comum (≥ 1/100 e <1/10); |
Não-comuns (≥1/1.000 para < 1/100) |
|
Distúrbios do Sistema Linfático54 e Sangue36 |
|
|
Queda na hemoglobina35 |
|
Distúrbios do Sistema Imunológico55 |
|
|
Hipersensividade |
|
Distúrbios Psiquiátricos |
|
Insônia |
Perda de Libido56 |
|
Distúrbios do Sistema Nervoso57 |
|
Tontura58, cefaleia59 |
|
|
Distúrbios Vasculares60 |
Rubor |
|
Hipertensão61 |
|
Distúrbios Gastrointestinais |
|
Náusea62, constipação63 |
Diarreia64 |
|
Distúrbios Hepato-biliares |
|
Aumento das Transaminases Hepáticas65 |
|
|
Distúrbios cutâneos e subcutâneos |
|
Suores noturnos |
Urticária15, Hiperidrose66, hiperpigmentação cutânea67 |
|
Distúrbios no Sistema reprodutor e mastológicos |
|
|
Disfunção erétil, atrofia68 testicular, ginecomastia69 |
|
Distúrbios gerais e condições em local de administração |
Eventos adversos no local de administração |
Arrepios, pirexia70, astenia71, fatiga |
Sintomas72 “Flu-like” |
|
Investigações |
|
Aumento de peso* |
|
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião dentista.
O QUE FAZER SE ALGUEM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
A administração de outras concentrações não é recomendada devido a formação do depósito de gel (formulação “depot”).
Em caso de administração de quantidade superior à que foi prescrita pelo médico, entrar em contato com o médico imediatamente.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.2876.0017
Farm. Resp.: Silvia Takahashi Viana – CRF/SP 38.932
Fabricado por (pó):
Ferring GmbH Wittland 11 - D-24109 – Kiel, Alemanha.
Fabricado por (diluente):
Ferring GmbH
Wittland 11 - D-24109 – Kiel, Alemanha.
Embalado por:
Ferring International Center SA – FICSA
Chemin de la Vergognausaz, 1162 - St. Prex, Suíça.
Importado, comercializado e registrado por:
Laboratórios Ferring Ltda.
Praça São Marcos, 624 05455-050 - São Paulo – SP
CNPJ: 74.232.034/0001-48
SAC 0800 772 4656






