Metaxon (Bula do profissional de saúde)
BLAU FARMACÊUTICA S.A.
IDENTIFICAÇÃO DO MEDICAMENTO
METAXON®
fosfato dissódico de dexametasona
APRESENTAÇÕES
Solução injetável 4 mg/mL. Embalagens contendo 1 ou 50 frascos-ampola de 2,5 mL.
VIA DE ADMINISTRAÇÃO: INTRAVENOSA, INTRAMUSCULAR, INTRA-ARTICULAR, INTRALESIONAL1 OU NOS TECIDOS MOLES
USO ADULTO E PEDIÁTRICO
COMPOSIÇÃO
Cada mL da solução injetável contém:
| fosfato dissódico de dexametasona (equivalente a 4 mg de fosfato de dexametasona) | 4,4 mg |
| excipientes (citrato de sódio, hidróxido de sódio, bissulfito de sódio, metilparabeno, propilparabeno, edetato dissódico, creatinina2 e água para injetáveis) q.s.p | 1 mL |
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE3
INDICAÇÕES
Condições nas quais os efeitos anti-inflamatórios e imunossupressores dos corticosteroides são desejados, especialmente para tratamento intensivo durante períodos mais curtos.
Indicações específicas
A. Por injeção4 intravenosa ou intramuscular, quando não seja viável a terapia oral:
Insuficiência5 adrenocortical: Metaxon® (fosfato dissódico de dexametasona) injetável possui atividade predominantemente glicocorticoide, com baixa atividade mineralocorticoide6. Por isso, não constitui terapia completa de substituição e seu uso deve ser suplementado com sal e/ou desoxicorticosterona. Quando assim suplementado, Metaxon® (fosfato dissódico de dexametasona) injetável é indicado na deficiência de toda atividade adrenocortical, como na doença de Addison ou após adrenalectomia7 bilateral, que requer substituição da atividade glicocorticoide e mineralocorticoide6.
Insuficiência5 adrenocortical relativa: na insuficiência5 adrenocortical relativa, que pode ocorrer após a cessação da terapia prolongada com doses supressivas de hormônios adrenocorticais, a secreção mineralocorticoide6 pode estar inalterada. A substituição por hormônio8 que atue predominantemente como glicocorticoide pode ser suficiente para restabelecer a função adrenocortical. Quando é imperativo instituir-se imediata proteção, Metaxon® (fosfato dissódico de dexametasona) injetável pode ser eficaz dentro de minutos após a aplicação e constituir medida capaz de salvar a vida.
Proteção pré e pós-operatória: pacientes submetidos à adrenalectomia7 bilateral ou hipofisectomia ou a qualquer outro procedimento cirúrgico, em que a reserva adrenocortical for duvidosa e no choque9 pós-operatório refratário à terapia convencional10.
Tireoidite não supurativa.
Choque9: Metaxon® (fosfato dissódico de dexametasona) injetável é recomendado para o tratamento auxiliar do choque9, quando se necessitam altas doses (farmacológicas) de corticosteroides como, por exemplo, no choque9 grave de origem hemorrágica11, traumática ou cirúrgica. O tratamento com Metaxon® (fosfato dissódico de dexametasona) injetável é auxiliar e não substituto das medidas específicas ou de apoio que o paciente possa requerer.
Distúrbios reumáticos: como terapia auxiliar na administração a curto prazo (durante episódio agudo12 ou exacerbação) em osteoartrite13 pós-traumática, sinovite14 da osteoartrite13, artrite reumatoide15, incluindo artrite reumatoide15 juvenil (casos selecionados podem requerer terapia de manutenção com baixas doses), bursite16 aguda e subaguda17, epicondilite, tenossinovite aguda inespecífica, artrite18 gotosa aguda, artrite18 psoriática e espondilite anquilosante.
Doença do colágeno19: durante exacerbação ou terapia de manutenção em casos selecionados de “lupus” eritematoso20 disseminado e cardite reumática aguda.
Doenças dermatológicas: pênfigo, eritema21 polimorfo grave (síndrome de Stevens-Johnson22), dermatite23 esfoliativa, dermatite23 herpetiforme bolhosa, dermatite seborreica24 grave, psoríase25 grave e micose26 fungoide.
Estados alérgicos: controle de afecções27 alérgicas graves ou incapacitantes, intratáveis com tentativas adequadas de tratamento convencional, asma28 brônquica, dermatite23 de contato, dermatite23 atópica, doença do soro29, rinites alérgicas perenes ou sazonais, reações de hipersensibilidade a drogas, reações urticariformes por transfusão30, edema31 laríngeo não infeccioso agudo12 e anafilaxia32 (epinefrina é o medicamento de primeira escolha).
Oftalmopatias: graves processos alérgicos e inflamatórios, agudos e crônicos envolvendo os olhos33 e seus anexos34, tais como: conjuntivite35 alérgica, ceratite, úlceras36 marginais corneanas alérgicas, herpes zoster37 oftálmico, irite38, iridociclite, coriorretinite, uveíte39 posterior e coroidite difusas, neurite40 óptica, oftalmia simpática e inflamação41 do segmento anterior do olho42.
Doenças gastrintestinais: para apoiar o tratamento durante o período crítico da doença em colite43 ulcerativa (terapia sistêmica) e enterite regional (terapia sistêmica).
Doenças respiratórias: sarcoidose44 sintomática45, síndrome46 de Loeffler não controlável por outros meios, beriliose47, tuberculose48 pulmonar fulminante ou disseminada, quando simultaneamente acompanhada de quimioterapia49 antituberculosa adequada e pneumonia50 aspirativa. Distúrbios hematológicos: anemia hemolítica51 adquirida (autoimune52), púrpura53 idiopática54 trombocitopênica em adultos (administração somente intravenosa; é contraindicada a via intramuscular), trombocitopenia55 secundária em adultos, eritroblastopenia (anemia56 por deficiência de hemácias57) e anemia56 hipoplástica congênita58 (eritroide).
Doenças neoplásicas59: no tratamento paliativo60 de hipercalcemia associada ao câncer61, leucemias e linfomas do adulto e leucemia62 aguda da infância.
Estados edematosos: para induzir diurese63 ou remissão da proteinúria64 na síndrome nefrótica65 sem uremia66, do tipo idiopático67 ou devido ao “lupus” eritematoso20.
Edema31 cerebral: Metaxon® (fosfato dissódico de dexametasona) injetável pode ser usado para tratar pacientes com edema31 cerebral de várias causas: a) associado com tumores cerebrais primários ou metastáticos, b) associado com neurocirurgia, c) associado com lesão68 craniana ou pseudotumor cerebral, d) associado com acidente vascular cerebral69 (“ictus” cerebral), exceto hemorragia70 intracerebral. Também pode ser utilizado no pré-operatório de pacientes com aumento da pressão intracraniana secundária a tumores cerebrais ou como medida paliativa em pacientes com neoplasias71 cerebrais inoperáveis ou recidivantes72. O uso de Metaxon® (fosfato dissódico de dexametasona) injetável no edema31 cerebral não constitui substituto de cuidadosa avaliação neurológica e tratamento definitivo, tal como neurocirurgia ou outros tratamentos específicos.
Várias: meningite73 tuberculosa com bloqueio subaracnoide ou bloqueio iminente, quando simultaneamente acompanhado por adequada quimioterapia49 antituberculosa, triquinose74 com comprometimento neurológico ou miocárdico.
Prova Diagnóstica da Hiperfunção Adrenocortical
Síndrome46 de sofrimento respiratório neonatal: profilaxia pré-natal. O uso de Metaxon® (fosfato dissódico de dexametasona) injetável em mães com alto risco de parto prematuro mostrou reduzir a incidência75 da síndrome46 de sofrimento respiratório neonatal.
B. Por injeção4 intra-articular ou nos tecidos moles: como terapia auxiliar para administração a curto prazo (para apoio do paciente durante episódio agudo12 ou exacerbação) em sinovite14 da osteoartrite13, artrite reumatoide15, bursite16 aguda e subaguda17, artrite18 gotosa aguda, epicondilite, tenossinovite aguda inespecífica e osteoartrite13 pós-traumática.
C. Por injeção4 intralesional1: queloides, lesões76 inflamatórias localizadas hipertróficas, infiltradas de líquen plano, placas77 psoriáticas, granuloma78 anular e líquen simples crônico79 (neurodermatite), “lupus” eritematoso20 discoide, “Necrobiosis lipoidica diabeticorum”, alopecia areata80. Pode também ser útil em tumores císticos de aponeurose ou tendão81 (gânglios82).
CARACTERÍSTICAS FARMACOLÓGICAS
Fosfato dissódico de dexametasona é um corticosteroide potente, altamente eficaz e versátil, que por ser uma verdadeira solução, pode ser administrado pela via intravenosa, intramuscular, intra-articular ou intrabursal. É um dos mais ativos glicocorticoides, sendo aproximadamente 25 a 30 vezes mais potente do que a hidrocortisona. Em doses anti-inflamatórias equipotentes à dexametasona é quase completamente isenta da propriedade retentora de sódio da hidrocortisona e dos seus derivados intimamente relacionados a ela.
CONTRAINDICAÇÕES
Metaxon® injetável é contraindicado em infecções83 fúngicas84 sistêmicas (vide item Advertências e Precauções: Anfotericina B). Hipersensibilidade a sulfitos ou qualquer outro componente desta medicação. Administração de vacina85 de vírus86 vivo (vide item Advertências e Precauções).
ADVERTÊNCIAS E PRECAUÇÕES
Metaxon® contém bissulfito de sódio, um sulfito que pode provocar reações alérgicas, inclusive sintomas87 de anafilaxia32 e episódios asmáticos com risco de vida ou menos severos em alguns indivíduos suscetíveis. A prevalência88 global de sensibilidade a sulfitos na população em geral é desconhecida e provavelmente baixa. A sensibilidade a sulfito é encontrada mais frequentemente em indivíduos asmáticos do que nos não asmáticos.
Os corticosteroides podem exacerbar as infecções83 fúngicas84 sistêmicas e, portanto, não devem ser usados na presença de tais infecções83, a menos que sejam necessários para o controle de reações medicamentosas devido à anfotericina B. Além disso, foram reportados casos nos quais, o uso concomitante de anfotericina B e hidrocortisona foi seguido de hipertrofia89 cardíaca e insuficiência cardíaca congestiva90. Relatos da literatura sugerem uma aparente associação entre o uso de corticosteroides e ruptura da parede livre do ventrículo esquerdo após infarto91 recente do miocárdio92; portanto, terapia com corticosteroides deve ser utilizada com muita cautela nestes pacientes.
Doses médias e grandes de hidrocortisona ou cortisona podem causar elevação da pressão arterial93, retenção de sal e água e maior excreção de potássio. Tais efeitos são menos prováveis com os derivados sintéticos, salvo quando se utilizam grandes doses. Pode ser necessária a restrição dietética de sal e suplementação94 de potássio. Todos os corticosteroides aumentam a excreção de cálcio.
Insuficiência5 adrenocortical secundária induzida por drogas pode resultar da retirada muito rápida de corticosteroide e pode ser minimizada pela redução posológica gradual. Este tipo de insuficiência5 relativa pode persistir por meses após a cessação do tratamento. Por isso, em qualquer situação de estresse que ocorra durante esse período, deve-se reinstituir a terapia corticosteroide ou aumentar a posologia em uso. Dada a possibilidade de prejudicar-se a secreção mineralocorticoide6, deve-se administrar conjuntamente sal e/ou mineralocorticoide6.
Após terapia prolongada, a retirada dos corticosteroides pode resultar em sintomas87 de síndrome46 da retirada de corticosteroides, compreendendo febre95, mialgia96, artralgia97 e mal-estar. Isso pode ocorrer mesmo em pacientes sem sinais98 de insuficiência5 suprarrenal. Devido à ocorrência de raros casos de reações anafilactoides em pacientes sob tratamento corticosteroide por via parenteral, deve-se tomar medidas de precaução apropriadas antes da administração, especialmente quando o paciente tem antecedentes de alergia99 a qualquer medicamento. A administração de vacinas com vírus86 vivos é contraindicada em indivíduos recebendo doses imunossupressoras de corticosteroides. Se forem administradas vacinas com vírus86 ou bactérias inativadas em indivíduos recebendo doses imunossupressoras de corticosteroides, a resposta esperada de anticorpos100 séricos pode não ser obtida. Entretanto, pode ser feito procedimento de imunização101 em pacientes que estejam recebendo corticosteroides como terapia de substituição como, por exemplo, na doença de Addison.
O uso de Metaxon® (fosfato dissódico de dexametasona) em altas dosagens ou por tempo prolongado pode causar imunossupressão102 semelhante a outros corticosteroides.
Medicamentos imunossupressores podem ativar focos primários de tuberculose48. Os médicos que acompanham pacientes sob imunossupressão102 devem estar alertas quanto à possibilidade de surgimento de doença ativa, tomando, assim, todos os cuidados para o diagnóstico103 precoce e tratamento.
O uso de Metaxon® (fosfato dissódico de dexametasona) injetável na tuberculose48 ativa deve restringir-se aos casos de doença fulminante ou disseminada, em que se usa o corticosteroide para o controle da doença, em conjunção com o tratamento antituberculoso adequado. Se houver indicação de corticosteroides em pacientes com tuberculose48 latente ou reação à tuberculina, torna-se necessária estreita observação, dada a possibilidade de ocorrer reativação da moléstia. Durante tratamento corticosteroide prolongado, esses pacientes devem receber quimioprofilaxia. Os esteroides devem ser utilizados com cautela na colite43 ulcerativa inespecífica, se houver probabilidade de iminente perfuração, abcessos ou outras infecções83 piogênicas, diverticulite104, anastomose105 intestinal recente, úlcera péptica106 ativa ou latente, insuficiência renal107, hipertensão108, osteoporose109 e “miastenia gravis”. Sinais98 de irritação peritoneal, após perfuração gastrintestinal, em pacientes recebendo grandes doses de corticosteroides, podem ser mínimos ou ausentes. Tem sido relatada embolia110 gordurosa como possível complicação do hipercortisolismo. Nos pacientes com hipotireoidismo111 e nos cirróticos há maior efeito dos corticosteroides. Em alguns pacientes os esteroides podem aumentar ou diminuir a motilidade e o número de espermatozoides112. Os corticosteroides podem mascarar alguns sinais98 de infecção113 e novas infecções83 podem aparecer durante o seu uso. Na malária cerebral, o uso de corticosteroides está associado com prolongamento do coma114 e a maior incidência75 de pneumonia50 e hemorragia70 gastrintestinal. Os corticosteroides podem ativar amebíase latente ou estrongiloidíase ou exacerbar a moléstia ativa. Portanto, é recomendado excluir a amebíase latente ou ativa e a estrongiloidíase antes de iniciar a terapia com corticosteroide em qualquer paciente sob o risco ou com sintomas87 sugestivos dessas condições. O uso prolongado dos corticosteroides pode produzir catarata115 subcapsular posterior, glaucoma116 com possível lesão68 do nervo óptico e estimular o desenvolvimento de infecções83 oculares secundárias devidas a fungos ou vírus86. Corticosteroides devem ser usados com cuidado em pacientes com herpes simples oftálmico devido à possibilidade de perfuração corneana. As crianças de qualquer idade, em tratamento prolongado com corticosteroides, devem ser cuidadosamente observadas quanto ao seu crescimento e desenvolvimento. A injeção4 intra-articular de corticosteroide pode produzir efeitos sistêmicos117 e locais. Pronunciado aumento da dor acompanhado de tumefação118 local, maior restrição do movimento articular, febre95 e mal-estar são sugestivos de artrite18 séptica. Se ocorrer esta complicação e confirmar-se o diagnóstico103 de “sepsis”, deve-se instituir terapia antimicrobiana adequada.
Deve-se evitar a injeção4 local de esteroide em área infectada. É necessário o exame adequado de qualquer líquido presente na articulação119, a fim de se excluir processos sépticos. Frequentes injeções intra-articulares podem resultar em dano para os tecidos articulares. Os corticosteroides não devem ser injetados em articulações120 instáveis. Os pacientes devem ser energicamente advertidos sobre a importância de não usarem demasiadamente as articulações120 sintomaticamente beneficiadas enquanto o processo inflamatório permanecer ativo.
Uso na gravidez121 e lactação122: pelo fato de não se terem realizados estudos de reprodução123 humana com corticosteroides, o uso destas substâncias na gravidez121 ou na mulher em idade fértil requer que os benefícios previstos sejam confrontados com os possíveis riscos para a mãe e o embrião ou feto124. Crianças nascidas de mães que receberam durante a gravidez121 doses substanciais de corticosteroides devem ser cuidadosamente observadas quanto a sinais98 de hipoadrenalismo. Os corticosteroides aparecem no leite materno e podem inibir o crescimento, interferir na produção endógena de corticosteroides ou causar outros efeitos indesejáveis. Mães que tomam doses farmacológicas de corticosteroides devem ser advertidas no sentido de não amamentarem.
Categoria de risco na gravidez121: C
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
INTERAÇÕES MEDICAMENTOSAS
O ácido acetilsalicílico deve ser utilizado cautelosamente em conjunção com os corticosteroides na hipoprotrombinemia. A fenitoína, o fenobarbital, a efedrina e a rifampicina podem aumentar a depuração metabólica dos corticosteroides, suscitando redução dos níveis sanguíneos e diminuição de sua atividade fisiológica125, o que exigirá ajuste na sua posologia. Essas interações podem interferir nos testes de supressão da dexametasona, que poderão ser interpretados com cautela durante a administração destas drogas. Foram relatados resultados falsos-negativos no teste de supressão da dexametasona em pacientes tratados com indometacina. O tempo de protrombina126 deve ser verificado frequentemente nos pacientes que estejam recebendo simultaneamente corticosteroides e anticoagulantes127 cumarínicos, dadas as referências de que os corticosteroides têm alterado a resposta a estes anticoagulantes127. Estudos têm mostrado que o efeito usual da adição dos corticosteroides é a inibição da resposta aos cumarínicos, embora tenham havido algumas referências conflitantes de potencialização, não corroborada por estudos.
Quando simultaneamente se administram os corticosteroides e diuréticos128 depletores de potássio, os pacientes devem ser observados estritamente quanto ao desenvolvimento de hipocalemia129. Além disso, os corticosteroides podem afetar os testes de nitroazul tetrazólio (NBT) para infecção113 bacteriana, produzindo resultados falso-negativos. O uso de anticoncepcionais orais pode inibir o metabolismo130 hepático do corticoide. Pela ação hiperglicemiante do Metaxon® (fosfato dissódico de dexametasona) injetável, o uso com hipoglicemiantes orais131 e insulina132 necessita de ajuste de dose de uma ou ambas as drogas.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Metaxon® deve ser mantido em sua embalagem original, em local fresco entre 8°C e 15°C e protegido da luz.
Prazo de validade: 24 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas
Solução límpida, incolor a levemente amarelada, com odor característico, isenta de partículas visíveis.
Antes de usar, observe o aspecto do medicamento.
Todo medicamento deve ser mantido fora do alcance das crianças.
POSOLOGIA E MODO DE USAR
Metaxon® (fosfato dissódico de dexametasona) injetável é apresentado na seguinte concentração: solução injetável 4 mg/mL - cada mL contém 4 mg de fosfato de dexametasona.
Este produto, como muitas outras preparações contendo esteroides, são sensíveis ao calor. Portanto, quando se deseja esterilizar externamente a ampola, não se deve autoclavá-la. Proteger contra o congelamento. Esta preparação pode ser retirada diretamente da ampola para aplicação, sem necessidade de mistura ou diluição. Ou se preferido, pode ser adicionada a solução fisiológica125 ou glicosada, sem perda de potência, e administrado gota133 a gota133 por via intravenosa. Soluções utilizadas para administração intravenosa, ou diluição posterior deste produto, não devem conter preservativos quando usadas no neonato134, especialmente na criança prematura.
Quando Metaxon® (fosfato dissódico de dexametasona) é adicionado à solução de infusão intravenosa, a mistura deve ser utilizada imediatamente, pois soluções de infusão não contém conservantes. Devem observar-se as técnicas de assepsia135 usualmente indicadas para injeções.
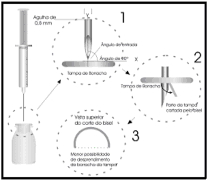
Com a finalidade de evitar o aparecimento de partículas de borracha após a inserção de agulha no frasco-ampola, proceder da seguinte forma:
- Encaixar uma agulha de injeção4 de no máximo 0,8 mm de calibre;
- Segurar a seringa136 verticalmente à borracha;
- Perfurar a tampa dentro da área marcada, deixando o frasco-ampola firmemente na posição vertical;
- É recomendado não perfurar mais de 4 vezes a área demarcada (ISO 7864).
Veja abaixo o procedimento:
Injeção4 Intravenosa e Intramuscular - a posologia inicial de Metaxon® (fosfato dissódico de dexametasona) usualmente utilizada pode variar de 0,5 a 20 mg por dia, dependendo da doença específica a ser tratada. Geralmente, a faixa posológica parenteral é um terço ou a metade da dose oral, dada a cada 12 horas. Entretanto, em certas situações agudas, desesperadoras, com risco de vida, foram administradas doses maiores do que as recomendadas. Nestas circunstâncias, deve-se ter em mente que a absorção é mais lenta pela via intramuscular. DEVE SER RESSALTADO QUE AS EXIGÊNCIAS POSOLÓGICAS SÃO VARIÁVEIS E DEVEM SER INDIVIDUALIZADAS COM BASE NA DOENÇA A SER TRATADA E NA RESPOSTA DO PACIENTE. Se o uso do medicamento tiver que ser suspenso depois de administrado durante alguns dias, recomenda-se fazê-lo gradual e não subitamente. Em emergências, a dose usual de Metaxon® (fosfato dissódico de dexametasona) para injeção4 intravenosa (IV) ou intramuscular (IM) é de 1 a 5 mL (4 a 20 mg): no choque9 deve ser utilizada apenas a via IV. Esta dose pode ser repetida até observar-se resposta adequada. Após melhora inicial, doses únicas de 0,5 a 1,0 mL (2 a 4 mg) devem ser repetidas segundo as necessidades.
A posologia total diária geralmente não precisa exceder 20 mL (80 mg), ainda que se trate de afecção137 grave. Quando se deseja efeito máximo e constante, a posologia deve ser repetida com intervalos de três a quatro horas, ou mantidas gota133 a gota133 por via IV lenta. As injeções intravenosas e intramusculares são aconselhadas nas doenças agudas. Uma vez superada a fase aguda, e tão logo seja possível, substitui-se as injeções pela terapia esteroide por via oral.
Choque9 (de origem hemorrágica11, traumática ou cirúrgica): a dose usual é de 2 a 6 mg/kg de peso corpóreo, dada de uma só vez, em injeção4 intravenosa. Pode ser repetida após 2 a 6 horas, se o choque9 persistir. Como alternativa administram-se de uma só vez 2 a 6 mg/kg de peso corpóreo de Metaxon® (fosfato dissódico de dexametasona) em injeção4 intravenosa, seguida imediatamente pela mesma dose em gotejamento intravenoso.
A terapia com Metaxon® (fosfato dissódico de dexametasona) é auxiliar e não substituta da terapia convencional10 (vide item Advertências e Precauções).
A administração de terapia corticosteroide em altas doses deve ser continuada apenas até que a condição do paciente tenha se estabilizado, o que usualmente não vai além de 48 a 72 horas.
Edema31 cerebral: associado com tumor138 cerebral primário ou metastático, neurocirurgia, trauma craniano, pseudotumor cerebral ou no pré- operatório de pacientes com aumento da pressão intracraniana secundária a tumor138 cerebral: inicialmente 10 mg (2,5 mL) de Metaxon® (fosfato dissódico de dexametasona) pela via intravenosa, seguidos de 4 mg (1 mL) pela via intramuscular a cada 6 horas, até cederem os sintomas87 do edema31 cerebral.
Usualmente, nota-se a resposta dentro de 12 a 24 horas; após 2 a 4 dias pode-se reduzir gradualmente a posologia até cessar a administração no período de 5 a 7 dias. Altas doses de Metaxon® (fosfato dissódico de dexametasona) são recomendadas para iniciar terapia intensiva139 a curto prazo do edema31 cerebral agudo12, com risco de vida. Após o esquema posológico “de ataque” do primeiro dia de tratamento, a posologia é reduzida gradualmente durante o período de 7 a 10 dias, e a seguir, reduzida a zero nos próximos 7 a 10 dias. Quando se requer terapia de manutenção, deve-se passar para fosfato dissódico de dexametasona oral, tão logo seja possível.
Sugestão de esquema posológico em altas doses no edema31 cerebral (vide Quadro abaixo).
Esquema de altas doses proposto para edema31 cerebral
|
Dose inicial |
Adultos 50 mg IV |
Crianças (35 kg ou mais) 25 mg IV |
Crianças (menos de 35 kg) 20 mg |
|
1º dia |
8 mg IV a cada 2 horas |
4 mg IV a cada 2 horas |
4 mg IV a cada 3 horas |
|
2º dia |
8 mg IV a cada 2 horas |
4 mg IV a cada 2 horas |
4 mg IV a cada 3 horas |
|
3º dia |
8 mg IV a cada 2 horas |
4 mg IV a cada 2 horas |
4 mg IV a cada 3 horas |
|
4º dia |
4 mg IV a cada 2 horas |
4 mg IV a cada 4 horas |
4 mg IV a cada 6 horas |
|
5º - 8º dia |
4 mg IV a cada 4 horas |
4 mg IV a cada 6 horas |
2 mg IV a cada 6 horas |
|
Após este período |
reduzir 4 mg diariamente |
reduzir 2 mg diariamente |
reduzir 1 mg diariamente |
No controle paliativo60 de pacientes com tumores cerebrais recidivantes72 ou inoperáveis: o tratamento de manutenção deve ser individualizado com Metaxon® (fosfato dissódico de dexametasona). A posologia de 2 mg, 2 a 3 vezes por dia, pode ser eficaz.
Associado com acidente vascular cerebral69 agudo12 (excluindo hemorragia70 intracerebral): inicialmente 10 mg (2,5 mL) de Metaxon® (fosfato dissódico de dexametasona) pela via intravenosa, seguidos de 4 mg pela via intramuscular a cada 6 horas, durante 10 dias. Nos 7 dias subsequentes, as doses devem ser gradualmente ajustadas até chegar a zero.
Deve-se utilizar a menor posologia necessária para o edema31 cerebral.
Terapia combinada140: nos distúrbios alérgicos agudos autolimitados ou nos surtos agudos dos distúrbios alérgicos crônicos (por exemplo: rinites alérgicas agudas, acessos de asma28 brônquica alérgica sazonal, urticária141 medicamentosa e dermatose142 de contato), sugere-se o seguinte esquema posológico combinando as terapias parenteral e oral:
1º dia: injeção intramuscular143 de 1 ou 2 mL (4 ou 8 mg) de Metaxon®. Posologia total diária: 4 ou 8 mg.
2º dia: 2 comprimidos de 0,5 mg de fosfato dissódico de dexametasona, duas vezes por dia. Posologia total diária: 4 comprimidos.
3º dia: 2 comprimidos de 0,5 mg fosfato dissódico de dexametasona, duas vezes por dia. Posologia total diária: 4 comprimidos.
4º dia: 1 comprimido de 0,5 mg de fosfato dissódico de dexametasona, duas vezes por dia. Posologia total diária: 2 comprimidos.
5º dia: 1 comprimido de 0,5 mg de fosfato dissódico de dexametasona, duas vezes por dia. Posologia total diária: 2 comprimidos.
6º dia: 1 comprimido de 0,5 mg de fosfato dissódico de dexametasona, por dia. Posologia total diária: 1 comprimido.
7º dia: 1 comprimido de 0,5 mg de fosfato dissódico de dexametasona, por dia. Posologia total diária: 1 comprimido.
8º dia: exame clínico de controle.
Injeções intra-articulares, intralesionais e nos tecidos moles: as injeções intra-articulares, intralesionais e nos tecidos moles geralmente são utilizadas quando as articulações120 ou áreas afetadas limitam-se a um ou dois locais.
Eis algumas das doses únicas usuais:
|
Local da injeção4 |
Volume da injeção4 (mL) |
Quantidade de fosfato |
|
Grandes articulações120 (por ex. joelho) |
0,5 a 1 |
2 a 4 |
|
Pequenas articulações120 (por ex. |
0,2 a 0,25 |
0,8 a 1 |
|
Bolsas sinoviais144 |
0,5 a 0,75 |
2 a 3 |
|
Bainhas tendinosas |
0,1 a 0,25 |
0,4 a 1 |
|
Infiltração nos tecidos |
0,5 a 1,5 |
2 a 6 |
|
Gânglios82 (cistos) |
0,25 a 0,5 |
1 a 2 |
A frequência da injeção4 varia desde uma vez, cada 3 a 5 dias, até uma vez, cada 2 a 3 semanas, dependendo da resposta ao tratamento.
Síndrome46 de sofrimento respiratório neonatal: profilaxia pré-natal.
A posologia recomendada de Metaxon® (fosfato dissódico de dexametasona) é de 5 mg (1,25 mL), administrado por via intramuscular na mãe cada 12 horas até o total de quatro doses. A administração deve ser iniciada de preferência entre 24 horas a sete dias antes da data estimada do parto.
Pacientes idosos
As mesmas orientações dadas aos adultos devem ser seguidas para os pacientes idosos, observando-se as recomendações específicas para grupos de pacientes descritos nos itens Advertências e Precauções e Contraindicações.
REAÇÕES ADVERSAS
Distúrbios hidroeletrolíticos: retenção de sódio, retenção de líquido, insuficiência cardíaca congestiva90 em pacientes suscetíveis, perda de potássio, alcalose145 hipocalêmica e hipertensão108.
Musculoesqueléticos: fraqueza muscular, miopatia146 esteroide, perda de massa muscular, osteoporose109, fraturas por compressão vertebral, necrose147 asséptica das cabeças femorais e umerais, fratura148 patológica dos ossos longos149 e ruptura de tendão81.
Gastrintestinais: úlcera péptica106 com eventual perfuração e hemorragia70, perfuração de intestino grosso150 e delgado, particularmente em pacientes com doença intestinal inflamatória, pancreatite151, distensão abdominal e esofagite152 ulcerativa.
Dermatológicos: retardo na cicatrização de feridas, adelgaçamento e fragilidade da pele153, petéquias154 e equimoses155, eritema21, hipersudorese, pode suprimir as reações aos testes cutâneos, ardor156 ou formigamento, mormente na área perineal (após injeção4 intravenosa). Outras reações cutâneas157, tais como dermatite23 alérgica, urticária141 e edema angioneurótico158.
Neurológicos: convulsões, aumento da pressão intracraniana com papiledema (pseudotumor cerebral), geralmente após tratamento, vertigem159, cefaleia160 e distúrbios psíquicos.
Endócrinos: irregularidades menstruais, desenvolvimento de estado síndrome de cushing161, supressão do crescimento da criança, ausência da resposta secundária adrenocortical e hipofisária, particularmente por ocasião de situação estressante, tais como traumas, cirurgias ou enfermidades, diminuição da tolerância aos carboidratos, manifestação do diabete melito latente, aumento das necessidades de insulina132 ou de agentes hipoglicemiantes orais131 no diabete e hirsutismo162.
Oftálmicos: catarata115 subcapsular posterior, aumento da pressão intra-ocular, glaucoma116 e exoftalmo.
Metabólicos: balanço nitrogenado negativo devido ao catabolismo163 proteico.
Cardiovasculares: ruptura do miocárdio92 após infarto91 recente do miocárdio92, cardiomiopatia hipertrófica em crianças nascidas abaixo do peso (vide item Precauções e Advertências).
Outros: reações anafilactoides ou de hipersensibilidade, tromboembolia, ganho de peso, aumento de apetite, náusea164, mal-estar, soluços. As seguintes reações adversas adicionais são relacionadas com o tratamento corticosteroide parenteral: raros casos de cegueira associados com tratamento intralesional1 na região da face165 e da cabeça166, hiperpigmentação ou hipopigmentação, atrofia167 subcutânea168 e cutânea169, abscesso170 estéril, fogacho após injeção4 (em seguida ao uso intra-articular), artropatia171 do tipo charcot.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.
SUPERDOSE
São raros os relatos de toxicidade172 aguda e/ou morte por superdosagem de glicocorticoides. Para a eventualidade de ocorrer superdosagem não há antídoto173 específico, o tratamento é de suporte e sintomático174.
A DL 50 intravenosa de fosfato dissódico de dexametasona em camundongos fêmeas foi de 794 mg/kg.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
Venda sob prescrição médica
Farm. Resp.: Eliza Yukie Saito - CRF-SP n° 10.878
Reg. MS. nº 1.1637.0116
Registrado por:
Blau Farmacêutica S.A.
Rodovia Raposo Tavares Km 30,5 - nº 2833 - Prédio 100
CEP 06705-030 - Cotia – SP
CNPJ 58.430.828/0001-60
Indústria Brasileira
Fabricado por:
Blau Farmacêutica S.A.
Rua Adherbal Stresser, 84
CEP 05566-000 – São Paulo – SP
CNPJ 58.430.828/0013-01
Indústria Brasileira
SAC 0800 7016399