Ozempic (Bula do profissional de saúde)
NOVO NORDISK FARMACÊUTICA DO BRASIL LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Ozempic®
semaglutida
Injetável 0,25 mg e 0,5 mg - Sistema de Aplicação 1,5 mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável em sistema de aplicação preenchido (multidose e descartável)
Embalagens contendo 1 sistema de aplicação preenchido e 6 agulhas descartáveis NovoFine® Plus contendo 1,5 mL.
VIA SUBCUTÂNEA1
USO ADULTO
COMPOSIÇÃO:
Cada mL de Ozempic® contém:
| semaglutida | 1,34 mg |
| veículo q.s.p. | 1 mL |
Veículo: fosfato de sódio dibásico di-hidratado, propilenoglicol, fenol, ácido clorídrico2 (ajuste de pH), hidróxido de sódio (ajuste de pH) e água para injetáveis.
A semaglutida é um agonista3 do receptor de GLP-1 (peptídeo símile ao glucagon4 1 humano) produzido em células5 Saccharomyces cerevisiae por tecnologia de DNA recombinante.
Um sistema de aplicação preenchido contém 2 mg de semaglutida em 1,5mL.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE6
INDICAÇÕES
Ozempic® é indicado para o tratamento de adultos com diabetes mellitus7 tipo 2 insuficientemente controlado, como adjuvante à dieta e exercício:
- em monoterapia, quando a metformina8 é considerada inapropriada devido a intolerância ou contraindicações;
- em adição a outros medicamentos para o tratamento do diabetes9.
- Para informação sobre os resultados de estudos relativos às associações, efeitos sobre o controle glicêmico e eventos cardiovasculares e as populações estudadas ver item “2. Resultados de Eficácia”.
RESULTADOS DE EFICÁCIA
Tanto a melhora do controle glicêmico como a redução da morbidade10 e mortalidade11 cardiovascular são partes integrantes do tratamento do diabetes mellitus7 tipo 2.
A eficácia e segurança de Ozempic® 0,5 mg e 1,0 mg, uma vez por semana, foram avaliadas em seis estudos de fase 3a, randomizados e controlados, que incluíram 7.215 pacientes com diabetes mellitus7 tipo 2 (4.107 pacientes foram tratados com Ozempic®). Desses, cinco estudos (SUSTAIN 1-5) tiveram a avaliação de eficácia glicêmica como desfecho primário, enquanto um estudo (SUSTAIN 6) teve o resultado cardiovascular como o desfecho primário.
Um estudo adicional (SUSTAIN 7) de fase 3b, incluindo 1.201 pacientes, foi realizado para comparar a eficácia e a segurança de Ozempic® 0,5 mg e 1,0 mg, uma vez por semana, em relação a dulaglutida 0,75 mg e 1,5 mg uma vez por semana, respectivamente. O tratamento com Ozempic® demonstrou reduções sustentadas, clinicamente significativas e estatisticamente superiores na HbA1c12 e no peso corporal por até 2 anos em comparação ao tratamento com placebo13 e controle ativo (sitagliptina, insulina glargina14, exenatida e dulaglutida).
A eficácia de Ozempic® não foi impactada por idade, sexo, raça, etnia, IMC15 basal, peso corporal basal (kg), duração do diabetes9 e nível de comprometimento da função renal16.
SUSTAIN 1 - Monoterapia
Em um estudo duplo cego17 placebo13 controlado de 30 semanas, 388 pacientes inadequadamente controlados com dieta e exercícios foram randomizados para receber Ozempic® 0,5 mg ou Ozempic® 1,0 mg, uma vez por semana, ou placebo13.
Tabela 1 – SUSTAIN 1: Resultados na semana 30
|
|
Ozempic® 0,5 mg |
Ozempic® 1,0 mg |
Placebo13 |
|
População intenção de tratar - ITT (N) |
128 |
130 |
129 |
|
HbA1c (%) |
|
|
|
|
Basal (média) |
8,1 |
8,1 |
8,0 |
|
Alteração a partir do basal na semana 30 |
-1,5 |
-1,6 |
0 |
|
Diferença do placebo13 [95% IC] |
-1,4 [-1,7; -1,1]a |
-1,5 [-1,8; -1,2]a |
- |
|
Pacientes (%) atingindo HbA1c <7% |
74 |
72 |
25 |
|
GPJ (mmol/L18) (mg/dL19) |
|||
|
Basal (média) |
9,7 (174,8 mg/dL19) |
9,9 (178,4 mg/dL19) |
9,7 (174,8 mg/dL19) |
|
Alteração a partir do basal na semana 30 |
-2,5 (-45,0 mg/dL19) |
-2,3 (-41,4 mg/dL19) |
-0,6 (-10,8 mg/dL19) |
|
Peso corporal (kg) |
|||
|
Basal (média) |
89,8 |
96,9 |
89,1 |
|
Alteração a partir do basal na semana 30 |
-3,7 |
-4,5 |
-1,0 |
|
Diferença de placebo13 [95% IC] |
-2,7 |
-3,6 |
- |
a valor p <0,0001 (bilateral) para superioridade
SUSTAIN 2 – Ozempic® versus sitagliptina, ambos em combinação com 1-2 medicamentos antidiabéticos orais20 (metformina8 e/ou tiazolidinedionas)
Em um estudo duplo-cego17 ativo-controlado de 56 semanas, 1.231 pacientes foram randomizados para receber Ozempic® 0,5 uma vez por semana, Ozempic® 1,0 mg uma vez por semana ou 100 mg de sitagliptina uma vez ao dia, todos em associação com metformina8 (94%) e /ou tiazolidinedionas (6%).
Tabela 2 – SUSTAIN 2: Resultados na semana 56
|
|
Ozempic® 0,5 mg |
Ozempic® 1,0 mg |
sitagliptina 100 mg |
|
População intenção de tratar - ITT (N) |
409 |
409 |
407 |
|
HbA1c (%) |
|
|
|
|
Basal (média) |
8,0 |
8,0 |
8,2 |
|
Alteração a partir do basal na semana 56 |
-1,3 |
-1,6 |
-0,5 |
|
Diferença de sitagliptina [95% IC] |
-0,8 |
-1,1 |
- |
|
Pacientes (%) atingindo HbA1c <7% |
69 |
78 |
36 |
|
GPJ (mmol/L18) (mg/dL19) |
|||
|
Basal (média) |
9,3 (167,6 mg/dL19) |
9,3 (167,6 mg/dL19) |
9,6 (173,0 mg/dL19) |
|
Alteração a partir do basal na semana 56 |
-2,1 (-37,8 mg/dL19) |
-2,6 (-46,8 mg/dL19) |
-1,1 (-19,8 mg/dL19) |
|
Peso corporal (kg) |
|||
|
Basal (média) |
89,9 |
89,2 |
89,3 |
|
Alteração a partir do basal na semana 56 |
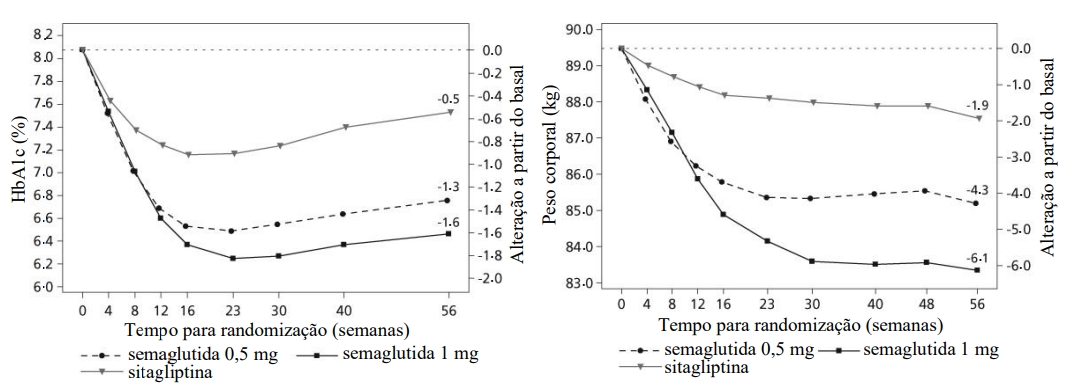
-4,3 |
-6,1 |
-1,9 |
|
Diferença de sitagliptina |
-2,3 |
-4,2 |
- |
|
|
|
|
|
a valor p <0,001 (bilateral) para superioridade
Figura 1. Alteração média na HbA1c12 (%) e no peso corporal (kg) desde o basal até a semana 56
SUSTAIN 3 – Ozempic® versus exenatida liberação prolongada, ambos em combinação com metformina8 ou metformina8 com sulfonilureia
Em um estudo aberto de 56 semanas, 813 pacientes recebendo somente metformina8 (49%), metformina8 com sulfonilureia (45%) ou outro (6%) foram randomizados para Ozempic® 1,0 mg uma vez por semana ou exenatida de liberação prolongada 2,0 mg uma vez por semana.
Tabela 3 - SUSTAIN 3: Resultados na semana 56
|
|
Ozempic® 1,0 mg |
Exenatida de liberação prolongada 2,0 mg |
|
População intenção de tratar - ITT (N) |
404 |
405 |
|
HbA1c (%) |
||
|
Basal (média) |
8,4 |
8,3 |
|
Alteração a partir do basal na semana 56 |
-1,5 |
-0,9 |
|
Diferença de exenatida [95% IC] |
-0,6 |
- |
|
Pacientes (%) atingindo HbA1c <7% |
67 |
40 |
|
GPJ (mmol/L18) (mg/dL19) |
||
|
Basal (média) |
10,6 (191,0 mg/dL19) |
10,4 (187,4 mg/dL19) |
|
Alteração a partir do basal na semana 56 |
-2,8 (-50,5 mg/dL19) |
-2,0 (-36,0 mg/dL19) |
|
Peso corporal (kg) |
||
|
Basal (média) |
96,2 |
95,4 |
|
Alteração a partir do basal na semana 56 |
-5,6 |
-1,9 |
|
Diferença de exenatida [95% IC] |
-3,8 |
- |
a valor p <0,0001 (bilateral) para superioridade
SUSTAIN 4 – Ozempic® versus insulina glargina14, ambos em combinação com 1–2 medicamentos antidiabéticos orais20 (metformina8 ou metformina8 e sulfonilureia)
Em um estudo aberto de 30 semanas, 1.089 pacientes foram randomizados para receber Ozempic® 0,5 mg ou 1,0 mg, uma vez por semana, ou insulina glargina14, uma vez ao dia, como adjuvante à metformina8 (48%) ou metformina8 e sulfonilureia (51%).
Tabela 4 – SUSTAIN 4: Resultados na semana 30
|
|
Ozempic® 0,5 mg |
Ozempic® 1,0 mg |
insulina glargina14 |
|
População intenção de tratar - ITT (N) |
362 |
360 |
360 |
|
HbA1c (%) |
|||
|
Basal (média) |
8,1 |
8,2 |
8,1 |
|
Alteração a partir do basal na semana 30 |
-1,2 |
-1,6 |
-0,8 |
|
Diferença de insulina glargina14 [95% IC] |
-0,4 |
-0,8 |
- |
|
Pacientes (%) atingindo HbA1c <7% |
57 |
73 |
38 |
|
GPJ (mmol/L18) (mg/dL19) |
|||
|
Basal (média) |
9,6 (173,0 mg/dL19) |
9,9 (178,4 mg/dL19) |
9,7 (174,8 mg/dL19) |
|
Alteração a partir do basal na semana 30 |
-2,0 (- 36 mg/dL19) |
-2,7 (- 48,6 mg/dL19) |
-2,1 (- 37,8 mg/dL19) |
|
Peso corporal (kg) |
|||
|
Basal (média) |
93,7 |
94,0 |
92,6 |
|
Alteração a partir do basal na semana 30 |
-3,5 |
-5,2 |
+1,2 |
|
Diferença de insulina glargina14 [95% IC] |
-4,6 [-5,3;-4,0]a |
-6,34 [-7,0;-5,7]a |
- |
a valor p <0,0001 (bilateral) para superioridade
SUSTAIN 5 – Ozempic® versus placebo13, ambos em combinação com insulina21 basal
Em um estudo duplo cego17 placebo13-controlado de 30 semanas, 397 pacientes inadequadamente controlados com insulina21 basal, com ou sem metformina8, foram randomizados para Ozempic® 0,5 mg ou 1,0 mg, uma vez por semana ou placebo13.
Tabela 5 – SUSTAIN 5: Resultados na semana 30
|
|
Ozempic® 0,5 mg |
Ozempic® 1,0 mg |
placebo13 |
|
População intenção de tratar - ITT (N) |
132 |
131 |
133 |
|
HbA1c (%) |
|||
|
Basal (média) |
8,4 |
8,3 |
8,4 |
|
Alteração a partir do basal na semana 30 |
-1,4 |
-1,8 |
-0,1 |
|
Diferença do placebo13 [95% IC] |
-1,4 [-1,6;-1,1]a |
-1,8 [-2,0;-1,5]a |
- |
|
Pacientes (%) atingindo HbA1c <7% |
61 |
79 |
11 |
|
GPJ (mmol/L18) (mg/dL19) |
|||
|
Basal (média) |
8,9 (160,4 mg/dL19) |
8,5 (153,2 mg/dL19) |
8,6 (155,0 mg/dL19) |
|
Alteração a partir do basal na semana 30 |
-1,6 (- 28,8 mg/dL19) |
-2,4 (- 43,2 mg/dL19) |
-0,5 (- 9,0 mg/dL19) |
|
Peso corporal (kg) |
|||
|
Basal (média) |
92,7 |
92,5 |
89,9 |
|
Alteração a partir do basal na semana 30 |
-3,7 |
-6,4 |
-1,4 |
|
Diferença do placebo13 [95% IC] |
-2,3 [-3,3;-1,3]a |
-5,1 [-6,1;-4,0]a |
- |
a valor p <0,0001 (bilateral) para superioridade
SUSTAIN 7 – Ozempic® versus dulaglutida, ambos em combinação com metformina8
Em um estudo aberto de 40 semanas, 1.201 pacientes tratados com metformina8 foram randomizados 1:1:1:1 para uma dose semanal de Ozempic® 0,5 mg, dulaglutida 0,75 mg, Ozempic® 1 mg ou dulaglutida 1,5 mg, respectivamente. O estudo comparou Ozempic® 0,5 mg versus dulaglutida 0,75 mg, e Ozempic® 1 mg versus dulaglutida 1,5 mg.
Os distúrbios gastrointestinais foram os eventos adversos mais frequentes e ocorreram em proporções semelhantes entre os pacientes que receberam Ozempic® 0,5 mg (129 pacientes [43%]), Ozempic® 1 mg (133 [44%]) e dulaglutida 1,5 mg (143 [48%]); menos pacientes apresentaram distúrbios gastrointestinais com dulaglutida 0,75 mg (100 [33%]).
Na semana 40, o aumento da frequência de pulso para o Ozempic® (0,5 mg e 1 mg) e dulaglutida (0,75 mg e 1,5 mg) foi de 2,4; 4,0 e 1,6; 2,1, batimentos/min, respectivamente.
Tabela 6 – SUSTAIN 7: Resultados na semana 40
|
|
Ozempic® 0,5 mg |
Ozempic® 1,0 mg |
dulaglutida 0,75 mg |
dulaglutida 1,5 mg |
|
População intenção de tratar - ITT (N) |
301 |
300 |
299 |
299 |
|
HbA1c (%) |
||||
|
Basal (média) |
8,3 |
8,2 |
8,2 |
8,2 |
|
Alteração a partir do basal na semana 40 |
-1,5 |
-1,8 |
-1,1 |
-1,4 |
|
Diferença de dulaglutida [95% IC] |
-0,4b [-0,6; -0,2]a |
-0,4c [-0,6; -0,3]a |
- |
- |
|
Pacientes (%) atingindo HbA1c <7% |
68 |
79 |
52 |
67 |
|
GPJ (mmol/L18) (mg/dL19) |
||||
|
Basal (média) |
9,8 (176,3 mg/dL19) |
9,8 (177,1 mg/dL19) |
9,7 (173,9 mg/dL19) |
9,6 (172,5 mg/dL19) |
|
Alteração a partir do basal na semana 40 |
-2,2 (- 39,6 mg/dL19) |
-2,8 (- 50,4 mg/dL19) |
-1,9 (- 34,2 mg/dL19) |
-2,2 (- 39,6 mg/dL19) |
|
Peso corporal (kg) |
||||
|
Basal (média) |
96,4 |
95,5 |
95,6 |
93,4 |
|
Alteração a partir do basal na semana 40 |
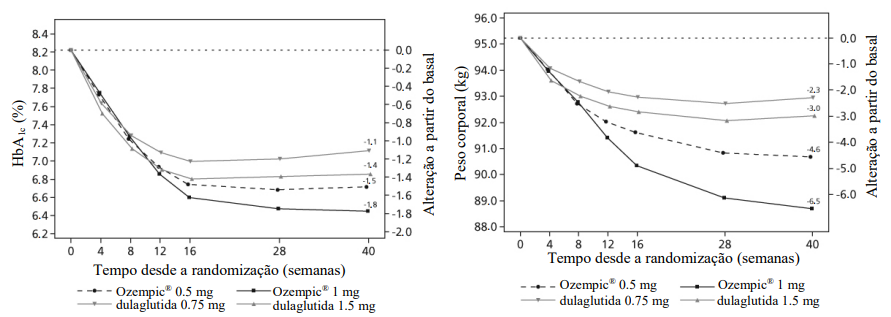
-4,6 |
-6,5 |
-2,3 |
-3,0 |
|
Diferença de dulaglutida[95% IC] |
-2,3b [-3,0; 1,5]a |
-3,6c [-4,3; -2,8]a |
- |
- |
a p<0,0001 (bilateral) para superioridade
b Ozempic® 0,5 mg vs dulaglutida 0,75 mg
c Ozempic® 1 mg vs dulaglutida 1,5 mg
Figura 2 – Alteração média na HbA1c12 (%) e no peso corporal (kg) a partir do basal até a semana 40
Associação com monoterapia de sulfonilureia
No estudo SUSTAIN 6 (vide item “Doença cardiovascular”), 123 pacientes receberam monoterapia de sulfonilureia no basal. A HbA1c12 basal era 8,2%, 8,4% e 8,4% para Ozempic® 0,5 mg, Ozempic® 1,0 mg e placebo13, respectivamente. Na semana 30, a alteração na HbA1c12 foi de -1,6%, -1,5% e 0,1% para Ozempic® 0,5 mg, Ozempic® 1,0 mg e placebo13, respectivamente.
Associação com pré-mistura de insulina21 ± 1–2 ADOs (medicamento antidiabético oral22)
No estudo SUSTAIN 6 (vide item “Doença cardiovascular”), 867 pacientes receberam pré-mistura de insulina21 (com ou sem antidiabéticos orais20) no basal. A HbA1c12 no período basal era 8,8%, 8,9% e 8,9% para Ozempic® 0,5 mg, Ozempic® 1,0 mg de e placebo13, respectivamente. Na semana 30, a alteração na HbA1c12 foi de -1,3%, -1,8% e -0,4% para Ozempic® 0,5 mg, Ozempic® 1,0 mg e placebo13, respectivamente.
Peso Corporal
Após um ano de tratamento, uma perda de peso de ≥ 5% e ≥ 10% foi atingida em mais indivíduos recebendo Ozempic® 0,5 mg (46% e 13%) e 1,0 mg (de 52 - 62% e de 21 - 24%) em comparação com os comparadores ativos sitagliptina (18% e 3%) e exenatida de liberação prolongada (até 17% e 4%).
No estudo de 40 semanas versus dulaglutida, uma perda de peso ≥ 5% e ≥ 10% foi alcançada para mais pacientes com Ozempic® 0,5 mg (44% e 14%) em comparação com a dulaglutida 0,75 mg (23% e 3%), e Ozempic® 1 mg (até 63% e 27%) em comparação com
dulaglutida 1,5 mg (30% e 8%).
Observou-se uma redução significativa e sustentada do peso corporal desde o início até a semana 104 com Ozempic® 0,5 mg e 1 mg versus placebo13 0,5 mg e 1 mg, além do tratamento padrão (-3,6 kg e -4,9 kg vs -0,7 kg e -0,5 kg, respectivamente) em SUSTAIN 6.
Doença cardiovascular
Em um estudo duplo-cego17 de 104 semanas (SUSTAIN 6), 3.297 pacientes com diabetes tipo 223 e alto risco cardiovascular foram randomizados para receber Ozempic® 0,5 mg ou 1,0 mg, uma vez por semana, ou o placebo13 correspondente, em adição ao tratamento padrão. Em seguida, os pacientes foram acompanhados por 2 anos. No total, 98,0% dos pacientes concluíram o estudo e o estado vital foi conhecido ao final do estudo para 99,6% dos pacientes.
A população do estudo foi distribuída por idade da seguinte forma: 1.598 pacientes (48,5 %) ≥ 65 anos, 321 (9,7%) ≥ 75 anos e 20 (0,6%) ≥ 85 anos. Havia 2.358 pacientes com função renal16 normal ou insuficiência renal24 leve, 832 com insuficiência renal24 moderada e 107 com insuficiência renal24 grave ou em estágio terminal. Havia 61% de homens, com idade média de 65 anos e IMC15 médio de 33 kg/m2. A duração média do diabetes9 era de 13,9 anos.
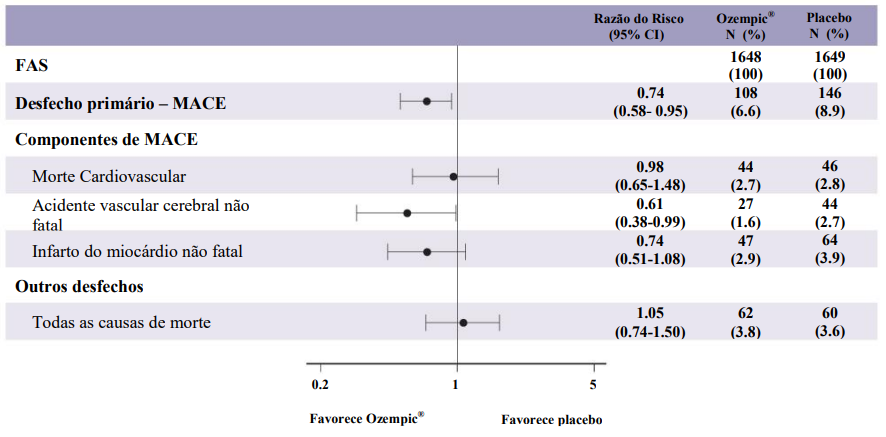
O desfecho primário foi o tempo desde a randomização até a primeira ocorrência de um evento adverso cardiovascular maior (MACE): morte cardiovascular, infarto do miocárdio25 não fatal ou acidente vascular cerebral26 não fatal. O número total de componentes de desfechos primários MACE foi 254, incluindo 108 (6,6%) com Ozempic® e 146 (8,9%) para placebo13. Veja Figura 4 para resultados dos desfechos primários e secundários dos eventos cardiovasculares.
O tratamento com Ozempic® resultou em uma redução de risco de 26% no resultado do componente primário composto por causas cardiovasculares, infarto do miocárdio25 não fatal ou acidente vascular cerebral26 não fatal. O número total de mortes por doenças cardiovasculares27, infartos do miocárdio28 não fatais e acidentes vasculares29 cerebrais não fatais foram 90, 111 e 71, respectivamente, incluindo 44 (2,7%), 47 (2,9%) e 27 (1,6%), respectivamente, com Ozempic® (Figura 4). A redução do risco no desfecho primário foi impulsionada principalmente pela diminuição da taxa de acidente vascular cerebral26 não fatal (39%) e infarto do miocárdio25 não fatal (26%) (Figura 3).
Figura 3. Gráfico de Kaplan-Meier do tempo até a primeira ocorrência do resultado composto: morte cardiovascular, infarto do miocárdio25 não fatal ou acidente vascular cerebral26 não fatal (SUSTAIN 6).

Figura 4. Gráfico Forest: análise do tempo até a primeira ocorrência do desfecho composto, seus componentes e todas as causas de morte (SUSTAIN 6)
Houve 158 eventos de nefropatia30 novos ou agravados. A razão de risco para o tempo até a nefropatia30 (início de macroalbuminúria31 persistente, duplicação de creatinina32 sérica persistente, necessidade de terapia de reposição renal16 contínua e óbito33 por doença renal16) foi de 0,64 [0,46; 0,88] dirigido por novo início de macroalbuminúria31 persistente.
Pressão arterial34
Reduções significativas na pressão arterial sistólica35 média foram observadas quando Ozempic® 0,5 mg (3,5–5,1 mmHg) e Ozempic® 1 mg (5,4–7,3 mmHg) foram utilizados em associação com medicamentos antidiabéticos orais20 ou insulina21 basal. Para pressão arterial diastólica36, não houve diferenças significativas entre Ozempic® e comparadores.
Referências
- Sorli C et al. Efficacy and safety of once-weekly semaglutide monotherapy versus placebo13 in patients with type 2 diabetes9 (SUSTAIN 1): a double-blind, randomised, placebo13-controlled, parallel-group, multinational, multicentre phase 3a trial. The Lancet Diabetes9 & Endocrinology. 2017;5(4):251-60.
- Ahrén B, Masmiquel L, Kumar H, Sargin M, Karsbøl JD, Jacobsen SH, et al. Efficacy and safety of once-weekly semaglutide versus once-daily sitagliptin as an add-on to metformin, thiazolidinediones, or both, in patients with type 2 diabetes9 (SUSTAIN 2): a 56-week, double-blind, phase 3a, randomised trial. The Lancet Diabetes9 & Endocrinology. 2017;5(5):341-54.
- Ahmann AJ et al. Efficacy and Safety of Once-Weekly Semaglutide Versus Exenatide ER in Subjects With Type 2 Diabetes9 (SUSTAIN 3): A 56-Week, Open-Label, Randomized Clinical Trial. Diabetes9 Care 2017;DOI: 10.2337/dc17-0417.
- Aroda V et al. Efficacy and safety of once-weekly semaglutide versus once-daily insulin glargine as add-on to metformin (with or without sulfonylureas) in insulin-naive patients with type 2 diabetes9 (SUSTAIN 4): a randomised, open-label, parallel-group, multicentre, multinational, phase 3a trial. Lancet Diabetes9 Endocrinol 2017;5:355–366.
- Rodbard H et al. Semaglutide Added to Basal Insulin in Type 2 Diabetes9 (SUSTAIN 5): A Randomized, Controlled Trial. J Clin Endocrinol Metab, June 2018, 103(6):2291–2301.
- Marso SP et al. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes9N Engl J Med 2016;375: 1834–1844.
- Seino Y et al. Safety and efficacy of semaglutide once weekly vs sitagliptin once daily, both as monotherapy in Japanese people with type 2 diabetes9. Diabetes9 Obes Metab 2018;20:378–388.
- Kaku K et al. Safety and efficacy of once-weekly semaglutide vs additional oral antidiabetic drugs in Japanese people with inadequately controlled type 2 diabetes9: A randomized trial. Diabetes9 Obes Metab. 2018;20:1202–1212.
- Pratley R.E. et al. Semaglutide versus dulaglutide once weekly in patients with type 2 diabetes9 (SUSTAIN 7): a randomised, open- label, phase 3b trial. Lancet Diabetes9 Endocrinol. 2018 Apr;6(4):275-286.
CARACTERÍSTICAS FARMACOLÓGICAS
Dados Farmacodinâmicos
Todas as avaliações farmacodinâmicas foram realizadas após 12 semanas de tratamento (incluindo o escalonamento de dose) no estado de equilíbrio com 1,0 mg de semaglutida uma vez por semana.
Glicose37 de jejum e pós-prandial
A semaglutida reduz as concentrações de glicose37 de jejum e pós-prandial. Em pacientes com diabetes mellitus7 tipo 2, o tratamento com semaglutida 1,0 mg resultou em reduções na glicose37 em termos de alteração absoluta desde o basal (mg/dL19) e redução relativa em comparação ao placebo13 (%) para glicose37 de jejum (28,8 mg/dL19; 22% de redução), glicose37 pós-prandial de 2 horas (73,8 mg/dL19; 37% de redução), concentração de glicose37 média 24 horas (30,6 mg/dL19; 22% de redução) e excursões de glicose37 pós-prandial em 3 refeições (10,8-19,8 mg/dL19) comparado ao placebo13.
Semaglutida reduziu a glicose37 de jejum após a primeira dose.
Função de células5 beta e secreção de insulina21
A semaglutida melhora a função das células5 beta. A semaglutida, em comparação ao placebo13, melhorou a resposta à insulina21 de primeira e segunda fases, com um aumento de 3 e 2 vezes, respectivamente, e aumentou a capacidade de secreção máxima das células5 beta em pacientes com diabetes mellitus7 tipo 2. Além disso, o tratamento com semaglutida aumentou as concentrações de insulina21 de jejum em comparação ao placebo13.
Secreção de glucagon4
A semaglutida reduz as concentrações de glucagon4 de jejum e pós-prandial. Em pacientes com diabetes mellitus7 tipo 2, a semaglutida resultou nas seguintes reduções relativas de glucagon4 em comparação ao placebo13: glucagon4 de jejum (8-21%), resposta do glucagon4 pós-prandial (14-15%) e concentração média de glucagon4 de 24 horas (12%).
Insulina21 dependente de glicose37 e secreção de glucagon4
A semaglutida reduziu as altas concentrações da glicemia38 por meio do estímulo de secreção de insulina21 e da diminuição da secreção de glucagon4 em um modo dependente da glicose37. Com semaglutida, a taxa de secreção de insulina21 em pacientes com diabetes mellitus7 tipo 2 foi comparável a de indivíduos sadios.
Durante a hipoglicemia39 induzida, a semaglutida, em comparação ao placebo13, não alterou as respostas contrarregulatórias de aumento de glucagon4 e não comprometeu a redução de peptídeos C em pacientes com diabetes mellitus7 tipo 2.
Esvaziamento gástrico
A semaglutida causou um pequeno retardo do esvaziamento gástrico inicial pós-prandial, reduzindo, assim, a taxa na qual a glicose37 aparece na circulação40 após a refeição.
Apetite, ingestão de energia e escolha alimentar
A semaglutida, em comparação ao placebo13, reduziu a ingestão energética de 3 refeições ad libitum consecutivas em 18-35%. Isso se deu por uma supressão de apetite induzida por semaglutida no estado de jejum, bem como no pós-prandial, melhora do controle alimentar, redução do desejo de comer e redução relativa da preferência por alimentos com alto teor de gordura41.
Lipídeos pós-prandial e em jejum
A semaglutida, em comparação ao placebo13, reduziu os triglicerídeos em jejum e as concentrações de colesterol42 VLDL em 12% e 21%, respectivamente. A resposta de triglicerídeos pós-prandial e colesterol42 VLDL a uma refeição com alto teor de gordura41 foi reduzida em > 40%.
Eletrofisiologia cardíaca (QTc)
O efeito da semaglutida na repolarização cardíaca foi testado em um estudo de QTc completo. A semaglutida não prolongou os intervalos de QTc em níveis de dose supraterapêuticos (até 1,5 mg no estado de equilíbrio).
Dados farmacocinéticos
Comparada ao GLP-1 endógeno, a semaglutida possui meia-vida prolongada de aproximadamente 1 semana, tornando-a adequada para a administração subcutânea1 (s.c.) uma vez por semana. O principal mecanismo de protração é a ligação à albumina43, que resulta na redução da depuração renal16 e proteção da degradação metabólica. Além disso, a semaglutida é estabilizada contra a degradação pela enzima44 DPP-4.
Absorção: A concentração máxima foi obtida em 1 a 3 dias após a dose.
A exposição no estado de equilíbrio foi atingida após 4–5 semanas de administração uma vez por semana. Em pacientes com diabetes mellitus7 tipo 2, as concentrações médias no estado de equilíbrio após administração s.c. de 0,5 mg e 1,0 mg de semaglutida foram de aproximadamente 16 nmol/L e 30 nmol/L, respectivamente.
A exposição à semaglutida aumentou de modo proporcional à dose nas concentrações 0,5 mg e 1,0 mg.
Uma exposição similar foi obtida com administração s.c. de semaglutida no abdome45, na coxa46, ou na parte superior do braço. A biodisponibilidade absoluta de semaglutida s.c. foi de 89%.
Distribuição: O volume de distribuição médio de semaglutida após administração s.c., em pacientes com diabetes mellitus7 tipo 2, foi de aproximadamente 12,5 L. A semaglutida liga-se extensivamente à albumina43 plasmática (>99%).
Metabolismo47/biotransformação: Antes da excreção, a semaglutida é extensivamente metabolizada através de clivagem proteolítica do esqueleto48 peptídico e beta- oxidação sequencial da cadeia lateral do ácido graxo. O envolvimento da enzima44 endopeptidase neutra (NEP) é esperado no metabolismo47 da semaglutida.
Eliminação: Em um estudo com uma dose única s.c. de semaglutida radiomarcada, verificou-se que as vias primárias de excreção de material relacionado a semaglutida foram urinária e fecal; aproximadamente 2/3 de materiais relacionados com a semaglutida foram excretados na urina49 e aproximadamente 1/3 nas fezes. Aproximadamente 3% da dose foi excretado como semaglutida intacta por meio da urina49.
A depuração da semaglutida em pacientes com diabetes mellitus7 tipo 2 foi de aproximadamente 0,05 L/h. Com uma meia-vida de eliminação de aproximadamente 1 semana, a semaglutida estará presente na circulação40 por cerca de 5 semanas após a última dose.
Populações especiais
Idosos: A idade não teve efeito na farmacocinética da semaglutida com base nos dados dos estudos de fase 3a, incluindo pacientes de 20- 86 anos de idade.
Sexo, raça e etnia: Sexo, raça (branca, negra ou afro-americana e asiáticos) e etnia (hispânica ou latina/não-hispânica ou não-latina) não tiveram efeito na farmacocinética da semaglutida.
Peso corporal: O peso corporal teve efeito na exposição da semaglutida. O peso corporal maior resulta em menor exposição; uma diferença de 20% no peso corporal entre os indivíduos resulta em um valor aproximado de 16% de diferença na exposição. As doses de 0,5 mg e 1,0 mg de semaglutida proporcionam exposição sistêmica adequada na faixa de peso corporal de 40-198 kg.
Comprometimento renal16: O comprometimento renal16 não impactou a farmacocinética de semaglutida de modo clinicamente relevante. Isso foi demonstrado com uma dose única de 0,5 mg de semaglutida para pacientes50 com diferentes graus de comprometimento renal16 (leve, moderado, grave ou em pacientes em diálise51) em comparação com indivíduos com função renal16 normal. Isso também foi demonstrado em indivíduos com diabetes mellitus7 tipo 2 e com comprometimento renal16 com base nos dados dos estudos de fase 3a, embora a experiência em pacientes com doença renal16 em estágio terminal fosse limitada.
Comprometimento hepático: O comprometimento hepático não impactou a exposição da semaglutida. A farmacocinética da semaglutida foi avaliada em pacientes com diferentes graus de comprometimento hepático (leve, moderado, grave) em comparação com indivíduos com função hepática52 normal em um estudo com dose única de 0,5 mg da semaglutida.
Pacientes Pediátricos: A semaglutida não foi estudada em pacientes pediátricos.
Mecanismo de ação
A semaglutida é um análogo de GLP-1 com 94% de homologia sequencial ao GLP-1 humano. A semaglutida age como um agonista3 do receptor de GLP-1 que se liga seletivamente e ativa o receptor de GLP-1, o alvo do GLP-1 endógeno.
O GLP-1 é um hormônio53 fisiológico54 que possui múltiplas ações na glicemia38, na regulação do apetite e no sistema cardiovascular55. A ação na glicemia38 e os efeitos no apetite são mediados especificamente pelos receptores de GLP-1 no pâncreas56 e no cérebro57. A semaglutida reduz a glicemia38 de uma forma dependente da glicose37, estimulando a secreção de insulina21 e diminuindo a secreção de glucagon4 quando a glicemia38 é alta. O mecanismo de redução da glicemia38 também envolve um pequeno atraso no esvaziamento gástrico na fase pós-prandial precoce. Durante a hipoglicemia39, a semaglutida diminui a secreção de insulina21 e não prejudica a secreção de glucagon4.
A semaglutida reduz o peso corporal e a massa corporal adiposa por meio da baixa ingestão energética, envolvendo uma redução do apetite de maneira geral. Além disso, a semaglutida reduz a preferência por alimentos com alto teor de gordura41.
Os receptores de GLP-1 também são expressos no coração58, na vasculatura no sistema imune59 e nos rins60.
A semaglutida teve um efeito benéfico sobre os lipídios plasmáticos, diminuiu a pressão arterial sistólica35 e reduziu a inflamação61 nos estudos clínicos.
Em estudos em animais, a semaglutida atenua o desenvolvimento de aterosclerose62 pela prevenção da progressão da placa63 aórtica e reduzindo a inflamação61 na placa63.
Informações de segurança pré-clínica
Dados pré-clínicos não revelaram riscos especiais para seres humanos com base nos estudos convencionais de segurança farmacológica, toxicidade64 de dose repetida ou genotoxicidade.
Tumores não letais de células5 C da tireoide65 observados em roedores são um efeito da classe dos agonistas do receptor de GLP-1. Nos estudos de carcinogenicidade de 2 anos em ratos e camundongos, a semaglutida causou tumores de células5 C da tireoide65 em exposições clinicamente relevantes. Nenhum outro tumor66 relacionado ao tratamento foi observado. Os tumores de células5 C de roedores são causados por um mecanismo mediado pelo receptor de GLP-1 específico e não genotóxico, o qual os roedores são particularmente sensíveis. A relevância para seres humanos é considerada baixa, mas não pode ser completamente excluída.
Nos estudos de fertilidade em ratos, a semaglutida não afetou o desempenho de acasalamento ou a fertilidade dos machos. Em ratas, foram observados aumento na duração do ciclo estral e uma pequena redução no corpo lúteo (ovulações) nas doses associadas à perda de peso corporal materno.
Nos estudos de desenvolvimento embriofetal em ratos, a semaglutida causou embriotoxicidade abaixo das exposições clinicamente relevantes. A semaglutida causou reduções acentuadas no peso corporal materno, e reduções na sobrevida67 e crescimento embrionário. Nos fetos, foram observadas malformações68 viscerais e esqueléticas importantes, incluindo efeitos nos ossos longos69, nas costelas70, nas vértebras, na cauda, nos vasos sanguíneos71 e nos ventrículos cerebrais. A embriotoxicidade demonstrou envolver o mecanismo mediado pelo receptor do GLP-1, levando a um suprimento nutricional comprometido para o crescimento embrionário.
Devido a diferenças de espécies na anatomia e função do saco vitelino, e devido à falta de expressão do receptor GLP-1 no saco vitelino de primatas não humanos, considera-se que este mecanismo é pouco relevante para os seres humanos. Entretanto, um efeito direto da semaglutida no feto72 não pode ser excluído.
Nos estudos de toxicidade64 de desenvolvimento em coelhos e macacos cynomolgus, foram observados um aumento na perda de gravidez73 e um leve aumento na incidência74 de anormalidades fetais em exposições clinicamente relevantes. Os achados coincidiram com a perda de peso corporal materno acentuada de até 16%. Não se sabe se esses efeitos estão relacionados à redução do consumo alimentar materno como efeito direto do GLP-1.
O crescimento e desenvolvimento pós-natal foram avaliados em macacos cynomolgus. Os filhotes eram ligeiramente menores no nascimento, mas se recuperaram durante o período de lactação75.
Em ratos jovens, a semaglutida causou o retardo da maturação sexual em machos e fêmeas. Esses atrasos não impactaram a fertilidade e a capacidade reprodutiva de nenhum gênero ou a capacidade de as fêmeas manterem a gravidez73.
CONTRAINDICAÇÕES
Hipersensibilidade ao princípio ativo ou a qualquer um dos excipientes listados em “Composição”.
ADVERTÊNCIAS E PRECAUÇÕES
Ozempic® não deve ser utilizado em pacientes com diabetes mellitus7 tipo 1 ou para o tratamento de cetoacidose diabética76.
Ozempic® não é um substituto de insulina21. Cetoacidose diabética76 foi relatada em pacientes insulinodependentes que tiveram descontinuação rápida ou redução da dose de insulina21 quando o tratamento com um agonista3 do receptor de GLP-1 foi iniciado (vide item “8. Posologia e Modo de usar”).
Tumores não-letais de células5 C da tireoide65 observados em roedores são um efeito de classe para os agonistas do receptor de GLP-1. Em estudos de carcinogenicidade de 2 anos em ratos e camundongos, a semaglutida causou tumores da célula77 C da tiróide em exposições clinicamente relevantes. Nenhum outro tumor66 relacionado ao tratamento foi observado. Os tumores de células5 C de roedores são causados por um mecanismo não genotóxico, específico do receptor de GLP-1, para o qual os roedores são particularmente sensíveis. A relevância para os seres humanos é considerada baixa, mas não pode ser completamente excluída. Portanto, Ozempic® deve ser usado com cautela em pacientes com histórico pessoal ou familiar de carcinoma78 medular de tireoide65 (CMT) ou em pacientes com Síndrome79 de Neoplasia80 Endócrina Múltipla tipo 2 (NEM 2).
Efeitos gastrointestinais
O uso de agonistas do receptor de GLP-1 pode estar associado a reações adversas gastrointestinais. Isso deve ser considerado ao tratar pacientes com comprometimento da função renal16, visto que náusea81, vômito82 e diarreia83 podem causar desidratação84, o que poderia levar à deterioração da função renal16 (vide item “9. Reações Adversas”).
Pancreatite85 aguda
A pancreatite85 aguda foi observada com o uso de agonistas do receptor de GLP-1. Os pacientes devem ser informados sobre os sintomas86 característicos da pancreatite85 aguda. Se houver suspeita de pancreatite85, Ozempic® deverá ser descontinuado; se confirmado, Ozempic® não deve ser reiniciado. Deve-se ter cautela com pacientes com histórico de pancreatite85.
Hipoglicemia39
Pacientes tratados com Ozempic® em associação com uma sulfonilureia ou insulina21 podem ter aumento no risco de hipoglicemia39. O risco de hipoglicemia39 pode ser reduzido pela diminuição da dose de sulfonilureia ou de insulina21 ao iniciar o tratamento com Ozempic® (vide item “9. Reações Adversas”).
Retinopatia diabética87
Em pacientes com retinopatia diabética87 tratados com insulina21 e semaglutida, um risco aumentado de desenvolvimento de complicações da retinopatia diabética87 foi observado (vide item “9. Reações Adversas”). O cuidado deve ser exercido quando se utiliza a semaglutida em pacientes com retinopatia diabética87 tratados com insulina21. Estes pacientes devem ser monitorados de perto e tratados de acordo com as diretrizes clínicas. Uma melhora rápida no controle glicêmico tem sido associada a um agravamento temporário da retinopatia diabética87, mas outros mecanismos não podem ser excluídos.
Insuficiência cardíaca88
Não há experiência terapêutica89 em pacientes com insuficiência cardíaca congestiva90 New York Heart Association (NYHA) classe IV e a semaglutida não é, portanto, recomendada para estes pacientes.
Conteúdo de sódio
Este medicamento contém menos de 1 mmol de sódio (23 mg) por dose, portanto, é essencialmente “livre de sódio”.
Fertilidade, Gravidez73 e Lactação75
O efeito de semaglutida na fertilidade de seres humanos é desconhecido. A semaglutida não afetou a fertilidade masculina de ratos. Em ratas, foram observados aumento na duração estral e uma pequena redução no número de ovulações em doses associadas à perda de peso corporal materno (vide item “3. Características Farmacológicas, Informações de segurança pré-clínica”).
Recomenda-se que as mulheres em idade fértil usem contraceptivos quando tratadas com semaglutida.
Estudos em animais demonstraram toxicidade64 reprodutiva (vide item “3. Características Farmacológicas, Informações de segurança pré-clínica”). Há dados limitados sobre o uso de semaglutida em mulheres grávidas. Portanto, semaglutida não deve ser utilizada durante a gravidez73. Se uma paciente desejar engravidar ou se ocorrer a gravidez73, semaglutida deverá ser descontinuada. A semaglutida deve ser descontinuada pelo menos 2 meses antes da gravidez73 planejada em razão da meia-vida longa de semaglutida (vide item “3. Características Farmacológicas, Dados Farmacodinâmicos”).
Em ratas lactantes91, semaglutida foi excretada no leite. Não se pode excluir um risco para crianças lactentes92. A semaglutida não pode ser utilizada durante a amamentação93.
Categoria de risco na gravidez73: C – Não há estudos adequados em mulheres. Em experiências animais ocorreram alguns efeitos colaterais94 no feto72, mas o benefício do produto pode justificar o risco potencial durante a gravidez73.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Efeitos na habilidade de dirigir e operar máquinas
Ozempic® possui pouca ou nenhuma influência na capacidade de dirigir ou operar máquinas. Quando é utilizado em associação com uma sulfonilureia ou insulina21, os pacientes devem ser aconselhados a se precaver para evitar hipoglicemia39 ao dirigir e operar máquinas.
INTERAÇÕES MEDICAMENTOSAS
A semaglutida retarda o esvaziamento gástrico e tem o potencial de influenciar a taxa de absorção se administrada concomitante com medicamentos orais. A semaglutida deve ser usada com precaução em pacientes tratados com medicamentos orais que requerem uma rápida absorção gastrointestinal.
Paracetamol
A semaglutida atrasa a taxa de esvaziamento gástrico, conforme avaliado pela farmacocinética do paracetamol durante teste de refeição padronizado. AUC0-60min e Cmax do paracetamol diminuíram cerca de 27% e 23%, respectivamente, após o uso concomitante de semaglutida 1 mg. A exposição total ao paracetamol (AUC0-5h) não foi afetada. Não é necessário ajuste posológico do paracetamol quando administrado com semaglutida.
Contraceptivos orais
Não é esperado que a semaglutida reduza a efetividade dos contraceptivos orais, visto que a semaglutida não alterou a exposição global de etinilestradiol e levonorgestrel em um grau clinicamente relevante quando uma associação de contraceptivos orais (0,03 mg de etinilestradiol/0,15 mg de levonorgestrel) foi coadministrada com semaglutida. A exposição do etinilestradiol não foi afetada; um aumento de 20% foi observado na exposição de levonorgestrel no estado de equilíbrio. A Cmax não foi afetada em qualquer um dos compostos.
Atorvastatina
Semaglutida não alterou a exposição global de atorvastatina após a administração de dose única de atorvastatina (40 mg). A Cmax de atorvastatina reduziu em 38%. Isso foi avaliado como não clinicamente relevante.
Digoxina
Semaglutida não alterou a exposição global ou a Cmax de digoxina após uma dose única de digoxina (0,5 mg).
Metformina8
Semaglutida não alterou a exposição global ou a Cmax de metformina8 após administração de 500 mg 2 vezes ao dia por 3,5 dias.
Varfarina
Semaglutida não alterou a exposição global ou a Cmax de varfarina R e S após uma dose única de varfarina (25 mg) e os efeitos farmacodinâmicos da varfarina, conforme medidos pela razão normalizada internacional (RNI), não foram afetados de modo clinicamente relevante. No entanto, após o início do tratamento com semaglutida em pacientes tratados com varfarina ou outros derivados cumarínicos, o monitoramento frequente da RNI é recomendado.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Prazo de validade: 36 meses.
Prazo de validade para o sistema de aplicação em uso: 6 semanas.
Antes de abrir (antes de iniciar o uso):
- Armazene em refrigerador (2 °C a 8 °C).
- Mantenha longe dos compartimentos próximos ao congelador.
- Mantenha o sistema de aplicação tampado para protegê-lo da luz.
- Não congele Ozempic® e não use se ele tiver sido congelado.
Durante o uso:
- Armazene abaixo de 30 °C ou em refrigerador (2 °C a 8 °C).
- Mantenha longe dos compartimentos próximos ao congelador.
- Não congele Ozempic® e não use se ele tiver sido congelado.
- Mantenha o sistema de aplicação tampado quando Ozempic® não estiver em uso para protegê-lo da luz.
Após aberto, válido por 6 semanas. Após este período, Ozempic® deve ser descartado mesmo que ainda tenha produto na embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original. Número de lote e datas de fabricação e validade: vide embalagem.
Ozempic® é uma solução isotônica95 límpida e incolor (pH=7,4). Ozempic® deve ser protegido da luz e calor excessivos.
Transporte:
O transporte do medicamento deverá ser realizado através de uma embalagem que proporcione proteção térmica e evite alteração brusca de temperatura, incidência74 de luz direta e vibração excessiva. No caso de viagens aéreas, não despachar o produto dentro das malas. O compartimento de bagagem dos aviões atinge temperaturas muito baixas, podendo congelar o medicamento.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Método de administração
Ozempic® deve ser administrado uma vez por semana, a qualquer momento do dia, acompanhado ou não de refeição.
Ozempic® deve ser injetado por via subcutânea1 no abdome45, na coxa46 ou na parte superior do braço. O local da injeção96 pode ser alterado sem ajuste de dose. Ozempic® não deve ser administrado por via intravenosa ou intramuscular.
O dia da administração semanal pode ser alterado, se necessário, contanto que o intervalo entre as duas doses seja de pelo menos 3 dias (> 72 horas). Após selecionar um novo dia para a aplicação, a administração semanal deve ser continuada.
Posologia
A dose inicial de Ozempic® é 0,25 mg, uma vez por semana. Após 4 semanas, a dose deve ser aumentada para 0,5 mg, uma vez por semana. Após pelo menos 4 semanas com uma dose de 0,5 mg, uma vez por semana, a dose pode ser aumentada para 1,0 mg, uma vez por semana, se um controle glicêmico adicional for necessário.
Ozempic® 0,25 mg não é uma dose de manutenção. Doses semanais maiores que 1,0 mg não são recomendadas.
Quando Ozempic® é adicionado à terapia existente de metformina8 e/ou tiazolidinediona, a dose de metformina8 e/ou tiazolidinediona pode continuar sem alterações.
Quando Ozempic® é adicionado à terapia existente de uma sulfonilureia ou insulina21, a redução na dose de sulfonilureia ou insulina21 deve ser considerada para reduzir o risco de hipoglicemia39 (vide item “5. Advertências e Precauções”). A automonitorização da glicemia38 não é necessária para ajustar a dose de Ozempic®. A automonitorização da glicemia38 é necessária para ajustar a dose de sulfonilureia e insulina21, particularmente quando Ozempic® é iniciado e a insulina21 é reduzida. Recomenda-se uma abordagem gradual para a redução da insulina21.
Populações Especiais
Pacientes idosos: Nenhum ajuste de dose é necessário com base na idade. A experiência terapêutica89 em pacientes ≥ 75 anos é limitada (vide item “3. Características farmacológicas”).
Pacientes com comprometimento hepático: Nenhum ajuste é necessário para pacientes50 com comprometimento hepático (vide item “3. Características farmacológicas”). A experiência com o uso de semaglutida em pacientes com insuficiência hepática97 grave é limitada. Deve-se ter cautela ao tratar estes pacientes com semaglutida.
Pacientes com comprometimento renal16: Nenhum ajuste é necessário para pacientes50 com comprometimento renal16 leve, moderado ou grave. A experiência com o uso de semaglutida em pacientes com doença renal16 grave é limitada. Semaglutida não é recomendada em pacientes com doença renal16 em estado terminal (vide item “3. Características farmacológicas”).
População pediátrica: A segurança e a eficácia de Ozempic® em crianças e adolescentes com menos de 18 anos de idade não foram estudadas. Não há dados disponíveis.
Dose esquecida
Se esquecer de tomar uma dose, ela deverá ser administrada logo que possível e no prazo de 5 dias após a dose esquecida. Se mais de 5 dias tiverem passado, a dose esquecida deverá ser pulada e a dose seguinte administrada no dia anteriormente programado. Em todos os casos, os pacientes podem retomar o cronograma de administração regular de uma vez por semana.
Incompatibilidades
Na ausência de estudos de compatibilidade, Ozempic® não deve ser misturado com outros medicamentos.
Precauções para descarte
O paciente deve ser advertido a descartar a agulha da injeção96 após cada aplicação, e armazenar o sistema de aplicação sem a agulha acoplada. Isso previne: agulhas entupidas, contaminação, infecção98, vazamento de solução e dosagem imprecisa.
O descarte de agulhas deve ser realizado através de embalagens coletoras resistentes, como latas e plásticos, para eliminar o risco de acidentes e contaminação. Os medicamentos usados, vencidos ou fora de uso, assim como seu sistema de aplicação e as embalagens coletoras contendo agulhas, devem ser descartados em Postos de Coleta localizados em Farmácias, Drogarias, Postos de Saúde6 ou Hospitais, que possuem coletores apropriados. O cartucho e a bula, que não possuem contato direto com o medicamento, podem ser descartados no lixo reciclável.
Não tente repor o conteúdo do sistema de aplicação ou reutilizá-lo. Uma vez vazio, ele deve ser descartado.
O sistema de aplicação Ozempic® é destinado somente ao uso individual. Ozempic® não deve ser utilizado se não estiver límpido e incolor.
Ozempic® não deve ser utilizado se tiver sido congelado.
Ozempic® pode ser administrado com agulhas de até 8mm de comprimento. O sistema de aplicação foi desenvolvido para ser utilizado com as agulhas descartáveis NovoFine®. As agulhas NovoFine® Plus são incluídas na embalagem.
REAÇÕES ADVERSAS
Resumo do perfil de segurança
Nos 8 estudos de fase 3a, 4.792 pacientes foram expostos ao Ozempic®.
As reações adversas mais frequentemente relatadas nos estudos clínicos foram os distúrbios gastrointestinais, incluindo náusea81 (muito comum), diarreia83 (muito comum) e vômito82 (comum). Em geral, essas reações foram de gravidade leve a moderada e de curta duração.
Reações adversas tabuladas
A Tabela 7 lista as reações adversas identificadas nos estudos de fase 3a em pacientes com diabetes mellitus7 tipo 2 (para maiores informações, vide item “2. Resultados de Eficácia”). As frequências de reações adversas são baseadas em um agrupamento dos estudos de fase 3a, exceto o estudo de desfechos cardiovasculares (vide Tabela 7 abaixo para detalhes adicionais).
As reações são listadas abaixo pela classe de sistema orgânico e frequência absoluta. As frequências são definidas como: muito comum: (≥1/10); comum: (≥ 1/100 a <1/10); incomum (≥ 1/1.000 a <1/100); rara: (≥ 1/10.000 a <1/1.000); muito rara: (<1/10.000) e desconhecida: não pode ser estimada a partir dos dados disponíveis. Dentro de cada agrupamento de frequência, as reações adversas são apresentadas em ordem decrescente de gravidade.
Tabela 7. Reações adversas dos estudos de fase 3a controlados incluindo o estudo de desfecho cardiovascular
|
Classe de Sistema Orgânico do MedDRA |
Muito comum |
Comum |
Incomum |
Rara |
Desconhecida |
|
Distúrbios do sistema imunológico99 |
|
|
Hipersensibilidadec |
Reação anafilática100 |
|
|
Distúrbios metabólicos e nutricionais |
Hipoglicemiaa quando utilizado com insulina21 ou sulfonilureia |
Hipoglicemia39a quando utilizado com outros ADOs Redução do apetite |
|
|
|
|
Distúrbios do sistema nervoso101 |
|
Tontura102 |
Disgeusia103 |
|
|
|
Distúrbios oftalmológicos |
|
Complicações de retinopatia diabética87b |
|
|
|
|
Distúrbios cardíacos |
|
|
Aumento da frequência cardíaca |
|
|
|
Distúrbios gastrointestinais |
Náusea81 Diarreia83 |
Vômito82 Dor abdominal Distensão abdominal Constipação104 Dispepsia105 Gastrite106 Doença do refluxo gastroesofágico107 Eructação108 Flatulência |
Pancreatite85 aguda |
|
|
|
Distúrbios hepatobiliares109 |
|
Colelitíase110 |
|
|
|
|
Distúrbios da pele111 e do tecido subcutâneo112 |
|
|
|
|
Angioedema113d |
|
Distúrbios gerais e condições do local de administração |
|
Fadiga114 |
Reações no local da injeção96 |
|
|
|
Investigações |
|
Lipase aumentada Amilase aumentada Perda de peso |
|
|
|
a Hipoglicemia39 definida como grave (necessita de assistência de outra pessoa) ou sintomática115 em associação com a glicemia38 < (55,8 mg/dL19).
b Complicações de retinopatia diabética87 é um composto de: necessidade de fotocoagulação da retina116, tratamento com agentes intravítreos, hemorragia117 vítrea, início de cegueira relacionada ao diabetes9 (incomum). Frequência baseada no estudo de desfechos cardiovasculares.
c Termo agrupado que abrange também eventos adversos relacionados à hipersensibilidade, como erupção118 cutânea119 e urticária120.
d A partir de relatos pós-comercialização.
Estudo de segurança e desfechos cardiovasculares de 2 anos
Em uma população com alto risco cardiovascular, o perfil de reação adversa foi similar ao observado em outros estudos de fase 3a (descrito no item “2. Resultados de Eficácia”).
Hipoglicemia39
Não foram observados episódios de hipoglicemia39 grave quando Ozempic® foi utilizado como monoterapia. Hipoglicemia39 grave foi principalmente observada quando Ozempic® foi utilizado com uma sulfonilureia (1,2% dos pacientes, 0,03 eventos/paciente-ano) ou insulina21 (1,5% dos pacientes, 0,02 eventos/paciente-ano). Poucos episódios (0,1% dos pacientes, 0,001 eventos/paciente-ano) foram observados com Ozempic® em associação com medicamentos antidiabéticos orais20, exceto sulfonilureia.
Reações adversas gastrointestinais
Náusea81 ocorreu em 17,0% e 19,9% dos pacientes quando tratados com Ozempic® 0,5 mg e 1,0 mg, respectivamente, diarreia83 em 12,2% e 13,3% e vômito82 em 6,4% e 8,4%. A maioria dos eventos foi de gravidade leve a moderada e de curta duração. Os eventos levaram à descontinuação do tratamento em 3,9% e 5% dos sujeitos. Os eventos foram relatados com maior frequência durante os primeiros meses do tratamento. Pacientes com baixo peso corporal podem ter mais efeitos colaterais94 gastrointestinais quando tratados com semaglutida.
Pancreatite85 aguda
A frequência de pancreatite85 aguda confirmada por adjudicação relatada nos estudos clínicos de fase 3a foi de 0,3% para Ozempic® e de 0,2% para o comparador, respectivamente. No estudo de desfechos cardiovasculares de 2 anos, a frequência de pancreatite85 aguda confirmada por adjudicação foi de 0,5% para Ozempic® e 0,6% para o placebo13 (vide item “5. Advertências e Precauções”).
Complicações da retinopatia diabética87
Em um estudo clínico de 2 anos envolvendo 3.297 pacientes com diabetes mellitus7 tipo 2 e alto risco cardiovascular, longa duração de diabetes9 e glicemia38 mal controlada, eventos adjudicados de complicações da retinopatia diabética87 ocorreram em mais pacientes tratados com Ozempic® (3,0%) em comparação ao placebo13 (1,8%). Isto foi observado em pacientes tratados com insulina21 com conhecida retinopatia diabética87. A diferença de tratamento apareceu cedo e persistiu durante todo o estudo. Uma avaliação sistemática da complicação da retinopatia diabética87 somente foi realizada nos desfechos cardiovasculares do estudo.
Em outros estudos clínicos de até 1 ano envolvendo 4.807 pacientes com diabetes mellitus7 tipo 2, eventos adversos relacionados à retinopatia diabética87 foram relatados em proporções similares de indivíduos tratados com Ozempic® (1,7%) e comparadores (2,0%).
Descontinuação em razão de evento adverso
A incidência74 de descontinuação do tratamento em razão de eventos adversos foi de 6,1% e 8,7% para pacientes50 tratados com Ozempic® 0,5 e 1,0 mg, respectivamente, versus 1,5% para placebo13. Os eventos adversos mais frequentes levando à descontinuação foram gastrointestinais.
Reações no local de injeção96
Reações no local de injeção96 (por exemplo erupção118 no local da injeção96, eritema121) foram reportadas por 0,6% e 0,5% de pacientes que receberam Ozempic® 0,5 mg e 1 mg, respectivamente. Essas reações geralmente foram leves.
Imunogenicidade
Consistente com as propriedades potencialmente imunogênicas dos medicamentos contendo proteínas122 ou peptídeos, os pacientes podem desenvolver anticorpos123 após o tratamento com semaglutida. A proporção de indivíduos com resultado positivo para anticorpos123 anti-semaglutida a qualquer momento após o período basal foi baixa (1–2%) e nenhum indivíduo possuía anticorpos123 neutralizantes anti-semaglutida ou anticorpos123 anti-semaglutida com efeito neutralizante de GLP-1 endógeno ao final do estudo.
Aumento da frequência cardíaca
Um aumento na frequência cardíaca foi observado com os agonistas do receptor do GLP-1. Nos estudos clínicos de fase 3a, foram observados aumentos médios de 1 a 6 batimentos por minuto (bpm) a partir do basal de 72 a 76 bpm em pacientes tratados com Ozempic®. Em um estudo clínico a longo prazo com pacientes com fatores de risco cardiovasculares, 16% dos pacientes tratados com Ozempic® tiveram um aumento na frequência cardíaca de > 10 bpm em comparação a 11% dos pacientes que receberam placebo13 após 2 anos de tratamento.
Resultado relatado por paciente
A notificação de suspeita de reações adversas do medicamento é importante. Isto permite uma monitorização contínua da relação benefício / risco do medicamento. Profissionais de saúde6 são alertados a relatarem qualquer suspeita de reação adversa.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, notifique os eventos adversos pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
As superdosagens de até 4 mg em dose única, e até 4 mg em uma semana foram relatadas nos estudos clínicos. O evento adverso mais comumente relatado foi náusea81. Todos os pacientes se recuperaram sem complicações.
Não há antídoto124 específico para superdosagem de Ozempic®. Em caso de superdosagem, deve-se iniciar um tratamento de suporte adequado de acordo com os sinais125 e sintomas86 clínicos do paciente. Um período prolongado de observação e tratamento desses
sintomas86 pode ser necessário, considerando a meia-vida longa de Ozempic® de aproximadamente 1 semana (vide item 3. “Características Farmacológicas”).
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Registro MS 1.1766.0036
Farmacêutico responsável: Luciane M. H. Fernandes – CRF/PR n° 6002
Fabricado por:
Novo Nordisk A/S Bagsværd, Dinamarca
Registrado por:
Novo Nordisk Farmacêutica do Brasil Ltda.
Rua Prof. Francisco Ribeiro, 683
Araucária/PR
CNPJ: 82.277.955/0001-55
Importado por:
Novo Nordisk Farmacêutica do Brasil Ltda.
Rua Francisco Munõz Madrid, 625
São José dos Pinhais/PR
SAC 0800 0144488