Wainua (Bula do profissional de saúde)
ASTRAZENECA DO BRASIL LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Wainua
eplontersena
Injetável 56 mg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Embalagem com 1 caneta aplicadora
VIA SUBCUTÂNEA
USO ADULTO
COMPOSIÇÃO:
Cada caneta aplicadora de dose única de Wainua contém:
| eplontersena (equivalente a 47 mg de eplontersena sódica) | 45 mg |
| excipiente q.s.p. | 0,8 mL. |
Excipientes: fosfato de sódio monobásico di-hidratado, fosfato de sódio dibásico, cloreto de sódio, ácido clorídrico, hidróxido de sódio, água para injetáveis.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE
INDICAÇÕES
Wainua é indicado para o tratamento da amiloidose hereditária mediada por transtirretina (ATTRv) em pacientes adultos com polineuropatia em estágio 1 ou 2.
RESULTADOS DE EFICÁCIA
Eficácia clínica
A eficácia e segurança de Wainua foram avaliadas em um estudo randomizado, multicêntrico, aberto e controlado externamente (NEURO-TTRansform) que incluiu um total de 168 participantes com polineuropatia causada por ATTRv (ATTRv-PN) estágio 1 ou estágio 2 (80% e 20% respectivamente). Os participantes foram randomizados em uma proporção de 6:1 para receber injeção subcutânea a cada 4 semanas com Wainua 45 mg (N = 144) ou inotersena 284 mg semanal (N = 24) como grupo de referência. A inclusão do grupo de referência inotersena teve o objetivo de verificar se não existem diferenças significativas na resposta do paciente entre o estudo anterior NEURO-TTR (ISIS 420915-CS2) e o estudo NEURO-TTRansform (ION-682884-CS3).
Dos 144 pacientes randomizados para eplontersena, 140 (97,2%) participantes completaram o tratamento até a Semana 35 e 135 (93,8%) completaram o tratamento até a Semana 65.
Um controle externo com placebo consistiu numa coorte de participantes com placebo do estudo pivotal de inotersena: estudo clínico multicêntrico, randomizado, duplo-cego, controlado por placebo, em participantes adultos com ATTRv-PN estágio 1 ou estágio 2 (NEURO-TTR). Essa coorte recebeu injeções subcutâneas de placebo uma vez por semana. Ambos os estudos empregaram critérios de elegibilidade idênticos.
As características dos grupos de eplontersena e placebo externo foram geralmente semelhantes, e potenciais desequilíbrios nas principais características basais (status da mutação Val30Met, estágio da doença e tratamento anterior) foram considerados na análise estatística pré-especificada. As características demográficas e da doença basais são mostradas na Tabela 1.
Tabela 1. Dados demográficos e características da doença basais no Estudo NEURO-TTRansform (conjunto de segurança)
| Placebo* (N=60) |
Wainua (N=144) |
|
|---|---|---|
|
Idade, anos Média (DP) Mediana (mín, máx) <65, n (%) 65-74, n (%) ≥75, n (%) |
59,5 (14,1) 63 (28, 81) 34 (56,7) 17 (28,3) 9 (15,0) |
53,0 (15,0) 51,5 (24, 82) 100 (69,4) 36 (25,0) 8 (5,6) |
| Sexo masculino, n (%) | 41 (68,3) | 100 (69,4) |
|
Raça, n (%) Asiática Negra ou afro-americana Branca Outros Múltipla |
3 (5,0) 1 (1,7) 53 (88,3) 2 (3,3) 1 (1,7) |
22 (15,4) 5 (3,5) 112 (78,3) 3 (2,1) 1 (0,7) |
|
Etnia, n (%) m Hispânica ou Latina |
60 7 (11,7) |
142 22 (15,5) |
|
Tratamento prévio com tafamidis ou diflunisal, n (%) Sim |
36 (60,0) |
100 (69,4) |
|
Estágio da doença ATTRv-PN1, n (%) Estágio 1 Estágio 2 |
42 (70,0) 18 (30,0) |
115 (79,9) 29 (20,1) |
| Escore composto mNIS+7, média (DP) | 74,8 (39,0) | 81,3 (43,4) |
|
Escore total do Norfolk QoL-DN, m média (DP) |
59 48,7 (26,8) |
137 44,1 (26,6) |
|
Mutação Val30Met da TTR, n (%) Sim2 Não3 Glu89Gln, Glu109Gln Leu58His, Leu78His Phe64Leu, Phe84Leu Ser50Arg, Ser70Arg Ser77Tyr, Ser97Tyr, S97Y Thr49Ala, Thr69Ala Thr60Ala, Thr80Ala Val122Ile, Val142Ile Outra3 |
33 (55,0) 27 (45,0) 0 3 (5,0) 3 (5,0) 1 (1,7) 5 (8,3) 0 8 (13,3) 1 (1,7) 6 (10,0) |
85 (59,0) 59 (41,0) 1 (0,7) 4 (2,8) 5 (3,5) 2 (1,4) 3 (2,1) 1 (0,7) 4 (2,8) 4 (2,8) 35 (24,3) |
|
Classificação da NYHA, n (%) I II |
40 (66,7) 20 (33,3) |
105 (72,9) 39 (27,1) |
| Duração da doença desde o diagnóstico de ATTRv- PN (meses), média (DP) | 39,3 (40,3) | 46,8 (58,1) |
| Duração desde o início dos sintomas de ATTRv-PN (meses), média (DP) | 64,0 (52,3) | 67,7 (50,9) |
|
Diagnosticado com cardiomiopatia amiloidótica familiar (CAF)4, n (%) Critérios utilizados para documentar o diagnóstico clínico de CAF4, n (%)5 Biópsia cardíaca Resultado de eco Outros |
22 (36,7)
5 (22,7) 17 (77,3) 0 |
39 (27,1)
1 (2,6) 24 (61,5) 24 (61,5) |
| Duração da doença desde o diagnóstico clínico de CAF4 da CRF (meses), média (DP) | 21,0 (22,5) | 18,5 (21,4) |
| Duração desde o início dos sintomas de CAF4 (meses), média (DP) | 34,1 (29,3) | 36,3 (63,8) |
| NT-proBNP (pmol/L), média (DP) | 82,0 (159,2) | 54,0 (122,6) |
| Questionário de saúde resumido com 36 itens (SF- 36) (Escore resumido do componente físico), média (DP) | 37,2 (9,8) | 39,7 (9,3) |
| Escore total de sintomas e alterações da neuropatia (NSC), média (DP) | 23,0 (12,6) | 23,1 (12,4) |
|
Escore de incapacidade da polineuropatia (PND), n (%) I II IIIa IIIb |
23 (38,3) 19 (31,7) 15 (25,0) 3 (5,0) |
56 (39,2) 61 (42,7) 16 (11,2) 10 (7,0) |
|
Índice de Massa Corporal (kg/m2) m média (DP) Mediana (Mín, Máx) |
60 24,2 (4,9) 23,8 (14,5, 39,8) |
138 24,4 (4,9) 24,1 (15,4, 35,4) |
|
Índice de Massa Corporal modificado (kg/m2 x g/L), m média (DP) Mediana (Mín, Máx) |
60 1049,89 (228,43) 1027,55 (668,7, 1710,0) |
138 1025,78 (235,12) 1003,14 (615,7, 1714,0) |
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
1 O estágio da doença é definido como estágio 1 = não requer assistência para deambulação e estágio 2 = requer assistência para deambulação.
2 Inclui os genótipos V30M, V50M, MUTAÇÃO V50M, VAL50MET e P.VAL50MET.
3 Baseado em banco de dados clínicos. Mutações não Val30Met incluídas: GLU89GLN, LEU58HIS, PHE64LEU, SER50ARG, SER77TYR, THR49ALA, THR60ALA, VAL122LLE e outras (incluindo ALA97SER).
4 Cardiomiopatia amiloidótica familiar = Amiloidose hereditária mediada por transtirretina com cardiomiopatia (ATTRv-CM).
5 O denominador para o cálculo percentual é o número de participantes com diagnóstico de CAF.
Apenas anos e meses foram coletados a partir da data de consentimento livre e esclarecido para calcular a duração da doença desde o diagnóstico e desde o início dos sintomas de ATTRv-PN, CAF.
N=número de participantes no conjunto de segurança; n=número de participantes em um subgrupo, m=número de participantes com dados não ausentes se diferente de N, CRF=ficha clínica; NT-proBNP=N-terminal do peptídeo natriurético tipo B; DP=desvio padrão.
Dos 39 pacientes (27,1%) do grupo eplontersena que apresentavam diagnóstico de cardiomiopatia por transtirretina (TTR) no início do estudo, 41,0% foram classificados como classe I e 59,0% como classe II da New York Heart Association (NYHA).
Análises da Semana 35 (análise interina)
O desfecho primário de eficácia foi a alteração desde o período basal até a Semana 35 no escore composto modificado do Neuropathy Impairment Score + 7 (mNIS+7). O escore composto mNIS+7 é uma avaliação objetiva da neuropatia e compreende os escores compostos NIS e Modificado +7. Na versão do escore composto mNIS+7 usada no estudo, o NIS mede objetivamente os déficits na função dos nervos cranianos, força muscular, reflexos e sensações, e o Modificado +7 avalia a resposta da frequência cardíaca à respiração profunda, testes sensoriais quantitativos (pressão de toque e dor por calor) e eletrofisiologia dos nervos periféricos. A versão validada do escore composto mNIS+7 usada no estudo teve um intervalo de -22,3 a 346,3 pontos, com pontuações mais altas representando uma maior severidade da doença.
O objetivo secundário foi a alteração desde o período basal no escore total do questionário Norfolk Quality of Life – Diabetic Neuropathy (QoL-DN). A escala Norfolk QoL-DN é uma avaliação relatada pelo participante que avalia a experiência subjetiva de neuropatia nos seguintes domínios: funcionamento físico/neuropatia de fibras grossas, atividades da vida diária, sintomas, neuropatia de fibras finas e neuropatia autonômica. A versão do escore total do Norfolk QoL-DN usada no estudo variou de -4 a 136 pontos, com pontuações mais altas representando maior comprometimento.
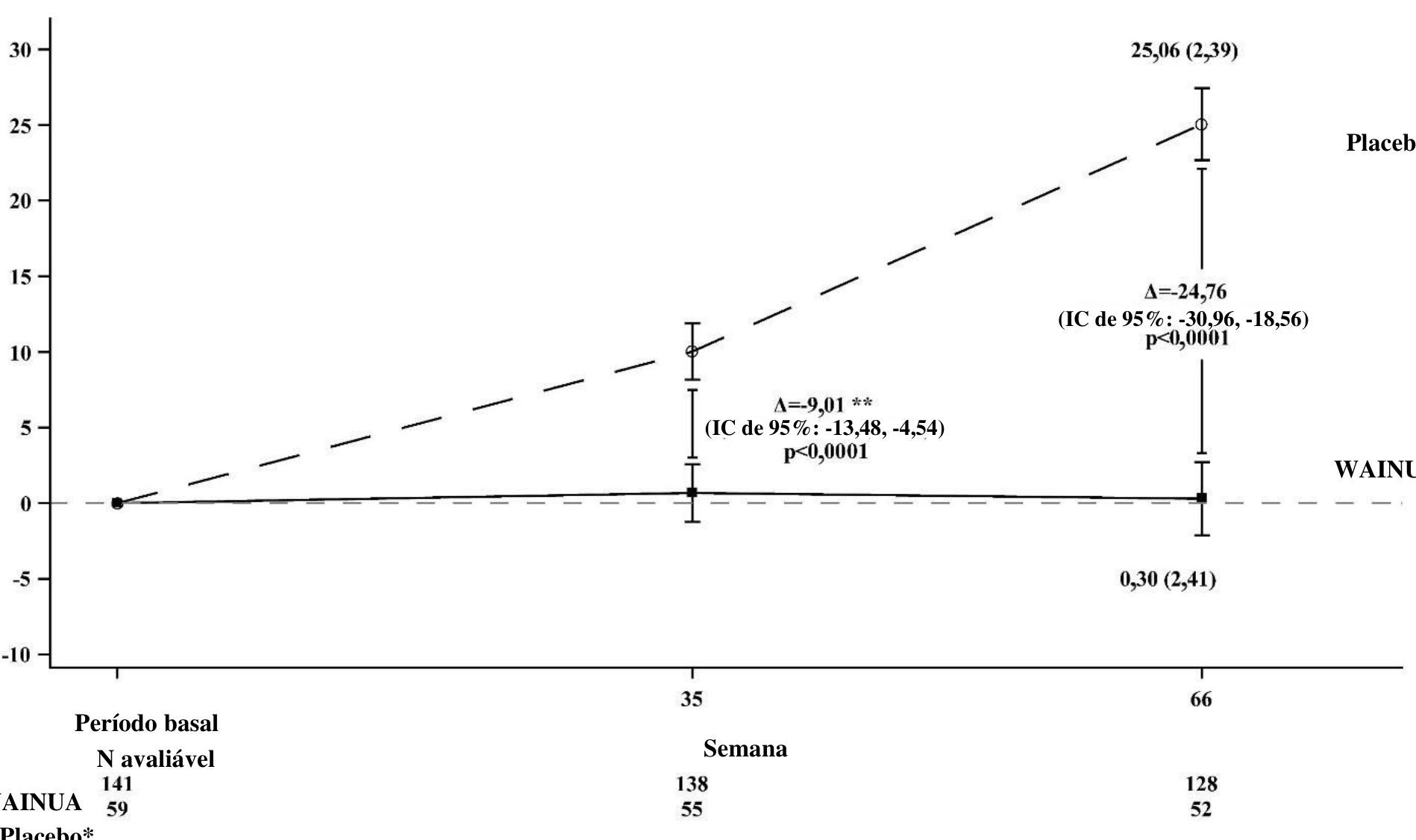
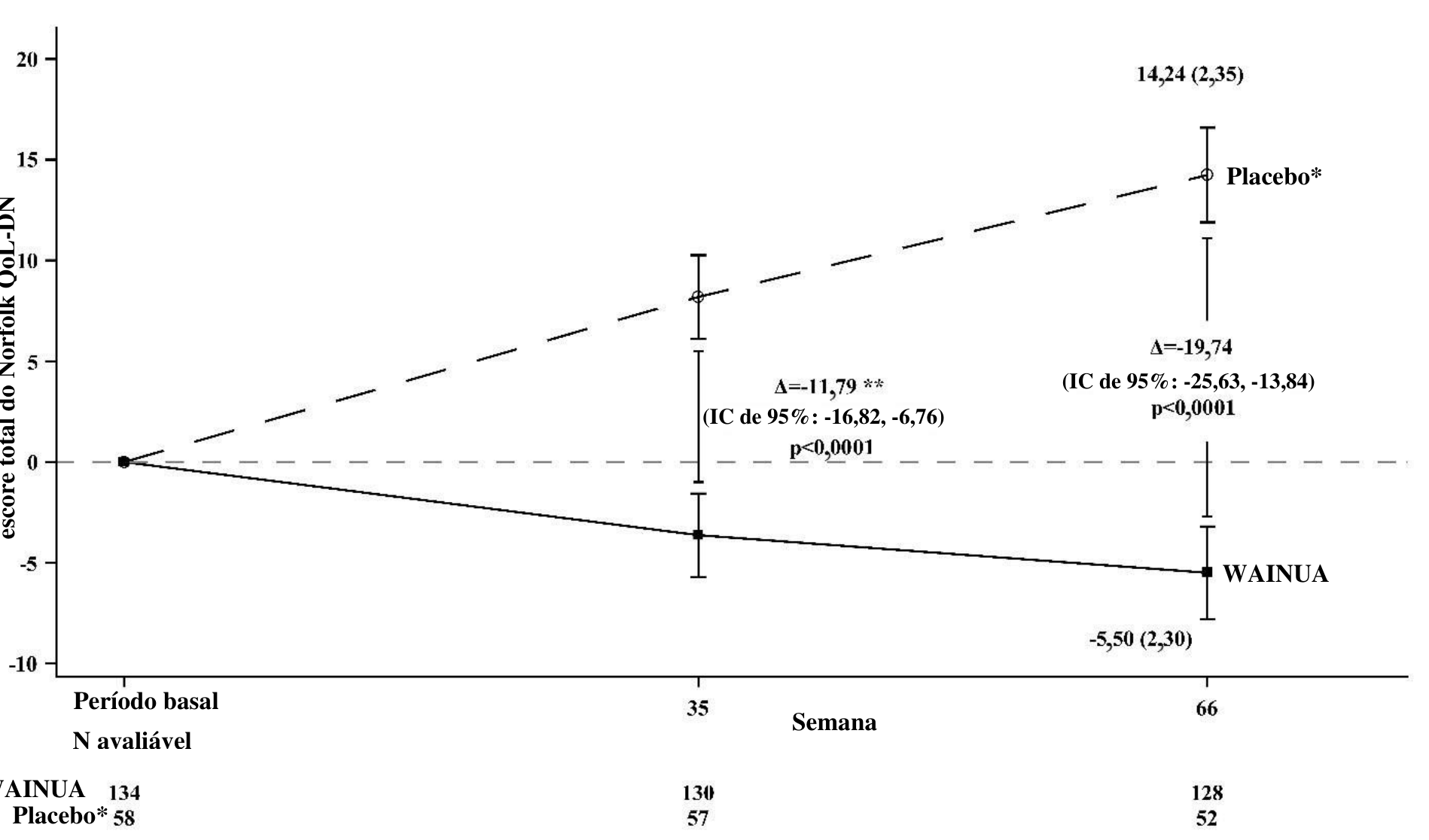
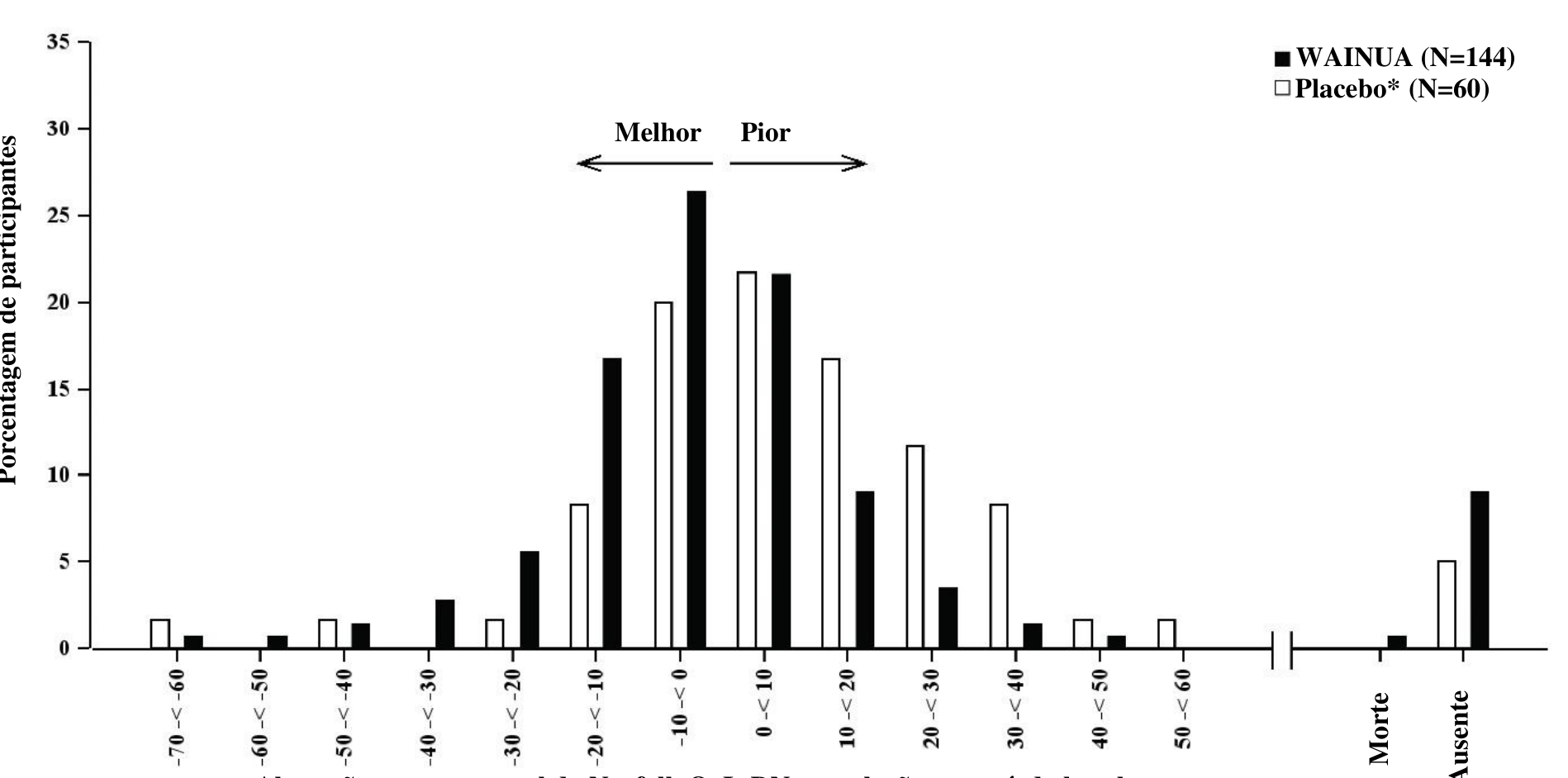
Wainua mostrou melhora estatisticamente significativa em comparação ao controle com placebo externo na Semana 35 para o escore composto mNIS+7 com diferença de LSM de -9,0 (IC de 95%: -13,5, -4,5; p<0,0001) (ver Figuras 1, 2a, 5a). Wainua mostrou melhora estatisticamente significativa em comparação ao controle externo com placebo na Semana 35 para o escore total do Norfolk QoL-DN com diferença de LSM de -11,8 (IC de 95%: -16,8, -6,8; p<0,0001) (Tabela 2 e Figuras 3, 4a, 6a).
Semana 65/66 (análise final)
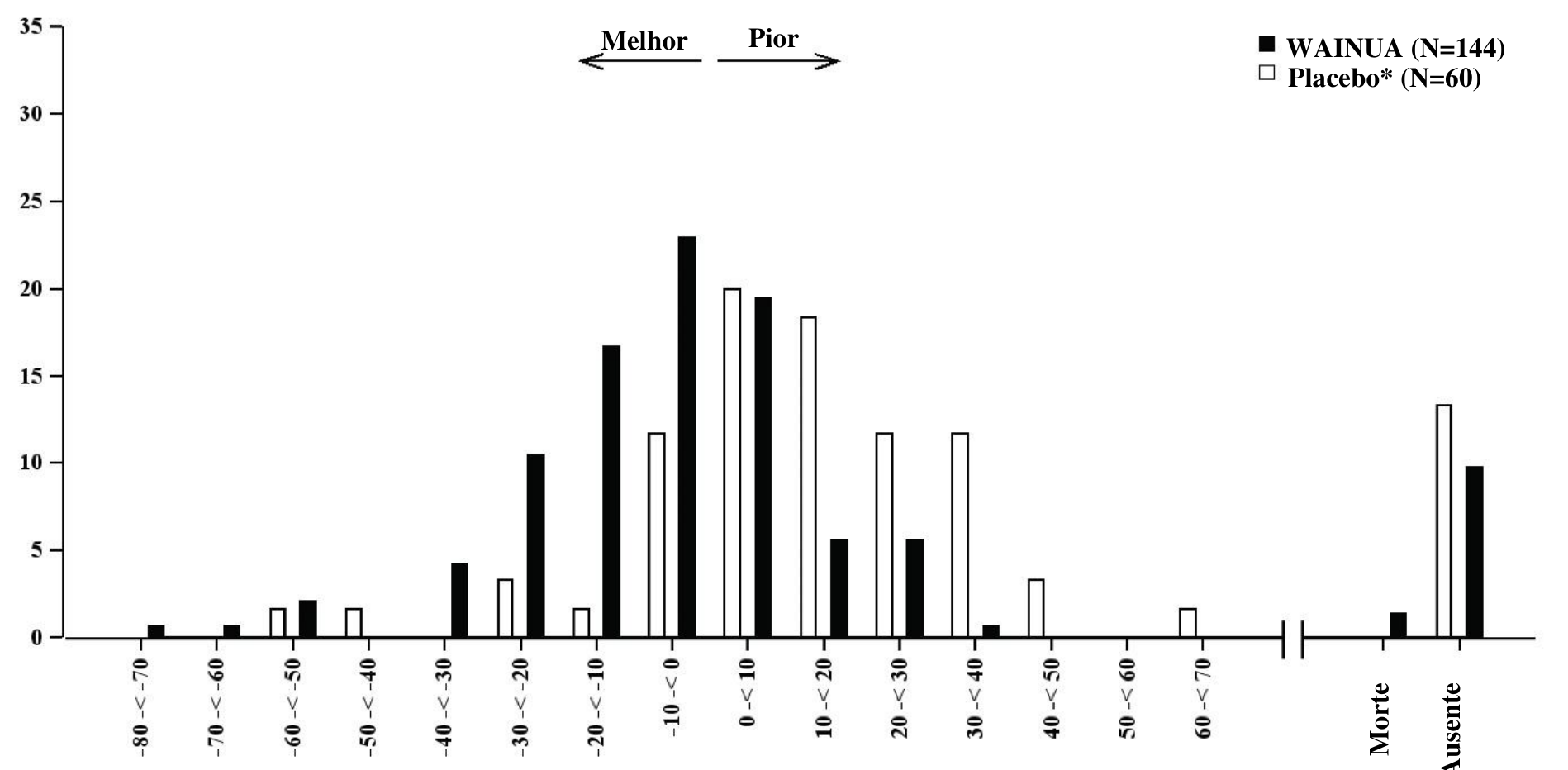
Os desfechos coprimários para o objetivo primário na análise final na Semana 66 incluíram alteração em relação ao período basal no escore composto mNIS+7 na Semana 66 e alteração em relação ao período basal no escore total do Norfolk QoL-DN na Semana 66. Além disso, os resultados na Semana 66 para o escore composto mNIS+7 e o escore total do Norfolk foram todos consistentes com os resultados da Semana 35 (ver Tabela 2 e Figuras 1, 2b, 3, 4b).
Os desfechos secundários foram alteração em relação ao período basal nos sintomas e alterações de neuropatia (NSC) nas Semanas 66 e 35, alteração em relação ao período basal no escore do componente físico (PCS) do questionário de saúde resumido de 36 itens (versão 2) (SF-36) na Semana 65, alteração em relação ao período basal no escore de incapacidade de polineuropatia (PND) na Semana 65 e alteração em relação ao período basal no índice de massa corporal modificado (IMCm) na Semana 65.
O NSC foi um questionário respondido pelo participante para quantificar o tipo, distribuição e severidade da fraqueza muscular, sintomas sensoriais, sintomas de dor e sintomas autonômicos. Escores mais altos representam sintomas piores.
O PCS do SF-36 incluiu 4 escalas que avaliam a função física, limitações de função causadas por problemas físicos, dores corporais e saúde geral. Escores mais altos representam melhor saúde física. O PND categoriza a incapacidade pela mobilidade (por exemplo, necessidade de bengala, muleta, cadeira de rodas ou cama). Escore do PND mais alto representa pior incapacidade.
O IMC modificado (IMC × albumina sérica) é um método aceitável de avaliação do status nutricional na ATTR.
Escores mais altos representam melhor status nutricional e são considerados um indicador de maior sobrevida em participantes com ATTRv-PN.
Todos os desfechos secundários mostraram superioridade estatisticamente significativa em relação ao placebo externo (ver Tabela 3).
Tabela 2 Efeito do tratamento para os desfechos primários e secundários principais (Estudo NEURO-TTRansform) (conjunto de análise completo)
|
Análise/Desfecho |
Período basal, Média (DP) |
Alteração em LSM/Alteração percentual em relação ao período basal, (SE) [IC de 95%] |
Wainua – Placebo Externo* Diferença em LSM (IC de 95%) |
Valor p |
||
|---|---|---|---|---|---|---|
|
Placebo externo* |
Wainua |
Placebo externo* |
Wainua |
|||
|
Semana 35 |
N = 59 |
N = 140 |
N = 59 |
N = 140 |
|
|
| Escore composto mNIS+7 2,3 Alteração em relação ao período basal | 74,1 (39,0) | 79,6 (42,3) | 9,2 (1,9) [5,54, 12,91] | 0,2 (1,9) [-3,46, 3,89] | -9,0 (-13,48, -4,54) | P < 0,0001 |
| Escore total do Norfolk QoL-DN 2,3 Alteração em relação ao período basal | 48,6 (27,0) | 43,5 (26,3) | 8,7 (2,1) [4,53, 12,81] | -3,1 (2,1) [-7,19, 0,96] | -11,8 (-16,82, -6,76) | P < 0,0001 |
|
Semana 65/66 |
N = 59 |
N = 141 |
N = 59 |
N = 141 |
|
|
| Escore composto mNIS+7 1 Alteração em relação ao período basal | 74,1 (39,0) | 79,8 (42,3) | 25,1 (2,4) [20,23, 29,88] | 0,3 (2,4) [-4,46, 5,06] | -24,8 (-30,96, -18,56) | p < 0,00014 |
| Escore total do Norfolk QoL-DN 1 Alteração em relação ao período basal | 48,6 (27,0) | 43,3 (26,2) | 14,2 (2,4) [9,51, 18,97] | -5,5 (2,3) [-10,03, -0,96] | -19,7 (-25,63, -13,84) | p < 0,00014 |
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
1 Com base no MMRM ajustado pelos pesos do escore de propensão com efeitos categóricos para tratamento, tempo, interação tratamento por tempo e estágio da doença, mutação Val30M, tratamento anterior e covariáveis fixas para o período basal e a interação período basal por tempo. Somente os dados até a Semana 66 são incluídos na análise da Semana 66.
2 Com base em um modelo ANCOVA ajustado pelo escore de propensão com os efeitos do tratamento, estágio da doença, mutação Val30M, tratamento anterior e valor basal. Somente os dados até a Semana 35 são incluídos na análise interina.
3 Participantes com ausência de mNIS+7 ou Norfolk QoL-DN na Semana 35 tiveram o valor imputado multiplamente usando um modelo de imputação. Cada um dos 500 conjuntos de dados imputados foi analisado usando o modelo ANCOVA simples e os 500 resultados do modelo ANCOVA foram combinados usando as regras de Rubin.
4 Não testado formalmente devido a resultados estatisticamente significativos na Semana 35. Análise baseada em dados coletados até 52 dias após a última dose do medicamento do estudo. Dados da Semana 35 da análise interina e dados da Semana 65/66 da análise da Semana 66. No Conjunto de Análise Completo, o grupo eplontersena incluiu 140 participantes na Semana 35 e 141 participantes na Semana 66. Um participante não teve uma avaliação de mNIS+7 ou Norfolk QoL-DN na Semana 35, mas teve uma avaliação para pelo menos um deles na Semana 66.
ANCOVA = análise de covariância; IC = intervalo de confiança; LSM = média dos mínimos quadrados; MMRM = modelo de efeitos mistos com medidas repetidas; mNIS+7 = Neuropathy Impairment Score modificado +7; N = número de participantes no grupo; Norfolk QoL-DN = questionário Norfolk Quality of Life – Diabetic Neuropathy; DP = desvio padrão; SE = erro padrão; TTR = transtirretina.
Tabela 3: Teste hierárquico de desfechos secundários (estudo NEURO-TTRansform)
| Desfecho secundário/ Grupo de tratamento (N) |
n | Alteração em relação ao período basal LSM (IC de 95%) |
Comparação de Wainua versus placebo externo* | ||
|---|---|---|---|---|---|
| Estimativa | IC de 95% | Valor p | |||
|
Alteração em LSM em NSC em relação ao período basal na Semana 66 |
|||||
| Wainua (N=141) | 132 | 0,0 (-1,92, 1,86) | -8.2 | -10,65, -5,76 | <0,0001 |
| Placebo externo* (N = 59) | 52 | 8,2 (6,24, 10,12) | |||
|
Alteração em LSM em NSC em relação ao período basal na Semana 35 |
|||||
| Wainua (N=141) | 141 | 0,8 (-0,92, 2,50) | -3,9 | -6,08, -1,80 | 0,0005 |
| Placebo externo* (N = 59) | 56 | 4,7 (2,98, 6,48) | |||
|
Alteração em LSM em PCS do SF-36 em relação ao período basal na Semana 65 |
|||||
| Wainua (N=141) | 136 | 0,85 (-0,711, 2,412) | 5,31 | 3,195, 7,416 | <0,0001 |
| Placebo externo* (N = 59) | 50 | -4,46 (-6,139, -2,770) | |||
|
Alteração em LSM no escore PND em relação ao período basal na Semana 65 |
|||||
| Wainua (N=141) | 134 | 0,1 (0,0, 0,2) | -0,2 | -0,4, 0,0 | 0,0241 |
| Placebo externo* (N = 59) | 51 | 0,3 (0,2, 0,4) | |||
|
Alteração em LSM em IMCm em relação ao período basal na Semana 65 |
|||||
| Wainua (N=141) | 130 | -8,1 (-28,55, 12,42) | 82,7 | 54,64, 110,76 | <0,0001 |
| Placebo externo* (N = 59) | 49 | -90,8 (-112,84, -68,69) | |||
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
N=Número de participantes no Conjunto de análise completo na Semana 66.
n=Número de participantes com dados não ausentes nas covariáveis do período basal e alteração em relação ao período basal no momento.
Análise baseada em dados coletados até 28 dias após a última dose do medicamento do estudo. A janela de visita de análise da Semana 65 vai do Dia 419 ao Dia 479.
Com base em um modelo de efeitos mistos com medidas repetidas (MMRM) ajustado pelos pesos do escore de propensão com efeitos categóricos para tratamento, tempo, interação tratamento por tempo e estágio da doença, mutação Val30M, tratamento anterior e covariáveis fixas para o período basal e a interação período basal por tempo. Somente os dados até a Semana 65 são incluídos na análise final da Semana 66.
IC = intervalo de confiança; LSM = média dos mínimos quadrados; IMCm = índice de massa corporal modificado; NSC = sintomas e alterações da neuropatia; PND = incapacidade da polineuropatia; PCS = escore do componente físico; SF?36 PCS= Escore do Componente Físico do questionário de pesquisa de saúde resumido de 36 itens.
Figura 1: Alteração na LSM no escore composto mNIS+7 desde o período basal (Estudo NEURO-TTRansform) (conjunto de análise completo)
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
** A diferença de tratamento apresenta resultados da análise interina formal da Semana 35. Com base no MI ANCOVA ajustado pelos pesos do escore de propensão com efeitos categóricos fixos para tratamento, estágio da doença, mutação Val30Met, tratamento anterior e covariáveis fixas para o período basal. Somente os dados até a Semana 35 são incluídos na análise interina da Semana 35.
Análise da Semana 66 baseada no MMRM ajustado pelos pesos do escore de propensão com efeitos categóricos para tratamento, tempo, interação tratamento por tempo e estágio da doença, mutação Val30Met, tratamento anterior e covariáveis fixas para o período basal e a interação período basal por tempo.
Análise baseada em dados coletados até 52 dias após a última dose do medicamento do estudo. Os dados até a Semana 66 estão incluídos.
A média de diferença de tratamento dos LS da Semana 35 e da Semana 66 (Wainua – Placebo) com IC de 95% (não ajustado) é apresentada.
IC = Intervalo de confiança; Média dos LS = Média dos mínimos quadrados; EPM = erro padrão da média, MI ANCOVA = Análise de covariância de imputação múltipla; MMRM = Modelo de efeitos mistos com medidas repetidas.
11
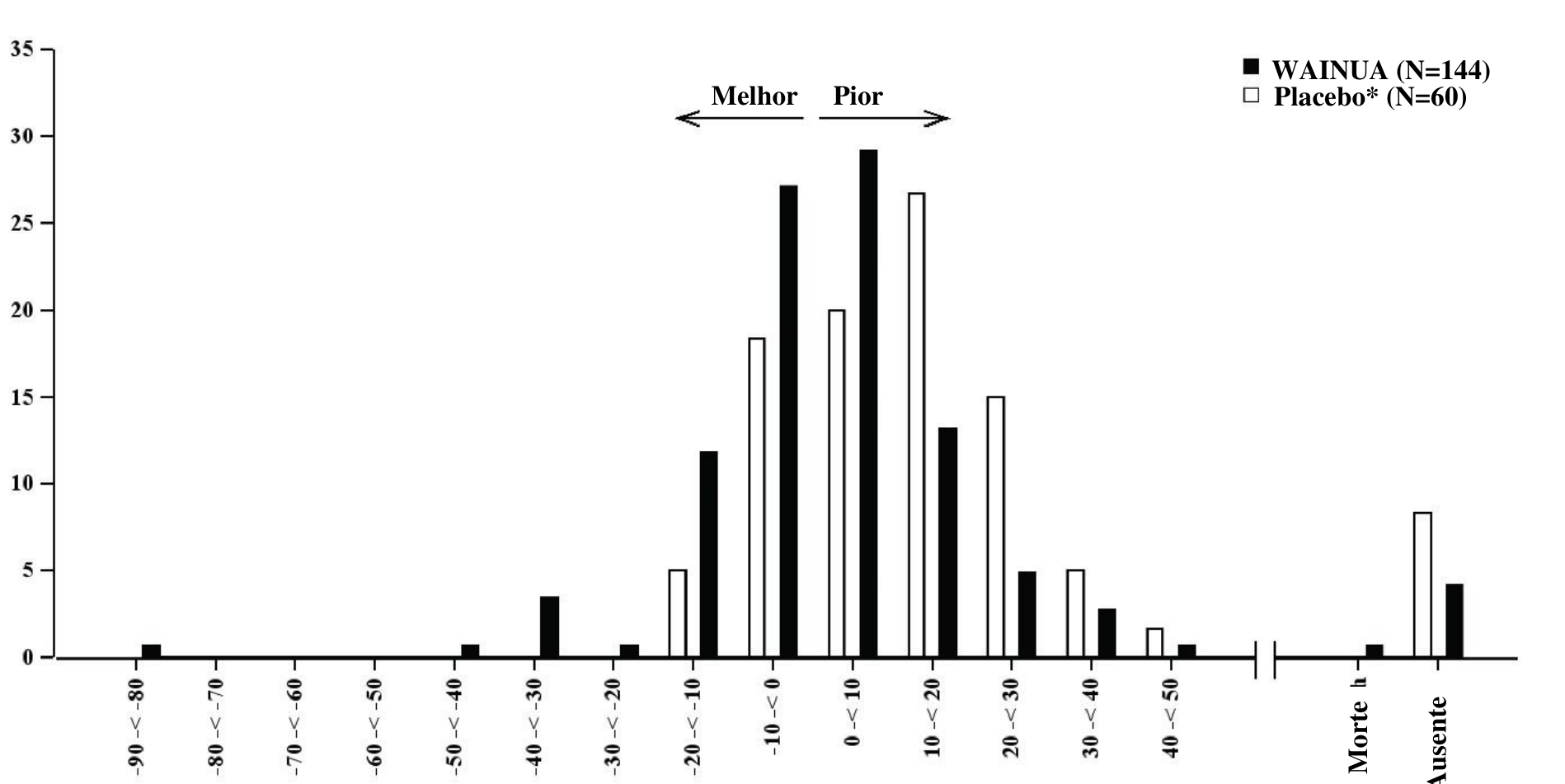
Figura 2: Histograma da alteração do escore composto mNIS+7 em relação ao período basal (Estudo NEURO-TTRansform) (conjunto de análise de segurança)
a) na Semana 35
Alteração do escore composto mNIS +7 desde o período basal na Semana 35
*Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
b) na semana 66
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
Figura 3: Alteração na LSM no escore total do Norfolk QoL-DN desde o período basal (Estudo NEURO-TTRansform)
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
** A diferença de tratamento apresenta resultados da análise interina formal da Semana 35. Com base no MI ANCOVA ajustado pelos pesos do escore de propensão com efeitos categóricos fixos para tratamento, estágio da doença, mutação Val30Met, tratamento anterior e covariáveis fixas para o período basal. Somente os dados até a Semana 35 são incluídos na análise interina da Semana 35.
Análise da Semana 66 baseada no MMRM ajustado pelos pesos do escore de propensão com efeitos categóricos para tratamento, tempo, interação tratamento por tempo e estágio da doença, mutação Val30Met, tratamento anterior e covariáveis fixas para o período basal e a interação período basal por tempo.
Análise baseada em dados coletados até 52 dias após a última dose do medicamento do estudo. Os dados até a Semana 66 estão incluídos.
A média de diferença de tratamento dos LS da Semana 35 e da Semana 66 (Wainua – Placebo) com IC de 95% (não ajustado) é apresentada.
IC = Intervalo de confiança; Média dos LS = Média dos mínimos quadrados; EPM = erro padrão da média, MI ANCOVA = Análise de covariância de imputação múltipla; MMRM = Modelo de efeitos mistos com medidas repetidas.
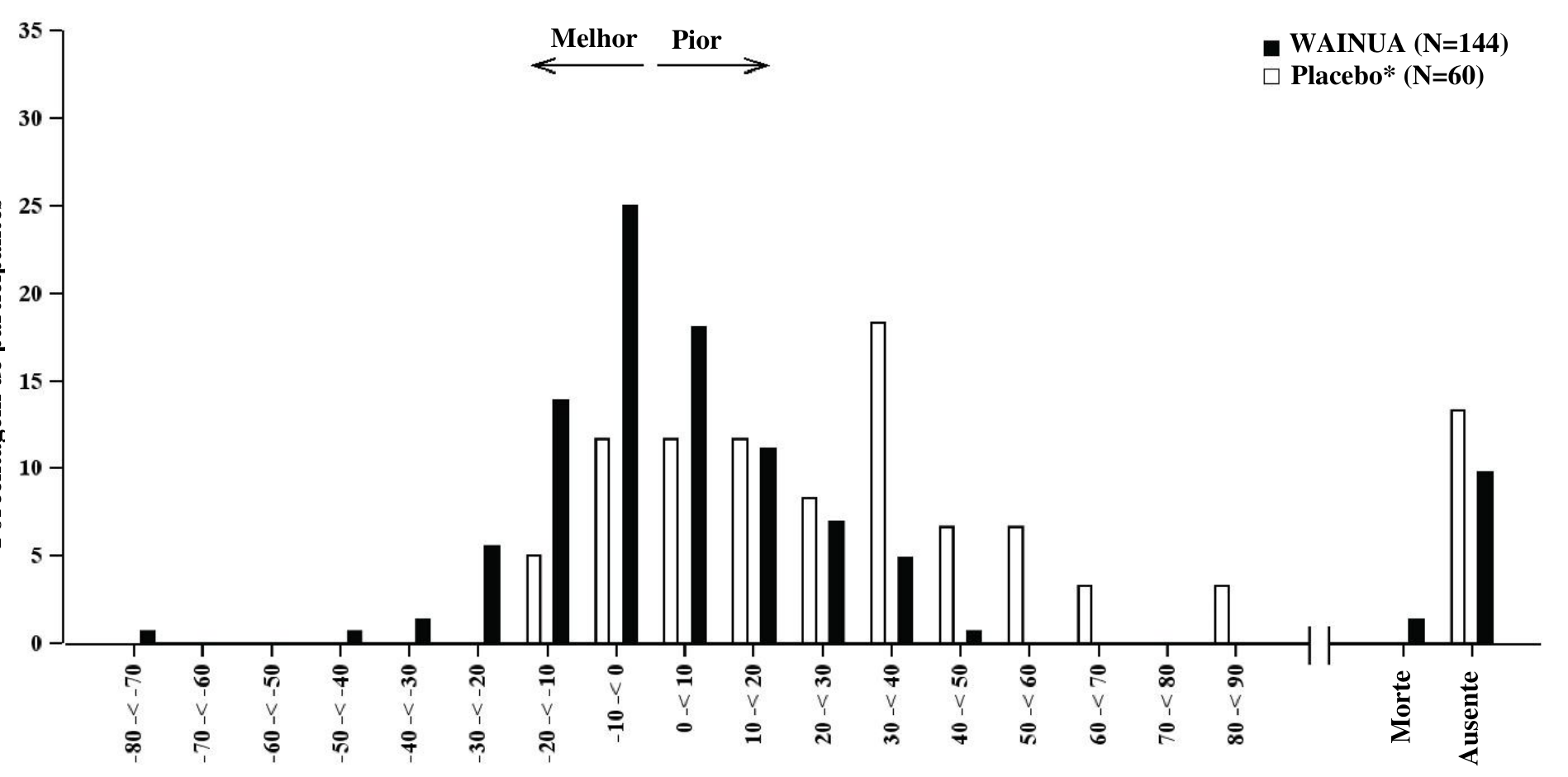
Figura 4: Histograma da alteração do escore total do Norfolk QoL-DN em relação ao período basal (Estudo NEURO-TTRansform) (conjunto de análise de segurança)
a) na Semana 35
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
b) na Semana 66
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
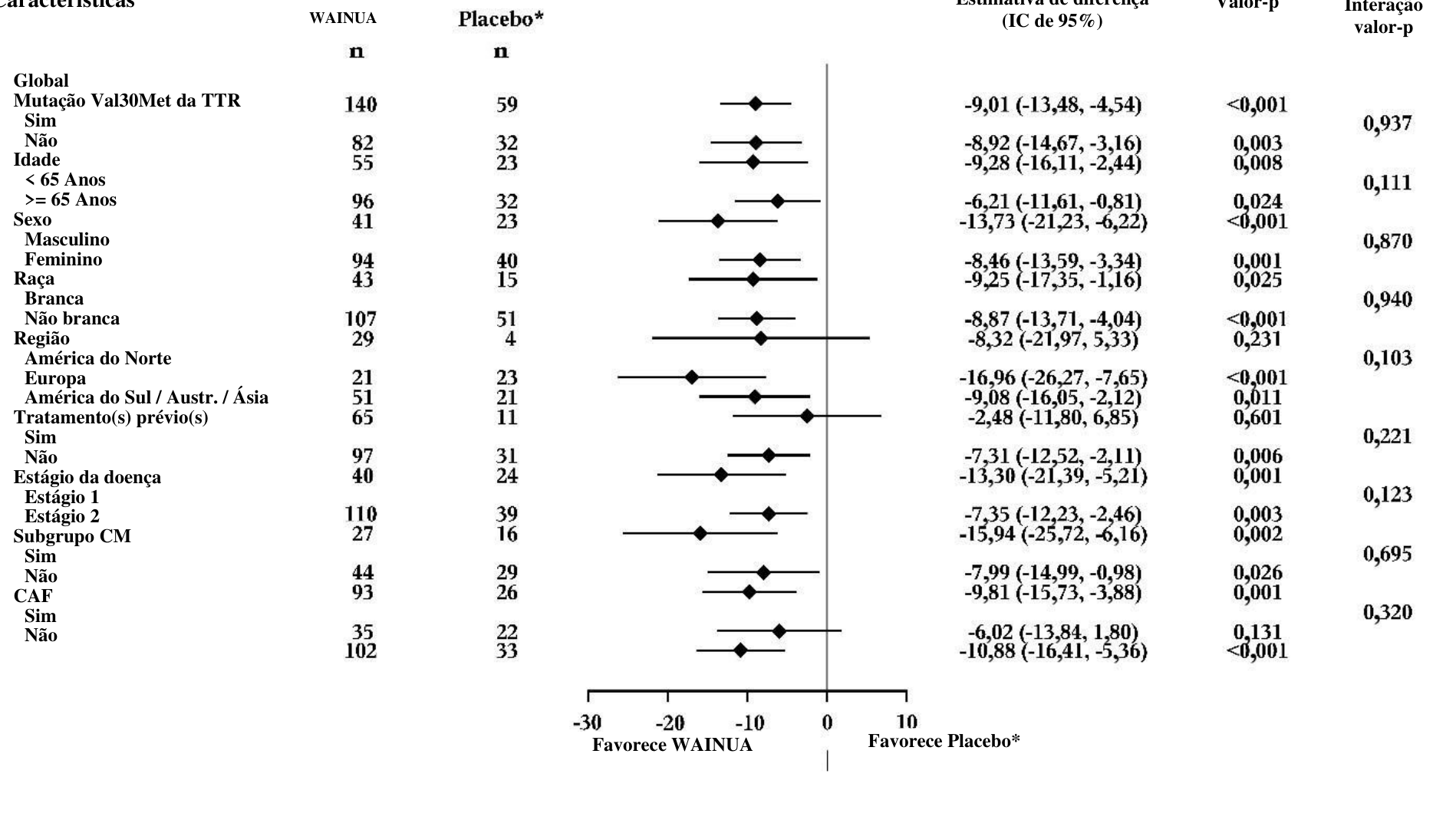
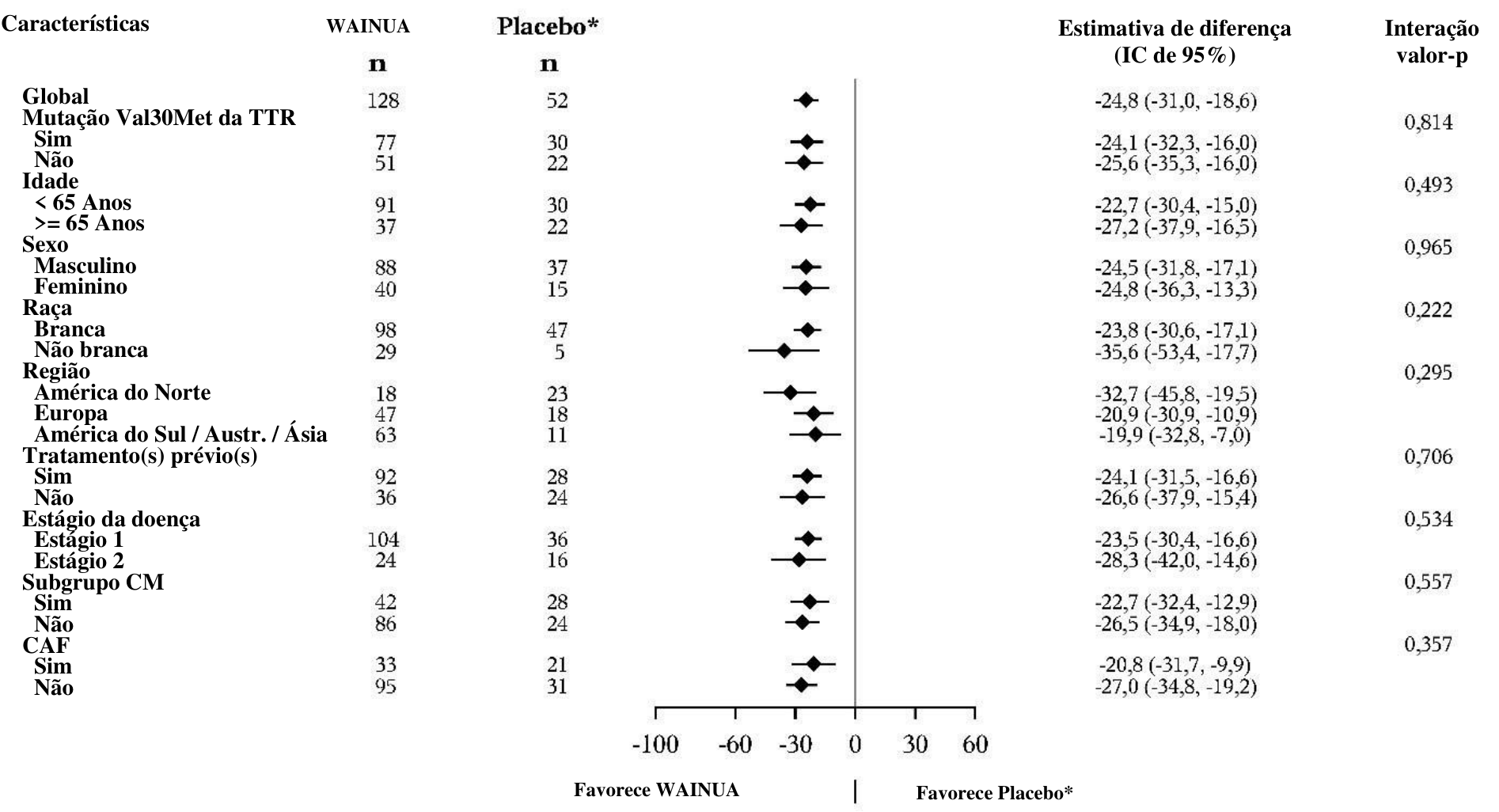
Tanto na Semana 35 quanto na Semana 65/66, os participantes que receberam Wainua apresentaram melhoras semelhantes em relação ao placebo no escore composto mNIS+7 e escore total do Norfolk QoL-DN em todos os subgrupos, incluindo idade, sexo, raça, região, status de mutação Val30Met, status de cardiomiopatia, diagnóstico de CAF basal e estágio da doença (Figuras 5a e b e 6a e b).
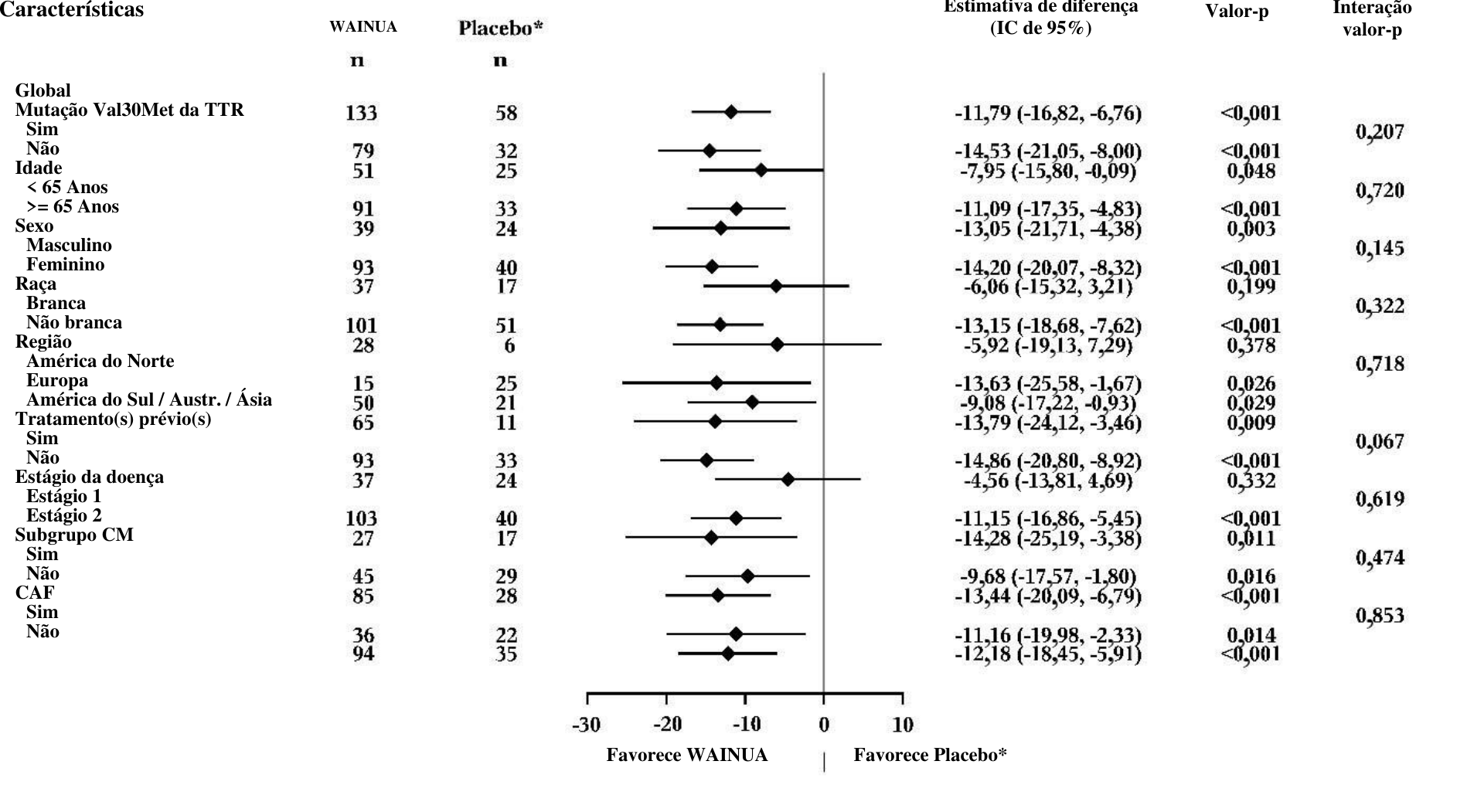
Figura 5: Gráfico de floresta da diferença de tratamento na LSM para alteração em relação ao período basal no escore composto mNIS+7 para subgrupos principais (Estudo NEURO-TTRansform) (conjunto de análise completo)
a) na semana 35
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
[a] Tratamento anterior com tafamidis ou diflunisal.
O subgrupo CM inclui participantes com diagnóstico de CAF no início do estudo ou espessura basal da parede do septo IV ≥ 13 mm sem hipertensão [histórico ou diagnóstico durante o estudo].
A diferença nas médias dos LS, intervalos de confiança e valores p são baseados em um modelo ANCOVA ajustado pelo escore de propensão com os efeitos do tratamento, fatores de subgrupo, estágio da doença, mutação Val30Met, tratamento anterior, interação tratamento por subgrupo e valor basal. Os dados até a Semana 35 são incluídos na análise da Semana 35.
b) na semana 66
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
[a] Tratamento anterior com tafamidis ou diflunisal.
Com base no MMRM ajustado pelos pesos do escore de propensão com efeitos categóricos para tratamento, tempo, interação tratamento por tempo e estágio da doença, mutação Val30Met, tratamento anterior e covariáveis fixas para o período basal e a interação período basal por tempo.
Os modelos de subgrupo também incluíram interações de tratamento por subgrupo, tempo por subgrupo e tratamento por tempo por subgrupo. Os dados até a Semana 66 estão incluídos.
O subgrupo CM inclui participantes com diagnóstico de CAF no início do estudo ou espessura basal da parede do septo IV ≥ 13 mm sem hipertensão [histórico ou diagnóstico durante o estudo].
A LSM da diferença de tratamentos na Semana 66 (Wainua – Placebo) com IC de 95% (não ajustado) é apresentada.
IC = Intervalo de confiança; LSM = Média dos mínimos quadrados; MMRM = Modelo de efeitos mistos com medidas repetidas, CM = cardiomiopatia, CAF = cardiomiopatia amiloidótica familiar.
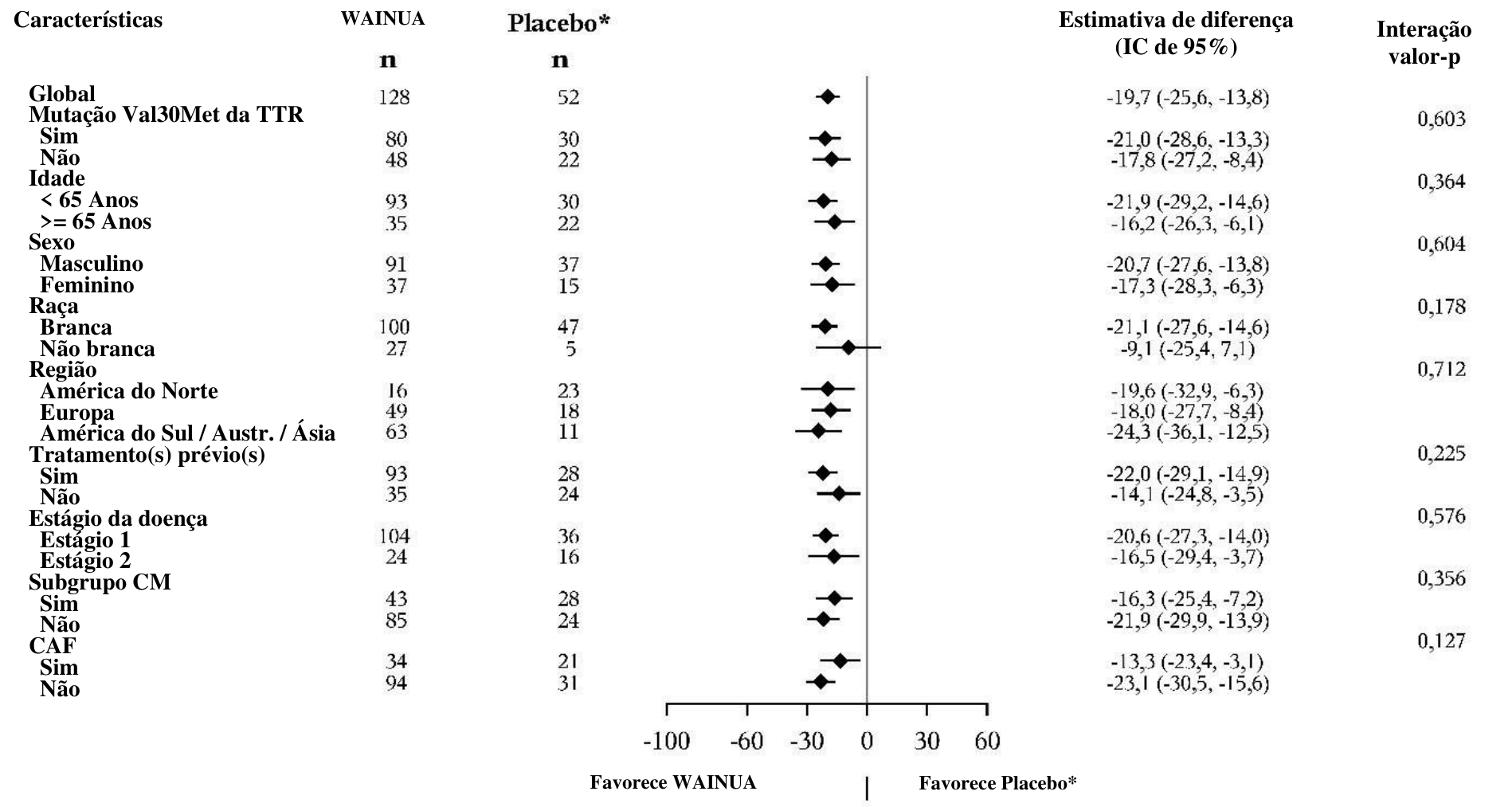
Figura 6: Gráfico de floresta da diferença de tratamento em LSM para a alteração em relação ao período basal no escore total do Norfolk QoL-DN para subgrupos principais (Estudo NEURO-TTRansform) (conjunto de análise completo)
a) na Semana 35
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
[a] Tratamento anterior com tafamidis ou diflunisal.
O subgrupo CM inclui participantes com diagnóstico de CAF no início do estudo ou espessura basal da parede do septo IV
≥ 13 mm sem hipertensão [histórico ou diagnóstico durante o estudo].
A diferença nas médias dos LS, intervalos de confiança e valores p são baseados em um modelo ANCOVA ajustado pelo escore de propensão com os efeitos do tratamento, fatores de subgrupo, estágio da doença, mutação Val30Met, tratamento anterior, interação tratamento por subgrupo e valor basal. Somente os dados até a Semana 35 são incluídos na análise interina da Semana 35.
b) na semana 66
* Grupo placebo externo de outro estudo controlado randomizado (NEURO-TTR).
[a] Tratamento anterior com tafamidis ou diflunisal.
Com base no MMRM ajustado pelos pesos do escore de propensão com efeitos categóricos para tratamento, tempo, interação tratamento por tempo e estágio da doença, mutação Val30Met, tratamento anterior e covariáveis fixas para o período basal e a interação período basal por tempo.
Os modelos de subgrupo também incluíram interações de tratamento por subgrupo, tempo por subgrupo e tratamento por tempo por subgrupo. Os dados até a Semana 66 estão incluídos.
O subgrupo CM inclui participantes com diagnóstico de CAF no início do estudo ou espessura basal da parede do septo IV ≥ 13 mm sem hipertensão [histórico ou diagnóstico durante o estudo].
A LSM da diferença de tratamentos na Semana 66 (Wainua – Placebo) com IC de 95% (não ajustado) é apresentada.
IC = Intervalo de confiança; LSM = Média dos mínimos quadrados; MMRM = Modelo de efeitos mistos com medidas repetidas, CM = cardiomiopatia, CAF = cardiomiopatia amiloidótica familiar.
Referências bibliográficas
ION-682884-CS3 (NEUROTTRansform): A Phase 3 Global, Open-Label, Randomized Study to Evaluate the Efficacy and Safety of ION-682884 in Patients with Hereditary Transthyretin-Mediated Amyloid Polyneuropathy
CARACTERÍSTICAS FARMACOLÓGICAS
Mecanismo de ação
Eplontersena é um oligonucleotídeo antisense (ASO) quimérico modificado com 2′-O-2-metoxietil (2′-MOE) conjugado com GalNAc com uma estrutura mista de ligações internucleotídicas de fosforotioato (PS) e diéster de fosfato (PO). O conjugado de GalNAc permite a distribuição direcionada do ASO aos hepatócitos. A ligação seletiva de eplontersena ao RNA mensageiro (mRNA) da TTR (transtirretina) nos hepatócitos provoca a degradação do mRNA da TTR mutante e do tipo selvagem (normal). Isto impede a síntese da proteína TTR no fígado, resultando em reduções significativas nos níveis de proteína TTR mutada e de tipo selvagem secretada pelo fígado para a circulação.
A TTR é uma proteína transportadora da proteína 4 de ligação ao retinol (RBP4), que é o principal transportador da vitamina A (retinol). Portanto, espera-se que uma redução na TTR plasmática resulte na redução dos níveis plasmáticos de retinol para abaixo do limite inferior do normal.
TTR é uma proteína transportadora menor de tiroxina. O principal transportador de tiroxina é a globulina de ligação à tiroxina. Conforme Classificação ATC, a classe terapêutica da eplontersena é ‘Outros medicamentos para o sistema nervoso’, código N07XX21.
Eletrofisiologia cardíaca
Estudos formais de QTc não foram realizados com Wainua. O potencial de prolongamento do intervalo QTc com eplontersena foi avaliado num estudo randomizado, controlado por placebo, em voluntários saudáveis. Com uma dose 2,7 vezes a dose recomendada de 45 mg de eplontersena, não foi observado efeito clinicamente relevante no intervalo QT.
Imunogenicidade
No estudo clínico em participantes com ATTRv-PN, após um período de tratamento de 84 semanas (duração mediana do tratamento de 561 dias (80 semanas), intervalo de 57 a 582 dias), 58 participantes (40,3%) desenvolveram anticorpos antimedicamento emergentes do tratamento (ADAs).
Nos participantes com resultados positivos para anticorpos antieplontersena, não houve impacto clinicamente significativo na eficácia, segurança, farmacocinética ou farmacodinâmica de Wainua.
Propriedades Farmacocinéticas
As propriedades farmacocinéticas (PK) de Wainua foram avaliadas após administração subcutânea de doses únicas e múltiplas (uma vez a cada 4 semanas) em participantes saudáveis e doses múltiplas (uma vez a cada 4 semanas) em participantes com ATTRv-PN.
Absorção
Após a administração subcutânea, a eplontersena é absorvida rapidamente na circulação sistêmica atingindo as concentrações plasmáticas máximas em aproximadamente 2 horas, com base nas estimativas populacionais.
Distribuição
Com base em estudos em animais (camundongo, rato e macaco), a eplontersena distribui-se principalmente no córtex hepático e renal após administração subcutânea. Eplontersena liga-se fortemente às proteínas plasmáticas humanas (>98%). As estimativas populacionais para o volume de distribuição central aparente é de 12,9 L e o volume de distribuição periférico aparente é de 11.100 L.
Biotransformação
Eplontersena é metabolizada por endo e exonucleases em pequenos fragmentos de oligonucleotídeos de tamanhos variados no fígado. Não houve metabólitos circulantes importantes em humanos. Agentes terapêuticos com oligonucleotídeos, incluindo eplontersena, normalmente não são metabolizados pelas enzimas CYP.
Eliminação
Eplontersena é eliminada principalmente por metabolismo seguido de excreção renal dos metabólitos oligonucleotídicos curtos. A fração média de ASO inalterado eliminado na urina foi inferior a 1% da dose administrada em 24 horas. A meia-vida de eliminação terminal é de aproximadamente 3 semanas com base nas estimativas populacionais.
Linearidade/não linearidade
A Cmax e a AUC de eplontersena mostraram um aumento ligeiramente maior que o proporcional à dose após doses subcutâneas únicas variando de 45 a 120 mg (ou seja, 1 a 2,7 vezes a dose recomendada) em voluntários saudáveis.
As estimativas populacionais de concentrações máximas em estado estacionário (Cmax), concentrações mínimas (Cmin) e área sob a curva (AUCτ) foram 0,218 μg/mL, 0,000200 μg/mL e 1,95 μg h/mL, respectivamente, após administração de 45 mg uma vez a cada 4 semanas em participantes com ATTRv-PN. Não foi observado acúmulo de Cmax e AUC de eplontersena no plasma após doses repetidas (uma vez a cada 4 semanas). O acúmulo foi observado na Cmin e o estado estacionário é alcançado após aproximadamente 17 semanas.
Populações especiais
Com base na análise farmacocinética e farmacodinâmica da população, o peso corporal, o sexo, a raça e o status da mutação Val30Met não têm qualquer efeito clinicamente significativo na exposição a eplontersena ou nas reduções séricas da TTR no estado estacionário. As avaliações definitivas foram limitadas em alguns casos, uma vez que as covariáveis foram limitadas pelos números globais baixos.
População idosa: Não foram observadas diferenças globais na farmacocinética entre participantes adultos e idosos (≥65 anos de idade).
Comprometimento renal: Não foram realizados estudos clínicos formais para investigar o efeito do comprometimento renal na PK da eplontersena. Uma análise farmacocinética e farmacodinâmica populacional não mostrou diferenças clinicamente significativas na farmacocinética ou farmacodinâmica da eplontersena com base em comprometimento renal leve e moderado (TFGe ≥45 a <90 mL/min). Eplontersena não foi estudada em participantes com comprometimento renal severo ou em participantes com doença renal em fase terminal.
Comprometimento hepático: Não foram realizados estudos clínicos formais para investigar o efeito do comprometimento hepático na eplontersena. Uma análise farmacocinética e farmacodinâmica populacional não mostrou diferenças clinicamente significativas na farmacocinética ou farmacodinâmica da eplontersena com base em comprometimento hepático leve (bilirrubina total ≤1 x ULN e AST >1 x ULN, ou bilirrubina total >1,0 a 1,5 x ULN e qualquer AST) .
Eplontersena não foi estudada em participantes com comprometimento hepático moderado ou severo ou em participantes com transplante hepático prévio.
Interação medicamentosa
Não foram realizados estudos clínicos formais de interação medicamentosa. Estudos in vitro indicam que a eplontersena não é um substrato ou inibidor de transportadores, não interage com medicamentos com forte ligação às proteínas plasmáticas e não é um inibidor ou indutor das enzimas CYP. Agentes terapêuticos oligonucleotídicos, incluindo a eplontersena, normalmente não são substratos das enzimas CYP. Portanto, não se espera que eplontersena cause ou seja afetada por interações medicamento-medicamento mediadas por transportadores de medicamentos, ligação às proteínas plasmáticas ou enzimas CYP.
Dados de segurança pré-clínica
Toxicidade não clínica/de doses repetidas A administração repetida de eplontersena ou substituto específico para roedores produziu redução nos níveis de mRNA da TTR hepática (reduções de até ~62% e 82% em macacos e camundongos, respectivamente), com reduções subsequentes nos níveis de proteína plasmática da TTR (redução de até 70% em macacos). Não houve resultados toxicologicamente relevantes relacionados com esta inibição farmacológica da expressão da TTR.
A maioria dos achados observados após doses repetidas por até 6 meses em camundongos e 9 meses em macacos foram relacionados à captação e acúmulo de eplontersena e não foram considerados adversos. Achados microscópicos relacionados à captação de eplontersena foram observados por vários tipos de células em múltiplos órgãos de todas as espécies animais testadas, incluindo monócitos/macrófagos, epitélio tubular proximal do rim, células de Kupffer do fígado e infiltrados de células histiocíticas em linfonodos e locais de injeção.
Contagens de plaquetas severamente diminuídas associadas a hemorragia espontânea foram observadas em um estudo de toxicidade subcrônica em um macaco na dose mais alta testada (24 mg/kg/semana). Achados semelhantes não foram observados em macacos que receberam uma dose média de 6 mg/kg/semana, que é 73 vezes a AUC humana na dose terapêutica recomendada de eplontersena.
Mutagenicidade e carcinogenicidade
Eplontersena não exibiu potencial genotóxico in vitro e in vivo e não foi carcinogênico em camundongos transgênicos ras.H2.
Eplontersena foi negativa para genotoxicidade em estudos in vitro (mutagenicidade bacteriana, aberração cromossômica no pulmão de hamster chinês) e in vivo (micronúcleo da medula óssea de camundongos).
Em um estudo de carcinogenicidade subcutânea em camundongos transgênicos ras.H2, eplontersena foi administrada por 26 semanas em doses de 250, 500 e 1,500 mg/kg/mês. Não houve evidência de carcinogenicidade para eplontersena após 26 semanas de tratamento em camundongos.
Toxidade reprodutiva
Toxicidade embriofetal/no desenvolvimento/Fertilidade
Eplontersena não teve efeitos na fertilidade ou no desenvolvimento embriofetal em camundongos até 38 vezes a dose mensal humana recomendada de 45 mg. Eplontersena não é farmacologicamente ativa em camundongos.
No entanto, não foi observado nenhum efeito na fertilidade ou no desenvolvimento embriofetal com um análogo específico de eplontersena em camundongos, que foi associado a uma inibição >90% da expressão de mRNA de TTR.
CONTRAINDICAÇÕES
Wainua é contraindicado em pacientes com hipersensibilidade prévia a eplontersena ou a qualquer um dos excipientes da formulação (veja item Identificação do Medicamento - COMPOSIÇÃO).
ADVERTÊNCIAS E PRECAUÇÕES
Níveis séricos reduzidos de vitamina A e suplementação recomendada
Com base no mecanismo de ação, espera-se que Wainua reduza a vitamina A sérica (retinol) abaixo dos níveis normais (ver seção 3. Características Farmacológicas - Propriedades Farmacodinâmicas).
Quaisquer sintomas ou sinais relacionados à deficiência de vitamina A devem ser avaliados antes de iniciar o tratamento com Wainua.
Os pacientes que recebem Wainua devem tomar suplementação oral da dose diária recomendada de vitamina A para reduzir o risco potencial de sintomas oculares devido à deficiência de vitamina A. Recomenda-se encaminhamento para avaliação oftalmológica se os pacientes desenvolverem sintomas oculares consistentes com deficiência de vitamina A, incluindo visão noturna reduzida ou cegueira noturna e olhos secos persistentes.
Não se sabe se a suplementação de vitamina A durante a gravidez será suficiente para prevenir a deficiência de vitamina A se a mulher grávida continuar a receber Wainua (ver seção 5. Advertências e Precauções - Gravidez). No entanto, devido ao mecanismo de ação da eplontersena, é improvável que o aumento da suplementação de vitamina A acima da dose diária recomendada durante a gravidez corrija os níveis séricos de retinol e pode ser prejudicial para a mãe e o feto.
Efeitos na habilidade de dirigir e operar máquinas
Wainua tem influência nula ou insignificante sobre a capacidade de dirigir e usar máquinas.
Gravidez e Lactação
Categoria de risco na gravidez: C – Não há estudos adequados em mulheres. Em experiências animais ocorreram alguns efeitos colaterais no feto, mas o benefício do produto pode justificar o risco potencial durante a gravidez.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Mulheres com potencial para engravidar
Wainua reduzirá os níveis plasmáticos de vitamina A, que é crucial para o desenvolvimento fetal normal. Não se sabe se a suplementação de vitamina A será suficiente para reduzir o risco para o feto. Por esta razão, a possibilidade de gravidez deve ser excluída antes do início da terapia com Wainua e as mulheres com potencial para engravidar devem utilizar contracepção eficaz.
Se uma mulher pretender engravidar, Wainua e a suplementação com vitamina A devem ser descontinuadas, e os níveis séricos de vitamina A devem ser monitorados até que voltem ao normal antes da tentativa de concepção. Devido à longa meia-vida de eplontersena (ver seção 3. Características Farmacológicas - Propriedades Farmacocinéticas), pode-se desenvolver um déficit de vitamina A mesmo após a interrupção do tratamento.
Contracepção em homens e mulheres
Mulheres com potencial para engravidar devem utilizar métodos contraceptivos eficazes.
Uso criterioso no aleitamento ou na doação de leite humano.
O uso deste medicamento no período da lactação depende da avaliação e acompanhamento do seu médico ou cirurgião-dentista.
Gravidez
Não existem dados relativos à utilização de Wainua em mulheres grávidas.
A administração de eplontersena ou de um substituto farmacologicamente ativo específico para roedores em doses até 38 vezes superiores à dose humana recomendada num estudo combinado de toxicidade de fertilidade e de desenvolvimento embriofetal em camundongos não resultou em efeitos na fertilidade masculina e feminina ou no desenvolvimento embriofetal (ver seção 3. Características Farmacológicas - Dados de segurança pré-clínica).
Devido ao potencial risco teratogênico decorrente de níveis desequilibrados de vitamina A, Wainua não deve ser utilizada durante a gravidez. Em caso de gravidez, deve ser realizada uma monitorização cuidadosa do feto e do nível de vitamina A, especialmente durante o primeiro trimestre.
Amamentação
Não foram realizados estudos de lactação em humanos ou animais para avaliar a presença de eplontersena ou dos seus metabolitos no leite materno, os efeitos no lactente amamentado ou os efeitos na produção de leite da mãe.
Um risco ao bebê em amamentação não pode ser descartado. Deve ser tomada uma decisão sobre a descontinuação da amamentação ou a descontinuação/abstenção da terapia com Wainua, tendo em conta o benefício da amamentação para a criança e o benefício da terapia para a mulher.
Fertilidade
Não existe informação disponível sobre os efeitos de eplontersena na fertilidade humana.
A administração de eplontersena ou de um substituto farmacologicamente ativo específico para roedores em doses até 38 vezes superiores à exposição humana recomendada em camundongos não indicou qualquer impacto de eplontersena na fertilidade masculina ou feminina.
INTERAÇÕES MEDICAMENTOSAS
Não foram realizados estudos clínicos de interação medicamentosa (ver seção 3. Características Farmacológicas - Propriedades Farmacocinéticas).
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Wainua deve ser armazenado em geladeira (entre 2 a 8°C).
Wainua poderá ser mantido sem refrigeração (abaixo de 30°C) na embalagem original por até 6 semanas. Se não for utilizado dentro de 6 semanas, deve ser descartado.
Manter na embalagem original para proteger da luz.
Não congelar. Não expor ao calor.
Wainua tem validade de 36 meses a partir da data de fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Wainua é apresentado como uma solução estéril de 0,8 mL em uma seringa de vidro tipo I de uso único com uma agulha de aço inoxidável de calibre 27 de ½ polegada (12,7 mm), uma proteção rígida da agulha e rolha de elastômero de clorobutila siliconizada em uma caneta aplicadora.
Wainua está disponível em embalagem contendo 1 caneta aplicadora para uso único.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Modo de usar
Apenas para uso subcutâneo.
A primeira injeção administrada pelo paciente ou cuidador deve ser realizada sob a orientação de um profissional de saúde devidamente qualificado. Os pacientes e/ou cuidadores devem ser treinados na administração subcutânea de Wainua.
A caneta aplicadora deve ser retirada do refrigerador pelo menos 30 minutos antes do uso e deixada até que atinja a temperatura ambiente antes da injeção. Outros métodos de aquecimento não devem ser utilizados.
Inspecione a solução visualmente antes de usar. A solução deve ter uma aparência límpida e incolor a amarela.
Não utilizar se a solução estiver turva, com coloração alterada ou contiver partículas visíveis antes da administração.
Se autoadministrado, injete Wainua no abdômen ou na região superior da coxa. Se um cuidador administrar a injeção, a região posterior superior do braço também pode ser usada.
Instruções completas para administração são fornecidas no documento “Instruções de uso”.
Instruções de descarte
A caneta aplicadora para uso único deve ser descartada em um recipiente para objetos cortantes resistente a perfurações.
Qualquer medicamento não utilizado ou resíduos devem ser eliminados de acordo com as exigências locais.
Incompatibilidades
Na ausência de estudos de compatibilidade, este produto não deve ser misturado com outros medicamentos.
Posologia
O tratamento deve ser prescrito e supervisionado por um médico com experiência no tratamento de pacientes com amiloidose.
A dose recomendada de Wainua é de 45 mg administrada por injeção subcutânea. As doses devem ser administradas mensalmente.
Dose perdida
Se for esquecida uma dose de eplontersena, a dose seguinte deverá ser administrada o mais rapidamente possível.
Retomar a administração em intervalos mensais a partir da data da última dose.
Populações especiais
Comprometimento renal
Não é necessário ajuste de dose em pacientes com insuficiência renal leve a moderada (taxa de filtração glomerular estimada [TFGe] ≥45 a <90 mL/min/1,73 m2) (ver seção 3. Características Farmacológicas - Propriedades Farmacocinéticas). Wainua não foi estudado em pacientes com TFGe <45 mL/min/1,73 m2 ou doença renal em estágio terminal.
Comprometimento hepático
Não é necessário ajuste de dose em pacientes com comprometimento hepático leve (ver seção 3. Características Farmacológicas - Propriedades Farmacocinéticas). Wainua não foi estudado em pacientes com comprometimento hepático moderado ou severo.
População idosa
Não é necessário ajuste de dose em pacientes idosos (≥65 anos de idade) (ver seção 3. Características Farmacológicas - Propriedades Farmacocinéticas).
População pediátrica
A segurança e eficácia de Wainua em crianças e adolescentes com menos de 18 anos de idade não foram estabelecidas. Não há dados disponíveis.
REAÇÕES ADVERSAS
Resumo global do perfil de segurança
Os dados de segurança descritos abaixo refletem a exposição a Wainua em 144 pacientes com polineuropatia causada por ATTRv (ATTRv-PN) randomizados para Wainua e que receberam pelo menos uma dose de Wainua. Destes, 141 pacientes receberam pelo menos 6 meses de tratamento e 137 pacientes receberam pelo menos 12 meses de tratamento. A duração média do tratamento foi de 541 dias (intervalo: 57 a 582 dias).
As reações adversas mais frequentes durante o tratamento com Wainua, observadas em ≥5% dos pacientes, foram vômitos e redução da vitamina A.
Reações adversas ao medicamento
As reações adversas ao medicamento (RAMs) são organizadas por classe de sistema de órgãos (SOC) do MedDRA. Dentro de cada SOC, os termos preferenciais são organizados por frequência decrescente e depois por gravidade. As frequências de ocorrência de reações adversas são definidas como: reação muito comum (≥1/10); reação comum (≥1/100 a <1/10); reação incomum (≥1/1.000 a <1/100); reação rara (≥1/10.000 a <1/1.000) e reação muito rara (<1/10.000).
Tabela 4: Resumo das reações adversas por categoria de frequência
| Classe de sistema de órgãos | Reação adversa | Frequência |
|---|---|---|
| Distúrbios gastrointestinais | Vômito | Comum |
| Distúrbios gerais e quadros clínicos no local de administração | Eritema no local da injeção | Comum |
| Dor no local da injeção | Comum | |
| Prurido no local da injeção | Comum | |
| Investigações | Vitamina A reduzida | Muito comum |
| Distúrbios renais e urinários | Proteinúria | Comum |
| Distúrbios cardíacos | Bloqueio atrioventricular | Comum |
Descrição da reação adversa selecionada
Vitamina A reduzida
No estudo clínico em participantes com ATTRv-PN, todos os participantes foram instruídos a tomar a dose diária recomendada de vitamina A. Todos os participantes tratados com Wainua apresentavam níveis normais de vitamina A no início do estudo, 96,5% deles desenvolveram níveis de vitamina A abaixo do limite inferior do normal (LLN) durante o estudo (ver seção 3. Características Farmacológicas - Propriedades Farmacodinâmicas).
Reações no local da injeção
Em participantes com ATTRv-PN tratados com Wainua, foram relatados eritema no local da injeção, dor no local da injeção e prurido no local da injeção em 3,5%, 3,5% e 2,1%, respectivamente.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, notifique os eventos adversos pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
Não há nenhum tratamento específico para uma superdosagem de eplontersena. Em caso de superdosagem, devem ser prestados cuidados médicos de suporte, incluindo consulta com um profissional de saúde.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO
MS - 1.1618.0307
Produzido por:
Vetter Pharma-Fertigung GmbH & Co. KG – Ravensburg – Alemanha
Registrado e Importado por:
AstraZeneca do Brasil Ltda.
Rod. Raposo Tavares, km 26,9 – Cotia – SP – CEP 06707-000
CNPJ 60.318.797/0001-00
SAC 0800 014 5578