Prostavasin
Aché Laboratórios Farmacêuticos S.A
IDENTIFICAÇÃO DO MEDICAMENTO
Prostavasin
alprostadil alfaciclodextrina
Injetável 20 mcg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Pó liofilizado1 para solução injetável
Embalagem com 10 ampolas
USO INTRAVENOSO OU INTRA-ARTERIAL
USO ADULTO
COMPOSIÇÃO:
Cada ampola de Prostavasin contém:
| alprostadil alfaciclodextrina (equivalente a 20 mcg de alprostadil) | 666,7 mcg |
| excipiente q.s.p. | 1 ampola |
Excipiente: lactose2 monoidratada.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Este medicamento está indicado para o tratamento de doença arterial crônica (deficiência de circulação3 nos membros inferiores) nos estágios III e IV em pacientes não escolhidos para revascularização (desobstrução ou reconstrução da circulação3 nos vasos por procedimentos invasivos) ou naqueles em que a revascularização foi insatisfatória.
A administração endovenosa para portadores de doença arterial oclusiva crônica estágio IV não é recomendada.
COMO ESTE MEDICAMENTO FUNCIONA?
Prostavasin atua promovendo a dilatação dos vasos acometidos por obstruções severas, melhorando as condições circulatórias e a oxigenação dos tecidos. O efeito benéfico ocorre geralmente após três semanas e o tratamento não deverá passar de 4 semanas.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Prostavasin é contraindicado para:
- Pessoas com hipersensibilidade (alergia4) ao alprostadil alfaciclodextrina ou aos outros componentes da fórmula.
- Pacientes com insuficiência cardíaca5 (coração6 enfraquecido ou com desempenho insuficiente) que apresentem queixa de falta de ar e cansaço para realizar esforços mínimos ou em repouso (classe funcional III ou IV de acordo com a Associação do Coração6 de Nova Iorque - NYHA).
- Pacientes com edema7 agudo8 de pulmões9 (água nos pulmões9) ou histórico, na vigência de insuficiência cardíaca5.
- Doença cardíaca coronariana (depósitos de gordura10 que podem obstruir a artéria11 coronária) inadequadamente tratada.
- Estenose12 aórtica e/ou mitral e/ou insuficiência13 (problemas nas válvulas mitral e/ou aórtica do coração6).
- Casos de arritmias14 cardíacas hemodinamicamente relevantes (que provoquem sintomas15 acentuados como falta de ar, tontura16 e desmaios).
- Pacientes que tiveram um infarto17 agudo8 do miocárdio18 ou acidente vascular cerebral19 nos últimos seis meses.
- Doença pulmonar obstrutiva crônica (DPOC) ou doença veno-oclusiva pulmonar (DVOP).
- Infiltração pulmonar disseminada.
- Hipotensão20 grave (pressão arterial21 muito baixa).
- Portadores de doenças hepáticas22 (doença do fígado23) com sinais24 de dano hepático agudo8 (elevação das enzimas transaminases ou gama GT) ou insuficiência13 da função hepática25 conhecida.
- Pacientes com insuficiência renal26 grave (oligoanúria, TFG ≤ 29 ml/min/1,73m2).
- Pacientes com sangramento ativo ou potencial, como casos de gastrite27 erosiva aguda, úlcera gástrica28 (no estômago29) e/ou duodenal ativa e/ou suspeita de hemorragia30 cerebral.
- Pacientes grávidas ou que estejam amamentando.
- Casos em que seja contraindicada a infusão de líquidos (por exemplo: insuficiência cardíaca congestiva31, edema pulmonar32 ou cerebral e hiperidratação).
Este medicamento é contraindicado para menores de 18 anos.
Este medicamento é contraindicado para uso em pacientes com hepatopatia (distúrbio no fígado23).
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Portadores de insuficiência renal26 devem receber orientação médica antes de usar essa medicação.
Pacientes com insuficiência renal26 leve (TFG ≤ 89 ml/min/1,73m2) ou moderada (TFG ≤ 59 ml/min/1,73m2) devem avisar o médico de tal condição, a qual requer cuidadosa monitoração (por exemplo, equilíbrio de fluidos e testes da função renal33).
Informe ao médico caso você tenha histórico de doenças gastrintestinais, como gastrite27 erosiva, sangramento gastrintestinal, úlcera gástrica28 e/ou duodenal, ou histórico de suspeita de hemorragia30 cerebral, ou de qualquer outra condição de sangramento.
Caso esteja utilizando outro(s) medicamento(s), principalmente anticoagulantes34 e inibidores de agregação de plaquetas35, informe ao médico.
Alprostadil não deve ser administrado através de injeção36 em bolus37.
Gravidez38 e Lactação39
Prostavasin é contraindicado em mulheres gestantes ou em fase de lactação39. Não deve ser usado também por mulheres que tenham possibilidade de engravidar.
Categoria de risco na gravidez38: C
Informe ao seu médico a ocorrência de gravidez38 na vigência do tratamento ou após o seu término. Informe ao seu médico se está amamentando.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
A eficácia deste medicamento depende da capacidade funcional do paciente.
Interações medicamentosas
Prostavasin pode inibir a agregação de plaquetas35 (coagulação40). Informe ao seu médico caso esteja utilizando anticoagulantes34 ou inibidores da agregação plaquetária.
Prostavasin pode aumentar o efeito de qualquer medicamento para baixar a pressão arterial21. Informe ao seu médico caso esteja utilizando medicamentos anti-hipertensivos ou vasodilatadores.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde41.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Você deve guardar este produto em temperatura ambiente (15–30°C), protegido da luz e umidade. Desde que respeitados os cuidados de armazenamento, o medicamento possui uma validade de 24 meses a contar da data de sua fabricação.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Prostavasin apresenta-se como pó branco e isento de odor.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
Este medicamento necessita sempre de um profissional de saúde41 habilitado para sua aplicação, conforme as orientações dadas pelo médico. Você não deverá nunca usar este medicamento sozinho.
O risco de administração por uma via não recomendada é a não obtenção do efeito esperado ou a ocorrência de efeitos indesejados.
Orientações para reconstituição do Prostavasin:
- Efetue assepsia42 das mãos43 com técnica apropriada e calce um par de luvas descartáveis. Efetue assepsia42 da ampola.
Sugere-se limpar o gargalo da ampola com algodão embebido em álcool 70%. - Segure a ampola com a marca vermelha para cima.

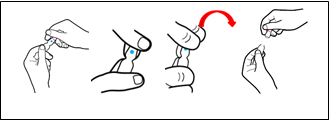
- A ampola de Prostavasin é pré-cortada abaixo do ponto azul (sistema OPC = One Point Cut). O OPC deve estar entre os polegares. Pressione com os polegares (apoio no estrangulamento) e apoie com os indicadores (envolver parte superior da ampola).
Quebre a ampola com a mão44 protegida por luvas. Para quebrá-la deve-se segurá-la a 45º e forçar este ponto para trás.
- A reconstituição (dissolução) do pó liofilizado1 de 1 ampola deve ser realizada com 2 mL de diluente.
Para dissolução sugere-se como diluente solução fisiológica45 0,9%. Aspire o diluente utilizando-se de seringa46/agulha.
Introduza cuidadosamente o diluente aspirado dentro da ampola sem tocar as bordas externas, com o bisel voltado para baixo.
Não é necessário agitar.
Aspire a solução formada (pó liofilizado1 reconstituído com diluente) com a seringa46/agulha.
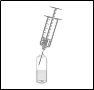
- O conteúdo aspirado deve ser diluído em bolsa de soro47 fisiológico48 de acordo com a via de administração.

Desprezar a ampola e os outros materiais (seringa46 e agulha) em recipiente adequado para coleta de materiais perfurantes/cortantes. Nunca guarde material residual.
Para informações sobre administração/diluição em bolsa de soro47 fisiológico48 e recomendações de doses, ver informações a seguir:
Terapia intra-arterial com Prostavasin nos estágios III e IV
Diluir o conteúdo reconstituído de uma ampola do liofilizado1 de Prostavasin (equivalente a 20 mcg de alprostadil) em 50 ml de solução fisiológica45.
A dose recomendada para terapia intra-arterial com Prostavasin é 10 mcg em 60 a 120 minutos, com o auxílio de uma bomba de infusão. Se necessário, especialmente na presença de necroses, desde que a tolerabilidade seja satisfatória, a dose pode ser ampliada para uma ampola (20 mcg). A dose é geralmente uma infusão ao dia. Na infusão através de cateter de demora, recomenda-se uma dosagem de 0,1 a 0,6 ng/kg/min, administrada com bomba de infusão por 12 horas (em torno de ¼ ou 1 ½ ampola de Prostavasin).
Terapia intravenosa com Prostavasin no estágio III
Recomenda-se diluir o conteúdo reconstituído de 2 ampolas de Prostavasin (40 mcg de alprostadil) em 50 ml a 250 ml de soro47 fisiológico48 e administrar por 2 horas. Esta dose é administrada 2 vezes ao dia, por via endovenosa. Alternativamente, pode-se administrar 3 ampolas (60 mcg de alprostadil) no volume de 50 a 250 ml, infundidos em 3 horas, 1 vez ao dia.
Pacientes com insuficiência renal26 (creatinina49 > 1,5 mg/dl50)
Pacientes com insuficiência renal26 leve (TFG ≤ 89 ml/min/1,73m2) ou moderada (TFG ≤ 59 ml/min/1,73m2) devem avisar o médico de tal condição, a qual requerem cuidadosa monitoração (por exemplo, equilíbrio de fluidos e testes da função renal33).
O tratamento intravenoso deve ser iniciado com 1 ampola de Prostavasin, duas vezes ao dia. De acordo com o quadro clínico, em dois a três dias a dose pode ser elevada até a dose normal recomendada.
Para pacientes51 que necessitam de restrições líquidas, como portadores de insuficiência renal26 e cardiopatias, o volume deve ser restrito a 50 a 100 ml/dia e as infusões devem ser administradas com bomba de infusão.
Populações especiais
Pacientes pediátricos: Alprostadil não é recomendado para uso em população pediátrica.
Mulheres em idade reprodutiva: Alprostadil não deve ser utilizado em mulheres que possam engravidar.
Administração e duração do uso:
O efeito benéfico de Prostavasin ocorre geralmente após três semanas. O tratamento não deverá exceder 4 semanas. Se não se verificarem os efeitos desejados nesse período, interromper o tratamento.
A via de administração endovenosa não é recomendada para portadores de doença arterial obstrutiva periférica em estágio IV.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Este medicamento deve ser sempre administrado por um profissional de saúde41 habilitado e sob supervisão médica. Em caso de esquecimento de doses, não devem ser administradas doses dobradas.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Informe ao seu médico o aparecimento de reações desagradáveis como dor, vermelhidão e inchaço52 no local da aplicação, tontura16, dor torácica e palpitações53.
Dor, eritema54 e edema7 frequentemente ocorrem no membro recebendo a infusão durante a administração intra-arterial de Prostavasin. Sintomas15 similares também ocorrem com a administração intravenosa. Esses efeitos adversos que são devidos ao fármaco55 ou à punção, desaparecem quando a dose é reduzida ou quando a infusão é interrompida. Independentemente da via de administração, ocorrem ocasionalmente: dor de cabeça56, reações gastrintestinais adversas (por exemplo, diarreia57, náusea58 e vômito59), rubor e parestesia60.
Raramente ocorre queda da pressão arterial21, taquicardia61, sintomas15 de angina62, valores hepáticos elevados (transaminases), queda ou elevação na contagem de glóbulos brancos (leucopenia63 ou leucocitose64), sintomas15 articulares, estados de confusão, convulsões de origem cerebral, elevação de temperatura, sudorese65, vertigens66, febre67, reações alérgicas e alterações da proteína C reativa. O quadro retorna rapidamente à normalidade após o tratamento.
Houve relatos de hiperostose (processo ósseo benigno, no qual ocorre um crescimento ósseo excessivo) reversível dos ossos longos68 em um número muito pequeno de pacientes com mais de 4 semanas de tratamento.
Um número muito pequeno de pacientes desenvolveu edema pulmonar32 agudo8 ou insuficiência cardíaca5 global durante o tratamento com Prostavasin.
Houve relatos na literatura de hiperglicemia69 (elevação do nível de glicose70 no sangue71) associada com o tratamento com alprostadil.
A seguir são listadas reações adversas classificadas de acordo com a frequência que são descritas na literatura médica.
Distúrbios no sangue71 e sistema linfático72
- Raro (≥ 1/10 000 a < 1/1 000): trombocitopenia73, leucopenia63 e leucocitose64.
Distúrbios do sistema nervoso central74
- Comum (≥ 1/10): cefaleia75 (dor de cabeça56).
- Raro (≥ 1/10 000 a < 1/1000): estados confusionais e convulsão76 de origem cerebral.
- Frequência não conhecida: acidente vascular cerebral19.
Distúrbios do sistema cardiovascular77
- Incomum (≥ 1/1 000 a < 1/100): queda de pressão arterial21, taquicardia61 e angina62 pectoris.
- Raro (≥ 1/10 000 a < 1/1 000): arritmia78 e insuficiência cardíaca5 biventricular.
- Frequência não conhecida: infarto do miocárdio79.
Distúrbios vasculares80
- Frequência não conhecida: hemorragia30.
Distúrbios respiratórios, torácicos e do mediastino81
- Raro (≥ 1/10 000 a < 1/1000): edema pulmonar32.
- Frequência não conhecida: dispneia82.
Distúrbios gastrintestinais
- Incomum (≥ 1/1000 a < 1/100): náusea58, vômitos83 e diarreia57.
- Raro (≥ 1/10 000 a < 1/1000): alteração de enzimas hepáticas84.
- Frequência não conhecida: sangramento gastrintestinal.
Distúrbios hepatobiliares85
- Raro (≥ 1/10 000 a < 1/1000): anormalidades das enzimas hepáticas84.
Distúrbios da pele e tecido subcutâneo86
- Comum (≥ 1/100 a < 1/10): vermelhidão, edema7 e calor local.
- Incomum (≥ 1/1 000 a < 1/100): reações alérgicas (hipersensibilidade cutânea87 como rash88, desconforto em articulações89, reações febris, transpiração90 e calafrios91).
Distúrbios gerais e/ou relacionados ao local da aplicação
- Comum (≥1/100 a < 1/10): dor e cefaleia75; após administração intra-arterial: sensação de inchaço52 e calor, edema7 localizado e parestesia60.
- Incomum (≥ 1/1 000 a < 1/100): após administração endovenosa: sensação de inchaço52 e calor, edema7 localizado e parestesia60.
- Muito raro (<1/10 000): anafilaxia92/reações anafiláticas93.
- Frequência não conhecida: flebite94 no local da injeção36, trombose95 no local da ponta do cateter, sangramento localizado.
Pós-comercialização
Durante a experiência pós-comercialização, foi observado que a reação adversa flebite94 (inflamação96 da parede dos vasos sanguíneos97) no local da injeção36 ocorreu com incidência98 muito rara (<1/10 000).
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Em caso de superdosagem de Prostavasin podem ocorrer os seguintes sintomas15 sistêmicos99: queda da pressão arterial21 com aumento dos batimentos cardíacos, desmaios com palidez, sudorese65, náuseas100 e vômitos83.
Sintomas15 locais no trajeto da veia infundida podem incluir dor, edema7 e vermelhidão.
Em casos de superdosagem ou sintomas15 de superdosagem, a infusão deve ter seu fluxo reduzido ou interrompido imediatamente. Em caso de hipotensão20, o paciente deve ser colocado deitado de costas101 e as pernas devem ser mantidas em posição elevada. Se os sintomas15 persistirem, devem ser realizados exames cardíacos e testes funcionais. Se necessário, devem ser administrados medicamentos para estabilizar as condições hemodinâmicas e circulatórias (por exemplo, agentes simpaticomiméticos). No caso de eventos cardiovasculares graves (por exemplo, isquemia102 miocárdica, insuficiência cardíaca5), a infusão deve ser interrompida imediatamente e devem ser iniciadas medidas e tratamento de emergência103.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações sobre como proceder.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.0573.0576.
Farmacêutica Responsável: Gabriela Mallmann - CRF-SP nº 30.138
Registrado por:
Aché Laboratórios Farmacêuticos S.A.
Av. Brigadeiro Faria Lima, 201 – 20º andar
São Paulo – SP
CNPJ 60.659.463/0029-92
Indústria Brasileira
Fabricado por:
IDT Biologika GmbH Dessau-RoBlau - Alemanha
Sob Licença de:
Amdipharm Ltd. Dublin - Irlanda
Importado e embalado por:
Aché Laboratórios Farmacêuticos S.A.
Av. das Nações Unidas, 22.428 - São Paulo - SP
SAC 0800 701 6900