

Noex (Bula do profissional de saúde)
EUROFARMA LABORATÓRIOS S.A.
IDENTIFICAÇÃO DO MEDICAMENTO
Noex
budesonida
Suspensão em spray estéril 32 mcg/dose, 64 mcg/dose, 50 mcg/dose, 100 mcg/dose
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Suspensão em spray estéril
Embalagem com frasco contendo 100, 120 ou 200 doses.
USO NASAL
USO ADULTO E PEDIÁTRICO ACIMA DE 6 ANOS
COMPOSIÇÃO:
Cada dose de Noex 32 mcg contém
| budesonida | 32 mcg |
| excipiente q.s.p. | 1 dose |
Excipientes: cloreto de sódio, polissorbato 80, celulose microcristalina, carmelose sódica, edetato dissódico, propilenoglicol, ácido clorídrico, hidróxido de sódio e água destilada.
Cada dose de Noex 64 mcg contém
| budesonida | 64 mcg |
| excipiente q.s.p. | 1 dose |
Excipientes: cloreto de sódio, polissorbato 80, celulose microcristalina, carmelose sódica, edetato dissódico, propilenoglicol, ácido clorídrico, hidróxido de sódio e água destilada.
Cada dose de Noex 50 mcg contém
| budesonida | 50 mcg |
| excipiente q.s.p. | 1 dose |
Excipientes: cloreto de sódio, polissorbato 80, celulose microcristalina, carmelose sódica, edetato dissódico, propilenoglicol, ácido clorídrico, hidróxido de sódio e água destilada.
Cada dose de Noex 100 mcg contém
| budesonida | 100 mcg |
| excipientes q.s.p. | 1 dose |
Excipientes: cloreto de sódio, polissorbato 80, celulose microcristalina, carmelose sódica, edetato dissódico, propilenoglicol, ácido clorídrico, hidróxido de sódio e água destilada.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE
INDICAÇÕES
Noex é indicado para pacientes com rinites não-alérgica e alérgica perenes e alérgica sazonal, tratamento de pólipo nasal e prevenção de pólipo nasal após polipectomia.
RESULTADOS DE EFICÁCIA
Rinite
A budesonida uma vez ao dia é efetivo no tratamento de rinite sazonal e perene em adultos e crianças, como demonstrado pelos resultados de estudos randomizados, duplo-cegos, controlados por placebo. A budesonida possui um rápido início de ação, com efeitos significativos em sintomas específicos após 3–5 horas, com eficácia geral atingida muito rapidamente em 7 horas. A budesonida também possui duração de ação prolongada, permitindo a administração diária única (DAY J et al. Am J Rhinol 1997).
Day et al. (2000) desenharam um estudo duplo cego randomizado de grupos paralelos, a budesonida spray aquosa nasal foi testada nas doses de 64 a 256 mcg versus placebo, em 217 pacientes com história de sensibilidade a pólen há pelo menos 1 ano e com provocação nasal como teste de controle, observou-se que entre 7 a 12 horas os usuários da budesonida apresentaram redução na obstrução nasal e nos sintomas quando comparados ao grupo placebo, sendo que o início de ação (por volta de 3 horas) foi menor no grupo que fez uso das maiores doses de budesonida quando comparado ao placebo. O grupo que fez uso da dose de 64 mcg apresentou resultados semelhantes, porém com início de ação por volta de 3 a 5 horas. A eficácia do tratamento foi maior para budesonida em comparação ao placebo a partir de 5 horas. Todos os tratamentos foram bem tolerados e nenhum evento adverso específico foi relatado (DAY JH et al. J Allergy Clin Immunol 2000; 105:489).
Com base no uso da budesonida tópica nasal para alívio dos sintomas da rinite alérgica, Gurevich et al. (2005) realizaram estudo cruzado, duplo-cego, placebo controlado com objetivo primário de avaliar a melhora do sono, diminuição da sonolência e da fadiga em pacientes tratados com budesonida intranasal spray. Os pesquisadores selecionaram 26 pacientes (n=26) que foram tratados com 128 mcg/dia de budesonida ou com placebo, e que foram avaliados segundo a Escala de Sonolência de Epworth, diário pessoal, e questionários com foco nos sintomas nasais, qualidade do sono, sonolência e fadiga diurna, durante o período de 8 semanas. Os resultados do estudo mostraram que os pacientes tratados com budesonida intranasal spray apresentaram melhora dos parâmetros analisados e que esta melhora foi estatisticamente significante para a congestão nasal (p = 0.04), sonolência diurna (p = 0.01) e redução na fadiga diurna (p= 0.08) quando comparada ao controle. As medidas do sono também mostraram melhora estatisticamente significativa dos parâmetros analisados (p=0,04). Budesonida intranasal spray foi efetiva na redução da congestão nasal, sonolência e fadiga diurna, além de melhorar a qualidade do sono do paciente com rinite alérgica perene (GUREVICH F et al. Allergy Asthma Proc 2005; 26:268).
Em uma revisão de estudos no MEDLINE (abril de 1966 - 2003), Stanaland (2004) analisou os resultados de estudos clínicos controlados, duplo-cegos e randomizados, considerando a eficácia, perfil de segurança, efeitos sobre a qualidade de vida, preferência do paciente e custo-efetividade da budesonida aquosa intranasal spray, aplicada uma vez ao dia, no tratamento da Rinite Alérgica. Com base nos resultados dos estudos analisados, a budesonida intranasal administrada uma vez ao dia foi considerada um tratamento eficaz para rinite alérgica sazonal e perene, mesmo em doses baixas como 64 mcg (32 mcg em cada narina). A budesonida intranasal foi bem tolerada nos estudos analisados, com um perfil de eventos adversos similar ao placebo, e não causou, clinicamente, supressão significativa da função do eixo hipotálamo-hipófise- adrenal, em doses 4 vezes superiores à dose inicial recomendada (STANALAND BE. Clin Ther 2004; 26:473).
Em conclusão, a budesonida intranasal uma vez por dia, é altamente eficaz e bem tolerada para a rinite alérgica sazonal e perene em adultos e crianças, com uma gama de eventos adversos similares a do placebo.
Rinite alérgica sazonal
Na rinite sazonal diversos estudos clínicos suportam a efetividade de budesonida em dosagens de 32-64 mcg 1-2 doses em cada narina, administrado inicialmente em uma dose inicial maior e depois ajustado para a dose de manutenção mínima (DAY J et al. Am J Rhinol 1997; 11:77, MELTZER E. Ann Allergy Asthma Immunol 1998; 81:128). Por exemplo, em um estudo em pacientes com rinite alérgica sazonal induzida por ambrósia, 64 mcg de budesonida uma vez ao dia foi dose mínima efetiva durante a estação de polinização (CRETICOS P et al. Allergy Asthma Proc 1998; 19:285). A melhora significativa devida ao tratamento com budesonida foi demonstrada em avaliação de qualidade de vida (OSTINELLI J et al. J Allergy Clin Immunol 1998; 101: S97).
Rinite alérgica perene
A budesonida é também bem documentado na rinite perene com alívio de sintomas como, por exemplo, obstrução nasal, coriza, espirros, prurido nasal e melhoria na saúde relacionada ao escore de qualidade de vida (DAY J et al. J Allergy Clin Immunol 1998; 102:902, MELTZER E. Ann Allergy Asthma Immunol 1998; 81:128, STÅHL E et al. J Allergy Clin Immunol 2000; 105(1): S94 (abstract 279)).
Rinite perene não-alérgica
Rinite perene não-alérgica é caracterizada por sintomas nasais persistentes que não resultam de eventos imunopatológicos mediados por IgE. O diagnóstico da rinite não alérgica é frequentemente um diagnóstico de exclusão, quando uma etiologia alérgica pode ser substanciada por testes diagnósticos. Os sintomas podem ser similares à rinite alérgica, mas com menor quantidade de prurido nasal, de número de episódios de espirros e queixas conjuntivais. Rinite vasomotora e rinite não-alérgica eosinofílica são causas comuns.
A budesonida mostrou ser eficaz em estudos clínicos (até 12 meses) demonstrando sintomas nasais reduzidos em doses de 200–400 mcg. Em estudos em pacientes com rinite não-alérgica perene, uma redução de secreção nasal induzida por metacolina e escores de sintomas foi demonstrada (MALM L et al. Allergy 1981; 36 (3):209). Em estudos de 12 meses, com dosagem de 400 mcg uma vez ao dia, reduziu efetivamente todos os sintomas nasais mensurados por escalas de pontuação de 4 pontos incluindo rinoscopia (SYNNERSTAD B et al. Br J Clin Pract. 1996; 50(7):363). Em um estudo de 6 meses de eficácia e 12 meses de segurança, no qual a maioria dos pacientes possuíam rinite perene não alérgica, tratamento efetivo e seguro foram concluídos na dosagem de 200–400 mcg uma vez ao dia (LINDQVIST N et al. Eur J Respir Dis 1982; 63 (Suppl 122):270; LINDQVIST N et al. Allergy 1986; 41(3):179). Um efeito significativo foi também confirmado em um estudo de 12 meses em comparação com cetirizina (RINNE J et al. J Allergy Clin Immunol. 2002; 109(3):426).
Tratamento de pólipos nasais
Prevenção de pólipos nasais após polipectomia
Pólipos nasais causam obstrução nasal e sintomas relacionados, como hiper-reatividade nasal não específica, rinorreia, espirros e perda do olfato. A maioria dos casos de pólipos nasais respondem bem ao tratamento de glicocorticosteroides nasais. Uma estratégia terapêutica combinada com cirurgia e tratamento com glicocorticosteroides nasais é comumente praticada. Após a remoção cirúrgica dos pólipos nasais, polipose nasal sintomática pode recorrer. Diversos estudos controlados demonstraram que a budesonida reduz o tamanho dos pólipos, melhora os sintomas nasais e reduz a frequência de recorrência de cirurgias (LILDHOLDT T et al. Archives of Otolaryngology - Head and Neck Surgery 1997; 123:595; RUHNO J et al. J Allergy Clin Immunol 1990;86:946-53; TOS M et al. Am J Rhinol 1998; 12:183).
CARACTERÍSTICAS FARMACOLÓGICAS
Modo de ação
Noex contém em sua fórmula um único princípio ativo, a budesonida, glicocorticoide não halogenado de síntese, cuja principal propriedade consiste na elevada relação entre sua potente atividade anti-inflamatória local e atividade sistêmica muito baixa. Seu início de ação ocorre em cerca de 10 a 24 horas após a administração, com pico de ação de 1 dia a 2 semanas.
Os corticosteroides têm vários mecanismos de ação, incluindo atividade anti-inflamatória, propriedades imunossupressoras e ações antiproliferativas. Os efeitos anti-inflamatórios resultam da redução da formação, liberação e atividade dos mediadores inflamatórios (ex.: cininas, histamina, lipossomas, prostaglandinas e leucotrienos). Assim, ocorre a redução das manifestações iniciais do processo inflamatório.
Os corticoides inibem a marginação e subsequente migração celular para o sítio inflamatório e também revertem a dilatação e o aumento da permeabilidade vascular local, levando à redução do acesso celular ao sítio. Essa ação vasoconstritora reduz o extravasamento vascular, o edema e o desconforto local.
Propriedades Farmacodinâmicas
A budesonida é um glicocorticosteroide com grande efeito anti-inflamatório local.
O mecanismo de ação exato dos glicocorticosteroides no tratamento da rinite não está totalmente definido. Ações anti-inflamatórias, como a inibição da liberação do mediador inflamatório e das respostas imunes mediadas pela citocina são provavelmente importantes. A potência intrínseca da budesonida, medida como a afinidade pelo receptor de glicocorticosteroide é cerca de 15 vezes maior que a da prednisolona.
Um estudo clínico em rinite sazonal comparando budesonida intranasal e oral com placebo mostrou que o efeito terapêutico da budesonida pode ser totalmente explicado pela ação local.
A budesonida administrada profilaticamente demonstrou ter efeito protetor contra a eosinofilia e a hiper-responsividade induzidas por provocação nasal.
As doses recomendadas de Noex não causam mudanças clínicas importantes, nem nos níveis de cortisol plasmático basal, nem na resposta a estimulação com ACTH nos pacientes com rinite. Entretanto, supressão dose-relacionada do cortisol plasmático e urinário tem sido observada em voluntários sadios após um curto período de administração de Noex.
Propriedades Farmacocinéticas Absorção:
A disponibilidade sistêmica da budesonida de Noex é de 33%. Em adultos, a concentração plasmática máxima após a administração de 256 mcg de Noex é de 0,64 nmol.h/L e é alcançada em 42 minutos. A área sob a curva de concentração plasmática vs. tempo (AUC) após a administração de 256 mcg de budesonida é 2,7 nmol.h/L em adultos.
Distribuição: A budesonida tem um volume de distribuição de aproximadamente 3 L/Kg. A ligação com as proteínas plasmáticas é em média 85–90%.
Biotransformação: A budesonida sofre extensa biotransformação hepática na primeira passagem pelo fígado (aproximadamente 90%) para metabólitos com baixa atividade glicocorticosteroide. A atividade glicocorticosteroide dos principais metabólitos, 6-beta-hidroxibudesonida e 16-alfa-hidroxiprednisolona, é menor que 1 % da atividade da budesonida. O metabolismo da budesonida é mediado principalmente pela CYP3A, um subgrupo do citocromo 450. A budesonida não sofre inativação metabólica local no nariz.
Eliminação: Os metabólitos são excretados como tal ou na forma conjugada, principalmente pela via renal. Não foi detectada budesonida íntegra na urina. A budesonida tem alta depuração sistêmica (aproximadamente 1,2 L/min) e a meia-vida plasmática após administração intravenosa é de 2–3 horas.
Linearidade: A cinética da budesonida é dose-proporcional para doses clinicamente relevantes.
A área sob a curva (AUC), após administração de 256 mcg de Noex, é 5,5 nmol.h/L em crianças, indicando uma exposição sistêmica mais alta ao glicocorticosteroide em crianças do que em adultos. Esta diferença observada na farmacocinética entre adultos e crianças, contudo, não resulta em efeitos sistêmicos mais pronunciados, nem em aumento da frequência de reações adversas.
Dados de segurança pré-clínica
Resultados de estudos de toxicidade aguda, subaguda e crônica mostraram que os efeitos sistêmicos da budesonida, como ganho de peso diminuído e atrofia dos tecidos linfoides e do córtex adrenal, são menos graves ou iguais aos observados com outros glicocorticosteroides.
A budesonida, avaliada em seis diferentes sistemas de teste, não mostrou efeito mutagênico ou clastogênico.
CONTRAINDICAÇÕES
Noex é contraindicado em casos de hipersensibilidade conhecida a budesonida e/ou demais componentes da formulação.
Este medicamento é contraindicado para menores de 6 anos de idade.
ADVERTÊNCIAS E PRECAUÇÕES
O uso de doses excessivas ou o tratamento a longo prazo com glicocorticosteroides pode levar ao aparecimento de sinais ou sintomas de hipercorticismo, supressão da função hipotálamo-hipófise-adrenal e/ou inibição do crescimento em crianças.
Os efeitos em longo prazo dos glicocorticosteroides nasais em crianças não são totalmente conhecidos. O médico deve acompanhar de perto o crescimento das crianças recebendo glicocorticosteroides por qualquer via por prazos maiores e pesar os benefícios do tratamento contra a possibilidade de inibição do crescimento. A velocidade do crescimento em crianças que usaram budesonida inalatória foi diferente das que tomaram placebo durante o primeiro ano de tratamento. Após 4 anos de tratamento, no entanto, a velocidade de crescimento entre pacientes tratados com budesonida e placebo foi similar. Crianças possuem tendência de absorver proporcionalmente maiores quantidades da medicação e estão mais suscetíveis à toxicidade sistêmica.
A redução da função hepática pode afetar a eliminação dos glicocorticosteroides.
A farmacocinética da budesonida intravenosa, entretanto, é similar em pacientes cirróticos e em indivíduos sadios. A farmacocinética após a ingestão oral da budesonida foi alterada devido ao comprometimento da função hepática, como evidenciado pelo aumento da disponibilidade sistêmica. Entretanto, esse fato é de importância clínica limitada para a budesonida, pois, após a inalação nasal, a contribuição oral para a disponibilidade sistêmica é relativamente pequena.
Especial atenção aos pacientes com tuberculose pulmonar. Noex deve ser administrado com cautela em pacientes com tuberculose pulmonar ativa ou quiescente; infecções fúngicas virais e bacterianas graves ou sem tratamento e herpes ocular simples.
Deve-se ter cautela em portadores de glaucoma, catarata, cirrose hepática, osteoporose e úlcera péptica.
A passagem de um tratamento oral com corticosteroides para um tratamento com budesonida inalatória deve ser lenta e gradual, devido principalmente à lenta normalização da função adrenal, previamente alterada pela corticoterapia oral. Essa transferência pode desmascarar condições alérgicas ocultadas pela terapia sistêmica. Evitar esta transferência em situações de “stress” como cirurgia, infecção e trauma.
Pode ser utilizado em pacientes com úlceras de septo recentes, epistaxes recorrentes, trauma nasal e cirurgias nasais recentes, desde que o quadro esteja controlado e sob controle médico rigoroso.
Deve-se tomar cuidado em caso de altas doses de corticosteroides inalatórios, como o Noex, pois podem interferir no controle da diabete, podendo causar hiperglicemia.
Pacientes que recebem tratamento em longo prazo devem tomar cuidado, pois os corticosteroides diminuem a absorção intestinal do cálcio e fosfato, além de aumentarem a excreção urinária do cálcio, podendo causar osteoporose.
Em casos de irritação, infecções fúngicas ou bacterianas locais pode-se descontinuar o tratamento com Noex, enquanto o tratamento específico é instalado.
A terapia com corticosteroides pode aumentar o risco de desenvolvimento de infecção grave ou fatal em indivíduos expostos a patologias virais como varicela ou sarampo. Evitar o contato do produto com os olhos.
Efeitos na habilidade de dirigir e operar máquinas
Noex não afeta a habilidade de dirigir veículos e de operar máquinas.
Gravidez e Lactação
Resultados de estudos epidemiológicos prospectivos e experiência pós-comercialização indicam que não há aumento do risco de má formação com o uso de budesonida intranasal ou inalada durante todo o período de gestação, inclusive na fase inicial.
Os estudos em animais demonstraram que os corticosteroides podem produzir vários tipos de malformações fetais, mas que não foram confirmadas em estudos controlados com mulheres grávidas. GLUCK et cols. (2005), publicaram uma revisão sobre os efeitos da exposição à budesonida inalatória ou intranasal em gestantes. Concluiu-se que a exposição materna à budesonida inalatória durante a gestação não está associada a um aumento no risco de malformações congênitas ou outros efeitos nocivos ao feto, em estudos com mais de 6600 recém-nascidos. Os dados disponíveis com o uso de budesonida nasal são limitados, porém as evidências indicam uma menor exposição sistêmica após a administração intranasal demonstrando um perfil de segurança ao menos similar à budesonida administrada por via inalatória (GLUCK PA, GLUCK JC. Curr Med Res Opin. 2005; 21:1075).
Baseados nestes dados, a budesonida inalatória, esta poderá ser recomendada, caso um corticoide intranasal precise ser iniciado durante a gestação.
Assim como outros fármacos a administração de budesonida durante a gravidez requer que os benefícios para a mãe sejam avaliados contra os riscos para o feto.
Os potenciais riscos e benefícios devem ser analisados antes de ser prescrito o tratamento às mulheres durante o período de aleitamento. A budesonida é excretada no leite materno. Portanto, seu uso durante a lactação deve ser sob orientação médica.
Categoria de risco na gravidez: B
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
INTERAÇÕES MEDICAMENTOSAS
Não foi observada interação da budesonida com qualquer fármaco usado para o tratamento da rinite.
O metabolismo da budesonida é mediado principalmente pela CYP3A, uma subgrupo do citocromo P450. Portanto, inibidores desta enzima, como o cetoconazol, podem aumentar a exposição sistêmica à budesonida. No entanto, o uso concomitante de cetoconazol com budesonida por períodos mais curtos tem importância clínica limitada.
A cimetidina nas doses recomendadas tem efeito discreto, mas clinicamente insignificante sobre a farmacocinética da budesonida oral.
Interação medicamento-medicamento:
Gravidade: Maior
- Efeito da interação: diminuição do limiar convulsivo.
- Medicamento: bupropiona.
Gravidade: Moderada
- Efeito da interação: aumenta a concentração plasmática da budesonida.
- Medicamento: claritromicina, eritromicina, itraconazol, cetoconazol.
- Efeito da interação: aumenta o efeito mieloproliferativo do sargramostim.
- Medicamento: sargramostim.
Gravidade: Menor
- Efeito da interação: aumenta o risco de desenvolver a síndrome de Cushing.
- Medicamento: amiodarona.
Interação medicamento-alimento
O uso concomitante de budesonida nasal e suco de grapefruit (toranja) pode aumentar os níveis séricos deste medicamento.
Não há dados que indiquem interação com álcool.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Conservar em temperatura ambiente (15–30°C). Proteger da luz. Sempre colocar a tampa protetora após o uso. O prazo de validade deste medicamento é de 24 meses.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Suspensão homogênea, branca, viscosa e isenta de partículas estranhas. Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Noex possui um dispositivo de inalação que dispensa o uso de conservantes em sua composição, mantendo a integridade do produto quanto ao risco de contaminação.
Posologia
A dose deve ser individualizada e titulada para a menor dose necessária para a manutenção do controle dos sintomas.
Adultos, idosos e crianças a partir de 6 anos:
Apresentação de 32 e 64 mcg/dose: recomenda-se iniciar com dose de 256 mcg/dia
- Apresentação de 32 mcg/dose: 4 aplicações em cada narina ou
- Apresentação de 64 mcg/dose: 2 aplicações em cada narina).
A dose pode ser administrada 1 vez ao dia pela manhã, ou dividida em 2 administrações pela manhã e à noite.
Apresentação de 50 e 100 mcg/dose: recomenda-se a dose de 400 mcg/dia
- Apresentação de 50 mcg/dose: 2 aplicações de em cada narina, 2 vezes ao dia ou 4 aplicações em cada narina pela manhã ou
- Apresentação de 100 mcg/dose: 1 aplicação em cada narina, 2 vezes ao dia ou 2 aplicações em cada narina, 1 vez ao dia.
Idosos: recomenda-se a mesma dosagem que para adultos.
Quando o efeito clínico desejado for obtido, a dose de manutenção deve ser reduzida à menor dose necessária ao controle dos sintomas.
Em pacientes com rinite alérgica sazonal e perene, a budesonida demonstrou melhora nos sintomas nasais (vs. placebo) em até 10 horas após a primeira dose. Isto é baseado em dois estudos de grupos paralelos, duplos cegos, placebo- controlados, randomizados, sendo que um realizado com pacientes com rinite alérgica sazonal, expostos ao pólen da Erva-de-Santiago em uma Unidade de Exposição Ambiental (UEA) e o outro, um estudo multicêntrico de quatro semanas em pacientes com rinite alérgica perene.
NOTA: o tratamento da rinite sazonal, sempre que possível, deve ser iniciado antes da exposição aos alérgenos. Algumas vezes pode ser necessário tratamento concomitante para controlar os sintomas oculares causados pela alergia.
Modo de usar:
Leia cuidadosamente as instruções de uso de Noex, seguindo-as corretamente.
1) Antes de usar, assoe seu nariz suavemente.

2) Agite o frasco e então remova a tampa protetora do aplicador. Segure o frasco na posição vertical com o dedo médio e o indicador sobre o aplicador e o polegar na base do frasco.
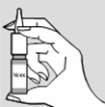
3) Antes de usar Noex pela primeira vez ou após 24 horas, a válvula deve ser carregada. Para isso, pressione o aplicador na posição vertical com os dedos indicador e médio por 8 vezes e descarte o conteúdo das 8 primeiras atomizações. Inicie a administração do produto a partir da 9ª dose de acordo com o procedimento descrito no item 4.
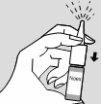
4) Pressione uma das narinas com o dedo indicador e na outra introduza a ponta do aplicador na posição vertical (com o bico para cima), conforme indicado na figura ao lado, pressionando o aplicador o número de vezes indicado pelo seu médico. Não inclinar a cabeça para trás no momento da aplicação.

5) Retire o aplicador da narina e respire pela boca.

6) Repetir na outra narina o mesmo procedimento.

7) Limpe o aplicador com um lenço de papel, recoloque a tampa protetora do aplicador e feche o frasco adequadamente. Mantenha o frasco em pé. Não congelar.
Noex não deve entrar em contato com os olhos. Caso isto ocorra, enxágue os olhos imediatamente com água.
Crianças: as crianças somente devem utilizar Noex sob supervisão de um adulto para assegurar que a dose seja corretamente administrada e esteja de acordo com a prescrição do médico.
Limpeza: limpe as partes plásticas regularmente. Lave o bico do aplicador com água. Seque e cubra com a tampa protetora.
Não se deve usar objetos perfurantes para tentar aumentar a saída do produto do aplicador. A abertura é padronizada para garantir a dosagem correta.
NÃO RETIRAR O APLICADOR.
NUNCA EMPRESTE SEU SPRAY NASAL PARA OUTRA PESSOA.
REAÇÕES ADVERSAS
Ensaios clínicos, dados da literatura e a experiência pós-comercialização sugerem que as seguintes reações adversas a droga pode ocorrer: irritação nasal, secreção hemorrágica discreta e epistaxe, reações de hipersensibilidade imediata e tardia, incluindo urticária, eritema, dermatite, angioedema e prurido. São extremamente raros os casos de ulcerações de membrana mucosa e perfuração de septo nasal após o uso de glicocorticosteroide intranasal.
Muito comum (> 1/10):
- Efeitos Gastrintestinais: náusea.
- Efeitos Neurológicos: dor de cabeça.
- Efeitos Respiratórios: disfonia, infecção do trato respiratório, sinusite.
Comum (≥ 1/100 e <1/10):
- Efeitos Cardiovasculares: palpitações, síncope e taquicardia.
- Efeitos Endócrinos/Metabólicos: hipocalemia, ganho de peso.
- Efeitos Gastrintestinais: dor abdominal, candidíase oral, indigestão, gastroenterite viral, vômito e xerostomia.
- Efeitos Hematológicos: equimose, leucocitose.
- Efeitos Imunológicos: doença infecciosa, doença viral.
- Efeitos Musculoesqueléticos: artralgia e mialgia.
- Efeitos Neurológicos: astenia, sonolência, insônia, enxaqueca.
- Efeitos Otológicos: otite média.
- Efeitos Respiratórios: rinite alérgica, alteração da voz, tosse, dificuldade na fala, epistaxe, congestão nasal, irritação nasal, nasofaringite, faringite, rinite e secreção hemorrágica.- Outros: febre, dor e boca seca.
Incomum (≥ 1/1.000 e <1/100):
- Efeitos imunológicos: reações de hipersensibilidade imediata e tardia incluindo urticária, exantema, dermatite, angioedema e prurido.
Rara (> 1/10.000 e < 1.000):
- Efeitos Dermatológicos: dermatite de contato e irritação.
- Efeitos Endócrinos/Metabólicos: Síndrome de Cushing hipoglicemia, alteração na taxa de lipídios e hiperglicemia.
- Efeitos Oftálmicos: catarata, glaucoma e aumento de pressão ocular.
- Efeitos Psiquiátricos: ansiedade, depressão, irritabilidade, problemas de comportamento e psicoses.
- Efeitos Respiratórios: broncoespasmo, irritação da garganta.
Muito rara (< 1/10.000):
- Efeitos Gastrintestinais: candidíase do esôfago.
- Efeitos imunológicos: reação anafilática.
- Efeitos respiratórios: ulcerações da membrana da mucosa e perfuração de septo nasal.
A literatura cita ainda as seguintes reações adversas, sem frequência conhecida: Acesso de espirros imediatamente após o uso do spray, rouquidão, aumento da tosse, alteração do paladar.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa
SUPERDOSE
Superdosagem aguda com Noex, mesmo com doses excessivas, geralmente não causa problemas clínicos.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
M.S.: 1.0043.0036
Farm. Resp. Subst.: Dra. Ivanete A. Dias Assi - CRF-SP 41.116
Fabricado por:
EUROFARMA LABORATÓRIOS S.A.
Rod. Pres. Castello Branco, km 35,6 – Itapevi - SP
Registrado por:
EUROFARMA LABORATÓRIOS S.A.
Av. Vereador José Diniz, 3.465 - São Paulo - SP
CNPJ: 61.190.096/0001-92
Indústria Brasileira






