Fragmin
LABORATÓRIOS PFIZER LTDA
IDENTIFICAÇÃO DO MEDICAMENTO
Fragmin®
dalteparina sódica
Injetável 12500 UI/mL e 25000 UI/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Embalagem contendo 10 seringas preenchidas com 0,2 mL (2.500 UI) + dispositivo de proteção para descarte da agulha.
VIA DE ADMINISTRAÇÃO: USO INJETÁVEL POR VIA SUBCUTÂNEA1 E INTRAVENOSA (vide Posologia)
USO ADULTO
COMPOSIÇÃO:
Cada mL de Fragmin® 2.500 UI contém:
| dalteparina sódica | 12.500 UI (anti-Xa) |
| veículo q.s.p. | 1 mL |
Veículo: cloreto de sódio, ácido clorídrico2(1), hidróxido de sódio(1) e água para injetáveis.
(1) para ajuste de pH.
Cada mL de Fragmin® 5.000 UI contém:
| dalteparina sódica | 25.000 UI (anti-Xa) |
| veículo q.s.p. | 1 mL |
Veículo: ácido clorídrico2(1), hidróxido de sódio(1) e água para injetáveis.
(1) para ajuste de pH.
A potência é descrita em unidades internacionais de anti-Xa (UI) segundo o 1º Padrão Internacional da heparina de Baixo Peso Molecular (HBPM).
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Fragmin® (dalteparina sódica) solução injetável é indicado para:
- Tratamento de trombose venosa profunda3 (TVP) (formação de um coágulo4 sanguíneo numa veia profunda) e embolia5 pulmonar (EP) (obstrução do fluxo de sangue6 do pulmão7) aguda.
- Prevenção de coagulação8 no sistema extracorpóreo durante hemodiálise9 (sistema de circulação10 de sangue6 fora do corpo) e hemofiltração (filtração do sangue6) em pacientes com insuficiência renal11 aguda ou insuficiência renal11 crônica (diminuição aguda ou crônica da função renal12, respectivamente).
- Tromboprofilaxia (prevenção de trombose13) associada à cirurgia.
- Tromboprofilaxia em pacientes com mobilidade (movimentação) restrita devido a condições médicas agudas.
- Doença arterial coronariana instável (doença das artérias14 do coração15) (angina16 (dor no peito17) instável e infarto18). Concomitante com Fragmin®, os pacientes devem receber também terapia com ácido acetilsalicílico (75 a 325 mg/ dia), a não ser que seja identificado pelo médico que o uso é contraindicado (para informações completas, vide o item “3. Quando não devo usar este medicamento?” item “4. O que devo saber antes de usar este medicamento?” e item “6. Como devo usar este medicamento?”).
- Tratamento prolongado de tromboembolismo19 venoso (TEV) (trombose13 e coágulo4 no pulmão7) sintomático20 [trombose venosa profunda3 (TVP) proximal21 e/ou embolia5 pulmonar (EP)] para reduzir a recorrência22 de tromboembolismo19 venoso (TEV) em pacientes com câncer23.
COMO ESTE MEDICAMENTO FUNCIONA?
Fragmin® age potencializando a inibição do Fator Xa e da trombina24 (substâncias que participam da coagulação8 sanguínea), diminuindo assim a chance de ocorrência de eventos tromboembólicos (decorrentes da formação e migração do coágulo4 para outros órgãos).
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Fragmin® não deve ser utilizado por pacientes que apresentem:
- história de trombocitopenia25 (diminuição das células26 de coagulação8 do sangue6: plaquetas27);
- sangramento ativo (como sangramento gastrintestinal ou sangramento cerebral);
- distúrbios graves da coagulação8;
- endocardite28 séptica (infecção29 do coração15) aguda ou sub aguda;
- lesões30 recentes ou procedimentos cirúrgicos no sistema nervoso central31 (cérebro32 e medula espinhal33), olhos34 e/ou ouvidos;
- hipersensibilidade à dalteparina (princípio ativo do Fragmin®), às heparinas e/ou a outras heparinas de baixo peso molecular (HBPMs) (classe de medicamento como o Fragmin®) ou a produtos de origem suína;
- devido ao risco aumentado de sangramento, o tratamento concomitante com altas doses de Fragmin® (como aquelas necessárias para tratar trombose venosa profunda3 aguda, embolia5 pulmonar e doença arterial coronariana instável) não deve ser utilizado em pacientes que serão submetidos à anestesia35 raquidiana ou epidural36 (vias de administração de anestesia35 na coluna) ou a outros procedimentos que requeiram punção espinhal (punção do líquido da medula espinhal33) (vide item “4. O que devo saber antes de usar este medicamento?”).
Este medicamento é contraindicado para menores de 18 anos.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Advertências e Precauções
Anestesia35 raquidiana ou epidural36
Antes de usar Fragmin® é preciso saber que quando é realizada a anestesia35 neuraxial (epidural36/raquidiana) ou punção espinhal, os pacientes anticoagulados (com capacidade de coagulação8 do sangue6 diminuída) ou programados para serem anticoagulados para prevenção de complicações tromboembólicas, constituem grupo de risco37 para desenvolvimento de hematoma38 epidural36 ou espinhal (acúmulo de sangue6 no espaço entre a meninge e a medula espinhal33 e na medula espinhal33), que pode resultar em paralisia39 permanente ou de longo prazo. O risco destes eventos é aumentado pelo uso de cateteres localizados no espaço epidural40 para administração de analgésicos41 ou pelo uso concomitante (ao mesmo tempo) de medicamentos que afetam a hemostasia42 (coagulação8), como os anti-inflamatórios não esteroides (AINEs), inibidores plaquetários ou outros anticoagulantes43. Punções espinhais ou epidurais, repetidas ou traumáticas, também parecem aumentar esse risco. Os pacientes devem ser monitorados frequentemente para sinais44 e sintomas45 de dano neurológico. Em caso de comprometimento neurológico, é necessário tratamento urgente (descompressão46 da medula espinhal33) (vide questão 3. Quando não devo usar este medicamento?).
Risco de hemorragia47
Fragmin® deve ser utilizado com cautela em pacientes com potencial elevado de risco de hemorragia47, como em pacientes com trombocitopenia25, disfunções plaquetárias, insuficiência hepática48 (do fígado49) ou renal12 (dos rins50) grave, hipertensão51 (pressão alta) não controlada, ou retinopatia (doença do fundo do olho52) hipertensiva (causada por pressão alta) ou diabética. Altas doses de Fragmin® devem ser usadas com cautela em pacientes recém- operados.
Trombocitopenia25
É recomendada a contagem de plaquetas27 antes de iniciar o tratamento com Fragmin®, e que esta seja regularmente acompanhada durante o tratamento. Caso a trombocitopenia25 se desenvolva rapidamente ou a um grau significativo (< 100.000 plaquetas27/mcL ou mm3), é recomendado teste in vitro (em laboratório) para anticorpos53 antiplaquetários na presença de heparinas ou heparinas de baixo peso molecular (HBPMs). Se o resultado do teste for positivo ou inconclusivo, ou se este teste não for realizado, o tratamento com Fragmin® deve ser interrompido.
Níveis de monitorização de anti-Xa (substância com o efeito anticoagulante54)
Geralmente, não é necessária a monitorização do efeito anticoagulante54 de Fragmin®, mas deve ser considerada em populações específicas de pacientes, como crianças, pacientes com insuficiência renal11, pacientes muito magros ou com obesidade55 mórbida, gestantes ou pacientes sob risco aumentado de sangramento ou recorrência22 de trombose13.
Hipercalemia56 (concentração de potássio no sangue6 aumentada)
A heparina e a heparina de baixo peso molecular (HBPM) podem suprimir a secreção do hormônio57 aldosterona liberado pela glândula58 adrenal levando à hipercalemia56 (quantidade de potássio no sangue6 aumentada), particularmente em pacientes com diabetes mellitus59, insuficiência renal11 (perda da função dos rins50.) crônica, acidose metabólica60 pré-existente (distúrbio do pH do sangue6), concentração de potássio no sangue6 aumentada ou sob tratamento com medicamentos poupadores de potássio. Deve-se medir a concentração de potássio no sangue6 em pacientes de risco.
Intercambialidade (troca) com outros anticoagulantes43
Fragmin® não pode ser substituído e nem substituir a heparina não fracionada, outras heparinas de baixo peso molecular (HBPMs), ou polissacarídeos sintéticos (tipos de anticoagulantes43). Cada um desses medicamentos é único e tem suas próprias instruções de uso.
As heparinas de baixo peso molecular (HBPMs) têm características e posologias diferentes. As instruções de uso para cada produto específico devem ser seguidas rigorosamente.
Se, apesar da profilaxia (prevenção) com Fragmin®, ocorrer um evento tromboembólico, deve-se descontinuar a profilaxia e instituir terapia adequada.
O médico deve considerar o benefício potencial versus o risco antes da intervenção neuraxial em pacientes anticoagulados.
Pode ocorrer trombocitopenia25 induzida pela heparina durante a administração de Fragmin®. A trombocitopenia25 de qualquer grau deve ser monitorada pelo médico.
Osteoporose61
Tratamento de longo prazo com heparina tem sido associado ao risco de desenvolvimento de osteoporose61. Embora isto não tenha sido observado com Fragmin®, o risco de desenvolver osteoporose61 não pode ser descartado.
Populações especiais
Uso em crianças: As informações sobre a eficácia e a segurança do uso de Fragmin® em pacientes pediátricos são limitadas. Se Fragmin® for utilizado nesses pacientes, os níveis de anti-Xa devem ser monitorados.
Uso em idosos: Pacientes idosos (especialmente pacientes com 80 anos de idade ou mais) podem apresentar risco aumentado de complicações de sangramento dentro dos intervalos da dose terapêutica62. É aconselhável cuidadoso monitoramento clínico.
Gravidez63 e Lactação64
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Estudos indicam que não há malformação65 ou toxicidade66 para o feto67 e que Fragmin® pode ser usado durante a gravidez63 se for clinicamente necessário, sempre indicado pelo médico.
Estão disponíveis dados limitados sobre excreção (eliminação) de Fragmin ® no leite humano. Pequenas quantidades já foram detectadas, mas as implicações clínicas no lactente68, se houver, são desconhecidas.
Informe ao seu médico se estiver amamentando.
Com base nos dados clínicos atuais, não há evidência de que Fragmin® afete a fertilidade.
Efeitos na habilidade de dirigir e operar máquinas
O efeito de Fragmin® na capacidade de dirigir e operar máquinas não foi sistematicamente avaliado.
Interações Medicamentosas
A administração concomitante de medicamentos que agem na hemostasia42, como agentes trombolíticos, outros anticoagulantes43, AINEs, inibidores plaquetários, ou dextrana, pode potencializar o efeito anticoagulante54 de Fragmin®.
Porém, a menos que especificamente contraindicado, pacientes com doença arterial coronariana instável tratados com Fragmin® devem receber também doses baixas de ácido acetilsalicílico (75 a 325 mg/dia) por via oral.
Uma vez que doses de AINEs e do analgésico69/anti-inflamatório ácido acetilsalicílico reduzem a produção de prostaglandinas70 vasodilatadoras e, consequentemente, o fluxo sanguíneo e a excreção renal12, deve-se ter cautela especial ao administrar Fragmin® concomitantemente com AINEs ou com altas doses de ácido acetilsalicílico em pacientes com insuficiência renal11.
Interações com testes laboratoriais: Durante o tratamento com dalteparina, é recomendado acompanhamento periódico de hemograma completo, incluindo contagem de plaquetas27, exames bioquímicos do sangue6 e exame de sangue6 oculto nas fezes. Quando utilizado em doses recomendada para profilalxia, testes de rotina de coagulação8 tais como teste de tempo de protrombina71 (PT) e tempo parcial ativo de tromboplastina72 (APTT), possuem suas medidas relativamente insensíveis à atividade da dalteparina, portanto não é adequado monitorar o efeito anticoagulante54 de dalteparina. O anti-Fator Xa pode ser usado para monitorar o efeito anticoagulante54 de dalteparina, tais como em pacientes com disfunção renal12 grave ou parâmetros anormais de coagulação8 ou sangramento durante a terapia com dalteparina.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde73.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Fragmin® deve ser conservado em temperatura ambiente (15–30°C) e protegido da luz.
Após o preparo da solução para infusão intravenosa (IV), esta deve ser utilizada em no máximo 12 horas.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Fragmin® é uma solução clara, incolor ou parda.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Vide item “4. O que devo saber antes de usar este medicamento?”.
Fragmin® não deve ser administrado por via intramuscular.
Técnica de Administração de Injeção Subcutânea74 (SC)
- Fragmin® deve ser administrado por injeção75 por via subcutânea1 (SC) profunda, com o paciente na posição sentada ou deitada.
- Não toque na agulha nem deixe que ela toque em nenhuma superfície. Não toque nem empurre o êmbolo76. Isso pode provocar extravasamento do líquido.
- Fragmin® deve ser injetado na região abdominal peri-umbilical (em volta do umbigo77), na face78 externa superior da coxa79 ou no quadrante superior externo da nádega. Deve-se variar diariamente o local da aplicação. Quando se utilizar a região abdominal peri-umbilical ou a face78 externa superior da coxa79, deve-se fazer uma dobra de pele80 com os dedos indicador e polegar enquanto se aplica a injeção75. A agulha deve ser totalmente inserida, num ângulo que varia de 45 a 90°.
Procedimento para o Acionamento do Dispositivo de Proteção para o Descarte da Agulha
O dispositivo de proteção para descarte da agulha é fixado ao rótulo da seringa81 de Fragmin® e se estende paralelamente à seringa81 até a ponta da tampa plástica da agulha.
- O administrador deve puxar o dispositivo de proteção para baixo, separando-o da tampa plástica da agulha.
- Em seguida, a tampa plástica da agulha deve ser removida da seringa81.
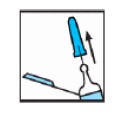
- O produto deve ser administrado normalmente.
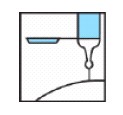
- Após a aplicação e remoção da agulha do paciente, o administrador deve ativar o dispositivo de proteção para descarte de todo o material, posicionando a seringa81 e a agulha sobre uma superfície estável e firme, e pressionando a seringa81 contra esta superfície de maneira que a agulha se encaixe no dispositivo de proteção. Um “click” é percebido quando a agulha estiver devidamente encaixada no dispositivo. A agulha deve então ser inclinada até que a seringa81 exceda um ângulo de 45° em relação à superfície plana, o que a torna inutilizável.
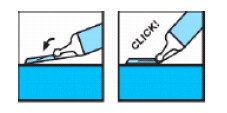
- Após os passos descritos anteriormente, a agulha e a seringa81 devem ser devidamente descartadas em local apropriado, conforme instruções abaixo.
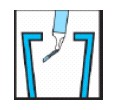
Manuseio e Descarte de Materiais Perfuro-Cortantes
No manuseio de seringas e agulhas descartáveis é necessário manter os seguintes cuidados:
- guardar o material, ainda na embalagem original, conforme cuidados de conservação já estabelecidos na embalagem deste produto;
- lavar as mãos82 com água e sabão antes do manuseio;
- manusear o material em campo limpo;
- antes de abrir, verificar:
- se a embalagem está íntegra e dentro do prazo de validade; e
- se o material é apropriado ao procedimento, a fim de evitar desperdício;
- abrir cuidadosamente a embalagem, na direção do êmbolo76 para a agulha, evitando a contaminação;
- usar luvas descartáveis para manuseio e aplicação do material.
Esta seringa81 e agulha devem ser descartadas no coletor de perfuro-cortantes, segundo recomendação das regulamentações vigentes, para evitar o risco de punção acidental do dedo ou da mão83. Quando não existir o recipiente apropriado, adaptar latas vazias com tampas, caixas de papelão duplamente reforçadas.
Todo o material a ser descartado deverá ser encaminhado a uma instituição de saúde73, de onde será coletado por empresas especializadas que se encarregam da coleta de resíduos biológicos e destruição por incineração.
A seringa81 preenchida é para administração única. A seringa81 e a agulha NUNCA devem ser reutilizadas. NUNCA reencapar a agulha com a tampa de borracha.
Compatibilidade com Soluções Intravenosas (IVs)
Fragmin® é compatível com solução para infusão de cloreto de sódio isotônica84 (9 mg/mL) ou de glicose85 isotônica84 (50 mg/mL) em frascos de vidro e recipientes plásticos.
Não foi estudada a compatibilidade entre Fragmin® e outros produtos; portanto, este produto não deve ser misturado com outras soluções injetáveis até que estejam disponíveis dados específicos de compatibilidade.
Tratamento de Trombose Venosa Profunda3 (TVP) e Embolia5 Pulmonar (EP) Agudas
Administrar Fragmin® por via subcutânea1 (SC) como uma injeção75 única diariamente ou como duas injeções diariamente. A anticoagulação simultânea com antagonistas de vitamina86 K orais pode ser iniciada imediatamente. Continuar com o tratamento combinado até que os exames do complexo protrombina71 tenham atingido níveis terapêuticos (geralmente pelo menos 5 dias). Tratamento ambulatorial é possível utilizando as mesmas doses recomendadas para tratamento em instituição médica.
Administração uma vez ao dia: 200 UI/kg de peso corporal total por via subcutânea1 (SC) uma vez ao dia, até um máximo de 18.000 UI. A monitorização do efeito anticoagulante54 não é necessária.
Administração duas vezes ao dia: Alternativamente, pode ser administrada uma dose de 100 UI/kg de peso corporal total por via subcutânea1 (SC) duas vezes ao dia. Se a monitorização for considerada necessária, os níveis sanguíneos de pico recomendados estão entre 0,5 e 1,0 UI anti-Xa/mL.
Prevenção de Coagulação8 no Sistema Extracorpóreo durante Hemodiálise9 e Hemofiltração
Administrar Fragmin® por via intravenosa (IV), selecionando o regime apropriado a partir das doses descritas abaixo.
Pacientes com insuficiência renal11 crônica ou pacientes com risco de sangramento: A monitorização frequente dos níveis de anti-Xa não é necessária para a maioria dos pacientes. As doses recomendadas geralmente produzem níveis no sangue6 de 0,5 a 1,0 UI anti-Xa/mL durante a diálise87.
Hemodiálise9 e hemofiltração até um máximo de 4 horas: Ou injeção75 em bolus88 IV de 30 a 40 UI/kg do peso corporal total seguida por infusão IV de 10 a 15 UI/kg/hora, ou injeção75 única em bolus88 IV de 5.000 UI.
Hemodiálise9 e hemofiltração por mais de 4 horas: Administrar injeção75 em bolus88 IV de 30 a 40 UI/kg do peso corporal total, seguida por infusão intravenosa (IV) de 10 a 15 UI/kg/hora.
Pacientes com insuficiência renal11 aguda ou pacientes com alto risco de sangramento: Administrar injeção75 em bolus88 IV de 5 a 10 UI/kg de peso corporal total, seguida por infusão intravenosa (IV) de 4 a 5 UI/kg/hora. Realizar monitorização abrangente dos níveis de anti-Xa. Os níveis sanguíneos recomendados estão entre 0,2 e 0,4 UI anti-Xa/mL.
Tromboprofilaxia Associada à Cirurgia
Administrar Fragmin® por via subcutânea1 (SC). A monitorização do efeito anticoagulante54 geralmente não é necessária. Se realizada, coletar amostras 3 a 4 horas após injeção subcutânea74 (SC), quando a droga atinge pico no sangue6. As doses recomendadas geralmente produzem níveis sanguíneos de pico entre 0,1 UI a 0,4 UI anti- Xa/mL.
Cirurgia geral com risco de complicações tromboembólicas
2.500 UI por via subcutânea1 (SC) até 2 horas antes da cirurgia e, nas manhãs após cirurgia, 2.500 UI por via subcutânea1 (SC) até mobilização do paciente (em geral, 5 a 7 dias ou mais).
Cirurgia geral com fatores de risco adicionais para tromboembolismo19 (por exemplo, malignidade)
Administrar Fragmin® até a mobilização do paciente (em geral, 5 a 7 dias ou mais).
A monitorização do efeito anticoagulante54 geralmente não é necessária, mas, se realizada, níveis sanguíneos de pico recomendados estão entre 0,5 e 1,0 UI anti-Xa/mL.
Início no dia anterior à cirurgia: 5.000 UI por via subcutânea1 (SC) na noite anterior e nas noites posteriores à cirurgia.
Início no dia da cirurgia: 2.500 UI por via subcutânea1 (SC) até 2 horas antes da cirurgia e 2.500 UI por via subcutânea1 (SC) após 8 a 12 horas, mas não antes de 4 horas após o fim da cirurgia, nos dias seguintes, 5000 UI por via subcutânea1 (SC) a cada manhã.
Cirurgia ortopédica (de osso)
Administrar Fragmin® por até 5 semanas após a cirurgia, selecionando um dos regimes posológicos listados abaixo:
Início na noite anterior à cirurgia: 5.000 UI por via subcutânea1 (SC) na noite anterior e nas noites posteriores à cirurgia.
Início no dia da cirurgia: 2.500 UI por via subcutânea1 (SC) até 2 horas antes da cirurgia e 2500 UI após 8 a 12 horas, mas não antes de 4 horas após o fim da cirurgia, nos dias seguintes, 5.000 UI por via subcutânea1 (SC) a cada manhã.
Início no pós-operatório: 2.500 UI por via subcutânea1 (SC) de 4 a 8 horas após a cirurgia, mas não antes de 4 horas após o fim da cirurgia, nos dias seguintes, 5.000 UI por via subcutânea1 (SC)por dia.
Tromboprofilaxia em Pacientes com Mobilidade Restrita
Administrar 5.000 UI por via subcutânea1 (SC) de Fragmin® uma vez ao dia, geralmente por 12 a 14 dias ou mais em pacientes com mobilidade restrita continuada. A monitorização do efeito anticoagulante54 geralmente não é necessária.
Doença Arterial Coronariana Instável (Angina16 Instável e Infarto do Miocárdio89 sem elevação ST)
Administrar 120 UI/kg de peso corporal total por via subcutânea1 (SC) de Fragmin® a cada 12 horas (dose máxima de 10.000 UI/12 horas), até que o paciente esteja clinicamente estável. Os pacientes também devem receber junto com Fragmin® o ácido acetilsalicílico (75 a 325 mg/dia), exceto naqueles pacientes que o médico identifique que o uso seja contraindicado. Depois disso, é recomendado tratamento prolongado com dose fixa de Fragmin® selecionada de acordo com o sexo e peso do paciente, até que o procedimento de revascularização (cateterismo90 ou ponte de safena) seja realizado. O período de tratamento total não deve exceder 45 dias:
- Para mulheres com menos de 80 kg e homens com menos de 70 kg, administrar 5.000 UI por via subcutânea1 (SC) a cada 12 horas.
- Para mulheres com pelo menos 80 kg e homens com pelo menos 70 kg, administrar 7.500 UI por via subcutânea1 (SC) a cada 12 horas.
Tratamento Prolongado de Tromboembolismo19 Venoso (TEV) Sintomático20 para Reduzir a Recorrência22 de TEV em Pacientes com Câncer23
Mês 1
Administrar 200 UI/kg de peso corporal total por via subcutânea1 (SC) de Fragmin® uma vez ao dia pelos primeiros 30 dias de tratamento. A dose diária total não deve exceder 18.000 UI por dia.
Meses 2–6
Fragmin® deve ser administrado na dose de aproximadamente 150 UI/kg por via subcutânea1 (SC) uma vez ao dia, utilizando seringas de dose fixa e a Tabela 1 abaixo.
Tabela 1. Determinação da dose para os meses 2 a 6
|
Peso Corporal (kg) |
Dose de Fragmin® (UI) |
|
≤ 56 |
7500 |
|
57 a 68 |
10.000 |
|
69 a 82 |
12.500 |
|
83 a 98 |
15.000 |
|
≥ 99 |
18.000 |
Reduções de dose para trombocitopenia25 induzida por quimioterapia91
No caso de contagens de plaquetas27 < 50.000/mm3, Fragmin® deve ser interrompido até que a contagem de plaquetas27 seja restabelecida acima de 50.000/mm3.
Para contagens de plaquetas27 entre 50.000/mm3 e 100.000/mm3, a dose de Fragmin® deve ser reduzida conforme Tabela 2. Quando a contagem de plaquetas27 for restabelecida para ≥ 100.000/mm3, Fragmin® deve ser restabelecido na dose total.
Tabela 2: Redução da dose de Fragmin® para trombocitopenia25 de 50.000/mm3 a 100.000/mm3
|
Peso Corporal (kg) |
Dose Planejada de Fragmin® (UI) |
Dose Reduzida de Fragmin® (UI) |
Redução Média da Dose (%) |
|
≤ 56 |
7500 |
5000 |
33 |
|
57 a 68 |
10.000 |
7500 |
25 |
|
69 a 82 |
12.500 |
10.000 |
20 |
|
83 a 98 |
15.000 |
12.500 |
17 |
|
≥ 99 |
18.000 |
15.000 |
17 |
Insuficiência renal11
No caso de insuficiência renal11 significante, o nível de anti-Xa deve ser monitorado e a dose de Fragmin® ajustada para manter nível terapêutico de anti-Xa de 1 UI/mL (intervalo de 0,5 – 1,5 UI/mL), medido 4 a 6 horas após a injeção75 de Fragmin®. Após ajuste, a medição de anti-Xa deve ser repetida após 3 – 4 novas doses. Este ajuste de dose deve ser repetido até que o nível terapêutico de anti-Xa seja alcançado.
Uso em Crianças
A segurança e eficácia da Fragmin® em crianças não foram estabelecidas. Se for utilizada nesta população, a monitorização com exame de sangue6 específico (medição dos níveis de pico de anti-Xa) deve ser considerada. Nos recém-nascidos a monitoração cuidadosa dos níveis de anti-Xa é necessária.
Como ocorre com todos os medicamentos anticoagulantes43, há risco de hemorragia47 com o uso da Fragmin. É preciso ter cuidado com o uso de doses elevadas de dalteparina sódica no tratamento de pessoas recém-operadas.
Depois de iniciado o tratamento, os pacientes devem ser monitorizados cuidadosamente quanto a complicações hemorrágicas92.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Caso você esqueça de aplicar Fragmin no horário estabelecido pelo seu médico, aplique-o assim que lembrar. Entretanto, se já estiver perto do horário de tomar a próxima dose, pule a dose esquecida e aplique a próxima, continuando normalmente o esquema de doses recomendado pelo seu médico. Neste caso, não aplique o medicamento em dobro para compensar doses esquecidas. O esquecimento de dose pode comprometer a eficácia do tratamento.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Aproximadamente 3% dos pacientes recebendo tratamento profilático relataram efeitos colaterais93.
As reações adversas relatadas, que podem estar associadas à Fragmin, estão listadas na tabela abaixo por frequência:
Reações comuns (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento): trombocitopenia25 (diminuição das células26 de coagulação8 do sangue6: plaquetas27) leve (tipo I) normalmente reversível durante tratamento, hemorragia47 (perda excessiva de sangue6), elevação transitória de transaminases (enzimas do fígado49), hematoma38 subcutâneo94 (sangue6 retido abaixo da pele80) no local da injeção75 e dor no local da injeção75.
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento): hipersensibilidade (reações alérgicas).
Reações raras (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento): necrose95 (morte das células26) de pele80 e alopecia96 (queda de cabelos) temporária.
Reações com frequência não conhecida (impossível estabelecer a partir dos dados disponíveis): trombocitopenia25 imunologicamente mediada induzida por heparina (tipo II com ou sem complicações trombóticas97 associadas); reações anafiláticas98 (reações alérgicas graves); sangramentos intracranianos (sangramento dentro do crânio99), alguns fatais; sangramentos retroperitoneais (na parte posterior do abdômen), alguns fatais; rash100 (vermelhidão na pele80) e hematoma38 espinhal ou epidural36 (acúmulo de sangue6 no espaço entre a meninge e a medula espinhal33) (vide item “3. Quando não devo usar este medicamento?” e “4. O que devo saber antes de usar este medicamento?”).
População pediátrica
É esperado que a frequência, o tipo e a gravidade das reações alérgicas em crianças sejam os mesmos que em adultos. A segurança da administração prolongada da dalteparina ainda não foi estabelecida.
Atenção: este produto é um medicamento que possui nova indicação terapêutica62 e nova via de administração no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico.
Informe também à empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Caso alguém use uma dose excessiva de Fragmin®, o efeito anticoagulante54 (que inibe a coagulação8) induzido por ele pode ser inibido pela protamina.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS - 1.0216.0234
Farmacêutica Responsável: Carolina C. S. Rizoli - CRF-SP Nº 27071
Registrado por:
Laboratórios Pfizer Ltda.
Rodovia Presidente Castelo Branco, nº 32.501, Km 32,5
CEP 06696-000 - Itapevi – SP
CNPJ nº 46.070.868/0036-99
Fabricado e Embalado (embalagem primária) por:
Vetter Pharma-Fertigung, GmbH & Co.
KG Ravensburg – Alemanha
Embalado (embalagem secundária) por:
Pfizer Manufacturing Belgium NV Puurs – Bélgica
Importado por:
Wyeth Indústria Farmacêutica Ltda.
Rodovia Presidente Castelo Branco, nº 32.501, Km 32,5
CEP 06696-000 - Itapevi – SP
SAC 0800 770 1575