Sarclisa
SANOFI MEDLEY FARMACÊUTICA LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
SARCLISATM
isatuximabe
APRESENTAÇÕES
Solução para diluição para infusão 100 mg/5 mL: embalagem contendo 1 frasco-ampola com 5 mL.
Solução para diluição para infusão 500 mg/25 mL: embalagem contendo 1 frasco-ampola com 25 mL
USO INTRAVENOSO (IV)
USO ADULTO
COMPOSIÇÃO
Cada mL da solução para diluição para infusão contém 20 mg de isatuximabe.
Excipientes: sacarose, histidina, cloridrato de histidina monoidratado, polissorbato 80 e água para injetáveis.
INFORMAÇÕES DO MEDICAMENTO
PARA QUE ESTE MEDICAMENTO É INDICADO?
SARCLISA é indicado para o tratamento de pacientes adultos com mieloma1 múltiplo (um tipo de câncer2 da medula óssea3). SARCLISA é utilizado juntamente com pomalidomida e dexametasona por pacientes com mieloma1 múltiplo recidivado e refratário que receberam pelo menos duas terapias anteriores, incluindo lenalidomida e um inibidor de proteassoma, e demonstraram progressão da doença na última terapia.
COMO ESTE MEDICAMENTO FUNCIONA?
O SARCLISA é um medicamento anticâncer que contém a substância ativa isatuximabe. O isatuximabe é um anticorpo4 monoclonal (proteínas5 que reconhecem e se ligam às proteínas5 específicas do corpo) que se liga a um epítopo extracelular específico do receptor CD38 e desencadeia vários mecanismos que levam à morte de células6 tumorais que expressam CD38.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Este medicamento não deve ser utilizado em pacientes alérgicos ao isatuximabe ou a qualquer outro componente da formulação.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Advertências e precauções
Reações à infusão
Reações à infusão podem ocorrer durante ou após a infusão com SARCLISA no dia da infusão. Informe imediatamente o seu médico se tiver sintomas7 de reação à infusão durante ou após a infusão de SARCLISA.
Os sintomas7 mais comuns incluem dispneia8 (falta de ar), tosse, calafrios9 e náusea10. Os sinais11 e sintomas7 graves mais comuns incluem hipertensão12 (pressão alta) e dispneia8 (vide item 8. Quais os males que este medicamento pode me causar?).
Interferência no teste sorológico (teste indireto de antiglobulina)
SARCLISA se liga ao CD38 nas células6 vermelhas do sangue13 (CVS) e pode resultar em um teste de antiglobulina indireta falso positivo (teste indireto de Coombs).
Para evitar possíveis problemas com a transfusão14 de sangue13, você deve realizar exames de tipo sanguíneo e de triagem antes da primeira infusão com SARCLISA.
Neutropenia15 (diminuição do número de glóbulos brancos do sangue13)
SARCLISA pode diminuir o número de seus glóbulos brancos, importantes no combate a infecções16. Informe imediatamente o seu médico se tiver febre17.
Interferência com testes laboratorial e diagnóstico18
Interferência nos testes sorológicos
Como a proteína CD38 é expressa na superfície de células6 vermelhas do sangue13, SARCLISA, um anticorpo4 anti-CD38, pode interferir nos testes sorológicos do banco de sangue13 com possíveis reações falso positivas em testes indiretos de antiglobulina (testes indiretos de Coombs), testes de detecção (triagem) de anticorpos19, painéis de identificação de anticorpos19 e combinações cruzadas de globulina20 anti-humano (GAH) em pacientes tratados com SARCLISA.
A interferência nos testes de eletroforese e imunofixação de proteínas5 séricas
SARCLISA pode ser detectada eventualmente por ensaios de eletroforese de proteínas5 séricas (EPS) e imunofixação (EFI) usados para o monitoramento da proteína M e pode interferir na classificação precisa da resposta.
Gravidez21 e lactação22
Informe o seu médico se você está grávida ou planejando engravidar, ou se você está amamentando. O uso de SARCLISA em mulheres gravidas não é recomendado.
Com base em seu mecanismo de ação, SARCLISA pode causar danos fetais quando administrado a uma mulher grávida. SARCLISA pode causar redução de células6 imunes fetais (CD38-positiva) e diminuição da densidade óssea.
A administração de vacinas vivas a recém-nascidos e bebês23 expostos ao SARCLISA no útero24 deve ser adiada até que uma avaliação hematológica seja realizada.
A combinação de SARCLISA com pomalidomida é contraindicada em mulheres grávidas, pois a pomalidomida pode causar defeitos congênitos25 e morte do feto26. Consulte as informações de prescrição da pomalidomida sobre o uso durante a gravidez21. Para outros medicamentos administrados com SARCLISA, consulte as respectivas informações de bulas atuais.
Não há dados disponíveis sobre a presença de SARCLISA no leite humano, na produção de leite ou os efeitos sobre o bebê amamentado. O uso de SARCLISA em mulheres que amamentam não é recomendado.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez21.
Fertilidade
Mulheres que estão utilizando SARCLISA e podem engravidar devem usar um método contraceptivo eficaz durante o tratamento e por pelo menos 5 meses após a última dose de SARCLISA.
Risco de novo câncer2
Você deve ser monitorado pelo seu médico quanto ao risco de desenvolvimento de um novo câncer2.
Alterações na capacidade de dirigir veículos e utilizar máquinas
Com base nas reações adversas relatadas, não se espera que SARCLISA influencie a capacidade de dirigir e utilizar máquinas. No entanto, foram relatadas fadiga27 e tontura28 em pacientes que tomam SARCLISA e isso deve ser levado em consideração ao dirigir ou utilizar máquinas.
Atenção diabéticos: este medicamento contém açúcar29.
INTERAÇÕES MEDICAMENTOSAS
A farmacocinética de SARCLISA e pomalidomida não foram influenciadas pela sua administração conjunta.
Informe ao seu médico se você está fazendo uso de algum outro medicamento.
Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde30.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Este medicamento deve ser mantido sob refrigeração (entre 2°C e 8ºC). Proteger da luz. Não congelar. Não agitar.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Após preparado manter entre 2°C e 8°C por até 48 horas, seguidas por 8 horas (incluindo o tempo de infusão) à temperatura ambiente.
Características do medicamento
Este medicamento apresenta-se como uma solução incolor a ligeiramente amarela, essencialmente livre de partículas visíveis.
Antes de usar, observe o aspecto do medicamento.
Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
Todo medicamento deve ser mantido fora do alcance das crianças.
COMO DEVO USAR ESTE MEDICAMENTO?
A dose recomendada de SARCLISA é de 10 mg/kg de peso corpóreo administrada por infusão (gota31 a gota31) em uma veia (intravenosa) em combinação com pomalidomida e dexametasona.
SARCLISA é utilizado em ciclos de tratamento de 28 dias (4 semanas) juntamente com pomalidomida e dexametasona.
No Ciclo 1: SARCLISA é administrado semanalmente nos dias 1, 8, 15 e 22
No Ciclo 2 e posteriores: SARCLISA é administrado a cada 2 semanas no dia 1 e 15.
Pré-medicação
A pré-medicação deve ser usada antes da infusão de SARCLISA com os seguintes medicamentos para reduzir o risco e a gravidade das reações à infusão (RIs):
- Dexametasona 40 mg via oral ou IV (ou 20 mg via oral ou IV em pacientes com idade >= 75 anos).
- Acetaminofeno 650 mg a 1000 mg via oral (ou equivalente).
- Antagonistas de H2 (ranitidina 50 mg IV ou equivalente [por exemplo, cimetidina]) ou inibidores da bomba de prótons por via oral (por exemplo, omeprazol, esomeprazol).
- Difenidramina 25 mg a 50 mg IV ou via oral (ou equivalente [por exemplo, cetirizina, prometazina, dexclorfeniramina]). A via intravenosa é preferida para pelo menos as 4 primeiras infusões.
A dose acima recomendada de dexametasona (via oral ou IV) corresponde à dose total a ser administrada apenas uma vez antes da infusão, como parte da pré-medicação e do tratamento da coluna vertebral32, antes da administração de SARCLISA e pomalidomida.
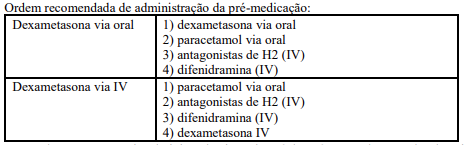
Caso a dexametasona seja administrada via oral, está deverá ser usada antes das demais pré-medicações, enquanto se for via IV, deverá ser administrada logo antes de SARCLISA, porém nunca de modo concomitante.
A dexametasona administrada antes da infusão de SARCLISA corresponde à terapia combinada33 proposta e, portanto, esta deve ser mantida mesmo na ausência de reações à infusão nas primeiras 4 administrações de SARCLISA.
Os agentes de pré-medicação recomendados devem ser administrados 15 a 60 minutos antes do início de uma infusão de SARCLISA. Pacientes que não apresentam RI nas 4 primeiras administrações de SARCLISA podem ter sua necessidade de pré-medicação subsequente reconsiderada.
Seu médico continuará o tratamento até a progressão da doença ou toxicidade34 inaceitável.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento.
Não interrompa o tratamento sem o conhecimento de seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Seu médico terá as instruções de quando administrar este medicamento para você.
Se uma dose planejada de SARCLISA for perdida, a dose deverá ser administrada o mais rápido possível e o esquema de tratamento deverá ser ajustado adequadamente, conforme orientação do seu médico.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Reação muito comum (ocorre em mais de 10% dos pacientes que utilizam este medicamento).
Reação comum (ocorre entre 1% e 10% dos pacientes que utilizam este medicamento).
Reação incomum (ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento).
Reação rara (ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento).
Reação muito rara (ocorre em menos de 0,01% dos pacientes que utilizam este medicamento).
Frequência não conhecida: não podem ser estimados com os dados disponíveis.
Como todos os medicamentos, este medicamento pode causar efeitos colaterais35, embora nem todos os apresentem. Reações adversas muito comuns:
- diminuição do número de glóbulos vermelhos (anemia36)
- diminuição do número de tipos de glóbulos brancos (neutrófilos37 ou linfócitos que são importantes no combate à infecção38)
- diminuição do número de plaquetas39 no sangue13 (trombocitopenia40). Informe o seu médico ou enfermeiro se tiver algum hematoma41 ou sangramento incomum.
- reações à infusão
- infecção38 dos pulmões42 (pneumonia43)
- infecção38 das vias aéreas (como nariz44, seios nasais45 ou garganta46)
- diarreia47
- bronquite
- sentir falta de ar (dispneia8)
- náusea10
- febre17 associada a uma diminuição grave do número de alguns glóbulos brancos (neutropenia15 febril)
- vômito48
Reações adversas comuns:
- arritmia49 cardíaca, na qual ritmo cardíaco é geralmente irregular e rápido (fibrilação atrial)
- desenvolvimento de um novo câncer2 (segunda malignidade primária)
- diminuição do apetite
- perda de peso
Reações de infusão
Reações de infusão (reações adversas associadas às infusões de SARCLISA, com início tipicamente dentro de 24 horas após o início da infusão) foram relatadas em pacientes tratados com SARCLISA.
Infecções16
A pneumonia43 foi a infecção38 grave mais comumente relatada.
Imunogenicidade
Como com todas as proteínas5 terapêuticas, existe um potencial de imunogenicidade com SARCLISA, ou seja, o produto pode levar a uma reação imunológica, ativando o sistema de defesa do organismo contra o agente externo.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico.
Nenhum caso de sobredosagem com isatuximabe foi reportado.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA. USO RESTRITO A HOSPITAIS.
MS 1.8326.0474
Farm. Resp: Ricardo Jonsson CRF-SP nº 40.796
Registrado e Importado por:
Sanofi Medley Farmacêutica Ltda.
Rua Conde Domingos Papaiz, 413 – Suzano – SP CNPJ: 10.588.595/0010-92
Indústria Brasileira
Fabricado e embalado por:
Sanofi-Aventis Deutschland GmbH
Brüningstrasse 50, 65926 Frankfurt am Main - Alemanha