Hibor
EMS S/A
IDENTIFICAÇÃO DO MEDICAMENTO
Hibor®
bemiparina sódica
Injetável 2.500 UI; 3.500 UI; 5.000 UI; 7.500 UI; 10.000 UI
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Seringas preenchidas de 0,2 mL, 0,3 mL ou 0,4 mL
USO INJETÁVEL (via subcutânea1)
USO ADULTO
COMPOSIÇÃO:
Cada seringa2 de Hibor® 2.500 UI contém:
| bemiparina sódica | 2.500 UI (anti-Xa) |
| veículo q.s.p. | 0,2 mL |
Veículo: água para injetáveis.
Cada seringa2 de Hibor® 3.500 UI contém:
| bemiparina sódica | 3.500 UI (anti-Xa) |
| veículo q.s.p. | 0,2 mL |
Veículo: água para injetáveis.
Cada seringa2 de Hibor® 5.000 UI contém:
| bemiparina sódica | 5.000 UI (anti-Xa) |
| veículo q.s.p. | 0,2 mL |
Veículo: água para injetáveis.
Cada seringa2 de Hibor® 7.500 UI contém:
| bemiparina sódica | 7.500 UI (anti-Xa) |
| veículo q.s.p. | 0,3 mL |
Veículo: água para injetáveis.
Cada seringa2 de Hibor® 10.000 UI contém:
| bemiparina sódica | 10.000 UI (anti-Xa) |
| veículo q.s.p. | 0,4 mL |
Veículo: água para injetáveis.
Atividade aproximada do Fator anti-X ativado (anti-Xa) em unidades internacionais (UI).
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Hibor® está indicado para prevenir a formação de coágulos (ou trombos3) dentro dos vasos sanguíneos4 (trombose venosa profunda5), em particular para os casos após a realização de uma cirurgia geral ou ortopédica, ou ainda, em pacientes não cirúrgicos que encontram-se acamados por causa de alguma doença Também previne a formação de coágulos durante tratamentos de hemodiálise6 (tratamento artificial de filtração do sangue7).
Hibor® está indicado no tratamento da trombose venosa profunda5 estabelecida (quando os coágulos já estão formados), com ou sem embolia8 pulmonar (que é quando esses coágulos migram para os pulmões9, entupindo as artérias10 pulmonares), evitando assim o crescimento dos coágulos já existentes, e impedindo o surgimento de novos coágulos.
COMO ESTE MEDICAMENTO FUNCIONA?
Hibor® diminui o risco de desenvolvimento de coágulos dentro dos vasos sanguíneos4 (trombose venosa profunda5), bem como sua consequência mais grave, que é quando esses coágulos chegam aos pulmões9, entupindo as artérias10 pulmonares (embolia8 pulmonar).
Hibor® previne e trata essas duas doenças, evitando o crescimento dos coágulos já formados, e impedindo o surgimento de novos coágulos que levariam à piora do quadro, ou ainda, a ocorrência de novos episódios de trombose11.
A duração do tratamento com Hibor® pode variar de um indivíduo para o outro.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
A bemiparina, como as outras heparinas de baixo peso molecular, não deve ser utilizada nos seguintes casos:
- Hemorragias12 ativas de grande porte e condições com alto risco de desenvolvimento de hemorragia13 incontrolável, incluindo acidente vascular cerebral14 hemorrágico15 (sangramento cerebral) recente.
- Hipersensibilidade (alergia16) à bemiparina, aos constituintes produto, à heparina ou a substâncias de origem suína.
- Antecedente ou suspeita de uma queda no número de plaquetas17 (trombocitopenia18) ou coagulação19 intravascular20 disseminada (CIVD) induzida por heparina;
- Insuficiência21 severa da função do fígado22 e/ou do pâncreas23;
- Lesões24 e operações no sistema nervoso central25, olhos26 e ouvidos;
- Endocardite27 bacteriana aguda ou subaguda28;
- Lesões24 orgânicas com alto risco de sangramento (ex: úlcera29 gastroduodenal ativa, hemorragia13 cerebral, aneurismas cerebrais ou neoplasias30 cerebrais).
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião dentista.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
Não administrar pela via intramuscular.
Devido ao risco de hematomas31 durante a administração de bemiparina, a injeção intramuscular32 de outros agentes deve ser evitada.
Cuidado especial está indicado nos casos de:
- Doença hepática33 ou renal34;
- Hipertensão arterial35 não controlada, antecedentes de úlcera29 gastroduodenal, cálculos renais ou uretrais, em caso de doença vascular36 ocular (coroides ou retina37) ou qualquer outra lesão38 orgânica com aumento do risco de sangramento;
- Em caso de níveis de potássio elevados no sangue7, como pode ocorrer caso tenha diabetes39, doença renal34 crônica, acidose40 no sangue7 ou se toma fármacos que alterem estes níveis, como alguns diuréticos41. O médico pode recomendar o controle dos níveis de potássio.
- Presença ou histórico de trombocitopenia18 (baixa de plaquetas17). O médico pode recomendar o controle de plaquetas17.
- Histórico de lesões24 cutâneas42 coincidindo com a administração de heparinas.
- Precaução especial em idosos, como ocorre com a maioria dos medicamentos.
Monitoramento da contagem de plaquetas17 (elemento do sangue7 que participa da coagulação19 sanguínea): O risco de trombocitopenia18 (diminuição no número de plaquetas17) induzida por heparina também existe com heparinas de baixo peso molecular. Pode ocorrer trombocitopenia18 geralmente entre o 5º e 21º dia após o início do tratamento com Hibor®. Portanto, recomenda-se a realização de contagem plaquetária antes do início e regularmente durante o tratamento com Hibor®.
Na prática, o tratamento deve ser descontinuado imediatamente e uma alternativa iniciada, se uma redução significante na contagem de plaquetas17 for observada (30 a 50%), associada com resultados positivos ou desconhecidos de testes in vitro para anticorpos43 antiplaquetários na presença de bemiparina ou de outra HBPM (heparina de baixo peso molecular) e/ou heparinas.
Assim como outras heparinas, casos de necroses cutâneas42, algumas vezes precedidos de manchas roxas eritematosas44 dolorosas têm sido relatados com bemiparina. Nestes casos, o tratamento deve ser descontinuado imediatamente.
Trombocitopenia18 induzida pela heparina: Hibor® deve ser utilizado com extrema cautela em pacientes com histórico de trombocitopenia18 induzida pela heparina, com ou sem trombose11. O risco de trombocitopenia18 induzida por heparina pode persistir por vários anos. Em caso de suspeita de histórico de trombocitopenia18 induzida por heparina, os testes de agregação plaquetária in vitro têm valor preditivo limitado. A decisão do uso de Hibor® em tais casos deve ser tomada somente por um especialista.
Anestesia45 espinhal / epidural46:
O médico deve decidir a administração do tratamento do anticoagulante47 no contexto da anestesia45 epidural46 ou espinhal, vigilância extrema e frequente monitoria devem ser exercidas para detectar qualquer sinal48 e sintomas49 neurológicos, como dor nas costas50, déficits sensoriais e motores (hipoestesia51 ou fraqueza nos membros inferiores) e disfunção intestinal ou urinária. Os pacientes devem ser instruídos a informar a enfermeira ou médico imediatamente se tiverem estes sintomas49.
Gravidez52 e Lactação53
Hibor®, como as outras heparinas de baixo peso, não deve ser utilizado por mulheres grávidas ou lactantes54 sem orientação médica. Informe ao seu médico ou cirurgião-dentista se ocorrer gravidez52 ou iniciar amamentação55 durante o uso deste medicamento.
Efeitos na capacidade de dirigir ou operar máquinas
Hibor® não influencia na capacidade de dirigir veículos ou operar máquinas.
Populações especiais:
Pediatria: A segurança e a eficácia de Hibor® em crianças ainda não foram estabelecidas. Cuidado especial em crianças, já que não há experiência no tratamento com estes pacientes.
Pacientes idosos: As doses e cuidados para pacientes56 idosos são as mesmas recomendadas para os adultos. Precaução especial com idosos, como ocorre com as heparinas de baixo peso, e com maioria dos medicamentos.
Toxicidade57 Reprodutiva/ Mutagenicidade
Dados pré-clínicos da bemiparina não revelam risco especial para humanos baseados em estudos convencionais de segurança farmacológica, toxicidade57 de dose única e repetida, genotoxicidade e toxicidade57 reprodutiva.
Carcinogenicidade
Não há dados de carcinogenicidade até o momento.
INTERAÇÕES MEDICAMENTOSAS
Medicamento-medicamento
Converse com seu médico caso esteja utilizando os medicamentos abaixo:
- salicilatos sistêmicos58, ácido acetilsalicílico e outros anti-inflamatórios não-esteroidais (AINEs), incluindo o cetorolaco;
- dextrana 40, ticlopidina e clopidogrel;
- glicocorticoides sistêmicos58;
- agentes trombolíticos e anticoagulantes59;
- outros agentes antiplaquetários, incluindo os antagonistas de glicoproteína IIb/IIIa.
- nitroglicerina
Em caso de qualquer uma destas associações, deve-se utilizar Hibor® sob monitoramento clínico e laboratorial quando apropriado.
Os fármacos que aumentam os níveis de potássio no plasma60 somente devem ser administrados sob supervisão médica.
Interferência em exames laboratoriais
As heparinas de baixo peso molecular podem causar alteração nos resultados de alguns exames laboratoriais, tais como potássio sérico, e outros exames que avaliam a coagulação19 do sangue7.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para sua saúde61.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Hibor® deve ser conservado em temperatura entre 15 e 30°C (não pode ser congelado), e protegido da luz, dentro de sua caixa original (cartucho).
Hibor® possui validade de 24 meses a partir da data de fabricação. As seringas são somente para uso único.
Descartar o resto do produto não utilizado.
Não utilize se a embalagem protetora estiver aberta ou danificada.
Depois de aberto, este medicamento deve ser utilizado imediatamente.
Características físicas e organolépticas do produto
Utilizar apenas se a solução estiver incolor, ou levemente amarelada, sem partículas visíveis.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo. Depois de aberto, este medicamento deve ser utilizado imediatamente.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
Hibor® deve ser administrado por via subcutânea1. Não administre por via intramuscular.
Devido ao risco de aparição de manchas roxas durante o tratamento com bemiparina, deve ser evitada a injeção intramuscular32 de outros agentes.
Hibor® 2.500 UI
Adultos
- Cirurgia Geral com risco moderado de tromboembolismo62 venoso: No dia do procedimento cirúrgico, 2.500 UI devem ser administradas por via subcutânea1, 2 horas antes ou 6 horas após a cirurgia. Nos dias subsequentes, 2.500 UI devem ser administradas por via subcutânea1 a cada 24 horas.
O tratamento profilático deve ser seguido de acordo com a opinião do médico durante o período de risco ou até o paciente ser mobilizado. Como regra geral, é necessário manter o tratamento profilático por pelo menos 7–10 dias após o procedimento cirúrgico, até a redução do risco de tromboembolismo62. - Prevenção do Tromboembolismo62 Venoso em pacientes não cirúrgicos: A posologia recomendada de bemiparina é de 2.500 UI administradas por via subcutânea1 uma vez por dia, quando o conjunto de fatores de risco apresentados pelo paciente definirem seu risco de incidência63 de evento tromboembólico como moderado.
O tratamento profilático deve ser continuado, de acordo com critério médico, durante o período de risco ou até a completa mobilização do paciente. - Prevenção da Coagulação19 no circuito extracorpóreo durante a hemodiálise6: Para pacientes56 submetidos a hemodiálises repetidas de não mais de 4 horas de duração e sem risco de sangramento, a prevenção da coagulação19 no circuito extracorpóreo durante a hemodiálise6 é obtida pela injeção64 de uma dose única in bolus65 na linha arterial no início da sessão da diálise66. Para pacientes56 que pesam menos que 60 kg, a dose deve ser de 2.500 UI, entretanto para pacientes56 pesando mais de 60 kg, a dose deve ser de 3.500 UI.
Crianças: A segurança e eficácia do uso da bemiparina em crianças não foram estabelecidas, portanto o uso em crianças não é recomendado.
Idosos: O ajuste de dose não é necessário.
Hibor® 3.500 UI
Adultos
- Cirurgia Ortopédica com alto risco de tromboembolismo62 venoso: No dia do procedimento cirúrgico, 3.500 UI devem ser administradas por via subcutânea1, 2 horas antes, ou 6 horas após a cirurgia. Nos dias subsequentes, 3.500 UI devem ser administradas por via subcutânea1 a cada 24 horas.
O tratamento profilático deve ser seguido de acordo com a opinião do médico durante o período de risco, ou até o paciente ser mobilizado. Como regra geral, é necessário manter o tratamento profilático por pelo menos 7–10 dias após o procedimento cirúrgico e até o risco da doença tromboembolítica diminuir. - Prevenção da Doença Tromboembólica em pacientes não cirúrgicos: A posologia recomendada de bemiparina é 3.500 UI uma vez por dia, quando o conjunto de fatores de risco que os pacientes apresentarem, o definam como de alto risco tromboembólico.
O tratamento profilático deve ser continuado, de acordo com critério médico, durante o período de risco ou até a completa mobilização do paciente. - Prevenção Secundária da recorrência67 de tromboembolismo62 venoso em pacientes com trombose venosa profunda5 e fatores de risco transitórios: A bemiparina pode ser administrada na dose fixa de 3.500 UI/dia (até no máximo 3 meses) em pacientes que receberam tratamento anticoagulante47 para trombose venosa profunda5 com ou sem tromboembolismo62 pulmonar, como terapia alternativa à administração de anticoagulantes59 orais ou se estes forem contraindicados.
- Prevenção da Coagulação19 no circuito extracorpóreo durante a hemodiálise6: Para pacientes56 submetidos a hemodiálises repetidas de não mais de 4 horas de duração e sem risco de sangramento, a prevenção da coagulação19 no circuito extracorpóreo durante a hemodiálise6 é obtida pela injeção64 de uma dose única in bolus65 na linha arterial no inicio da sessão da diálise66. Para pacientes56 que pesam menos que 60 kg, a dose deve ser de 2.500 UI. Entretanto, para pacientes56 pesando mais de 60 kg, a dose deve ser de 3.500 UI.
Crianças: A segurança e eficácia do uso da bemiparina em crianças não foram estabelecidas, portanto o uso em crianças não é recomendado.
Idosos: O ajuste de dose não é necessário.
Hibor® 5.000 UI; Hibor® 7.500 UI; Hibor® 10.000 UI
Adultos
- Tratamento da trombose venosa profunda5: Hibor® (bemiparina sódica) deve ser administrado por via subcutânea1 na dose fixa de 115 UI anti-Xa/kg de peso, uma vez ao dia. A duração recomendada do tratamento é de 7 ± 2 dias. A dose diária geralmente corresponde (conforme a variação do peso corpóreo) às seguintes doses e volumes do produto em seringas preenchidas: <50 kg, 0,2 mL (5.000 UI anti-Xa); 50–70 kg, 0,3 mL (7.500 UI anti-Xa), >70 kg, 0,4 mL (10.000 UI anti-Xa).
Em pacientes pesando mais que 100 kg, a dose deve ser calculada baseado na seguinte equação: 115 UI anti-Xa/kg/dia, sendo a concentração de 25.000 UI/mL.
Na ausência de qualquer contraindicação, o anticoagulante47 oral deve ser iniciado de 3–5 dias após o início da primeira administração de Hibor® (bemiparina sódica), e a dose ajustada de modo a manter o valor da Razão Normalizada Internacional (INR), entre 2–3 vezes o valor do controle. A administração de bemiparina pode ser interrompida assim que o valor estabelecido pela INR for atingido. O anticoagulante47 oral deve ser continuado por no mínimo 3 meses.
Em pacientes com trombose venosa profunda5 e fatores de risco transitórios, como alternativa à administração de anticoagulantes59 orais ou em casos de contraindicação de seu uso, Hibor® (bemiparina sódica) poderá ser administrado na dose fixa de 3.500 UI uma vez por dia, por via subcutânea1, pelo período máximo de 3 meses.
Crianças: A segurança e eficácia do uso da bemiparina em crianças não foram estabelecidas, portanto o uso em crianças não é recomendado.
Idosos: O ajuste de dose não é necessário.
Insuficiência Renal68 e Hepática33: Não há dados suficientes de recomendação do ajuste de dose da bemiparina neste grupo de pacientes.
INSTRUÇÕES DE USO
Como faço para injetar Hibor®?
Hibor® nunca deve ser injetado num músculo, pois pode causar hemorragia13.
Antes da primeira aplicação, você receberá instruções sobre a maneira correta de usar esta medicação e a técnica adequada de autoinjeção. Estas instruções devem ser dadas por um médico ou outro profissional de saúde61 devidamente qualificado.
Siga estes passos:
- Lave bem as mãos69 e sente-se ou deite-se em uma posição confortável.
- Escolha uma área da cintura que esteja a pelo menos, cinco centímetros do umbigo70 e de qualquer cicatriz71 ou contusão72, e limpe a pele73 nessa área também.
- Utilize, a cada dia, diferentes locais para a injeção64 (por exemplo, primeiro à esquerda e da próxima vez, à direita).
- Retire a tampa que cobre a agulha da seringa2 de Hibor®.
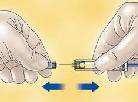
Para manter a agulha estéril, assegure-se de que ela não toque em nada.
- A seringa2 preenchida está pronta para utilização.
- Antes da injeção64, não empurre o êmbolo74 para remover bolhas de ar, pois pode-se perder medicamento. Caso apareça uma gota75 na ponta da agulha, remova-a antes de aplicar o medicamento através de batidas suaves no corpo da seringa2 com a agulha apontada para baixo (para que a bolha76 de ar permaneça na seringa2)
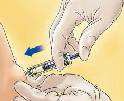
- Segure a seringa2 com uma mão77, e, com a outra, usando o polegar e o dedo indicador, comprima a pele73 na área que foi limpa, formando uma prega.
- Insira toda a agulha na prega da pele73 mantendo a seringa2 o quanto possível na posição vertical sobre a superfície do corpo num ângulo de 90°.
- Empurre o êmbolo74, assegurando-se de que a dobra da pele73 permaneça na mesma posição até que o êmbolo74 esteja completamente abaixado.
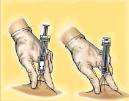
- Retire a seringa2 do local da injeção64, mantendo o dedo sobre a haste do êmbolo74 e a seringa2 na posição vertical. Solte a dobra da pele73.
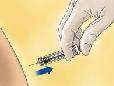
- Para seringas com dispositivo de segurança: aponte a agulha para longe de si e de qualquer pessoa presente, e ative o sistema de segurança, pressionando firmemente a haste do êmbolo74. A capa protetora cobrirá automaticamente a agulha e você ouvirá um clique que confirmará a ativação do protetor.

- Descarte a seringa2 imediatamente, jogando no recipiente para objetos pérfuro-cortantes (com a agulha para dentro). Feche bem o recipiente com tampa e coloque-o fora do alcance das crianças.

Observações:
O sistema de segurança só pode ser ativado uma vez que a seringa2 estiver vazia.
A ativação do sistema de segurança só deve ser feita após a remoção da agulha da pele73 do paciente.
- Não reutilize a capa da agulha após a injeção64.
- Na ativação do sistema de segurança pode espirrar uma quantidade mínima de líquido. Para sua maior proteção, ative o sistema de segurança direcionando-o para baixo e longe de si e de qualquer pessoa presente.
- Não esfregue a pele73 onde a injeção64 foi aplicada. Isso ajudará a evitar hematomas31.
Se perceber qualquer sangramento, informe ao seu médico imediatamente.
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Não tome uma dose dupla para compensar a dose esquecida e consulte o médico, para que seja orientado o que fazer neste caso.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
A bemiparina, como as outras heparinas de baixo peso molecular, está associada a:
Reações adversas muito comuns (≥ 1/10): Hematoma78 e/ou equimose79 no local da injeção64, ocorre em aproximadamente 15% dos pacientes que receberam bemiparina.
Reações comuns (≥ 1/100, < 1/10): Hematoma78 e dor no local da injeção64; Sangramentos complicados (pele73, membranas mucosas80, feridas, TGI, TU); Elevações transitórias e leves das transaminases (SGPT, SGOT) e níveis gama-GT.
Reação incomum (≥ 1/1000, < 1/100): Reações alérgicas cutâneas42 (urticária81, prurido82); Trombocitopenia18 transitória e leve (tipo I).
Reação rara (< 1/1000): Reações anafiláticas83 (náuseas84, vômitos85, febre86, dispneia87, bronco espasmo88, edema89 de glote90, hipotensão91, urticária81, prurido82); Trombocitopenia18 severa (tipo II); Necroses cutâneas42 no local da injeção64; Hematoma78 epidural46 e espinhal seguido de anestesia45 epidural46 ou espinhal punção lombar. Esses hematomas31 têm causado vários graus de prejuízos neurológicos, incluindo paralisia92 prolongada ou permanente.
Em ocasiões muito raras, caso tenha sido tratado com medicamentos anticoagulantes59 e seja submetido a anestesia45 epidural46 ou espinhal, pode ocorrer um sangramento no canal espinhal. Isto pode prejudicar os nervos causando uma perda de força ou de sensibilidade nas pernas ou na metade inferior do corpo.
Caso isto ocorra, consulte imediatamente seu médico.
Osteoporose93 tem sido associada com o tratamento em longo prazo com bemiparina.
ATENÇÃO: Este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe seu médico ou cirurgião dentista.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Em caso de superdose algum tipo de sangramento pode ocorrer, neste caso consulte imediatamente um médico.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
Registro no M.S. sob No: 1.0235.1102
Farm. Resp.: Dr. Ronoel Caza de Dio CRF-SP nº: 19.710
Fabricado e embalado por:
Rovi Contract Manufacturing, S.L. Madrid - Espanha
Registrado, importado e comercializado por:
EMS S/A
Rodovia Jornalista Francisco Aguirre Proença, Km 08 - Chácara Assay
Hortolândia – SP
CEP: 13186–901
CNPJ: 57.507.378/0003–65
Indústria Brasileira
SAC 0800 191914