

Lacrifilm (Bula do profissional de saúde)
UNIÃO QUÍMICA FARMACÊUTICA NACIONAL S/A
IDENTIFICAÇÃO DO PRODUTO
Lacrifilm®
carmelose sódica
Solução oftálmica 5 mg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução oftálmica estéril
Embalagem contendo frasco de 5 mL, 10 mL ou 15 mL
USO ADULTO
USO OFTÁLMICO
COMPOSIÇÃO:
Cada mL (19 gotas) de Lacrifilm contém:
| carmelose sódica | 5,0 mg (0,263 mg/gota1) |
| veículo q.s.p. | 1 mL |
Veículo: cloreto de sódio, fosfato de sódio monobásico, ácido bórico, perborato de sódio, ácido clorídrico2 e água para injetáveis.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE3
INDICAÇÕES
Lacrifilm é indicado para o tratamento da melhora da irritação, ardor4 e secura dos olhos5, que podem ser causadas pela exposição ao vento, sol, calor, ar seco, e também como protetor contra irritações oculares.
É também indicado como lubrificante e re-umidificante durante o uso de lentes de contato para aliviar o ressecamento, irritação, desconforto e coceira.
RESULTADOS DE EFICÁCIA
Os indivíduos com olho6 seco foram incluídos em um estudo de grupos paralelos de 3 meses, randomizado7, para comparar a segurança e eficácia de Refresh OPTIVE, carmelose sódica e Systane.
Não houve diferença estatisticamente significativa entre os três grupos em relação à incidência8 dos eventos adversos relacionados ao tratamento, sendo que nenhum evento foi considerado sério.
No grupo tratado com carmelose sódica, houve melhora estatística e clinicamente significativa observada pelos resultados obtidos no questionário Index da Doença para Superfície Ocular (OSDI), nos sintomas9 de secura ocular, teste de Schirmer, estabilidade do filme lacrimal, manchas na córnea10 e conjuntiva11 e na avaliação do conforto observado nas visitas de acompanhamento.
Os questionários de conforto e aceitabilidade indicaram que carmelose sódica foi aceito pela maioria dos indivíduos do estudo, em todos os aspectos avaliados1.
Referências bibliográficas
- Study AG9689-001: A Multi-Center, Double-Masked, Randomized, Parallel-Group Study to Compare the Efficacy and Safety of an Investigational Multi-Dose Lubricant Eye Drop with Refresh Tears® and Systane® Lubricant Eye Drops for Three Months in Subjects with Dry Eye. Allergan, 2009.
CARACTERÍSTICAS FARMACOLÓGICAS
Lacrifilm contém uma série de substâncias que lhe conferem semelhança com a lágrima natural.
O princípio ativo, a carmelose sódica (carboximetilcelulose sódica ou CMC), combina-se com as próprias lágrimas do paciente para proporcionar melhora imediata da irritação, ardor4 e secura ocular, que podem ser causados por exposição ao vento, sol, calor, ar seco e proporciona maior conforto durante o uso de lentes de contato. O modo de ação do CMC como lubrificante é completamente mecânico para cobrir e proteger a superfície ocular. Não há atividade farmacológica.
Farmacocinética e metabolismo12 clínico
Não foram realizados estudos farmacocinéticos clínicos ou não clínicos. A CMC é farmacologicamente inerte e devido ao seu alto peso molecular, não é esperado que seja absorvida sistemicamente após a administração tópica de Lacrifilm.
CONTRAINDICAÇÕES
Lacrifilm é contraindicado em pacientes com história de hipersensibilidade à carmelose sódica ou a qualquer um dos componentes do medicamento.
ADVERTÊNCIAS E PRECAUÇÕES
Lacrifilm é de uso tópico13 ocular.
Para evitar a contaminação ou possíveis danos ao olho6, orientar o paciente a não tocar com a ponta do frasco nos olhos5, nos dedos e nem em outra superfície qualquer. Fechar bem o frasco depois de usar.
Lacrifilm não deve ser utilizado caso haja sinais14 de violação e/ou danificações do frasco. Não utilizar se ocorrer modificação da coloração da solução ou se a solução se tornar turva.
Em caso de aparecimento de dor, alterações da visão15, ou se ocorrer piora ou persistência da vermelhidão, ou da irritação dos olhos5, descontinuar o tratamento e orientar o paciente a procurar auxílio médico.
Não utilizar medicamento com o prazo de validade vencido.
Gravidez16 e Lactação17
Não há dados sobre o uso de Lacrifilm durante a gravidez16 e lactação17 em humanos. Os estudos animais não apresentaram efeitos nocivos com CMC.
Lacrifilm também não foi estudado em mulheres durante a amamentação18. Contudo, como CMC não é absorvido sistemicamente, não há potencial conhecido para excreção em leite humano.
Categoria de risco na gravidez16: C
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Populações especiais
Pacientes pediátricos: A segurança e a eficácia de Lacrifilm não foram avaliadas em pacientes pediátricos.
Pacientes idosos: Não foram observadas diferenças em relação à segurança e eficácia do medicamento entre pacientes idosos e adultos.
Pacientes que utilizam mais de um medicamento oftálmico: Quando mais de um colírio19 estiver sendo utilizado pelo paciente, deve ser respeitado o intervalo de pelo menos cinco minutos entre a administração dos medicamentos.
Efeitos na habilidade de dirigir e usar máquinas
Se os pacientes apresentarem visão15 borrada transitória, devem ser advertidos a esperar até que a visão15 normalize antes de conduzir ou utilizar máquinas.
INTERAÇÕES MEDICAMENTOSAS
Não são conhecidas interações com outros medicamentos.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Manter o produto em sua embalagem original e conservar em temperatura ambiente (entre 15° e 30°C). O prazo de validade é de 18 meses a partir da data de fabricação (vide cartucho).
Após aberto, válido por 120 dias.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Solução límpida, incolor e transparente.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
A dose usual é de 1 a 2 gotas no(s) olho6(s) afetado(s), tantas vezes quantas forem necessárias.
Como utilizar
- Lave as mãos20 cuidadosamente e seque-as em pano ou papel limpo anteriormente a utilização do medicamento;
- Desenrosque a tampa do medicamento somente antes de sua aplicação.
- Com um dedo limpo puxe a pálpebra inferior para baixo até que se forme uma bolsa entre a pálpebra e o olho6, conforme indicado na figura abaixo.
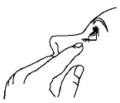
- Segure o frasco, virado para baixo, entre o polegar e os dedos e incline ligeiramente a cabeça21 para trás.
- Não toque o conta-gotas no olho6 ou na pálpebra e não permita que o conta-gotas entre em contato com a face22, dedos ou qualquer outra superfície para evitar sua contaminação.
- Pressione levemente a base do frasco para administrar a gota1 na bolsa formada entre a pálpebra e o olho6, conforme indicado na figura abaixo.
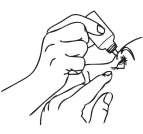
- Utilize um espelho para auxiliá-lo durante o gotejamento caso seja necessário.
- Após administrar o medicamento, pressione leve e cuidadosamente o canto inferior do olho6 para impedir que o medicamento se espalhe para outras regiões da face22, conforme indicado na figura abaixo.
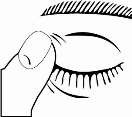
- Se necessitar utilizar as gotas em ambos os olhos5, repita os passos descritos para o outro olho6.
- Feche bem o frasco imediatamente após a utilização.
REAÇÕES ADVERSAS
As reações adversas observadas nos estudos clínicos realizados com carmelose sódica, por ordem de frequência foram:
Reação comum (> 1/100 e < 1/10): irritação, queimação e desconforto ocular, distúrbios visuais.
Reação incomum (> 1/1.000 e 1/100): secreção nos olhos5, dor nos olhos5, prurido23 ocular e hiperemia24 palpebral.
Pós-comercialização: Outras reações adversas relatadas após a comercialização de carmelose sódica foram: sensação de corpo estranho nos olhos5, hiperemia24 ocular, hipersensibilidade incluindo alergia25 ocular com sintomas9 de inchaço26 dos olhos5, edema27 ou eritema28 da pálpebra.
Em casos de eventos adversos, notifique ao Sistema de Notificação de Eventos Adversos a Medicamentos – VIGIMED, ou para a Vigilância Sanitária Estadual ou Municipal.
SUPERDOSE
Não há relatos de superdose. A carmelose sódica é farmacologicamente inerte e não deve ser absorvida sistemicamente, portanto não causa problemas oculares ou sistêmicos29 mesmo quando aplicado em doses excessivas, não havendo condutas especiais nesses casos.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
Siga corretamente o modo de usar, não desaparecendo os sintomas9 procure orientação médica.
Registro MS - 1.0497.1289
Farm. Resp.: Florentino de Jesus Krencas CRF-SP: 49136
UNIÃO QUÍMICA FARMACÊUTICA NACIONAL S/A
Rua Cel. Luiz Tenório de Brito, 90
Embu-Guaçu – SP – CEP: 06900-000
CNPJ: 60.665.981/0001-18
Indústria Brasileira
Fabricado na unidade fabril:
Av. Pref. Olavo Gomes de Oliveira, 4.550 Bairro São Cristovão
Pouso Alegre – MG – CEP: 37550-000 CNPJ 60.665.981/0005-41
Indústria Brasileira
SAC 0800 11 1559






