

Tensuril (Bula do profissional de saúde)
CRISTÁLIA PRODUTOS QUÍMICOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Tensuril
diazóxido
Injetável 15 mg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução injetável
Cartucho com 1 ampola de 20 mL
USO INTRAVENOSO
USO ADULTO E PEDIÁTRICO
COMPOSIÇÃO:
Cada mL de Tensuril contém:
| diazóxido | 15 mg |
| veículo q.s.p. | 1 mL |
Veículo estéril: propilenoglicol, hidróxido de sódio e água para injetáveis.
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE1
INDICAÇÕES
Tensuril é uma solução injetável para uso exclusivo intravenoso indicado para o uso por curto prazo na redução emergencial da pressão arterial2 na hipertensão3 grave, não maligna e maligna, de pacientes adultos hospitalizados; na hipertensão3 aguda grave de crianças hospitalizadas e que necessitam de rápida e urgente diminuição da pressão diastólica4.
O tratamento com agentes anti-hipertensivos orais somente deve ser instituído após a estabilização da pressão arterial2. O uso de Tensuril por mais de 10 dias não é recomendado.
O Tensuril injetável não é eficaz contra a hipertensão3 devida ao feocromocitoma5.
RESULTADOS DE EFICÁCIA
O’Brien, em 1975, publicou um estudo avaliando o efeito do diazóxido intravenoso no tratamento da hipertensão3 associada com infarto do miocárdio6 recente. Vinte pacientes (20) com pressão arterial2 acima de 180/110 mmHg, uma hora após a admissão em uma unidade coronariana e com infarto7 agudo8 do miocárdio9 recente, receberam diazóxido intravenoso em bolus10 de 300 mg. A pressão arterial2 caiu consideravelmente em todos os pacientes, sendo que seis pacientes necessitaram repetir as injeções. A queda média foi de 58 mmHg na sistólica e 40 mmHg na diastólica. Nenhum paciente ficou gravemente hipotenso.
- O'Brien KP, Grigor RR, Taylor PM. Intravenous diazoxide in treatment of hypertension associated with recent myocardial infarction. Br Med J. 1975 Oct 11;4(5988):74–7.
Pohl, em 1971, avaliou a terapia anti-hipertensiva com diazóxido em paciente hipertensos graves e resistentes. O tratamento com diazóxido intravenoso e oral foi administrado a um grupo de 39 pacientes com hipertensão3 grave, associada à insuficiência renal11 e resistente à medicamentos. O controle da hipertensão3, rápido e de longo prazo foi atingido em todos os casos, sem a produção de hipotensão12 postural clinicamente significativa.
- Pohl JE, Thurston H. Use of diazoxide in hypertension with renal13 failure. Med J. 1971 Oct 16;4(5780):142–5.
Ogilvie estudou a relação concentração-resposta do diazóxido no tratamento da hipertensão3 com relação a farmacocinética e da resposta anti-hipertensiva de doses em bolus10 de diazóxido de 1 , 2 ou 4 mg/kg durante 5, 10 ou 20 segundos. Foram examinados sete pacientes com hipertensão3 essencial estável crônica e as médias de pressão arterial2 média (PAM) entre 122 e 155 milímetros Hg. As curvas de concentração-tempo individuais foram analisados para determinar o volume aparente de distribuição no steady-state, (Vdss, 178-,250 L/kg) , t 1/2 beta (32–62,5 horas), e a taxa de depuração plasmática (Clp, 2,2–5,3 ml/kg.hora-1) para o cálculo14 da dose de manutenção e doses destinadas a produzir concentrações de steady state a 0,5 horas. Com o uso de princípios cinéticos, o diazóxido produziu reduções graduais e previsíveis da PAM em pacientes com hipertensão3 acelerada, uma vez que a resposta era proporcional à concentração plasmática de diazóxido.
- Ogilvie RI, Nadeau JH, Sitar DS. Diazoxide concentration-response relation in hypertension. Hypertension. 1982 Jan-Feb;4(1):167–73.
CARACTERÍSTICAS FARMACOLÓGICAS
Diazóxido é um derivado benzotiadiazínico anti-hipertensivo, quimicamente semelhante aos diuréticos15 tiazídicos, porém sem atividade diurética.
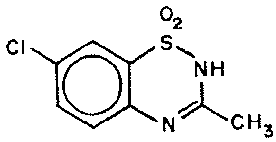
Estrutura do Diazoxido e de um diuretico16 benzotiadizÍdico.
Diazóxido é um ativador de canais de potássio, o que provoca o relaxamento do músculo liso17, aumentando a permeabilidade18 da membrana aos ions19 potássio, que desativa a ligação aos canais de cálcio e inibe a geração de um potencial de ação.
É um potente agente antihipertensivo de ação rápida. Liga-se extensamente a àlbumina sérica e aos tecidos vasculares20.
Diazóxido é metabolizado por conjugação oxidativa e sulfídica, sendo excretado lentamente na urina21 por filtração glomerular de 4 a 5 mL/min ou 10 a 90%, sendo excretado como diazóxido ou metabólitos22 através dos rins23. Diazóxido é parcialmente metabolizado no fígado24, sendo que apenas pequenas quantidades são excretadas nas fezes.
O medicamento atravessa a placenta e a barreira hematoencefálica.
A meia vida do diazóxido no plasma25 é de aproximadamente de 21–48 horas em adultos com função renal13 normal. Porém, valores de até 60 horas foram relatados. Seu longo tempo de meia vida é devido ao fato de 90% do fármaco26 ligar-se à albumina27.
Em crianças a meia vida pode ser menor do que em adultos. Em crianças de 4 meses a 6 anos, a meia-vida plasmática variou 9,5–24 horas após administração oral de longo prazo.
A meia-vida é prolongada na insuficiência renal11, pois a ligação de diazoxido às proteínas28 séricas é diminuída. Neste caso a meia-vida sérica aumenta com a diminuição do clearance de creatinina29. Pacientes com insuficiência renal11 geralmente requerem doses usuais de diazóxido.
A meia-vida no soro30 é pelo menos três vezes maior do que a sua ação hipotensora. Quando administrada em intervalos de 4 a 12 horas, a droga se acumula extensivamente no corpo. Não há nenhuma correlação entre a concentração de diazóxido no soro30, na fase pós-distribuição e a intensidade da ação hipotensiva, porque este último depende da concentração inicial de droga livre nos vasos.
Diazóxido pode ser removido do corpo por diálise peritoneal31 ou hemodiálise32, porém, em quantidade relativamente baixa, devido a grande ligação à albumina27 sérica.
A duração da ação após uso intravenoso ocorre dentro de cinco minutos e persiste por 4–12 horas. A eliminação do fármaco26 ocorre entre 20–36 horas.
Farmacologia33 Clínica
O diazóxido reduz rapidamente a pressão arterial2 no homem, por relaxamento da musculatura lisa da arteríola34 periférica. O débito cardíaco35 é aumentado e a pressão arterial2 é diminuída.
Os estudos em animais demonstram que o fluxo sanguíneo das coronárias é mantido, enquanto que o fluxo sanguíneo renal13 é aumentado após diminuição inicial.
Pode ocorrer hiperglicemia36 transitória na maioria dos pacientes tratados com Tensuril, que normalmente somente requer tratamento nos pacientes com diabetes mellitus37. A hiperglicemia36 deve responder às medidas de tratamento usuais, incluindo a insulina38.
A glicemia39 deve ser monitorizada, especialmente nos pacientes com diabetes40 e naqueles que necessitam de injeções múltiplas de diazóxido. Em alguns animais que receberam doses diárias repetidas de diazóxido intravenoso, observou-se a formação de catarata41.
O diazóxido causa retenção de sódio, e as injeções repetidas do produto podem precipitar edema42 e insuficiência cardíaca congestiva43. O volume aumentado do fluido extracelular pode ser a causa da falha do tratamento em pacientes não-responsivos. O aumento no volume do fluido responde caracteristicamente aos agentes diuréticos15, se existir função renal13 adequada. A administração concomitante de diuréticos15 tiazídicos pode potencializar as ações anti-hipertensiva e hiperuricêmica do diazóxido.
O diazóxido liga-se extensamente às proteínas28 séricas (> 90%). A meia-vida plasmática é de 28 ± 8,3 horas; contudo, a duração do seu efeito anti-hipertensivo é variável, permanecendo por não menos de 12 horas.
CONTRAINDICAÇÕES
O Tensuril (diazóxido) não deve ser usado no tratamento da hipertensão3 compensatória, tal como aquela associada com a coarctação da aorta44 ou fístulas45 arteriovenosas.
Também não deve ser usado por pacientes que apresentem hipersensibilidade ao diazóxido, outras tiazidas, outros fármacos derivados sulfonamídicos ou a qualquer um dos componentes da fórmula.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
ADVERTÊNCIAS E PRECAUÇÕES
ADVERTÊNCIAS
Diminuição Rápida da Pressão Arterial2
Deve-se tomar cuidado quando da redução acentuada da pressão arterial2. O diazóxido somente deve ser administrado utilizando-se a dose em minibolus de 150 mg. O uso da dose intravenosa de 300 mg tem sido associada com angina46 e com infarto do miocárdio6 e cerebral. Foi relatado um caso de infarto7 do nervo óptico quando ocorreu uma redução de 100 mmHg na pressão diastólica4, após 10 minutos de uma dose única de 300 mg em bolus10. Em um ensaio prospectivo47 conduzido em pacientes com hipertensão3 grave e doença coronariana48 arterial coexistente, foi observada, após uma dose única de 300 mg de diazóxido em bolus10, uma incidência49 de 50% de alterações isquêmicas no eletrocardiograma50. Portanto, a redução desejada da pressão arterial2 deve ser conseguida no período de tempo compatível com o estado do paciente. Recomenda-se, no mínimo algumas horas e preferencialmente um a dois dias.
Uma maior segurança com igual eficácia pode ser conseguida administrando-se o Tensuril em minibolus (1 a 3 mg/kg, a cada 15 minutos, até o máximo de 150 mg em injeção51 única) até que a pressão arterial diastólica52 esteja abaixo de 100 mmHg. O produto não deve ser administrado em bolus10 de 300 mg pois, este modo de administração é menos previsível e controlável do que a dosagem por minibolus. Se ocorrer hipotensão12 grave, resultante da redução na pressão arterial2 que necessite de terapia, normalmente a mesma responde à manobra Trendelenberg. Se necessário, podem ser administrados agentes simpatomiméticos como a dopamina53 ou a norepinefrina.
Deve-se ter especial atenção com os pacientes com diabetes mellitus37 e com aqueles nos quais a retenção de sal e água pode representar sérios problemas.
Lesões54 do Miocárdio9 em Animais
A administração intravenosa de diazóxido em cães induziu a necrose55 subendocárdica e necrose55 dos músculos papilares56. Essas lesões54, que também são produzidas por outras drogas vasodilatadoras (como a hidralazina, minoxidil) e por catecolaminas, presumivelmente estão relacionadas à anoxia57 resultante da combinação da taquicardia58 reflexa e de perfusão diminuída.
PRECAUÇÕES:
Gerais: o Tensuril injetável é um agente anti-hipertensivo eficaz, que necessita de monitorização constante da pressão arterial2 do paciente, em intervalos frequentes. Sua administração pode causar ocasionalmente hipotensão12, necessitando dessa forma tratamento com agentes simpatomiméticos.
Dessa forma, o produto deve ser usado primariamente em hospitais ou em locais com instalações adequadas para o tratamento dessas respostas adversas. O produto somente deve ser administrado em veia periférica. Deve-se evitar a injeção51 extravascular59 ou vazamento, devido à alcalinidade da solução, que é irritante aos tecidos. Se ocorrer vazamento no tecido subcutâneo60, a área deve ser tratada com compressas quentes e repouso.
O Tensuril deve ser usado com cuidado em pacientes com alterações na circulação61 cerebral ou cardíaca, isto é, naqueles em que a redução abrupta na pressão arterial2 pode ser um fator agravante ou naqueles em que a taquicardia58 leve ou perfusão sanguínea diminuída pode ser deletória. A hipotensão12 prolongada deve ser evitada para não agravar eventual insuficiência renal11 preexistente.
Durante e imediatamente após a injeção51 intravenosa de Tensuril, o paciente deve permanecer na posição supina.
Testes Laboratoriais: Os testes diagnósticos laboratoriais necessários para o estabelecimento da condição e do estado do paciente deve ser realizado antes do tratamento com o produto. Durante e após o tratamento com o Tensuril, devem ser realizados testes laboratoriais para monitorizar os efeitos do tratamento com esta droga e as condições do paciente. Entre os testes (não necessariamente todos) estão: hematológico (hematócrito62, hemoglobina63, leucócito e contagem de plaquetas64); metabólico (glicose65, ácido úrico, proteína total, albumina27); eletrólito66 (sódio, potássio) e osmolalidade67; função renal13 (creatinina29, proteinúria68); eletrocardiograma50.
Carcinogênese, Mutagênese, Diminuição da Fertilidade: Não foram feitos estudos de longa duração em animais, com diferentes doses, para avaliar o potencial carcinogênico do diazóxido. Não foram feitos estudos laboratoriais do potencial mutagênico ou estudos em animais sobre os efeitos na fertilidade.
Gravidez69 e Lactação70
Categoria C – Não há estudos adequados em mulheres. Em experiências animais ocorreram alguns efeitos colaterais71 no feto72, mas o benefício do produto pode justificar o risco potencial durante a gravidez69.
O diazóxido mostrou reduzir a sobrevivência73 fetal e/ou do embrião; também, reduz o crescimento fetal de ratos, coelhos e cães nas doses diárias de 30, 21 ou 10 mg/kg, respectivamente. Em ratos tratados a termo, o diazóxido, em doses de 10 mg/kg e acima, prolongam o parto. A segurança do produto na gravidez69 não foi estabelecida. O produto não deve ser usado durante a gravidez69. A administração durante o parto pode causar interrupção da contração uterina, necessitando da administração de agente ocitócico.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Não se tem conhecimento se ocorre a passagem do diazóxido para o leite materno. Devido ao fato que muitos fármacos são excretados no leite materno e devido ao potencial para a ocorrência de reações adversas com o diazóxido em crianças que estejam em fase de amamentação74, deve-se tomar uma decisão sobre a descontinuidade da amamentação74 ou da droga, levando-se em consideração a importância do fármaco26 para a mãe.
O diazóxido atravessa a barreira placentária e aparece no cordão umbilical75. Quando administrado à parturiente, o fármaco26 pode produzir no feto72 ou no recém-nascido: hiperbilirrubinemia, trombocitopenia76, metabolismo77 alterado dos carboidratos e possivelmente outros efeitos colaterais71 que ocorrem em adultos.
INTERAÇÕES MEDICAMENTOSAS
O diazóxido é fortemente ligado às proteínas28 plasmáticas. Pode ser que desloque outras substâncias também altamente ligadas à proteína, como a bilirrubina78, cumarina e seus derivados, resultando em níveis sanguíneos mais altos das mesmas.
Pode ocorrer hipotensão12 indesejável quando o diazóxido é administrado a pacientes que receberam outra medicação anti-hipertensiva dentro de seis horas.
Em um estudo clínico, um paciente apresentou hipotensão12 acentuada após administração concomitante de diazóxido com hidralazina e metildopa. Um episódio de hipotensão12 materna e bradicardia79 fetal ocorreu em uma parturiente que recebeu reserpina e hidralazina antes da administração do diazóxido. Também existe relato de hiperglicemia36 neonatal após administração intraparto de diazóxido.
O Tensuril não deve ser administrado dentro de seis horas da administração de: hidralazina, reserpina, alfaprodina, metildopa, betabloqueadores, prazosina, minoxidil, nitritos e outros compostos tipo papaverina. A administração concomitante com tiazidas ou outros diuréticos15 comumente usados pode potencializar os efeitos hiperuricêmicos e anti-hipertensivos do diazóxido.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Tensuril deve ser conservado em temperatura ambiente (15–30°C), protegido da luz. O prazo de validade do medicamento a partir da data de fabricação é de 24 meses.
O medicamento deverá ser armazenado em sua embalagem secundária até o momento do uso. Em caso de necessidade, o produto, em sua embalagem primária, poderá ficar exposto à iluminação em ambientes fechados por um período de até 30 dias.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use o medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Solução incolor a levemente amarelada, límpida, essencialmente livre de partículas visíveis.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
O Tensuril foi inicialmente recomendado para ser administrado em bolus10 de 300 mg. Os estudos recentes demonstraram que a administração em minibolus, isto é, doses de 1 a 3 mg/kg, repetidas em intervalos de 5 a 15 minutos são igualmente eficazes na redução da pressão arterial2. A administração em minibolus geralmente provoca uma redução mais gradual na pressão arterial2 e dessa forma, espera-se que reduza os riscos circulatórios e neurológicos associados com a hipotensão12 aguda.
O Tensuril é administrado sem diluição, rapidamente, por via intravenosa, na concentração de 1 a 3 mg/kg até o máximo de 150 mg, em dose única. A dose pode ser repetida em intervalos de 5 a 15 minutos até que redução satisfatória na pressão arterial2 seja atingida (pressão diastólica4 abaixo de 100 mmHg).
Com o paciente deitado, a dose calculada de Tensuril injetável é administrada intravenosamente em 30 segundos ou menos.
O Tensuril somente deve ser aplicado em veia periférica. Não deve ser injetado por via intramuscular, subcutânea80 ou em cavidades do corpo. Deve ser evitado o extravasamento do fármaco26 para os tecidos subcutâneos.
Após o uso de Tensuril, a pressão arterial2 deve ser monitorizada cuidadosamente até a estabilização. Em seguida, medidas devem ser feitas de hora em hora, durante a fase de equilíbrio, até que não se obtenha qualquer resposta não esperada. Uma diminuição na pressão arterial2 após 30 minutos ou mais após a injeção51 deve ser investigada, por motivos outros que a ação do Tensuril.
É preferível manter o paciente na posição supina por no mínimo uma hora após a injeção51. Em pacientes ambulatoriais, a pressão arterial2 deve também ser medida com o paciente em pé, antes do término da monitorização.
A administração repetida de Tensuril em intervalos de 2 a 24 horas, normalmente manterá a pressão arterial2 abaixo dos níveis de pré-tratamento, até que possa ser instituído um regime com anti-hipertensivos orais. O intervalo entre as injeções pode ser ajustado pela duração da resposta a cada injeção51. Usualmente não é necessário continuar o tratamento com Tensuril por mais de 4 a 5 dias.
Pelo fato da administração repetida de Tensuril poder levar à retenção de sódio e água, pode ser necessário a administração de um diurético16 para a redução da pressão arterial2 máxima e para prevenir a insuficiência81 congestiva.
Posologia
Pacientes idosos: Inexistem informações sobre a relação entre idade e os efeitos do diazóxido parenteral nos pacientes geriátricos. Contudo, os pacientes idosos estão mais sujeitos à insuficiência renal11 relacionada à idade, necessitando da redução da dose de diazóxido injetável.
REAÇÕES ADVERSAS
As reações podem ser classificadas em:
|
Categoria |
Frequência |
|
Muito comum |
≥ 10% |
|
Comum |
≥ 1% e < 10% |
|
Incomum |
≥ 0,1% e < 1% |
|
Raro |
≥ 0,01% e < 0,1% |
|
Muito raro |
< 0,01% |
|
Desconhecida |
Não pode ser estimada pelos dados disponíveis |
Existe razão para se pensar que a substituição da dose de 300 mg em bolus10 pelo minibolus, na clínica prática, resulta em reações adversas similares em características mas, de menor frequência e gravidade.
Na experiência clínica com a administração rápida de 300 mg em bolus10, as reações adversas: Comuns (>1% e <10%): hipotensão12 (7%); náusea82 e vômito83 (4%); tontura84 e fraqueza (2%).
Reações adversas adicionais relatadas com frequência não conhecida, com a dose de 300 mg em bolus10:
Cardiovascular: ocorre retenção de sódio e água após injeção51 rápida, especialmente em pacientes com reserva cardíaca diminuída; hipotensão12 grave (choque85); isquemia86 miocárdica, usualmente transitória e manifestada por angina46, arritmias87 atrial e ventricular, e mudanças eletrocardiográficas acentuadas, levando ocasionalmente ao infarto do miocárdio6; infarto7 do nervo óptico, seguido de diminuição muito rápida da hipertensão3 grave; taquicardia58 supraventricular e palpitação88; bradicardia79; desconforto no tórax89 ou pressão torácica não relacionada com angina46 pectoris.
Sistema Nervoso Central90: isquemia86 cerebral, normalmente transitória mas ocasionalmente levando ao infarto7 e manifestada por inconsciência91, convulsões, paralisia92, confusão ou déficit neurológico focal como dormência93 das mãos94; fenômenos de vasodilatação, como hipotensão12 ortostática, sudorese95, rubor facial e sensações de calor localizadas ou generalizadas. Também, outras várias reações neurológicas transitórias secundárias à alteração no fluxo sanguíneo regional para o cérebro96, como a cefaleia97 (às vezes com pulsação), tontura84, indiferença, sonolência (também citada como letargia98), euforia ou “sensação de alegria”, zumbido e perda momentânea da audição, e fraqueza de curta duração; apreensão ou ansiedade.
Gastrintestinal: raramente, pancreatite99 aguda; náusea82, vômito83 e/ou desconforto abdominal; anorexia100; alteração no paladar101; inchaço102 da parótida103; salivação; boca104 seca; íleo105; obstipação106 e diarreia107.
Outras: hiperglicemia36 em pacientes diabéticos, especialmente após injeções repetidas; coma108 hiperosmolar109 em crianças; hiperglicemia36 transitória em pacientes não-diabéticos; retenção transitória de metabólitos22 nitrogenados, reações respiratórias secundárias ao relaxamento da musculatura lisa, como dispneia110, tosse e sensação de asfixia111; calor ou dor na veia injetada; celulite112 sem descamação113 e/ou flebite114 no local de extravasamento; dor nas costas115 e nictúria116; reações de hipersensibilidade, tais como rash117 cutâneo118, leucopenia119 e febre120; papiledema induzido pela expansão do volume plasmático secundária à administração do diazóxido, citada em um paciente que recebeu onze injeções (300 mg/dose) por 22 dias; mal-estar e visão121 turva; catarata41 transitória em uma criança; hirsutismo122 e libido123 diminuída.
Alterações de exames laboratoriais:
Os efeitos hiperglicêmicos e hiperuricêmicos do diazóxido impedem a avaliação adequada destes estados metabólicos. Notou-se aumento da secreção de renina, concentrações de IgG e diminuição da secreção de cortisol. O diazóxido inibe a liberação da insulina38 estimulada pelo glucagon124 e causa uma resposta falso- negativa de insulina38 para o glucagon124. No rato, cão e macaco, o diazóxido aumenta os ácidos graxos livres séricos e diminui os níveis de insulina38 plasmática.
Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
A superdosagem de Tensuril pode causar hipotensão12 indesejável. Isto pode ser controlado com a manobra de Trendelenberg. Se necessário, podem ser administrados agentes simpatomiméticos como a dopamina53 ou a norepinefrina. A falha no aumento da pressão arterial2 em resposta a tais agentes sugere que a hipotensão12 pode ter sido causada por outro motivo que não o diazóxido. A excessiva hiperglicemia36 resultante da superdosagem responderá à terapia convencional125 da hiperglicemia36.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS N.º 1.0298.0041
Farm. Resp.: José Carlos Módolo - CRF-SP Nº 10.446
Registrado por:
CRISTÁLIA - Produtos Químicos Farmacêuticos Ltda.
Rodovia Itapira-Lindóia, km 14 - Itapira - SP
CNPJ nº 44.734.671/0001-51
Indústria Brasileira
Fabricado por:
CRISTÁLIA - Produtos Químicos Farmacêuticos Ltda.
Av. Nossa Senhora da Assunção, 574 - Butantã - São Paulo - SP
CNPJ nº 44.734.671/0008-28
Indústria Brasileira
SAC 0800 7011918






