
INDICAÇÕES DEPAKOTE ER
Transtorno Afetivo Bipolar (TAB): DEPAKOTE ER (divalproato de sódio) é destinado para o
tratamento de episódios agudos de mania ou episódios mistos associados com transtornos afetivos bipolares, com ou sem características psicóticas.
Um episódio de mania é um período distinto de humor anormalmente e persistentemente elevado, expansivo ou irritável. Os sintomas1 típicos de mania incluem taquilalia, hiperatividade motora, redução da necessidade de dormir, fuga de ideias, grandiosidade, prejuízo da crítica, agressividade e possível hostilidade. Um episódio misto é caracterizado pela presença simultânea de critérios diagnósticos para um episódio de mania e para um episódio depressivo (humor deprimido, perda do interesse ou prazer em quase todas as atividades).
A eficácia do divalproato de sódio de liberação prolongada foi baseada parcialmente em estudos de divalproato de sódio de liberação lenta para essa indicação e foi estabelecida em estudos de três semanas com pacientes que se enquadravam nos critérios da DSM-IV TR para transtorno afetivo bipolar I, tipo mania ou tipo misto, que foram hospitalizados com diagnóstico2 de mania aguda.
A eficácia de divalproato de sódio de liberação prolongada durante uso prolongado em mania, isto é, mais do que três semanas, não foram sistematicamente avaliadas nos estudos clínicos controlados. Portanto, os médicos que optam pelo uso de divalproato de sódio por períodos extensos deverão reavaliar continuamente a utilidade a longo prazo do medicamento para cada paciente.
Epilepsia3: DEPAKOTE ER (divalproato de sódio) é destinado como monoterápico ou como terapia adjuvante ao tratamento de pacientes adultos e crianças acima de 10 anos com crises parciais complexas, que ocorrem tanto de forma isolada ou em associação com outros tipos de crises.
DEPAKOTE ER também é destinado como monoterápico ou como terapia adjuvante no tratamento de quadros de ausência simples e complexa.
Ausência simples é definida como breve obscurecimento sensorial ou perda de consciência, acompanhada de certo número de descargas epilépticas generalizadas, sem outros sinais4 clínicos detectáveis. A ausência complexa é a expressão utilizada quando outros sinais4 também estão presentes.
Profilaxia da Migrânea5 (Enxaqueca6): DEPAKOTE ER (divalproato de sódio) é destinado na profilaxia de enxaquecas7 em adultos. Não existe evidência de que o divalproato de sódio de liberação prolongada seja útil no tratamento agudo8 da enxaqueca6. Uma vez que o ácido valproico pode ser perigoso para o feto9, divalproato de sódio de liberação prolongada não deve ser considerado para mulheres em idade fértil a não ser que o medicamento seja essencial para o gerenciamento da sua condição médica.
DEPAKOTE ER (divalproato de sódio) é contraindicado para o uso na profilaxia de enxaquecas7 por mulheres grávidas.
- 2. RESULTADOS DE EFICÁCIA
Transtorno Afetivo Bipolar
A eficácia de divalproato de sódio de liberação prolongada para o tratamento de mania aguda foi demonstrada em um estudo multicêntrico, randomizado10, duplo-cego, controlado por placebo11 e por grupo paralelo de 3 semanas. O estudo foi elaborado para avaliar a segurança e eficácia de divalproato de sódio no tratamento do transtorno bipolar I, tipo mania ou tipo misto, em adultos.
O estudo incluiu pacientes (homens e mulheres) adultos que preencheram os critérios do DSM-IVTR para transtorno bipolar I, tipo mania ou tipo misto e que foram hospitalizados por mania aguda.
O divalproato de sódio de liberação prolongada foi iniciado com doses de 25mg/kg/dia, administrados uma vez ao dia, aumentado para 500 mg/dia no dia 3, e então ajustado para atingir concentrações séricas de valproato em um intervalo de 85 a 125 mcg/ml. As doses médias de divalproato de sódio para os que completaram este estudo foram 2362 mg (variação: 500-4000), 2874 mg (variação: 1500-4500), 2993 mg (variação: 1500-4500), 3181 mg (variação: 1500-5000), and 3353 mg (variação: 1500-5500) nos dias 1, 5, 10, 15 e 21, respectivamente. A média da concentração de valproato foi de 96,5 µg/ml, 102,1 µg/ml, 98,5 µg/ml, 89,5 µg/ml nos dias 5, 10, 15 e 21, respectivamente. Os pacientes foram avaliados pela escala de Mania (Mania Rating Scale MRS; pontuação varia de 0-52).
O divalproato de sódio de liberação prolongada foi estatisticamente superior ao placebo11 na redução da pontuação total de MRS.
Epilepsia3
Crises Parciais Complexas (CPC)
A eficácia do divalproato de sódio na redução da incidência12 de crises parciais complexas (CPC)
que ocorrem de forma isolada ou em associação com outros tipos de crises foi estabelecida em dois ensaios controlados usando divalproato de sódio comprimidos revestidos.
Em um estudo multiclínico, placebo11-controlado, empregado como terapia adjuvante, 144 pacientes que apresentaram oito ou mais CPCs durante oito semanas, por um período de oito semanas de monoterapia com doses de fenitoína ou carbamazepina suficientes para assegurar as concentrações plasmáticas no "intervalo terapêutico", foram randomizados para receber, em adição às suas medicações antiepiléticas originais, divalproato de sódio ou placebo11.
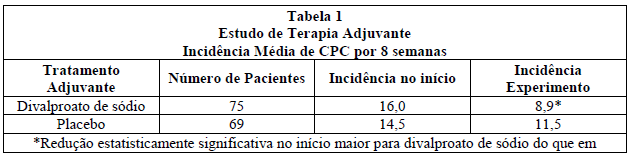
Pacientes foram escolhidos ao acaso para prosseguir os estudos para um total de 16 semanas. A Tabela 1 descreve os achados.
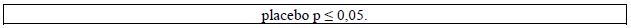
A Figura 1 apresenta a proporção de pacientes (eixo X) cuja porcentagem de redução das taxas de crises parciais complexas no início foi pelo menos tão elevada quanto a indicada no eixo Y no estudo de tratamento adjuvante. Uma redução percentual positiva indica uma melhora (ou seja, redução na frequência das crises), enquanto que uma redução percentual negativa indica uma piora.
Deste modo, em uma exposição deste tipo, a curva que demonstra um tratamento efetivo é deslocada para a esquerda da curva do placebo11. O resultado demonstrou que a proporção de pacientes que atingiram um determinado nível de melhoria com divalproato de sódio foi consistentemente maior do que os pacientes que usaram placebo11. Por exemplo, 45% dos pacientes tratados com divalproato de sódio tiveram uma redução na taxa de CPCs maior ou igual a 50%, comparado a 23% de melhoria para os pacientes que usaram placebo11.
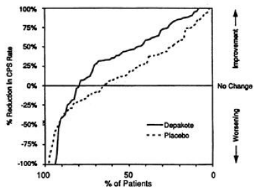
Figura 1
O segundo estudo avaliou a capacidade do divalproato de sódio em reduzir a incidência12 de CPCs como monoterapia antiepilética. O estudo comparou a incidência12 de CPCs entre os pacientes randomizados para receber altas ou baixas doses de tratamento. Os pacientes foram selecionados para participarem dos estudos somente se:
1) apresentassem duas ou mais CPCs por quarto semanas, durante um período de oito a doze semanas de monoterapia com doses adequadas de antiepiléticos (fenitoína, carbamazepina, fenobarbital, primidona); e 2) pacientes que passaram por uma transição de duas semanas bem sucedida para divalproato de sódio.
Os pacientes foram então submetidos à ingestão das doses determinadas, com diminuição gradual da medicação antiepilética concomitante, por um período de 22 semanas. Porém, menos de 50% dos pacientes finalizaram os estudos. Nos pacientes convertidos à monoterapia com divalproato de sódio, a média total das concentrações de valproato durante a monoterapia foram de 71 e 123 mcg/ml para a dose baixa e dose alta, respectivamente. A Tabela 2 apresenta os achados para todos os pacientes randomizados que passaram por pelo menos uma avaliação pós-randomização.

A Figura 2 apresenta a proporção de pacientes (eixo X) cuja porcentagem de redução nas taxas de crises parciais complexas no início foi pelo menos tão elevada quanto a indicada no eixo Y do estudo monoterápico. Uma redução percentual positiva indica uma melhora (ou seja, redução na frequência das crises), enquanto que uma redução percentual negativa indica uma piora. Deste modo, em uma exposição deste tipo, a curva que demonstra um tratamento mais efetivo é deslocada para a esquerda da curva que demonstra um tratamento menos efetivo.
Os resultados mostraram que a redução na incidência12 de CPCs foi significantemente maior quando administrada altas doses de divalproato de sódio. Por exemplo, quando da alteração da monoterapia de carbamazepina, fenitoína, fenobarbital ou primidona para administração de doses elevadas de divalproato de sódio como monoterapia, 63% dos pacientes sofreram nenhuma alteração ou uma redução de taxas de epilepsia3 parcial complexa, em comparação com 54% dos pacientes que receberam doses mais baixas de divalproato de sódio.
Figura 2
Migrânea5
Os resultados de um estudo clínico multicêntrico, randomizado10, duplo-cego e placebo11-controlado, demonstraram a eficácia do divalproato de sódio comprimidos revestidos na profilaxia da enxaqueca6. Deste estudo, participaram pacientes com histórico de crises de enxaqueca6, com ou sem aura que ocorreram duas vezes ou mais por mês pelos últimos três meses. Pacientes com cefaleia13 em crises ou dor de cabeça14 crônica diária foram excluídos dos estudos. Mulheres em idade fértil foram incluídas no estudo, desde que comprovassem o uso de um método contraceptivo eficaz.
Os pacientes que sofreram duas ou mais enxaquecas7 no período basal de quatro semanas foram escolhidos ao acaso para a administração de divalproato de sódio ou de placebo11, na proporção 1:1 e tratados pelo período de doze semanas. Os pacientes iniciaram o tratamento com uma dose de 500 mg uma vez ao dia durante uma semana, que depois foi aumentada para 1000 mg uma vez ao dia, com a opção de diminuir a dose definitivamente para 500 mg uma vez ao dia durante a segunda semana de tratamento, caso ocorresse intolerância à medicação. Noventa e oito dos 114 pacientes tratados com divalproato (86%) e 100 dos 110 pacientes tratados com placebo11 (91%), por pelo menos duas semanas, mantiveram a dose de 1000 mg uma vez ao dia durante o período do tratamento. O resultado do tratamento foi avaliado com base na redução da enxaqueca6 após quatro semanas de tratamento, em comparação com o período inicial.
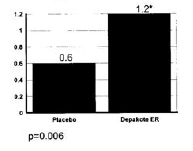
Pacientes (50 H e 187 M) com idade variando de 16 a 69 foram tratados com divalproato sódio de liberação prolongada (n = 122) ou placebo11 (n = 115). Quatro pacientes estavam abaixo dos 18 anos e três acima dos 65 anos de idade. Duzentos e dois pacientes (101 de cada grupo de tratamento) completaram o período de tratamento. A taxa de redução média de enxaqueca6, em quatro semanas de tratamento, foi de 1,2 a partir de uma base média de 4,4 com uso de divalproato de sódio de liberação prolongada, versus 0,6 a partir de uma base média de 4,2 com uso de placebo11. A diferença entre a eficácia dos tratamentos foi estatisticamente significante (veja a figura 3).
Figura 3
Taxa de redução média de enxaqueca6, em quatro semanas de tratamento.
Referências Bibliográficas
Caso haja interesse em conhecer as referências bibliográficas e/ou estudos clínicos disponíveis para este medicamento, por favor, entre em contato com nosso Serviço de Atendimento ao Consumidor – Abbott Center através do telefone 0800 7031050.
- 3. CARACTERÍSTICAS FARMACOLÓGICAS
Descrição
O divalproato de sódio é um composto de coordenação estável de valproato de sódio e ácido valproico em uma relação molar de 1:1, formado durante a neutralização parcial do ácido valproico com 0,5 Eq de hidróxido de sódio.
Farmacodinâmica
O divalproato de sódio é dissociado em íon15 valproato no trato gastrintestinal. O mecanismo pelo qual o valproato exerce seu efeito terapêutico não está bem estabelecido. Foi sugerido que sua atividade na epilepsia3 está relacionada ao aumento das concentrações cerebrais de ácido gama-aminobutírico (GABA16).
Farmacocinética
Absorção e Biodisponibilidade: a biodisponibilidade absoluta dos comprimidos de liberação prolongada de DEPAKOTE ER (divalproato de sódio), administrados em dose única após uma refeição foi de aproximadamente 90% em relação à infusão intravenosa. Quando administrados em doses equivalentes, a biodisponibilidade de divalproato de sódio ER é menor que a de divalproato de sódio comprimidos de liberação entérica. Em cinco estudos de doses múltiplas, realizados com indivíduos saudáveis (n = 82) e pacientes com epilepsia3 (n = 86), o comprimido de liberação prolongada, administrado uma vez ao dia em jejum ou imediatamente após refeições menores, teve uma biodisponibilidade média de 89% em relação aos comprimidos de liberação entérica (DEPAKOTE) administrados duas, três ou quatro vezes ao dia.
Nestes estudos, foram encontradas concentrações plasmáticas máximas (Cmáx) de valproato em média 4 a 17 horas após a ingestão de comprimidos de divalproato de sódio de liberação prolongada. Após múltiplas doses de divalproato de sódio de liberação prolongada, a concentração plasmática de valproato era 10 a 20% menor que a resultante da administração de divalproato de sódio administrado duas, três ou quatro vezes ao dia.
Conversão do divalproato de sódio para o divalproato de sódio de liberação prolongada:
quando o divalproato de sódio de liberação prolongada é administrado em doses de 8 a 20% maior do que a dose total diária de divalproato de sódio, as duas formulações são bioequivalentes. Em dois estudos randomizados e cruzados, doses múltiplas diárias de divalproato de sódio foram de 8 a 20% maior do que a dose única diária do divalproato de sódio de liberação prolongada. Nestes estudos, o divalproato de sódio de liberação prolongada e o divalproato de sódio foram equivalentes com respeito à área sob a curva (ASC, uma medida de extensão da biodisponibilidade). Adicionalmente, a Cmáx foi menor, e a Cmin ou foi maior ou indiferente, para o divalproato de sódio de liberação prolongada, em relação ao divalproato de sódio.

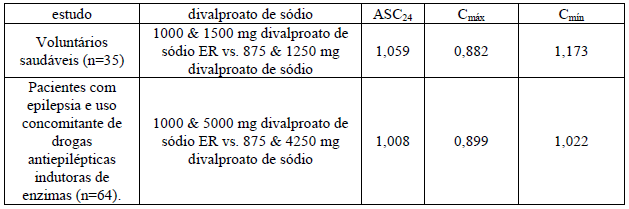
Foram avaliadas drogas antiepilépticas concomitantes, que induzem o sistema das isoenzimas do citocromo P450 (topiramato, fenobarbital, carbamazepina, fenitoína e lamotrigina), e não foram demonstradas alterações significativas na biodisponibilidade do valproato tanto para divalproato de sódio quanto para divalproato de sódio ER.
Distribuição:
Ligação às proteínas17: a ligação do valproato a proteínas17 plasmáticas é dependente da concentração e a fração livre aumenta de aproximadamente 10% com concentração de 40 mcg/ml para 18,5% com concentração de 130 mcg/ml. A ligação protéica do valproato é reduzida em idosos, em pacientes com doenças hepáticas18 crônicas, em pacientes com insuficiência renal19 e na presença de outros fármacos (ex: ácido acetilsalicílico). Por outro lado, o valproato pode deslocar certas ligações protéicas de fármacos (ex: fenitoína, carbamazepina, varfarina e tolbutamida).
Distribuição no SNC20: as concentrações de valproato no líquor21 aproximam-se das concentrações de valproato não ligado a proteínas17 no plasma22 (aproximadamente 10% da concentração total).
Metabolismo23: o valproato é metabolizado quase que totalmente pelo fígado24. Em pacientes adultos sob o regime de monoterapia, 30% a 50% de uma dose administrada aparece na urina25 como conjugado glicuronídeo. A beta-oxidação mitocondrial é outra via metabólica importante, metabolizando mais de 40% da dose. Geralmente, menos de 15 a 20% da dose administrada é eliminada por outros mecanismos oxidativos. Menos de 3% da dose administrada é excretada de forma inalterada pela urina25. A relação entre dose e concentração total de valproato não é linear; a concentração não aumenta proporcionalmente à dose, mas numa extensão menor, devido à saturação da ligação protéica plasmática. A cinética26 do fármaco27 não ligado a proteínas17 plasmáticas é linear.
Eliminação: a depuração plasmática média e o volume de distribuição do valproato total são de 0,56 L/h/1,73m2 e 11 L/1,73m2 , respectivamente. A depuração plasmática média e o volume de distribuição do valproato livre são de 4,6 L/h/1,73 m2 e 92 L/1,73 m2 , respectivamente. A meiavida terminal média para a monoterapia com valproato varia de 9 a 16 horas após a administração oral de 250 a 1000 mg. As estimativas citadas aplicam-se principalmente a pacientes que não estão recebendo medicamentos que afetam os sistemas de metabolização de enzimas hepáticas28. Por exemplo, pacientes que tomam medicamento anticonvulsivante que seja indutor enzimático (carbamazepina, fenitoína e fenobarbital) irão depurar valproato mais rapidamente. Devido a estas alterações na depuração do valproato, a monitorização das concentrações dos anticonvulsivantes deve ser intensificada, tanto na introdução quanto na descontinuação do tratamento.
Populações especiais
Neonatos29: (Nota: A segurança e a eficácia do divalproato de sódio de liberação prolongada na profilaxia de enxaqueca6 em crianças não foram estabelecidas. Dessa forma, a informação abaixo é aplicável em pacientes pediátricos somente nos casos de epilepsia3).
Crianças nos dois primeiros meses de vida tem capacidade de eliminação de valproato bastante reduzida quando comparadas com crianças mais velhas e adultos. Isto é resultado tanto da redução da depuração (talvez em virtude da demora no desenvolvimento da glicuronosil-transferase e outros sistemas enzimáticos envolvidos na eliminação do valproato), quanto do aumento do volume de distribuição (devido, em parte, à ligação protéica plasmática diminuída). Por exemplo, em um estudo, a meia-vida em crianças com menos de 10 dias variou de 10 a 67 horas e em crianças com mais de dois meses de vida, de 7 a 13 horas.
Crianças: (Nota: A segurança e a eficácia do divalproato de sódio de liberação prolongada na profilaxia de enxaqueca6 em crianças não foram estabelecidas. Dessa forma, a informação abaixo é aplicável em pacientes pediátricos somente nos casos de epilepsia3).
Pacientes pediátricos (entre 3 meses e 10 anos) tem depuração 50% mais alta do que os adultos, em relação ao peso (ml/ min/ kg). Acima dos 10 anos de idade, as crianças tem parâmetros farmacocinéticos que se aproximam dos adultos.
O perfil farmacocinético do valproato após a administração de divalproato de sódio de liberação prolongada foi analisado em um estudo multicêntrico aberto de doses múltiplas com crianças e adolescentes.
A dosagem de DEPAKOTE ER (divalproato de sódio) variou de 250 mg a 1750 mg, uma vez ao dia.
Os parâmetros de concentração-tempo produzidos com a administração de DEPAKOTE ER (divalproato de sódio) em pacientes pediátricos (10-17 anos) foram semelhantes aos observados em adultos.
Idosos: pacientes idosos (entre 68 e 89 anos) tem uma capacidade diminuída de eliminação de valproato, quando comparados a adultos jovens (entre 22 e 26 anos). A depuração intrínseca está diminuída em 39% e a fração livre de valproato está aumentada em 44%; portanto, a dosagem inicial deverá ser reduzida em idosos.
Gênero: não há diferenças no clearance da droga não ligada quando se ajusta a área de superfície corporal ente homens e mulheres (4,8 ± 0,17 e 4,7 ± 0,07 L/h/1,73m2 , respectivamente).
Etnia: os efeitos da etnia sobre a cinética26 do valproato não foram estudados.
Doenças hepáticas18: ver “4. CONTRAINDICAÇÕES” e “5. ADVERTÊNCIAS E PRECAUÇÕES – Hepatoxicidade”. Doenças hepáticas18 diminuem a capacidade de eliminação de valproato (ver Contraindicações e Precauções e Advertências - Hepatotoxicidade30). Em um estudo, a depuração de valproato livre estava diminuída em 50% em sete pacientes com cirrose31 e em 16% em quatro pacientes com hepatite32 aguda, em relação a 6 indivíduos saudáveis. Neste estudo, a meia-vida do valproato foi aumentada de 12 para 18 horas. Doença hepática33 também está associada com decréscimo das concentrações de albumina34 e com frações mais altas de valproato não ligado (aumento de 2 a 2,6 vezes). Consequentemente, a monitoração de concentrações totais pode ser enganosa, uma vez que as concentrações livres podem estar substancialmente elevadas em pacientes com doença hepática33, enquanto as concentrações totais podem parecer normais.
Doenças renais: uma pequena redução (27%) na depuração de valproato não ligado foi relatada em pacientes com insuficiência renal19 (clearance de creatinina35 < 10 ml/minuto); no entanto, a hemodiálise36 tipicamente reduz as concentrações de valproato em torno de 20%. Portanto, ajustes de doses parecem não ser necessários em pacientes com insuficiência renal19. A ligação protéica nestes pacientes está substancialmente reduzida, assim, a monitoração das concentrações totais pode ser enganosa.
Níveis plasmáticos e efeitos clínicos: a relação entre concentração plasmática e resposta clínica não está totalmente esclarecida. Um fator contribuinte é a ligação protéica não linear e concentração-dependente do valproato, que afeta a depuração da substância. Então, o monitoramento do valproato sérico total não pode fornecer um índice confiável das espécies bioativas de valproato.
Por exemplo, tendo em vista que a ligação protéica plasmática do valproato é dependente da concentração, a fração livre aumenta cerca de 10% em 40 mcg/ml para 18,5% em 130 mcg/ml.
Ocorrem frações livres maiores do que o esperado em idosos, pacientes hiperlipidêmicos e pacientes com doença hepática33 ou renal37.
Mania: em um estudo clínico placebo11-controlado de mania aguda, pacientes receberam doses obtendo resposta clínica com concentrações plasmáticas entre 85 e 125 µg/ml.
Epilepsia3: a faixa terapêutica38 para epilepsia3 é geralmente considerada entre 50 e 100 mcg/ml de valproato total, embora alguns pacientes possam ser controlados com concentrações plasmáticas menores ou até maiores.


