
PRECAUÇÕES E ADVERTÊNCIAS ASSERT
Inibidores da monoamino oxidase (IMAO1): Casos de reações graves, algumas vezes fatais, foram relatados em pacientes que estavam recebendo Assert® (cloridrato de sertralina) em associação a um inibidor da monoamino oxidase (IMAO1), incluindo o IMAO1 seletivo, selegilina, e o IMAO1 reversível, moclobemida. Alguns casos apresentaram-se com sinais2 semelhantes à síndrome serotoninérgica3, cujos sintomas4 incluem: Hipertermia, rigidez, espasmo5 clônico, instabilidade autonômica com possibilidade de rápidas flutuações dos sinais vitais6, alterações mentais que incluem confusão, irritabilidade e agitação extrema progredindo para delírio7 e coma8. Portanto, a sertralina não deve ser usada em combinação com um IMAO1 ou dentro de 14 dias após a descontinuação do tratamento com IMAO1. Similarmente, um intervalo de no mínimo 14 dias deverá ser respeitado após a descontinuação do tratamento com sertralina antes de iniciar um tratamento com um IMAO1 (vide “contraindicações”).
Outros fármacos serotoninérgicos: A co-administração de Assert® (cloridrato de sertralina) com outros fármacos que aumentam os efeitos da neurotransmissão serotoninérgica, assim como o triptofano, fenfluramina, ou agonistas 5-HT, deve ser realizada com cuidado e ser evitada sempre que possível devido ao potencial de interação farmacodinâmica.
Substituição de antidepressivos inibidores seletivos da recaptação de serotonina (ISRS) ou outros: Existe um número limitado de experiências controladas com relação ao momento ideal para substituir a terapia com antidepressivos ISRS por Assert® (cloridrato de sertralina). É necessário cuidado e avaliação médica prudente ao realizar a mudança, particularmente de agentes de ação prolongada, como a fluoxetina. A duração do período de washout9 necessário para a substituição de um ISRS por outro ainda não foi estabelecida.
Ativação de mania/hipomania: Em estudos iniciais pré-comercialização, hipomania ou mania ocorreram em aproximadamente 0,4% dos pacientes tratados com sertralina. A ativação de mania/hipomania também tem sido relatada numa pequena proporção de pacientes com transtorno afetivo maior tratados com outros antidepressivos disponíveis.
Convulsões: Convulsões são um risco potencial com o uso de medicamentos antidepressivos.
Foram observadas convulsões em aproximadamente 0,08% dos pacientes tratados com Assert® (cloridrato de sertralina) no programa de desenvolvimento para depressão.
Nenhum caso de convulsão10 foi relatado no programa de desenvolvimento para o distúrbio do pânico. Durante o programa de desenvolvimento para TOC, 4 pacientes de um total de aproximadamente 1.800 pacientes expostos ao Assert® (cloridrato de sertralina) apresentaram convulsões (aproximadamente 0,2%). Três desses pacientes eram adolescentes, dois com transtornos convulsivos e um com histórico familiar de transtorno convulsivo, nenhum desses pacientes estavam recebendo medicação anticonvulsivante. Em todos estes casos, a relação com o tratamento com sertralina foi incerta. Uma vez que o Assert® (cloridrato de sertralina) não foi avaliado em pacientes com transtornos convulsivos, ela deve ser evitada em pacientes com epilepsia11 instável. Pacientes com epilepsia11 controlada devem ser cuidadosamente monitorados. O Assert® (cloridrato de sertralina) deve ser descontinuado em qualquer paciente que desenvolva convulsões.
Suicídio: Uma vez que a possibilidade de uma tentativa de suicídio é inerente à depressão e pode persistir até que uma remissão significativa ocorra, os pacientes devem ser cuidadosamente supervisionados durante o período inicial da terapia.
Devido à comorbidade12 estabelecida entre TOC e depressão, Transtorno do Pânico e depressão,
TEPT e depressão e Fobia13 Social e depressão, as mesmas precauções observadas durante o tratamento de pacientes com depressão devem ser observadas durante o tratamento de pacientes com TOC, Transtorno do Pânico, TEPT ou Fobia13 Social.
Uso na Insuficiência Hepática14
A sertralina é extensamente metabolizada pelo fígado15. Um estudo farmacocinético de dose múltipla em indivíduos com cirrose16 estável de grau leve, demonstrou uma meia-vida de eliminação prolongada e Cmáx e área sob a curva (AUC17) aproximadamente 3 vezes maior em comparação a indivíduos sadios. Não foram observadas diferenças significantes na ligação às proteínas18 plasmáticas entre os dois grupos. O uso de Assert® (cloridrato de sertralina) em pacientes com doença hepática19 deve ser feito com cuidado. Uma dose menor ou menos freqüente deve ser considerada para pacientes20 com insuficiência hepática14.
Uso em portadores de insuficiência renal21
A sertralina é extensamente metabolizada. A excreção do fármaco22 inalterado na urina23 é uma via de eliminação pouco significativa. Em pacientes com insuficiência renal21 de grau leve a moderado (clearance de creatinina24 de 30 a 60 mL/min) ou insuficiência renal21 de grau moderado a grave (clearance de creatinina24 de 10 a 29 mL/min), os parâmetros farmacocinéticos de dose múltipla (AUC17 0-24 ou Cmáx) não foram significativamente diferentes quando comparados aos controles. As meias-vidas foram similares e não houve diferenças na ligação às proteínas18 plasmáticas em todos os grupos estudados. Este estudo indica que, de acordo com a baixa excreção renal25 da sertralina, as doses de sertralina não precisam ser ajustadas com base no grau de insuficiência renal21.
Uso em crianças
A segurança e a eficácia do uso da sertralina foi estabelecida para pacientes20 pediátricos (com idades variando entre 6 a 17 anos) apenas para o tratamento do TOC (vide “Posologia e Administração – Uso em Crianças”).
Uso durante a gravidez26 e lactação27
Estudos de reprodução28 foram realizados em ratos e coelhos com doses até aproximadamente 20 e 10 vezes a dose máxima diária em humanos (mg/kg), respectivamente. Não foi observada qualquer evidência de teratogenicidade em qualquer nível de dose. Contudo, nas doses correspondentes à aproximadamente 2,5 a 10 vezes a dose máxima diária em humanos (mg/kg), a sertralina foi associada com retardo no processo de ossificação dos fetos, provavelmente secundários aos efeitos maternos.
Houve diminuição da sobrevida29 neonatal após a administração materna de sertralina em doses aproximadamente 5 vezes superior à dose máxima indicada para humanos (mg/kg).
Efeitos similares na sobrevida29 neonatal foram também observados com outros fármacos antidepressivos. O significado clínico destes efeitos é desconhecido.
Não há estudos adequados e bem controlados em mulheres grávidas. Uma vez que estudos de reprodução28 em animais nem sempre prevêem a resposta humana, a sertralina deverá ser usada durante a gravidez26 somente quando os benefícios superarem os riscos potenciais.
Mulheres em idade fértil devem empregar métodos adequados de contracepção30 quando em tratamento com Assert® (cloridrato de sertralina).
Apenas dados limitados a respeito dos níveis de sertralina no leite materno estão disponíveis.
Estudos isolados em um número muito pequeno de lactantes31 e seus recém-nascidos indicaram níveis de sertralina desprezíveis ou indetectáveis no soro32 da criança recémnascida,
embora os níveis no leite materno foram mais concentrados do que aqueles no soro32 materno. O uso em lactantes31 não é recomendado a menos que, na avaliação do médico, os benefícios superarem os riscos.
Se a sertralina for administrada durante a gravidez26 e/ou lactação27, o médico responsável deve ser informado que sintomas4, incluindo aqueles compatíveis com as reações de abstinência, foram relatados em alguns neonatos33, cujas mães estavam sob tratamento com antidepressivos ISRS, incluindo a sertralina.
Efeitos sobre a habilidade de dirigir veículos e/ou operar máquinas
Estudos clínicos de farmacologia34 demonstraram que Assert® (cloridrato de sertralina) não produz efeito na atividade psicomotora35. Contudo, uma vez que medicamentos psicotrópicos36 podem interferir nas habilidades mentais ou físicas necessárias para a realização de tarefas potencialmente arriscadas como dirigir e operar máquinas, o paciente deve ser advertido adequadamente.
- INTERAÇÕES MEDICAMENTOSAS
IMAO1: Vide item “Precauções e Advertências” e “Contraindicações”.
Depressores do SNC37 e álcool: A administração concomitante com 200 mg diários de sertralina não potencializa os efeitos do álcool, carbamazepina, haloperidol ou fenitoína nas atividades psicomotoras e cognitivas em indivíduos sadios; entretanto, o uso concomitante de Assert® (cloridrato de sertralina) e álcool não é recomendado.
Lítio: Em estudos placebo38-controlados realizados em voluntários sadios, a co-administração de sertralina e lítio não alterou significativamente a farmacocinética do lítio porém, em relação ao placebo38, resultou em um aumento no tremor, indicando uma possível interação farmacodinâmica. Os pacientes que estiverem sob tratamento concomitantemente com sertralina e outros medicamentos, como o lítio, que podem atuar por mecanismos serotoninérgicos, devem ser apropriadamente monitorizados.
Fenitoína: Em um estudo placebo38-controlado com voluntários sadios, a administração crônica de sertralina 200 mg/dia, não produz inibição clinicamente importante do metabolismo39 da fenitoína. Entretanto, após o início do tratamento com sertralina, é recomendado que as concentrações plasmáticas de fenitoína sejam monitorizadas e sua dose seja ajustada adequadamente.
Sumatriptano: No período pós-comercialização, foram relatados raros casos de pacientes apresentando fraqueza, hiper-reflexia, incoordenação motora, confusão, ansiedade e agitação, após o tratamento com sertralina e sumatriptano. Se o tratamento concomitante com sertralina e sumatriptano for clinicamente justificado, recomenda-se que os pacientes sejam acompanhados adequadamente (vide “Precauções e Advertências – Outros fármacos serotoninérgicos”).
Outros fármacos serotoninérgicos: Vide item “Precauções e Advertências”.
Fármacos que se ligam a proteínas18 plasmáticas: Uma vez que a sertralina liga-se às proteínas18 plasmáticas, o potencial da mesma em interagir com outros fármacos que se ligam às proteínas18 plasmáticas deve ser levado em consideração. Entretanto, em três estudos formais de interação com diazepam, tolbutamida e varfarina respectivamente, a sertralina não apresentou efeitos significantes na ligação do substrato às proteínas18 (vide também os itens “Varfarina” e “Interações com outros fármacos”).
Varfarina: A co-administração de 200 mg diários de sertralina com varfarina resultou em um aumento pequeno mas, estatisticamente significante, no tempo de protrombina40; a significância clínica deste fato é desconhecida. Sendo assim, o tempo de protrombina40 deve ser cuidadosamente monitorado quando a terapia com a sertralina for iniciada ou interrompida.
Interações com outros fármacos: Estudos formais de interação medicamentosa foram realizados com sertralina. A co-administração de 200 mg diários de sertralina com diazepam ou tolbutamida resultou em pequenas alterações estatisticamente significantes em alguns parâmetros farmacocinéticos. A co-administração com a cimetidina causou um decréscimo significativo na eliminação da sertralina. O significado clínico destas alterações é desconhecido. A sertralina não apresentou qualquer efeito sobre a capacidade bloqueadora beta-adrenérgica do atenolol.
Nenhuma interação foi observada com 200 mg diários de sertralina e glibenclamida ou digoxina.
Terapia eletroconvulsiva (TEC): Não existem estudos clínicos estabelecendo os riscos ou benefícios do uso combinado de TEC e sertralina.
Fármacos metabolizados pelo citocromo P450 (CYP) 2D6: Há uma variabilidade entre os antidepressivos no que se refere ao grau de inibição da atividade da isoenzima CYP 2D6. A significância clínica desse achado depende do grau de inibição e da indicação terapêutica41 do fármaco22 que será co-administrado. Os substratos da isoenzima CYP 2D6 que apresentam uma indicação terapêutica41 restrita incluem os antidepressivos tricíclicos e antiarrítmicos da classe 1C, tais como a propafenona e a flecainida. Em estudos formais de interação, a administração crônica de 50 mg diários de sertralina demonstrou uma elevação mínima (23%-37%, em média) nos níveis plasmáticos de steady state de desipramina (um marcador da atividade da isoenzima CYP 2D6).
Fármacos metabolizados por outras enzimas do CYP (CYP 3A3/4, CYP 2C9, CYP 2C19, CYP1A2):
CYP 3A3/4: Estudos de interação in vivo demonstraram que a administração crônica de 200 mg diários de sertralina não inibe a 6-beta hidroxilação do cortisol endógeno mediada pelo CYP 3A3/4 nem o metabolismo39 da carbamazepina ou da terfenadina. Além disso, a administração crônica de sertralina 50 mg, diariamente, não inibe o metabolismo39 do alprazolam que é mediado pelo CYP 3A3/4. Os resultados desses estudos sugerem que a sertralina não seja um inibidor clinicamente relevante do CYP 3A3/4.
CYP 2C9: A aparente ausência de efeitos clinicamente significantes da administração crônica de 200 mg diários de sertralina nas concentrações plasmáticas de tolbutamida, fenitoína e varfarina sugere que a sertralina não é um inibidor clinicamente relevante do CYP 2C9 (vide os itens “interações com outros fármacos”, “fenitoína” e “varfarina”).
CYP 2C19: A aparente ausência de efeitos clinicamente significantes da administração crônica de 200 mg diários de sertralina nas concentrações plasmáticas de diazepam sugere que a sertralina não é um inibidor clinicamente relevante do CYP 2C19 (vide o item “interação com outros fármacos”).
CYP 1A2: Estudos in vitro indicam que a sertralina apresenta pouco ou nenhum potencial de inibir o CYP 1A2.
- REAÇÕES ADVERSAS
Em estudos com doses múltiplas de Assert® (cloridrato de sertralina), para depressão, as reações adversas que ocorreram com freqüência significativamente maior em relação ao placebo38 foram:
• Sistema nervoso autônomo42: Boca43 seca e aumento da sudorese44.
• Sistema nervoso central45 e periférico: Tontura46 e tremor
• Gastrintestinal: Diarréia47/fezes amolecidas, dispepsia48 e náusea49.
• Psiquiátrico: Anorexia50, insônia e sonolência.
• Reprodutivo: Disfunção sexual (principalmente retardo na ejaculação51).
O perfil de efeito adverso normalmente observado em estudos duplo-cegos, placebocontrolados em pacientes com transtorno obsessivo compulsivo (TOC), transtorno do pânico, transtorno do stress pós-traumático (TEPT) e fobia13 social foi semelhante ao observado em experiências clínicas em pacientes com depressão.
Incidência52 em testes clínicos controlados
A tabela que segue enumera os efeitos adversos que ocorreram com uma freqüência de 1% ou mais entre pacientes tratados com sertralina que participaram dos ensaios controlados comparados com pacientes que receberam placebo38. A maior parte dos pacientes receberam doses de 50 a 200 mg por dia. O médico deve estar ciente que estes dados não podem ser usados para predizer a incidência52 de efeitos adversos no curso da prática médica usual onde as características do paciente e outros fatores diferem daqueles pré-avaliados nos ensaios clínicos53. Similarmente, as freqüências citadas não podem ser comparadas com os dados obtidos por outras investigações clínicas envolvendo tratamentos, usos e indivíduos diferentes.
TABELA 1: Incidência52 de efeitos adversos durante tratamentos em ensaios clínicos53 placebo38-controlados.*
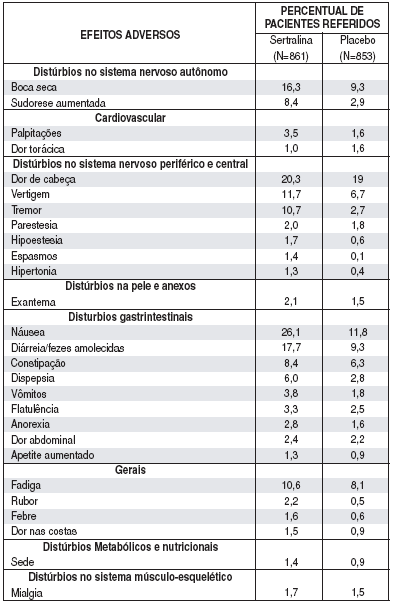
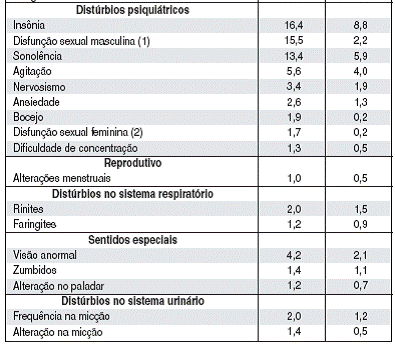
(*) Eventos relatados em pelo menos 1% de pacientes tratados com sertralina.
(1) (ejaculação51 retardada principalmente) % baseada somente em pacientes masculinos: 271 tratados com sertralina e 271 tratados com placebo38.
(2)% baseada somente em pacientes femininos: 590 tratados com sertralina e 582 tratados com placebo38.
Outros efeitos observados durante a avaliação pré-comercialização de sertralina:
Durante a pesquisa, doses múltiplas de sertralina foram administradas a aproximadamente 2.700 indivíduos. As condições e duração de exposição à sertralina variaram amplamente, e incluíram (em categorias coincidentes) estudos farmacológicos clínicos, estudos duplo-cegos e abertos, estudos controlados e não-controlados, estudos em pacientes hospitalizados e não-hospitalizados, estudos para outras indicações além de depressão. Efeitos adversos associados com esta exposição foram registrados por pesquisadores usando terminologia de sua preferência. Conseqüentemente não foi possível estipular a estimativa expressiva da proporção de indivíduos que apresentaram efeitos adversos, sem que antes os efeitos tivessem sido agrupados em um pequeno número de categorias padronizadas.Os efeitos são classificados da seguinte forma: efeitos adversos freqüentes são aqueles que ocorrem em uma ou mais ocasiões em pelo menos 1/100 pacientes (somente aqueles que não foram anteriormente listados nos resultados dos testes placebo38-controlados aparecem nesta lista); efeitos adversos pouco freqüentes são aqueles que ocorrem em 1/100 até 1/1000 pacientes; efeitos raros são aquelesque ocorrem em menos que 1/1000 pacientes.
Distúrbios do sistema nervoso autônomo42: Pouco freqüente: rubor, midríase54, aumento de salivação, pele55 viscosa e fria; raro: palidez.
Cardiovascular: Pouco freqüente: tontura46 postural, hipertensão56, hipotensão57, hipotensão57 postural, edema58, edema58 dependente, edema58 periorbital, edema58 periférico, isquemia59 periférica, síncope60, taquicardia61; raro: dor torácica precordial62, dor torácica substernal, hipertensão56 grave, enfarte do miocárdio63, veias64 varicosas.
Distúrbios no sistema nervoso central45 e periférico: Freqüente: confusão; pouco freqüente:
ataxia65, coordenação anormal, marcha anormal, hiperestesia, hipercinesia66, hipocinesia, enxaqueca67, nistagmo68, vertigem69; raro: anestesia70 local, coma8, convulsões, discinesia, disfonia71, hiporreflexia,hipotonia72, ptose73.
Alterações na pele55 e anexos74: Pouco freqüente: acne75, alopecia76, prurido77, exantema78 eritematoso79, exantema78 maculopapular80, pele55 seca; raro: erupção81 vesiculosa, dermatite82, eritema multiforme83, textura capilar84 anormal, hipertricose85, reação de fotossensibilidade, exantema78 folicular, descoloração da pele55, odor anormal da pele55, urticária86.
Distúrbios endócrinos: Raro: exoftalmia, ginecomastia87.
Distúrbios gastrintestinais: Pouco freqüente: disfagia88, eructação89; raro: diverticulite90, incontinência fecal91, gastrite92, gastroenterite93, glossite94, hiperplasia95 gengival, hemorróidas96, soluço, melena97, úlcera péptica98 hemorrágica99, proctite100, estomatite101, estomatite101 ulcerativa, tenesmo102, edema58 de língua103, ulceração104 na língua103.
Geral: Freqüente: astenia105; pouco freqüente: mal-estar, edema58 generalizado, calafrios106, perda de peso, aumento de peso; raro: abdômen aumentado, halitose107, otite média108, estomatite101 aftosa.
Hematopoético e linfático109: Pouco freqüente: linfadenopatia, púrpura110; raro: anemia111, hemorragia112 de câmara anterior113 do olho114.
Distúrbios metabólicos e nutricionais: Raro: desidratação115, hipercolesterolemia116, hipoglicemia117.
Distúrbios no sistema músculo-esquelético: Pouco freqüente: atralgia, artrose118, distonia119, espasmo5 muscular, debilidade muscular; raro: hérnia120.
Distúrbios psiquiátricos: Pouco freqüente: pesadelos, reação agressiva, amnésia121, apatia122, delírio7, despersonalização, depressão, depressão grave, labilidade emocional, euforia,alucinação123, neurose124, reação paranóica, planejamento e tentativa de suicídio, ranger de dentes, pensamentos anormais; raro: histeria, sonambulismo, síndrome125 de abstinência.
Reprodutivo: Pouco freqüente: dismenorréia126 (2), hemorragia112 intermenstrual (2); raro: amenorréia127 (2), balanopostite128(1), aumento da mama129 (2), dor mamária (2), leucorréia130 (2),menorragia131 (2), vaginite132 atrófica133 (2).
(1) % baseada somente em indivíduos masculinos: 1.005
(2) % baseada somente em indivíduos femininos: 1.705.
Distúrbios do sistema respiratório134: Pouco freqüente: broncospasmo, tosse, dispnéia135, epistaxe136; raro: bradipnéia, hiperventilação, sinusite137, estridor.
Sentidos especiais: Pouco freqüente: acomodação anormal, conjuntivite138, diplopia139, dor de ouvido, dor nos olhos140, xeroftalmia141; raro: lacrimejamento anormal, fotofobia142, problema no campo visual143.
Distúrbios no sistema urinário144: Pouco freqüente: disúria145, edema58 de face146, noctúria, poliúria147, incontinência urinária148; raro: oligúria149, dor renal25, retenção urinária150.
Testes laboratoriais: Elevações assintomáticas nas transaminases séricas (TGO e TGP) têm sido relatadas com pouca freqüência (aproximadamente 0,8%) em associação à administração de sertralina. Estas elevações enzimáticas habitualmente ocorrem dentro da primeira à nona semana de tratamento e diminuem rapidamente após interrupção do fármaco22. A terapia com sertralina foi associada com pequenos aumentos na média total de colesterol151 (aproximadamente 3%) e triglicerídeos (aproximadamente 5%), e uma pequena diminuição na média de ácido úrico sérico (aproximada-mente 7%), aparentemente sem importância clínica.
Dados do período pós-comercialização
Relatos espontâneos de eventos adversos em pacientes sendo tratados com cloridrato de sertralina recebidos desde a introdução do medicamento no mercado. Estes relatos incluem: Sistema nervoso autônomo42: midríase54 e priapismo152.
• Geral: Reação alérgica153, alergia154, reação anafilactóide, astenia105, fadiga155, febre156,rubor, mal-estar, diminuição do peso e aumento do peso.
• Cardiovascular: Dor torácica, edema58 periférico, hipertensão56, palpitações157, edema58 periorbital, síncope60 e taquicardia61.
• Sistema nervoso central45 e periférico: Coma8, convulsões, dor de cabeça158, enxaqueca67, distúrbios motores (incluindo sintomas4 extrapiramidais tais como, hipercinesia66, hipertonia159, ranger de dentes e distúrbios da marcha), contrações musculares involuntárias, parestesia160 e hipoestesia161. Também foram relatados sinais2 e sintomas4 associados à síndrome125 de serotonina: em alguns casos associados com o uso concomitante de fármacos serotoninérgicos incluindo agitação, confusão, sudorese44, diarréia47, febre156, hipertensão56, rigidez e taquicardia61.
• Endócrino162: Galactorréia163, ginecomastia87, hiperprolactinemia, hipotireoidismo164, síndrome125 da secreção inapropriada de hormônio165 anti-diurético166 (adh).
• Gastrintestinal: Dor abdominal, aumento do apetite, constipação167, pancreatite168 e vômito169. • Audição/ vertibular: Tinido.
• Hematopoiético: Função plaquetária alterada, distúrbios hemorrágicos170 (tais como epistaxe136, hemorragia112 gástrica e hematúria171), leucopenia172, púrpura110 e trombocitopenia173.
• Alterações laboratoriais: Resultados clínicos laboratoriais anormais. Hepático/biliar: eventos hepáticos graves (incluindo hepatite174, icterícia175 e disfunção hepática19) e elevações assintomáticas das transaminases hepáticas176 (TGO e TGP).
• Metabólico/nutricional: Hiponatremia177 e aumento do colesterol151 sérico. Muscoloesquelético: artralgia178.
• Psiquiátrico: Agitação, reações agressivas, ansiedade, sintomas4 de depressão, euforia, alucinações179, diminuição do libido180 feminino e masculino, paroníria, psicose181 e bocejo.
• Reprodutivo: Irregularidades menstruais.
• Respiratório: Broncoespasmo182.
• Pele55: Alopecia76, angioedema183, reação de fotossensibilidade na pele55, puridro, rash184 (incluindo casos raros de graves distúrbios esfoliativos da pele55, por exemplo síndrome125 de stevensjohnson e necrose185 epidérmica) e urticária86. Urinário: edema58 facial, incontinência urinária148 e retenção urinária150. Visão186: visão186 anormal.
• Outros: Foram relatados sintomas4 seguidos da descontinuação do uso da sertralina, e incluem agitação, ansiedade, tontura46, dor de cabeça158, náusea49 e parestesia160.
INFORME SEU MÉDICO O APARECIMENTO DE REAÇÕES DESAGRADÁVEIS.
- POSOLOGIA E ADMINISTRAÇÃO
Assert® (cloridrato de sertralina) deve ser administrado em dose única diária, pela manhã ou à noite. Assert® (cloridrato de sertralina) comprimidos revestidos pode ser administrado com ou sem alimentos.
TRATAMENTO INICIAL
Depressão e TOC: O tratamento com Assert® (cloridrato de sertralina) deve ser feito com uma dose de 50 mg/dia.
Transtorno do Pânico e Transtorno do Stress Pós-Traumático (TSPT) e Fobia13 Social: O tratamento deve iniciar com 25 mg/dia, aumentando para 50 mg/dia após uma semana. Este regime de dosagem demonstrou reduzir a freqüência de efeitos colaterais187 emergentes no início do tratamento, característicos do transtorno do pânico.
Síndrome125 da Tensão Pré-Menstrual (STPM) e Transtorno Disfórico Pré-Menstrual (TDPM): O tratamento deve ser iniciado com 50 mg/dia, podendo-se adotar o tratamento contínuo (durante todo o ciclo menstrual) ou apenas durante a fase lútea do ciclo, de acordo com orientação médica.
TITULAÇÃO
Depressão, TOC, Transtorno do Pânico, Transtorno do Stress Pós –Traumático e Fobia13
Social: Os pacientes que não responderem à dose de 50 mg, podem ser beneficiados com um aumento da dose. As alterações nas doses devem ser realizadas com um intervalo mínimo de 1 semana, até a dose máxima recomendada de sertralina que é de 200 mg/dia.
Alterações nas doses não devem ser feitas mais que 1 vez por semana devido à meia-vida de eliminação da sertralina de 24 horas.
O início dos efeitos terapêuticos pode ocorrer dentro de 7 dias. Entretanto, períodos maiores são usualmente necessários, especialmente em TOC.
Síndrome125 da Tensão Pré-Menstrual (STPM) e Transtorno Disfórico Pré-Menstrual (TDPM): Uma vez que a relação entre dose e efeito ainda não foi estabelecida para o tratamento dos sintomas4 da Síndrome125 da Tensão Pré-Menstrual e/ou Transtorno Disfórico Pré-Menstrual, as pacientes que participaram dos estudos clínicos foram tratadas com doses variando entre 50-150 mg/dia, com aumentos de dose a cada novo ciclo menstrual.
As pacientes que não estiverem obtendo resultados com a dose de 50 mg/dia, podem ser beneficiadas com aumentos de dose (incrementos de 50 mg a cada ciclo menstrual), até um máximo de 150 mg/dia quando administrado diariamente durante todo o ciclo menstrual, ou até um máximo de 100 mg/dia quando administrado somente durante a fase lútea do ciclo. Se a dose de 100 mg/dia for estabelecida para a fase lútea, titulações equivalentes a 50 mg/dia, por três dias, devem ser utilizadas no início do tratamento de cada fase lútea do ciclo.
MANUTENÇÃO
A dose de Assert® (cloridrato de sertralina) durante a terapia de manutenção prolongada deverá ser mantida com a menor dose eficaz, com subsequentes ajustes dependendo da resposta terapêutica41.
USO EM CRIANÇAS
Tratamento do TOC: A segurança e a eficácia do uso da sertralina foi estabelecida para pacientes20 pediátricos (com idades variando entre 6 e 17 anos) apenas para o tratamento do TOC. A administração de sertralina em pacientes pediátricos com idades variando entre 13 e 17 anos, deve começar com 50 mg/dia. O tratamento de pacientes pediátricos com idades variando entre 6 e 12 anos, deve começar com 25 mg/dia e aumentar para 50 mg/dia após uma semana. No caso de ausência de resposta clínica, a dose pode ser subseqüentemente aumentada em incrementos de 50 mg/dia, até 200 mg/dia, se necessário. Em um estudo clínico com pacientes com idades variando entre 6 e 17 anos, com depressão ou TOC, a sertralina mostrou um perfil farmacocinético similar àquele observado em adultos. Entretanto, o menor peso corpóreo de uma criança, quando comparado ao de um adulto, deve ser considerado quando se pensar em aumentar a dose de 50 mg.
Titulação em Crianças e Adolescentes: Uma vez que a meia-vida de eliminação da sertralina é de aproximadamente 24 horas, as mudanças de dosagem não devem ocorrer em intervalos menores que uma semana.
Uso na Insuficiência Hepática14: O uso da sertralina em pacientes com doença hepática19 deve ser feito com cuidado. Uma dose menor ou menos freqüente deve ser considerada para pacientes20 com insuficiência hepática14 (vide item “Precauções e Advertências”).
Uso na Insuficiência Renal21: A sertralina é extensamente metabolizada. A excreção do fármaco22 inalterado na urina23 é uma via de eliminação pouco significativa. De acordo com a baixa excreção renal25 da sertralina, as doses de sertralina não precisam ser ajustadas com base no grau de insuficiência renal21 (vide item “Precauções e Advertências”).
- SUPERDOSAGEM
Conforme as evidências disponíveis, Assert® (cloridrato de sertralina) tem ampla margem de segurança em superdosagem. Superdosagem com Assert® (cloridrato de sertralina) isoladamente em doses de até 13,5 g foram relatadas. Foram relatadas mortes envolvendo superdosagens com Assert® (cloridrato de sertralina), principalmente em associação a outros fármacos e/ou álcool. Portanto, qualquer superdosagem deve ser tratada rigorosamente. Os sintomas4 de superdosagem incluem: efeitos adversos mediados pela serotonina tais como sonolência, distúrbios gastrintestinais (como náusea49 e vômito169), taquicardia61, tremor, agitação e tontura46. Coma8 foi reportado com menor freqüência. Não existem antídotos específicos para sertralina. Estabeleça e mantenha respiração assistida, assegure ventilação188 e oxigenação adequadas, se necessário. O carvão ativado, o qual pode ser utilizado com um agente catártico, pode ser tão ou mais eficaz do que a lavagem e deve ser considerado no tratamento da superdosagem. A indução de vômito169 não é recomendada. Monitorizações cardíaca e dos sinais vitais6 são recomendadas juntamente com o controle dos sintomas4 e medidas gerais de suporte. Devido ao amplo volume de distribuição da sertralina, diurese189 forçada, diálise190, hemoperfusão e transfusão191 de sangue192 provavelmente não trarão benefícios.


