
REAÇÕES ADVERSAS FEMOSTON CONTI
As reações adversas mais comumente reportadas pelas pacientes tratadas com estradiol/didrogesterona em estudos clínicos foram dor de cabeça1, dor abdominal, dor/sensibilidade nas mamas2 e dor nas costas3.
Os seguintes efeitos adversos foram observados com a frequência indicada abaixo durante estudos clínicos (n=4929):
Reações muito comuns (> 1/10)
Desordens do Sistema Nervoso4: dor de cabeça1
Desordens gastrointestinais: dor abdominal
Desordens do tecido conjuntivo5 e musculoesquelético: dor nas costas3
Desordens do Sistema Reprodutivo e mama6: dor/sensibilidade aumentada nas mamas2
Reações comuns (≥ 1/100 e <1/10)
Infecções7 e infestações: candidíase8 vaginal;
Desordens psiquiátricas: depressão e nervosismo;
Desordens do Sistema Nervoso4: enxaqueca9 e tontura10;
Desordens gastrointestinais: náusea11, vômito12 e flatulência;
Desordens da pele e tecido subcutâneo13: reações alérgicas na pele14 (por exemplo: rash15, urticária16, prurido17);
Desordens do Sistema Reprodutivo e mama6: desordens menstruais (incluindo metrorragia18, menorragia19, oligo/amenorreia20, menstruação21 irregular, dismenorreia22, sangramentos de escape, dor pélvica23 e secreção cervical;
Desordens gerais e alterações no local de administração: condições de astenia24 (astenia24, fatiga, indisposição) e edema25 periférico;
Investigações: aumento de peso.
Reações incomuns (≥ 1/1.000 e <1/100)
Neoplasias26 benignas, malignas e não especificadas: aumento no tamanho do leiomiomas;
Desordens do Sistema Imunológico27: hipersensibilidade;
Desordens psiquiátricas:influência na libido28;
Desordens vasculares29: tromboembolismo30 venoso (ver abaixo mais informações);
Desordens hepatobiliares31: função hepática32 anormal, ocasionalmente com icterícia33, astenia24 ou mal-estar e dor abdominal, e desordens da vesícula biliar34;
Desordens do sistema Reprodutivo e mamas2: aumento das mamas2 e síndrome35 pré-menstrual;
Investigações: diminuição de peso.
Reações raras (≥ 1/10.000 e <1/1.000)
Desordens cardíacas: infarto do miocárdio36;
Desordens da pele e tecido subcutâneo13: angiodema, púrpura37 vascular38.
Risco de câncer39 de mama6
Um aumento de 2 vezes no risco de apresentar câncer39 de mama6 diagnosticado é reportado em mulheres que utilizaram terapia combinada40 de estrogênio e progestagênio por mais de 5 anos.
Qualquer aumento no risco de pacientes que utilizam a terapia de estrogênios isolados é substancialmente menor do que observado em pacientes que utilizam a terapia combinada40 de estrogênios e progestagênios.
O aumento de risco é dependente da duração do tratamento (ver “5. Advertências e Precauções”).
Resultados do principal estudo clínico randomizado41 e controlado por placebo42 (Estudo WHI) e o principal estudo epidemiológico (MWS) são apresentados a seguir:
Estudo MWS (Million Women Study) – Risco adicional estimado de câncer39 de mama6 após 5 anos de tratamento:
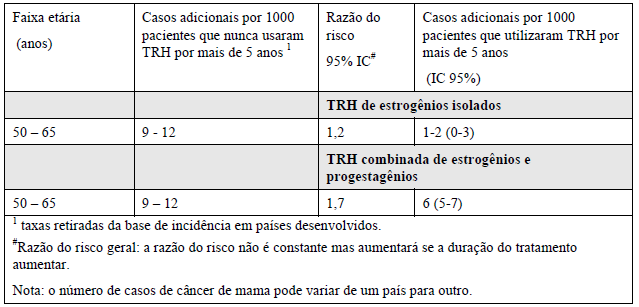
Estudo WHI (Womes’s Health Initiative) – Risco adicional de câncer39 de mama6 após 5 anos de tratamento:

Risco de câncer39 endometrial (Mulheres pós-menopausa43 com útero44 intacto)
O risco de câncer39 endometrial é cerca de 5 em cada 1000 mulheres com útero44 intacto e que não utilizaram a TRH.
Em mulheres com o útero44 intacto, o uso de TRH com estrogênios isolados não é recomendado porque este aumenta o risco de câncer39 endometrial (ver “5. Advertências e Precauções”). Dependendo da duração do tratamento e da dose utilizada de estrogênios isolados, o aumento de risco de câncer39 endometrial em estudos epidemiológicos, variou entre 5 e 55 casos diagnosticados a cada 1000 mulheres na faixa etária de 50 e 65 anos.
Adicionar um progestagênio à terapia com estrogênio isolado por no mínimo 12 dias por ciclo pode prevenir este risco aumentado. No estudo MWI o uso de TRH combinada (sequencial ou contínua) por 5 anos não aumentou o risco de câncer39 endometrial [RR de 1,0 (0,8 – 1,2)].
Câncer39 do ovário45
O uso a longo prazo da TRH combinada ou com estrogênios isolados foi associado a um ligeiro aumento no risco de câncer39 do ovário45. No estudo MWI 5 anos de TRH resultou em 1 caso extra a cada 2500 pacientes.
Risco de Tromboembolismo30 venoso
TRH está associada com um aumento de 1,3 a 3 vezes no risco de desenvolvimento de tromboembolismo30 venoso, ou seja, trombose venosa profunda46 ou embolismo47 pulmonar. A ocorrência desses eventos é mais frequente entre no primeiro ano de uso da TRH (ver “5. Advertência e Precauções”). Os resultados dos estudos WHI são apresentados a seguir:
Estudo WHI (Womes’s Health Initiative) – Risco adicional de TEV após 5 anos de tratamento:

Risco de Doença Arterial Coronariana
O risco de doença arterial coronariana é levemente aumentado em pacientes com 60 anos ou mais utilizando TRH combinada (ver “5. Advertência e Precauções”).
Risco de Acidente Vascular Cerebral48 Isquêmico49
O uso da terapia combinada40 ou com estrogênios isolados está associado a um aumento de 1,5 vezes no risco de ataque isquêmico49. O risco de ataque hemorrágico50 não é aumentado durante o uso da TRH.
O risco relativo não é dependente da idade ou da duração do tratamento, mas como o risco limiar é fortemente dependente da idade, o risco geral de ataque em mulheres que utilizam TRH aumentará com a idade (ver “5. Advertência e Precauções”).
Estudo WHI (Womes’s Health Initiative) combinado – Risco adicional de AVC isquêmico49 após 5 anos de tratamento:

Outras reações adversas foram relatadas em associação ao tratamento com estrogênio/progestagênio (incluindo estradiol/didrogesterona):
Neoplasias26 benignas, malignas e não especificadas: neoplasias26 dependentes de estrogênios tanto benignas quanto malignas, por exemplo, câncer39 endometrial e câncer39 ovariano. Aumento no tamanho de neoplasias26 dependentes de progestagênios, por exemplo: meningioma;
Desordens do sangue51 e sistema linfático52: anemia hemolítica53;
Desordens do Sistema Imunológico27: lúpus54 eritematoso55 sistêmico56;
Desordens do metabolismo57 e nutrição58: hipertrigliceridemia;
Desordens do Sistema Nervoso4: provável demência59, coreia, exacerbação da epilepsia60;
Desordens oculares: intolerância a lentes de contato e modificações na curvatura da córnea61;
Desordens da pele e tecido subcutâneo13: eritema multiforme62, eritema nodoso63, cloasma64 ou melasma65 (que podem persistir quando o medicamento é descontinuado);
Desordens vasculares29: tromboembolismo30 arterial;
Desordens gastrointestinais: pancreatite66 (em mulheres com hipertrigliceridemia pré-existente);
Desordens do tecido conjuntivo5 e musculoesquelético: cãibras nas pernas;
Desordens renais e urinárias: incontinência urinária67;
Desordens do Sistema Reprodutor e Mamas2: alterações fibrocísticas das mamas2 e erosão cervical uterina;
Desordens genéticas ou congênitas68: agravamento da porfiria69;
Investigações: aumento do hormônio70 tireoidiano total.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.
- 10. SUPERDOSE
Tanto estradiol quanto a didrogesterona são substâncias com baixa toxicidade71. Sintomas72 como náusea11, vômito12, sensibilidade nas mamas2, tontura10, dor abdominal, sonolência/fadiga73 e sangramento podem ocorrer em casos de superdosagem. É improvável que haja necessidade de tratar sintomas72 específicos.
Estas informações também são aplicáveis para superdosagem em crianças.
Em caso de intoxicação, ligue para 0800 722 6001, se você precisar de mais orientações.


