Clonidin
CRISTÁLIA PRODUTOS QUÍMICOS FARMACÊUTICOS LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Clonidin®
cloridrato de clonidina
Injetável 150 mcg/mL
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Solução Injetável
Ampola de 1 mL
USO INTRATECAL, EPIDURAL1, INTRAMUSCULAR E INTRAVENOSO
USO ADULTO
COMPOSIÇÃO:
Cada mL de Clonidin® contém:
| cloridrato de clonidina (equivalente a 129,482 mcg de clonidina) | 150 mcg |
| veículo q.s.p. | 1 mL |
Veículo: cloreto de sódio e água para injetáveis.
INFORMAÇÕES AO PACIENTE
PARA QUE ESTE MEDICAMENTO É INDICADO?
Clonidin® solução injetável possui ação analgésica e ação sinérgica com anestésicos opioides lipofílicos, morfina e anestésicos locais. Atua na estabilização hemodinâmica2. Dentre suas aplicações podemos destacar:
- Analgésico3 potente de curta duração (4 a 6 horas) por via intratecal ou epidural1.
- Adjuvante em analgesia intratecal ou epidural1: potencializa a ação de anestésicos tais como a lidocaína e a bupivacaína, favorecendo diminuição de dose e prolongamento da ação. Associada à bupivacaína isobárica, diminui a incidência4 de “Tourniquet Pain”.
- Adjuvante em analgesia pós-operatória: redução de morfina e opioides lipofílicos com consequente diminuição de seus efeitos colaterais5.
A medicação pré-anestésica com Clonidin® já é rotineira e inclui ainda as seguintes indicações:
- Promover estabilização hemodinâmica2
- Reduzir níveis plasmáticos de catecolaminas
- Reduzir a demanda por anestésicos opioides e anestésicos gerais
- Prolongar a anestesia6 intratecal por tetracaína
- Reduzir a pressão intraocular7 em cirurgia oftálmica
COMO ESTE MEDICAMENTO FUNCIONA?
A clonidina é um agonista8 α2 adrenérgico9 parcial, interagindo também com receptores imidazolínicos. O perfil farmacológico é complexo, tendo como variáveis principais: a dose; a distribuição dos receptores no SNC10, tecidos vasculares11 e órgãos; via de administração e interação com outros fármacos. Em doses terapêuticas pela via sistêmica age de forma sinérgica com anestésicos opioides lipofílicos e com benzodiazepínicos. A demanda de oxigênio é diminuída. Através das vias intratecal e epidural1, a clonidina exerce efeito analgésico3 de ação opioide, por interação com receptores adrenérgicos12 localizados no corno dorsal da medula13.
Atua sinergicamente com opioides lipofílicos e anestésicos locais.
Em doses baixas, o efeito hipotensivo é predominante e está relacionado com a inibição dos neurônios14 catecolaminérgicos na região dos núcleos reticulares15 no tronco cerebral16. Receptores imidazolínicos, situados ventro-lateralmente na medula13 oblonga também estariam envolvidos neste efeito.
A elevada lipossolubilidade da clonidina (coeficiente de partição octanol/água de 114:1) explica a sua distribuição predominante no sistema nervoso17. Após 10 minutos de infusão intravenosa de 300 mcg de clonidina a cinco voluntários do sexo masculino, os níveis plasmáticos de clonidina mostraram uma fase de distribuição inicial rápida seguido de uma fase de eliminação mais lenta durante 24 horas.
A meia-vida de eliminação está entre 9 a 12 horas. Cerca de 50% são metabolizados para componentes inativos no fígado18 e o restante é eliminado inalterado pelos rins19. O desempenho insuficiente da função renal20 pode alterar estes valores, prolongando a retenção do fármaco21.
O efeito analgésico3 inicia-se 15 minutos após a aplicação intratecal, epidural1, intramuscular ou intravenosa.
A analgesia é potente e de curta duração (4 a 6 horas) para as aplicações intratecais e epidurais; é menos consistente nas aplicações intramuscular e intravenosa.
Apenas a administração intratecal segue um perfil dose-dependente: o tempo para o início da analgesia pode ser reduzido para 3 minutos e a duração prolongada para até 14 horas em função da dose.
QUANDO NÃO DEVO USAR ESTE MEDICAMENTO?
Este medicamento é contraindicado em pacientes com histórico de reações de hipersensibilidade à clonidina, bem como a outros componentes do medicamento.
A administração epidural1 é contraindicada na presença de infecção22 no local da injeção23, em pacientes sob terapia anticoagulante24 e naqueles com diátese hemorrágica25.
A administração de Clonidin® acima de C4 é contraindicada uma vez que não existem dados de segurança suficientes para este uso.
O medicamento também é contraindicado em caso de:
- Diferentes formas de agitação e perturbações do coração26, como por exemplo, "síndrome de Sinusknoten" ou bloqueio átrio-ventricular II e III
- Pacientes portadores de doença no nó sinusal27
- Frequência cardíaca abaixo de 50 batidas por minuto
- Período de amamentação28
- Depressão
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO?
As indicações para o produto não preveem tratamento prolongado.
O uso prolongado (6 ou mais dias) requer cuidados especiais: o tratamento não deve ser interrompido abruptamente; pode haver efeito rebote, com desestabilização do quadro hemodinâmico. Em portadores de hipertensão29, a interrupção brusca pode levar as crises hipertensivas graves, de consequências imprevisíveis.
O fármaco21 deve ser usado com cautela em portadores de doenças vasculares11 cerebrais, nos casos de insuficiência30 coronária ou de infarto do miocárdio31 recente, nos portadores de distúrbios vasculares11 periféricos oclusivos tais como a doença de Raynaud32 e em casos de histórico depressivo.
Durante o tratamento com Clonidin®, a frequência cardíaca não deve estar abaixo de 56 batimentos por minuto. Os portadores de lentes de contato devem ocasionalmente observar a diminuição do fluxo lacrimal.
Gerais
Efeitos Cardíacos: a clonidina epidural1 causa frequentemente diminuição na frequência cardíaca. A bradicardia33 sintomática34 pode ser tratada com atropina. Raramente foi relatado bloqueio atrioventricular maior do que o do I Grau. O fármaco21 não altera a resposta hemodinâmica2 ao exercício, mas pode mascarar o aumento do batimento cardíaco associado com a hipovolemia35.
Depressão Respiratória e Sedação36: a administração de clonidina pode resultar em sedação36 através da ativação dos alfa-adrenoceptores no tronco cerebral16. Altas doses de clonidina causam sedação36 e anormalidades ventilatórias normalmente moderadas. Pode haver desenvolvimento de tolerância a esses efeitos com a administração crônica. Esses efeitos têm sido relatados com doses em bolus37, que são significativamente maiores que a velocidade de infusão recomendada para o tratamento da dor no câncer38.
Depressão: tem ocorrido depressão em pequena porcentagem de pacientes tratados com clonidina oral ou transdérmica. A depressão ocorre normalmente em pacientes com câncer38 e pode ser exacerbada pelo tratamento com a clonidina. Os pacientes, especialmente aqueles com história conhecida de desordens afetivas, devem ser monitorados em relação aos sinais39 e sintomas40 de depressão.
Dor de Origem Visceral ou Somática: em pesquisas clínicas, nas doses testadas, a clonidina mostrou-se mais efetiva na dor neuropática41 bem localizada, caracterizada como de natureza elétrica, de queimação, pontada, localizada nos dermátomos42 ou distribuida ao longo do nervo periférico. O medicamento pode ser menos efetivo, ou possivelmente inefetivo no tratamento da dor difusa, pouco localizada ou de origem visceral.
Hipotensão43
Pode ocorrer grave hipotensão43 após a administração de Clonidin® e, portanto, cuidados devem ser tomados com todos os pacientes. O produto não é recomendado na maioria dos pacientes com doença cardiovascular grave ou para aqueles que são hemodinamicamente instáveis. O benefício de sua administração nesses pacientes deve ser cuidadosamente calculado contra os potenciais riscos resultantes da hipotensão43.
Os sinais vitais44 devem ser frequentemente monitorados, especialmente durante os primeiros dias da terapia epidural1 com Clonidin®. Quando a clonidina é infundida nos segmentos espinhais torácicos superiores, podem ser verificadas quedas mais pronunciadas na pressão sanguínea.
A clonidina diminui o estímulo simpático45 do sistema nervoso central46 resultando em diminuição da resistência periférica47, resistência vascular48 renal20, frequência cardíaca e pressão sanguínea. Contudo, na ausência de hipotensão43 profunda, o fluxo arterial renal20 e a taxa de filtração glomerular permanecem essencialmente inalterados.
Os relatos publicados sobre o uso de clonidina epidural1 na analgesia intra e pós-operatória, também demonstram hipotensão43 consistente e marcante como resposta ao fármaco21. Pode ocorrer hipotensão43 grave mesmo se houver pré-tratamento com fluído intravenoso.
Abstinência
A interrupção repentina do tratamento com clonidina, independente da via de administração, tem resultado, em alguns casos, em sintomas40 como nervosismo, agitação, cefaleia49 e tremor, acompanhado ou seguido por uma rápida elevação na pressão sanguínea. A probabilidade de tais reações parece ser maior com o uso de doses mais altas ou com o tratamento concomitante com beta-bloqueadores. Nestas situações devem ser tomados cuidados especiais. Após retirada abrupta de clonidina foram relatados casos raros de encefalopatia hipertensiva50, acidentes cerebrovasculares e óbito51. Pacientes com histórico de hipertensão29 e/ou outras condições cardiovasculares subjacentes podem estar sob risco das consequências da descontinuação abrupta da clonidina.
O monitoramento cuidadoso do funcionamento da bomba de infusão e a inspeção52 do cateter, verificando a existência de obstrução ou deslocamento, pode reduzir o risco de supressão abrupta inadvertida de clonidina epidural1. Os pacientes devem comunicar imediatamente seu médico se houver interrupção inadvertida, por qualquer razão, da administração de clonidina. Os pacientes também devem ser instruídos para não descontinuar a terapia sem consultar o médico.
Quando houver descontinuação da terapia epidural1 com clonidina, o médico deve reduzir a dose gradualmente por 2 a 4 dias para evitar os sintomas40 de abstinência.
Um excessivo aumento na pressão arterial53, após a descontinuação da clonidina epidural1, pode ser tratado com clonidina ou fentolamina intravenosa. Se a terapia tiver que ser descontinuada em pacientes sob tratamento concomitante com clonidina e beta-bloqueadores, o beta-bloqueador deve ser interrompido vários dias antes da descontinuação gradual da clonidina epidural1.
Infecções54
As infecções54 relacionadas com os cateteres epidurais implantados são um sério risco. A ocorrência de febre55 em paciente que esteja recebendo clonidina epidural1 deve incluir a possibilidade de infecção22 relacionada com o cateter, tal como a meningite56 ou abcesso epidural1.
Informação para pacientes57
Os pacientes devem ser instruídos sobre os riscos da hipertensão29 rebote e avisados para não descontinuar a clonidina, exceto sob a supervisão de um médico. Os pacientes devem notificar o seu médico imediatamente se o uso de clonidina for inadvertidamente interrompido por qualquer razão. Os pacientes que se envolvem em atividades potencialmente perigosas, tais como a utilização de máquinas ou de condução, devem ser aconselhados sobre os efeitos sedativo e hipotensor potenciais da clonidina epidural1. Eles também devem ser informados de que os efeitos sedativos podem ser aumentados por fármacos depressores do SNC10 como o álcool e barbitúricos, e que os efeitos hipotensores podem ser aumentados por opiaceos.
Carcinogenicidade, Mutagenicidade e Diminuição da Fertilidade
A clonidina não mostrou potencial carcinogênico em estudo com animais. A fertilidade de ratos machos ou fêmeas não foi afetada pelas doses de cloridrato de clonidina de 150 mcg/kg, ou cerca de 0,5 vez a dose máxima humana recomendada. A
fertilidade de ratos fêmeas, contudo, pareceu ser afetada em outra experiência com níveis de doses orais de 500 a 2000 mcg/kg, ou 2 a 7 vezes a dose máxima humana recomendada.
Uso em Analgesia Pós-Operatória ou Obstétrica
Clonidin® não é recomendado para o controle da analgesia do parto, pós-parto ou peri-cirúrgica. O risco de instabilidade hemodinâmica2, especialmente hipotensão43 e bradicardia33, após clonidina epidural1, pode ser inaceitável nesses pacientes.
Gravidez58
Categoria de Risco C – Não há estudos adequados em mulheres. Em experiências animais ocorreram alguns efeitos colaterais5 no feto59, mas o benefício do produto pode justificar o risco potencial durante a gravidez58.
Os estudos de reprodução60 em coelhos, com doses de cloridrato de clonidina em concentrações de até a dose máxima humana recomendada, não demonstraram evidência de potencial teratogênico61 ou embriotóxico. Em ratos, contudo, doses baixas de até 1/3 da dose máxima humana recomendada, foram associadas com reabsorções aumentadas, em um estudo no qual as ratas foram tratadas continuamente dois meses antes do acasalamento.
A clonidina atravessa rapidamente a placenta e suas concentrações são similares no plasma62 materno e no do cordão umbilical63; as concentrações do fluído amniótico podem ser 4 vezes àquelas encontradas no soro64. Não existem estudos adequados e bem controlados em mulheres grávidas durante o início da gestação, quando ocorre a formação dos órgãos. Os estudos utilizando clonidina epidural1 durante o parto, não têm demonstrado reações adversas aparentes na criança no momento do parto. Contudo, esses estudos não monitoram os efeitos hemodinâmicos na criança, nos dias após o parto. O cloridrato de clonidina injetável deve ser usado durante a gravidez58 somente se os potenciais benefícios justificarem o potencial risco ao feto59.
Parto e trabalho de parto
Não existem estudos clínicos adequadamente controlados avaliando a segurança, eficácia e dose da clonidina em procedimentos obstétricos. O uso de clonidina como analgésico3 durante o parto e trabalho de parto não é indicado, pelo fato de a perfusão materna da placenta ser criticamente dependente da pressão sanguínea.
Amamentação28
As concentrações de clonidina no leite humano são de aproximadamente duas vezes àquelas encontradas no plasma62 materno. Deve haver muito cuidado ao se administrar clonidina a mulheres em fase de amamentação28. Deve-se tomar a decisão de descontinuar a amamentação28 ou a administração de clonidina, em função do potencial para a ocorrência de reações adversas nas crianças lactentes65.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Uso pediátrico
A segurança e a eficácia da clonidina, nesta indicação e população clínica é limitada.
Efeitos na habilidade de dirigir e usar máquinas
Durante o tratamento com Clonidin® o paciente não deve dirigir veículos, operar máquinas ou trabalhar em serviços contínuos, pois a sua habilidade e atenção podem estar prejudicadas.
Interações Medicamentosas
A clonidina potencializa os efeitos depressivos do SNC10 do álcool, barbitúricos ou outros fármacos sedativos. Os analgésicos66 narcóticos podem potencializar os efeitos hipotensivos da clonidina.
Não deve ser usada com antidepressivos tricíclicos, agentes bloqueadores beta-adrenérgicos12. Os primeiros podem antagonizar os efeitos hipotensivos da clonidina, sendo que seus efeitos sobre a ação analgésica da clonidina são desconhecidos. Os agentes beta-bloqueadores podem contribuir com a hipotensão43 aguda e também podem exacerbar a resposta hipertensiva verificada com a supressão da clonidina. Também, devido ao potencial para efeitos aditivos como a bradicardia33 e o bloqueio AV, cuidados devem ser tomados em pacientes recebendo clonidina que estejam sob tratamento com agentes que afetem a função do nó sinusal27 ou a condução AV nodal, isto é, digitálicos, bloqueadores do canal de cálcio e beta-bloqueadores.
Existe um relato de caso de paciente com delírio67 agudo68 associado com o uso simultâneo de flufenazina e clonidina oral. Os sintomas40 cessaram quando houve a suspensão da clonidina e houve recorrência69 quando a clonidina foi reinstituída.
A clonidina epidural1 pode prolongar a duração dos efeitos farmacológicos dos anestésicos locais epidurais, incluindo tanto o bloqueio sensitivo quanto o motor.
Nota: O medicamento é restrito ao uso hospitalar e sua administração somente deve ser feita por profissionais familiarizados com os procedimentos anestésicos.
Informe ao seu médico ou cirurgião-dentista se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde70.
ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO?
Cuidados de conservação
Conservar o produto em temperatura ambiente, entre 15 e 30°C, protegido da luz. O medicamento não contém conservantes.
O prazo de validade é de 24 meses a partir da data de fabricação impressa na embalagem.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
Solução límpida, incolor, praticamente isenta de partículas.
Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
COMO DEVO USAR ESTE MEDICAMENTO?
As necessidades posológicas são variáveis e devem ser individualizadas conforme a indicação e perfil clínico do paciente.
Na medicação pré-anestésica: as aplicações mais aconselháveis são IM profunda, IV lenta (7 a 10 minutos) ou diluída, por gotejamento intravenoso. clonidina é compatível com cloreto de sódio 0,9% para diluição. Em procedimentos cirúrgicos de longa duração, dose adicional de 150 mcg ou manutenção por gotejamento intravenoso pode ser necessário.
Na analgesia pós-operatória: a dose inicial recomendada de Clonidin® para infusão epidural1 contínua é de 30 mcg/h. Embora a dose possa ser titulada para mais ou menos, dependendo do alívio da dor e ocorrência de reações adversas, a experiência com doses acima de 40 mcg/h é limitada. É essencial estar familiarizado com os dispositivos de infusão epidural1 contínua, e os pacientes devem ser cuidadosamente monitorados nos primeiros dias, avaliando sua resposta.
A dose usual está entre 2-4 mcg/kg por via epidural1 e 0,5-1 mcg/kg por via intratecal produz analgesia de curta duração (4 a 6 horas) e deverá ser repetida de acordo com as respostas do paciente. Na aplicação intratecal, a analgesia é de duração dose dependente.
Em associação com outros fármacos: a posologia deve ser individualizada para cada caso. Nas associações com anestésicos locais (lidocaína, bupivacaína e mepivacaína) o procedimento e a dose mais usual consiste na adição de 150 mcg de Clonidin® solução injetável à dose escolhida do anestésico local, antes da aplicação.
INSTRUÇÕES
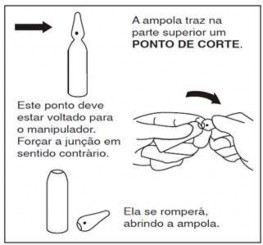
IMPORTANTE: Ampola com ponto de corte
Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento do seu médico.
O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO?
Uma vez que este medicamento é administrado por um profissional da saúde70 em ambiente hospitalar não deverá ocorrer esquecimento do seu uso.
Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico, ou cirurgião-dentista.
QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR?
Reação muito comum (>1/10): Hipotensão43, hipotensão43 ortostática, náuseas71, xerostomia72, astenia73, confusão, tontura74, sonolência
Reação comum (>1/100 e <1/10): Bradiarritmia, precordialgia, diminuição ou aumento do débito cardíaco75, taquicardia76, sudorese77, obstipação78, zumbido, agitação, nervosismo, alucinações79, disfunção erétil, diminuição da atividade sexual, perda da libido80, fadiga81
Reação incomum (>1/1.000 e <1/100): Palpitação82, alopecia83, erupções na pele84, Prurido85, rash86, urticaria87, ginecomastia88, pseudo-obstrução intestinal crônica, parotidite89, cefaléia49, insônia, depressão, dificuldade de micção90, noctúria, retenção urinária91, angioedema92, mal-estar.
Reação rara (>1/10.000 e <1.000): Bloqueio atrioventricular, bradicardia33 atrioventricular nó sinoatrial93, insuficiência cardíaca congestiva94, fenômeno de Raynaud95, bradicardia33 sinusal, ritmo nodal sinusal, síncope96, trombocitopenia97, hepatite98, acidente vascular cerebral99, visão100 embaçada, sensação de queimação nos olhos101, olhos101 ressecados, delírio67, distúrbios do sonho, inquietação, ressecamento de mucosa102 nasal, acidente vascular cerebral99 após abrupta interrupção do tratamento com clonidina, morte após abrupta interrupção do tratamento com clonidina.
Relatos de casos: Prolongamento do intervalo QT, hipertensão29 rebote, obstrução gastrointestinal, aumento da pressão intracraniana, episódios de apneia103, abuso do fármaco21, arritmias104 ventriculares sérias após abruptas interrupções do tratamento com clonidina.
Sem informação detalhada: Diminuição da pressão arterial diastólica105 e sistólica, lúpus106 eritematoso107 sistêmico108, desordens psicóticas agudas (exacerbação de tiques ou alucinações79 visuais e auditivas), depressão respiratória, depressão respiratória, retirada da droga: o aumento agudo68 da pressão arterial53 (crise hipertensiva) após a interrupção abrupta da terapêutica109 clonidina é bem documentado, síndrome110 de abstinência aguda da clonidina (dor de cabeça111, tonturas112, transpiração113, palpitações114, ansiedade, insônia, tremores, dispneia115 e compressão do peito116, aumento da excreção de adrenalina117 e noradrenalina118 urinária (catecolaminas) e aumento da atividade da renina plasmática), eventos adversos neurológicos associados com a privação de clonidina (cefaleia49), eventos adversos psiquiátricos associados com a privação de clonidina (ansiedade, suor, palpitações114 e tremores).
Informe ao seu médico, cirurgião-dentista ou farmacêutico o aparecimento de reações indesejáveis pelo uso do medicamento. Informe também à empresa através do seu serviço de atendimento.
O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO?
Pode haver desenvolvimento de hipertensão29 precoce seguida de hipotensão43, bradicardia33, depressão respiratória, hipotermia119, sonolência, reflexos diminuídos ou ausentes, irritabilidade e miose120. Com doses orais excessivas foram relatadas, alterações na condução cardíaca reversível ou arritmias104, apneia103, coma121 e convulsões.
Inexiste antídoto122 específico para a superdose de clonidina. A terapia de suporte pode incluir sulfato de atropina para a bradicardia33, fluídos intravenosos e/ou agentes vasopressores para a hipotensão43. A hipertensão29 associada com a superdose tem sido tratada com furosemida intravenosa, diazóxido ou agentes alfa-bloqueadores como a fentolamina. A naloxona pode ser um auxiliar no tratamento da hipotensão43 e/ou coma121 induzida pela clonidina; a pressão arterial53 deve ser monitorada pois a administração de naloxona pode resultar ocasionalmente em hipertensão29 paradoxal123. A administração de tolazolina forneceu resultados inconsistentes e não é recomendada como terapia de primeira linha. A diálise124 não parece aumentar significativamente a eliminação de clonidina.
A maior superdose relatada até agora envolveu um paciente branco de 28 anos de idade, que ingeriu 100 mg de cloridrato de clonidina em pó. Este paciente desenvolveu hipertensão29 seguida de hipotensão43, bradicardia33, apneia103, alucinações79, semicoma e contrações ventriculares prematuras. O paciente recuperou-se completamente após tratamento intensivo.
Em casos de superdose observa-se uma baixa considerável da pressão arterial53 (sem colapso125) acompanhada de uma sonolência profunda, podendo levar a um estado semicomatoso com hipotermia119 e bradicardia33. Este estado é revertido espontaneamente em 24 a 48 horas.
A normalização dos valores tensionais pode ser obtida rapidamente por administração de agentes alfa-inibidores.
Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
USO RESTRITO A HOSPITAIS
MS nº 1.0298.0193
Farm. Resp.: Dr. José Carlos Módolo - CRF-SP nº 10.446
Registrado por:
CRISTÁLIA - Produtos Químicos Farmacêuticos Ltda.
Rodovia Itapira-Lindóia, km 14 – Itapira / SP
CNPJ N.º 44.734.671/0001-51
Indústria Brasileira
Fabricado por:
CRISTÁLIA - Produtos Químicos Farmacêuticos Ltda.
Av. Nossa Senhora da Assunção, 574 - Butantã - São Paulo - SP
CNPJ nº 44.734.671/0008-28
SAC 0800 7011918