Rinvoq (Bula do profissional de saúde)
ABBVIE FARMACÊUTICA LTDA.
IDENTIFICAÇÃO DO MEDICAMENTO
Rinvoq®
upadacitinibe
Comprimido 15 mg
FORMA FARMACÊUTICA E APRESENTAÇÃO:
Comprimido revestido de liberação prolongada
Embalagem contendo 30 comprimidos
USO ORAL
USO ADULTO
COMPOSIÇÃO:
Cada comprimido de Rinvoq® contém:
| upadacitinibe (equivalente a 15,40 mg de upadacitinibe hemi-hidratado) | 15 mg |
| excipiente q.s.p. | 1 comprimido |
Excipientes: celulose microcristalina, hipromelose, manitol, ácido tartárico, dióxido de silício, estearato de magnésio e Opadry II (álcool polivinílico, macrogol 3350, talco, dióxido de titânio, óxido de ferro preto e óxido de ferro vermelho).
INFORMAÇÕES TÉCNICAS AOS PROFISSIONAIS DE SAÚDE1
INDICAÇÕES
Rinvoq® é indicado para o tratamento de pacientes adultos com artrite reumatoide2 ativa moderada a grave que não responderam adequadamente ou que foram intolerantes a uma ou mais drogas antirreumáticas modificadoras de doença (DMARD).
Rinvoq® pode ser utilizado como monoterapia ou em combinação com metotrexato ou outras drogas antirreumáticas sintéticas convencionais modificadoras do curso da doença (csDMARDs).
RESULTADOS DE EFICÁCIA
A eficácia e segurança de Rinvoq® 15 mg uma vez ao dia foram avaliadas em cinco estudos de Fase 3, multicêntricos, randomizados, duplo-cegos em pacientes com artrite reumatoide2 ativa moderada a grave e que atendiam aos critérios de classificação ACR/EULAR 2010 (vide Tabela 1). Eram elegíveis a participar pacientes com idade a partir de 18 anos. A presença de no mínimo 6 articulações3 dolorosas e 6 articulações3 edemaciadas4 e evidência de inflamação5 sistêmica com base na elevação da proteína C reativa de alta sensibilidade (hsPCR) foram exigidas na visita basal. Quatro estudos incluíram extensões a longo prazo por até 5 anos e um estudo (SELECT-COMPARE) incluiu uma extensão a longo prazo por até 10 anos.
Tabela 1. Resumo dos estudos clínicos
|
Nome do estudo |
População (n) |
Grupos de tratamento |
Principais medidas de resultado |
|
SELECT- EARLY |
Não tratados anteriormente com MTXa (947) |
Monoterapia |
Desfecho primário:
|
|
Principais desfechos secundários:
|
|||
|
SELECT- MONOTHERAPY |
MTX-IRb (648) |
Monoterapia |
Desfecho primário:
|
|
Principais desfechos secundários:
|
|||
|
SELECT- NEXT |
csDMARD -IRc (661) |
Em terapia de base com csDMARDs |
Desfecho primário:
|
|
Principais desfechos secundários:
|
|||
|
SELECT- COMPARE |
MTX-IRd (1629) |
|
Desfecho primário:
|
|
|
|
Com terapia de base com MTX |
Principais desfechos secundários:
|
|
SELECT- BEYOND |
bDMARD-IRe (499) |
Em terapia de base com csDMARDs |
Desfecho primário:
|
|
Principal desfecho secundário:
|
Abreviações: ACR20 (ou 50) = melhora de ≥20% (ou ≥50%) no American College of Rheumatology, bDMARD = droga antirreumática biológica modificadora do curso da doença; CR = Resposta clínica, PCR6 = Proteína C-reativa, DAS28 = Índice de atividade da doença em 28 articulações3, mTSS = Índice total de Sharp modificado, csDMARD = droga antirreumática modificadora do curso da doença convencional sintética, HAQ-DI = Questionário de avaliação de saúde1 - Índice de Incapacidade, IR = respondedor inadequado, MTX = metotrexato, SF-36= versão curta do questionário de coleta de dados de saúde1 – resumo do componente físico, FACIT-F= escala de avaliação funcional de terapia de doença crônica-fadiga8
a Pacientes não haviam sido tratados anteriormente com MTX ou receberam não mais que 3 doses semanais de MTX
b Pacientes que apresentaram resposta inadequada a MTX
c Pacientes com resposta inadequada a csDMARDs; pacientes com exposição anterior a no máximo uma bDMARD foram elegíveis (até 20% do número total de pacientes), caso tivessem exposição limitada (< 3 meses) ou tivessem que descontinuar a bDMARD devido à intolerância
d Pacientes com resposta inadequada a MTX; pacientes com exposição anterior a no máximo uma bDMARD (exceto adalimumabe) foram elegíveis (até 20% do número total de pacientes em estudo) caso tivessem exposição limitada (< 3 meses) ou tivessem que descontinuar a bDMARD devido à intolerância
e Pacientes com resposta inadequada ou intolerância a no mínimo uma bDMARD
Resposta Clínica
Remissão e baixa atividade da doença
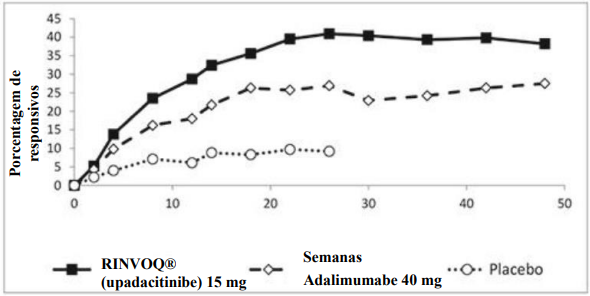
Em todos os estudos, uma proporção significativamente maior de pacientes tratados com Rinvoq® 15 mg atingiu tanto baixa atividade da doença (DAS28-PCR6 ≤ 3,2) como remissão clínica (DAS28-PCR6 < 2,6) em comparação ao placebo7, MTX ou adalimumabe (Tabela 2). Em comparação a adalimumabe, foram atingidas respostas significativamente maiores logo na Semana 8 e mantidas até a Semana 48 (Figura 1). Também foram observadas respostas significativamente maiores para outros resultados de atividade da doença, incluindo CDAI ≤ 2,8, SDAI ≤ 3,3 e remissão Booleana. De modo geral, a baixa atividade da doença e as taxas de remissão clínica foram consistentes entre as populações de pacientes com ou sem MTX.
Figura 1. Remissão Clínica (DAS28-PCR6) ao longo do tempo no estudo SELECT-COMPARE
Resposta ACR
Em todos os estudos, mais pacientes tratados com Rinvoq® 15 mg atingiram signitivamente respostas ACR20, ACR50 e ACR70 na semana 12 em comparação ao placebo7 ou MTX, exceto para ACR70 no estudo SELECT-BEYOND (Tabela 2, Figura 2). O tempo até o início da eficácia foi rápido nas diferentes medidas, com respostas significativamente mais elevadas observadas logo na semana 1 para ACR20. Foram observadas taxas de resposta duradouras (com ou sem MTX), com respostas ACR20/50/70 mantidas por pelo menos 1 ano.
O tratamento com Rinvoq® 15 mg, isoladamente ou em combinação com csDMARDs, resultou em melhoras significativas nos componentes individuais do ACR, incluindo contagens de articulações3 dolorosas e edemaciadas4, avaliações globais do paciente e do médico, HAQ-DI, avaliação de dor e hsPCR, em comparação com placebo7 ou à monoterapia com MTX (Tabela 3).
No estudo SELECT-COMPARE, uma proporção significativamente mais elevada de pacientes tratados com Rinvoq® 15 mg atingiu ACR20/50/70 nas Semanas 12 até semana 48 em comparação ao adalimumabe. Além disso, foram observadas maiores melhorias nos os componentes individuais do ACR (Tabela 3).
Figura 2. Porcentagem de pacientes que atingiram ACR20 no estudo SELECT-COMPARE
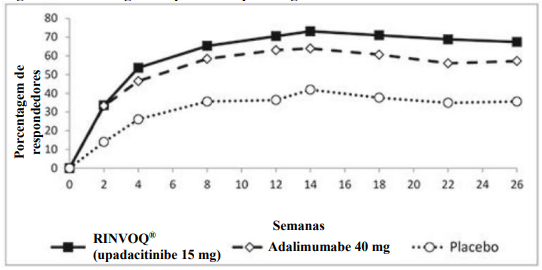
Tabela 2. Resposta e Remissão
|
Estudo |
SELECT EARLY |
SELECT MONO MTX-IR |
SELECT NEXT csDMARD-IR |
SELECT COMPARE MTX-IR |
SELECT BEYOND bDMARD-IR |
||||||
|
|
MTX |
UPA 15 mg |
MTX |
UPA 15 mg |
PBO |
UPA 15 mg |
PBO |
UPA 15 mg |
ADA 40 mg |
PBO |
UPA 15 mg |
|
N |
314 |
317 |
216 |
217 |
221 |
221 |
651 |
651 |
327 |
169 |
164 |
|
Semana |
|||||||||||
|
LDA DAS28-PCR6 ≤ 3,2 (% de pacientes) |
|||||||||||
|
12a/14b |
28 |
53e |
19 |
45e |
17 |
48e |
14 |
45e,h |
29 |
14 |
43e |
|
24c/26d |
32 |
60e |
|
|
|
|
18 |
55e,h |
39 |
|
|
|
48 |
39 |
59e |
|
|
|
|
|
50h |
35 |
|
|
|
CR DAS28-PCR6 < 2,6 (% de pacientes) |
|||||||||||
|
12a/14b |
14 |
36e |
8 |
28e |
10 |
31e |
6 |
29e,h |
18 |
9 |
29e |
|
24c/26d |
18 |
48e |
|
|
|
|
9 |
41e,h |
27 |
|
|
|
48 |
29 |
49e |
|
|
|
|
|
38i |
28 |
|
|
|
ACR20 (% des pacientes) |
|||||||||||
|
12a/14b |
54 |
76e |
41 |
68e |
36 |
64e |
36 |
71e,j |
63 |
28 |
65e |
|
24c/26d |
59 |
79e |
|
|
|
|
36 |
67e,i |
57 |
|
|
|
48 |
57 |
74e |
|
|
|
|
|
65i |
54 |
|
|
|
ACR50 (% de pacientes) |
|||||||||||
|
12a/14b |
28 |
52e |
15 |
42e |
15 |
38e |
15 |
45e,h |
29 |
12 |
34e |
|
24c/26d |
33 |
60e |
|
|
|
|
21 |
54e,h |
42 |
|
|
|
48 |
43 |
63e |
|
|
|
|
|
49i |
40 |
|
|
|
ACR70 (% de pacientes) |
|||||||||||
|
12a/14b |
14 |
32e |
3 |
23e |
6 |
21e |
5 |
25e,h |
13 |
7 |
12 |
|
24c/26d |
18 |
44e |
|
|
|
|
10 |
35e,h |
23 |
|
|
|
48 |
29 |
51e |
|
|
|
|
|
36h |
23 |
|
|
|
SDAI ≤ 3,3 (% de pacientes) |
|||||||||||
|
12a/14b |
6 |
16e |
1 |
14e |
3 |
10f |
3 |
12e,j |
7 |
5 |
9 |
|
24c/26d |
9 |
28e |
|
|
|
|
5 |
24e,h |
14 |
|
|
|
48 |
16 |
32e |
|
|
|
|
|
25i |
17 |
|
|
|
CDAI ≤ 2,8 (% de pacientes) |
|||||||||||
|
12a/14b |
6 |
16e |
1 |
13e |
3 |
9f |
3 |
13e,i |
8 |
5 |
8 |
|
24c/26d |
11 |
28e |
|
|
|
|
6 |
23e,h |
14 |
|
|
|
48 |
17 |
32e |
|
|
|
|
|
25i |
17 |
|
|
|
Remissão Booleana (% de pacientes) |
|||||||||||
|
12a/14b |
6 |
13f |
1 |
9e |
4 |
10f |
2 |
10e,i |
4 |
2 |
7g |
|
24c/26d |
7 |
24e |
|
|
|
|
4 |
18e,h |
10 |
|
|
|
48 |
13 |
28e |
|
|
|
|
|
21j |
15 |
|
|
Abreviações: ACR20 (ou 50 ou 70) = melhora de ≥ 20% (ou ≥ 50% ou ≥ 70%) do American College of Rheumatology; ADA = adalimumabe; bDMARD = droga antirreumática biológica modificadora do curso da doença; CDAI = Índice clínico de atividade da doença; CR = Remissão clínica; csDMARDs = droga antirreumática modificadora do curso da doença convencional sintética; IR = respondedor inadequado; PCR6 = proteína C-reativa; DAS28 = Índice de atividade da doença em 28 articulações3; LDA = Baixa atividade da doença; MTX = metotrexato; PBO = placebo7; SDAI = Índice simplificado de atividade da doença; UPA= upadacitinibe
a SELECT-NEXT, SELECT-EARLY, SELECT-COMPARE, SELECT-BEYOND
b SELECT-MONOTHERAPY
c SELECT-EARLY
d SELECT-COMPARE
e p≥0,001upadacitinibe vs placebo7 ou em comparação com MTX
f p≥0,01 upadacitinibe vs placebo7 ou em comparação com MTX
g p≥0,05 upadacitinibe vs placebo7 ou em comparação com MTX
h p≥0,001 upadacitinibe vs adalimumabe
i p≥0,01 upadacitinibe vs adalimumabe
j p≥0,05 upadacitinibe vs adalimumabe
Tabela 3. Componentes de Resposta ACR (alteração média desde o valor basal a
|
Estudo |
SELECT EARLY |
SELECT MONO MTX-IR |
SELECT NEXT csDMARD- IR |
SELECT COMPARE MTX-IR |
SELECT BEYOND bDMARD- IR |
||||||
|
|
MTX |
UPA 15 mg |
MTX |
UPA 15 mg |
PBO |
UPA 15mg |
PBO |
UPA 15 mg |
ADA 40 mg |
PBO |
UPA 15 mg |
|
N |
314 |
317 |
216 |
217 |
221 |
221 |
651 |
651 |
327 |
169 |
164 |
|
Semana |
|
||||||||||
|
Número de articulações3 dolorosas (0-68) |
|||||||||||
|
12b/14c |
-13 |
-17h |
-11 |
-15h |
-8 |
-14h |
-10 |
-16h,k |
-14 |
-8 |
-16h |
|
24d/26e |
-16 |
-19h |
|
|
|
|
-9 |
-18h,j |
-15 |
|
|
|
Número de articulações3 edemaciadas4 (0-66) |
|||||||||||
|
12b/14c |
-10 |
-12h |
-8 |
-11h |
-6 |
-9h |
-7 |
-11h |
-10 |
-6 |
-11h |
|
24d/26e |
-12 |
-14h |
|
|
|
|
-6 |
-12h |
-11 |
|
|
|
Dorf |
|||||||||||
|
12b/14c |
-25 |
-36h |
-14 |
-26h |
-10 |
-30h |
-15 |
-32h,i |
-25 |
-10 |
-26h |
|
24d/26e |
-28 |
-40h |
|
|
|
|
-19 |
-37h,j |
-32 |
|
|
|
Avaliação Global do Pacientef |
|||||||||||
|
12b/14c |
-25 |
-35h |
-11 |
-23h |
-10 |
-30h |
-15 |
-30h,i |
-24 |
-10 |
-26h |
|
24d/26e |
-28 |
-39h |
|
|
|
|
-18 |
-36h,j |
-30 |
|
|
|
Índice de Incapacidade (HAQ-DI)g |
|||||||||||
|
12b/14c |
-0,5 |
-0,8h |
-0,3 |
-0,7h |
-0,3 |
-0,6h |
-0,3 |
-0,6h,j |
-0,5 |
-0,2 |
-0,4h |
|
24d/26e |
-0,6 |
-0,9h |
|
|
|
|
-0,3 |
-0,7h,j |
-0,6 |
|
|
|
Avaliação Global do médicof |
|||||||||||
|
12b/14c |
-35 |
-46h |
-26 |
-40h |
-23 |
-38h |
-25 |
-39h |
-36 |
-26 |
-39h |
|
24d/26e |
-45 |
-50h |
|
|
|
|
-27 |
-45h,j |
-41 |
|
|
|
hsPCR (mg/L) |
|||||||||||
|
12b/14c |
-10,6 |
-17,5h |
-1,1 |
-10,2h |
-0,4 |
-10,1h |
-1,7 |
-12,5h,j |
-9,2 |
-1,1 |
-11,0h |
|
24d/26e |
-11,6 |
-18,4h |
|
|
|
|
-1,5 |
-13,5h,j |
-10,3 |
|
|
Abreviações: ACR = American College of Rheumatology; ADA = adalimumabe; bDMARD = droga antirreumática biológica modificadora do curso da doença; csDMARDs = droga antirreumática modificadora do curso da doença convencional sintética; PCR6 = proteína C-reativa; HAQ-DI = Questionário de avaliação de saúde1 - Índice de incapacidade; IR = respondedor inadequado; MTX = metotrexato; PBO = placebo7; UPA = upadacitinibe
a Os dados ilustrados são a média
b SELECT-NEXT, SELECT-EARLY, SELECT-COMPARE, SELECT-BEYOND
c SELECT-MONOTHERAPY
d SELECT-EARLY
e SELECT-COMPARE
f Escala visual analógica : 0 = melhor/nenhuma dor , 100 = pior
g Questionário de Avaliação de Saúde1 - Índice de Incapacidade: 0=melhor (nehuma dificuldade), 3=pior (incapaz de realiza-la); 20 questões; 8 domínios: vestir-se e arrumar-se, levantar-se, comer, caminhar, higiene, alcançar, agarrar e atividades.
h p≤0,001 upadacitinibe vs placebo7 ou em comparação com MTX
i p≤0,001 upadacitinibe vs adalimumabe
j p≤0,01 upadacitinibe vs adalimumabe
k p≤0,05 upadacitinibe vs adalimumabe
Resposta radiográfica
A inibição de progressão da lesão9 articular estrutural foi avaliada com o uso do índice total de Sharp modificado (mTSS) e seus componentes, escore de erosão e escore de estreitamento do espaço articular nas semanas 26 e 48 (SELECT-COMPARE) e na semana 24 (SELECT-EARLY). O tratamento com Rinvoq® 15 mg resultou em inibição significativamente mais elevada da progressão da lesão9 articular estrutural em comparação ao placebo7 nas semanas 26 e 48 no estudo SELECT-COMPARE e como monoterapia em comparação ao MTX na semana 24 no estudo SELECT-EARLY (Tabela 4). Também foram atingidos resultados estatisticamente significativos para as pontuações de erosão e estreitamento de espaço articular. A proporção de pacientes sem progressão radiográfica (alteração de mTSS ≤ 0) foi significativamente mais elevada com Rinvoq® 15 mg em comparação ao placebo7 nas semanas 26 e 48 (SELECT- COMPARE) e em comparação ao MTX na semana 24 (SELECT-EARLY).
Tabela 4. Alterações Radiográficas
|
Estudo |
SELECT EARLY |
SELECT COMPARE MTX-IR |
|||
|
Grupo de tratamento |
MTX |
UPA 15 mg |
PBOa |
UPA 15 mg |
ADA 40 mg |
|
Escore Sharp total modificado, alteração média desde o valor basal |
|||||
|
Semana 24b/26c |
0,7 |
0,1f |
0,9 |
0,2e |
0,1 |
|
Semana 48 |
|
|
1,7 |
0,3e |
0,4 |
|
Escore de Erosão, alteração média desde o valor basal |
|||||
|
Semana 24b/26c |
0,3 |
0,1e |
0,4 |
0e |
0 |
|
Semana 48 |
|
|
0,8 |
0,1e |
0,2 |
|
Escore de Estreitamento do Espaço Articular, alteração média desde o valor basal |
|||||
|
Semana 24b/26c |
0,3 |
0,1g |
0,6 |
0,2e |
0,1 |
|
Semana 48 |
|
|
0,8 |
0,2e |
0,2 |
|
Proporção de pacientes sem progressão radiográficad |
|||||
|
Semana 24b/26c |
77,7 |
87,5f |
76,0 |
83,5f |
86,8 |
|
Semana 48 |
|
|
74,1 |
86,4e |
87,9 |
Abreviações: ADA = adalimumabe; IR = responsivo inadequado; MTX = metotrexato; PBO = placebo7; UPA= upadacitinibe
a Todos os dados com placebo7 na semana 48 derivados com uso de extrapolação linear
b SELECT-EARLY
c SELECT-COMPARE
d Sem progressão definida como alteração de mTSS ≤0
e p≤0,001 upadacitinibe vs placebo7 ou em comparação com MTX
f p≤0,01 upadacitinibe vs placebo7 ou em comparação com MTX
g p≤0,05 upadacitinibe vs placebo7 ou em comparação com MTX
Resposta de função física e resultados relacionados à saúde1
O tratamento com Rinvoq® 15 mg, isoladamente ou em combinação com csDMARDs, resultou em uma melhora significativa na função física em comparação a todos os comparadores (placebo7, MTX, adalimumabe) conforme medido por HAQ-DI. Foram observadas melhoras logo na Semana 1 em comparação ao placebo7 nos estudos SELECT-NEXT e SELECT- BEYOND e foram mantidas por até 60 semanas. No estudo SELECT-COMPARE, pacientes tratados com Rinvoq® 15 mg apresentaram melhora significativamente maior na função física em comparação a adalimumabe logo na semana 8 e foi mantida até a semana 48.
Em todos os estudos, o tratamento com Rinvoq® 15 mg, isoladamente ou em combinação com csDMARDs, resultou em melhora significativamente maior na dor em comparação a todos os comparadores, conforme medida em uma escala visual analógica de 0–100, nas semanas 12/14, com respostas mantidas por até 48–60 semanas. Foi observada redução significativamente maior na dor logo na Semana 1 em comparação ao placebo7 e logo na Semana 4 em comparação a adalimumabe.
Em todos os estudos, o tratamento com Rinvoq® 15 mg resultou em melhora significativamente maior na duração média e gravidade de rigidez articular matutina em comparação ao placebo7 ou MTX. No estudo SELECT-COMPARE, pacientes tratados com Rinvoq® apresentaram melhora significativamente maior na gravidade da rigidez articular matutina em comparação a adalimumabe.
Entre todos os estudos, pacientes que receberam Rinvoq® 15 mg apresentaram melhora significativamente maior no escore de resumo do componente físico (PCS) do Formulário Resumido de Avaliação de Saúde1 (SF-36) em comparação ao placebo7, adalimumabe ou MTX. No estudo SELECT-EARLY, SELECT-MONOTHERAPY e SELECT-COMPARE, pacientes que receberam Rinvoq® 15 mg apresentaram melhora significativamente maior desde o valor basal nas pontuações do resumo do componente mental (MCS) e em todos os 8 domínios de SF-36 em comparação ao placebo7 ou MTX.
Fadiga8 foi avaliada pelo questionário FACIT-F (Functional Assessment of Chronic Illness Therapy-Fatigue) nos estudos SELECT-EARLY, SELECT-NEXT, SELECT-EARLY e SELECT- COMPARE.O tratamento com Rinvoq® 15 mg resultou em melhora significativa na fadiga8 em comparação ao placebo7, MTX ou adalimumabe.
A instabilidade no trabalho associada à AR foi avaliada pela Escala de Instabilidade no Trabalho por Artrite Reumatoide2 (RA-WIS) em pacientes dos estudos SELECT-NEXT e SELECT- COMPARE. O tratamento com Rinvoq® 15 mg resultou em redução significativamente maior na instabilidade no trabalho em comparação ao placebo7.
DADOS DE SEGURANÇA PRÉ-CLÍNICA
O upadacitinibe é teratogênico10 em ratos e coelhos (vide item “5. ADVERTÊNCIAS E PRECAUÇÕES – Gravidez”).
Carcinogenicidade: O potencial carcinogênico de upadacitinibe foi avaliado em ratos Sprague-Dawley e camundongos transgênicos rasH2. Não foi observada evidência de tumorigenicidade em ratos machos ou fêmeas que receberam upadacitinibe por até 101 semanas em doses orais de até 15 ou 20 mg/kg/dia, respectivamente (aproximadamente 4 e 10 vezes a dose clínica de 15 mg com base em uma AUC11 para machos e fêmeas, respectivamente). Não foi observada evidência de tumorigenicidade em camundongos transgênicos rasH2 que receberam upadacitinibe por 26 semanas em doses orais de até 20 mg/kg/dia em camundongos machos ou fêmeas.
Mutagenicidade: O upadacitinibe não foi mutagênico ou genotóxico com base nos resultados de testes in vitro e in vivo para mutações gênicas e aberrações cromossômicas.
Comprometimento da fertilidade
O upadacitinibe não causou efeito na fertilidade em ratos machos ou fêmeas em doses de até 50 mg/kg/dia em machos e 75 mg/kg/dia em fêmeas em um estudo de fertilidade e desenvolvimento embrionário inicial. Os aumentos relacionados à dose nas reabsorções fetais associadas a perdas pós-implantação nas doses de 25 e 75 mg/kg/dia neste estudo foram atribuídos aos efeitos no desenvolvimento/teratogênicos12 de upadacitinibe em ratos.
Farmacologia13 e/ou toxicologia em animais: Em estudos não clínicos em animais, foram observadas reduções nos linfócitos circulantes e celularidade de tecidos linfoides14, bem como supressão da eritropoiese15, em ratos e cães em doses clinicamente relevantes. Foram observados efeitos secundários relacionados a infecções16 oportunistas, como demodicose (sarna17) em cães, em exposições aproximadamente duas vezes a exposição esperada (AUC11) na dose clínica de 15 mg.
Referências Bibliográficas
- Burmester GR, KremerJM, Van den Bosch F et al. Safety and efficacy of upadacitinib in patients with rheumatoid arthritis and inadequate response to conventional synthetic disease-modifying anti-rheumatic drugs (SELECT-NEXT): a randomised, double-blind, placebo7-controlled phase 3 trial. Lancet 2018; 23;391(10139):2503-2512
- Genovese MC, Fleischmann R, Combe B et al. Safety and efficacy of upadacitinib in patients with active rheumatoid arthritis refractory to biologic disease-modifying anti- rheumatic drugs (SELECT-BEYOND): a double-blind, randomised controlled phase 3 trial. Lancet 2018; 23;391(10139):2513-2524
- van Vollenhoven R, Takeuchi T, Pangan AL et al. Phase 3, Randomized, Controlled Trial Comparing Upadacitinib Monotherapy to MTX Monotherapy in MTX-Naïve Patients with Active Rheumatoid Arthritis. . Arthritis Rheumatol. 2018; 70 (suppl 10). ABSTRACT NUMBER: 89. Oral presentation at 2018 ACR/ARHP Annual Meeting, October 19-24th, Chicago, IL
- Fleischmann R, Pangan AL, Mysler E et al. A Phase 3, RandomizedDouble-Blind Study Comparing Upadacitinib to Placebo7 and to Adalimumab, in Patients with Active Rheumatoid Arthritis with Inadequate Response to Methotrexate . Arthritis Rheumatol. 2018; 70 (suppl 10). ABSTRACT NUMBER: 890. Oral presentation at 2018 ACR/ARHP Annual Meeting, October 19-24th, Chicago, IL.
- Smolen JS, Cohen S, Emery P, Rigby WFC, Tanaka Y, Zhang Y, Friedman A, Othman AA, Camp HS, Pangan AL. Upadacitinib As Monotherapy: A Phase 3 Randomized Controlled Double-Blind Study in Patients with Active Rheumatoid Arthritis and Inadequate Response to Methotrexate . Arthritis Rheumatol. 2018; 70 (suppl 10). ABSTRACT NUMBER: 889. Oral presentation at 2018 ACR/ARHP Annual Meeting, October 19-24th, Chicago, IL.
CARACTERÍSTICAS FARMACOLÓGICAS
Rinvoq® é formulado com upadacitinibe, um inibidor de JAK.
Upadacitinibe é um pó branco a marrom claro com o seguinte nome químico: (3S,4R)-3-Etil-4-(3H- imidazo[1,2-a]pirrolo[2,3-e]pirazina-8-il)-N-(2,2,2-trifluoroetil)pirrolidina-1-carboxamida hidratada (2:1).
A potência de upadacitinibe se baseia em upadacitinibe anidro. A solubilidade de upadacitinibe em água é de 38 a menos de 0,2 mg/mL na variação de pH de 2 a 9 a 37°C.
Upadacitinibe possui um peso molecular de 389,38 g/mol e uma fórmula molecular de C17H19F3N6O • ½ H2O. A estrutura química de upadacitinibe é:
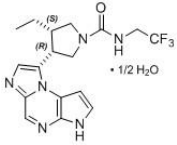
Os comprimidos revestidos de liberação prolongada não contêm glúten18.
Mecanismo de ação
Janus Quinases (JAKs) são importantes enzimas intracelulares que transmitem sinais19 de citocinas20 ou de fatores de crescimento envolvidos em uma ampla gama de processos celulares, incluindo respostas inflamatórias, hematopoiese e vigilância imunológica. A família JAK de enzimas contém quatro membros, JAK1, JAK2, JAK3 e TYK2, que sinalizam em pares para fosforilar e ativar transdutores de sinal21 e ativadores de transcrição (STATs). Esta fosforilação, por sua vez, modula expressão gênica e função celular. JAK1 é importante na sinalização de citocinas20 inflamatórias, ao passo que JAK2 é importante para maturação de eritrócitos22, e os sinais19 de JAK3 desempenham um papel na imunovigilância e função de linfócitos.
O upadacitinibe é um inibidor seletivo e reversível da JAK1. O upadacitinibe inibe de modo mais potente JAK1 em comparação a JAK2 e JAK3. Em ensaios de potência celular que se correlacionam com respostas farmacodinâmicas in vivo, o upadacitinibe demonstrou 50–70 vezes maior seletividade para JAK1 em relação a JAK2 e >100 vezes para JAK1 em relação a JAK3.
Farmacodinâmica
Inibição de STAT3 induzida por IL-6 e fosforilação de STAT5 induzida por IL-7: Em voluntários saudáveis, a administração de upadacitinibe (formulação de liberação imediata) resultou em uma inibição dependente de dose e de concentração da STAT3 induzida por IL-6 (JAK1/JAK2) e da fosforilação de STAT5 induzida por IL-7 (JAK1/JAK3) no sangue23 total. A inibição máxima foi observada 1 hora após a administração, que retornou próximo do valor basal até o final do intervalo de administração.
Linfócitos: O tratamento com upadacitinibe foi associado a um aumento pequeno e temporário na CAL (contagem absoluta de linfócitos) média desde o valor basal até a Semana 36, que gradualmente retornou aos níveis basais ou próximos destes com a continuação do tratamento.
Imunoglobulinas24: No período controlado, foram observadas pequenas reduções a partir do valor basal nos níveis médios de IgG e IgM com o tratamento com upadacitinibe; contudo, os valores médios na visita basal e em todas as visitas estiveram dentro da variação de referência normal.
hsPCR: O tratamento com upadacitinibe foi associado a reduções significativas a partir do valor basal nos níveis médios de hsPCR logo na Semana 1, que foram mantidas com a continuação do tratamento.
Eletrofisiologia cardíaca: O efeito de upadacitinibe no intervalo QTc foi avaliado em indivíduos que receberam doses únicas e múltiplas de upadacitinibe. O upadacitinibe não prolonga o intervalo QTc em concentrações plasmáticas terapêuticas ou supraterapêuticas.
Estudo com vacinas: A influência de Rinvoq® na resposta humoral25 após a administração da vacina26 pneumocócica conjugada 13-valente inativada foi avaliada em 111 pacientes com artrite reumatoide2 sob tratamento estável com upadacitinibe 15 mg (n = 87) ou 30 mg (n = 24). 97% dos pacientes (n = 108) estavam em uso concomitante de metotrexato. A vacinação resultou em uma resposta humoral25 satisfatória em 67,5% (IC 95%: 57,4, 77,5) e 56,5% (IC 95%: 36,3, 76,8) dos pacientes tratados com upadacitinibe 15 mg e 30 mg, respectivamente.
Farmacocinética: As exposições plasmáticas ao upadacitinibe são proporcionais à dose na variação de dose terapêutica27. As concentrações plasmáticas no estado de equilíbrio são atingidas em 4 dias, com acúmulo mínimo após administrações múltiplas uma vez ao dia. As propriedades farmacocinéticas de Rinvoq® são apresentadas na Tabela 5.
Tabela 5. Propriedades farmacocinéticas de Rinvoq®
|
Absorção |
|
|
Tmax (h) |
2–4 |
|
Efeito de refeição hipercalórica (em relação ao jejum) |
Sem efeito clinicamente relevante AUC11: ↑ 29%, Cmax ↑ 39% |
|
Distribuição |
|
|
% Ligada às proteínas28 plasmáticas humanas |
52 |
|
Proporção sangue23-plasma29 |
1,0 |
|
Metabolismo30 |
|
|
Metabolismo30 |
CYP3A4, CYP2D6 (menor) |
|
Eliminação |
|
|
t1/2 de eliminação de fase terminal (h) |
9–14 |
|
Clearance oral aparente (L/h) |
40,5 |
|
Variabilidade interindividual no clearance em pacientes com artrite reumatoide2 |
37 |
|
% da dose excretada não metabolizada na urinaa |
24 |
|
% da dose excretada não metabolizada nas fezesa |
38 |
|
% da dose excretada como metabólitosa |
34 |
a Com base na administração de dose única de [14C] upadacitinibe solução de liberação imediata em um estudo de equilíbrio de massa
Farmacocinética em populações especiais
Comprometimento renal32: O comprometimento renal32 não causou efeito clinicamente relevante na exposição ao upadacitinibe. A AUC11 do upadacitinibe foi 18%, 33% e 44% mais elevada em indivíduos com comprometimento renal32 leve, moderado e grave, respectivamente, em comparação a indivíduos com função renal32 normal. A Cmax do upadacitinibe foi similar em indivíduos com função renal32 normal e comprometida.
Comprometimento hepático: O comprometimento hepático leve (Child-Pugh A) e moderado (Child-Pugh B) não possuem efeito clinicamente relevante na exposição ao upadacitinibe. A AUC11 do upadacitinibe foi 28% e 24% mais elevada em indivíduos com comprometimento hepático leve e moderado, respectivamente, em comparação a indivíduos com função hepática33 normal. A Cmax do upadacitinibe não foi alterada em indivíduos com comprometimento hepático leve e 43% mais elevada em indivíduos com comprometimento hepático moderado em comparação a indivíduos com função hepática33 normal. O upadacitinibe não foi estudado em pacientes com comprometimento hepático grave (Child-Pugh C).
Fatores intrínsecos: Idade, sexo, peso corporal, raça e etnia não possuem um efeito clinicamente significativo na exposição à upadacitinibe.
Interações medicamentosas
Potencial para outras drogas afetarem a farmacocinética do upadacitinibe
O upadacitinibe é metabolizado in vitro pela CYP3A4, com uma contribuição menor pela CYP2D6. O efeito de drogas administradas concomitantemente nas exposições plasmáticas do upadacitinibe é apresentado na Tabela 6.
Tabela 6. Alteração na farmacocinética de upadacitinibe na presença de drogas administradas concomitantemente
|
Droga administrada concomitantemente |
Regime de droga administrada concomitantemente |
Regime de upadacitinibe |
N |
Proporção (IC de 90%)a |
Impacto Clínico |
|
|
Cmax |
AUC11 |
|||||
|
cetoconazol |
400 mg uma vez ao dia |
Dose única de 3 mgb |
11 |
1,70 |
1,75 |
Utilizar com cautela se utilizado cronicamente |
|
rifampicina |
600 mg uma vez ao dia |
Dose única de 12 mgb |
12 |
0,49 |
0,39 |
Poderá reduzir a eficácia |
IC: Intervalo de confiança
a As proporções para Cmax e AUC11 comparam a administração concomitante da medicação com upadacitinibe vs. administração de upadacitinibe isoladamente.
b O upadacitinibe foi administrado como uma formulação de liberação imediata.
O metotrexato, inibidores de transportadores de OATP1B e medicamentos modificadores de pH (por exemplo, antiácidos34 ou inibidores da bomba de próton) não causam efeito nas exposições plasmáticas de upadacitinibe. O fenótipo35 metabólico CYP2D6 não causou efeito na farmacocinética de upadacitinibe, indicando que inibidores da CYP2D6 não causam efeito clinicamente relevante nas exposições a upadacitinibe.
Potencial para upadacitinibe afetar a farmacocinética de outras drogas
O efeito de upadacitinibe nas exposições plasmáticas de outras drogas é apresentado na Tabela 7.
Tabela 7. Alteração na farmacocinética de droga administradas concomitantemente na presença de upadacitinibe
|
Droga administrada concomitantemente |
Regime de droga administrada concomitantemente |
Regime de upadacitinibe |
N |
Proporção (IC de 90%)a |
Impacto Clínico |
|
|
Cmax |
AUC11 |
|||||
|
midazolam |
Dose única de 5 mg |
30 mg uma vez ao dia |
20 |
0,74 |
0,74 |
Sem ajuste de dose |
| rosuvastatina | Dose única de 5 mg | 30 mg uma vez ao dia x 10 dias |
12 | 0,77 (0,63–0,94) |
0,67 (0,56–0,82) |
Sem ajuste de dose |
| atorvastatina | Dose única de 10 mg | 30 mg uma vez ao dia x 10 dias |
24 | 0,88 (0,79–0,97) |
0,77 (0,70–0,85) |
Sem ajuste de dose |
IC: Intervalo de confiança
a As proporções para Cmax e AUC11 comparam a administração concomitante da medicação com upadacitinibe vs. a administração da medicação isoladamente.
O upadacitinibe não possui efeitos relevantes nas exposições plasmáticas a etinilestradiol, levonorgestrel, metotrexato ou drogas substratos para o metabolismo30 pela CYP1A2, CYP2B6, CYP2D6, CYP2C19 ou CYP2C9.
CONTRAINDICAÇÕES
Rinvoq® não deve ser utilizado em pacientes com insuficiência hepática36 grave.
Este medicamento é contraindicado para uso por pacientes com insuficiência hepática36 grave.
ADVERTÊNCIAS E PRECAUÇÕES
Infecções16 graves: foram relatadas infecções16 graves e algumas vezes fatais em pacientes recebendo Rinvoq®. As infecções16 graves mais comuns relatadas com Rinvoq® incluíram pneumonia37 e celulite38 (vide item “9. REAÇÕES ADVERSAS”). Entre as infecções16 oportunistas, tuberculose39, herpes zoster40 em múltiplos dermátomos41, candidíase42 oral/esofágica e criptococos foram relatadas com Rinvoq®.
Rinvoq® deve ser evitado em pacientes com uma infecção43 grave ativa, incluindo infecções16 localizadas. Os riscos e benefícios do tratamento devem ser considerados antes de iniciar o uso de Rinvoq® em pacientes:
- com infecção43 crônica ou recorrente;
- que foram expostos à tuberculose39;
- com histórico de infecção43 grave ou oportunista;
- que residiram em áreas de tuberculose39 endêmica ou micoses endêmicas ou viajaram para tais áreas; ou
- com condições subjacentes que podem predispô-los à infecção43.
Os pacientes devem ser cuidadosamente monitorados quanto ao desenvolvimento de sinais19 e sintomas44 de infecção43 durante e após o tratamento com Rinvoq®. Rinvoq® deve ser interrompido se o paciente desenvolver uma infecção43 grave ou oportunista. O paciente que desenvolver uma nova infecção43 durante tratamento com Rinvoq®, deve ser submetido a um teste diagnóstico45 imediato e completo apropriado para um paciente com comprometimento imunológico; a terapia antimicrobiana apropriada deve ser iniciada, o paciente deve ser cuidadosamente monitorado e Rinvoq® deve ser interrompido se o paciente não estiver respondendo à terapia antimicrobiana Rinvoq® poderá ser reiniciado após o controle da infecção43.
Tuberculose39: Medicamentos imunossupressores podem ativar focos primários de tuberculose39. Os médicos que acompanham pacientes sob imunossupressão46 devem estar alertas quanto à possibilidade de surgimento de doença ativa, tomando, assim, todos os cuidados para o diagnóstico45 precoce e tratamento.
Os pacientes deverão ser testados para rastrear a presença tuberculose39 (TB) antes de iniciar Rinvoq®. Rinvoq® não deverá ser administrado a pacientes com TB ativa. A terapia antituberculose deve ser considerada antes do início da administração de Rinvoq® em pacientes com TB latente não tratada anteriormente.
Recomenda-se consultar com médico com experiência no tratamento de TB para auxiliar na decisão se o início da terapia antituberculose é adequado para o paciente em questão.
Os pacientes devem ser monitorados quanto ao desenvolvimento de sinais19 e sintomas44 da TB, incluindo pacientes com teste negativo para infecção43 latente por TB antes do início da terapia.
Reativação viral: reativação viral, incluindo casos de reativação do vírus47 da herpes (por exemplo, herpes zoster40), foi relatada em estudos clínicos (vide item “9. REAÇÕES ADVERSAS”). O risco de herpes zoster40 parece ser maior em pacientes tratados com Rinvoq® no Japão. Caso um paciente desenvolva herpes zoster40, considerar a interrupção temporária de Rinvoq® até a resolução do episódio.
A triagem para hepatite48 viral e monitoramento quanto à reativação deverão ser realizadas de acordo com as diretrizes clínicas antes do início e durante a terapia com Rinvoq®. Pacientes que apresentaram resultados positivos para anticorpo49 contra hepatite48 C e RNA do vírus47 da hepatite48 C e, antígeno50 de superfície de hepatite48 B ou DNA de vírus47 da hepatite48 B, foram excluídos dos estudos clínicos. Caso seja detectado DNA de vírus47 da hepatite48 B enquanto recebe Rinvoq®, um hepatologista deverá ser consultado.
Vacinações: não há dados disponíveis sobre a resposta à vacinação com vacinas vivas em pacientes que estão recebendo Rinvoq®. O uso de vacinas vivas atenuadas durante ou imediatamente antes da terapia com Rinvoq® não é recomendado. Antes de iniciar o uso de Rinvoq®, recomenda-se que o paciente tenha todas as vacinas atualizadas, incluindo vacinações profiláticas contra zoster40, de acordo com as diretrizes de vacinação vigentes (vide 3. PROPRIEDADES FARMACOLÓGICAS – Estudos com vacinas, para dados sobre a vacina26 pneumocócica conjugada 13-valente inativada e uso concomitante com Rinvoq®.
Malignidades: o risco de malignidades, incluindo linfoma51, é aumentado em pacientes com artrite reumatoide2. Medicamentos imunomoduladores poderão aumentar o risco de malignidades, incluindo linfoma51. Os dados clínicos são atualmente limitados e estudos de longo prazo estão em andamento.
Foram observadas malignidades em estudos clínicos de Rinvoq® (vide item “9. REAÇÕES ADVERSAS”). Considerar os riscos e benefícios do tratamento com Rinvoq® antes de iniciar a terapia em pacientes com uma malignidade conhecida, exceto câncer52 de pele53 não melanoma54 (NMSC) tratado com sucesso ou ao considerar manter o uso de Rinvoq® em pacientes que desenvolvam uma malignidade.
Câncer52 de pele53 não melanoma54: cânceres de pele53 não melanoma54 foram reportados em pacientes tratados com Rinvoq®. Exame periódico da pele53 é recomendado para pacientes55 que apresentammaior risco para o câncer52 de pele53.
Parâmetros laboratoriais:
Neutropenia56: o tratamento com Rinvoq® foi associado a uma maior incidência57 de neutropenia56 (CAN <1000 células58/mm3). Não houve associação clara entre as baixas contagens de neutrófilos59 e a ocorrência de infecções16 graves.
Linfopenia: as contagens de linfócitos <500 células58/mm3 foram reportadas em estudos clínicos com Rinvoq®. Não houve associação clara entre as baixas contagens de linfócitos e a ocorrência de infecções16 graves.
Anemia60: foram reportadas reduções nos níveis de hemoglobina61 para <8 g/dL em estudos clínicos com Rinvoq®.
A maior parte das alterações laboratoriais hematológicas mencionadas anteriormente foi temporária e se resolveu com interrupção temporária do tratamento.
Realizar avaliação na visita basal e posteriormente de acordo com o tratamento de rotina do paciente. O tratamento não deverá ser iniciado ou deverá ser temporariamente interrompido em pacientes que atendem aos critérios descritos na Tabela 8 (vide item “8. POSOLOGIA E MODO DE USAR”).
Lipídios: o tratamento com Rinvoq® foi associado a aumentos nos parâmetros lipídicos, incluindo colesterol62 total, colesterol62 da lipoproteína de baixa densidade (LDL63) e colesterol62 da lipoproteína de alta densidade (HDL64) (vide item “9. REAÇÕES ADVERSAS”). Aumentos no colesterol62 LDL63 foram reduzidos aos níveis pré-tratamento em resposta à terapia com estatina. O efeito destas elevações nos parâmetros lipídicos na morbidade65 e mortalidade66 cardiovasculares não foi determinado.
Os pacientes deverão ser monitorados por 12 semanas após o início do tratamento e posteriormente, de acordo com as diretrizes clínicas internacionais para hiperlipidemia67.
Elevações de enzimas hepáticas68: o tratamento com Rinvoq® foi associado com um aumento da incidência57 de elevação das enzimas hepáticas68 em comparação ao placebo7.
Realizar avaliação na visita basal e posteriormente de acordo com o tratamento de rotina do paciente. Recomenda-se a investigação da causa da elevação das enzimas hepáticas68 para identificar possíveis causas de lesão9 hepática33 induzida pelo medicamento.
Caso sejam observados aumentos de ALT ou AST durante o tratamento de rotina do paciente e haja suspeita de lesão9 hepática33 induzida por droga, Rinvoq® deverá ser interrompido até que este diagnóstico45 seja descartado.
Tromboembolismo69 venoso: foram relatados eventos de trombose venosa profunda70 (TVP) e embolia71 pulmonar (EP) em pacientes que receberam inibidores de JAK, incluindo upadacitinibe. O upadacitinibe deve ser usado com cautela em pacientes com alto risco de TVP / EP. Se ocorrerem características clínicas da TVP / EP, o tratamento com upadacitinibe deve ser temporariamente interrompido e os pacientes devem ser avaliados imediatamente, seguido de tratamento apropriado.
Medicamentos imunossupressores: a combinação com outros potentes imunossupressores como azatioprina, ciclosporina, tacrolimo e DMARDs biológicas ou inibidores de JAK não foi avaliada em estudos clínicos e não é recomendada uma vez que o risco de imunossupressão46 aditiva não pode ser excluído.
Populações especiais
Uso pediátrico: não é recomendado o uso de Rinvoq® em crianças e adolescentes menores de 18 anos de idade. Rinvoq® não foi estudado nesta faixa etária.
Gravidez72 e Lactação73
Os dados limitados em humanos com Rinvoq® não são suficientes para informar o risco associado à droga sobre má formação ao nascimento e aborto espontâneo em gestantes.
Com base em estudos em animais, o upadacitinibe apresenta potencial de afetar um feto74 em desenvolvimento.
Em estudos de desenvolvimento embriofetal em animais, o upadacitinibe demonstrou ser teratogênico10 em ratos e coelhos quando animais prenhes receberam upadacitinibe durante o período de organogênese em exposições múltiplas de 1,6 e 15 vezes a dose clínica de 15 mg para ratos e coelhos, respectivamente (vide Dados em Animais). Além disso, em um estudo de desenvolvimento pré/pós-natal em ratos, a administração de upadacitinibe não resultou em efeitos relacionados à droga nas mães ou filhotes.
Dados em Animais: O upadacitinibe demonstrou ser teratogênico10 em ratos e coelhos quando administrado em exposições de 1,6 e 15 vezes a dose clínica de 15 mg (com base na AUC11 nas doses orais maternas de 4 mg/kg/dia e 25 mg/kg/dia, respectivamente).
Em dois estudos de desenvolvimento embriofetal em ratos, os animais prenhes foram tratados durante o período de organogênese desde o dia de gestação (GD) 6 ao GD 17. O upadacitinibe foi teratogênico10 em todos os níveis de dose estudados em ratos, exceto com a menor dose de 1,5 mg/kg/dia. Em doses de 4, 5, 25 e 75 mg/kg/dia, os efeitos relacionados ao upadacitinibe incluíram um aumento em duas malformações75 esqueléticas em particular (isto é, úmero76 de formato incorreto e escápula77 dobrada) e, na dose de 75 mg/kg/dia, um aumento nos ossos dobrados dos membros torácicos e pélvicos78. Além disso, nas doses de 25 e 75 mg/kg/dia, houve um aumento nas costelas79 dobradas, uma variação esquelética, que também foi considerada relacionada ao upadacitinibe.
Em um estudo de desenvolvimento embriofetal em coelhos, os animais prenhes foram tratados durante o período de organogênese desde o GD 7 ao GD 19. O upadacitinibe foi teratogênico10 quando administrado em doses de 25 mg/kg/dia. Os efeitos no desenvolvimento observados na dose de 25 mg/kg/dia em coelhos incluíram um aumento nas perdas pós-implantação, aumento nas reabsorções totais e precoces, menores pesos corporais fetais e aumento da incidência57 de malformações75 cardíacas. Além disso, a toxicidade80 materna foi evidente no grupo de dose de 25 mg/kg/dia como perda de peso, menor consumo de alimento e aumento da ocorrência de abortos.
Em um estudo de desenvolvimento pré/pós-natal em ratos, o desenvolvimento da prole em consequência à exposição das mães desde a implantação até a lactação73 e o desmame foi testado. Uma vez que as manifestações dos efeitos induzidos durante este período podem ser postergadas, as observações continuaram até a maturidade sexual dos filhotes. As mães foram tratadas desde o GD 6 até o Dia da Lactação73 (LD) 20. O upadacitinibe não causou efeitos em nenhum nível de dose em mães ou sua prole nos tempos de estudo comportamentais ou reprodutores.
Categoria C: Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Lactação73: não se sabe se o upadacitinibe/metabólitos31 são excretados no leite humano. Dados farmacodinâmicos/toxicológicos disponíveis em animais demonstraram excreção de upadacitinibe no leite.
Um risco aos neonatos81/bebês82 não poderá ser descartado. Rinvoq® não deverá ser utilizado durante a amamentação83.
Mulheres em idade fértil: em estudos de desenvolvimento embriofetal em animais, upadacitinibe foi teratogênico10 em ratos e coelhos (vide Dados em Animais).
Mulheres com potencial reprodutivo devem ser aconselhadas a usar contracepção84 efetiva durante o tratamento com Rinvoq®, e por 4 semanas após a última dose.
Fertilidade: com base em achados em ratos, o tratamento com upadacitinibe não reduz a fertilidade em machos ou fêmeas com potencial reprodutor (vide item “2. RESULTADOS DE EFICÁCIA - DADOS DE SEGURANÇA PRÉ-CLÍNICA”).
Dados em Animais
Após a administração de upadacitinibe a ratas lactantes85, as concentrações de upadacitinibe no leite com o tempo foram aproximadamente 30 vezes mais elevadas que a exposição no leite em relação ao plasma29 materno. Aproximadamente 97% do material relacionado à droga no leite foi a droga precursora.
Efeitos na habilidade de dirigir e operar máquinas
Rinvoq® não possui efeito na capacidade de dirigir e operar máquinas.
INTERAÇÕES MEDICAMENTOSAS
Inibidores potentes de CYP3A4
A exposição ao upadacitinibe é aumentada quando coadministrado com inibidores potentes da CYP3A4 (por exemplo, cetoconazol) (vide item “3. CARACTERÍSTICAS FARMACOLÓGICAS”). Rinvoq® deverá ser utilizado com cautela em pacientes que recebem tratamento crônico86 com inibidores potentes da CYP3A4.
Indutores potentes da CYP3A4
A exposição ao upadacitinibe é reduzida quando coadministrado com indutores potentes de CYP3A4 (por exemplo, rifampicina), o que poderá causar redução do efeito terapêutico de Rinvoq® (vide item “3. CARACTERÍSTICAS FARMACOLÓGICAS”). Os pacientes deverão ser monitorados quanto a alterações na atividade da doença caso Rinvoq® seja administrado concomitantemente com indutores potentes de CYP3A4.
CUIDADOS DE ARMAZENAMENTO DO MEDICAMENTO
Cuidados de conservação
Rinvoq® deve ser mantido em temperatura ambiente (15–30°C) em sua embalagem original. Proteger da umidade. Nestas condições, o medicamento apresenta 24 meses de validade.
Após aberto, válido por 60 dias.
Número de lote e datas de fabricação e validade: vide embalagem.
Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original.
Características físicas e organolépticas do produto
O comprimido revestido de liberação prolongada apresenta coloração roxa biconvexo, oblongo, com dimensões de 14 x 8 mm e com gravação ‘a15’ em um dos lados.
Antes de usar, observe o aspecto do medicamento.
TODO MEDICAMENTO DEVE SER MANTIDO FORA DO ALCANCE DAS CRIANÇAS.
POSOLOGIA E MODO DE USAR
Dose recomendada
A dose oral recomendada de Rinvoq® é de 15 mg uma vez ao dia com ou sem alimento. A dose máxima não deve exceder 15mg/dia. Aproximadamente 80% do upadacitinibe presente no comprimido de liberação prolongada é liberado em 8 horas.
Rinvoq® poderá ser utilizado como monoterapia ou em combinação com metotrexato ou outras DMARDs convencionais sintéticas.
Rinvoq® deve ser ingerido inteiro com água aproximadamente no mesmo horário a cada dia.
O tratamento deve ser continuado durante o tempo definido pelo médico.
Este medicamento não deve ser partido, aberto ou mastigado.
Dose esquecida
Se uma dose de Rinvoq® for esquecida, esta deve ser administrada assim que possível. A dose subsequente deverá ser administrada no horário regularmente agendado.
Interrupção de dose
Recomenda-se que Rinvoq® não seja iniciado em pacientes com contagem absoluta de linfócitos (CAL) menor que 500 células58/mm3, contagem absoluta de neutrófilos59 (CAN) menor que 1000 células58/mm3 ou que possuam níveis de hemoglobina61 menores que 8 g/dL (vide itens “5. ADVERTÊNCIAS E PRECAUÇÕES” e “9. REAÇÕES ADVERSAS”).
O tratamento com Rinvoq® deverá ser interrompido se um paciente desenvolver uma infecção43 grave até que esta seja controlada (vide item “5. ADVERTÊNCIAS E PRECAUÇÕES”).
Tabela 8. Interrupções de dose recomendadas para anormalidades laboratoriais
|
Valor laboratorial |
Medida |
|
Contagem Absoluta de Neutrófilos59 (CAN) |
O tratamento deverá ser interrompido se a CAN for <1000 células58/mm3 e poderá ser reiniciado após o retorno da CAN acima deste valor |
|
Contagem Absoluta de Linfócitos (CAL) |
O tratamento deverá ser interrompido se a CAL for <500 células58/mm3 e poderá ser reiniciado após o retorno da CAL acima deste valor |
|
Hemoglobina61 (Hb) |
O tratamento deverá ser interrompido se a Hb for < 8 g/dL e poderá ser reiniciado após o retorno da Hb acima deste valor |
|
Transaminases hepáticas87 |
O tratamento deverá ser interrompido temporariamente se houver suspeita de lesão9 hepática33 induzida por droga |
Administração em populações especiais
Pacientes pediátricos: a segurança e a eficácia de Rinvoq® em crianças e adolescentes de 0 a menores que 18 anos de idade ainda não foram estabelecidas. Não há dados disponíveis.
Pacientes idosos: dos 4381 pacientes tratados nos cinco estudos clínicos de fase 3, um total de 906 pacientes com artrite reumatoide2 tinha 65 anos de idade ou mais. Não foram observadas diferenças na efetividade entre estes pacientes e pacientes mais jovens; no entanto, houve uma taxa mais elevada de eventos adversos gerais em idosos.
Pacientes com comprometimento renal32: não é necessário ajuste de dose em pacientes com comprometimento renal32 leve, moderado ou grave. O uso de Rinvoq® não foi estudado em indivíduos com nefropatia88 em estágio terminal. A hemodiálise89 não deverá causar um efeito clinicamente relevante nas exposições plasmáticas do upadacitinibe devido à importante contribuição do clearance não renal32 para a eliminação geral de upadacitinibe (vide item “3. CARACTERÍSTICAS FARMACOLÓGICAS”).
Pacientes com comprometimento hepático: não é necessário ajuste de dose em pacientes com comprometimento hepático leve (Child-Pugh A) ou moderado (Child-Pugh B). Rinvoq® não é recomendado para uso em pacientes com comprometimento hepático grave (Child Pugh C) (vide item “3. CARACTERÍSTICAS FARMACOLÓGICAS”).
REAÇÕES ADVERSAS
Experiência em estudos clínicos
Um total de 4.443 pacientes com artrite reumatoide2 foi tratado com upadacitinibe em estudos clínicos que representam 5.263 pacientes-ano de exposição a droga, dos quais 2.972 foram expostos por no mínimo um ano. Nos estudos de fase 3, 2.630 pacientes receberam no mínimo 1 dose de Rinvoq® 15 mg, dos quais 1.607 foram expostos por no mínimo um ano.
Três estudos controlados com placebo7 foram integrados (1.035 pacientes com Rinvoq® 15 mg uma vez ao dia e 1.042 pacientes com placebo7) para avaliar a segurança de Rinvoq® 15 mg em comparação ao placebo7 por até 12–14 semanas após início do tratamento.
A frequência de reações adversas listadas abaixo é definida com uso da seguinte convenção: muito comum (≥ 1/10); comum (≥ 1/100 a < 1/10), incomum (≥ 1/1.000 a < 1/100). Em cada agrupamento de frequência, as reações adversas são apresentadas em ordem de seriedade decrescente.
Infecções16 e infestações
- Reação muito comum (≥ 1/10): infecções16 do trato respiratório superior (ITRS*).
- Reação incomum (≥ 1/1.000 a < 1/100): pneumonia37, herpes zoster40, herpes simples**, candidíase42 oral.
Distúrbios do sistema sanguíneo e linfático90
- Reação comum (≥ 1/100 a < 1/10): neutropenia56
Distúrbios metabólicos e nutricionais
- Reação comum (≥ 1/100 a < 1/10): hipercolesterolemia91, hipertrigliceridemia
Distúrbios respiratórios, torácicos e mediastinais
- Reação comum (≥ 1/100 a < 1/10): tosse
Distúrbios gastrointestinais
- Reação comum (≥ 1/100 a < 1/10): náusea92
Distúrbios gerais e condições no local de administração
- Reação comum (≥ 1/100 a < 1/10): pirexia93
Investigações
- Reação comum (≥ 1/100 a < 1/10): aumento de creatina fosfoquinase sérica (CPK), aumento de ALT, aumento de AST, aumento de peso
*ITRS inclui: sinusite94 aguda, laringite95, nasofaringite, dor orofaríngea96, faringite97, faringotonsilite, rinite98, sinusite94, tonsilite, infecção43 viral do trato respiratório superior
** Herpes simplex inclui herpes oral
Reações Adversas Específicas
Infecções16: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, a frequência de infecções16 em 12/14 semanas no grupo Rinvoq® 15 mg foi de 27,4% em comparação a 20,9% no grupo placebo7. Em estudos controlados com metotrexato (MTX), a frequência de infecção43 em 12/14 semanas no grupo de monoterapia com Rinvoq® 15 mg foi de 19,5% em comparação a 24,0% no grupo MTX. A taxa geral crônica de infecções16 para o grupo Rinvoq® 15 mg entre todos os cinco estudos clínicos de fase 3 (2.630 pacientes) foi de 93,7 eventos a cada 100 pacientes-ano.
Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, a frequência de infecção43 grave em 12/14 semanas no grupo Rinvoq® 15 mg foi de 1,2% em comparação a 0,6% no grupo placebo7. Em estudos controlados com MTX, a frequência de infecção43 grave em 12/14 semanas no grupo de monoterapia com Rinvoq® 15 mg foi de 0,6% em comparação a 0,4% no grupo MTX. A taxa geral de infecções16 sérias a longo prazo para o grupo Rinvoq® 15 mg entre todos os cinco estudos clínicos de fase 3 foi de 3,8 eventos a cada 100 pacientes-ano. As infecções16 sérias relatadas mais frequentemente foram pneumonia37 e celulite38. A taxa de infecções16 sérias permaneceu estável com a exposição a longo prazo.
Houve uma taxa mais elevada de infecções16 graves em pacientes com idade ≥ 75 anos, embora os dados sejam limitados.
Tuberculose39: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, não houve casos ativos de TB (tuberculose39) relatados em qualquer grupo de tratamento. Em estudos controlados com MTX, não houve casos em 12/14 semanas no grupo de monoterapia com Rinvoq® 15 mg ou no grupo MTX. A taxa geral de TB (tuberculose39) ativa a longo prazo para o grupo Rinvoq® 15 mg entre todos os cinco estudos clínicos de fase 3 foi de 0,1 eventos a cada 100 pacientes-ano.
Infecções16 oportunistas (excluindo tuberculose39): Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, a frequência de infecções16 oportunistas em 12/14 semanas no grupo Rinvoq® 15 mg foi de 0,5% em comparação a 0,3% no grupo placebo7. Em estudos controlados com MTX, não houve casos de infecções16 oportunistas em 12/14 semanas no grupo de monoterapia com Rinvoq® 15 mg e 0,2% no grupo MTX. A taxa geral de infecções16 oportunistas a longo prazo para o grupo Rinvoq® 15 mg entre todos os cinco estudos clínicos de fase 3 foi de 0,6 eventos a cada 100 pacientes-ano.
Malignidades: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, a frequência de malignidades, excluindo NMSC em 12/14 semanas no grupo Rinvoq® 15 mg foi de < 0,1% em comparação a < 0,1% no grupo placebo7. Em estudos controlados com MTX, a frequência de malignidades, excluindo Câncer52 de Pele53 não Melanoma54 em 12/14 semanas no grupo de monoterapia com Rinvoq® 15 mg foi de 0,6% em comparação a 0,2% no grupo MTX. A taxa geral de incidência57 de malignidades excluindo NMSC a longo prazo para o grupo Rinvoq® 15 mg no programa de estudo clínico foi 0,8 a cada 100 pacientes-ano.
Perfurações Gastrointestinais: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, a frequência de perfurações gastrointestinais no grupo Rinvoq® 15 mg foi de 0,2% em comparação a 0% no grupo placebo7. Em estudos controlados com MTX, não houve perfurações gastrointestinais em 12/14 semanas no grupo de monoterapia com Rinvoq® 15 mg ou grupo MTX. A taxa geral de perfuração gastrointestinal a longo prazo para o grupo Rinvoq® 15 mg entre todos os cinco estudos clínicos de fase 3 foi de 0,08 eventos a cada 100 pacientes-ano.
Trombose99: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, houve dois (0,2%) eventos de trombose99 venosa (embolia71 pulmonar ou trombose venosa profunda70) no grupo Rinvoq® 15 mg em comparação a um evento (0,1%) no grupo placebo7. Em estudos controlados com MTX, houve um evento de trombose99 venosa (0,2%) em 12/14 semanas no grupo de monoterapia com Rinvoq® 15 mg e não houve eventos no grupo MTX. A taxa geral de incidência57 de eventos de trombose99 venosa a longo prazo para o grupo Rinvoq® 15 mg entre todos os cinco estudos clínicos de fase 3 foi de 0,6 a cada 100 pacientes-ano.
Elevações de transaminases hepáticas87: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, por até 12/14 semanas, elevações de alanina transaminase (ALT) e aspartato transaminase (AST) de ≥ 3 x limite superior da normalidade (ULN) em no mínimo uma medição foram observadas em 2,1% e 1,5% dos pacientes tratados com Rinvoq® 15 mg, em comparação a 1,5% e 0,7%, respectivamente, dos pacientes tratados com placebo7. A maior parte dos casos de elevações de transaminase hepática33 foi assintomática e temporária.
Em estudos controlados com MTX, por até 12/14 semanas, elevações de ALT e AST de ≥ 3 x ULN em no mínimo uma medição foram observadas em 0,8% e 0,4% dos pacientes tratados com Rinvoq® 15 mg, em comparação a 1,9% e 0,9%, respectivamente, dos pacientes tratados com MTX.
O padrão e a incidência57 de elevação de ALT/AST permaneceram estáveis com o tempo, inclusive em um estudo de extensão a longo prazo.
Elevações lipídicas: O tratamento com Rinvoq® 15 mg foi associado a aumentos nos parâmetros lipídicos, incluindo colesterol62 total, triglicerídeos, colesterol62 LDL63 e colesterol62 HDL64. As elevações de colesterol62 LDL63 e HDL64 tiveram seu pico até a semana 8 e permaneceram estáveis posteriormente. Em estudos controlados, por até 12/14 semanas, as alterações desde o valor basal nos parâmetros lipídicos em pacientes tratados com Rinvoq® 15 mg são resumidos abaixo:
- Aumento de colesterol62 LDL63 médio em 0,38 mmol/L100.
- Aumento de colesterol62 HDL64 médio em 0,21 mmol/L100.
- A proporção LDL63/HDL64 médio permaneceu estável.
- Aumento de triglicerídeos médios em 0,15 mmol/L100.
Elevações de creatina fosfoquinase: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, por até 12/14 semanas, foram observados aumentos nos valores de creatina fosfoquinase (CPK). Foram relatadas elevações de CPK > 5 x ULN em 1,0% e 0,3% dos pacientes por 12/14 semanas nos grupos Rinvoq® 15 mg e placebo7, respectivamente. A maior parte das elevações > 5 x ULN foi temporária e não necessitou de descontinuação do tratamento. Os valores médios de CPK aumentaram até a semana 4 e então permaneceram estáveis no valor aumentado posteriormente, inclusive com terapia prolongada.
Neutropenia56: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, por até 12/14 semanas, houve reduções nas contagens de neutrófilos59 abaixo de 1.000 células58/mm3 em no mínimo uma medição em 1,1% e <0,1% dos pacientes nos grupos utilizando Rinvoq® 15 mg e placebo7, respectivamente. Em estudos clínicos, o tratamento foi interrompido em resposta a CAN <1.000 células58/mm3. O padrão e a incidência57 de reduções nas contagens de neutrófilos59 permaneceram estáveis em um valor menor que o basal ao longo do tempo, inclusive com a terapia prolongada.
Linfopenia: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, por até 12/14 semanas, houve reduções nas contagens de linfócitos abaixo de 500 células58/mm3 em no mínimo uma medição em 0,9% e 0,7% dos pacientes nos grupos utilizando Rinvoq® 15 mg e placebo7, respectivamente.
Anemia60: Em estudos clínicos controlados por placebo7 com histórico de uso de DMARDs, por até 12/14 semanas, houve reduções de hemoglobina61 abaixo de 8 g/dL em no mínimo uma medição em <0,1% dos pacientes nos grupos utilizando Rinvoq® 15 mg e placebo7.
Atenção: este produto é um medicamento novo e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Em casos de eventos adversos, notifique pelo Sistema VigiMed, disponível no Portal da Anvisa.
SUPERDOSE
O upadacitinibe foi administrado em estudos clínicos até doses equivalentes na AUC11 diária de até 60 mg em liberação prolongada uma vez ao dia. Os eventos adversos foram comparáveis aos observados em doses menores e não foram identificadas toxicidades específicas. Aproximadamente 90% do upadacitinibe na circulação101 sistêmica é eliminado no período de 24 horas da administração (na variação de doses avaliadas em estudos clínicos). Em caso de uma superdose, é recomendado que o paciente seja monitorado quanto aos sinais19 e sintomas44 de reações adversas. Pacientes que venham desenvolver reações adversas deverão receber tratamento adequado.
Em caso de intoxicação ligue para 0800 722 6001, se você precisar de mais orientações.
DIZERES LEGAIS
VENDA SOB PRESCRIÇÃO MÉDICA
MS: 1.9860.0017
Farm. Resp.: Joyce M. C. Camargo CRF-SP nº 17.077
Fabricado por:
AbbVie Ireland NL B.V. - Sligo - Irlanda
Embalado por:
AbbVie Inc.
1 N. Waukegan Rd, North Chicago – EUA
Importado por:
AbbVie Farmacêutica Ltda.
Av. Guido Caloi, 1935, 1º andar, Bloco C - São Paulo - SP
CNPJ: 15.800.545/0001-50
AbbVie Farmacêutica LTDA
Av. Guido Caloi, 1935 – 1º andar – Bloco C
Santo Amaro
São Paulo - SP, Brasil, CEP 05802-140
AbbVie Farmacêutica LTDA
Avenida Jornalista Roberto Marinho, 85 - 7º andar Brooklin
São Paulo – SP, Brasil, CEP 04576-010