
POSOLOGIA E MODO DE USAR BLOPRESS
BLOPRESS deve ser administrado via oral, uma vez ao dia, com ou sem alimentos.
O efeito anti-hipertensivo máximo é atingido no período de 4 semanas após o início do tratamento.
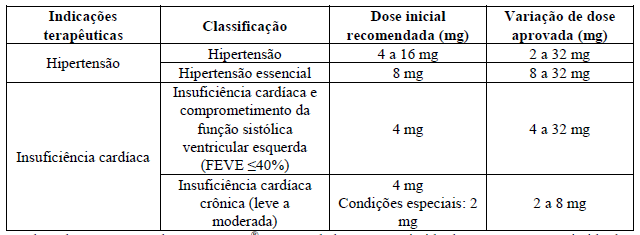
A dose de manutenção de BLOPRESS recomendada é 1 comprimido de 8 mg ou 1 comprimido de 16 mg, uma vez ao dia.
Terapia concomitante
Hipertensão1: a posologia deve ser ajustada de acordo com a resposta do paciente ao tratamento. BLOPRESS pode ser administrado com outros agentes anti-hipertensivos. A adição de um diurético2 mostrou uma efeito anti-hipertensivo aditivo com diversas doses de BLOPRESS.
Populações Especiais
Pacientes com depleção3 de volume intravascular4: considerar a menor dose inicial em pacientes com depleção3 do volume intravascular4.
Pacientes idosos:não há necessidade de ajuste de dose.
Pacientes com comprometimento renal5: não é necessário ajuste inicial da dose em pacientes com comprometimento renal5 leve a moderado (depuração de creatinina6 > 30 ml/min/1,73 m2 de área corpórea). Em pacientes com comprometimento renal5 grave (depuração de creatinina6 < 30 ml/min/1,73 m2 de área corpórea), a experiência clínica é limitada, devendo-se considerar uma dose inicial de 2 a 4 mg. A posologia deve ser ajustada conforme a resposta do paciente ao tratamento. A candesartana cilexetila não é recomendada a pacientes com comprometimento renal5 grave ou terminal (depuração de creatinina6 < 15 ml/min).
Pacientes com comprometimento hepático: a dose inicial recomendada a pacientes com comprometimento hepático leve ou moderado é 2 a 4 mg de candesartana cilexetila, uma vez ao dia. A dose pode ser ajustada de acordo com a resposta do paciente. Não existem experiências, até o momento, em pacientes com comprometimento hepático grave, como por exemplo, em pacientes cirróticos.
Pacientes pediátricos: a segurança e eficácia de BLOPRESS® (candesartana cilexetila) não foram estabelecidas em crianças.
Insuficiência Cardíaca7
Disfunção ventricular esquerda (FEVE≤ 40%)
A dose inicial recomendada é de 4 mg (meio comprimido de 8 mg) uma vez ao dia. O intervalo de dose aprovado é de 4 mg a 32 mg.
Insuficiência Cardíaca7 Crônica (leve a moderada)
A dose inicial recomendada é de 4 mg (meio comprimido de 8 mg) uma vez ao dia. Em pacientes com pressão arterial sistólica8 (PAS) < 120 mm Hg, disfunção renal5 uso de diurético2 ou insuficiência cardíaca7 grave a dose inicial recomendada deve ser reduzida para 2 mg uma vez ao dia (1/4 do comprimido de 8 mg). O intervalo de dose aprovado é de 2 a 8 mg.
Populações Especiais
Depleção3 do volume intravascular4: considerar a menor dose inicial em pacientes com depleção3 do volume intravascular4.
Pacientes idosos: não é necessário ajuste de dose inicial para pacientes9 idosos.
Pacientes pediátricos: a segurança e eficácia de BLOPRESS® (candesartana cilexetila) não foram foi estabelecida (não há experiência clínica).
Comprometimento da função renal5: não é necessário ajuste de dose inicial para pacientes9 com comprometimento renal5.
Comprometimento da função hepática10: não é necessário ajuste de dose inicial para pacientes9 com comprometimento hepático.
- 9. REAÇÕES ADVERSAS
Estudos clínicos para o tratamento da hipertensão1:
Em estudos clínicos controlados para a hipertensão1, os eventos adversos foram leves e transitórios quando comparados com o placebo11.
A incidência12 total de efeitos adversos não mostrou associação com dose, idade ou sexo. A interrupção do tratamento em decorrência de efeitos adversos foi semelhante com candesartana cilexetila e placebo11 (3,1% e 3,2% respectivamente).
De acordo com análise dos dados dos estudos clínicos, as seguintes reações adversas classificadas como comum (>1/100) com candesartana cilexetila foram relatadas baseadas na incidência12 de eventos adversos com candesartana cilexetila pelo menos 1% maior que a incidência12 observada com o placebo11.
Reações comuns (> 1/100 e < 1/10):
Infecções13 e infestações: infecção14 respiratória.
Distúrbios no sistema nervoso15: tontura16, vertigem17 e cefaleia18.
Estudos clínicos para o tratamento da insuficiência cardíaca7:
O perfil de eventos adversos com o uso de candesartana cilexetila em pacientes com insuficiência cardíaca7 foi consistente com a farmacologia19 do fármaco20 e com o estado de saúde21 do paciente.
No estudo clínico CHARM, comparando doses de candesartana cilexetila de até 32 mg (n=3,803) com placebo11 (n=3,796), 21,0% do grupo tratado com candesartana cilexetila e 16,1% do grupo tratado com placebo11 descontinuaram o tratamento devido aos eventos adversos. As reações adversas comumente (≥ 1/100, < 1/10) observadas foram:
Reações comuns (> 1/100 e < 1/10):
Distúrbios vasculares22: hipotensão23.
Distúrbios metabólicos e nutricionais: hipercalemia24.
Distúrbios renais e urinários: comprometimento renal5.
Exames laboratoriais: aumentos nos níveis de creatinina6, ureia25 e potássio. Recomenda-se o monitoramento periódico dos níveis séricos de creatinina6 e potássio.
Experiência pós-comercialização (hipertensão1 e insuficiência cardíaca7)
As reações adversas a seguir têm sido reportadas muito raramente (<1/10.000) na experiência pós-comercialização:
Reações muito raras (<1/10.000):
Distúrbios do sistema sanguíneo e linfático26: leucopenia27, neutropenia28 e agranulocitose29.
Distúrbios do metabolismo30 e nutrição31: hipercalemia24 e hiponatremia32.
Distúrbios do sistema nervoso15: tontura16
Distúrbios do sistema respiratório33, torácico e mediastínico: tosse
Distúrbios hepatobiliares34: aumento das enzimas hepáticas35, função hepática10 anormal ou hepatite36.
Distúrbios de pele37 e do tecido subcutâneo38: angioedema39, rash40, urticária41 e prurido42.
Distúrbios do tecido conjuntivo43, músculo-esquelético e dos ossos: lombalgia44
Distúrbios renais e urinários: comprometimento renal5, incluindo insuficiência renal45 em pacientes suscetíveis.
Em casos de eventos adversos, notifique ao Sistema de Notificações em Vigilância Sanitária – NOTIVISA, disponível em http://www.anvisa.gov.br/hotsite/notivisa/index.htm, ou para a Vigilância Sanitária Estadual ou Municipal.


